Вакцины против ротавирусной инфекции телят
Обновлено: 24.04.2024
Ключевые слова: вакцинопрофилактика, ротавирусная инфекция, иммунопатогенез, дети
Keywords: vaccination, rotavirus infection, immunopathogenesis, children
Резюме. В статье представлены данные о заболеваемости детей раннего возраста ротавирусной инфекцией, особенностях ее иммунопатогенеза, клинического течения и исходах, что свидетельствует об актуальности этой проблемы для здравоохранения. Освещены возможности иммунопрофилактики как эффективного и безопасного метода борьбы с ротавирусной инфекцией в современных условиях.
Summary. The article presents data on the incidence of rotavirus infection in young children, features of its immunopathogenesis, clinical course and outcomes, which indicates the relevance of this problem for public health. The possibilities of immunoprophylaxis as an effective and safe method of controlling rotavirus infection in modern conditions are shown.
Ротавирусная инфекция – наиболее частая причина диареи в детском возрасте. По оценкам экспертов Всемирной организации здравоохранения (ВОЗ), практически каждый ребенок, независимо от расы и социально-экономического статуса, в течение первых 3-5 лет жизни переносит ротавирусную инфекцию [1]. Актуальность данной проблемы определяется не только чрезвычайно широкой распространенностью ротавируса в популяции, но и довольно тяжелым течением заболевания с развитием эксикоза различной степени, нарушений ферментации углеводов, дисбиоза кишечника, высоким риском осложнений (гиповолемического шока, поражения центральной нервной системы и др.), а также возможностью внутрибольничного инфицирования, что приводит к ухудшению состояния больного и увеличению длительности госпитализации.
В настоящее время установлено, что иммунокомпетентные клетки экспрессируют рецепторы, способные распознавать различные специфические микробные компоненты (toll-like рецепторы, TLR). Выделяют TLR 3, 7, 8 и 9-го типов, которые располагаются внутри клетки и отвечают за распознавание нуклеиновых кислот различных вирусов, в том числе и ротавируса, вызывающего до 80% всех случаев острой инфекционной диареи у детей раннего возраста. TLR-3, TLR-7 и TLR-8 экспрессируются главным образом в клетках моноцитарно-макрофагального ряда, при этом TLR-3 являются ключевым элементом системы противовирусного иммунного ответа, поскольку при их взаимодействии с двуспиральной вирусной РНК (именно такую РНК содержит ротавирус) индуцируется синтез β-интерферона – основного противовирусного медиатора врожденного иммунитета [2].
В немногочисленных отечественных работах 6 изучены отдельные аспекты иммунопатогенеза ротавирусной инфекции, однако до настоящего времени роль TLR в клиническом течении этого заболевания не рассматривалась. На основании имеющихся научных данных можно предположить, что тяжесть течения и исход ротавирусной инфекции (выздоровление, формирование вирусоносительства, вторичной лактазной недостаточности, дисбиоза кишечника и пр.) у детей раннего возраста в определенной мере зависят от экспрессии TLR. Установление таких взаимосвязей представляется чрезвычайно важным, в том числе для прогнозирования клинико-иммунологической эффективности вакцинопрофилактики ротавирусной инфекции у детей раннего возраста.
Важную роль в элиминации ротавируса и защите организма от повторного инфицирования играют Т-клеточное и В-клеточное звенья иммунитета – врожденного и адаптивного. В частности, активация TLR, синтез провоспалительных цитокинов (интерлейкинов 1β, 4, 8, 10, ФНО-α) и последующая продукция α- и γ-интерферонов способны критически влиять на развитие ротавирусной инфекции [7].
Научные исследования факторов врожденного клеточного иммунитета в настоящее время проводятся в основном в экспериментах на животных. Так, в гнотобиологическом исследовании на свиньях, инфицированных вирулентным штаммом ротавируса человека, продемонстрировано, что эта инфекция приводит к выраженной продукции γ-интерферона Т-лимфоцитами, находящимися преимущественно в подвздошной кишке, что играет важную роль в противовирусной защите [8]. M.S.P. Azevedo и соавт. в аналогичном эксперименте выявили высокий уровень провоспалительных цитокинов (интерлейкинов 6, 10, 12, ФНО-α) в сыворотке крови животных, инфицированных вирулентным штаммом ротавируса, что указывает на сбалансированный ответ Т-хелперов 1-го и 2-го типов и имеет важное значение в патогенезе ротавирусной инфекции [9].
Таким образом, более глубокое изучение иммунопатогенеза ротавирусной инфекции на основе определения уровня TLR у детей позволит оценить влияние этих факторов врожденного клеточного иммунитета на течение и исход заболевания, а также усовершенствовать его иммунотерапию и иммунопрофилактику, что отвечает потребностям как медицинской науки (испытывающей в настоящее время дефицит данных по этой проблеме), так и практического здравоохранения, особенно детской инфектологии.
В настоящее время иммунопатогенез ротавирусной инфекции до конца не изучен [10]. Тем не менее доказано важное значение CD4 + -лимфоцитов при первичном и при повторном инфицировании детей ротавирусом и при вакцинации против этого заболевания. Установлено, что и количество, и функциональный профиль CD4 + -лимфоцитов в детском возрасте снижены, а это, в свою очередь, ведет к нарушению выработки цитокинов, в частности γ-интерферона 12.
В исследовании И.Д. Майковой и соавт. изучена роль системы интерферонов и ряда других факторов гуморального иммунитета, а также фагоцитоза в защите организма ребенка в острый период ротавирусной инфекции и в период ранней реконвалесценции, а также продемонстрированы возможности коррекции выявленных нарушений иммунитета препаратом человеческого рекомбинантного α-интерферона [6]. Повышение уровня γ-интерферона, снижение количества Т-хелперов и цитотоксических лимфоцитов в острый период ротавирусной инфекции и нормализация интерферонового статуса, а также содержания основных субпопуляций Т-лимфоцитов при умеренном повышении содержания зрелых В-лимфоцитов и сывороточного IgA в период реконвалесценции отмечается в работе К.Д. Ермоленко и соавт. [4].
В исследовании Р.К. Бабик и Е.В. Корнеевой, проведенном с участием небольшого числа детей (n = 27), выявлен повышенный уровень α/γ-интерферонов, а также установлена роль других факторов гуморального иммунитета при одновременном снижении числа нейтрофильных гранулоцитов для благоприятного течения острой кишечной инфекции, в том числе ротавирусной. Снижение уровня провоспалительного γ-интерферона и некоторых цитокинов было характерно для тяжелого течения этих заболеваний [3]. Влияние γ-интерферона, интерлейкинов 10 и 12 на тяжесть течения и формирование неблагоприятных исходов ротавирусной инфекции у детей отмечают и другие авторы [5].
Таким образом, до настоящего времени недостаточно изучен вопрос о действии ротавируса на факторы врожденного клеточного иммунитета. Практически отсутствуют работы, посвященные изучению роли TLR, что может иметь значение для последующего формирования вирусоносительства, рецидивов и других неблагоприятных исходов ротавирусной инфекции. В свою очередь, уточнение представлений о нарушениях клеточного иммунитета как одних из ведущих факторов защиты при этом заболевании позволит теоретически обосновать возможность проведения интерферонотерапии у детей раннего возраста с ротавирусной инфекцией, разработать методы коррекции выявленных нарушений и оценить клинико-иммунологическую эффективность вакцинопрофилактики этого заболевания.
Ввиду высокой контагиозности ротавируса, недостаточной эффективности санитарно-гигиенических мероприятий и отсутствия этиотропной терапии единственным эффективным методом контроля заболеваемости ротавирусной инфекцией является массовая вакцинация детей раннего возраста. ВОЗ настоятельно рекомендует включение ротавирусной вакцины в национальные программы вакцинации всех стран мира. По данным ВОЗ, по состоянию на май 2018 г. обязательная вакцинация против ротавирусной инфекции внедрена в национальные календари прививок более чем 100 государств [16].
По данным эпидемиологических исследований, внедрение вакцинации позволило добиться снижения частоты госпитализаций по поводу ротавирусной инфекции у детей младше 5 лет на 49-92%, частоты госпитализаций и смертности по причине острой кишечной инфекции (любой этиологии) – соответственно на 17-55 и 22-50% [19].
Немаловажными представляются результаты оценки популяционного иммунитета (снижение заболеваемости ротавирусной инфекцией у невакцинированных когорт). Так, в США было зафиксировано снижение частоты ротавирусной инфекции у лиц в возрасте 5-14 лет на 25%, у лиц в возрасте 15-24 лет – на 7%, расчетные предотвращенные затраты составили 204 млн долларов США [20].
Согласно приказу Минздрава России № 125н от 21.03.2014, вакцинация против ротавирусной инфекции включена в национальный календарь профилактических прививок по эпидемиологическим показаниям. В то же время объемы вакцинации сейчас не могут существенно снизить заболеваемость ротавирусной инфекцией [21].
В настоящий момент 12 регионов России реализуют пилотные программы вакцинопрофилактики против ротавирусной инфекции: Москва, Московская, Тверская, Ярославская, Свердловская, Тюменская и Сахалинская области, Республика Саха (Якутия), Красноярский и Краснодарский края, Ненецкий и Ханты-Мансийский автономные округа [22]. Аналогичную программу планируют провести в Санкт-Петербурге. Предполагается, что ее внедрение позволит снизить заболеваемость острыми кишечными инфекциями на 47%, сократить количество обращений за амбулаторной помощью более чем на 4000 и количество госпитализаций на 319. Согласно расчетным данным, затраты на проведение этого пилотного проекта окупятся уже через 1 год, при этом ежегодная экономия бюджетных средств Санкт-Петербурга составит 157,5 млн рублей (в ценах 2016 г., рассчитывается исходя из разницы между предотвращенным экономическим ущербом от ротавирусной инфекции и затратами на вакцинацию против нее [23]).
Из тех регионов России, где уже внедрена иммунопрофилактика ротавирусной инфекции как пилотный проект, предварительные результаты получены в Тюменской области [24]. Этот регион неслучайно одним из первых начал активно вакцинировать детей раннего возраста против данного заболевания: до 1995 г. заболеваемость ротавирусной инфекцией здесь была спорадической – 2,4-2,6 случая на 100 тыс. жителей, в 2001 г. она возросла до 8,8 случая, а в 2002 г. достигла 40,2 случая. В последующем рост заболеваемости продолжался: в 20032004 гг. она составила 50,6-64,0 случая, а максимальной была в 2010 г. – 391,1 случая на 100 тыс. человек. В этиологической структуре острых кишечных инфекций в Тюменской области на долю ротавирусной в 2011-2013 гг. приходилось 82,0-87,5%. При этом интенсивность эпидемического процесса в городах была в 3,75 раза выше, чем в сельской местности. Уровень заболеваемости ротавирусной инфекцией с 2002 г. в России вырос в 2,5 раза, а в Тюменской области – в 9,8 раза. Доля детей, перенесших ротавирусную инфекцию, в данном регионе составила в эти годы 82-85%. Среднемноголетний показатель заболеваемости в 1994-2010 гг. колебался в пределах 0,94-136,20 случая на 100 тыс. детей в возрасте до 14 лет и превышал таковой у лиц старше этого возраста в 2,9 раза. У детей младше 1 года среднемноголетняя заболеваемость ротавирусной инфекцией составила 45,8 случая. Среди организованных детей 1-2 лет она была ниже, чем в целом по данной возрастной группе, а у детей 3-6 лет, посещавших детские дошкольные учреждения, этот показатель не отличался от такового в данной возрастной группе в целом и составил 6,5-6,6 на 100 тыс.
При генотипировании выделенных от больных штаммов ротавируса установлено, что в 2005-2009 гг. в Тюменской области доминировал генотип G1[P]8 – 74,5%, менее распространены оказались генотипы G4[P]8 – 13,8% и G3[P]8 – 6,9%. При этом за 4 года наблюдений удельный вес доминирующего генотипа нескольку уменьшился, появились новые варианты ротавируса типа А и нетипируемые ротавирусы.
Все это стало снованием для проведения массовой вакцинации детей раннего возраста против ротавирусной инфекции, которая началась в 2014 г. В течение этого года которого было иммунизировано 1000 детей в Тюмени. Из них лишь у 5 привитых отмечались реакции на вакцину в виде кратковременного субфебрилитета и легкой диареи. У вакцинированных детей в течение 6 мес наблюдения случаи ротавирусной инфекции не регистрировались. Количество госпитализаций за указанный период по поводу острых кишечных инфекций в группе привитых детей по сравнению с непривитыми оказалось в 4 раза меньше.
Аналогичный пилотный проект иммунопрофилактики был реализован в Красноярском крае [25]. В этом регионе доля ротавирусной инфекции в среднем составляет 88% от общего числа случаев диареи вирусной этиологии. Динамика многолетней заболеваемости отражает тенденцию к росту заболеваемости, которая к 2015 г. достигла 61,2 случая на 100 тыс. человек, что в 11,5 раза выше по сравнению с уровнем 2007 г. Активность эпидемического процесса поддерживалась в основном за счет детского населения, доля которого в структуре заболевших в 2015 г. оказалась равна 97,4%, преимущественно это были дети первых 2 лет жизни.
Особенно неблагополучная ситуация по ротавирусной инфекции сложилась в г. Ачинске Красноярского края, который и решено было выбрать стартовой площадкой для массовой иммунизации детей раннего возраста. Вакцинация там началась в июле 2015 г. и продолжалась по апрель 2016 г. Всего было вакцинировано 616 детей, из которых у 16,2% наблюдались следующие поствакцинальные реакции: назофарингит, температура тела выше 38°С, беспокойство, диарея, вялость.
По результатам российских фармакоэкономических исследований, ежегодная вакцинация 95% новорожденных против ротавирусной инфекции позволила бы снизить затраты, связанные с этим заболеванием, на 45,31 млрд рублей, из них 18,98 млрд рублей – затраты на амбулаторное лечение и 26,33 млрд рублей – на госпитализацию [27].
Таким образом, ввиду актуальности проблемы ротавирусной инфекции для здравоохранения России, обусловленной повсеместным распространением этого заболевания, вовлечением в эпидемический процесс преимущественно детей раннего возраста, у которых ротавирусная инфекция протекает иногда тяжело и имеет неблагоприятные исходы (формирование вирусоносительства, дисбиоза и различной хронической патологии желудочно-кишечного тракта), что обусловлено особенностями иммунопатогенеза, широкое внедрение вакцинопрофилактики позволило бы существенно снизить заболеваемость ротавирусной инфекцией и минимизировать связанные с нею материальные затраты, а главное – улучшить состояние здоровья детей первых лет жизни.
Основано на официально утвержденной инструкции по применению препарата ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ для специалистов и утверждено компанией-производителем для электронного издания справочника Видаль Ветеринар 2013 года
Лекарственная форма
Форма выпуска, состав и упаковка
Суспензия для инъекций однородная, розового цвета; при хранении выпадает рыхлый осадок, легко разбивающийся при встряхивании.
Изготавливлена из культуральных жидкостей клеток млекопитающих (СПЭВ, RBT, Taurus-2, MDBK или Vero), инфицированных ротавирусом крупного рогатого скота (КРС) штамм 101 и коронавирусом штамм ВНИИЗЖ, инактивированных аминоэтилэтиленимином, с добавлением 33% гидроокиси алюминия и 0.83% сапонина.
Расфасовывана по 45 или 90 мл (15 или 30 прививных доз) во флаконы стеклянные соответствующей вместимости. Флаконы герметично укупорены резиновыми пробками, укрепленными алюминиевыми колпачками. Флаконы с вакциной упаковывают в ящики из картона (транспортная тара). В каждый ящик с вакциной вкладывают три инструкции по применению.
Фармакологические (биологические) свойства и эффекты
Вакцина вызывает формирование иммунного ответа у крупного рогатого скота к ротавирусу и коронавирусу через 14-21 сутки после двукратного применения продолжительностью не менее 6 месяцев.
Механизм действия препарата заключается в выработке специфического иммунитета к возбудителям ротавирусной и коронавирусной инфекций крупного рогатого скота в организме вакцинированных коров (или нетелей) после двукратной иммунизации. Образовавшиеся антитела передаются с молозивом и обеспечивают пассивную защиту новорожденных телят от ротавирусной и коронавирусной инфекций в первые 45 дней жизни теленка.
Вакцина безвредна, лечебными свойствами не обладает.
Показания к применению препарата ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ
- для профилактики ротавирусной и коронавирусной инфекций крупного рогатого скота в неблагополучных и угрожаемых по данным заболеваниям хозяйствах.
Порядок применения
В угрожаемых хозяйствах вакцинируют нетелей и коров двукратно с интервалом 21-30 суток за 1.5-2 месяца до отела.
Одна прививная доза вакцины составляет 3 см 3 .
Вакцину вводят внутримышечно в область средней трети шеи, место инъекции обрабатывают 70% раствором этилового спирта или другим дезинфицирующим раствором.
Перед применением, а также периодически в процессе использования, вакцину взбалтывают до приобретения однородной консистенции.
Для вакцинации используют одноразовые или многоразовые шприцы и иглы, а также автоматические инъекторы, которые стерилизуют кипячением в течение 15-20 минут. Стерилизация шприцов, игл, автоматических инъекторов химическими средствами не допускается.
Следует избегать нарушений схемы (сроков) введения вакцины, поскольку это может привести к снижению эффективности иммунопрофилактики ротавирусной и коронавирусной инфекций КРС. В случае пропуска очередного введения вакцины
необходимо провести иммунизацию как можно скорее.
Побочные эффекты
При применении вакцины в соответствии с настоящей инструкцией побочных явлений и осложнений, как правило, не отмечается.
У отдельных животных после вакцинации может наблюдаться кратковременное повышение температуры тела на 0.5°С (до 48 ч), образование незначительной припухлости (до 5 мм) на месте инъекции, исчезающей через 3-4 суток. При этом рекомендуется применять антигистаминные препараты и проводить симптоматическое лечение.
Симптомов проявления ротавирусной, коронавирусной инфекций или других патологических признаков при передозировке вакцины не установлено.
Противопоказания к применению препарата ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ
- клинически больные и/или ослабленные животные.
Особые указания и меры личной профилактики
Применение вакцины против ротавирусной и коронавирусной инфекций КРС сорбированной инактивированной не исключает использование других иммунобиологических и лекарственных препаратов (антибиотиков, сульфаниламидов и пр.). Не разрешается смешивать вакцину с другими лекарственными препаратами.
Продукты убоя, мясо и молоко от вакцинированных животных реализуют без ограничения независимо от сроков вакцинации.
Меры личной профилактики
При работе с вакциной следует соблюдать общие правила личной гигиены и техники безопасности, предусмотренные при работе с лекарственными средствами ветеринарного назначения.
Все лица, участвующие в проведении вакцинации, должны быть в спецодежде и обеспечены индивидуальными средствами защиты: халат или комбинезон, головной убор, марлевая повязка, резиновые перчатки. В местах работы должна быть аптечка первой доврачебной помощи.
При попадании вакцины на кожу и/или слизистые оболочки их рекомендуется промыть большим количеством чистой воды.
После работы следует тщательно вымыть руки с мылом, переодеться.
При случайном введении препарата человеку, место инъекции необходимо немедленно обработать 70% раствором этилового спирта, обратиться в медицинское учреждение и сообщить об этом врачу.
Условия хранения ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ
Вакцину хранят и транспортируют в сухом темном месте при температуре от 2°С до 8°С. Замораживание вакцины не допускается. Вакцину следует хранить в местах, недоступных для детей.
Срок годности ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ
Срок годности вакцины - 12 месяцев с даты выпуска при соблюдении условий хранения и транспортирования. По истечении срока годности вакцина к применению не пригодна.
Флаконы с вакциной без этикеток, с истекшим сроком годности, нарушением целостности и/или герметичности укупорки, измененным цветом и/или консистенцией содержимого, наличием посторонних примесей, а также остатки вакцины, неиспользованные в день вскрытия флакона, подлежат выбраковке и обеззараживанию путем кипячения втечение 30 минут.
Утилизация обеззараженной вакцины не требует соблюдения специальных мер предосторожности.
Контакты для обращений
Пожалуйста, заполните поля и убедитесь в их правильности
Спасибо за Ваш отзыв, он будет опубликован после проверки
ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ отзывы
Помогите другим с выбором, оставьте отзыв об ВАКЦИНА ПРОТИВ РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Произведено:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Рота-V-Эйд ®
Лиофилизат для приготовления раствора для приема внутрь в виде однородной пористой, рыхлой массы от розоватого до желтовато-белого цвета.
| 1 доза | |
| вакцина для профилактики ротавирусной инфекции, пентавалентная, живая | 2.5 мл |
| живые реассортанты человеческого и бычьего ротавирусов: ротавирус типа G1 не менее 10 5,6 ФФЕ* ротавирус типа G2 не менее 10 5,6 ФФЕ* ротавирус типа G3 не менее 10 5,6 ФФЕ* ротавирус типа G4 не менее 10 5,6 ФФЕ* ротавирус типа G9 не менее 10 5,6 ФФЕ* |
Вспомогательные вещества: сахароза - 50 мг, глицин - 50 мг, среда МЕМ - 17 мг
* ФФЕ - фокус флуоресцирующие единицы
1 доза - флаконы в комплекте: растворитель (флаконы), адаптер - 1 шт. и шприц- 1 шт. - пачки картонные.
2 доза - флаконы в комплекте: растворитель (флаконы), адаптер - 1 шт. и шприц- 1 шт. - пачки картонные.
Фармакологическое действие
Живая пероральная пентавалентная вакцина, содержащая пять живых реассортантных штаммов ротавируса (бычьих и человеческих). На поверхности четырех вакцинных реассортантов ротавируса экспрессированы один из наружных капсидных белков VP7 (серотипы G1, G2, G3, или G4) человеческого родительского штамма ротавируса и белок VP4 (серотип Р7[5]) бычьего родительского штамма ротавируса (белок VP4 отвечает за прикрепление ротавируса к поверхности клеток). На поверхности пятого реассортанта вируса экспрессирован белок VP4 (серотип Р1А[8]) человеческого родительского штамма ротавируса и наружный капсидный белок VP7 (серотип G6) бычьего родительского штамма ротавируса.
Механизм иммунной защиты организма вакциной от гастроэнтерита, вызванного ротавирусами, до конца не изучен. Взаимосвязь между содержанием антител к ротавирусам после вакцинации ротавирусными вакцинами и степенью защиты против ротавирусного гастроэнтерита не установлена. Вакцина вызывает иммунный ответ, т.е. образование сывороточных нейтрализующих антител, к пяти капсидным белкам ротавирусов человека, содержащихся в реассортантах вакцины (G1, G 2, G,3, G 4 и Р1А[8]).
Показания активных веществ препарата Рота-V-Эйд ®
Активная иммунизация детей в возрасте от 6 до 32 недель с целью профилактики гастроэнтерита, вызываемого ротавирусами серотипов G1 , G2, G3, G4 и серотипов G, содержащих Р1А[8] (например, G9).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Побочное действие
Инфекционные и паразитарные заболевания: инфекции верхних дыхательных путей; назофарингит, средний отит.
Со стороны пищеварительной системы: диарея, рвота; боль в верхних отделах живота, гематохезия; инвагинация кишечника.
Со стороны кожи и подкожных тканей: сыпь; крапивница.
Со стороны дыхательной системы: бронхоспазм.
Общие расстройства: гипертермия.
Противопоказания к применению
Инвагинация кишечника в анамнезе; врожденные пороки развития желудочно-кишечного тракта, предрасполагающие к инвагинации кишечника; иммунодефицит, подозрение на иммунодефицит или ВИЧ-носительство; острые воспалительные процессы, сопровождающиеся высокой температурой (в этих случаях вакцинацию проводят после выздоровления или в стадии ремиссии). Инфекционное заболевание легкой степени тяжести не должно служить причиной отказа от вакцинации; острая форма диареи или рвоты (в этих случаях вакцинацию проводят на стадии ремиссии); повышенная чувствительность к любому компоненту вакцины, введение вакцины в анамнезе.
При активных заболеваниях ЖКТ, включая хроническую диарею (отсутствие клинических данных); при задержке развития (отсутствие клинических данных); при иммунокомпрометированном состоянии (например, в результате злокачественных новообразований или иммунодепрессивной терапии); при трансфузии крови или продуктов крови, включая иммуноглобулины, менее чем за 42 дня до намеченной вакцинации.
Применение у детей
Хорошо переносится и обладает высокой эффективностью по предотвращению ротавирусного гастроэнтерита при применении у детей в возрасте от 6 до 32 недель.
Эффективность и безопасность не были установлены у детей в возрасте младше 6 недель.
Особые указания
По данным клинических исследований вакцинный вирус обнаруживался в кале у 8.9% вакцинированных детей только в течение 1 недели после введения первой дозы вакцины и только у 0.3% детей (1 случай) после введения 3-й дозы. Согласно пострегистрационным данным возможна передача вакцинного вируса невакцинированным лицам. Вакцина должна с осторожностью назначаться детям, находящимся в тесном контакте с людьми с иммунодефицитом (в т.ч. с онкологическими заболеваниями, иммунокомпрометированными или людьми, получающими иммуносупрессивную терапию). Следует соблюдать особые гигиенические правила при контакте с калом вакцинированного ребенка.
В связи с недостаточностью клинических данных не рекомендуется назначение вакцины при бессимптомной ВИЧ-инфекции.
У детей с тяжелым комбинированным иммунодефицитом были отмечены случаи гастроэнтерита, вызванного штаммами ротавируса, входящими в вакцину.
Как и любая другая вакцина, не может обеспечить полную защиту всех вакцинированных. Эффективна только против ротавирусной инфекции и не защищает от гастроэнтерита, вызванного другими патогенными микроорганизмами.
В работе представлены результаты эпизоо-тологического мониторинга диарей новорожденных телят в животноводческих хозяйствах РФ, Украины и Белоруссии, а также экспериментальные данные по применению вакцин против рота- и коронавирусной инфекций на глубокостельных коровах.
В структуре заболеваний телят в ранний постнатальный период превалирующее место занимают нарушения функций пищеварительной системы, клинически проявляющиеся диареей, обуславливающей развитие выраженной дегидратации, токсемии, иммунодефицита в, нарушения обмена веществ.
Этиопатогенетически поражения органов пищеварения отличаются значительным полиморфизмом, включающим широкий спектр различных факторов, в том числе генетических, физиологических, санитарно-гигиенических и инфекционных. Массовые нарушения функций пищеварения, клинически проявляющиеся диареями, регистрируются у 70-80% новорожденных телят уже к концу первых суток после рождения. Больные телята отказываются от молозива, постоянно лежат, быстро наступает обезвоживание, интоксикация, энофталь--мия, резко понижается тонус.
Гибель новорожденных телят, как правило, наступает на 2-5-й или 7-10-й дни. Обычно погибает от 15 до 55% новорожденных телят [6,10,11].
Ведущей причиной гастроэнтеритов новорожденных телят являются инфекционные агенты, в том числе вирусы, бактерии, простейшие и грибы, вирулентность которых повышается на фоне различных неблагоприятных условий содержания и кормления. Возбудители инфекционных заболеваний попадают в организм обычно в первый день жизни телят [12,15].
Считается, что вирусы являются пусковым механизмом для развития патологии кишечника. При диареях новорожденных телят выделяют рота-, корона-, парво-, торо-, калици-, пес-ти-, астро- и реовирусы [3,12,16].
В основном диарея новорожденных телят протекает в виде смешанных инфекций. При смешанных инфекциях трудно определить роль того или иного инфекционного агента, который выделяется от больных диарей телят. Факт обнаружения того или иного возбудителя от больных диарей новорожденных телят не служит убедительным доказательством его этиологической роли в патологии.
Вирусная инфекция начинается с адсорбции возбудителей на рецепторных клетках цилиндрического эпителия тонкого отдела кишечника. В процессе репродукции вируса происходит гибель пораженных клеток, их десквамация и нарушение целостности эпителия кишечника. Цилиндрический эпителий быстро сменяется на дифференцированный кубический и плоский. Это приводит к нарушению всасывающей и секретирующей способности клеток тонкого кишечника и усилению его перистальтики.
Ряд исследователей диареи новорожденных телят относят её к мембранопатологиям. Заболевания животных, которые протекают с симптомами поражения желудочно-кишечного тракта и токсикоза, сопровождаются активацией процессов перекислого окисления липидов, накоплением в межклеточном пространстве супероксидного иона перекиси водорода и гипероксидного радикала, являющиеся основной причиной повреждения тканей. В организме больного теленка происходят существенные биохимические изменения. Интоксикация влечет за собой существенные изменения в обмене, которые приводят к иммуносупрессии и антиоксидантному стрессу [1,13].
Все это позволяет рассматривать диарею новорожденных телят как комплексную патологию организма, при которой доминируют признаки нарушения функции пищеварения: общей интоксикации, обезвоживания, мембранопатологии и иммуносупрессии.
В последнее время установлено, что при вирусных инфекциях происходят аберрации хромосом клеток больного животного [5].
Материалы и методы
Изучение эффективности вакцинопрофилактики вирусных диарей новорожденных телят ротавирусной и коронавирусной этиологии проводили в животноводческих хозяйствах различных регионов Российской Федерации, Украины и Белоруссии. В хозяйствах, избранных для испытания препаратов, зарегистрированы нарушения функции пищеварения новорожденных теляти в результате проведенной индикации, были обнаружены ротавирус и коронавирус крупного рогатого скота.
Животные : глубокостельные коровы черно-пестрой гол-штинофризской, красно-пестрой голштинофризской, симментальской, швицкой, красно-горбатовской, сычевской, костромской и арийской пород.
Коммерческие серии вакцин :
- против ротавирусной инфекции крупного рогатого скота сорбированной инактивированной (ТУ-9384-033-00495527-02);
- против коронавирусной инфекции крупного рогатого скота сорбированной инактивированной (ТУ-9384-034-00495527-02);
- против рота- и коронавирусной инфекций крупного рогатого скота сорбированной инактивированной (ТУ 9384-035-00495527-02).
Индикацию вирусов в пробах фекалий проводили при помощи электронной микроскопии, иммунной электронной микроскопии, иммуноферментного анализа в реакции диффузионной преципитации, реакции гемагглютинации. В отдельных пробах результаты иммунохимических методов были подтверждены методом полимеразной цепной реакции. Планирование испытаний вакцин проводили по методу когортно-го исследования [4, 7].
Результаты и обсуждение
При исследовании сывороток крови коров и телят из хозяйств, неблагополучных по вирусным гастроэнтеритам новорожденных телят, антитела к ротавирусу обнаружены в 76,9%, к коронавирусу - в 68,6% материала. В 48,4% проб сыворотки крови телят выявили одновременно антитела к ротавирусу крупного рогатого скота.
Эпизоотологический мониторинг диарей среди новорожденных телят с инфекционной этиологией проводили в животноводческих хозяйствах с различным поголовьем дойных коров и уровнем их продуктивности. Результаты проведенных исследований свидетельствуют, что в обследованных хозяйствах условия содержания и кормления коров и их продуктивность не являются определенными в этиопатогенезе ротавирусной и корона вирусной диареи новорожденных телят. Не установлено разницы в проявлении диареиных заболеваний новорожденных телят, полученных о коров разных пород. Однако, четко просматривается зависимость между количеством погибших телят и временем суток, когда происходил отел. Среди "ночных" телят заболеваемость и гибель значительно превышают аналогичные показатели "дневных". Вероятно, это связано с несвоевременной выпойкой молозива. Падеж отмечен во все месяцы года, примерно в тодинаковом соотношении к количеству родившихся телят, что указывает на отсутствие сезонности заболевания. Анализ эпизоотической ситуации в ряде племенных хозяйств свидетельствует о том, что у животных, переболевших ротавирусной или коронавирусной диареей, значительно чаще регистрируются респираторные заболевания в 15-60 - дневном возрасте. Широко используемая антибиотикотерапия в большинстве случаев неэффективна вследствие резистентности микрофлоры к применяемым лечебным препаратам.
В литературе описано несколько методических подходов по вопросу борьбы и профилактики ротавирусного и корона-вирусного энтерита новорожденных телят. Ряд исследователей считает, что профилактика ротавирусной инфекции (как "факторной" болезни) новорожденных телят с помощью специфических средств (вакцин) малоэффективна, и поэтому все усилия целесообразно направлять на повышение естественной резистентности организма новорожденного [4].
В то же время специалисты, занимающиеся изучением болезней новорожденных телят, считают, что кормление телят молозивом от коров-матерей, ранее иммунизированных ина-ктивированной вакциной, может предотвращать появление диарей новорожденных [3, 9,11,14,16].
Принимая во внимание существование различных мнений о средствах и методах профилактики ротавирусной и коронавирусной диарей новорожденных телят, были проведены широкие производственные испытания инактивированных вакцин против указанных возбудителей.
Таблица 1. Результаты испытания вакцины против ротавирусной инфекции КPC сорбированной инактивированной на глубокостельных коровах
Живые реассортанты человеческого и бычьего ротавирусов, выращенные на культуре клеток Веро:
Ротавирус типа G1 – не менее 10 5,6 ФФЕ*
Ротавирус типа G2 – не менее 10 5,6 ФФЕ*
Ротавирус типа G3 – не менее 10 5,6 ФФЕ*
Ротавирус типа G4 – не менее 10 5,6 ФФЕ*
Ротавирус типа G9 – не менее 10 5,6 ФФЕ*
ФФЕ* – фокус флуоресцирующие единицы
Сахароза 50,0 мг, глицин 50,0 мг, среда МЕМ 17,0 мг.
Лимонной кислоты моногидрата 24,0 мг, натрия бикарбоната 64,0 мг, вода для инъекций до 2,5 мл.
Примечание:
1 – Вакцина и растворитель не содержат консервантов.
Описание
Лиофилизат для приготовления раствора для приема внутрь – однородная пористая, рыхлая масса от розоватого до желтовато-белого цвета.
После восстановления растворителем – прозрачная жидкость от розоватого до желтоватого цвета.
Растворитель – прозрачная бесцветная жидкость.
Характеристика
Препарат Рота-V-Эйд ® представляет собой пероральную, пентавалентную, живую вакцину для профилактики ротавирусной инфекции, которая содержит пять реассортантных (человеческие и бычьи реассортантные штаммы) штаммов ротавируса серотипов G1, G2, G3, G4 и G9, выращенных на культуре клеток линии Веро. Все штаммы содержат ген YP7 соответствующего серотипа из штаммов человеческих вирусов, реассортантных с бычьим ротавирусом (UK).
При производстве вакцины используются материалы животного происхождения.
Вакцина и растворитель не содержит консервантов. Вспомогательные вещества не содержат веществ животного происхождения.
Фармакотерапевтическая группа:
Код ATX:
Фармакологические свойства
В умеренной климатической зоне ротавирусный гастроэнтерит является основным сезонным заболеванием с увеличением заболеваемости (эпидемиями) в зимние месяцы. При отсутствии лечения ротавирусный гастроэнтерит может привести к летальной дегидратации.
По данным клинических исследований эффективность вакцины Рота-V-Эйд ® была продемонстрирована в отношении гастроэнтерита, вызванного ротавирусами серотипов G1,G2, G3, G4, G9.
Эффективность вакцины Рота-V-Эйд ® при трехкратном пероральном введении изучали в клинических исследованиях с участием 15 000 детей.
Вакцинация препаратом Рота-V-Эйд ® позволила предотвратить 4,30 эпизодов тяжелого ротавирусного гастроэнтерита в расчете на 100 человеко-лет. Совокупный риск развития тяжелого ротавирусного гастроэнтерита у вакцинированных был значительно ниже, чем в группе плацебо. Отмечали увеличение эффективности вакцины по мере повышения тяжести ротавирусного гастроэнтерита любого генеза. Показатель эффективности вакцины Рота-V-Эйд ® составил 73,2%.
В результате клинических исследованиях показано, что для достижения необходимого уровня и длительности защиты против ротавирусного гастроэнтерита необходима трехкратная вакцинация.
При оценке иммуногенности были получены следующие результаты:
- 2-х, 3-х и 4-х кратное увеличение величины титров IgA составило 75% в группе, привитых вакциной Рота-V-Эйд ® и 20% в группе, получившей Плацебо.
- Уровень сероконверсии через 28 дней после введения 3-й дозы составлял 48% в группе привитых вакциной Рота-V-Эйд ® и 21% в группе, получившей Плацебо.
В целях регистрации вакцины Рота-V-Эйд ® в Российской Федерации были проведены клинические исследования с участием детей.
В анализ иммуногенности вакцины Рота-V-Эйд ® были включены данные 97 детей-участников исследования – 48 детей из группы трехкратно привитых вакциной Рота-V-Эйд ® и 49 детей из группы трехкратно принимавших Плацебо. Доля детей-участников клинического исследования, которые были серопозитивными с концентрацией ротавирусспецифического IgA ≥20 Ед/мл на момент их включения в исследование перед приемом первой дозы, составила 20,8% в группе вакцины Рота-V-Эйд ® и 32,7% в группе Плацебо. Проведение трехкратной вакцинации серопозитивных детей-участников исследования позволило достичь показателя сероконверсии до 50%. В группе исходно серонегативных участников клинического исследования до 92,11% привитых препаратом Рота-V-Эйд ® имели четырехкратное и более увеличение титра специфических антител.
Увеличение специфических антител IgA после трехкратного введения вакцины Рота-V-Эйд ® наблюдали у 90% привитых детей-участников, при этом кратность увеличения уровня IgA в группе привитых вакциной Рота-V-Эйд ® статистически значимо отличалась от кратности увеличения уровня IgA в группе Плацебо.
При изучении иммуногенности вакцины Рота-V-Эйд ® в общей популяции серонегативных и серопозитивных детей-участников исследования показано, что после трехкратной иммунизации среднегеометрическая величина титра (СГТ) специфических антител в группе привитых вакциной Рота-V-Эйд ® достоверно статистически значимо превышала СГТ антител в группе Плацебо и составляла 130,81 ЕД/мл. Кратность прироста СГТ антител в группе вакцины Рота-V-Эйд ® составляла 39,05, в группе Плацебо – 2,80. Уровни сероконверсии (с двух-, трех- и четырехкратным приростом антител) в группе привитых вакциной Рота-V-Эйд ® составляли от 79,17% до 83,33%.
Механизм иммунной защиты организма вакциной Рота-V-Эйд ® от ротавирусного гастроэнтерита до конца не изучен. Взаимосвязь между содержанием антител к серотипам ротавируса G1, G2, G3, G4, G9 после вакцинации ротавирусными вакцинами и степенью защиты против ротавирусного гастроэнтерита не установлена.
По данным клинических исследований после проведения полного курса вакцинации, состоящего из трех доз препарата Рота-V-Эйд ® , у 92,11% исходно серонегативных детей-участников исследования в сыворотке крови наблюдалось значительное повышение уровня анти-ротавирусного IgA.
Показания к применению
Активная иммунизация здоровых детей в возрасте от 6 недель до 32 недель с целью профилактики гастроэнтерита, вызванного ротавирусами серотипов G1, G2, G3, G4, G9.
Противопоказания
- Повышенная чувствительность к любому компоненту вакцины Рота-V-Эйд ® , а также на введение любой вакцины для профилактики ротавирусной инфекции в анамнезе.
- Врожденные пороки развития желудочно-кишечного тракта, предрасполагающие к инвагинации кишечника.
- Тяжёлый комбинированный иммунодефицит (ТКИД). Поскольку у детей с ТКИД были зафиксированы случаи развития гастроэнтерита, вызванного другими живыми ротавирусными вакцинами.
- Инвагинация кишечника в анамнезе.
- Глюкозо-галактозная мальабсорбция и непереносимость сахарозы.
- Острые инфекционные и неинфекционные заболевания и обострение хронических заболеваний являются временными противопоказаниями, прививки проводят через 2 недели после выздоровления.
- Тяжелая форма диареи.
С осторожностью
- Детям с ослабленным иммунитетом и детям, находящимся в тесном контакте с лицами с иммунодефицитом (отсутствие клинических данных).
- Субфебрильная температура тела.
- Инфекции верхних дыхательных путей лёгкой степени тяжести.
- Заболевания ЖКТ, включая хроническую диарею.
- Задержка развития.
Применение при беременности и в период грудного вскармливания
Вакцина Рота-V-Эйд ® предназначена только для детей. Нет данных о применении препарата у беременных женщин и в период грудного вскармливания.
Способ применения и дозы
Вакцина Рота-V-Эйд ® предназначена только для приема внутрь!
Перед применением вакцину Рота-V-Эйд ® необходимо развести прилагаемым растворителем (см. Рекомендации по подготовке и проведению вакцинации).
Вакцина Рота-V-Эйд ® может вводиться вне зависимости от приема пищи или любой жидкости, включая грудное молоко. Вакцину Рота-V-Эйд ® нельзя смешивать с другими лекарственными средствами.
Разведённую вакцину Рота-V-Эйд ® необходимо использовать в течение 6 часов после разведения либо до конца времени иммунизации, в зависимости от того, что наступает раньше, при условии хранения при температуре от 2°С до 8°С.
Курс вакцинации состоит из трех доз препарата Рота-V-Эйд ® , каждая доза по 2,5 мл.
Препарат Рота-V-Эйд ® следует вводить трижды, с интервалами между введением очередной дозы не менее 4-х недель, начиная с 6-недельного возраста.
При введении неполной дозы вакцины (например, ребенок выплюнул или срыгнул часть дозы), на усмотрение врача, можно разово применить замещающую дозу вакцины на том же визите вакцинации. Оставшиеся дозы вакцины Рота-V-Эйд ® следует вводить согласно схеме вакцинации.
Согласно рекомендаций Всемирной Организации Здравоохранения, если плановая иммунизация начата позже 6 месяцев и/или интервал составляет более 4 недель, можно осуществлять введение вакцины Рота-V-Эйд ® самостоятельно либо с вакцинами АКДС, инактивированной полиомиелитной вакциной, оральной полиомиелитной вакциной, вакциной против Haemophilus influenzae типа b и против гепатита В.
Рекомендовано, чтобы дети, которые получали вакцину для профилактики ротавирусной инфекции, пентавалентную, живую для первой иммунизации против ротавируса, продолжали получать дозы этой же вакцины в дальнейшем (3 дозы).
Рекомендации по подготовке и проведению вакцинации
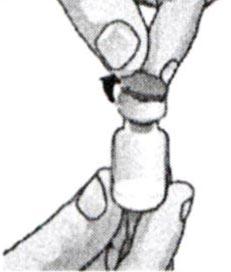
1. Снимите пластиковые колпачки с флаконов, содержащих растворитель и лиофилизат.
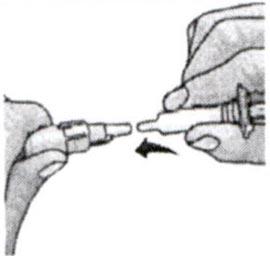
2. Присоедините адаптер и шприц к флакону с растворителем, нажав вниз до тех пор, пока наконечник надёжно не установится. Наберите весь растворитель в шприц.
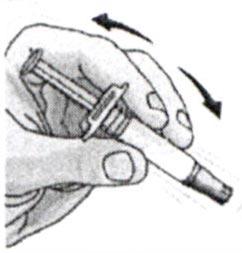
3. Уберите приспособление с флакона с растворителем. Встряхните шприц, содержащий растворитель.
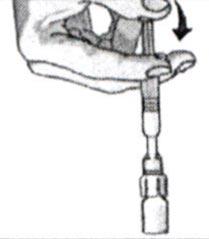
4. Введите всё содержимое шприца во флакон, содержащий лиофилизат.
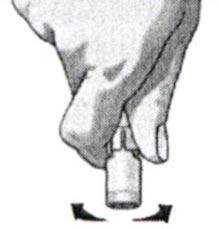
5. Встряхните флакон и просмотрите его, чтобы лиофилизат полностью растворился. Разведённая вакцина представляет собой прозрачный раствор от розоватого до желтоватого цвета.
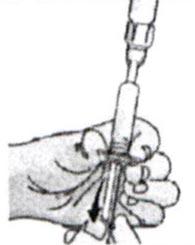
6. Наберите одну дозу (2,5 мл) восстановленного раствора вакцины обратно в шприц.
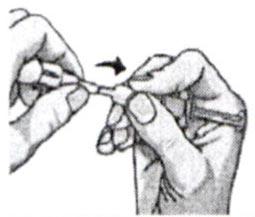
7. Отсоедините шприц от адаптера.
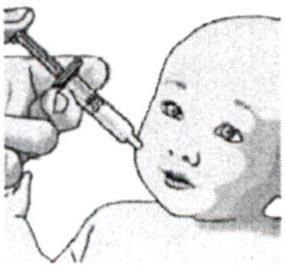
8. Осторожно введите всё содержимое шприца (одна доза 2,5 мл) в рот ребёнка (в направлении внутренней стороны щеки). Ребёнок должен находиться в положении полулежа.
Не вводить в виде инъекции!
Побочное действие
На основании объединенных данных 5 клинических исследований (более 15 000 участников) перечислены нежелательные реакции, частота которых в группе вакцины Рота-V-Эйд ® не превышала частоту в группе Плацебо.
- Инфекционные и паразитарные заболевания
Часто: инфекции нижних дыхательных путей, бронхиолит, бронхопневмония, воспаление лёгких, инфекции верхних дыхательных путей*.
Нечасто: назофарингит*, средний отит*.
- Нарушения со стороны иммунной системы
Неизвестно: анафилактическая реакция*.
- Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Редко: бронхоспазм*.
- Нарушения со стороны желудочно-кишечного тракта
Очень часто: гастроэнтерит, снижение аппетита, рвота, диарея.
Нечасто: гематохезия*, боль в верхних отделах живота*.
Редко: инвагинация кишечника**.
- Нарушения со стороны кожи и подкожных тканей
Нечасто: сыпь*.
Редко: крапивница*.
Неизвестно: ангиоэдема*.
- Общие расстройства и нарушения в месте введения
Очень часто: гипертермия, раздражительность.
*Данные нежелательные реакции возможны при применении вакцины Рота-V-Эйд ® и установлены в ходе проведения клинических исследований Вакцины для профилактики ротавирусной инфекции, пентавалентной, живой (РотаТек ® ).
** До начала первичного анализа нежелательных явлений возникло 7 случаев инвагинации кишечника, из которых 4 случая были в группе привитых вакциной для профилактики ротавирусной инфекции, пентавалентной, живой и 3 в группе Плацебо. Ни один случай не возник в течение 28 дней после введения вакцины Рота-V-Эйд ® .
Передозировка
О случаях передозировки вакцины Рота-V-Эйд ® не сообщалось.
Учитывая, что вакцинация должна проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Взаимодействие с другими лекарственными средствами
Вакцину Рота-V-Эйд ® можно вводить одновременно с другими вакцинами в рамках программы иммунизации детей, включая комбинированную вакцину против коклюша, дифтерии и столбняка (АКДС), инактивированную полиомиелитную вакцину (ИПВ), оральную полиомиелитную вакцину (ОПВ), вакцину против Haemophilus influenzae типа b (Hib) и против гепатита В. Исследования взаимодействия вакцины Рота-V-Эйд ® с другими лекарственными средствами у детей не проводились.
Иммуносупрессивная терапия, включая облучение, антиметаболиты, алкилирующие средства, цитотоксические средства и кортикостероиды (используемые в дозах больших, чем минимальные), могут снижать иммунный ответ на вакцинацию.
Особые указания
Данные по безопасности и эффективности вакцины Рота-V-Эйд ® у детей с ослабленным иммунитетом, детей, инфицированных ВИЧ или детей с хроническим гастроэнтеритом, отсутствуют.
Вакцину Рота-V-Эйд ® можно с осторожностью вводить детям с ослабленным иммунитетом и детям, находящимся в тесном контакте с лицами с иммунодефицитом, если, по мнению врача, польза значительно перевешивает риск вакцинации.
Острая инфекция или лихорадочное заболевание могут быть основанием для отсрочки введения вакцины Рота-V-Эйд ® .
Субфебрильная температура тела и инфекция верхних дыхательных путей лёгкой степени тяжести не являются противопоказанием к введению вакцины Рота-V-Эйд ® .
Доступные опубликованные данные показывают незначительное увеличение частоты возникновения инвагинации кишечника после введения других живых пероральных вакцин для профилактики ротавирусных инфекций, в особенности после введения первой дозы.
Данные по безопасности, полученные в клинических исследованиях вакцины Рота-V-Эйд ® , не показывают увеличения риска возникновения инвагинации кишечника. Однако медицинские работники должны тщательно оценивать случаи с симптомами, напоминающими инвагинацию кишечника. Подобно другим вакцинам для профилактики ротавирусных инфекций, иммунизация вакциной Рота-V-Эйд ® не может обезопасить всех реципиентов вакцины от ротавирусной инфекции.
Вакцина Рота-V-Эйд ® не обеспечивает защиту от гастроэнтерита, вызванного другими патогенными организмами.
Влияние на способность управлять транспортными средствами, механизмами
Исследований по изучению влияния вакцины на способность к управлению транспортными средствами и механизмами не проводилось.
Форма выпуска
Лиофилизат для приготовления раствора для приема внутрь, 2,5 мл/доза.
По 1 или 2 дозы лиофилизата во флаконах вместимостью 4 мл или 5 мл соответственно из бесцветного прозрачного стекла, укупоренных пробками из бромбутилкаучука серого цвета и завальцованных алюминиевыми колпачками с пластиковой крышечкой типа флип-офф лилового цвета.
По 2,5 мл (для 1 дозы вакцины) или 5,0 мл (для 2-х доз вакцины) растворителя во флаконах вместимостью 4 мл или 5 мл соответственно из бесцветного прозрачного стекла, укупоренных пробками из галогенбутилкаучука серого цвета и завальцованных алюминиевыми колпачками с пластиковой крышечкой типа флип-офф синего цвета.
Комплектность для 1 дозы вакцины
По 1 флакону с лиофилизатом вместимостью 4 мл, 1 флакону с растворителем вместимостью 4 мл с 1 адаптером и 1 стерильным одноразовым шприцем для перорального приема в прозрачном пластиковом контейнере. По 1 пластиковому контейнеру вместе с инструкцией по применению помещают в пачку картонную.
Комплектность для 2 доз вакцины
По 1 флакону с лиофилизатом вместимостью 5 мл, 1 флакону с растворителем вместимостью 5 мл с 1 адаптером и 2 стерильными одноразовыми шприцами для перорального приема в прозрачном пластиковом контейнере. По 1 пластиковому контейнеру вместе с инструкцией по применению помещают в пачку картонную.
Условия хранения
Лиофилизат
При температуре от 2 до 25 °С в защищенном от света месте.
Растворитель
При температуре от 2 до 25 °С в защищенном от света месте. Не замораживать!
Комплект (лиофилизат, растворитель, адаптер, шприц)
При температуре от 2 до 25 °С в защищенном от света месте. Не замораживать!
Хранить в недоступном для детей месте.
Срок годности
Лиофилизат: 30 месяцев.
Растворитель: 60 месяцев.
Срок годности комплекта указывается по наименьшему сроку годности одного из компонентов.
Не применять препарат по истечении срока годности.
Условия отпуска
Производитель
Серум Инститьют оф Индия Пвт. Лтд, Индия.
Serum Institute of India Pvt. Ltd.
Адрес: 212/2, Офф Соли Пунавалла Роуд, Хадапсар, Пуне-411028, Махараштра, Индия.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей
Рота-V-Эйд - цена, наличие в аптеках
Указана цена, по которой можно купить Рота-V-Эйд в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
Читайте также:

