Вирус чикунгунья вопросы вирусологии
Обновлено: 24.04.2024
Распространение и вспышки чикунгуньи
Вирус чикунгуньи был впервые выявлен в Танзании в 1952 г. и затем на протяжении примерно 50 лет выявлялся и становился причиной спорадических вспышек в Африке и Азии. Быстрое распространение чикунгуньи происходит начиная с 2004 г., и на сегодняшний день она выявлена в более чем 60 странах Азии, Африки, Европы и Америки.
В 2015 г. Европейский центр по профилактике и контролю заболеваний отметил снижение заболеваемости чикунгуньей по сравнению с 2014 г. до 624 случаев. Африканское региональное бюро ВОЗ (АФРО) зафиксировало вспышку в Сенегале – первый случай активной циркуляции вируса в этом районе за пять лет. В странах Америки региональное бюро Панамериканской организации здравоохранения (ПАОЗ) получило информацию о 693 489 подозрительных и 37 480 подтвержденных случаях заболевания чикунгуньей, из которых наибольшее бремя болезни – 356 079 случаев – пришлось на Колумбию. Вместе с тем бремя чикунгуньи в странах Америки было значительно ниже, чем в предыдущем году.
Передача инфекции
Вирус чикунгуньи передается от человека к человеку комарами. Наивный к вирусу (неинфицированный) комар может стать переносчиком вируса в результате всасывания крови виремичного лица (у которого вирус циркулирует в крови) при укусе. Затем вирус в течение некоторого времени реплицируется в организме комара, после чего он может быть передан новому наивному хозяину при следующем укусе. В организме нового инфицированного лица вирус вновь размножается и достигает высоких концентраций. Если в период циркуляции вируса в крови зараженного его кусает комар, вирусные частицы могут передаться комару, в результате чего начнется следующий цикл передачи.
Репликация вируса в организме комара происходит в средней кишке. Затем инфекция проникает во вторичные ткани, в том числе слюнные железы. CHIKV способен передаваться новому наивному хозяину быстрее, другие передаваемые комарами вирусы; в ходе лабораторных экспериментов было показано, что вирус может быть обнаружен в слюне уже через 2–3 дня после всасывания крови [1]. Это дает основания предполагать, что длительность полного цикла передачи инфекции от человека к комару и обратно может составлять не более недели. Считается, что после инфицирования комар способен передавать вирус в течение всей своей жизни.
В цикле передачи чаще всего участвуют комары Aedes aegypti и Aedes albopictus. Оба вида могут также передавать другие арбовирусные инфекции, включая вирусы денге и лихорадки зика.
Экология переносчиков инфекции
Крупные вспышки чикунгуньи вызываются комарами как вида Ae. Aegypti, так и вида Ae. Albopictus. Если ареал Ae. Aegypti ограничивается тропиками и субтропиками, то Ae. Albopictus обитает также в районах с умеренным и даже умеренно-холодным климатом. Эти комары могут кусать людей в течение всего светлого времени суток, однако пик их активности приходится на раннее утро и конец второй половины дня. Оба вида комаров кусают людей вне помещений, а Ae. Aegypti – также внутри помещений.
По сравнению с комарами Ae. Aegypti для размножения Ae. Albopictus подходит более широкий спектр емкостей, заполненных водой, включая скорлупу кокосовых орехов, стручки какао-бобов, обломки бамбука, дупла деревьев и скальные углубления, а также искусственные емкости, такие как автопокрышки и поддоны под цветочными горшками. Такое разнообразие мест обитания объясняет распространенность комаров Ae. Albopictus в сельских и пригородных районах, а также в тенистых городских парках. За последние десятилетия Ae. Albopictus проник из Азии в районы Африки, Европы и Америки. Расширение ареала обитания этого компетентного переносчика, а также увеличение частоты завозных случаев повышает вероятность местной передачи вируса в ранее не затронутых им районах.
Вид Ae. Aegypti более тесно привязан к человеческому жилью и использует для размножения места внутри помещений, в том числе цветочные вазы, сосуды для хранения воды и бетонные емкости для воды в ванных комнатах, а также те же искусственные емкости вне помещений, что и Ae. albopictus.
В Африке в передаче заболевания задействованы также и некоторые другие виды комаров, включая виды из группы A. furcifer-taylori и A. luteocephalus. Имеются фактические данные о том, некоторые животные, в том числе не относящиеся к приматам, грызуны, птицы и мелкие млекопитающие могут выступать резервуарами вируса, вызывая повторные волны его распространения после периодов неактивности у людей.
Характеристики заболевания (признаки и симптомы)
Симптомы заболевания обычно появляются через 4–8 дней после укуса человека инфицированным комаром, но этот период может составлять от 2 до 12 дней. Для чикунгуньи характерна внезапная лихорадка, часто сопровождаемая болью в суставах. Боль в суставах часто бывает очень изнурительной; она обычно проходит через несколько дней, но может длиться неделями, месяцами и даже годами. Поэтому данная вирусная инфекция может протекать в острой, подострой или хронической формах. Другие распространенные признаки и симптомы заболевания включают боль в мышцах, отеки суставов, головную боль, тошноту, усталость и сыпь.
Обычно заболевание протекает с легкими симптомами, повышая вероятность невыявления или неправильной диагностики инфекции. По своей симптоматике данная инфекция может напоминать другие арбовирусы; чикунгунью часть принимают за денге в районах одновременной циркуляции этих вирусов [2]. Однако в отличие от денге чикунгунья редко вызывает жизнеугрожающие состояния.
В большинстве случаев перенесшие инфекцию пациенты полностью выздоравливают, однако в некоторых случаях могут в течение нескольких месяцев или даже лет страдать болями в суставах. После выздоровления у пациента с большой вероятностью остается иммунитет, защищающий его от дальнейших инфекций.
Диагностика
Для диагностики вирусной инфекции чикунгунья можно применять несколько методов. Наличие антител IgM и IgG к вирусу чикунгуньи может быть подтверждено серологическими исследованиями, такими как как иммуносорбентный анализ с применением фиксированных ферментов (ELISA). Самые высокие концентрации антител IgM достигаются через 3–5 недель после наступления болезни и сохраняются примерно в течение двух месяцев.
Кроме того, в течение нескольких первых дней после инфицирования вирус может быть выявлен непосредственно в крови. Поэтому образцы, взятые в течение первой недели после появления симптомов, должны исследоваться при помощи как серологических, так и вирусологических методов (в частности методом полимеразной цепной реакции с обратной транскрипцией, ОТ-ПЦР). При всем разнообразии применяемых методов ОТ-ПЦР они имеют различную чувствительность. Некоторые из них подходят для клинической диагностики. Полученные из клинических образцов продукты ОТ-ПЦР могут быть также использованы для генотипирования вируса, что позволяет сравнивать образцы вирусов из различных географических районов.
Лечение
Каких-либо специальных противовирусных препаратов для лечения чикунгуньи нет. Оказание помощи пациенту направлено, главным образом, на облегчение симптомов, в том числе боли в суставах, с помощью жаропонижающих средств, оптимальных болеутоляющих препаратов, обильного питья и режима покоя.
Для облегчения боли и снижения температуры тела рекомендуются такие препараты, как парацетамол или ацетаминофен. С учетом сходства симптомов чикунгуньи и денге в районах одновременной циркуляции обоих вирусов пациенты с подозрением на чикунгунью должны до момента исключения диагноза денге избегать приема аспирина и нестероидных противовоспалительных препаратов (НПВП) (поскольку у пациентов с денге эти препараты могут повышать риск кровотечения).
Вакцинация против чикунгуньи
Профилактика и борьба
Пациентам с установленной чикунгуньей следует избегать дальнейших укусов комаров в течение первой недели заболевания. Поскольку в этот период времени вирус может циркулировать в крови, он может передаваться другим комарам, которые, в свою очередь, могут заражать других людей.
Близость мест размножения комаров-переносчиков заболевания к человеческому жилью является значительным фактором риска заболевания чикунгуньей и другими болезнями, передаваемыми комарами Aedes. В настоящее время единственным способом противодействия передаче вируса чикунгуньи и профилактики заболеваемости является борьба в комарами-переносчиками. Основным методом профилактики и борьбы с заболеванием является уменьшение количества естественных и искусственных резервуаров воды, служащих средой обитания и размножения комаров. Для этого среди населения районов распространения инфекции и районов повышенного риска следует проводить еженедельные мероприятия по опорожнению и чистке емкостей с водой, поскольку это позволяет сдерживать размножение комаров и последующее появление взрослых особей. Систематические мероприятия на местах по уничтожению мест размножения комаров могут быть эффективной тактикой сокращения популяций переносчиков.
Во время вспышек заболевания могут применяться инсектициды, которые можно распылять в воздухе для уничтожения летающих комаров, наносить на внутренние и внешние поверхности емкостей, на которые садятся комары, и использовать для обработки воды в емкостях для уничтожения незрелых личинок. Данные меры могут также применяться органами здравоохранения в качестве экстренной меры по ограничению популяции комаров.
В целях защиты во время вспышек чикунгуньи рекомендуется носить одежду, которая максимально закрывает кожу от укусов комаров в дневное время. Открытые участки кожи или одежду можно опрыскивать репеллентами в строгом соответствии с указаниями, содержащимися в аннотациях. Репелленты должны содержать DEET (N, N-диэтил-3-метилбензамид), IR3535 (3-[N-ацетил-N-бутил]-этиловый эфир аминопропионовой кислоты) или икаридин (1-пипеколиновая кислота, 2-(2-гидроксиэтил)-1-метилпропиловый эфир).
Поскольку максимальная пищевая активность комаров, передающих чикунгунью, наблюдается в дневные часы, эффективную защиту лиц, спящих в дневное время, особенно детей раннего возраста, больных и пожилых людей, можно обеспечивать при помощи обработанных инсектицидом противомоскитных сеток. Лица, совершающие поездки в районы повышенного риска, должны соблюдать элементарные меры предосторожности, в том числе пользоваться репеллентами, носить одежду с длинными рукавами и брюки и следить за тем, чтобы помещения были оснащены оконными сетками для предотвращения проникновения насекомых.
Деятельность ВОЗ
ВОЗ принимает следующие меры по борьбе с чикунгуньей:
- содействие странам в подтверждении вспышек через сеть сотрудничающих лабораторий;
- предоставление странам технической и методической поддержки по вопросам эффективной борьбы со вспышками болезней, передаваемой комарами;
- мониторинг разработки новых средств борьбы с заболеванием, в том числе инсектицидов и технологий их нанесения;
- разработка научно обоснованных стратегий, мер политики и планов по противодействию вспышкам;
- предоставление странам технической и методической поддержки по вопросам эффективного оказания помощи заболевшим и противодействия вспышкам;
- содействие странам в вопросах модернизации существующих систем отчетности;
- организация совместно с рядом сотрудничающих центров региональных учебных мероприятий по вопросам клинического ведения пациентов, диагностики и борьбы с переносчиками;
- публикация для государств-членов руководств и справочников по эпидемиологическому надзору, лабораторному обеспечению, клиническому ведению случаев и борьбе с переносчиками.
ВОЗ рекомендует странам создать и поддерживать ресурсную базу, необходимую для выявления и подтверждения случаев заболевания, ведения пациентов и осуществления стратегий информирования общественности в целях сокращения популяций комаров-переносчиков.
Цитируемые ссылки
[1] Dubrulle, M., et al., Chikungunya virus and Aedes mosquitoes: Saliva is infectious as soon as two days after oral infection. PLOS ONE, 2009. 4(6): p. e5895.
[2] Silva, M.M.O., et al., Concomitant Transmission of Dengue, Chikungunya, and Zika Viruses in Brazil: Clinical and Epidemiological Findings From Surveillance for Acute Febrile Illness. Clinical Infectious Diseases, 2018.
[3] Goyal, M., et al., Recent development in the strategies projected for chikungunya vaccine in humans. Drug Design Development and Therapy, 2018. 12: p. 4195-4206.
Лихорадка чикунгунья (ЛЧ) представляет собой природно-очаговое вирусное заболевание с трансмиссивным механизмом передачи комарами семейства Aedes. Все увеличивающиеся миграционные потоки привели к заносу инфекции в новые регионы и, следовательно, к расширению ареала болезни, включая европейские страны. Для ревматологов ЛЧ представляет несомненный интерес, в первую очередь в связи с развитием выраженного суставного синдрома (артралгии/артриты), развивающегося на всех стадиях болезни. В настоящем обзоре представлены данные об этиологии, патогенезе и эпидемиологии ЛЧ. Подробно изложена клиническая картина, методы диагностики и дифференциальная диагностика, а также основные подходы к терапии этого заболевания.
Ключевые слова
Об авторах
Борис Сергеевич Белов
115522, Москва, Каширское шоссе, 34А
115522, Москва, Каширское шоссе, 34А
115522, Москва, Каширское шоссе, 34А
Литература
2. Ларичев ВФ, Сайфуллин МА, Акиншин ЮА и др. Завозные случаи арбовирусных инфекций в Российской Федерации. Эпидемиология и инфекционные болезни. 2012;(1):35-8.
3. Rezza G. Chikungunya is back in Italy: 2007-2017. J Travel Med. 2018 Jan 1;25(1). doi: 10.1093/jtm/tay004.
4. Delisle E, Rousseau C, Broche B, et al. Chikungunya outbreak in Montpellier, France, September to October 2014. Euro Surveill. 2015 Apr 30;20(17). pii: 21108.
5. Chow A, Her Z, Ong EK, et al. Persistent arthralgia induced by Chikungunya virus infection is associated with interleukin-6 and granulocyte macrophage colony-stimulating factor. J Infect Dis. 2011 Jan 15;203(2): 149-57. doi: 10.1093/infdis/jiq042.
8. Runowska M, Majewski D, Niklas K, Puszczewicz M. Chikungunya virus: a rheumatologist's perspective. Clin Exp Rheumatol. 2018 May-Jun;36(3):494-501. Epub 2018 Mar 2.
9. Marques CDL, Duarte ALBP, Ranzolin A, et al. Recommendations of the Brazilian Society of Rheumatology for diagnosis and treatment of Chikungunya fever. Part 1 – Diagnosis and special situations. Rev Bras Reumatol Engl Ed. 2017;57 Suppl 2:421-437. doi: 10.1016/j.rbre.2017.05.006. Epub 2017 Jul 25.
10. Economopoulou A, Dominguez M, Helynck B et al. Atypical Chikungunya virus infections: clinical manifestations, mortality and risk factors for severe disease during the 2005-2006 outbreak on Reunion. Epidemiol Infect. 2009 Apr;137(4):534-41. doi: 10.1017/S0950268808001167/
11. Josseran L, Paquet C, Zehgnoun A, et al. Chikungunya disease outbreak, Reunion Island. Emerg Infect Dis. 2006 Dec;12(12): 1994-5.
12. Oliver M, Grandadam M, Marimoutou C, et al. Persisting mixed cryoglobulinemia in Chikungunya infection. PLoS Negl Trop Dis. 2009;3(2):e374. doi: 10.1371/journal.pntd.0000374. Epub 2009 Feb 3.
14. Essackjee K, Goorah S, Ramchurn SK, et al. Prevalence of and risk factors for chronic arthralgia and rheumatoid-like polyarthritis more than 2 years after infection with chikungunya virus. Postgrad Med J. 2013 Aug;89 (1054):440-7. doi: 10.1136/postgradmedj2012-131477.
15. Manimunda SP, Vijayachari P, Uppoor R, et al. Clinical progression of chikungunya fever during acute and chronic arthritic stages and the changes in joint morphology as revealed by imaging. Trans R Soc Trop Med Hyg. 2010 Jun;104(6):392-9. doi: 10.1016/j.trstmh.2010.01.011.
16. Bouquillard E, Combe B. A report of 21 cases of rheumatoid arthritis following Chikungunya fever. A mean follow-up of two years. Joint Bone Spine. 2009 Dec;76(6): 654-7. doi: 10.1016/j.jbspin.2009.08.005.
17. Simon F, Javelle E, Cabie A, et al. French guidelines for the management of chikungunya (acute and persistent presentations). November 2014. Med Mal Infect. 2015 Jul; 45(7):243-63. doi: 10.1016/j.medmal.2015. 05.007.
18. Parola P, de Lamballerie X, Jourdan J, et al. Novel chikungunya virus variant in travelers returning from Indian Ocean islands. Emerg Infect Dis. 2006 Oct;12(10):1493-9.
20. Rosario V, Munoz-Louis R, Valdez T, et al. Chikungunya infection in the general population and in patients with rheumatoid arthritis on biological therapy. Clin Rheumatol. 2015 Jul; 34(7):1285-7. doi: 10.1007/s10067-015-2979-x.
22. Региональная рамочная программа по эпиднадзору и борьбе с инвазивными видами комаров-переносчиков и возвращающимися трансмиссивными болезнями 2014–2020. ВОЗ; 2013. 35 с.
23. Zaid A, Gerardin P, Taylor A, et al. Chikungunya Arthritis: Implications of Acute and Chronic Inflammation Mechanisms on Disease Management. Arthritis Rheumatol. 2018 Apr;70(4):484-495. doi: 10.1002/art.40403. Epub 2018 Mar 23.
24. Miner JJ, Lenschow DJ. Editorial: Lessons Learned From Chikungunya in the Americas. Arthritis Rheumatol. 2018 Apr;70(4): 477-479. doi: 10.1002/art.40421. Epub 2018 Mar 13.
2. Ларичев В.Ф., Сайфуллин М.А., Акиншина Ю.А., Хуторец-кая Н.В., Бутенко А.М. Завозные случаи арбовирусных инфекций в Российской Федерации // Эпидемиология и инфекционные болезни. – 2012. – № 1. – С. 35-38.
4. Bouquillard E., Combe B. A report of 21 cases of rheumatoid arthritis following Chikungunya fever. A mean follow-up of two years // Joint Bone Spine. – 2009. – Vol. 76 (6). – P. 654-657.
5. Chandrakant L., Pradhan S.K. Emergence of chikungunya virus in Indian subcontinent after 32 years: a review // J. Vect Borne Dis. – 2006. – 43. – P. 151-160.
7. Gerardin P., Fianu A., Malvy D. et al. Perceived morbidity and community burden after a Chikungunya outbreak: the TELECHIK survey, a population-based cohort study // BMC Med. – 2011. – 9. – 5. – Published online 2011 Jan 14. – DOI: 10.1186/1741-7015-9-5.
8. Grandadam M., Caro V., Plumet S. et al. Chikungunya virus, southeastern France // Emerg Infect Dis. – 2011. – May. – Vol. 17, № 5. – P. 910-913. – DOI: 10.3201/eid1705.101873.
10. Javelle E., Ribera A., Degasne I. et al. Specific Management of Post-Chikungunya Rheumatic Disorders: A Retrospective Study of 159 Cases in Reunion Island from 2006-2012 // PLoS Negl Trop Dis. – 9 (3). – e0003603. – DOI:10.1371/journal. pntd.0003603.
11. Khairallah M., Phaik Chee Soon., Rathinam S.R. et al. Novel infectious agents causing uveitis // Int Ophthalmol. – 2010. – 30. – 465-483.
12. Lalitha P., Rathinam S., Banushree K. et al. Ocular involvement associated with an epidemic outbreak of chikungunya virus infection // American Journal of Ophthalmology. – 2007. – № 144. – P. 552-556.
13. Lumsden W.H. An epidemic of virus disease in Southern Province, Tanganyika Territory, in 1952–53. II. General description and epidemiology // Trans. R. Soc. Trop. Med. Hyg. – 1955. – 49 (1). – 33-57. – DOI:10.1016/0035-9203(55)90081-X. PMID 14373835.
16. Nasci R.S. Movement of Chikungunya Virus into the Western Hemisphere // Emerg Infect Dis. – 2014. – 20 (8). – 1394-1395. – DOI: 10.3201/eid2008.140333.
17. Rezza G., Nicoletti L., Angelini R. et al. Infection with chikungunya virus in Italy: an outbreak in a temperate region // Lancet. – 2007. – Dec. – 370 (9602). – 1840-1846.
19. Scripsema N.K., Sharifi E., Samson C.M. et al. Chikungunyaassociated uveitis and exudative retinal detachment: a case report // Retin Cases Brief Rep. – 2015. – Fall. – 9 (4). – P. 352-356. – DOI: 10.1097/ICB.0000000000000232.
21. Weaver S.C., Osorio J.E., Livengood J.A. et al. Chikungunya virus and prospects for a vaccine // Expert Review of Vaccines. - 2012. – № 9. – P. 1087-1101.
22. WHO. Guidelines on Clinical Management of Chikungunya Fever. World Health Organization, Regional Office for SouthEast Asia, Indraprastha Estate, Mahatma Gandhi Marg. – New Delhi, 2008
Инкубационный период при ЛЧ обычно составляет 2-6 дней [20, 22]. Для заболевания характерно острое начало с повышением температуры тела длительностью 2-10 дней, иногда двухволновая температурная кривая, лимфаденопатия, суставной синдром и экзантема [22]. Наиболее частые проявления у лиц, перенесших ЛЧ, – длительные артралгии и артриты [7, 22].
Интенсивность суставного синдрома, ассоциированного с ЛЧ, вариативна, а длительность может составлять от нескольких недель до 2 лет. [5]. Развитие ревматоидного артрита после перенесенного заболевания описано у лиц пожилого возраста [4, 6].
До 2006 г. поражение органа зрения при ЛЧ описано не было, однако в последующем описаны множественные варианты патологических изменений от доброкачественных до угрожающих осложнений [14, 19]. В острой фазе заболевания заинтересованность глаз может проявляться в виде светобоязни, ретроорбитальной боли и конъюнктивитом. Передний увеит и ретинит являются наиболее распространенными глазными осложнениями ЛЧ, составляя до 25% от всех поражений [12, 14, 15]. Описаны также неврит зрительного нерва, кератит, эписклерит, центральная окклюзия артерии сетчатки, экссудативная отслойка сетчатки [10, 11, 12, 19]. Патогенез поражения глаз при ЛЧ изучен недостаточно. В качестве основных гипотез выдвигаются как непосредственное воздействие вируса, так и дизрегуляция работы иммунной системы [14, 15].
На территории России регистрируются единичные завозные случаи ЛЧ [2, 3]. Осведомленность медицинских работников об эпидемиологии и течении ЛЧ остается низкой. В этой связи представляется важным клиническое наблюдение за пациенткой с ЛЧ, протекавшей с полиартралгией и панувеитом. Пациентка Ч., 28 лет, с 19 по 22 августа 2016 г. находилась в Индии (Нью-Дели) в служебной командировке. Отмечала укусы комаров. С 23.08 отметила повышение температуры до 38,7°С, озноб, появление сыпи на бедрах, груди, затем по всему телу, ломоту в голеностопных суставах, головную боль в затылочной области. По поводу сохраняющейся лихорадки принимала антипиретики. Была осмотрена врачом 24.08, заподозрено течение краснухи. На следующий день больная обратила внимание на увеличение шейных лимфоузлов, появление зудящей сыпи на руках на фоне сохраняющейся субфебрильной температуры. Самостоятельно обратилась в Инфекционную клиническую больницу № 1. В анамнезе жизни – хронических заболеваний не отмечено. У отца пациентки глаукома, получает антиглаукоматозные препараты.
При поступлении в больницу состояние средней тяжести. В сознании, менингеальной и очаговой симптоматики нет. Кожа загорелая. На туловище, руках не яркая мелкая пятнистая сыпь с невыраженным зудом. Слизистая ротоглотки розовая, чистая. Выраженный конъюнктивит справа. Периферические лимфоузлы: затылочные до 0,5 см. Заднешейные до 1 см, подмышечные и паховые до 1,5 см, чувствительные при пальпации, не спаянные с тканями, подвижные. Кожа над ними не изменена. В легких дыхание везикулярное, проводится во все отделы, хрипов нет. Тоны сердца громкие, ритмичные. Живот мягкий, безболезненный, доступный пальпации. Печень, селезенка не увеличены. Симптом поколачивания отрицательный. Стул и диурез не нарушены. Дизурии нет.
В анализе крови от 29.08: гемоглобин 125 г/л, лейкоциты 2,8×109/мл, тромбоциты 173×109/мл, нейтрофилы 52%, лимфоциты 30%, моноциты 14%, базофилы 3%, эозинофилы 1%, с-реактивный белок (СРБ) 6 мг/л.
В биохимическом анализе отклонений от нормы не выявлено. При обследовании на малярию методом толстой капли малярийные плазмодии не обнаружены. В стационаре осмотрена офтальмологом. Заключение офтальмолога: острый вирусный конъюнктивит.
Осмотрена на кафедре офтальмологии педиатрического факультета РНИМУ им. Н.И. Пирогова. Острота зрения правого глаза (ОД) 0,3 н/к, левого глаза (OS) 0,9. Глазные щели симметричны. Подвижность глазных яблок в полном объеме, слегка болезненна.
ОД – смешанная инъекция глазного яблока слабовыраженная. Отделяемого из конъюнктивальной полости нет. Роговица – запотелость эндотелия, единичные мелкие преципитаты. Передняя камера – равномерная, влага прозрачная. Зрачок узкий, плохо реагировал на свет. При инстилляции мидриатиков расширялся до 3,5-4 мм неравномерно, вытянут по диагонали за счет образования задних синехий. Хрусталик прозрачный. В стекловидном теле – нежная взвесь клеточных элементов. Глазное дно – рефлекс розовый.
Поставлен диагноз: острый передний вирусный экссудативно-пролиферативный увеит правого глаза. Назначен курс противовоспалительной, противовирусной, антибактериальной терапии (местно). Введен противовоспалительный препарат Дипроспан ретробульбарно по 0,5 мл 1 раз в 10 дней № 3. Одновременно получала сосудоукрепляющие препараты, антиоксиданты, мидриатики, десенсибилизирующие препараты. Курс лечения составил 4 недели.
Далее в период с ноября по январь дважды на фоне повышения температуры, симптомов общей интоксикации пациентка предъявляла жалобы на снижение остроты зрения, болезненность при движении глаз. При обследовании острота зрения правого глаза 0,5 н\к, левого глаза – 0,9. Глазные щели симметричны. Правый глаз – слабовыраженная смешанная инъекция, на эндотелии роговицы множественные мелкие преципитаты, запотелость эндотелия, передняя камера средней глубины, влага прозрачна, радужка – слегка стушеван рисунок, в цвете не изменена, зрачок под действием мидриатиков расширялся равномерно до 4-5 мм, в стекловидном теле нежные дистрофические изменения, глазное дно – рефлекс розовый, диск зрительного нерва бледно-розового цвета с четкими контурами, а:в=1:2. Левый глаз – здоров.
Авторефрактометрия OD sph -0,75 дптр, OS sph – 0,5 дптр.
Пациентка получала курсы противовирусной, антибактериальной, противовоспалительной терапии в сочетании с ангиопротекторами, антиоксидантами, мидриатиками и нейротрофическими препаратами. После окончании курса лечения острота зрения восстанавливалась до возрастной нормы.
В связи с суставными болями проводилась терапия ибупрофеном (600 мг в сутки) в течение одной недели с положительной динамикой, однако после завершения курса возобновилась боль в голеностопных суставах, появилась артралгия плечевых суставов, отмечена болезненность и небольшая гиперемия в области реберно-грудинных суставов. При этом сохранялась выраженная слабость, снижение работоспособности.
При осмотре 20 сентября (28 день от начала заболевания) пациентка предъявляла жалобы на слабость, нечеткость зрения, боли в области грудины, в плечевых суставах, усиливающиеся при поднятии предметов. В клиническом анализе крови отклонений не выявлено, с-реактивный белок, ревматоидный фактор – не обнаружены. При исследовании слезной жидкости методом полимеразной цепной реакции (ОТ-ПЦР) фрагменты нуклеиновой кислоты (РНК) вируса не обнаружены. Был проведен повторный курс противовоспалительной терапии (ибупрофен 600 мг в сутки в течение 2 недель). Для коррекции астенического синдрома был назначен адамантил-бромфениламин в дозе 100 мг в сутки.
При осмотре 7 октября (45 день от начала заболевания) – состояние пациентки удовлетворительное, у нее сохраняется не выраженная слабость, нечеткость зрения. В общеклиническом анализе крови изменений не выявлено. Рекомендовано постепенное увеличение физических нагрузок.
Осмотр 25 ноября (3 месяца от начала заболевания): жалобы на тянущие ощущения в лучезапястных суставах при поднятии тяжестей. Со стороны других суставов жалоб нет. Объективно состояние удовлетворительное. Температура тела нормальная. Кожа, слизистые чистые. Гиперемии, отечности суставов нет. Лимфатические узлы (подмышечные, паховые) до 1 см., паховые – чувствительные при пальпации. В общем анализе крови: лейкоциты 5,5×109/л, нейтрофилы 58%, лимфоциты 36%, моноциты 6%, СОЭ 20 мм/ч., с-реактивный белок, антистрептолизин О – отрицательные.
Дополнительно проведено обследование сыворотки на маркеры аутоиммунных заболеваний.
Напряженная эпидемиологическая ситуация по арбовирусным инфекциям в мире, сложившаяся в последние годы, служит веским основанием для дальнейшего исследования проблемы завозных тропических заболеваний. Благодаря мировому распространению лихорадка Чикунгунья считается изученной инфекцией, однако некоторые вопросы патогенеза, в том числе и соединительнотканных поражений при ЛЧ широко обсуждаются в мировой научной литературе. На территории РФ опыт диагностики и лечения данной патологии практически отсутствует.
Лихорадка Чикунгунья считается доброкачественным заболеванием, проходящим самостоятельно. Этиотропной терапии заболевания к настоящему времени не разработано. В острой фазе рекомендована оральная регидратация, прием нестероидных противовоспалительных препаратов для снижения температуры и обезболивания при выраженных артралгиях [22].
В случаях поражения суставов рекомендуется применение нестероидных противовоспалительных препаратов, физиотерапия, постепенное увеличение физических нагрузок. При развитии ревматоидного артрита рекомендована терапия системными кортикостероидами и метотрексатом (терапия моделируется в зависимости от возраста, пола, степени выраженности суставного синдрома, наличия факторов риска) [6, 10].
Лечение и диспансерное наблюдение при поражении глаз должно быть длительным, с назначением местной и системной противовоспалительной, антибактериальной, противовирусной терапии в острой период и назначение сосудоукрепляющих препаратов, антиоксидантов, нейротрофических препаратов в период ремиссии. Абсолютным показанием для назначения системных кортикостероидов служит наличие неврита зрительного нерва [14, 15].
Специфическая профилактика ЛЧ в настоящий момент не разработана. При посещении эндемичных регионов рекомендуется использование репеллентов, противомоскитных сеток, ношение одежды, препятствующей укусам комаров.
Таким образом, особенности течения лихорадки Чикунгунья представляют собой междисциплинарную проблему, требующую участия не только инфекционистов, но и специалистов в области офтальмологии и ревматологии. При развитии лихорадочного заболевания, ассоциированного с поездкой в эндемичный по лихорадке Чикунгунья и сопровождаемого экзантемой, лимфаденопатией, суставным синдромом, целесообразно проведение ряда обследований, направленных на верификацию заболевания, и при его выявлении – активное ведения пациента, как в остром лихорадочном периоде, так и диспансерное наблюдение не менее 6-12 мес. после перенесенного заболевания, с обязательным участием врачей-специалистов.
Необходимо также проведение первичной профилактики заболевания: информирование туристов, предотвращения укусов комаров в эндемичных регионах.
Сведения об авторах
Карань Людмила Станиславовна – науч. сотрудник ФБУН ЦНИИ эпидемиологии Роспотребнадзора
Лихорадка чикунгунья ‒ это острое вирусное инфекционное заболевание с трансмиссивным путем передачи, вызываемое одноименным арбовирусом. Специфическим проявлением лихорадки является воспаление суставов ‒ полиартриты. Для клиники болезни также характерны высокая лихорадка, симптомы интоксикации (слабость, утомляемость, снижение работоспособности, умеренная головная боль) и сыпи. Диагностика лихорадки основана на обнаружении самого возбудителя (вируса чикунгунья) и антител к нему в крови человека. Лечение симптоматическое: жаропонижающие и обезболивающие препараты, антигистаминные средства, вазопротекторы.
МКБ-10
Общие сведения

Причины
Возбудитель инфекции – РНК-содержащий вирус чикунгунья, классифицируемый как арбовирус (передающийся при укусе членистоногих), представитель семейства Тогавирусы, рода Альфавирус. Источниками и резервуарами инфекции являются больные люди, приматы и некоторые грызуны, переносчиками – самки комаров рода Aedes. В зависимости от вида данные комары могут обитать и нападать как снаружи (в утреннее время), так и внутри помещения (чаще всего комары обитают в вазах, поддонах для цветов и растений, в мисках для кормления домашних животных). Больной человек не представляет опасности для окружающих, но может послужить источником заражения комаров, а те – других людей.
Патогенез
Патогенез болезни изучен недостаточно. Считается, что при укусе самкой комара вместе со слюной вирус чикунгунья попадает в кровь человека. Возбудитель поражает эндотелий сосудов, в клетках которого активно размножается и накапливается, проникая затем в кровоток. Вирус чикунгунья проявляет тропность к суставной ткани, однако, имеются данные о вовлечении в патологический процесс сердечной мышцы, пищеварительного тракта, глаз и мозга. Поражение сосудистой стенки усиливает её проницаемость, что приводит к выходу плазмы и форменных элементов (в основном, эритроцитов) в ткани и клинически проявляется геморрагическим синдромом. Наличие и напряженность иммунитета после инфекции в настоящее время исследуются.
Симптомы лихорадки чикунгунья
Инкубационный период составляет 4-8 дней, в некоторых случаях может укорачиваться до 2-х суток либо удлиняться до 12 дней. Начало болезни всегда острое, внезапное на фоне удовлетворительного самочувствия. Характерно резкое повышение температуры тела, нередко сразу до высоких цифр (39 0 С и выше). Лихорадка сопровождается ознобами, резкой слабостью, потерей аппетита и мышечными болями.
Патогномоничным является возникновение сильнейших суставных болей, затрагивающих мелкие суставы: запястья, ступни, голеностопы, кисти. Суставы значительно увеличиваются в размерах, становясь практически неподвижными, а при попытке движения возникает резкая боль, несколько уменьшающаяся в покое. На ощупь суставы горячие, припухшие, с красноватой кожей над ними. Характерным для лихорадки является так называемый мигрирующий полиартрит ‒ суставные изменения переходят с одной конечности на другую, причем предыдущее поражение исчезает самостоятельно.
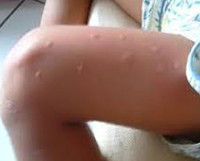
Пациенты часто предъявляют жалобы на боли в животе, срывы стула, тошноту и редко – рвоту. На коже верхней половины туловища, верхних и нижних конечностей у больных обнаруживается папулёзная (бугорковая) сыпь с выраженным зудом, проходящая затем с небольшим шелушением. Поскольку вирус чикунгунья патологически изменяет стенку сосудов, нередко возникновение петехиальных (точечных) высыпаний, десневых и носовых кровотечений.
Осложнения
В тяжёлых случаях возможно появление кровотечений из желудочно-кишечного тракта, мочеполовых путей, кровоизлияний в сетчатку глаза и головной мозг. После выздоровления может длительно сохраняться тугоподвижность суставов. Не исключается присоединение вторичной бактериальной инфекции в связи с инвазивными методами диагностики и лечения (забор крови, искусственная вентиляция лёгких, инъекции, установка внутривенных и мочевых катетеров), нередко развивается застойная пневмония. Смертельные исходы лихорадки чаще всего обусловлены поздним обращением за медицинской помощью и развитием синдрома диссеминированного внутрисосудистого свёртывания крови (ДВС-синдрома).
Диагностика
При подозрении на лихорадку чикунгунья обязательна консультация инфекциониста, дерматовенеролога и терапевта, при появлении симптомов поражения глаз и головного мозга – офтальмолога и невролога. Базовая диагностика инфекционной патологии включает в себя лабораторные и инструментальные методы:
- Определение инфекционных маркеров. Уже с первых дней заболевания удается выделить возбудителя из крови больного с помощью ПЦР. Методом ИФА исследование крови на наличие антител к вирусу чикунгунья проводят в динамике – при обращении пациента и через 14 дней. Для подтверждения диагноза необходим минимум двукратный рост титра антител.
- Клинико-биохимические исследования крови. В общем анализе крови при заражении вирусом чикунгунья наблюдается лейкопения и тромбоцитопения, ускорение СОЭ. Биохимические показатели отражают повышение уровня СРБ, активности трансаминаз (АЛТ, АСТ), реже – увеличение содержания билирубина.
- Лучевое исследование суставов. УЗИ суставов позволяет выявить наличие воспалительных изменений, в том числе суставного выпота. Рентгенологически поражение суставов при лихорадке чикунгунья не имеет выраженных морфологических признаков, поэтому артрография применяется, главным образом, с целью исключения других артропатий.
Дифференциальную диагностику проводят с другими геморрагическими лихорадками (денге, долины Рифт, крымской геморрагической, Ласса, Марбург и Эбола) и инфекциями (гриппом, лептоспирозом, малярией, гепатитом В, тифами и паратифами). Также необходимо исключить аутоиммунные васкулиты, онкологические заболевания, пневмонию, декомпенсацию сахарного диабета, пиелонефрит, мочекаменную болезнь, сепсис, сифилис и ревматоидный артрит.
Лечение лихорадки чикунгунья
Терапия проводится в инфекционном стационаре. Рекомендован постельный режим до 2-3-х дней устойчивого снижения температуры тела, применение противомоскитных сеток над кроватью, обильное питьё и частое дробное питание с исключением жирной, жареной пищи, алкоголя и приправ. На данном этапе развития медицины специфическое противовирусное лечение лихорадки чикунгунья не разработано; терапия заболевания симптоматическая (жаропонижающие, болеутоляющие, антигистаминные средства, препараты, укрепляющие сосудистую стенку). Применение аспирина и его аналогов при этой инфекционной патологии запрещено из-за возможного усиления геморрагического синдрома.
Прогноз и профилактика
Прогноз при своевременно выявленной инфекции благоприятный, различные осложнения и смертельные исходы чаще встречаются у ослабленных, пожилых лиц и детей. В популяции, где отсутствует иммунитет к болезни и имеются условия для массового выплода и существования комаров-переносчиков вируса чикунгунья, лихорадка способна передаваться быстрыми темпами и поражать большое количество здоровых лиц (что особенно заметно при ежегодных вспышках в африканских странах). При неосложненном течении болезнь длится около двух недель, при этом суставные боли самостоятельно проходят в 80% случаев. У части пациентов артралгии могут сохраняться более полугода после перенесенной инфекции.
Сообщается о создании вакцины против лихорадки чикунгунья, однако на сегодняшний день препарат еще проходит этапы регистрации. В дальнейшем вакцина может быть использована для иммунизации проживающих в районах с высокой заболеваемостью, а также для лиц, желающих их посетить с туристическими или трудовыми целями. Неспецифическая профилактика подразумевает борьбу с комарами, своевременное выявление и изоляцию больных. Лицам, находящимся в местах обитания переносчиков болезни, следует пользоваться одеждой закрытого типа, защитными сетками и репеллентами.
1. Геморрагические лихорадки у туристов и мигрантов (медицина путешествий). Ч.4/ Нечаев В.В., Шведов А.К., Погромская М.Н., Гришанова Г.И.; под ред. Ю.В. Лобзина. — 2015.
4. Случай лихорадки Чикунгунья: взгляд инфекциониста и офтальмолога/ Сайфуллин М.А., Жильцова Е.Ю., Обрубов С.А., Карань Л.С., Зверева Н.Н., Ларичев В.Ф., Бутенко А.М., Аксёнова И.И.// Российская детская офтальмология. – 2018 - №3.
Читайте также:

