Вирус эхо 1 при лечении рака
Обновлено: 26.04.2024
Многие вирусы — наши враги. Они вызывают опасные заболевания, некоторые из которых распространяются в масштабах крупных эпидемий и сильно меняют жизнь всего общества. За примерами далеко ходить не нужно — в 2020 году инфекция COVID-19, вызванная новым коронавирусом, унесла многие жизни и стала серьезным испытанием для мировой экономики.
Некоторые вирусные инфекции способствуют развитию онкологических заболеваний. Так, вирусы папилломы человека (ВПЧ) 16 и 18 типов являются причиной 70% случаев рака шейки матки, вирусные гепатиты B и C приводят к раку печени.
Еще в конце XIX века врачи заметили, что у некоторых онкологических пациентов, заразившихся вирусными инфекциями, происходил спонтанный регресс злокачественных опухолей. С тех пор онкологов не покидала идея найти или создать вирус, который мог бы прицельно уничтожать раковые клетки. Цель была достигнута только столетие спустя — в октябре 2015 года, когда Управление по контролю качества медикаментов и пищевых продуктов США (FDA) зарегистрировало T-VEC. Пока это единственный в своем роде препарат, но продолжаются поиски новых.

Лечение с лавинообразным эффектом
В настоящее время существует много разных препаратов для лечения рака: к классической химиотерапии добавилась таргетная терапия и иммунотерапия, изучаются новые молекулы, возможности применения наночастиц. Так чем же ученых так заинтересовали онколитические вирусы?
Хуан Фуэйо (Juan Fueyo), доктор медицинских наук из онкологического центра Андерсона Техасского университета (Texas MD Anderson Cancer Center), занимающийся созданием онколитических вирусов, отмечает:
Онколитическая вирусная терапия вызывает растущий интерес со стороны исследователей по одной причине: она работает.
Завербованный враг: какой вирус входит в состав Имлайджика?
Ученые смогли изменить ДНК вируса так, чтобы он заражал только опухолевые клетки. При этом злокачественная опухоль получает двойной удар:
Механизмы действия талимогена лахерпарепвека пока еще изучены не до конца, их можно схематически представить следующим образом:
Генетически модифицированный вирус вводят в злокачественную опухоль
Вирус поражает опухолевые клетки и активирует иммунный ответ
Когда зараженная клетка разрушается, из нее выходят новые копии вируса и поражают другие клетки
Как проводят лечение?
Имлайджик применяют для лечения прогрессирующей меланомы III–IV стадий, которая не может быть удалена хирургически. Это помогает затормозить прогрессирование заболевания и продлить жизнь пациента. Препарат вводят непосредственно в злокачественную опухоль. С помощью T-VEC можно лечить меланому разных локализаций:
- на поверхности кожи;
- под кожей;
- метастатические очаги в лимфатических узлах.
Первые две инъекции препарата проводят с интервалом в 3 недели. Затем введения повторяют через каждые 2 недели. Курс обычно продолжается не менее 6 месяцев. Врач рассчитывает дозу препарата, в зависимости от размеров и количества опухолей. Инъекция может быть сделана только в один очаг или в несколько разных.
Перед началом лечения пациент должен сообщить врачу обо всех своих сопутствующих заболеваниях и препаратах, которые принимает, особенно если это глюкокортикостероиды и другие лекарственные средства, подавляющие иммунитет, противовирусные препараты. Необходимо поставить врача в известность, если пациент находится в постоянном близком контакте с людьми, у которых ослаблена иммунная система.
Чем подтверждена эффективность препарата?
Талимоген лахерпарепвек был одобрен FDA в октябре 2015 года по результатам III фазы клинических испытаний, в которых показал высокую эффективность при прогрессирующей неоперабельной меланоме.
Эффективность препарата Имлайджик была изучена во время исследования, в котором приняли участие 436 пациентов с меланомой на стадиях IIIB/C (опухоль, которая распространилась в регионарные лимфоузлы, соседние ткани) и IV (меланома с отдаленными метастазами). Пациентов случайным образом поделили на две группы: одни получали талимоген лахерпарепвек, другие — гранулоцитарно-макрофагальный колониестимулирующий фактор. Были получены следующие результаты:
- У 48 (16,3%) из 295 пациентов, получавших Имлайджик, отмечался стойкий ответ, по сравнению с 2,1% (3 из 141 пациента) в контрольной группе. При этом у 14 (29,1%) из 48 пациентов, ответивших на лечение вирусом, отмечался стойкий полный ответ (исчезновение опухоли в течение 6 месяцев лечения и более), у 34 пациентов (70,8%) — стойкий частичный ответ (в течение 6 месяцев лечения и более опухоли уменьшились не менее чем на 50%).
- У 78 (26,4%) из 295 пациентов, получавших Имлайджик, меланомы уменьшились в два раза и более. Аналогичный эффект в контрольной группе отмечался только у 8 (5,7%) пациентов.
- В среднем у пациентов, получавших Имлайджик, ответ был достигнут через 4,1 месяца. При этом некоторые участники начали реагировать на лечение уже спустя 1,2 месяца, а некоторые — только через 16,7 месяца.
Также были проведены клинические испытания, которые показали хорошую эффективность онколитического вируса при меланоме в сочетании с иммунопрепаратами из группы ингибиторов контрольных точек — Пембролизумабом (Кейтруда), Ипилимумабом (Ервой). В настоящее время проводятся новые исследования, которые помогут лучше определить показания к применению талимогена лахерпарепвека самостоятельно и в комбинациях с другими препаратами.

Противопоказания и побочные эффекты
Как и всякий лекарственный препарат, талимоген лахерпарепвек может вызывать некоторые побочные эффекты. Чаще всего встречаются такие общие симптомы, как постоянное чувство усталости, повышенная утомляемость, озноб, повышение температуры тела, болезненность в месте введения препарата, проявления, напоминающие грипп.
Необходимо немедленно обратиться к врачу, если появились такие симптомы, как:
На данный момент известны пока еще не все побочные эффекты данного препарата, их изучение продолжается в клинических исследованиях и в рамках постмаркетинга.
Основные противопоказания к применению препарата:
- ВИЧ-инфекция.
- Прием глюкокортикостероидов и других препаратов, подавляющих иммунитет.
- Злокачественные заболевания крови, опухолевое поражение красного костного мозга.
- Другие иммунодефицитные состояния.
- Беременность.
Меры предосторожности
Несмотря на то, что вирус герпеса в препарате генетически модифицирован и ослаблен, он продолжает оставаться возбудителем инфекционного заболевания. Во время лечения нужно соблюдать некоторые меры, чтобы не допустить его распространения:
- После укола врач наложит повязку. Нельзя ее трогать, прикасаться к месту инъекции, чесать его.
- Место инъекции не должно соприкасаться с кожей других людей.
- Перед тем как самостоятельно менять повязку, нужно надеть медицинские перчатки. Это можно делать только с разрешения врача. Лучше, если смену повязки будут производить медицинские сотрудники в клинике.
- Как минимум в течение одной недели (или дольше, если имеется мокнутие) место укола нужно защищать повязкой, которая не допускает доступа воздуха и влаги.
- Если повязка перестала плотно держаться, ее нужно немедленно заменить.
- Снятую повязку и все средства, которыми обрабатывалось место укола, нужно сразу поместить в герметичный пакет, плотно закрыть, после чего его можно выбросить.
Поиски союзников в мире вирусов продолжаются
Терапия онколитическими вирусами — одновременно очень давнее и молодое направление в лечении онкологических заболеваний. Ученые уже целое столетие работают над созданием возбудителей, которые могли бы прицельно поражать раковые клетки, но первый и единственный препарат появился совсем недавно. Исследователи не планируют на нем останавливаться.
Большинство научных работ посвящено применению вирусов при меланоме и опухолях головного мозга. Классически такие препараты предлагается вводить непосредственно в злокачественное новообразование. Однако, в ходе одного исследования было обнаружено, что онколитический реовирус, введенный внутривенно, может успешно проникать в центральную нервную систему и находящуюся в ней опухолевую ткань. Этот возбудитель вызывает у человека симптомы простуды и кишечной инфекции.
В другом исследовании изучалось терапевтическое применение вируса Мараба как способ повысить эффективность химиотерапии при трижды негативном раке молочной железы у мышей. Эти злокачественные опухоли лишены рецепторов к гормонам и белка-рецептора HER2, и их сложно лечить.
Еще одним перспективным кандидатом в онколитические вирусы является возбудитель кори. В России в 2020 году успешно завершился доклинический этап испытаний генетически модифицированного онколитического вируса на основе вакцины против оспы.
Вирусные болезни как причина онкологических заболеваний - рака

Вирусные инфекции ответственны за развитие примерно 10-15% всех онкологических заболеваний у человека. Значимость вирусных инфекций в онкологии значительно возросла с возникновением эпидемии синдрома приобретенного иммунодефицита (СПИД), так как при этом заболевании смертность от рака преобладает в общем числе смертных случаев.
Механизмы вирус-индуцированного канцерогенеза будут обсуждаться в отдельной статье на сайте. Среди вирусов, наиболее часто ассоциируемых с онкологическими заболеваниями, находятся вирус Эпштейна-Барра (ВЭБ), герпесвирус саркомы Капоши ((ГСК) или герпесвирус человека серотипа 8 (ГВЧ8)) и вирус человеческой папилломы. Вирус ВЭБ вызывает лимфому Беркита и рак носоглоточной полости у небольшого процента зараженных им людей.
Лимфома наиболее часто встречается в районах Африки, прилегающих к пустыне Сахара, и в районах с эндемическими очагами малярии. Распространение саркомы Капоши также в основном характерно для близлежащим к Сахаре регионов и в большой степени этому заболеванию подвержены евреи, проживающие в средиземноморском регионе. Известно, что инфицированность ГВЧ8 тесно связана с риском развития саркомы в ходе течения связанных со СПИДом заболеваний.
ГВЧ8 также увеличивает риск развития многоцентровой болезни Каслемана и первичной эффузионной лимфомы. У жителей Италии и Северной Африки отмечается повышенное в сравнении с жителями Великобритании или США содержание антител к вирусу ГВЧ8 (ГСК).
Существенным фактором риска при развитии рака шейки матки являются папилломавирусы. Среди более 100 разновидностей этих вирусов наибольшую опасность представляют серотипы 16, 18, 31 и 33 (несколько менее опасны серотипы 6 и 11).
Рак могут вызывать и представители семейства ретровирусов. Наиболее общеизвестный пример — вирус Т-клеточной лейкемии, серотип 1 (ВТКЛ-1) который является эндемической инфекцией в южной Японии и на Карибском море. У жителей этих регионов опухоли развиваются только у незначительной части инфицированных. Вирус может передаваться от матери к ребенку во время беременности через плаценту, а также с молоком при кормлении. Возможна передача вируса через сперму.
ДНК-Содержащий вирус гепатита В передается через кровь или при половых контактах и вызывает гепатит и цирроз печени. Среди людей, пораженных таким вирусом, печеночно-клеточная карцинома встречается в 100 раз чаще, чем у неинфици-рованных. РНК-Содержащий вирус гепатита С также вызывает хронический гепатит и значительно повышает риск заболеваемости печеночно-клеточной карциномой.
Оба вируса широко распространены по всему миру, но особенно часто встречаются у жителей Китая и Тайваня, а также среди лиц, принимающих наркотики внутривенно. Эти два вируса являются основной причиной смертности от заболеваний раком печени.
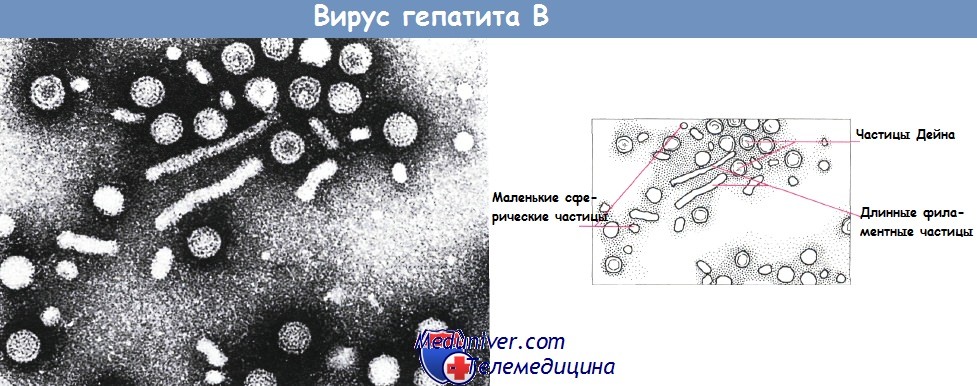
Электронная микрофотография вируса гепатита В.
На срезе видны мелкие сферические частицы с диаметром 28 нм (HBsAg); более крупные сферические двумембранные частицы Дейна (42 нм), продолговатые филаментозные частицы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Стадии онкологических заболеваний
Стадия рака — один из самых важных показателей, влияющих на прогноз и выбор тактики лечения. Для стадирования злокачественных опухолей врачи всего мира используют общепринятую классификацию TNM. Буквы в этой аббревиатуре обозначают размеры, степень инвазии (вторжения в ткани) и другие особенности первичной опухоли (T), распространение рака в регионарные лимфатические узлы (N) и наличие отдаленных метастазов (M). Рядом с каждой буквой ставят цифру или другое обозначение:
Классификация TNM довольно сложна. Чтобы ее упростить, разные значения T, N и M объединяют в пять групп, их обозначают римскими числами от 0 до IV. Практически любую злокачественную опухоль можно охарактеризовать одной из этих пяти стадий. Исключение составляют лимфомы, злокачественные заболевания крови и новообразования головного мозга — для них применяют свои системы стадирования.
Стадия 0
Стадия I
Раковые клетки начали вторгаться в окружающую ткань, но неглубоко, и сама опухоль имеет небольшие размеры, ее можно удалить хирургически. Как и при стадии 0, нет ни очагов в регионарных лимфоузлах, ни метастазов. Такие злокачественные опухоли тоже обычно не вызывают симптомов, и их сложно выявить. В этом помогают скрининговые исследования.
Стадия II
На этой стадии злокачественная опухоль имеет более крупные размеры, сильнее распространяется в окружающие ткани, может вторгаться в соседние органы, регионарные лимфоузлы. Такой рак зачастую можно удалить хирургически.
Стадия III
По сравнению со второй стадией, опухоли стадии III больше в размерах, сильнее распространяются в соседние анатомические структуры, поражают большее количество регионарных лимфоузлов. Тем не менее, радикальная операция зачастую все еще возможна.
Стадия IV
Обычно стадия IV — это рак с метастазами (метастатический рак). Раковые клетки распространяются с током лимфы (лимфогенно), крови (гематогенно) и образуют вторичные очаги в разных органах.
В онкологии есть правило: всегда указывать в диагнозе ту стадию опухоли, которая была установлена изначально. Например, если был диагностирован рак III стадии, а потом появились метастазы, врачи будут по-прежнему указывать III стадию, дописывая произошедшие изменения.
Описания стадий 0—IV, представленные выше, справедливы для большинства злокачественных опухолей, но бывают исключения. При разных типах рака стадии определяют немного по-разному. Поэтому, если вы хотите получить информацию о вашем заболевании, о том, что означает стадия в вашем случае, и каков прогноз — расспросите лечащего врача.
Помимо показателей T, N и M, важно учитывать и другие характеристики:
Важное значение имеет и тип рака. Например, злокачественные опухоли молочной железы, толстой кишки, простаты, щитовидной железы в настоящее время успешно лечатся даже при относительно поздних стадиях. А такие онкозаболевания, как рак поджелудочной железы, пищевода, печени характеризуются намного более низкими показателями пятилетней выживаемости на всех стадиях.
Можно ли победить рак IV стадии?
Единичные метастазы можно удалить, как и первичную опухоль. К сожалению, такие ситуации встречаются очень редко. Чаще всего вторичных очагов много, и их нельзя удалить полностью. Обычно ремиссия при IV стадии рака с метастазами невозможна.
В 2013 году у 49-летней Джуди Перкинс, инженера из Флориды (США), был диагностирован рак молочной железы IV стадии. Метастатические очаги уже распространились по ее телу, и радикальная операция была невозможна. Женщина проходила курсы химиотерапии, гормональной терапии, участвовала в клиническом исследовании нового таргетного препарата под названием Люцитаниб. Но болезнь продолжала прогрессировать. Врачи давали Джуди лишь несколько месяцев.
Спустя некоторое время у Джуди наступила ремиссия: опухолевые очаги в ее теле исчезли. Обследование спустя несколько лет показало, что болезнь не вернулась.
Этот метод борьбы с раком пока еще не применяется широко, он считается экспериментальным. Но кто знает, насколько бурно будет развиваться медицина в будущем, и какие возможности появятся?
Продолжительность жизни при разных стадиях рака
Для оценки продолжительности жизни при онкологических заболеваниях обычно используют показатель пятилетней выживаемости. Это процент больных, которые остались в живых спустя пять лет после установления диагноза. Он наиболее высок при ранних стадиях рака.
Вот примеры пятилетней выживаемости при IV стадии разных видов злокачественных опухолей (по данным Американского онкологического общества):
- рак молочной железы — 28%;
- немелкоклеточный рак легкого — 7%;
- мелкоклеточный рак легкого — 3%;
- рак толстой кишки — 16%;
- рак прямой кишки — 14%;
- рак желудка — 6%;
- рак поджелудочной железы — 3%;
- рак печени — 3%;
- рак предстательной железы — 30%;
- рак щитовидной железы — 3–76% (в зависимости от гистологического типа).
В каких случаях нельзя вылечить онкологию?
За редкими исключениями, единственный способ полностью избавиться от злокачественной опухоли — ее хирургическое удаление. В целом можно сказать, что неизлечимый рак — тот, при котором нельзя выполнить радикальную операцию:
- если имеется много метастазов в разных органах;
- если опухоль сильно проросла в соседние органы, вторглась в сосудистые и нервные пучки, критически важные анатомические структуры;
- если состояние пациента настолько плохое, что он, скорее всего, не перенесет хирургическое вмешательство.
Как артериальная гипертония и сахарный диабет
Лечить нужно не всегда
Даже такое грозное заболевание, как рак, нужно лечить не всегда. Самый яркий пример — злокачественные опухоли предстательной железы. Если заболевание прогрессирует медленно, а мужчине уже много лет, то вероятность того, что его убьет именно рак простаты, стремится к нулю. В таких случаях можно ограничиться просто наблюдением в динамике.
Можно ли излечиться, если произошел рецидив рака?
Чтобы ответить на этот вопрос, сперва нужно рассказать о видах рецидивов, в зависимости от локализации:
- Местные рецидивы возникают там же, где находилась первичная опухоль.
- Региональные рецидивы возникают рядом с местом локализации первичной опухоли или в регионарных лимфатических узлах.
- Отдаленные рецидивы возникают в виде метастазов в разных органах.
Что делать, если лечение не помогает?
К сожалению, любые противоопухолевые препараты помогают только в течение определенного времени. Затем в опухолевых клетках возникают новые мутации, и развивается лекарственная устойчивость — резистентность. В этом случае есть разные выходы:
Тем не менее, в последние десятилетия адекватная противовирусная терапия позволила не только улучшить результаты противоракового воздействия, но и в разы уменьшить вероятность развития злокачественного процесса у ответственного пациента.
Когда при ВИЧ появляются злокачественные опухоли
Рак и другие злокачественные опухоли развиваются при переходе ВИЧ-инфекции в позднюю стадию болезни, когда концентрация иммунных клеток устремляется к минимальной, позволяя активно и почти беспрепятственно размножаться разнообразной микрофлоре — от простейший и грибов до бактерий и вирусов.
Всё, что происходило в организме инфицированного пациента ранее, было обычной ВИЧ-инфекцией, появление рака или других опухолей, а также тяжёлых распространённых инфекций — это уже СПИД.
Благодаря лечению период от заражения вирусом иммунодефицита до последней стадии болезни растянулся почти на три десятилетия, тогда как в конце 1980-х годов занимал несколько лет.
Какие раки развиваются при ВИЧ-инфекции
В конце ХХ века выявление определённых, практически не встречающихся при нормальном иммунитете заболеваний и злокачественных процессов, позволяло ставить диагноз ВИЧ/СПИД без сложных лабораторных исследований. Такие процессы обозначили как ассоциированные с вирусом иммунодефицита или, по-современному, СПИД-индикаторные. В этот список наряду с необычными инфекциями включены инвазивный рак шейки матки, саркома Капоши и злокачественные лимфомы, вероятность которых у инфицированного пациента возрастает в сотни раз.
Значительно чаще, но не в сотни раз, при ВИЧ-инфекции вероятно развитие плоскоклеточного рака анального канала и рака вульвы, карциномы лёгкого и злокачественных опухолей яичка, плоскоклеточного рака головы и шеи, меланомы и рака кожи.
Для большинства злокачественных процессов доказана основополагающая патогенетическая роль вирусов, в первую очередь, папилломы человека (ВПЧ) и гепатита В, С и D. Способствует раннему развитию злокачественных новообразований носительство вирусов герпеса, особенно 4 типа — вируса Эпштейна-Барр. Традиционно значимы у ВИЧ-инфицированных факторы риска злокачественного перерождения клеток бронхолегочной системы — курение и наследственная предрасположенность.
Как ВИЧ-инфекция влияет на течение рака
Однозначно — очень неблагоприятно, усугубляя скорость прогрессирования и увеличивая массив опухолевого поражения. И хотя рак у ВИЧ-инфицированного пациента возникает много раньше, чем в общей популяции, практически в молодом возрасте, пациенты не могут похвастать исходным хорошим здоровьем.

Как ВИЧ сказывается на переносимости химиотерапии
В большинстве случаев злокачественный процесс на фоне ВИЧ-инфекции течёт агрессивнее, поэтому на первом этапе требует системного лечения с использованием противоопухолевых препаратов, гарантирующих разнообразный спектр токсических реакций. При этом ни в коем случае нельзя отказываться от специфической противовирусной терапии, также изобилующей неблагоприятными проявлениями.
В итоге переносимость противоракового лечения, проводимого на фоне ВААРТ, ухудшается, а продолжительность жизни пациентов не в пример короче, чем это могло быть в отсутствии ВИЧ. При активной противоопухолевой и противовирусной терапии больше года после выявления опухоли живёт только каждый четвёртый, пятилетку — всего 19%.
Существует ещё одна серьёзная проблема — клинического изучения эффективности противоопухолевой терапии у ВИЧ-инфицированных не проводится из-за малочисленности групп пациентов и, следовательно, сомнительной достоверности результатов. Поэтому очень важно в этот тяжёлый период найти клинику и специалистов одинаково высоко компетентных в вопросах лечения ВИЧ и противораковой химиотерапии.
Как лечат рак у ВИЧ-инфицированных
В большинстве случаев терапия рака не должна отличаться от таковой у пациентов с нормальными показателями иммунитета.
При технической возможности хирургической операции ВИЧ-пациенту от неё нельзя отказываться, поскольку излечение возможно только при удалении всех очагов рака. Если для злокачественной опухоли лимфатической системы признана необходимость высокодозной химиотерапии с трансплантацией стволовых клеток, то и инфицированный вирусом пациент должен получить программное лечение. При раке шейки матки практически невозможно обойтись без лучевой терапии.
ВИЧ-компрометированному пациенту потребуется ВААРТ и гораздо более серьёзное сопроводительное лечение. Чтобы провести химиотерапию без сокращения доз и интервалов необходима индивидуальная программа реабилитационного воздействия. Кроме того, пациент должен получать множество препаратов для лечения грибковых поражений и сдерживания вирусов герпеса, разнообразные антибактериальные средства, каждое из которых имеет собственную токсичность.

Такое комплексное воздействие способна осуществить только команда врачей разных специальностей, блестяще ориентированная как в потребностях онкологического пациента, так и в возможностях организма инфицированного.
Читайте также:

