Вирус герпеса краснухи при беременности
Обновлено: 19.04.2024
Л.А.МАРЧЕНКО, доктор медицинских наук, ведущий научный сотрудник отделения гинекологической эндокринологии. Герпетическая инфекция нередко является причиной гибели зародыша. Ее последствия могут привести к возникновению у плода пороков развития.
Вагинальные инфекции относятся к разряду наиболее часто встречающихся заболеваний нижнего отдела полового тракта. Патологические выделения из влагалища являются симптомом более 20 заболеваний, поэтому первоначально правильно установленный этиологический диагноз во многом не только определяет успех лечения, но и является гарантом отсроченных осложнений.
В последние годы наряду с общеизвестными микроорганизмами, вызывающими специфические и неспецифические инфекционные заболевания половых путей, все чаще диагностируются поражения, обусловленные вирусной инвазией гениталий, среди которых, несомненно, важная роль принадлежит вирусу простого герпеса (ВПГ).
Различают два типа ВПГ. Большинство вирусов составляет 2-ю, антигенную группу - ВПГ-2, которые преимущественно вызывают генитальную патологию, ВПМ вызывают экстрагенитальные поражения.
Пути передачи. Эпидемиология
Генитальный герпес (ГГ) относится к заболеваниям, передающимся половым путем (ЗППП).
Заражение может происходить в случае, когда у партнера, являющегося источником инфекции, на половых органах имеются типичные герпетические высыпания (рецидив заболевания) или, что особенно важно, когда он выделяет вирус, не имея при этом клинических симптомов заболевания (атипичная форма, или бессимптомное вирусоносительство).
Инфицирование возможно также при орогенитальных контактах. Бытовой путь переноса инфекции встречается крайне редко и полностью исключается, если секрет, содержащий вирус, высыхает.
Генитальный герпес может вызываться вирусом и 1-го и 2-го типа.
Известно, что степень распространенности ВПГ-2 инфекции зависит от пола обследуемых, числа их сексуальных партнеров, возраста, низкого образовательного уровня и этнической принадлежности. Исследования в 10 развитых странах показали, что серопозитивными на ВПГ-2 являются 107 млн. человек, при этом частота инфицирования в США составляет от 22 до 33%, в Европе - от 7 до 24%, в странах Индокитая - до 6%. Ситуация с инфицированием ГГ в России остается во многом крайне неясной, так как, хотя ГГ и отнесен в группу ЗППП, учет заболеваемости ведется плохо. Согласно проведенным в 1994 г. эпидемиологическим исследованиям на примере закрытой популяции в Москве, частота инфицирования генитальным герпесом составляет 19,7%. Выявлено два ее возрастных пика - 16-24 года и 35-40 лет. Женщины в 1,7 раза чаще инфицируются ВПГ-2, чем мужчины, подобных половых различий в инфицировании экстрагенитальным герпесом не выявлено.
Многие исследователи считают, что истинная ситуация в мире в отношении роста заболеваемости ГГ в достаточной мере не контролируется в связи со значительным процентом его асимптомных форм. Частота последних составляет 40-74%.
Нередко психосоциальные последствия ГГ бывают более выраженными и значимыми, чем физические страдания, связанные с частыми обострениями заболевания. ГГ, безусловно, влияет на качество жизни пациентов, т.к. уже с момента обращения к врачу перед ними возникает ряд психологических и медицинских проблем, среди которых ведущая роль принадлежит следующим: страх обнаружения вируса, депрессия; влияние на сексуальную и интимную жизнь; снижение социальной активности и изменение образа жизни; отношение к ГГ, как к болезни, передающейся половым путем; страх заразиться или быть зараженным; страх быть отвергнутым обществом; боязнь быть неизлеченным и т.д.
Клиника. Диагностические критерии
По особенностям клинических проявлений инфекции ГГ разделяют на типичный и атипичный.
Инкубационный период в среднем составляет 3-9 дней, в течение которых экспрессия вируса минимальна.
Острый период заболевания при типичной форме инфекции характеризуется обширными эрозивно-язвенными высыпаниями на слизистой больших и малых половых губ, промежности, влагалища, шейки матки. Ему всегда предшествует продромальный период, сопровождающийся субъективными ощущениями в виде боли, зуда, жжения, парестезий в области гениталий, а также общей симптоматикой - недомогание, озноб, лихорадка и т.д. При этом в 13-35% случаев наблюдается асептический менингит с тошнотой, рвотой, онемением затылка, головной болью. Все эти симптомы самостоятельно проходят с появлением высыпаний, в 10-15% отмечается фарингостоматит.
Довольно часто при первичном эпизоде заболевания отмечается поражение мочевой системы, проявляющееся от незначительной дизурии до стойкой задержки мочеиспускания, обусловленной отеком и резкой болезненностью в области уретры в результате обширных герпетических язв или вовлечения в воспалительный процесс слизистой оболочки мочевого пузыря и уретры.
Для ГГ характерна фиксированность очагов высыпания. В зависимости от локализации последних выделяют следующие стадии поражения:
I - наружные гениталии;
II - влагалище и шейка матки;
III - матка и область придатков.
Однако подобная стадийность весьма условна. После первичного эпизода заболевания под влиянием провоцирующих факторов периодически возникают рецидивы инфекции.
Анализ провоцирующих факторов показал, что наиболее часто обострение возникает на фоне стресса (78%); переутомления (56%); менструации (50%), перенесенной простуды (24%), в то время как ультрафиолетовое облучение, физические нагрузки и употребление алкоголя встречаются, соответственно, в 12, 10 и 6% случаев.
При ГГ рецидивы возникают в 50-75% случаев, что значительно выше показателей обострения при экстрагенитальной инфекции. Это объясняется особенностями антигенной структуры вируса 2-го типа.
Частота рецидивов у многих пациентов с годами снижается. Однако довольно часто после длительной ремиссии возникает период учащения рецидивов.
В зависимости от частоты обострений выделяют три степени тяжести ГГ:
тяжелое течение - ремиссии от нескольких дней до 6 недель;
средней тяжести - ремиссии от 2 до 3 месяцев;
легкое - ремиссии не менее 4 месяцев.
Клиническая картина рецидивов хронической генитальной герпетической инфекции разнообразна. В 50-85% случаев ей сопутствует продромальный период в виде чувства жжения, зуда, болезненности в очаге поражения. В 25% случаев выявляется болевой синдром - боль иррадиирует в ногу, пах, ягодицу. В 10% случаев появляются лимфаденит, общее недомогание, озноб.
В 70% случаев во время рецидива визуализируются микроскопические везикулезно-язвенные очаги, при рецидиве не обнаруживаются какие-либо патологические изменения, и обострение бывает трудно диагностировать без дополнительных лабораторных методов исследования. Рецидив протекает, как правило, легко, продолжительность высыпаний не превышает 3-5 дней, после чего слизистые или кожные покровы полностью эпителизируются.
Диссеминация ГГ наблюдается крайне редко, только в случаях тяжелой сопутствующей инфекции либо у больных с выраженным наследственным или приобретенным иммунодефицитом.
Диагностическим критерием наличия ГГ во многом являются местные проявления заболевания. Однако при атипичных формах отсутствует манифестный признак инфекции - сгруппированные везикулы, наполненные серозной жидкостью, трансформирующиеся в эрозии и язвы, что в значительной степени затрудняет постановку диагноза. Отдует особо подчеркнуть, часто подобный тип течения ГГ характерен в значительном проценте случаев с самого начала заболевания, поэтому первичный эпизод инфекции ретроспективно выявить бывает крайне трудно.
В настоящее время в 40-75% случаев ГГ протекает атипично - без появления характерных герпетических высыпаний, включая первичный эпизод заболевания.
На основании многолетних наблюдений и соотношения жалоб с данными вирусологических исследований нами были разработаны клинические критерии, позволяющие в большинстве случаев подтвердить герпетическую природу заболевания при атипичных формах инфекции. Ведущими среди них являются стойкий зуд и жжение вульвы и влагалища; кольпиты, не поддающиеся традиционной антибактериальной терапии; рецидивирующие эрозии и лейкоплакии шейки матки; привычное невынашивание беременности; стойкий вегетативный тазовый ганглионеврит (см. рис.).
СЕМИОТИКА АТИПИЧНОЙ ФОРМЫ ГЕНИТАЛЬНОГО ГЕРПЕСА
Значение этих критериев чрезвычайно важно для выявления групп инфицированных. Необходимо информирование больных о часто встречающихся атипичных симптомах заболевания в связи с возможностью бессимптомной передачи инфекции. Согласно данным отдельных исследователей, только 20% инфицированных ВПГ имеют диагностированный симптоматический герпес, 60% - нераспознанный симптоматический ГГ (атипичную форму) и 20% - бессимптомный герпес.
К четвертому, относительно редко встречающемуся варианту течения инфекции относят бессимптомный герпес, или вирусоносительство, при котором нет никаких клинических проявлений инфекции, однако в образцах слизи из цервикального канала или в мазках-отпечатках с половых органов выявляется вирус герпеса.
Знание этих вариантов течения инфекции важно для разработки тактики ведения беременных, страдающих ГГ.
Существует три основных механизма инфицирования плода ВПГ-2:
- вирусы из влагалища и шейки матки могут проникать к плодному яйцу восходящим путем или эмбрион может быть инфицирован во время имплантации инфицированной спермой;
- трансплацентарный переход вирусов к плоду при наличии их в крови беременных;
- заражение плода при прохождении через инфицированные родовые пути.
Последствиями герпетической инфекции являются гибель зародыша, пороки развития (микроцефалия, хориоретинит, дисплазия сетчатки, микрофтальмия, помутнение хрусталика, пороки сердца, гепатоспленомегалия, поражение отдельных органов и систем).
При ведении пациенток с генитальным герпесом врачу необходимо ставить перед собой следующие цели:
- купирование симптомов;
- проведение профилактики последствии инфекции и ее передачи половому партнеру и новорожденному.
Риск внутриутробного заражения плода ВПГ определяется совокупностью факторов - вариантом клинического течения ГГ (первичный эпизод заболевания или рецидив), особенностями клинической картины (типичное, атипичное или бессимптомное течение инфекции), продолжительностью контакта плода с инфицированными родовыми путями матери и стадией герпетических высыпаний.
При совпадении первичного эпизода заболевания ГГ с I или III триместром беременности в 40-50% случаев наблюдается либо мертворождение, либо рождение ребенка с врожденным поражением мозга (микроцефалия и другие аномалии). Поэтому, согласно рекомендациям ВОЗ, при первичном эпизоде заболевания, особенно в случае первичной инфекции в I триместре, целесообразно беременность прервать.
При рецидивирующем герпесе риск инфицирования плода составляет всего О-8%, что объясняется пассивной передачей материнских антител, более низкими титрами вируса и более коротким периодом его воздействия. В этих случаях беременность следует сохранить.
Наибольшую значимость в плане возможного инфицирования плода имеют атипично протекающие формы хронической ге-нитальной герпетической инфекции. В 70% случаев дети с неонатальным герпесом рождаются именно от матерей с атипичными или бессимптомными формами ГГ, при том, что частота бессимптомного носительства ВПГ-2 составляет в различных популяциях 0,5-8%. Смертность новорожденных от неонатального герпеса в этой группе составляет 50-70%; из выживших новорожденных здоровыми остаются только 15%.
Таким образом, становятся понятны социальная значимость для нашей страны проблемы генитальной герпетической инфекции и ее неблагоприятный вклад в заболеваемость и перинатальные потери.
Для установления нормального контакта между врачом и пациентом необходимо:
- неосуждение со стороны врача;
- вовлечение пациента в управление своей болезнью;
- возможность больного получить лучшее из доступного на текущий момент лечение.
Принципы современной терапии
К базисному виду терапии относится прежде всего комплекс противовирусного лечения - длительная блокада репродукции вируса современными химиопрепаратами, на фоне которых следует проводить стимуляцию неспецифической и специфической резистентности организма. Необходимо подчеркнуть, что лечение всегда целесообразно подбирать индивидуально и в каждом конкретном случае выбор медикаментозного комплекса определяется клинической формой инфекции, фазой заболевания (рецидив или ремиссия), иммунологическим состоянием пациента, предшествующим лечением и его эффективностью, наличием сопутствующих заболеваний (особое внимание необходимо уделять аллергоанамнезу).
Идеальный противовирусный препарат должен обладать селективным и специфическим механизмом действия, не быть токсичным (мутагенным, тератогенным, канцерогенным), не иметь побочных эффектов, не вызывать резистентность. Препарат должен характеризоваться хорошей биодоступностью, не взаимодействовать с другими лекарствами и иметь удобный режим дозирования.
Наиболее безопасным вариантом химиотерапии оказалось создание синтетических аналогов какого-либо структурного компонента (нуклеозид) герпес-вирусной ДНК, который избирательно фосфорилируется не клеткой, а вирусспецифическим ферментом - тимидинкиназой.
К наиболее широко используемым в мировой клинической практике аномальным нуклеозидам относятся ацикловир (зовиракс, виролекс), валацикловир (валтрекс), фамцикловир (пенцикловир), ганцикловир и т.д. К аналогам пирофосфата относится триаптен. К препаратам с другим механизмом действия (специфические ингибиторы) - бонафтон, алпизарин, флакозид, хелипин, флореналь.
Чаще всего для лечения генитального герпеса используют ацикловир (АЦ), обладающий высокой степенью сродства и селективности в отношении герпес-вирусов.
Ацикловир проникает преимущественно в зараженные ВПГ клетки, однако в неизмененном виде инертен и малотоксичен, прежде чем стать активным, он должен фосфорилироваться.
Существует две методики лечения рецидивирующей герпетической инфекции АЦ: эпизодическое лечение каждого обострения и продолжительная супрессивная терапия с целью предотвращения рецидивов. Выбор режима терапии определяется клиническим вариантом инфекции (первичный эпизод или рецидив) и степенью ее тяжести, а также проблемой передачи инфекции в случае, если один из партнеров серонегативен, и при планировании беременности.
В последние годы в России в качестве химиопрепарата широко использовался алпизарин. Проведенное сравнительное исследование лечебного и профилактического эффекта алпизарина и зовиракса при тяжелом течении ГГ показало, что прием зовиракса в режиме супрессивной терапии по 800 мг в сутки способствовал стойкой ремиссии у 73% больных, в то время как прием алпизарина вызывал подобный эффект только в 19% случаев. Профилактический эффект зовиракса более чем в 5 раз превосходит эффект алпизарина по восстановлению качества жизни больных.
Однако биодоступность перорально вводимого ацикловира составляет всего 15-21 %, поэтому в течение последних 10 лет с целью повышения его эффективности разрабатывались различные аминокислотные эфиры ацикловира.
Всего было синтезировано более 18 аминокислотных эфиров. Валацикловир (L-валиловый эфир) показал биодоступность, равную 63%. В отличие от ацикловира валацикловир (валтреке) под влиянием фермента валацикловиргидролазы хорошо всасывается в кишечнике и быстро метаболизируется в печени, полностью превращаясь в ацикловир. Фармакокинетика и токсические свойства валацикловира идентичны таковым для ацикловира.
В клинической практике (особенно при лечении привычного невынашивания беременности) нередко возникает необходимость одновременно проводить профилактику как генитального герпеса, так и ЦМВ-инфекции. Использование в этих случаях валтрекса в значительной степени облегчает задачу врача, так как наиболее специфичный для ЦМВ-инфекции химиопрепарат ганцикловир оказывает выраженный гепатотоксический эффект и вызывает гипоплазию костного мозга.
Более высокие концентрации ацикловира в плазме как конечного продукта введения валацикловира позволяют также использовать его в случаях инфицирования больных резистентными штаммами герпес-вируса. Поддержание высоких уровней ацикловира в плазме при лечении валацикловиром позволяет уменьшить кратность приема препарата и способствует лучшему его усвоению.
В режиме эпизодической терапии валтрекс следует назначать по 500 мг 2 раза в день в течение 5 дней. Для профилактики рецидивов инфекции - по 100 мг один раз в сутки в течение 4-6 месяцев. За безопасностью применения ацикловира и его аналогов наблюдают с 1982 года. Подобная программа принята и для валацикловира. Наиболее частыми побочными эффектами являются головная боль, тошнота, диарея. Однако они не выражены.
Высокой биодоступностью (77%) обладает и фамцикловир (диацетил-6 - дезоксипроизводное пенцикловира). Пенцикловир имеет сходный, но не аналогичный ацикловиру спектр действия, включающий вирус ветряной оспы, ВПГ-1, ВПГ-2, а также вирус гепатита В. Фамцикловир превращается в пенцикловир при всасывании и пассаже через печень, последний активируется вирусной тимидинкиназой. Фамцикловир хорошо переносится, однако в дозе в 50 мг раз выше, чем терапевтическая повышает риск развития аденокарциномы груди у мышей.
Однако ни ацикловир, ни другие противовирусные агенты - фамцикловир, валацикловир - не предотвращают ни перехода вируса в латентное состояние, ни возникновения рецидивов после их отмены, ни передачи инфекции, а также, к сожалению, не влияют на естественное течение этой инфекции в плане полного излечения. Поэтому на протяжении последних 20 лет ученые изыскивают методы непосредственного воздействия на иммунную систему больных ГГ с целью стимуляции специфических и неспецифических ее факторов, тем самым способствуя блокаде репродукции вируса. Одним из перспективных подходов профилактики и лечения герпес-вирусных заболеваний являются применение препаратов иммуноглобулинов человека и вакцинотерапия.
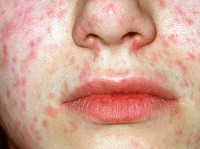
Краснуха при беременности – вирусная инфекция, передающаяся воздушно-капельным путем и провоцирующая тяжелые пороки развития у плода. Заболевание сопровождается увеличением лимфоузлов, гипертермией, кашлем, конъюнктивитом. Спустя 2-3 дня после заражения краснуха при беременности проявляется папулезной сыпью, патологические элементы изначально возникают на лице, затем распространяются на тело, руки и ноги. Для диагностики заболевания используются серологические тесты, позволяющие определить иммунологические маркеры IgM. Специфическое лечение отсутствует, при наличии тяжелых пороков развития плода краснуха при беременности является показанием к ее прерыванию.
Общие сведения
Опасность краснухи при беременности заключается еще и в том, что она способна протекать не только в острой, но и в хронической форме, никак клинически не проявляясь. В такой ситуации отсутствует возможность своевременно выявить риски для плода и определиться с дальнейшей тактикой ведения беременности с учетом наличия или отсутствия врожденной патологии малыша. Краснуха при беременности представляет различную степень угрозы в зависимости от срока эмбриогенеза. Заражение в первом триместре, особенно в первые недели, в 80% случаев заканчивается пороками развития. Во втором триместре риск неблагоприятного исхода наблюдается у 75% малышей, после 28 недель показатель снижается до 50%.

Причины краснухи при беременности
Краснуха при беременности вызывается возбудителем рода тогавирусов, тропным к эмбриональной и лимфоидной тканям. Заражение происходит преимущественно воздушно-капельным путем при тесном контакте с источником инфекции. Распространение вирусов начинается еще в инкубационном периоде, когда явные признаки болезни отсутствуют, что не позволяет исключить контакты с инфицированными людьми. Контагиозность сохраняется на протяжении 7 суток до появления сыпи и в течение 1-2 недель после ее возникновения. Краснуха при беременности также может передаваться бытовым путем при использовании общих предметов, на которых сохранились следы биологических жидкостей инфицированного человека. Доказано, что возбудитель присутствует не только в носоглоточной слизи, но и в крови, моче, кале.
Краснуха при беременности передается плоду по сосудистому руслу. Изначально патагент проникает в лимфатические узлы матери, поражает ткани дыхательных органов, после чего поступает в кровь, достигает плаценты и попадает в организм малыша. Окончательно последовательность тератогенного воздействия краснухи при беременности не изучена, однако доказано, что возбудитель провоцирует хромосомные изменения, способствует расстройству митотической активности эмбриональных клеток. Часто встречающиеся гидроцефалии, замедление умственного и физического развития при таком диагнозе обусловлены ингибицией и апоптозом тканей, расстройством циркуляции крови, вызванными пагубным воздействием вируса.
Симптомы краснухи при беременности
Краснуха при беременности, так же, как и вне ее, начинается с инкубационного периода, который длится 11-24 дня. Затем появляется характерный признак – увеличение и болезненность затылочных, шейных и околоушных лимфоузлов. Примерно треть женщин страдает от суставных болей, вызванных проникновением возбудителя в синовиальную жидкость. По истечении нескольких дней с момента возникновения этих симптомов краснуха при беременности проявляется мелкой папулезной сыпью розового цвета. Элементы могут сливаться между собой. Изначально они локализуются на коже лица, затем распространяются на тело и конечности. Исчезают высыпания в той же последовательности.
Краснуха при беременности сопровождается множественными эмбриопатиями. Со стороны плода, прежде всего, наблюдается характерная триада Грегга. Она включает в себя такие пороки, как глухота, слепота, поражение сердца. Не исключено развитие катаракты. Также краснуха при беременности становится причиной нарушения умственного и физического развития плода, врожденной дистрофии, ДЦП, идиопатической тромбоцитопенической пурпуры. При поражении женщины на поздних сроках вынашивания со стороны малыша возможны такие проявления, как васкулит, склонность к пневмониям с постоянными рецидивами, хроническая экзантема. Примерно в трети случаев краснуха при беременности заканчивается летальным исходом для ребенка.
Даже если краснуха при беременности не спровоцировала тяжелых врожденных пороков со стороны плода, что характерно для заражений во 2-3 триместре, она может иметь отдаленные последствия. В частности, заболевание способно давать отдаленные проявления в период полового созревания ребенка и вызывать панэнцефалит, недостаточное продуцирование гормона роста. Часто перенесенная матерью краснуха при беременности становится причиной возникновения инсулинозависимой формы сахарного диабета у ребенка в юношеском возрасте. Также возможны нарушения слуха, тиреоидит аутоиммунного происхождения.
Диагностика краснухи при беременности
Краснуха при беременности диагностируется путем проведения специфических серологических анализов, свидетельствующих о наличии антител к возбудителю в крови женщины. При выявлении симптомов или в случае нахождения будущей матери в очаге инфекции следует незамедлительно обратиться к акушеру-гинекологу и инфекционисту для проведения своевременного обследования и оценки рисков для здоровья плода. Краснуха при беременности чаще выявляется с помощью иммуноферментного метода (ИФА), который показывает уровень IgM. Антитела к возбудителю начинают циркулировать в крови больной через 7 суток после занесения патагента в организм и остаются там на протяжении 1-2 месяцев.
Из-за высокой опасности краснухи при беременности для малыша пациенткам назначается ПЦР (метод полимерной цепной реакции). Его цель заключается в подтверждении недавнего инфицирования женщины, определении РНК вируса. Как уже было сказано выше, также при подозрении на краснуху при беременности проводится ИФА крови на авидность IgG к возбудителю. О заражении свидетельствует присутствие в исследуемой биологической субстанции высокого количества антител титра IgM. Именно они говорят об остром течении заболевания. В данном случае следует установить вероятный период заражения, оценить состояние плода (используется преимущественно кордоцентез) и определиться с возможностью дальнейшего ведения беременности.
Лечение краснухи при беременности
Краснуха при беременности, возникшая до 12 недель, является абсолютным показанием к искусственному прерыванию, так провоцирует формирование тяжелейших пороков развития у плода. При инфицировании на сроке 13-28 недель эмбриогенеза собирается консилиум, который решает, есть ли возможность сохранения беременности. Если установлено, что краснуха при беременности не нанесла вреда здоровью ребенка или прерывание не осуществлялось по каким-либо другим причинам, пациентке вводится иммуноглобулин в дозировке 20-30 мл путем внутримышечной инъекции.
Специфическое лечение краснухи при беременности не разработано. Больным показана полная изоляция с целью предупреждения распространения инфекции и постельный режим. При необходимости назначается симптоматическая терапия. Краснуха при беременности может требовать введения жаропонижающих препаратов, спазмолитиков, противовоспалительных средств. Если принято решение о продолжении вынашивания плода, женщина заносится в группу высокого риска по развитию врожденных аномалий младенца. Дополнительно применяется лечение для профилактики плацентарной недостаточности, предполагающее употребление лекарственных средств для нормализации кровотока. Каких-либо особенностей в ведении родов или послеродового периода в случае перенесенной краснухи при беременности нет. Малыш может появиться на свет как при прохождении через естественные родовые пути, так и путем кесарева сечения.
Прогноз и профилактика краснухи при беременности
При диагностировании краснухи при беременности прогноз крайне неблагоприятный. Заражение в первом триместре в 80% случаев заканчивается развитием тяжелых пороков, несовместимых с жизнью. При продолжении вынашивания в 20% происходит мертворождение. Еще столько же детей, появившихся на свет с врожденной формой болезни, погибают в первый месяц жизни. У 30% женщин краснуха при беременности заканчивается самопроизвольным абортом. В 20% случаев продолжения вынашивания отмечается внутриутробная гибель плода. Именно поэтому такой диагноз на начальных сроках гестации является абсолютным показанием к прерыванию.
Специфическая профилактика краснухи при беременности заключается в исследовании серологического статуса женщины и проведении вакцинации по индивидуальным показаниям за 2-3 месяца до запланированного зачатия. Такой же подход применяется, если количество противокраснушных антител в крови ниже 15 МЕ/мл. Чтобы снизить вероятность развития краснухи при беременности на сроке до 16 недель в случае попадания пациентки в очаг инфекции, осуществляется введение иммуноглобулина, содержащего антитела к возбудителю. После зачатия вакцинация против краснухи противопоказана, хотя ее случайное проведение не является поводом для искусственного прерывания. Неспецифическая профилактика краснухи при беременности предполагает исключение контактов с возможными носителями инфекции и укрепление иммунитета.
Материал составлен на основе фундаментальных трудов западных ученых.
Токсоплазма, краснуха, цитомегаловирус и беременность
При беременности назначают анализы на антитела к инфекциям - токсоплазме, цитомегаловирусу и краснухе. Определяется два вида антител – IgG и IgM, по которым судят о встрече с инфекционным агентом, а также о времени этой встречи. Самое страшное – заражение во время беременности (краснуха, токсоплазма, ЦМВ) или активация инфекции (ЦМВ).
Специфические антитела класса IgM, в частности, антитела к краснухе, относятся к факторам, циркулирующим в крови экстремально низких концентрациях. Поэтому анализы не в цифрах (количественно), а в виде положительности (=реактивности) или отрицательности (=отсутствии реактивности). Отрицательный и положительный результаты отделяет друг от друга так называемый порог отсечки (cutoff). Цифры показателя выше данного порога считаются положительными, а ниже порога — отрицательными. Зона значений порог ± 10%) является „зоной неопределенности”.
Быстрые уточняющие методы диагностики
Используются два способа: подтверждающие анализы методом иммуноблот и анализ на авидность антител IgG.
Если Вы сдаете эти анализы, исчезает необходимость ЖДАТЬ 2 недели плюс дни готовности анализа. Вы получаете сведения о своем состоянии ВОВРЕМЯ.
Подтверждающие анализы на токсоплазму, краснуху, ЦМВ методом иммуноблот:
- Высокочувствительный и специфичный тест!
- Чувствительность 97 %
- Специфичность 99 %
Используется для подтверждения результатов скрининговых исследований, таких как ИФА (ELISA) или иммунофлуоресцентный анализ (IFA).
Будьте уверены в анализе!
Зачем это нужно:
- точное и своевременное выявление позволит правильно определить тактику ведения беременности
- нет необходимости терять время на ожидание следующего анализа
Тактика врача определяется в каждом конкретном случае по-разному (подготовка к беременности, начало беременности, период новорожденности и т.д.)
Авидность антител IgG
Определить время, когда произошло инфицирование можно и по авидности антител IgG. Этот анализ менее точен по срокам, чем подтверждающий анализ методом иммуноблот.
Низкоавидные антитела встречаются при острой, недавно развившейся инфекции
Высокоавидные антитела – если встреча с инфекцией состоялась давно.
Определение авидности антител помогает врачу оценить ситуацию по инфекции и решить вопрос о дальнейших действиях.
Кому нужно полное обследование на инфекции?
- женщинам во время подготовки к беременности
- беременным
- новорожденным для диагностики врожденного инфицирования
Дополнительная справка: если анализы сданы во время беременности
- IgM методом иммуноблот
- IgM методом иммуноблот
Основные сведения о цитомегаловирусе (ЦМВ)
ЦМВ человека относится к вирусам, вызывающим схожие заболевания у различных животных. Все эти заболевания связаны с появлением характерных увеличенных клеток - отсюда и название цитомегаловирус (цито - клетка, мегало - большая). Вирус может размножаться в различных клетках организма человека, но предпочтительно этими клетками являются фибробласты (клетки соединительной ткани).
В добавок к тому, что ЦМВ вызывает тяжелые врожденные дефекты, он может привести к целому ряду заболеваний у детей и взрослых.
Существует три основных клинических вида цитомегаловируса:
- Генитальная ЦМВ инфекция может привести к гепатоспленомегалии (увеличению печени и селезенки), ретиниту (воспаление сетчатки), появлению сыпи и поражению центральной нервной системы.
- У около 10 процентов детей и взрослых первичная цитомегаловирусная инфекция вызывает мононуклеозный синдром с лихорадкой, общим недомоганием, атипичным лимфоцитозом и фарингитом.
- Пациенты с трансплантантатами и ВИЧ-инфицированные люди могут заболеть угрожающим жизни заболеванием, которое охватывает легкие, желудочно-кишечный тракт, сетчатку, печень и центральную нервную систему.
Существует предположение, что вирус обладает онкогенным эффектом и в редких случаях может трансформировать фибробласты.
Подробнее о цитомегаловирусе (ЦМВ)
Эпидемиология цитомегаловирусной инфекции (ЦМВ)
Цитомегаловирус распространен по всему миру, но проживание в плохих социальных условиях и не соблюдение правил личной гигиены сильно способствует передаче микроба. Часто встречаются инфекции у новорожденных и маленьких детей. Вирус можно обнаружить в молоке, слюне, фекалиях и моче. Была прослежена передача вируса от маленького ребенка к его беременной матери, и затем к развивающемуся плоду. К счастью, вирус плохо передается при случайных контактах, так как для его передачи необходимо время. ЦМВ часто передается половым путем, его выделяют из семени или цервикальной слизи. Однажды заразившись, человек, возможно, будет носителем данного вируса в течение всей жизни.
Заболевания, вызываемые ЦМВ, и их клинические проявления
Генитальная цитомегаловирусная инфекция (ЦМВ)
Инфекции у плода варьируются от легких форм до тяжелых и диссеминированных. Петехии (точечные кровоизлияния), гепатоспленомегалия и желтуха - наиболее часто встречаемые проявления. Микроцефалия с (или без) церебральной кальцификации, внутриматочная задержка роста и преждевременное развитие встречаются (что это такое. ) в 30-50 процентах случаев. Лабораторные аномалии включают повышение уровня аланинаминотрансферазы, тромбоцитопению (уменьшенное число тромбоцитов), гипербилирубинемию (повышение уровня билирубина в крови), гемолиз (разрушение клеток крови) и увеличение уровня белка спинномозговой жидкости. Прогнозы для новорожденных с тяжелыми формами заболевания весьма печальны: процент смертности очень велик, а те, кому удается преодолеть болезнь, в будущем встречаются с трудностями в интеллектуальном развитии и развитии слуха.
Зачастую генитальный цитомегаловирус никак не проявляется у новорожденных, а потому не лечится своевременно, что приводит к отклонениям у таких детей в различных системах, которые проявляются в течение первых лет их жизни.
Перинатальная ЦМВ инфекция
Новорожденные могут заразиться ЦМВ при прохождении родового канала или при последующем контакте с материнским молоком или другими выделениями. Огромное количество случаев инфицирования новорожденных протекает асимптоматически. Однако длительная интерстициальная пневмония связана с цитомегаловирусом. Иногда она сопровождается присоединением других инфекций, таких как Chlamidia trachomatis или Ureaplasma urealyticum. Медленное набирание веса, аденопатия, сыпь, гепатит, анемия и атипичный лимфоцитоз также могут сопутствовать заболеванию.
Мононуклеозный синдром
Этот синдром возникает у 10 процентов первично зараженных людей, у оставшихся первичная инфекция протекает бессимптомно. Для пациентов с этим синдромом характерно наличие лихорадки, общего недомогания, атипичного лимфоцитоза и, в редких случаях, цервикальной аденопатии или гепатита.
Большинство пациентов выздоравливают без последствий, хотя послевирусная астения может продолжаться в течение нескольких месяцев.
ЦМВ и трансплантация органов
Считается, что ЦМВ является одним из основных патогенов, осложняющих трансплантацию органов. У пациентов, которым пересаживают почку, сердце, легкие и трансплантаты печени, ЦМВ вызывает множество синдромов, включающих лихорадку и лейкопению, гепатит, пневмонит, эзофагит, гастрит, колит и ретинит. Период максимального риска находится между первым и четвертым месяцами после трансплантации.
ЦМВ у людей с поражениями иммунной системы.
Цитомегаловирус признан важным паразитом у ВИЧ-инфицированных людей, у которых он вызывает ретинит или диссиминированные (охватывающие весь организм) заболевания. Хотя случаи серьезных ЦМВ заболеваний снизились, установление высокоактивного режима приема антиретровирусных препаратов иногда вызывает острые вспышки ЦМВ-ого ретинита в течение первых нескольких недель терапии.
Диагностика цитомегаловируса
Диагностику ЦМВ инфекции невозможно убедительно провести только по клиническим проявлениям. Необходимо выделение вируса или определение цитомегаловирусных антигенов или ДНК из клинических образцов. Кроме того, важно проследить рост уровня антител в крови. Вирус легко определяется в культуре фибробластов. Если содержание вируса велико, что зачастую имеет место при генитальной ЦМВ инфекции, характерные изменения в клетках будут видны в течение нескольких дней. Но если содержание вируса мало, как при цитомегаловирусном мононуклеозе, такая диагностика может занять несколько недель. Многие лаборатории применяют метод, включающий в себя центрифугирование и определение антител к раннему ЦМВ- антигену. Такое исследование может дать результат раньше, чем метод культур.
![308_1.jpg]()
Вирусные инфекции приобретают особую актуальность в период беременности, так как могут влиять на здоровье не только будущей мамы, но и плода. Герпес среди них занимает одно из главных мест, поскольку это заболевание очень часто встречается у беременных женщин.
Герпетическая инфекция - это большая группа инфекционных заболеваний, вызываемых вирусами герпеса человека. Это одно из наиболее распространенных заболеваний человека. По данным многочисленных исследований, к 18 годам более 90% населения планеты инфицируются одним или несколькими штаммами вирусов герпеса. Среди инфекций, передающихся половым путем, генитальный герпес занимает второе место после трихомониаза.
Особенностью герпеса является его рецидивирующее течение. Находящийся в спящем состоянии вирус пробуждается при снижении иммунитета, а беременность сама по себе обладает свойством ослабления иммунных сил организма, так как организм женщины вынашивает наполовину чужеродный с иммунологической точки зрения плод, что невозможно без снижения интенсивности работы ряда звеньев иммунитета. Именно поэтому обострения герпеса во время беременности происходят довольно часто.
Проявления заболевания
Клинические проявления герпеса зависят от многих факторов - типа вируса, локализации поражения, возраста и иммунного статуса человека. Классическая симптоматика - это появление группы мелких пузырьков, наполненных прозрачной жидкостью. Для герпеса характерно появление пузырьков при очередном рецидиве всегда в одном и том же месте.
При генитальном варианте герпеса высыпания локализуются на половых губах, на коже промежности, внутренней поверхности бедер, лобке или вокруг заднего прохода.
Сыпь сопровождается неприятными ощущениями, зудом, жжением, болью. Затем пузырьки лопаются, на их месте образуются сначала язвочки, затем корочки. Герпетические язвочки характерно болезненны, а образующиеся на их месте корочки исчезают бесследно через 2—3 дня, не оставляя на коже ни пигментации, ни рубцов.
Общая симптоматика заболевания весьма разнообразна: повышение температуры тела, увеличение лимфатических узлов (чаще – паховых), суставная и мышечная боли, упорные мигрени, раздражительность, отсутствие аппетита и т.д.
Типичная клиническая картина проявляется не более чем в трети случаях носительства генитального герпеса. Нередко генитальный герпес протекает бессимптомно или без характерных высыпаний.
Атипичное течение герпеса более коварно: отсутствие пузырьковых высыпаний с лихвой компенсируется многообразием общих проявлений, что часто создает трудности в постановке верного диагноза. Симптомы атипичного герпеса - жжение, трещины промежности, поло¬вых губ или заднего прохода, отек, покраснение слизистых оболочек. В таких случаях часто диагноз ставится неверно либо женщины, уверенные в наличии кандидоза (молочницы) или бактериального вагиноза, безрезультатно занимаются самолечением.
Тяжесть любых проявлений герпетической инфекции определяется состоянием иммунитета.
Разновидности вируса
Наиболее распространенными являются ВПГ 1 и 2 - вирус простого герпеса первого и второго типов. ВПГ 1 чаще всего проявляется в виде пузырьковых высыпаний на губах, возможны поражения глаз, ротовой полости, носа. Классическая локализация ВПГ 2 (генитального герпеса) - слизистая оболочка мочеполового тракта. В некоторых случаях наблюдается следующий феномен перекрестного инфицирования: виновником герпетических высыпаний верхней половины туловища является ВПГ 2 (генитальный) и наоборот - ВПГ 1 вызывает развитие инфекции нижней половины. Как правило, это связано с двумя причинами: нарушением элементарных правил гигиены, когда происходит самозаражение - перенос вируса через кожу и слизистые оболочки, и орально-генитальными контактами.
Заражение герпесом половых путей происходит в основном только через незащищенный половой контакт. В редких случаях возможна передача инфекции через поцелуй, использование общей посуды и белья. Это так называемый горизонтальный путь передачи. При вертикальном пути передачи происходит передача вируса от матери плоду во время беременности (при прохождении ребенка через родовые пути при условии наличия в слизистой вируса герпеса, то есть при родах в момент обострения герпес-вирусной инфекции). При локализации очагов на губах можно заразиться через общую посуду, полотенца и поцелуи. Надо отметить, что риск внутриутробного инфицирования плода при первичном герпесе составляет 50%, при рецидиве – не более 4%, во время родов при наличии высыпаний на шейке матки и наружных половых органов – 90%.
Как действует вирус?
Рассмотрим некоторые особенности взаимодействия вируса с организмом человека.
Обострения герпеса могут быть связаны с двумя факторами:
- уже имеющимся иммунодефицитом, что является пусковым механизмом для рецидива герпетической инфекции;
- влиянием вируса на сам иммунитет. Длительное нахождение герпеса в организме обладает прямым повреждающим действием на клетки иммунной системы. Таким образом, развивается порочный круг: ослабленный иммунитет запускает рецидив герпетической инфекции, а вирус герпеса еще более усугубляет имеющийся иммунодефицит.
Диагностика
Диагностика герпеса при типичной картине не представляет сложности для врача (да и для пациента тоже). Клинические проявления герпетической инфекции весьма яркие: характерные пузырьковые высыпания, рецидивирующее течение говорят сами за себя.
В случаях атипичного герпеса, вирусоносительства и при профилактическом обследовании методы лабораторной диагностики приобретают особое значение.
Основные направления лабораторных методов исследований:
- Определение непосредственно самих вирусных частиц. Для этого используются методы электронной микроскопии с использованием специальных методов окрашивания мазков, ИФА (иммуноферментный ана¬лиз) и ПЦР. Последний метод (полимеразная цепная реакция) широко распространен и дает достаточно точные результаты - он доступен, высокочувствителен, специфичен. Как правило, материал для анализа ПЦР берут путем соскоба (мазка) с шейки матки, влагалища, уретры, также исследуют соскоб со дна ранки или содержимое пузырька. При подозрении на скрытое течение инфекции исследуют еще мочу и слюну.
- Исследование крови на антитела к вирусу простого герпеса, при котором выявляется иммуноглобулины классов М и G. Если заражение человека произошло впервые (первичное инфицирование) или в момент диагностики соответствует острой фазе заболевания (рецидив), то в крови обнаруживают ранние антитела класса М.
Определение поздних иммуноглобулинов класса G свидетельствует о том, что встреча организма с вирусом уже произошла много ранее.
Особое внимание уделяется лабораторной диагностике в случае впервые выявленных симптомов герпеса при беременности. Такая ситуация может отвечать как первичному эпизоду, так и первому рецидиву (т.е. ранее организм уже встречался с вирусом, но проявлений не давал).
Если в крови есть IgG (поздние иммуноглобулины), значит, герпес рецидивирующий и угрозы для плода или эмбриона практически нет. Если в крови нет Ig, а есть IgМ, то необходимо проявить крайнюю степень настороженности, поскольку это является лабораторным подтверждением первичного эпизода.
Генитальный герпес и беременность
Особую же актуальность в период беременности приобретает именно генитальный герпес.
Очевидно, что при возникновении проблемы герпеса у будущей мамы появляется масса волнений. К счастью, в большинстве случаев эти тревоги безосновательны.
Когда же действительно есть повод для волнений? Наибольшую опасность представляет ситуация, когда заражение герпесом происходит у женщины во время беременности - первичный эпизод генитального герпеса. Такая ситуация характеризуется выраженными проявлениями, т.к. в организме матери нет защищающих от герпеса антител. Для плода риск особенно высок при заражении генитальным герпесом в первом и третьих триместрах. Инфицирование плода в первом триместре беременности приводит к возникновению гидроцефалии (накоплению жидкости в головном мозге), пороков сердца, аномалий развития желудочно-кишечного тракта и др. Такие случаи чрезвычайно редки, так как при первичном эпизоде герпеса, как правило, происходит самопроизвольное прерывание беременности до срока 10 недель.
Лечение герпеса во время беременности
При доказанном первичном инфицировании на ранних сроках беременности обсуждается вопрос о ее прерывании.
Лечение рецидивов герпеса во время беременности и вне ее не имеет принципиальных различий. В любом случае преследуются одинаковые цели: снижение выраженности симптомов (боль, зуд, лихорадка и т.д.), сокращение сроков заживления ран, предотвращение новых обострений. Следует помнить, что чем скорее начато лечение, тем больший эффект оно будет иметь. Если лечение начато в продромальный период (когда появляются начальные признаки заболевания – покалывание или легкий зуд на месте будущих пузырьков, озноб, недомогание), то это достоверно поможет снизить выраженность проявлений герпеса.
Особенностью лечения герпетической инфекции является точное соблюдение назначенной дозы и режима приема препаратов. Если пропущена очередная доза противовирусного препарата, то вирус герпеса может успеть в этот период размножиться, что приведет к неэффективности лечения.
Единственными препаратами, обладающими доказанной эффективностью в лечении герпетической инфекции, являются специфические виростатики – аналоги нуклеозидов (АЦИКЛОВИР, ВАЛАЦИКЛОВИР, ПЕНЦИКЛОВИР, ФАМЦИКЛОВИР).
Лечение герпетической инфекции при беременности подразумевает использование разрешенных противовирусных препаратов (ацикловир ЗОВИРАКС и валацикловир ВАЛТРЕКС) в виде мазей, кремов и таблеток.
Одновременно с противовирусными препаратами в комплексном лечении используют иммуномодуляторы (ВИФЕРОН), витамины, физиотерапевтические методы, местные антисептики для более быстрого заживления ранок.
Безусловно, целесообразность и курс лечения определяются в каждом индивидуальном случае. Ситуация сочетание беременности и герпеса должна находится под бдительным контролем врача и самолечение в этих случаях просто недопустимо.
Герпес новорожденных
В каких же случаях коварный вирус все-таки достигает своей цели и вызывает заболевание у новорожденных? В подавляющем большинстве случаев (90%) заражение происходит контактным путем при прохождении через родовые пути. Внутриутробное заражение новорожденного отмечается только в 5% случаев герпеса новорожденных. Причем важным условием является наличие у мамы именно первичного эпизода гениального герпеса, в случаях бессимптомного носительства или рецидивирующего герпеса инфицирование плода в родах случается не чаще, чем в 4% случаев.
Симптомы и признаки герпеса у младенцев появляются уже на 2-й неделе после рождения. Для герпеса новорожденного характерно наличие пузырьков на коже, слизистых оболочках (полости рта, половых органов) и конъюнктиве глаз. Чем более недоношенными рождаются дети, тем более сложнее протекает инфекция; в таких случаях часто встречается поражение головного мозга (герпетический энцефалит).
Профилактика
Специфических методов профилактики герпеса, к сожалению, не существует. Профилактика инфекции на этапе планирования, при беременности и после родов носит исключительно предупредительный характер. Применяются следующие меры:
Однако это определение справедливо для течения этой инфекции только у детей, так как заболевание краснухой беременных чревато серьезными последствиями для будущего ребенка.
Опасность вируса краснухи в том, что он практически всегда передается от матери плоду свободно проходит через плацентарный барьер- так как это вирус- (частица меньше клетки крови) и повреждает его. В зависимости от срока беременности, на котором происходит заражение, у плода c различной вероятностью формируются пороки развития.
Да, заболевание у детей протекает очень легко, организм сам справляется с возбудителем (вирус краснухи), чаще всего можно обойтись ограничением режима, обильным питьем и витаминами. Это действительно так. Но! При беременности у плода формируется синдром врожденной краснухи (катаракта, повреждение внутреннего уха, дефекты сердца, микроцефалия).
Во многих странах острая краснуха является медицинским показанием для прерывания беременности, потому что синдром у плода возникает практически во всех случаях, когда мать заболевает краснухой в первые месяцы беременности. Если девочку не привили в детстве, если она не переболела краснухой, остается опасность заразиться краснухой, будучи взрослой. Не имеют такой защиты 15-30% женщин детородного возраста.
![]()
Итак, что же это такое- краснуха?
- Чем опасна?
- Кого и когда необходимо обследовать?
- Как определить есть ли опасность для малыша и что делать?
Краснуха – это инфекционное заболевание, вирусной природы, которое отличается высокой заразностью, проявляется сыпью на коже, которая имеет склонность к быстрому распространению, увеличением лимфоузлов (затылочная группа) и незначительным повышением температуры. Наблюдаются периодические подъемы заболеваемости с интервалом в 5-7 лет, кроме того присутствует осеннее-весенняя сезонность. Передается вирус краснухи воздушно-капельным путем. Кроме того, существует передача вируса от матери к плоду через плаценту при беременности (трансплацентарный путь передачи).
- Источником вируса чаще бывают дети, особенно те, которые посещают детский сад, спортивную секцию или школу. Поэтому женщина, не имеющая иммунитета к краснухе, беременная вторым ребенком имеет больше шансов заразиться вирусом краснухи. Коварство краснухи состоит в том, что инкубационный период, то есть период между заражением и появлением первых симптомов заболевания, длится примерно 2-3 недели.
- При этом в течение последней недели инкубационного периода больной уже выделяет вирус и представляет опасность заражения для окружающих, несмотря на то, что сам он чувствует себя прекрасно и о своем заболевании может не знать.
- Краснуха считается заразной 7 дней до появления сыпи и еще 7—10 дней после ее исчезновения.
- Кроме того, очень часто (50-90% случаев) краснуха протекает бессимптомно, но человек при этом также выделяет вирус и может заражать окружающих. В целом, заболевание протекает легко, осложнения наблюдаются редко.
- Наиболее грозным осложнением является краснушный энцефалит, который к счастью встречается достаточно редко (1:5000-1:6000).
У подростков и взрослых краснуха протекает значительно тяжелее, чем у детей. Однако большинство больных не нуждаются в специальном лечении. Применяются средства для лечения симптомов и осложнений, облегчающие общее состояние. После перенесенного заболевания развивается пожизненный иммунитет, однако его напряженность с возрастом и под воздействием различных обстоятельств, может снижаться. Таким образом, перенесенное в детстве заболевание краснухой не может служить 100% гарантией от повторного заболевания.
Какова опасность для плода?
Краснуху принято считать легким заболеванием. Однако это определение справедливо для течения этой инфекции только у детей, так как заболевание краснухой беременных чревато серьезными последствиями для будущего ребенка.
Опасность вируса краснухи в том, что он практически всегда передается от матери плоду и повреждает его.
В зависимости от срока беременности, на котором происходит заражение, у плода c различной вероятностью (в I триместре вероятность достигает 90%, во втором - до 75%, в третьем - 50%) формируются множественные пороки развития. Наиболее характерными являются поражение органа зрения (катаракта, глаукома, помутнение роговицы), органа слуха (глухота), сердца (врожденные пороки).
Также к синдрому врожденной краснухи относят дефекты формирования костей черепа, головного мозга (малый размер мозга, умственная отсталость), внутренних органов (желтуха, увеличение печени, миокардит и др.) и костей (участки разрежения костной ткани длинных трубчатых костей). В 15% случаев краснуха у беременных приводит к выкидышу, мертворождению.
При выявлении краснухи всегда осуществляется искусственное прерывание беременности.
Какие методы используют для диагностики краснухи?
Наиболее широкое применение в диагностике краснухи нашли серологические методы, в частности метод иммуноферментного анализа (ИФА).
- Иммунологическим маркером первичной инфекции является IgM к вирусу краснухи. IgM начинает вырабатываться в первые дни заболевания, достигает максимального уровня на 2—3 неделе и исчезает через 1-2 месяца. Но период циркуляции IgM антител может значительно варьировать в зависимости от инфекционного возбудителя и индивидуальных особенностей иммунного ответа организма.
- При инфицировании краснухой следовые количества IgM-антител к вирусу краснухи в некоторых случаях выявляются в течение 1-2 и более лет. Таким образом, их присутствие в крови беременной женщины не всегда является подтверждением первичного инфицирования в период беременности. Кроме того, специфичность даже лучших коммерческих тест-систем для обнаружения IgM-антител не абсолютна. В некоторых ситуациях, как следствие очень высокой чувствительности тестов, возможны неспецифические ложноположительные результаты. IgG выявляются на 2-3 дня позже, чем IgM, нарастают до максимума к месяцу от начала заболевания и персистируют в течение всей жизни. У зараженного плода противокраснушные IgM начинают вырабатываться с 16-24 недель и могут персистировать в течение длительного времени (до года и дольше). До 6 месячного возраста у новорожденного циркулируют материнские IgG, а затем у ребенка с врожденной краснухой в течение первого года жизни начинают продуцироваться специфические IgG.
- Так как риск патологии развития плода при остром первичном инфицировании вирусом краснухи во время беременности значителен, чтобы подтвердить или исключить факт недавнего инфицирования вирусом краснухи беременной женщины применяют ПЦР исследование биологических жидкостей на наличие РНК вируса краснухи и анализ крови методом ИФА на авидность IgG к вирусу краснухи.
С целью ранней диагностики краснухи у беременной или внутриутробного заражения для выявления РНК вируса краснухи методом ПЦР может быть использована:
- кровь из вены матери,
- кровь из пуповины, полученная путем кордоцентеза,
- околоплодные воды,
- ворсинки хориона, полученые от зараженных беременных женщин путем трансабдоминального амниоцентеза.
- Выявление в крови высокоавидных IgG антител (авидность IgG ≥70%) позволяет исключить недавнее первичное инфицирование.
Низкоавидные IgG-антитела (авидность IgG ≤ 50%), в среднем, выявляются в течение 3-5 месяцев от начала инфекции (это может в определенной степени зависеть от метода определения), но иногда вырабатываются и в течение более длительного срока. Само по себе выявление низкоавидных IgG-антител не является безусловным подтверждением факта свежего инфицирования, но служит дополнительным подтверждающим свидетельством в ряду остальных серологических тестов.
Кого нужно обследовать?
![]()
Особенно важна лабораторная диагностика краснухи у следующих категорий обследуемых:
- Женщины, которые планируют беременность, либо беременные с целью выявления группы риска. Если женщина ранее не болела краснухой, не уверена в том что болела, либо достоверно не знает об этом, необходимо провести исследование уровня специфического IgG методом ИФА. В случае положительного результата риск инфицирования плода отсутствует. В случае отрицательного результата рекомендуется проведение вакцинации. При этом планируемую беременность необходимо отложить на три месяца.
- Беременные с подозрением на инфицирование вирусом краснухи и взрослые люди с тяжелым течением, либо наличием осложнений краснухи. Необходимо определение специфических IgM и IgG и интерпретация результатов анализов у инфекциониста, для выбора дальнейшей тактики.
В целом диагностический алгоритм выглядит так:
- IgM – не обнаружены, IgG – не обнаружены, либо концентрация их не достаточна для защиты от инфекции. Рекомендуется: исключить контакт с больными краснухой, повторить обследование через 2 недели, в течение которых провести медицинское наблюдение за беременной. При повторном отрицательном результате провести третье серологическое обследование, продолжая медицинское наблюдение. При отрицательном анализе в третьем исследовании наблюдение прекратить, беременную предупредить о том, что она восприимчива к краснушной инфекции.
- IgM – не обнаружены, IgG – обнаружены, концентрация их соответствует защитному уровню. При первичном обследовании беременной на ранних сроках беременности, дальнейшее наблюдение по краснушной инфекции не показано.
- Обнаружены специфические антитела IgM к возбудителю краснухи. При этом IgG-антитела либо обнаружены, либо не обнаружены. Имеется риск врожденной патологии плода.
Показано повторное серологическое исследование через 2 недели, с дальнейшей консультацией инфекциониста. Для исключения перекрестного реагирования и влияния ревматоидного фактора, подтверждения/исключения диагноза рекомендуется сделать тест авидности IgG, провести количественный анализ на IgM и ПЦР исследование крови матери на наличие РНК вируса краснухи.
Новорожденные с признаками врожденной краснухи.
При подозрении у новорожденного внутриутробного инфицирования вирусом краснухи необходимо исследовать уровень IgМ в сыворотке крови новорожденного. Положительный результат анализа свидетельствует об острой инфекции. Диагноз может быть подтвержден, если в крови матери также выявляется положительный титр IgM. В тех случаях, когда инфицирование произошло в I или II триместре беременности, IgM может не выявляться. Тогда о наличии инфицирования можно судить по динамике IgG. При наличии инфицирования уровень IgG в первые месяцы жизни новорожденного растет.
При отсутствии инфицирования IgG в крови новорожденного либо не выявляется (мать серонегативна), либо падает (элиминация материнских антител).
Наличие специфических IgG у ребенка старше 6 месяцев указывает на внутриутробное инфицирование.
Что делать беременной женщине, если она оказалась в очаге краснухи?
Если беременная женщина, которая не болела краснухой, не делала прививку и не проводила определения иммунитета к вирусу краснухи, окажется в очаге краснушной инфекции (контакт с человеком, который болен краснухой), ей необходимо незамедлительно обратиться к инфекционисту!
Как было сказано выше, опасность заражения беременных женщин при контакте с больным краснухой существует лишь для тех женщин, которые восприимчивы к вирусу краснухи в следствие отсутствия защитного иммунитета. Наличие специфических антител (IgG к вирусу краснухи) свидетельствует о невосприимчивости пациентки.
Очень важно начать обследование по возможности на более ранних сроках после контакта. Если антитела к вирусу краснухи в защитных концентрациях обнаружены у женщины в первые 6 дней после контакта, то эти антитела являются следствием давно перенесенной краснухи. В этом случае женщина не восприимчива к вирусу краснухи, и контакт не представляет опасности для нее. Отсутствие антител или слабоположительный результат на ранних сроках обследования свидетельствует о том, что женщина не защищена против краснухи, и угроза заражения существует.
Но и отчаиваться заранее не стоит, так как известно, что восприимчивые женщины, контактировавшие с больными краснухой, могут не заболеть.
Для исключения заражения необходимо проводить повторное серологическое обследование в динамике через 2-4 недели после контакта.
Серологический контроль за контактировавшими женщинами необходимо осуществлять до конца 2-го триместра беременности.
Если женщина обращается на поздних сроках после контакта (через неделю и более после контакта с заболевшим) необходимо методом ИФА выявлять IgG, IgM и авидность IgG к вирусу краснухи, методом ПЦР исследовать кровь на РНК вируса краснухи.
Кроме визита к инфекционисту, женщина обязана обратиться к гинекологу, который назначит необходимые исследования для определения состояния плода (детальное УЗИ, скрининговые исследования 2го и 3го триместров). Если эти анализы, свидетельствуют о каком-либо неблагополучии в развитии ребенка, могут назначить процедуру амниоцентеза.
Далее, по результатам всех обследований и анализов решается вопрос о наличии врожденных пороков и прерывании беременности. Во многих странах краснуха, выявленная на первом триместре беременности, является показанием для прерывания беременности. При осложнении беременности краснухой на 14-16 неделях вопрос о рекомендации по сохранению беременности решается на консилиуме врачей. В случае невозможности сделать аборт беременной внутримышечно вводят иммуноглобулин в дозе 20–30 мл внутримышечно. В дальнейшем проводятся профилактические мероприятия по защите плода, лечение плацентарной недостаточности, профилактика и лечение не вынашивания беременности.
Профилактика краснухи у беременных женщин.
![]()
Для профилактики синдрома врожденной краснухи ВОЗ (Всемирная организация здравоохранения) рекомендует сочетать три принципиальных подхода к ликвидации краснухи и синдрома врожденной краснухи:
- вакцинация детей,
- вакцинация девушек-подростков
- вакцинация женщин детородного возраста, планирующих иметь детей.
По данным статистики не защищено от краснухи 11-30% женщин детородного возраста.
Если девушка или молодая женщина не болела краснухой и не привита, то перед тем, как планировать беременность, ей самой нужно подумать о соответствующей прививке.
- Нужно сдать кровь на антитела к краснухе .
- Если нет антител, необходимо сделать прививку от краснухи за 3 месяца до предполагаемой беременности. Вакцинация защищает практически в 100%, иммунитет после однократной прививки сохраняется в среднем 15-20 лет, потом иммунизацию можно повторить.
Необходимо помнить, что после введения краснушной вакцины не рекомендуется беременеть в течение 3 месяцев.
Но . Если беременность наступила раньше этого срока или была привита женщина, уже ожидающая ребенка, это не является показанием к прерыванию беременности.
В заключение хотелось бы напомнить, что безвыходных ситуаций не бывает! Они появляются лишь в том случае, если Вы позволяете им войти в свою жизнь. Родить здорового малыша не только необходимо, но и возможно!
Читайте также: