Вирус герпеса медицинский университет
Обновлено: 23.04.2024
Инфекция вызванная вирусом простого герпеса: диагностика, лечение, профилактика
Патогенез и эпидемиология инфекции вызванной вирусом простого герпеса. Механизм передачи — контактный (от человека к человеку). При возникновении заболевания наблюдают появление везикулёзных высыпаний на коже, что обусловлено цитолитической активноствю возбудителя. Вирус вызывает местное поражение и по чувствительным нейронам проникает в чувствительные ганглии, где затем персистирует в латентной форме.
Обострение происходит под воздействием физических факторов (инфекция, солнечный свет) или психологического стресса. Поскольку контроль заболевания осуществляет клеточный иммунитет, в группу повышенного риска входят пациенты со сниженным иммунитетом, у которых активация вируса может привести к тяжёлым последствиям.
Клинические признаки инфекции вызванной вирусом простого герпеса. Заболевание, вызванное вирусом простого герпеса типа 1, обычно протекает бессимптомно, но у детей часто наблюдают лихорадку, лимфаденопатию, везикулярный гингивит и стоматит, а у взрослых — фарингит и тонзиллит. Иногда наблюдают первичные офтальмологические заболевания, сопровождающиеся тяжёлым кератоконъюнктивитом.
При этом рецидивирующая инфекция может вызвать рубцовые изменения роговицы. Первичные кожные заболевания (герпетический панариций) обычно возникают при повреждении кожного покрова (обычно на пальцах). Также известны смертельные случаи энцефалита. При передаче вируса от матери к ребенку во время родов возникают генерализованные инфекции и энцефалит новорождённых.
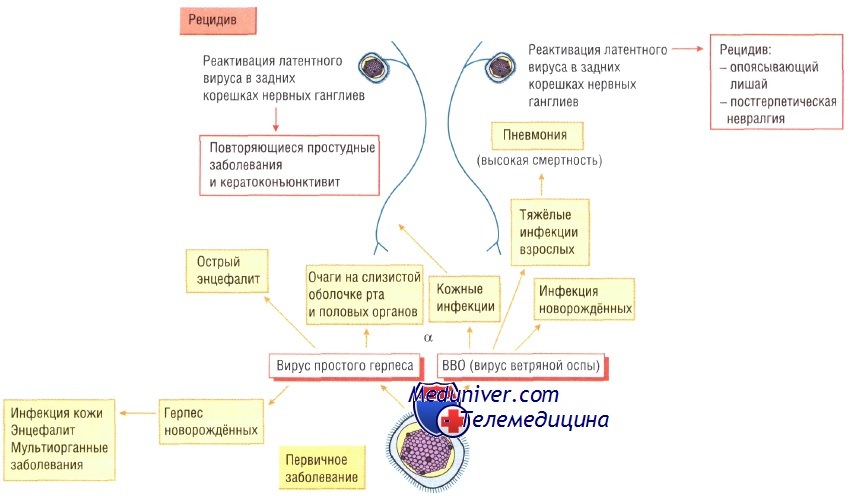
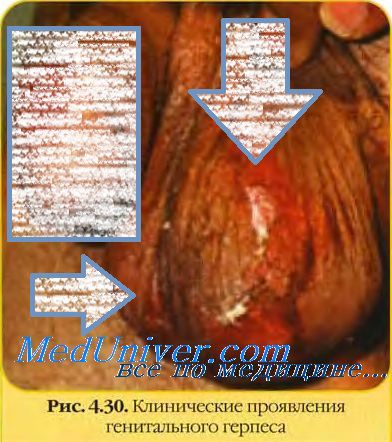
Инфекции, вызванные вирусом простого герпеса типа 2, характеризуются выраженным болевым синдромом, тяжёлым изъязвлением в области половых органов. Продолжительность заболевания до 3 нед. Повторная инфекция протекает в более лёгкой форме и со сниженным выделением вируса. При этом повышается вероятность заражения при половом контакте. Кроме того, генитальный герпес играет важную роль в передаче ВИЧ. Редкое осложнение инфекции — менингит.
Диагностика инфекции вызванной вирусом простого герпеса. В настоящее время всё большую значимость в диагностике заболевания приобретает молекуляно-генетический метод. Для накопления возбудителя применяют культуры тканей (везикулярная жидкость, тампоны из зева, половых органов). Кроме того, вирус может быть обнаружен с помощью электронной микроскопии везикулярной жидкости.
Применение серологических методов достаточно ограничено. Определение разницы в титре антител в сыворотке крови и спинномозговой жидкости используют для диагностики герпетического энцефалита. Магнитно-резонансная и компьютерная томография головного мозга помогают обнаружить очаги заболевания в височной доле (характерный признак герпетического энцефалита).
Лечение инфекции вызванной вирусом простого герпеса. Для лечения инфекции применяют противовирусные препараты для местного, внутривенного введения и приёма внутрь (ацикловир). Валацикловир и фамцикловир лучше всасываются при приёме внутрь. При энцефалите назначают внутривенные инъекции ацикловира.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
По данным ВОЗ заболевания, передаваемые вирусом герпеса, занимают 2-е место (15,8%) после гриппа (35,8%) как причина смерти от вирусных инфекций.
На территории России и в странах СНГ от хронической герпетической инфекции страдает не менее 22 миллионов человек [5]. Среди вирусных инфекций, поражающих генитальные органы, герпетическая инфекция встречается наиболее часто. Этому возбудителю принадлежит преобладающая роль в этиологии спонтанных абортов и преждевременных родов, в нарушении эмбрио- и органогенеза, врожденной патологии новорожденных.
Почти треть населения Земли поражена герпетической инфекцией и у 50% из них ежегодно наблюдаются рецидивы заболевания, так как иммунитета против этой вирусной инфекции нет. Имеются данные, что к 5 летнему возрасту около 60% детей уже инфицировано вирусом герпеса, а к 15 годам - почти 90% детей и подростков. Большинство людей являются пожизненными вирусоносителями. Причем в 85-99% случаев первичная инфекция у них протекает бессимптомно и только в 1-15% - в виде системной инфекции.
При обследовании студентов одного из колледжей США у 1-4% лиц были выявлены антитела к вирусу простого герпеса 1 и 2 типов; среди студентов университета - у 9%; лиц, посещающих клинику по планированию семьи - 22%, среди беременных женщин (не имеющих в анамнезе генитальный герпес) - 32% и лиц, посещающих клинику по поводу лечения заболеваний, передаваемых половым путем - в 46% случаев (Frenkel М., 1993).
Под герпетической инфекцией понимают болезни, характеризующиеся высыпаниями на коже, и/или слизистых оболочках в виде сгруппированных на отечно-эритематозном основании пузырьков и протекающие с поражением внутренних органов.
Этиология: герпес вирусы - "ползучие" ДНК, содержащие вирусы размером 150-300 нм.
Классификация:
Группа вирусов герпеса включает следующие подгруппы:
1. Вирус простого герпеса (ВПГ) - herpes simplex:
1.1. ВПГ 1 типа (ВПГ-1) клинически проявляется в виде герпеса губ, полости рта, глаз, генитального герпеса.
1.2. ВПГ 2 типа (ВПГ-2) - генитальный герпес и генерализованный герпес новорожденных.
2. V. Varicella Zoster - ветряная оспа и опоясывающий герпес (лишай).
3. Вирус Эпштейна-Барра - инфекционный мононуклеоз и лимфома Беркета.
4. Цитомегаловирус (ЦМВ) - цитомегалия.
Вирус простого герпеса.
Воротами инфекции являются губы, кожа, слизистые оболочки (в том числе и глаз). После инфицирования ВПГ-инфекция восходит по периферическим нервам до ганглиев, где и сохраняется пожизненно. Латентная герпетическая инфекция ВПГ-1 персистирует в ганглии тройничного нерва, а ВПГ-2 - в ганглии крестцового сплетения. При активации вирус распространяется по нерву к первоначальному очагу поражения [1].
Считается, что распространение герпетической инфекции поддерживается не цепочкой непрерывных заражений, а периодической активацией латентной инфекции, переходящей в клинически выраженные формы под влиянием факторов, снижающих функционирование иммунной системы (грипп, переохлаждение, лечение иммунодепрессантами, стресс и др.)
ВПГ-1.
Пути передачи: от больного человека здоровому при прямом контакте (чаще через поцелуй), воздушно-капельный, через предметы обихода, трансплацентарный, фекально-оральный и половой. ВПГ-1 можно выделить из слюны у 2-2,5% внешне здоровых лиц. Около 5% здоровых людей имеют вирус простого герпеса во рту, носоглотке, слезной жидкости, а иногда в спинномозговой жидкости и выделяют с фекалиями.
Герпес губ.
Клинически проявляется в виде группы пузырьков 1-3 мм в диаметре, расположенных на отечном гиперемированном основании. Пузырьки заполнены серозным содержимым и сгруппированы вокруг рта, на губах, крыльях носа. Иногда наблюдается распространенная герпетическая сыпь на коже рук, ягодиц.
Заболевание склонно к рецидивированию. Появление сыпи зачастую сочетается с головной болью, недомоганием, субфебрилитетом, чувством жжения, покалывания, зуда. Регрессируя, пузырьки ссыхаются с образованием корочки, либо вскрываются с образованием эрозий. Выздоровление наступает через 7-10 дней.
Лечение: мази ацикловир, зовиракс, госсипол, теброфеновая, а при корочках - тетрациклиновая или эритромициновая мазь.
Герпес полости рта протекает в виде герпетического стоматита и проявляется высыпаниями на слизистой оболочке полости рта в виде везикул, которые вскрываются с образованием эрозий с серовато-белым налетом (афтозный стоматит).
Лечение: обработка слизистых полости рта 0,1% раствором 5-йод-дезоксиуридина (керицид), таблетки ацикловир 200 мг 5 раз в сутки в течение 5 дней.
Герпес глаз протекает в виде кератитов (поверхностных или глубоких). Заболевание склонно к длительному рецидивирующему течению. Болезнь часто приводит к стойкому помутнению роговицы и снижению остроты зрения. Самыми опасными осложнениями являются: перфорация роговицы, эндофтальмит, повышение внутриглазного давления, развитие катаракты.
Лечение: таблетки ацикловир 200 мг 5 раз в сутки в течение 5 дней; закапывание раствора человеческого лейкоцитарного интерферона на конъюнктиву глаз, иммуностимуляторы.
ВПГ-2, генитальный герпес.
Основной путь передачи - половой. Заражение обычно происходит в том случае, когда у партнера, являющегося источником инфекции, наблюдается рецидивирование инфекции. Наряду с выраженными формами заболевания больше распространены асимптомные и не диагностируемые генитальные заболевания, обусловленные ВПГ-2. Такие больные становятся резервуаром и носителями вирусной инфекции, заражая других. Так, среди взрослого населения США их насчитывается 65-80% [1]. Асимптоматическое выявление ВПГ более определяется у женщин, чем у мужчин и более типично для ВПГ-2, чем ВПГ-1 [9].
Клиника.
1. Первичный генитальный герпес у лиц, не имевших контакта с ВПГ, характеризуется генитальными и экстра генитальными поражениями. Чаще всего процесс протекает на больших и малых половых губах, слизистой влагалища и шейки матки, в области балано-препуционной бороздки, крайней плоти, слизистой головки полового члена и мочеиспускательного канала [7]. После скрытого периода, длящегося от 1 до 5 дней, появляются боль, зуд в местах поражения, выделения. У 60% больных наблюдается повышение температуры, головные и мышечные боли, в 23% случаев - увеличение паховых и бедренных лимфоузлов. На пораженных участках возникают мелкие, 1-3 мм в диаметре серозные пузырьки, сидящие на гиперемированном основании. Вначале прозрачное, содержимое пузырьков становится мутным, гноевидным. Вскрываются пузырьки с образованием ярко-красной эрозии, покрываясь тонкой корочкой, которая по мере эпителизации отпадает. Заживление происходит без рубцов, но остается временная гиперемия или пигментация. Средняя продолжительность местных проявлений 10-12 дней.
Поражение мочеиспускательного канала начинается внезапно с выделения слизи в виде "утренней капли", почти бесцветной. Больные жалуются на расстройство мочеиспускания, боли, чувство жара, иногда зуда или жжения в области наружных гениталий [9]. Через 1-2 недели симптомы исчезают, но у большинства больных возникают рецидивы болезни с интервалами от нескольких недель до нескольких лет.
2. Вторичный генитальный герпес протекает легче, и выздоровление наступает быстрее. Высыпанных элементов мало. Рецидивы при ВПГ-2 проявляются раньше и чаще, чем при ВПГ-1.
Анализ сывороток различных групп населения показал очень высокое содержание антител против ВПГ-2 у пациентов с инвазивной карциномой шейки матки (в 83% случаев, против 20% в контрольной). Врачи должны более тщательно обследовать больных с герпетической инфекцией гениталий, как на вирусное, так и злокачественное заболевание шейки матки [4].
Вторичный генитальный герпес способствует возникновению рака головки полового члена.
Лечение: зависит от формы и периода заболевания.
При первичном генитальном герпесе местно 5% мазь или крем ацикловир, таблетки ацикловир по 200 мг 5 раз в день в течение 5 дней или внутривенное введение ацикловира 5мг/кг каждые 8 часов в течение 5 дней, бонофтоновая, теброфеновая или оксолиновая мази 6 раз в сутки в течение 15-20 дней, иммуностимуляторы.
При поражении уретры - введение каплями раствора интерферона [2].
При эрозиях - примочки или суппозитории с интерфероном, виферон.
При рецидивирующем генитальном герпесе:
- эпизодическое лечение каждого обострения: наружно 5% крем ацикловир 5 раз в день в течение 10 дней, иммуностимуляторы,
- при 6 и более обострений в год - продолжительная терапия ацикловиром по 200 мг 4-5 раз в день в течение 3 месяцев, иммуностимуляторы.
Профилактика заключается в 100% обследовании супругов и беременных женщин для выявления антител к вирусам герпеса. При явных клинических проявлениях генитального герпеса у беременной - рождение ребенка кесаревым сечением.
Прогноз - сомнительный, смертность достигает 90%.
2. Трансплацентарно или путем восходящей инфекции, особенно после преждевременного разрыва оболочек, а также путем передачи вирусов со спермой через инфицированную яйцеклетку, развивается внутриутробное инфицирование, на 50% обусловленное ВПГ-2. Наибольшее число заболеваний у новорожденных встречается при первичной инфекции у матери на поздних сроках беременности [6]. Это может привести к молниеносной диссеминирующей инфекции плода и послужить причиной нарушения органогенеза и возникновения уродств или обусловливает самопроизвольное преждевременное прерывание беременности, мертворождение и раннюю детскую смертность. Дети могут рождаться с недоразвитостью головного мозга, гепатитом, желтухой, менингитом, отложением кальция в головном мозге, поражением глаз, зрительного нерва, клеток крови, надпочечников и др. Такие дети, как правило, нежизнеспособны.
Вирус Зостер.
1. Ветряная оспа - развивается при отсутствии предшествующего иммунитета. Возбудитель передается воздушно-капельным путем. Чаще болеют дети. После исчезновения клинических проявлений вирус в организме сохраняется пожизненно.
2. При резком снижении защитных сил организма вирус персистирует, что манифестно проявляется в виде клиники ветряной оспы (у лиц, уже переболевших ей). Затем наступает (атентный период, характеризующийся развитием вирусов в ганглиях периферической нервной системы, и развивается клиника, широко известная под названием опоясывающий лишай [11]. Появляется сильное чувство жжения, стреляющие боли, покалывания. Боли часто симулируют клинику стенокардии, аппендицита и др. Вскоре на отечном гиперемированном основании развиваются многочисленные пузырьки с серозным содержимым. Высыпания локализуются по ходу нервов (чаще межреберных и тройничных). Присоединяются резкие, жгучие боли такой интенсивности, что больные кричат, вынуждены искать положение тела, при котором боли менее сильные. Пузырьки сливаются в буллы, появляются очаги некроза. Длительность заболевания 3-4 недели, после чего сыпь исчезает, боль может оставаться несколько месяцев или лет.
Больных с опоясывающим герпесом нужно наиболее тщательно обследовать на выявление онкологических заболеваний.
Лечение: местно в остром периоде жидкий анальгин и флуцинар; мази госсипол, теброфеновая, Ацикловир по 800 мг 5 раз в день в течение 7-10 дней и иммунокорректоры. После однократно перенесенного заболевание не повторяется.
Вирус Эпштейна-Барра.
С этим вирусом связано развитие инфекционного мононуклеоза. Заболевание часто дает малигнизацию в лимфому Беркета. Встречается больше в странах Африки и Азии, поражая детей 2-15 лет. Процесс протекает в верхней челюсти, яичниках, орбитах глаз, почках, селезенке, периферических лимфоузлах [12]. Лечение по схеме полихимиотерапии агрессивных лимфом.
Вирус Цитомегалии.
Инфекционный процесс характеризуется поражением слюнных желез с образованием в тканях гигантских клеток с внутриядерными включениями, ассоциирован с ВИЧ [10]. Для передачи возбудителя требуется длительный и тесный контакт [8].
Основной путь передачи - половой. Вирус обнаруживается в слюне, моче, крови, грудном молоке, сперме (очень много). Выделяется со слюной до 4 недель, с мочой - до 2-х лет.
Заболевание протекает бессимптомно или с небольшой клиникой. При внутриутробном заражении дети рождаются с недоразвитым головным мозгом, с массивными отложениями кальция в нем, водянкой головного мозга, гепатитом, желтухой, увеличением печени и селезенки, пневмонией, пороками сердца, поражением миокарда, паховой грыжей, врожденными уродствами и др.
Лечение: ацикловир внутривенно 5 мг/кг веса (10 мг/кг) 3 раза в день в течение 10 дней в сочетании с иммуностимулирующей терапией.
Литература.
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
СПИСОК ЛИТЕРАТУРЫ
Более 20 лет назад — в 1993 году — в Российской Федерации была введена обязательная регистрация случаев генитального герпеса. Тем не менее гиподиагностика этого заболевания до сих пор остаётся актуальной практической проблемой, и таким же образом дело обстоит не только у нас, но и в странах ближнего зарубежья.
Просто сравним цифры: в США заболеваемость составляет 200 случаев на 100 тыс. жителей в год. В Западной Европе поменьше — в среднем 80 на 100 тыс. населения. И это в целом вполне можно принять на веру. Но можно ли поверить официальной статистике Украины — 15 случаев на 100 тыс. — или России — 21,7 случаев (данные 2005 года) 7,9,10 ? А недооценка этого заболевания опасна, особенно в акушерстве, поскольку неонатальный герпес способен уносить жизни до 80% инфицированных новорождённых, оставляя выживших инвалидами с нарушением работы центральной нервной системы 5 .
Если рассматривать заболеваемость герпесом на карте мира, то сразу видны два правдоподобных полюса. Место наивысшего накала — конечно, Африка: до 80% взрослых женщин и до 50% мужчин серопозитивны по ВПГ-2. Кстати, независимо от географии, наиболее высокие показатели инфицированности ВПГ-2 отмечены у ВИЧ-позитивных лиц, что отражает как проблемность социального поведения этой группы населения, так и взаимопотенцирующее действие обеих инфекций 7 . Не менее высока доля серопозитивных лиц среди пациентов клиник, специализирующихся на лечении и профилактике заболеваний, передаваемых половым путём, — до 86%8. Самый спокойный на карте уголок — Испания, в которой серопозитивны 4% женского и 3% мужского населения соответственно. Если взять эту страну за эталон, то наиболее близки к нему Италия и Великобритания со своими одинаковыми показателями — 7 и 5% женского и мужского населения. В среднем же в Западной Европе показатель серопозитивности держится на уровне 16,5%.
По данным ВОЗовской глобальной оценки распространённости (общее количество случаев) и заболеваемости (число новых случаев) ВПГ-2, в мире инфицированы более чем полмиллиарда людей, и каждый год к ним прибавляются ещё по 24 млн 5 . Существует мнение, что в развитых странах генитальным герпесом может страдать 10–20% взрослого населения 7 . В многочисленных популяционных исследованиях показано, что уровень заболеваемости генитальным герпесом повышается с возрастом: единичные случаи выявляют в возрасте до 14 лет, а самая высокая заболеваемость — у 20–29-летних. Второй пик приходится на 35–40 лет. Основными факторами риска генитального герпеса выступают большое количество половых партнёров на протяжении жизни, раннее начало половой жизни, мужской гомосексуализм, принадлежность к негроидной расе, женский пол (!) и наличие в анамнезе инфекций, передаваемых половым путём 2,7,8 .
Что же касается России, то эпидемиология генитального герпеса у нас изучена явно недостаточно. Известно, что доля серопозитивных людей в популяции увеличивается с возрастом: от 1% у подростков 14–17 лет до 19–38% в возрасте 55–64 года. Более точных достоверных цифр, которые можно было бы сравнить с зарубежными, за последние 10–15 лет найти не удаётся 32 . При этом регистрируемая заболеваемость (чуть менее 22 на 100 тыс.) сравнительно с развитыми странами подозрительно низка.
Вероятно, мы наблюдаем недорегистрацию, и причины этого явления довольно легко обозначить. Первая — низкая обращаемость вследствие недостатка информированности населения. Часть больных с такой симптоматикой, как зуд, жжение или выделения из половых путей не считают её достаточным поводом, чтобы обращаться к врачу, а значит, не получают лечения, не заботятся о предохранении и длительное время выступают резервуаром генитального герпеса в популяции. Вторая причина — частные клиники, не всегда добросовестно подающие сведения в органы регистрирующие инстанции.
Штрихи к портрету
ДНК-содержащие вирусы семейства Herpesviridae персисти-руют в организме хозяина пожизненно — генетический материал вируса встраивается в ДНК нервных клеток человека: ВПГ-1 обычно осваивает ганглии тройничного нерва, ВПГ-2 — тазовые ганглии (а также клетки слизистых оболочек половых путей, например цервикального эпителия). Это едва ли не самые распространённые в популяции патогенные микро-организмы 1–3 . Сегодня известны восемь типов герпесвирусов, однако орофациальные и генитальные поражения вызывают только два типа: ВПГ-1 (преимущественно лабиальный герпес) и более опасный последствиями ВПГ-2 4,7 . Передача ВПГ-2, как правило, происходит половым путём, но возможен и вертикальный путь передачи — от матери ребёнку во время родов.
У 70–80% больных генитальным герпесом заболевание вызвано ВПГ-2, а у остальных 20–30% — ВПГ-1. Однако в последние годы ВПГ-1 в мочеполовом тракте выявляют всё чаще 6 . Скорее всего, происходит это по двум причинам: во-первых, в социуме всё большее распространение получают орогенитальные контакты, а во-вторых (и эта причина гораздо прозаичнее), с внедрением высокоточных методов диагностики вирусные инфекции стали лучше выявлять.
Небезопасный спутник
Как и всякое заболевание, передаваемое половым путём, генитальный герпес нередко становится виновником психологических и психосексуальных расстройств. И этот аспект инфектологии изучен ещё далеко недостаточно. В частности, многие проведённые в этом направлении исследования, к сожалению, используют ограниченную выборку, слишком разнообразные для сравнивания анкеты и отчётности, отсутствуют контрольные группы, не ведётся учёт уже существующих до инфицирования психопатологических отклонений. Так, хотя было показано, что рецидивы генитального герпеса и стресс часто совпадают по времени, не удаётся установить, что же из них первично — данные ретроспективных и проспективных исследований расходятся.
Тем не менее есть причины утверждать, что у страдающих рецидивами генитального герпеса нередко возникают депрессии; у них снижена уверенность в себе, они испытывают подавленность, гнев и враждебные чувства по отношению к человеку, который, как они полагают, их заразил 11,12,17 .
В исследовании белорусских коллег были использованы анкеты-опросники DIQL (Дерматологический индекс качества жизни) и RGHQoL (Опросник качества жизни пациентов с рецидивирующим генитальным герпесом), и оказалось, что качество жизни пациентов с рецидивирующим генитальным герпесом средней степени тяжести значительно снижено и не превышает 30% нормы 36 .
В числе отрицательных следствий генитального герпеса значится также и влияние на половую потенцию — доказано, что ВПГ-инфицированные мужчины достоверно чаще обращаются к врачу по поводу эректильной дисфункции 18 .
При беременности и потом
В ряде европейских стран по ВПГ-2 серопозитивны от 10 до 40% беременных. В России этот показатель достигает 31%. У беременных ВПГ-2 опасен не только везикулярными высыпаниями и нарушением психологического равновесия — описаны случаи гораздо более серьёзных осложнений: острого гепатита с тромбоцитопенией и коагулопатией 21 , эндометрита, диссеминированной инфекции 23 . И хотя частота таких осложнений невелика, о потенциальной возможности подобных состояний врачу следует помнить. Любое необъяснимое осложнение во время беременности должно быть рассмотрено в том числе и с точки зрения вероятности герпетической атаки.
Однако наиболее серьёзную опасность ВПГ представляет для плода ввиду несформированности его иммунной системы. Риск передачи инфекции плоду максимален в III триместре; при этом в 80% случаев инфицирование происходит интранатально, в 15% — постнатально и в 5% — антенатально 31 . К счастью, частота неонатального герпеса относительно невелика. В США, где учёт проводят очень скрупулёзно, статистика приводит показатель заболеваемости неонатальным герпесом 3,3 на 100 тыс. новорождённых 28 , для контраста в Малави (Восточная Африка) заболеваемость в 22 раза выше — 72 на 100 тыс. 29 . А вот что касается России, то достоверных и свежих данных по количеству заболевших новорождённых найти не удалось; публикации на эту тему, представленные в интернете, не отличаются высокой достоверностью и весьма противоречивы. По крайней мере, в 1995 году этот показатель держался на уровне 14,1 на 100 тыс. 30 . Получается, мы где-то посередине, но где именно — установить не так-то просто. А между тем осложнения неонатального герпеса разнообразны и часто фатальны (летальность может достигать 80%). Перенесённый неонатальный герпес нередко выливается в инвалидность.
- Невезикулярные поражения гортани и гениталий плода 23 .
- Водянка плода и преждевременные роды 20 .
- Эпиглоттит новорождённого с тяжёлой интоксикацией 22 .
- Тяжёлые поражения кожи и центральной нервной системы, гиперлейкоцитоз 25 .
- Сепсис в первые 5 нед 24 .
- Энцефалит, при подостром течении приводящий к мультикистозной энцефалопатии с минерализацией и дефицитом цереброспинальной жидкости 19 .
- Респираторный дистресс-синдром, апноэ, гепатомегалия, гемофагоцитоз, менингит 26 .
- Острый некроз сетчатки глаза 27 .
С сибирской обстоятельностью
Для того факта, что в России сложно получить эпидемиологические данные, есть довольно простое объяснение. Дело в том, что для такого рода исследований необходимо финансирование, которое во всём мире происходит за счёт государственных средств и фондов научных исследовательских центров, что в России пока случается совсем нечасто. Тем ценнее редкие и качественные российские научные работы. Так, в течение многих лет, с 1994 по 2005 год проходило крупное исследование популяций народов Сибири, включая городские и сельское население — в Новосибирске, Республике Горный Алтай и Республике Тыва.
Эта работа была инициирована в рамках международных исследований: WHO MONICA (Мониторинг заболеваемости и смертности от сердечнососудистых заболеваний и уровней их факторов риска) и HAPIEE (Детерминанты сердечно-сосудистых заболеваний в Восточной Европе: мультицентровое когортное исследование). Вот его хронология.
В общей сложности были проанализированы образцы сыворотки крови 1014 жителей; 47,4% составили мужчины и 52,6% — женщины. Протокол исследования одобрен Этическим комитетом НИИ терапии Сибирского отделения РАМН. Все обследованные подписали информированное согласие для участия в исследовании.
Обсуждаем и сравниваем
Общая распространённость антител к ВПГ-1 у взрослых не различалась между обследованными популяциями и в целом составила 99,4%. Таким образом, инфицированы этим вирусом почти все взрослые жители обследованных регионов. Среди школьников 14–17 лет антитела выявляли гораздо реже — серопозитивными оказались 78,8% подростков (рРаспространённость антител к ВПГ-2 у взрослого населения Новосибирска в целом за 1994–2005 года составила 21,1%, будучи выше у женщин по сравнению с мужчинами (26,3 и 17% соответственно; p13. Не исключено, что достаточно низкая инфицированность сибирских подростков связана с тем, что в этом регионе очень распространён ВПГ-1, в результате чего возникает перекрёстный иммунитет заодно и к ВПГ-2 5 . Как и ожидали исследователи, общая частота выявления антител к ВПГ-2 возрастала пропорционально возрасту (см. инфографику).
Что касается Тывы и Горного Алтая, то распространённость антител к ВПГ-2 у коренного населения в целом составила 20,2%. Однако женщины были инфицированы достоверно чаще мужчин — 23,5 и 7,9% соответственно (p=0,03). В целом Западная и Восточная Сибирь не различались по частоте выявления антител к ВПГ-2, а значит, этот показатель не зависит от этнической принадлежности (европеоиды и монголоиды), а также уровня урбанизации (промышленный мегаполис или посёлок) — распространение инфекции в Сибири универсально. А вот в США данные контрастны: неевропеиоидное население инфицируется ВПГ-2 почти в 3 раза чаще (45,9%), чем европеоидное (17,6%) 14 .
Если сравнивать распространённость ВПГ-2 в Сибири с другими регионами мира, то получается, что показатели наиболее близки к США и Скандинавским странам, и до благополучной Испании нам ещё далеко. С другой стороны, не может не радовать, что лидируем по частоте серопозитивности всё-таки не мы, а Африка.
В разных популяциях Сибири женщины ожидаемо оказались в 1,5–3 раза чаще инфицированы ВПГ-2, чем мужчины. Сходные данные отмечают практически во всех исследованиях мира. Дело в том, что поверхность слизистой оболочки половых органов у женщин значительно обширнее по площади, что повышает вероятность инокуляции вируса. Кроме того, у мужчин чаще возникают рецидивы, при которых клинические проявления менее выражены. А значит, мужчины смело вступают в половые контакты и заражают партнёрш в наиболее контагиозный период. Не исключено также, что молодые женщины чаще имеют контакты с более взрослыми партнёрами, частота инфицирования которых выше, чем у молодых. И, наконец, вероятность передачи вируса от мужчины женщине шестикратно превышает риск заражения мужчины от женщины 7 . При этом женщины в возрасте от 18 до 39 лет составляют группу риска, у них заболеваемость генитальным герпесом достигает 136 на 100 тыс. населения данного пола и возраста 9,10 .
Она растёт
Эпидемиологические исследования — не только показатель интереса интеллектуального сообщества к тому или иному вопросу. Врачу на приёме, через кабинет которого ежедневно проходят примерно 30 женщин, следует чётко представлять, что почти все они, за казуистическим исключением, носительницы ВПГ-1, и каждая пятая рискует обострением ВПГ-2.
Такая настороженность — очевидный путь преодоления гиподиагностики генитального герпеса, а значит, и всех сопутствующих ему проблем.
Для выявления возбудителя инфекций вирусов простого герпеса используют вирусоскоспический, вирусологический, биологический и серологические методы.
Материал для исследования инфекций вирусов простого герпеса — содержимое пузырьков, слюна, соскобы роговицы и др.
• При микроскопии мазков, окрашенных по Романовскому-Гимзе, выявляют многоядерные гигантские клетки (клетки Цанка) с тельцами включений (тельца Коудри).
• Для выделения вирусов простого герпеса используют культуры клеток и проводят посев исследуемого материала на куриные эмбрионы. В культурах клеток вирусы образуют бляшки (бляшки, образованные ВПГ 2-го типа крупнее) и дают характерный цитопатический эффект на куриных эмбрионах.
• Заражение лабораторных животных вирусом простого герпеса применяют редко. При заражении мозга белых мышей развивается специфический энцефалит; при заражении роговицы кроликов — герпетический кератит. Активность возбудителей in vivo нейтрализуют стандартные иммунные антисыворотки.
• Сывороточные AT к вирусам простого герпеса выявляют при РН, РСК или ИФА; однако ввиду значительной инфицированности населения обнаружение сывороточных AT не имеет существенной диагностической ценности. Большую ценность представляет выявление Аг вирусов в исследуемом материале методами РП и иммунодиффузии. Также используют РИФ с моноклональными AT,

Лечение и профилактика инфекций вируса простого герпеса
Поражения, вызванные ВПГ 1-го типа, обычно проходят самостоятельно и требуют лишь проведения местных мероприятий, направленных на профилактику вторичного бактериального инфицирования очагов поражения.
При тяжёлых поражениях назначают ацикловир; возможно его наружное применение в составе специальных мазей и кремов. При плохой переносимости препарата назначают фамцикловир, реже вызывающий побочные эффекты.
Для специфической иммунопрофилактики разработаны инактивированные вакцины, многократная иммунизация которыми снижает частоту рецидивов герпетической инфекции.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

