Вирус герпеса у лошадей
Обновлено: 26.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Постгерпетическая невралгия: причины появления, симптомы, диагностика и способы лечения.
Определение
Постгерпетическая невралгия - это боль или аномальные чувствительные ощущения, связанные с поражением нервной системы вирусом ветряной оспы.
Причины постгерпетической невралгии
После перенесенной ветряной оспы (ветрянки) вирус герпеса человека 3-го типа – вирус Варицелла Зостер (Varicella zoster) - из высыпаний на коже и слизистых может перемещаться в чувствительные ганглии (узлы, состоящие из скопления нейронов) спинномозговых нервов грудного, поясничного уровней или тройничного нерва. Там вирус в течение десятилетий способен оставаться в латентном (неактивном) состоянии. При снижении иммунитета (например, на фоне вирусных заболеваний, химиотерапии, онкологических заболеваний, терапии глюкокортикостероидными гормонами системных заболеваний соединительной ткани (ревматических болезней)) вирус может активироваться и вызывать развитие опоясывающего герпеса (опоясывающего лишая, Herpes zoster) или невралгии тройничного нерва.
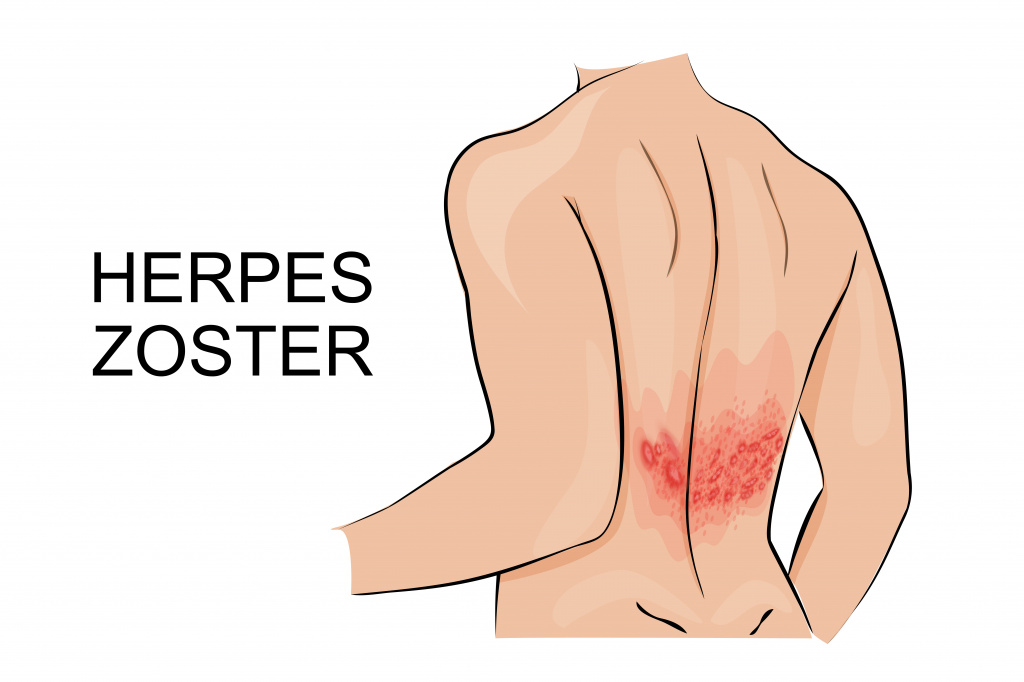
Заболевание начинается с односторонней боли, чувства жжения, повышенной кожной чувствительности, после чего, иногда спустя 1-2 недели появляется покраснение, а затем - пузырьковые высыпания на коже. У 50% больных высыпания локализуются на туловище (как правило, вдоль межреберных промежутков на уровне грудного отдела позвоночника, иногда – в области поясницы, крестца), у 20% - на голове (при поражении тройничного нерва, возможно поражение глаз, ушей), у 15% - на руках, и у 15% - на ногах. В большинстве случаев с течением времени боль проходит самостоятельно - выздоровление происходит через 2-3 недели, но иногда (примерно у 20% больных) развивается осложнение опоясывающего герпеса - постгерпетическая невралгия.
Постгерпетическая невралгия редко наблюдается у детей и молодых людей, но ее частота значительно увеличивается в пожилом возрасте.
Реальная распространенность постгерпетической невралгии неизвестна, поскольку нет единой точки зрения на временной промежуток между высыпаниями, появлением боли и продолжительностью болевого синдрома.
Классификация постгерпетической невралгии
Ряд авторов предлагают различать три временные фазы болевого синдрома, связанного с Herpes zoster.
- Острая герпетическая невралгия, при которой боль длится до 30 дней с момента появления сыпи.
- Подострая герпетическая невралгия, продолжающаяся 30-120 дней после возникновения сыпи.
- Постгерпетическая невралгия, при которой боль сохраняется более 120 дней после возникновения сыпи.
Симптомы постгерпетической невралгии
Основной жалобой пациентов является боль. Она характеризуется различной интенсивностью и частотой – от легкой до крайне мучительной, от кратковременной до постоянной. При опоясывающем герпесе болевые ощущения могут распространяться за пределы локализации высыпаний. В клинической картине постгерпетической невралгии можно выделить следующие типы боли:
- постоянная боль, которую пациенты описывают как тупую, давящую или жгучую;
- пароксизмальная (приступообразная) боль, которая возникает внезапно, острая, стреляющая, пронзающая;
- аллодиния – боль, возникающая в ответ даже на очень слабые раздражители, которые при обычных обстоятельствах боль не вызывают, – например, на легкое прикосновение холодной рукой.
Некоторые пациенты жалуются на интенсивный зуд, который локализуется, как правило, в области головы и шеи.
Диагностика постгерпетической невралгии
В начале заболевания опоясывающим герпесом, когда пациентов беспокоит только боль, врач может подозревать заболевание сердца, межреберную невралгию, остеохондроз. Однако с появлением высыпаний диагноз становится очевидным.
Инструментальная и лабораторная диагностика, как правило, не проводятся.
В нетипичных случаях может быть назначен серологический тест 256 в комплексе с тестом № 257 (IgM антитела) для диагностики ветряной оспы. Кроме того, эти исследования могут потребоваться для оценки иммунитета к вирусу.
Синонимы: Анализ крови на антитела к вирусу ветрянки; Ветряная оспа; Вирус герпеса человека 3-го типа; ВГВ-3 типа; Вирус varicellae-zoster; Опоясывающий герпес. Chickenpox; Human herpesvirus 3 IgG; Varicellazoster virus IgG; Herpeszoster IgG. Краткое описание исследования Антитела.
Герпесвирусные инфекции лошадей
[Equine herpesvirus infections]
Герпесвирус лошадей представлен следующими типами: Equine herpes virus type l (ринопневмония), herpesvirus type 2 (коитальная экзантема) и Equine herpesvirus type 3 (цитомегалоподобная инфекция лошадей).
По клиническому проявлению герпетической инфекции указанное разделение герпесвирусов лошадей несколько условно, так как иногда, например, Herpesvirus equi-2, помимо коитальной экзантемы, вызывает у жеребят кератоконъюнктивит. Помимо того, из костного мозга, лейкоцитов крови и культуры почечных клеток клинически здоровых лошадей удавалось выделить ряд латентных герпетических вирусов, роль которых в патологии этих животных неясна. В 1973 г. К. П. Юров и В. К. Сологуб изолировали четыре штамма латентного герпесвируса лошадей из культуры почечных клеток жеребят. Установлена высокая выделяемость (89 %) герпесвирусов лошадей второго типа 2 из лейкоцитов крови лошадей. От лошадей, имевших лихорадку, выделен вирус, классифицированный как Herpesvirus equi-2. В Нью-Маркете 90 % лошадей имели AT к вирусу герпеса лошадей типов 1 и 2. Впоследствии был выделен вирус, отличный от возбудителя РПЛ и обозначен как Equine herpesvirus-3. Выделен и Herpesvirus egui-4, который вначале рассматривали как лошадиный цитомегалови-рус. Герпесвирусы лошадей 2-, 3- и 4-го типов в АГ отношении оказались между собой более родственны, чем с вирусом РПЛ. Вирусы коитальной экзантемы лошадей (HV-Eq-2) выделяли из лейкоцитов внешне здоровых кобыл и от кобыл с клиническими признаками пузырьковой сыпи. Однако при интраназальном заражении этим вирусом у жеребых кобыл происходили аборты. Выделено 26 штаммов из различных органов абортированных плодов и носовых истечений лошадей, больных ринитом. Все штаммы принадлежали к одному типу EA/S kovbinde, который в РН оказался идентичным американскому штамму Ку-13. В дальнейшем было выделено много подобных штаммов от клинически здоровых лошадей.
Химический состав не отличается от HV-Eq-1. Секвенировали ДНК ГВЛ-5 в регионе гликопротеина В и провели анализ его аминокислотной последовательности.
Вирусы термолабильны, инактивируются при 56 °С в течение 30 мин, чувствительны к рН 3 и эфиру. Сохраняют инфекционность в среде, свободной от сыворотки в течение 3 мес; при — 40 °С — 1,5 лет. Действие трипсина на различные штаммы вируса герпеса лошадей оказалось неодинаковым. АГ структура не изучена.
АГ активность детально не изучена; у кроликов вирусы индуцируют образование ВНА. Специфические ВНА обнаружены в сыворотке клинически здоровых лошадей. В образцах сыворотки лошадей обнаружены в 27,7—29,3 % случаях антитела к лошадиному герпесвирусу (ЕНУтипа 3), у молодых жеребцов — 1,6 %. Антитела против хламидий присутствовали у 5,1 % молодых жеребцов, 31.4 % взрослых жеребцов и 24,6 % Кобыл.
Вирусы герпеса лошадей в АГ отношении отличаются от вируса РПЛ (вирусного аборта) лошадей 1- и 2-го подтипов. Поэтому их предложено отнести к типу 3 герпесвирусов лошадей. Среди множества выделенных штаммов этого типа антипенных различий в РН не обнаружено. Однако штаммы, относящиеся к типу HV-Eq-З в РН, отличались от герпесвирусов лошадей 1- и 2-го типов. Среди трех штаммов вируса герпеса лошадей типа 3, выделенных из культуры лейкоцитов от здоровых лошадей, один обнаружил АГ родство с цитомегаловирусом. В исследованиях Пламмера и др., (1973 г.) из 19 изученных штаммов 9 оказались идентичны вирусу ринопневмонии, 10 медленно размножающихся вирусов были АГ неоднородны и не имели серологического родства с 9 штаммами вируса ринопневмонии лошадей.
Спектр патогенности в естественных условиях не изучен. Многие выделенные штаммы НУ-ЕяЗ-вызывали латентную инфекцию. Локализация вируса, вирусемия, вирусоносительство, вирусовыделение детально не изучены. Известно, что вирус герпеса лошадей типа 3 удавалось выделить из лейкоцитов клинически здоровых лошадей. Экспериментальная инфекция воспроизводилась на кроликах, заражаемых в спинной мозг. У животных развивалась хроническая инфекция без клинических проявлений. При гистологическом исследовании у них обнаруживали менингомиелит в области шейного, грудного и поясничного отделов спинного мозга. Нервные клетки оставались неповрежденными. Вирус герпеса лошадей типа 3 оказался непатогенным для КЭ, новорожденных мышат, хомячков, молодых морских свинок и кроликов при разных методах заражения.
Многие штаммы, относящиеся к HV-Eq-З, размножаются в первичной культуре клеток почки жеребят, обезьян, коровьих и овечьих эмбрионов, вызывая дегенерацию клеточного монослоя и образование эозинофильных внутриядерных включений типа А. Инфекционность культуральной жидкости достигала 105ТЦД,5о/мл. Герпесвирусы лошадей типа 3 культивируются и образовывают бляшки в клетках РК-15 и Z. Для получения бляшек использовали сложное покрытие с метилцеллюлозой. Размер бляшек 0,85—1,5 мм в значительной степени зависел от числа пассажей вируса в культуре клеток РК-15. Культуры клеток почек эмбриона свиней, HeLa, KB, почечных фибробластов кроликов оказались нечувствительными. Особенности внутриклеточной репродукции не изучены. Эпизоотологические особенности, источники и пути передачи инфекции не описаны.
Специальные методы диагностики не разработаны. Диагностика может производиться в научно-исследовательских учреждениях. Разработан блокирующий ELISA на основе МКАдля выявления двух типов лошадиного герпеса вируса. Были установлены высокие титры антител в кроличьей антисыворотке и жеребячьей антисыворотке животных инфицированных, EHV1 и EHV4. В 344 сывороточных образцах найдено хорошее совпадение между титрами VN (вирусной нейтрализации) и ELISA. Относительная чувствительность и специфичность блокирующей ELISA по сравнению с РН была 99,9 и 71 % соответственно. Титры увеличивались также в ELISA после вакцинации вакциной EHV1 и после первичных полевых инфекций у жеребят. Сделано заключение, что блокирующий ELISA более чувствителен, легче и быстрее по исполнению и более воспроизводим, чем тесты РН. Этот тест рассматривается как ценный инструмент для серологического диагноза обоих инфекций — EHV1 и EHV4. Применяется и ПЦР для дифференциации серотипов вирусов герпеса лошадей.
У лошадей вирус герпеса регистрируется очень часто. В одном исследовании молодняка имелись 100 % серологические данные поражения лошадей вирусом герпеса EHV-4, который является основной причиной заболеваний верхних дыхательных путей. Заражение EHV-1 встречается реже, и вдобавок к клиническим признакам, аналогичным EHV-4, он вызывает огромное количество непредсказуемых выкидышей, гибель новорожденных жеребят и миелоэнцефалопатию. Патогенный потенциал EHV-2 неясен; однако, серологическое исследование показывает, что большинство лошадей являются носителями данного вируса. EHV-2 обычно выявляется в крови здоровых жеребят и в секрете дыхательных путей жеребят с заболеваниями дыхательной системы. Коитальная экзантема представляет собой венерическое заболевание, вызываемое EHV-3. На пенисе и крайней плоти жеребца, а также на слизистой наружных половых органов кобылы появляются везикулярные поражения.
Более распространенной формой EHV является инфекция дыхательных путей, она высококонтагиозна и ограничивает активность животного, что имеет экономическое значение. Реже встречаются абортивная форма и миелоэнцефалопатия, но и они имеют экономическую значимость из-за высокого процента летальности.
Лечение EHV представляет сложность в связи с вирусоносительством и наличием латентного течения, которое может давать рецидивы без клинических признаков. Кроме того, EHV-1 может поражать иммунную систему и вызывать состояние иммуносупрессии. Иммунитет после естественного заражения или вакцинации нестерильный, и лошади могут заражаться повторно в течение жизни.
ЗАБОЛЕВАНИЯ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Принимая во внимание иммуносупрессивное свойство EHV инфекций, у некоторых лошадей развивается синдром острого воспалительного процесса в дыхательных путях, ограничивающий активность, даже после исчезновения клинических признаков острой фазы инфекционного заболевания. Другими осложнениями EHV инфекций являются вызванная нагрузкой дисфункция акта глотания после воспаления дыхательных путей.
Четырехкратное увеличение нейтрализации вируса (VN) или титры комплемент-связывающих (CF) антител говорят о заражении EHV. Однако такое увеличение с трудом поддается демонстрации, так как внутри инфекции быстро увеличивается количество титров, особенно в начале появления клинических признаков. При CF и VN анализе происходит перекрестная реакция между EHV-1 и EHV-4, но возможно проведение ELISA на специфичность.
Данный вирус выделяют из мазка с носоглотки или цитрированной или гепаринизированной цельной крови в течение 12 дней после заражения. Пробы из носоглотки берут стерильным марлевым тампоном 2 дюйма х 2 дюйма (5,08 см х 5,08 см), прикрепленным к скрученной проволоке из нержавеющей стали, или маточной инфузионной пипеткой. Марлю затем помещают в транспортную питательную среду, а затем кладут в холодильник или замораживают при транспортировке в лабораторию.
Полимеразная цепная реакция (PCR) является быстрым чувствительным и недорогим диагностическим методом, используемым в настоящее время для клинического применения. Для ее проведения необходимы мазки из носовой полости и собранная цельная кровь с этилендиаминтетрауксусной кислотой (EDTA) в качестве антикоагулянта.
Лечение и контроль
Большинство неосложненных респираторных EHV инфекций проходят самопроизвольно в течение нескольких недель. Предоставление отдыха и высококачественного сена играет важную роль в процессе выздоровления. Животные должны отдыхать до исчезновения признаков кашля, выделений из носовой полости и патологических хрипов в легких. EHV-1 вызывает подавление иммунной системы, и зараженных лошадей нужно наблюдать на наличие вторичной бактериальной инфекции. У некоторых лошадей развивается стойкое воспаление нижнего отдела дыхательных путей, признаками которого являются непереносимость нагрузки, стойкий кашель и патологические хрипы в легких после перенесенной респираторно-вирусной инфекции. Данный синдром нужно дифференцировать от бактериальной пневмонии и бронхита, исследовав образцы, полученные посредством аспирации трахеи. Цефтиофур (2,2 мг/кг в/м через каждые 24 часа) или комбинация сульфаметоксазола с триметопримом (25 мг/кг перорально через каждые 12 часов) подходят для начального этапа лечения вторичной бактериальной инфекции.
Поскольку инфекции вируса герпеса вызывают подавление и поражение иммунной системы, в качестве дополнительной терапии могут использоваться иммуномодуляторы. Внутривенное введение инактивированного Propionibacterium acnes (EqStim) является для здоровых лошадей эффективным иммуномодулятором, но тщательные клинические исследования не были проведены для подтверждения его эффективности при лечении респираторно-вирусных заболеваний. Хотя интерферон-альфа не всасывается при оральном приеме (50 Ед. перорально через каждые 12 часов в течение 5 суток), он уменьшает признаки воспаления нижнего отдела дыхательных путей у скаковых лошадей, возможно посредством стимуляции фарингеальных лимфоидных тканей.
Вакцинация против EHV-1 и -4 уменьшает продолжительность и тяжесть течения патологического процесса, но не всегда предотвращает заражение или носительство вируса. Кроме того, продолжительность иммунитета после вакцинации недлительная; поэтому рекомендуется ревакцинация с перерывом в 3-4 месяца для лошадей с высоким риском заражения. Первичная вакцинация жеребят должна начинаться в 4-6 месяцев, 3-х кратно, с месячным интервалом.
Миелоэнцефалопатия у лошадей, вызванная вирусом герпеса (EHM), является распространенной причиной заболевания центральной нервной системы (ЦНС) у лошадей. Подавляющее большинство EHM вызывается EHV-1 типом; ее редко вызывает EHV-4. Хотя вид вируса герпеса, вызывающий миелоэнцефалопатию, не был досконально изучен, строгий ферментный анализ показал схожесть изолятов при вспышках EHM. Вирусный рецидив или капельная инфекция приводят к виремии. Поражение васкулярного эндотелия ЦНС приводит к тромбозу и ишемической миелоэнцефалопатии. Вовлечение иммунной системы влечет за собой отсутствие клинических признаков у жеребят, не поражавшихся ранее вирусом EHV.
Анализ цереброспинальной жидкости (CSF) лошадей при EHM показывает повышенное содержание общего белка, с незначительными патологическими изменениями или их отсутствием в ядросодержащих клеток. Наличие этой диссоциации между концентрацией альбумина и цитологией, в сочетании с характерными клиническими признаками в значительной мере подтверждает диагноз. Наличие патологических изменений в CSF не связано с клиническими признаками или прогнозом. При цитологическом исследовании CSF сначала обнаруживаются одноядерные клетки. CSF часто приобретает желтый цвет (ксантрохромия), вызванный распадом эритроцитов. Выделить вирус из CSF редко удается. Серологическое исследование, PCR и методы выделения вируса, используемые для диагностики респираторных заболеваний, вызванных EHV, подходят также и для диагностики EHM.
Для лечения EHM были одобрены кортикостероиды (дексаметазон 0,05-0,10 мг/кг в/в или в/м через каждые 12 часов). При применение кортикостероидов нужно взвесить их противовоспалительные свойства и отрицательное воздействие на иммунную функцию, а также возможность появления ламинита. Оценка эффективности кортикостероидов представляет сложность, учитывая естественный ход данного заболевания. Хотя эффективность диметил сульфоксида (DMSO; 1 г/кг, разведенный в физиологическом растворе до 10 %, в/в через каждые 24 часа в течение 3 дней) при лечении EHM не была изучена, имеются сведения о его способности подавлять агрегацию тромбоцитов и уничтожать свободные радикалы, что говорит в пользу его применения. Флуниксин меглумин (1,1 мг/кг в/в через каждые 24 часа) назначают для лечения васкулита ЦНС.
При лечении лошадей находящихся в лежачем положении очень важную роль играет правильный уход. Во время вспышек ЕНМ лошадей можно лечить в родном питомнике. Лошадей находящихся в лежачем положении нужно держать в таком положении как можно дольше, либо поддерживать их с помощью подвязки. В тяжелых случаях назначается противомикробное лечение (комбинация сульфометоксазола с триметопримом 25 мг/кг перорально через каждые 12 часов или цефтиофур 2,2 мг/кг в/м через каждые 12 часов), поскольку подавление иммунной системы, вызванное кортикостероидами, катетеризация мочи и пролежни могут привести к вторичной бактериальной инфекции. У лошадей с затруднением акта глотания нужно тщательно следить за приемом воды и корма. При наличии атонии мочевого пузыря по крайней мере дважды в день должна проводиться катетеризация мочи. Лежачие и послушные амбулаторные лошади спокойно выносят постоянные катетеры-баллоны Фолея (24-28 French).
Для лечения ЕНV инфекций одобрен ацикловир (10 мг/кг перорально 5 раз в день); однако, имеются данные, что он не оказывает эффективного действия при заражении EHV-1, а исследования его фармакокинетических свойств при применении у лошадей отсутствуют. Пенцикловир эффективнее in vitro против EHV-1, но о его применении у лошадей ничего не известно. При лечении ацикловиром нужно следить за функцией почек.
Обычно прогноз зависит от тяжести клинических признаков и начальной реакции на лечение. Прогноз для лошадей находящихся в лежачем положении и которые отвечают слабой реакцией на действующее лечение, неблагоприятный. У многих выживших лошадей с признаками атаксии задних конечностей имеются остаточные нарушения, которые мешают их возвращению к спортивным соревнованиям. Лошади с умеренными нарушениями могут вернуться в конный спорт.
Профилактика и контроль
Вакцинация во время вспышек вызывает сомнения. Имеющиеся в настоящее время вакцины не дают гарантий в заражении EHM. Вакцинация уменьшает вирусоносительство, но не предупреждает возникновение инфекции. Поскольку раннее воздействие EHV-1 или -4 может служить фактором риска для возникновения ЕНМ, автор данной статьи не одобряет вакцинацию во время вспышки.
Известно повсеместное возникновение выкидышей вследствие заражения EHV, который является наиболее важной причиной инфекционного абортирования у кобыл. Выкидыши обычно вызываются EHV-1; однако, известны единичные случаи абортирования, вызванных EHV-4. Заражение происходит воздушно-капельным путем или при рецидиве латентного носительства в период стрессов. У абортированных кобыл могут отсутствовать признаки заболевания дыхательных путей. Виремия приводит к заражению плода или васкулиту эндометрия. В большинстве случаев абортированный плод является сильно инфицированным и служит важным источником заражения для других кобыл; однако, плод может оказаться незаразным при быстром изгнании его из матки в результате сильного воспаления эндометрия.
Абортированный плод без предварительных признаков изгнания плода является характерным симптомом заражения EHV. Плацента бывает без патологических изменений либо слегка отечная и выходит вместе с плодом. Тяжелые поражения абортированного плода включают окрашивание мекония, отек легких, желтуху, петехии, подкожный отек, увеличение селезенки и избыточное количество перитонеального и плеврального выпота. В печени наблюдается большое количество бело-серых 5-мм очагов некроза. Абортированный плод, который является источником заражения, нужно унести в целлофановом пакте во избежание кантаминирования окружающей среды. Патологическое вскрытие абортированного плода следует проводить на отдаленном участке с приспособлением для проведения дезинфекции. Против EHV эффективны дезинфицирующие средства на основе фенола.
Аборты возникают в период от двух недель до нескольких месяцев после вирусного заражения. Большинство кобыл абортируют в последние 4 месяца жеребости. Чаще встречаются эпизодические случаи абортирования одной или двух кобыл в стаде; однако, вспышки абортирования жеребых кобыл могут наблюдаться более чем в половине стада.
Серологическая диагностика весьма проблематична, поскольку заражение может произойти за несколько недель до абортирования, а данный рецидив может не вызывать реакцию антител. Если в диагностической лаборатории нельзя подвергнуть исследованию свежий абортированный плод, для исследования берутся замороженные парные пробы легких, печени, вилочковой железы и надпочечников абортированного плода, содержащихся в формалине. Для подтверждения диагноза могут служить флуоресцентное окрашивание антител, иммуногистохимический анализ и изоляция вируса из тканей плода.
Лечение и контроль
Иммунитет нестерильный, и кобылы не застрахованы от повторного заражения и абортирования в будущем. Вирус не задерживается в репродуктивной системе и если абортирование произошло без осложнений, способность к оплодотворению не подвергается риску, и специфическое лечение не назначают.
Главным источником EHV является выдыхаемый респираторный секрет, и поэтому лошадей с признаками заболевания дыхательных путей нужно изолировать. В связи с широкой распространенностью EHV молодых кобыл на последних месяцах жеребости нужно отделить от других кобыл с жеребятами, а так же от жеребят без подсоса, годовалых жеребят и рабочих лошадей. Кобыл нужно разделить на небольшие группы в зависимости от срока жеребости. Стресс может вызвать рецидив латентного вируса; поэтому лошадей на поздних сроках жеребости не стоит перевозить на большие расстояния. Вакцинация привела к уменьшению возникновения абортирования вследствие данной патологии, но не дает 100 % гарантии. Кобыл нужно вакцинировать на пятом, седьмом и девятом месяце жеребости патентованной инактивированной вакциной для предупреждения абортирования при заболевании EHV. Многие ветеринары также одобряют вакцинацию на третьем месяце жеребости.
В случае абортирования, все жеребые кобылы должны оставаться на ферме до выжеребки, поскольку продолжительность между заражением и абортированием составляет несколько месяцев. Если абортирование плода случилось в стойле, данный участок должен быть продезинфицирован, а подстилка сожжена. Другие лошади должны оставаться на ферме в течение 1 месяца после последнего абортирования. Всех лошадей, покинувших ферму во время подозреваемого выкидыша вследствие вируса герпеса, нужно изолировать от кобыл, находящихся на поздних сроках жеребости. Для ограничения распространения заболевания, всех жеребых кобыл разделяют на небольшие группы.
Коитальная экзантема лошадей имеет широкое распространение и вызывается EHV-3. Это высококонтагиозное, но проходящее само собой венерическое заболевание, вызывает везикулярные поражения пениса и крайней плоти жеребцов и слизистой оболочки наружных половых органов кобылы. Кобылы с латентными признаками заражения передают вирус жеребцам. Заболевание у жеребцов протекает в более тяжелой форме, чем у кобыл, и в состав клинических признаков входят апатия, анорексия и лихорадка. Могут возникать неострые инфекции без проявления клинических признаков. Примерно через 2-5 суток после заражения появляются везикулы, сначала на пенисе, а затем на крайней плоти. Везикулы переходят в пустулы, а затем отшелушиваются, приводя к изъязвлениям вплоть до 1,5 см в диаметре. Заживление происходит в течение месяца, но могут оставаться депигментированные участки. У кобыл возникают аналогичные эрозии на слизистой оболочке наружных половых органов и коже промежности, которые превращаются в корочки, а затем заживают. Возможно наличие поражений на коже в области губ и носовых отверстий, а также конъюнктивы. Могут возникать аналогичные поражения в области морды жеребенка, сосущего молоко зараженной кобылы. Хотя передача вируса главным образом происходит половым путем, также возможна ятрогенная передача посредством зараженных предметов ухода.
Возможно существование латентного течения инфекции, а также возникают повторное инфицирование без проявления клинических признаков. Рецидивы могут возникать у племенных кобыл с клиническими признаками заражения на поздних стадиях жеребости. Диагностика зависит от клинических признаков и истории болезни. Максимальный титр антител наблюдается на 2-3 неделе после заражения. VN антитела могут обнаруживаться более, чем через год после инфекции, а CF антитела обнаруживаются лишь в течение 2 месяцев после заражения. Данный вирус можно изолировать из мест эрозий во время острой фазы воспаления.
Хотя заражение, по-видимому, не влияет на способность к оплодотворению и возможности жеребости, некоторые жеребцы могут отказываться спариваться с кобылами, и многие ветеринары рекомендуют, чтобы жеребцы спаривались лишь после заживления поражений. Применение искусственного влагалища с открытым концом и искусственного осеменения снижает вероятность передачи вируса. Лечение поражений местными антибиотическими мазями помогает предотвратить возникновение вторичных инфекций.
ПЕРИНАТАЛЬНОЕ ЗАРАЖЕНИЕ ЛОШАДЕЙ ВИРУСОМ ГЕРПЕСА 1
Заражение кобылы EHV-1 на позднем сроке жеребости может привести к синдрому тяжелого заболевания новорожденного жеребенка. Согласно многим данным относительно перинатальной инфекции EHV, существуют подтверждения заболеваний, связанных с EHV, в том числе случаи абортирования и миелоэнцефалопатии в питомнике. Жеребята могут рождаться слабыми или внешне нормальными. Клинические признаки появляются в течение 48 часов после родов и включают угнетение дыхания, слабость, желтуху, лихорадку, тахикардию и в некоторых случаях диарею. Большинство жеребят с вышеуказанными клиническими признаками, зараженных EHV-1 в перинатальный период, гибнут, а те, кто выжил, нуждаются в интенсивной терапии. Лейкопения со сдвигом влево, нейтропения и тяжелая лимфопения говорят о перинатальном заражении EHV-1. В некоторых случаях увеличивается количество печеночных ферментов.
Жеребята, выжившие после заражения EHV-1, не обязательно приобретают сероконверсию; однако данный вирус можно выделить – а возможно и распознать с помощью PCR – из клеток периферической крови. При патологоанатомическом вскрытии обнаруживаются интерстициальная пневмония, некроз вилочковой железы и адренокортикальное кровотечение. Наличие заражения можно подтвердить путем изоляции вируса из патматериала или путем идентификации EHV-1 антигена посредством иммуногистохимического анализа.
Ринопневмония лошадей. Вирус ринопневмонии лошадей.
Ринопневмония лошадей - острое респираторное заболевание лошадей. Вирус размножается и накапливается в слизистой оболочке верхних дыхательных путей и в легких, вызывая ринопневмонию. У беременных животных вирус проникает в матку, плод и околоплодные оболочки, вызывая патологический процесс и аборт во второй половине беременности. Герпесвирус, обозначавшийся в течение 50 лет как вирус ринопневмонии — аборта лошадей, на самом деле представляет не один, а два различних вируса. Герпесвирус 1 лошадей (ГВЛ-1) вызывает аборты и респираторную патологию, а герпесвирус 4 лошадей (ГВЛ-4) — ринопневмонию. Оба вируса вызывают сходную патологию респираторных органов. ГВЛ-1 вызывает аборты, как правило, в последние 4 мес. беременности. Плоды обычно рождаются мертвыми. Аборты, гибель плодов в период беременности и реже энцефалиты в неблагополучных стадах могут встречаться у 70% лошадей.
В связи с установлением этиологической роли двух герпесвирусов (ГВЛ-1 и ГВЛ-2) в патологии двух клинически сходных заболеваний лошадей возникла необходимость пересмотреть многие вопросы, в том числе специфическую профилактику этих болезней, вызываемых двумя вирусами. Антигенное родство этих вирусов дает возможность использовать гетерологичные вакцины, например, вакцину из ГВЛ-1 для профилактики инфекции ГВЛ-4, хотя более действенным является применение гомологичных вакцин против каждого возбудителя. Вероятно, более эффективный контроль болезней, вызываемых ГВЛ-1 и ГВЛ-4, может быть достигнут с помощью бивалентной вакцины, содержащей оба вируса. Основные вспышки эпизоотических абортов у лошадей связаны с ГВЛ-1. ГВЛ-4 удается выделить после гибели животного из пораженной нервной ткани.
Естественный иммунитет после переболевания ринопневмонией (ГВЛ-4) сохраняется не более 4 мес, а после аборта (ГВЛ-1) - несколько дольше. Для профилактики болезни в основном применяют живые вакцины. Генетические изменения вируса особенно быстро происходят при культивировании в клетках неестественного хозяина. Живая вакцина из штамма RAC-H получена адаптацией вируса к сирийским хомякам, а затем длительным пассированием (360 раз) в первичной культуре клеток почки телят. ГВЛ-1 выделяли из абортированных плодов и от новорожденных жеребят, ГВЛ-4 выделяли при респираторных заболеваниях. ГВЛ-4, в отличие от ГВЛ-1, не репродуцировался в культурах клеток эмбрионов кошек и морских свинок, почки кролика и теленка, не выявлялся в лейкоцитах крови лошадей и не вызывал аборты у жеребых кобыл после интраназального введения. Кроме того, наблюдали различия в степени нейтрализации ГВЛ-1 и ГВЛ-4 гетерологичными антисыворотками. Установлено наличие не более 20% гомологии ДНК и различия восьми структурных белков ГВЛ-1 и ГВЛ-4.
Штамм ВС аттенуирован в течение 53-56 пассажей в первичной культуре клеток тестикулярной ткани поросят. Вакцинация беременных лошадей аттенуированным штаммом СВ/69 сопровождалась умеренно выраженной реакцией и не влияла на плодоношение. Способ введения вакцины из штамма СВ/69 существенно не влияет на титр гуморальных антител, тогда как титр секреторных антител был выше при интраназальном применении.
Аттенуированный штамм ГВЛ-4 получен путем размножения в первичной культуре клеток почки поросенка в присутствии мутагена (5-йод-2-дезоксиуридин). Живая вакцина создавала напряженный иммунитет, сохранявшийся на протяжении года. Мутант ГВЛ-4 был нереверсибельным. Случаев абортов, заболевания или вирусоносительства у привитых животных не наблюдали.
Лиофилизированная вакцина сохраняла биологические свойства при 4°С в течение двух лет. После контрольного заражения у ранее вакцинированных животных отмечено значительное возрастание титра антител. У вакцинированных особей вирулентный вирус в смывах носоглотки обнаруживали в течение одного дня, а у контрольных — три дня после заражения.
Результаты испытаний инактивированных вакцин показали, что по сравнению с живыми вакцинами они менее иммуногенны. Иммуногенные препараты получены с глютаральдегидом в качестве инактиватора и адъювантом СТС. Вакцина обладала защитным эффектом для новорожденных жеребят, особенно если матерей реиммунизировали на 6—7-м мес. беременности. Применение инактивированных вакцин оказалось менее эффективным даже после двух-трех-кратного введения. Так было, например, с вакциной Pneumabort-K из ГВЛ-1. Вакцинация снижала тяжесть заболевания, продолжительность выделения и титр выделяемого вируса (в 10-100 раз), но не создавала защиты от заражения ГВЛ-1. Подобные результаты получены в другом исследовании с аналогичной вакциной.
Двукратно привитые жеребята были чувствительными к заражению: температурная реакция и продолжительность экскреции вируса не отличались от наблюдаемых в группе контрольных животных, хотя количество экскретируемого вируса было значительно снижено.
Таким образом, клинически выраженное заболевание лошадей, характеризующееся признаками ринопневмонии и сопровождающееся абортами, вызывается двумя тесно связанными вирусами: герпесвирусами лошадей 1 и 4. Естественный иммунитет при этих заболеваниях кратковременный. Вероятно, он связан в основном с антителами. Имеются инактивированная (цельновирионная или субъединичная) и живая вакцины. Живая вакцина из ГВЛ типа 1, аттенуированного в гетерологичной культуре клеток, применялась в ряде стран. Ее применение предупреждает развитие патологии органов дыхания и аборты.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Герпес: причины появления, симптомы, диагностика и способы лечения.
Определение
Герпесом, или герпетической инфекцией, называют несколько заболеваний, вызываемых вирусами отряда Herpesvirales семейства Herpesviridae.
Все они характеризуются поражением кожи, слизистых оболочек с локализацией либо в области глаз, носа и губ, гениталий, а также нервных волокон.
У лиц с иммунодефицитом могут наблюдаться генерализованные формы инфекции с вовлечением в процесс других органов и тканей.

Среди известных науке восьми типов герпеса самым распространенным является вирус герпеса простого типа (Herpes simplex virus).
Простой вирус герпеса достаточно неустойчив во внешней среде. В условиях комнатной температуры сохраняется до 24 часов, на металле — до 2 часов. Под действием температуры выше 50°C погибает за 30 минут, под действием спирта и хлорсодержащих веществ - в течение нескольких минут, при замораживании сохраняется до пяти суток.
Причины герпетической инфекции
Источником инфицирования всегда служит человек. Он заразен в любую фазу болезни или носительства, но преимущественно при обострении.
Возбудитель может передаваться воздушно-капельным, контактно-бытовым или половым путем, а также от матери плоду через плаценту, во время родов или грудного вскармливания.
К вирусу восприимчивы все люди, хотя у многих отмечаются бессимптомные формы заболевания. Попадая через слизистую рта, половых органов или дыхательные пути в организм человека, герпесная инфекция остается в нем навсегда. Вирус, скрытый внутри клетки-хозяина, не доступен для иммунных клеток, уничтожающих возбудителей. Вирус активизируется при ослаблении иммунитета в результате переохлаждения, перегрева, простудного заболевания, недостатка витаминов, переутомления, стресса, нехватки сна. Рецидив инфекции могут вызвать травмы, оперативные вмешательства, а также половой контакт при условии повреждения слизистой оболочки. Использование лекарственных и косметических средств, содержащих стероидные гормоны, также способствует манифестации вируса герпеса.
Классификация герпеса
В МКБ-10 (Международной классификации болезней) выделяют две группы заболеваний, связанных с вирусом простого герпеса:
- Инфекционные герпетические заболевания:
- герпетическая экзема (экзема Капоши);
- герпетический везикулярный дерматит;
- герпетический гингивостоматит и фаринготонзиллит;
- герпетический менингит;
- герпетический энцефалит;
- офтальмогерпес;
- диссеминированная герпетическая болезнь (герпетический сепсис);
- другие формы герпетических инфекций;
- неуточненная герпетическая инфекция.
- Генитальные герпетические инфекции:
- герпетические инфекции перианальных кожных покровов и прямой кишки;
- неуточненная аногенитальная герпетическая инфекция.
По клинической картине и локализации высыпаний:
- Типичные формы:
- герпес кожи — с поражением губ, крыльев носа, лица, рук, ягодиц и других частей тела;
- герпес глаз — иридоциклит, кератит, конъюнктивит, неврит зрительного нерва;
- герпес слизистых оболочек желудочно-кишечного тракта — стоматит, гингивит, фарингит, эзофагит;
- герпес половых органов — поражение слизистой оболочки полового члена, влагалища, вульвы, цервикального канала;
- герпес внутренних органов — гепатит, пневмония, панкреатит, трахеобронхит;
- герпес нервной системы — неврит, менингит, менингоэнцефалит, поражения бульбарных нервов, энцефалит;
- генерализованный простой герпес — висцеральная форма (пневмония, гепатит, эзофагит) и диссеминированная форма (сепсис).
- Атипичные формы:
- герпетиформная экзема Капоши — обширные сливающиеся высыпания по всему телу;
- абортивный герпес — почти незаметные папулы на грубой коже или дискомфорт без высыпаний;
- язвенно-некротический герпес — с развитием некроза тканей;
- эрозивно-язвенный герпес — с образованием язв и эрозий;
- геморрагический герпес — с кровянистым пропитыванием высыпаний и тканей;
- отечный герпес — с отеком тканей и болью в области губ и век;
- зостериформный простой герпес — с локализацией по ходу нервного ствола;
- диссеминированный герпес — с тенденцией перехода в генерализованную форму при ВИЧ;
- рупиоидный герпес — возникает на лице с присоединением вторичной бактериальной флоры;
- мигрирующий герпес — с тенденцией к изменению локализации высыпаний.
- латентная стадия — носительство с отсутствием симптомов;
- локализованная стадия — наличие одного очага поражения;
- распространенная стадия — наличие не менее двух очагов поражения;
- генерализованная стадия — висцеральная, диссеминированная.
При заражении герпесом детей в возрасте от 6 месяцев до 3 лет чаще всего развивается герпетический стоматит, для которого характерно острое начало с симптомами интоксикации и подъемом температуры.
На слизистой оболочке полости рта появляются сгруппированные пузырьки с прозрачным содержимым, на месте которых после вскрытия образуются болезненные эрозии. У детей старшего возраста первичный герпес характеризуется появлением зудящих пузырьков на красной кайме губ и коже носогубного треугольника. После их вскрытия остаются неглубокие язвочки, которые покрываются корочками. Корочки, отпадая, не оставляют следов на коже.
При первичном заражении взрослых вирусом простого герпеса симптомы более выражены, чем при дальнейших рецидивах. Больной испытывает озноб, головные боли, повышенную утомляемость, у него отсутствует аппетит, может наблюдаться расстройство сна. Покраснение, а затем характерные пузырьки появляются на губах, возле крыльев носа. В некоторых случаях увеличиваются подчелюстные лимфоузлы.
Герпетические нейроинфекции сопровождаются наиболее тяжелым течением, особенно если вирус поражает оболочки или ткань головного мозга.
В этих случаях симптомы включают головные боли, подъем температуры тела, напряжение затылочных мышц, психомоторное возбуждение (болезненное состояние, при котором наблюдается беспокойство и двигательная активность различной степени выраженности, вплоть до судорог). При несвоевременной диагностике заболевания существует риск летального исхода.
Офтальмогерпес сопровождается покраснением глаза, развитием блефаро- или кератоконъюнктивита, эрозиями роговицы.
Диагностика герпеса
Типичные случаи герпетической инфекции выявляются на основании клинической картины и анамнеза заболевания. Характерно его волнообразное течение со сменой периодов обострения и ремиссии.
Косвенным признаком служит склонность к простудным заболеваниям, чувствительность к переохлаждению, периодически возникающие состояния, сопровождаемые подъемом температуры, усталостью, депрессией.

При атипичных формах герпетической инфекции необходимы дополнительные обследования: клинический анализ крови, биохимический анализ крови (общий белок, белковые фракции, С-реактивный белок, АЛТ, АСТ, ЛДГ, креатинин, электролиты: калий, натрий, хлор, кальций) и клинический анализ мочи - для выявления поражения внутренних органов и предупреждения осложнений.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

