Вирус от пчелы человеку
Обновлено: 17.04.2024
Первопроходцем в диагностике вирусных болезней пчел в Беларуси стал Институт экспериментальной ветеринарии им. С.Н. Вышелесского (г. Минск), специалисты которого столкнулись с проблемой — нежеланием пчеловодов предоставлять больных насекомых, необходимых для настройки приборов. Такие исследования успешно проводятся в странах Европейского союза в рамках программ по выяснению причин коллапса пчелиных семей. Диагностикой некоторых вирусных инфекций пчел занимаются и в Российской Федерации.
Вирусы вызываются внутриклеточными паразитами, которые могут размножаться только в живых клетках хозяина, разрушая их. Вирусы проникают в организм насекомого через органы пищеварения, поступая с кормом, или через травмированные участки поверхности тела. Распространенный путь заражения пчел — попадание вирусов в гемолимфу при укусах клещей варроа или других паразитов. При этом происходит самое быстрое размножение вирусов до смертельных для пчелы пределов. Переполненные насекомыми ульи и высокий уровень контактов между членами пчелиной семьи обеспечивают идеальную среду для передачи патогенов.
Для некоторых вирусов пчел доказано существование и вертикального пути передачи —к потомству от матки, когда она откладывает уже зараженные яйца.
Передача вирусов от инфицированных семей здоровым может произойти во время сбора нектара с цветков, при разворовывании слабых и больных семей.
Заражение вирусами медоносных пчел может происходить на разных этапах их развития, в том числе на стадии яйца, личинки, куколки, а также взрослых насекомых — рабочих пчел, трутней и маток.
Вирусы часто вызывают у пчел скрытые инфекции без явных признаков заболевания, однако при этом могут существенно повлиять на здоровье насекомых и сократить продолжительность их жизни.
Когда пчелы находятся в благоприятных условиях, вирусы могут сохраняться в их семьях и передаваться вертикально (от матки с яйцами), не нанося при этом ощутимого вреда насекомым. В стрессовых ситуациях, например при инвазии клещами варроа и ноземой, или при снижении обеспеченности семьи кормом может произойти горизонтальная передача вирусов (от пчел к пчелам) и усиленное их размножение. Подобные обстоятельства могут быть вызваны такими факторами окружающей среды, как низкая температура воздуха или неблагоприятная для лета пчел погода в течение длительного периода времени, когда они вынуждены подолгу находиться в улье.
Длительный безоблетный период может привести к испражнению пчел в улье. Фекальные загрязнения на сотах, являясь основным источником некоторых вирусов, могут стать причиной быстрого распространения заболевания в семье. Усиленное размножение вирусов повышает их заразность, что приводит к росту смертности среди насекомых, а в некоторых случаях и к краху всей пчелиной семьи.
При явном течении инфекции симптомы некоторых вирусных заболеваний пчел ярко выражены. Однако их отсутствие не исключает присутствие вируса, так как он может сохраняться в теле хозяина в латентной форме, образуя своеобразный резервуар инфекции.
Наиболее распространенные вирусы пчел
DWV — вирус деформации крыла
DWV — один из немногих вирусов, сопровождающихся четко выраженными симптомами заболевания у инфицированных пчел. Типичные признаки болезни: усохшие, смятые крылья, уменьшение размеров тела и изменение его цвета у взрослых пчел. Механизм, из-за которого DWV вызывает морфологические уродства у зараженных насекомых, неясен. Взрослые пчелы, инфицированные DWV, обычно выглядят нормально, но имеют меньшую продолжительность жизни. Доказано, что у DWV-инфицированных пчел нарушается способность к обучению. Самый главный источник распространения этого вируса — клещи варроа. Исследования по наличию вируса в клещах варроа показали, что он присутствует почти у 100% проверенных клещей.

Рис. 1. Молодые пчелы, пораженные вирусом деформации крыла.
SBV — вирус мешотчатого расплода
SBV может заражать расплод и взрослых пчел, однако наиболее восприимчивы к нему личинки. SBV влияет на взрослых особей, не вызывая явных признаков болезни, но частенько сокращая продолжительность их жизни. Первоначальное распространение SBV в семьях происходит при удалении пчелами-кормилицами погибших от вируса личинок. Вирусные частицы, накапливаясь в гипофарингеальных железах пчел-кормилиц, выделяются с маточным молочком. Таким образом, инфицированные пчелы начинают распространять вирус в семье при кормлении личинок и обмениваясь пищей с другими взрослыми пчелами. Зараженные летные пчелы распространяют вирус путем передачи его с секретом слюнных желез при формировании пыльцевой обножки во время сбора пыльцы.
Инфицированные взрослые пчелы быстро перестают потреблять в пищу пыльцу и вскоре прекращают вскармливание личинок, переходят на сбор нектара. Нектар, содержащий вирус, разбавляется в семье с нектаром от других сборщиц. Пыльца (перга) от больных пчел — более значимый источник вируса, чем мед, поэтому необходимо быть крайне осторожным при подстановке рамок с пергой от других семей.
Молодые личинки заражаются вирусом при потреблении зараженной им пищи. Между телом больной личинки и ее кожицей от предыдущей линьки накапливается большое количество жидкости, содержащей миллионы частиц SBV (рис. 2). Вирусных частиц из одной личинки, погибшей от мешотчатого расплода, достаточно, чтобы заразить весь расплод в тысяче пчелиных семей.
В пораженных семьях при остром течении болезни появляются личинки, подобные водянистым мешкам, которые легко удалять из ячеек. Больные личинки лежат в ячейке спинкой вниз, головой к крышечке, при этом голова обычно приподнята вверх (вид китайского башмачка) (рис. 4). Цвет личиночной жидкости постепенно меняется от жемчужно-белого до бледно-желтого, начиная с головы. После того как личинка умирает, она становится темно-коричневого цвета с черной головой (рис. 3).


Рис. 2. Классические симптомы мешотчатого расплода: личинка в кожистом мешке, заполненном жидкостью.
Рис. 3. Погибшая усыхающая личинка при мешотчатом расплоде: потемнение со стороны головы.
Установлено, что распространенность SBV в семьях медоносных пчел варьирует по сезонам года. В весенне-летний период богатые источники нектара и пыльцы стимулируют выращивание расплода, появляется большое количество молодых пчел-кормилиц, что создает благоприятные условия для заражения пчел вирусом и его распространения в семьях. Вспышки болезни обычно отмечаются в это время при длительном отсутствии взятка. Болезнь часто остается незамеченной, так как при слабом поражении пчелы успевают распознавать и удалять из запечатанных ячеек больных личинок. При этом может отмечаться лишь пестрота расплода, в некоторых случаях удается найти вскрытые ячейки с еще не удаленными личинками (рис. 4).

Рис. 4. Стрелками отмечены вскрытые пчелами запечатанные ячейки с личиками, больными мешотчатым расплодом. В центре — пчела, пораженная вирусом деформации крыла.
Так же как DWV, SBV может переноситься клещами варроа. Российские ученые доказали вертикальный путь передачи SBV (маткой), а также то, что передача вируса к здоровым семьям происходит при установке сотов, взятых от больных семей.
По данным российских исследователей, при вялотекущем мешотчатом расплоде симптомы болезни могут отличаться от классических. Больные личинки могут длительное время оставаться живыми, при этом у них частично продолжается метаморфоз. Характерным признаком болезни в такой форме может быть появление у личинок пигментированных глаз при отсутствии конечностей.
Важное доказательство наличия мешотчатого расплода — полное отсутствие бактерий в больных личинках, подтверждаемое при микробиологических исследованиях в случае подозрения на гнильцы.
BQCV — вирус черного маточника
BQCV впервые был выделен от мертвых личинок и предкуколок маток, запечатанных в маточники с измененным цветом — от темно-коричневого до черного. BQCV поражает в основном развивающихся личинок и куколок маток после запечатки маточника. По распространенности уступает только DWV. Существует связь вспышек заболевания BQCV с заболеванием семей нозематозом, что доказано при проведении полевых наблюдений. Механизм такой зависимости до сих пор не изучен.
KBV — кашмир-вирус пчел
KBV был обнаружен впервые у медоносных пчел в Австралии в 1979 году. Поражает пчел на всех этапах жизненного цикла. Инфекция обычно протекает в скрытой форме. Болезнь и гибель от KBV происходит на разных стадиях развития пчел без четко определенных симптомов. Среди всех вирусов, поражающих медоносных пчел, KBV, как и почти неотличимый от него израильский вирус острого паралича (IAPV), считается самым опасным, поскольку очень быстро размножается. Попадание нескольких вирусных частиц в гемолимфу пчел может привести к гибели насекомого в течение трех дней. KBV по генетическим признакам близок к вирусу острого паралича пчел. Заражение медоносных пчел KBV напоминает инфекцию, вызванную вирусом острого паралича и, как правило, сохраняется в семьях медоносных пчел в латентной форме. Этот вирус также переносится клещами варроа, которые могут также активизировать скрытые инфекции вплоть до летального уровня.
ABPV — вирус острого паралича пчел
Распространение ABPV в пчелосемьях, вероятно, происходит с помощью секрета слюнной железы зараженных взрослых насекомых, когда он попадает с кормом молодым личинкам или в пыльцевую обножку. Зараженные личинки либо умирают до запечатывания в ячейке, если внутри них скопилось большое количество вирусных частиц, либо выживают, чтобы появиться на свет инфицированными взрослыми пчелами без признаков болезни.
CBPV — вирус хронического паралича пчел
Симптомы заболевания наблюдаются у взрослых пчел, при этом известно два типа течения болезни.
Тип 1. Симптомы: дрожащие движения крыльев и органов взрослых пчел, отсутствие у насекомых способности к полету. Пчелы ползают по земле, по стеблям растений, часто собираются вместе, могут также иметь вздутое брюшко, признаки дизентерии. Умирают в течение нескольких дней после появления симптомов.

Рис. 5. Пчелы, погибшие от вируса хронического паралича (тип 2). Борисовский район, 2014 год.
Оба типа болезни могут иметь место в пределах одной семьи. Сильно пораженные семьи (в основном это самые сильные на пасеке) быстро теряют летную пчелу, в результате чего приходят в полный упадок, при этом в гнезде часто остается всего несколько взрослых пчел с маткой.
Указанные симптомы, однако, сходны с таковыми при других болезнях (акарапидоз, отравления, другие вирусы), и по ним можно поставить ошибочный диагноз.
Передача вирусов в основном происходит при непосредственном телесном контакте пчел, хотя существует, но менее опасна, и передача при обмене кормом. Прямая передача вируса хронического паралича контактным путем происходит при переполненном пчелами улье, когда они задерживаются в гнезде в течение длительного периода времени (из-за плохой погоды или во время перевозки на дальние расстояния) или когда слишком много семей размещено на одном точке при монокультурных медоносах. В обоих случаях вирус распространяется через небольшие порезы на кутикуле взрослых пчел, полученные от надломанных волосков других пчел, либо при прямом контакте с инфицированными взрослыми пчелами через открытые поры. Если перезаражение происходит быстро, вспышка болезни приводит к высокой смертности в семье.
Фекалии инфицированных пчел в пределах семьи также могут быть заразными. Распространение вируса и вспышка болезни могут произойти в любое время года. Весной и летом признаки болезни и гибель пчел отмечаются чаще, но следует учитывать, что вирус может сохраняться в семьях круглый год, никак себя проявляя.
Противовирусная защита
Факт, когда вирусы сохраняются в практически здоровых семьях в латентной форме, говорит о том, что медоносные пчелы имеют врожденную способность противостоять им. Одним из важнейших механизмов защиты медоносных пчел от вирусов является выработка ими универсального противовирусного вещества интерферона.
Противовирусных лекарственных препаратов, напрямую уничтожающих вирусов в организме пчел, практически не существует. Именно поэтому так важно для каждого пчеловода соблюдать ветеринарно-санитарные правила содержания пчел: поддерживать пасеку в должном санитарном состоянии, создавать условия, при которых формируется хороший уровень защитных сил у пчел, принимать меры по предупреждению распространения и локализации болезней.
Виталий ГРАБЛЮК,
главный ветврач-паразитолог Белорусского государственного ветеринарного центра
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 35 лет.
Над статьей доктора Борисова Э. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
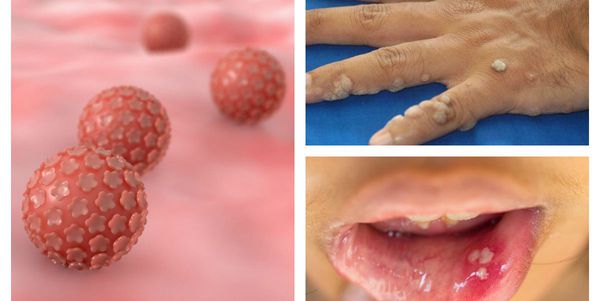
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
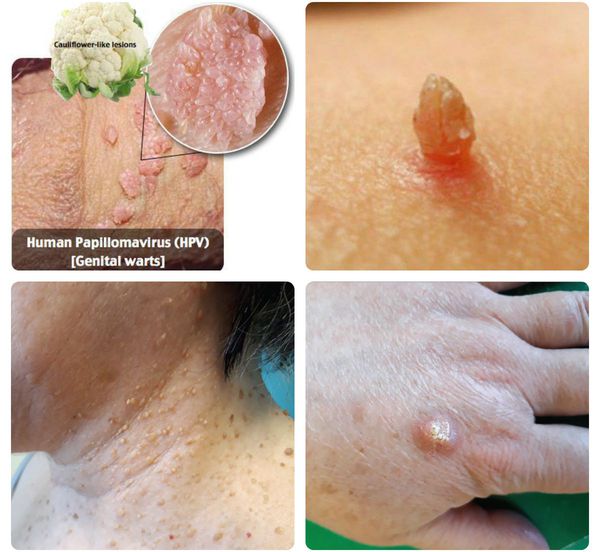
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
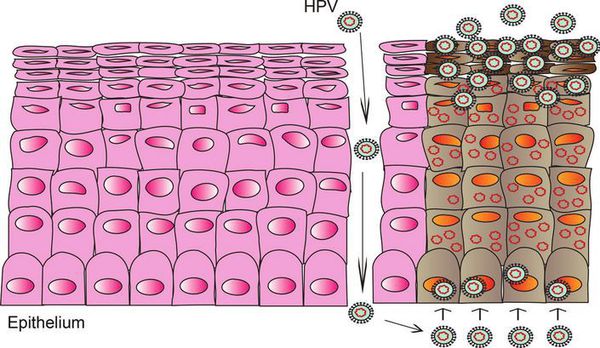
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
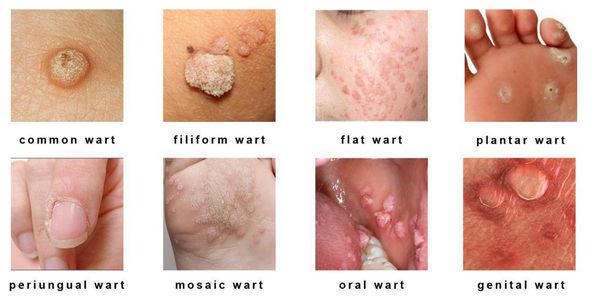
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
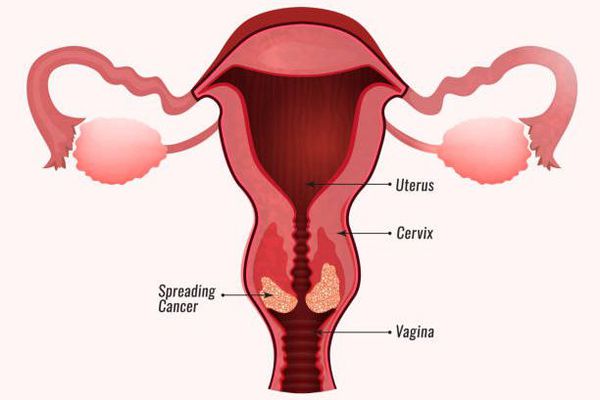
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
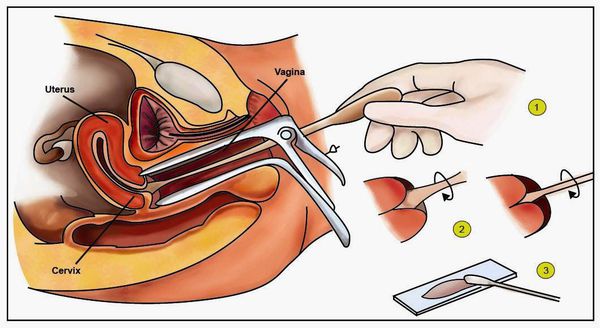
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
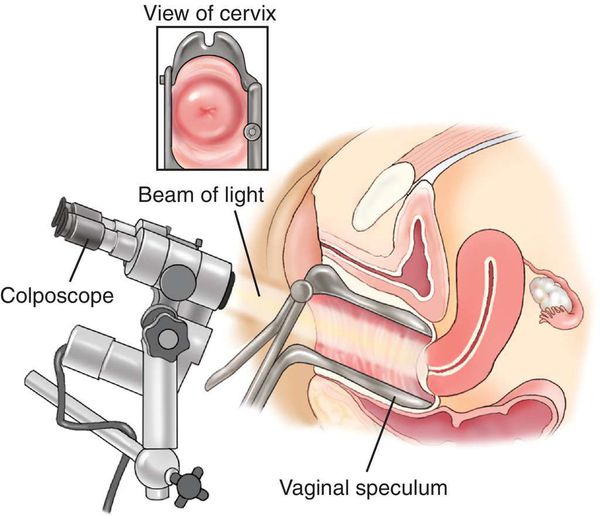
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
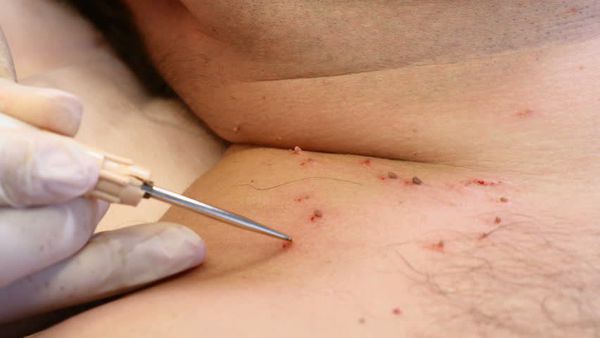
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
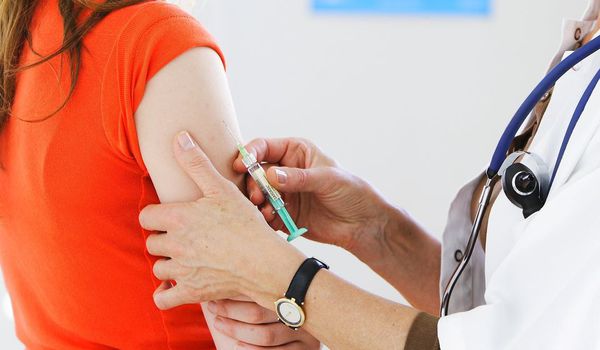
Пчелиный яд является очень сильным аллергеном. В его состав входят ферменты и биологически активные вещества, в том числе гистамин, который может усиливать проявления аллергической реакции. Контакт с данным аллергеном происходит при ужаливании человека пчелой или при использовании пчелиного яда как лекарственного средства. Появлениями аллергии могут быть как местные реакции в виде аллергического дерматита, так и общие: крапивница, отек Квинке, анафилактический шок. Определение специфического иммуноглобулина Е к данному аллергену в повышенном количестве указывает на наличие сенсибилизации организма к нему.
Синонимы русские
Специфические иммуноглобулины класса Е к апитоксину (яду пчелы медоносной).
Синонимы английские
Allergen i1, Venom, Honeybee, IgE.
Метод исследования
Единицы измерения
МЕ/мл (международная единица на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Пчелы – высокоорганизованные насекомые отряда перепончатокрылых. Медоносные пчелы распространены по всем континентам. Они являются основными естественными опылителями растений.
Лечение ядом пчелы – апитоксинотерапия применяется в медицине при заболеваниях опорно-двигательного аппарата и нервной системы, аутоиммунных болезнях. Однако укусы пчел, как и других перепончатокрылых, могут представлять угрозу здоровью и жизни людей с системными реакциями на их яд. По статистике, системные анафилактические реакции на яд перепончатокрылых могут возникнуть у 0,15-5% населения. Наибольшему риску подвергаются пасечники. Анафилактический шок с летальным исходом у сенсибилизированных лиц возможен даже после одного укуса.
Пчелы являются единственными насекомыми, которые погибают после ужаливания, оставляя жало в коже. Известно, что 90% объема яда поступает в первые 20 секунд после укуса. В месте укуса пчелы появляется боль, покраснение и отек. Реакция может быть локальной, региональной или генерализованной с системной анафилактической реакцией. Замедленные типы гиперчувствительности после укуса редки, но возможны. Анафилактические реакции на укусы перепончатокрылых не зависят от дозы яда или количества укусов. Известны случаи развития тяжелых системных анафилактических реакций после 1-2 укусов насекомых. Однако сильнейшая интоксикация, вызванная поступлением большого количества яда в организм, может быть смертельной и для человека без сенсибилизации. При попадании массивных доз яда в организм поражаются внутренние органы человека, особенно почки. При прогрессировании симптомов и развитии анафилаксии требуется срочная госпитализация.
Яд пчелы относится к наиболее изученным ядам. Основными аллергенами в нем являются фосфолипаза А2, гиалуронидаза, кислая фосфатаза и меллитин. Яд пчелы содержит также биогенные амины, например гистамин, полипептиды и ферменты, выделение которых может привлекать и других пчел к атаке. Отмечается значительная перекрестная реактивность между антигенами яда пчел и шершней. Есть некоторые данные о возможности аллергических реакций на различные продукты пчеловодства, например маточковое молочко, прополис, при наличии сенсибилизации к пчелиному яду.
Сенсибилизация к аллергенам яда пчелы подтверждается определением высокого титра специфических IgE в сыворотке крови. По результатам исследования может проводиться отбор пациентов для специфической иммунотерапии ядом насекомых.
Ложь: Пчелиный яд сам по себе имеет антиретровирусный эффект.
Правда: Компонент яда медоносной пчелы, мелиттин (пептид из 26 аминокислот, обладающий свойствами поверхностно-активного вещества), показал активность против штаммов ВИЧ в лабораторных условиях.

"А вы знали? Учёные выяснили, что пчелиный яд убивает вирусы, не причиняя вред орагнизму"
Как это работает?
В 2013 году в журнале Antiviral Therapy была опубликована статья о том, что компонент яда медоносной пчелы активен против вируса иммунодефицита человека. Целью исследования стала проверка противовирусной эффективности геля, содержащего мелиттин. Предполагалось, что его можно использовать как профилактику ВИЧ, нанося на гениталии до полового контакта.
Мелиттин имеет цитолитическое свойство, то есть способен разрушать клетки и увеличивать их проницаемость. Проблема в том, что мелиттин оказывает эффект не только на инфицированные клетки, но и на здоровые:
"Пчелиный яд содержит мощный токсин под названием мелиттин, который может создавать отверстия в защитной оболочке, окружающей ВИЧ и другие вирусы. Большое количество свободного мелиттина может причинить клеткам вред".

"Пчелиный яд убивает ВИЧ"
В рамках исследования учёные смогли присоединять мелиттин к сложным наночастицам. Это соединение воздействовало ВИЧ, не вступая в контакт с неинфицированными клетками:
"Новое исследование показывает, что мелиттин, соединённый с наночастицами, не наносит вреда здоровым клеткам, поскольку [исследователи] добавили защитные бамперы на поверхности наночастиц. Когда они контактируют с неинфицированными клетками, которые значительно больше по размеру, частицы просто отскакивают. ВИЧ меньше наночастицы, он лавирует между защитными бамперами и вступает в контакт с поверхностью наночастиц, где находится мелиттин".
Результаты опыта были многообещающими. Мелиттин, не привязаный к модифицированным наночастицам, подавлял способность ВИЧ инфицировать клетки. Также было доказано, что он не токсичен для клеток влагалища:
"Мелиттин вместе с наночастицами был инертен по отношению к клеткам эпителия влагалища".
Более поздние исследования показали, что гель не токсичен и для спермы. По мнению авторов, масштабная разработка лекарственного геля может помочь дискордантным парам, в которых один из партнёров ВИЧ-положительный.
Стоит отметить, что хоть мелиттин и является компонентом пчелиного яда, сам по себе он не является средством против ВИЧ. Учёные даже не использовали мелиттин от настоящих пчёл, а заменили его синтетическим вариантом.
Компоненты пчелиного яда используются и в других средствах для профилактики ВИЧ. В частности, в начале 2017 года пройдёт вторая фаза клинических испытаний новой вакцины против вируса. Её основа – ВИЧ-1, модифицированный с использованием генетического материала медоносных пчёл.
Читайте также:

