Вирус папилломы человека и рассеянный склероз
Обновлено: 23.04.2024
Точнее, так: говорить о легких и проходящих осложнениях прививок, разумеется, можно. На разных сайтах, информирующих о Гардасиле и Цервариксе, обычно приводится примерно такой список негативных эффектов: боль и припухлость в месте инъекции, зуд, кровотечение, головная боль, лихорадка, тошнота, головокружение, обморок.
Однако упоминание осложнений, значительно снижающих качество жизни или влекущих смерть, вызывает во врачебной среде бурную негативную реакцию.
Более того, сравнительно недавнее исследование британских ученых свидетельствует о том, что чем больше официальная медицина борется с условным антивакцинизмом, тем менее люди доверяют ей. (Подробно об этом здесь).
Это кажется удивительным только на первый взгляд, ведь когда какая-то тема под запретом, на этом месте образуется темная зона, в которой, как известно, рождаются чудовища.
К ним относится, например, утверждение о том, что создатели вакцины от ВПЧ замыслили с ее помощью ограничить фертильность девушек стран третьего мира и, снизив численность населения в странах Азии, Африки и Латинской Америки, захватить их природные ресурсы.
Однако та озабоченность, которую высказывает ряд экспертов по поводу безопасности Гардасила и Церварикса, не имеет ничего общего с бредовыми теориями.
Рассеянный склероз – после или вследствие?
Совсем недавно, в мае 2018 года, мета-анализ клинических испытаний вакцин от ВПЧ опубликовала Кокрановская группа экспертов.
Исследователи установили, что риск серьезных осложнений был примерно одинаков в группах вакцинированных и плацебо-группах, хотя количество смертей было выше среди вакцинированных, особенно в возрастной группе после 25 лет. В целом же отклонение в рамках статистической погрешности: 11:10 000 у невакцинированных, 14:10 000 у вакцинированных.
И тем не менее, ряд экспертов настаивает на том, что успокаиваться по поводу безопасности не следует, необходимо фиксировать все случаи серьезного нездоровья, связанного по времени с вакцинацией Гардасилом и Цервариксом, и анализировать их.
Сравнительно недавно, в феврале 2018 года на форуме ACTRIMS (Американского комитета по лечению рассеянного склероза и научным исследованиям в это области) в Сан-Диего (США) исследователь Е Ху из Университета Майами доложил о двух случаях рассеянного склероза у подростков после прививки Гардасилом.
У 14-летнего юноши и 17-летней девушки развились сходные симптомы в течение двух недель после вакцинации (у юноши – после третьей дозы, у девушки – после первой).
Оба страдали от нечеткого зрения, девушка испытывала также перемежающуюся немоту и слабость в ногах. На ее МРТ были обнаружены поражения во фронтальной и затылочно-теменной зонах мозга.
У обоих подростков на МРТ присутствовали повреждения белого вещества мозга, а в цереброспинальной жидкости исследователи обнаружили олигоклонические полосы (диагностический признак рассеянного склероза).
Исследователи предполагают, что Гардасил может повышать риск начала демиелинизации нервного волокна у индивидов, предрасположенных к рассеянному склерозу, либо выступать триггером РС через активацию иммунного ответа организма.
Ряд экспертов считает, что адъювант алюминий, добавляемый в вакцины для усиления иммунного ответа, у некоторых особенно чувствительных индивидов может вызвать чрезмерную активацию, приводящую к запуску аутоиммунных процессов.
Международная группа ученых под руководством Шонфилда проанализировала 300 случаев развития синдрома, 48 из которых ассоциированы с вакцинами от папилломавируса.
При этом 89% пациентов (от общего числа) получили определенные клинические диагнозы, наиболее частым из которых были: недифференцированное заболевание соединительной ткани, фибромиалгия и/или синдром хронической усталости, системная эритематозная волчанка, неврологические аутовоспалительные заболевания.
Значит ли это, что РС у обоих подростков непременно является результатом вакцинации? Нет, такое заключение сделать нельзя, как нельзя и исключить, что заболевание является тяжелым осложнением.
Ненастоящее плацебо
В обзоре клинических испытаний и постмаркетинговых исследований вакцин Гардасил, Гардасил 9 и Церварикс мексиканские ученые Мануэль Мартинез-Лавин и Луис Амезкуа-Гуэрра отмечают ряд тревожных фактов, и один из них связан с алюминиевым адъювантом, причем самым неожиданным образом.
Дело в том, что в подавляющем большинстве клинических испытаний вакцин от ВПЧ, предшествовавших лицензированию препаратов, в качестве плацебо контрольная группа участников исследований получала… соли алюминия или другие вакцины, содержащие алюминевый адъювант.
Даже при том, что не все эксперты признают существование синдрома ASIA, никто не спорит с тем фактом, что алюминиевый адъювант – активное вещество, усиливающее иммунный ответ организма. Собственно, именно поэтому его и добавляют в вакцины.
Получается, что в большинстве исследований группа плацебо была не группой отсутствия вмешательства, а своего рода группой частичного вмешательства, а значит, сравнение количества серьезных побочных эффектов в двух группах не является вполне корректной процедурой оценки безопасности вакцины.
Постмаркетинговые исследования: симптомы и кластеры
Еще одним тревожным фактом Мартинез-Лавин и Амезкуа-Гуэрра называют результаты некоторых постмаркетинговых исследований.
Они разнятся между собой.
Два скандинавских исследования 2013 и 2017 года не находят связи между вакцинацией от ВПЧ и развитием неврологических заболеваний у вакцинированных девушек.
В испанском же исследовании 2014 года зафиксирован уровень побочных реакций 1:1000, что в 10 раз выше, чем количество осложнений от любой другой вакцины, получаемой девочками того же возраста.
Случаи обмороков составили 17:100 000, судорог – 3,2:100 000, в то время как для других вакцин эти показатели составили соответственно 6,4 и 0,4.
Довольно высокий уровень осложнений после вакцинации от папилломавируса был зафиксирован учеными в Словении. Он составил 149 случаев на 100 000 доз, случаи госпитализации составили 8:100 000, хотя, как указывают исследователи, серьезных последствий для здоровья пациенток они не имели.
Сочетание головной боли и головокружения с усталостью либо обмороком гораздо чаще встречалось после вакцинации от ВПЧ, чем после других прививок у пациенток от 9 до 25 лет.
Этот разрыв сохранился даже после того, как исследователи исключили все случаи, в которых девушкам были поставлены четкие диагнозы (комплексный регионарный болевой синдром и синдром постуральной ортостатической тахикардии). При этом от 44% до 89% случаев в данных кластерах были квалифицированы как серьезные осложнения.
Кейс-контрольные исследования – в чем их значение?
Авторы обзора приводят ряд кейс-контрольных исследований, то есть работ, в которых задокументированы конкретные случаи серьезных заболеваний, последовавших после вакцинации Гардасилом или Цервариксом. Это такие заболевания, как комплексный регионарный болевой синдром, синдром постуральной ортостатической тахикардии, ранняя недостаточность яичников, синдром хронической усталости, соматоформное расстройство, фибромиалгия, невропатия мелких волокон.
Некоторые из перечисленных заболеваний исчисляются десятками, другие – единицами, но в любом случае – даже если считать, что причиной всех этих заболеваний является прививка – их следует признать очень редкими осложнениями на фоне нескольких миллионов доз введенных вакцин.
Практически во всех описанных случаях, вопрос о причинно-следственной связи прививки и осложнения остается открытым: на данном этапе не хватает данных ни для того, чтобы однозначно подтвердить такую связь, ни для того, чтобы ее полностью опровергнуть.
Тем не менее, нельзя просто отмахнуться от этих случаев. Фиксируя их, ученые исследуют возможные патогенетические механизмы этих болезней, и накапливаемые данные со временем позволят дать определенный ответ на вопрос о том, являются ли они в действительности поствакцинальными осложнениями.
Существует гипотеза, что частицы вируса и/или алюминиевый адъювант у особенно чувствительных индивидов могут вызывать нейротоксический эффект и повреждать спинальные ганглии, провоцировать вегетативную недостаточность и невропатию мелких волокон. Эту гипотезу подтверждает то, что у нескольких пациентов с осложнениями обнаружены антитела к рецепторам вегетативной нервной системы (в двух американских исследованиях, этом и этом).
Кроме того, даже если эти осложнения грозят единицам, ими нельзя пренебрегать, и задача научного и медицинского сообщества – научиться выявлять тех, чью жизнь прививка может резко изменить к худшему.
Пока ученые спорят
Печальную особенность современных исследований эффективности и безопасности вакцинации отмечает группа бразильских ученых в своем обзоре научной литературы, посвященной вакцинам от ВПЧ. Она заключается в том, что практически все клинические испытания финансируются компаниями-производителями вакцин, и это может сказываться на интерпретации результатов.
Время от времени организации, продвигающие антивакцинную повестку, тоже финансируют некоторые исследования, хотя их материальные возможности гораздо скромнее.
Что же делать простому пациенту, чтобы не оказаться в рамках статистической погрешности?
Принимая решение о вакцинации, необходимо взвесить возможную пользу от нее и сопоставить ее с пользой скрининга.
Скрининг необходим всем, а вот нужна ли вам или вашему ребенку дополнительная защита в виде вакцины, во многом зависит от возраста и образа жизни пациента.
Да, вероятность осложнения прививки низка, но, как говорит доктор Диана Харпер, анализы на папилломавирус уж точно не способны ни убить, ни покалечить.
Источники:
Что такое рассеянный склероз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Новиков Ю. О., остеопата со стажем в 41 год.
Над статьей доктора Новиков Ю. О. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Рассеянный склероз (РС) является одним из частых хронических аутоиммунных заболеваний центральной нервной системы (ЦНС).
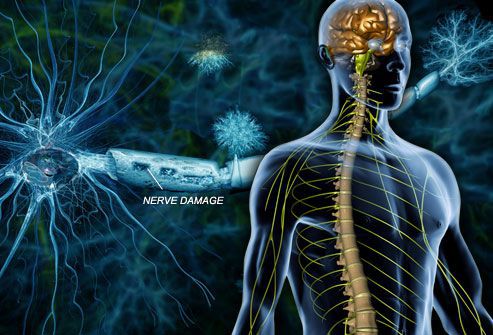
Распространенность РС высока и делится на зоны с высокой, умеренной и низкой встречаемости заболевания. Высокая распространённость отмечена в Северной Америке и Северо-Западной Европе.
В мире выявлено около 2 млн больных РС. В нашей стране в различных областях количество заболвших РС колеблется от 2 до 70 больных на 100 000 человек, причём значительно реже болезнь встречается в Средней Азии и Закавказье. В крупных промышленных районах и городах заболеваемость выше, чем в сельской местности, у лиц мужского и женского пола она одинакова.
- начало болезни в молодом возрасте, обычно между 20 и 35 годами (в отдельных случаях заболевают люди и более молодого, и более старшего возраста);
- многосимтомность;
- полиморфизм (многообразность) проявлений;
- прогрессирующее течение с весьма типичной наклонностью к ремиссиям и новым обострениям. [1][2]
Причина возникновения РС точно не установлена. Высказывалось мнение об инфекционной природе этого заболевания. Такое предположение основывается на случае острого развития заболевания с повышением температуры и свойственными инфекционным заболеваниям изменениям ликвора и крови, а также патоморфологических данных.
В настоящее время известно, что возбудителем РС может являться нейтропный фильтрующийся вирус, идентичный вирусу рассеянного энцефаломиелита. Исследователи из Гарвардской медицинской школы обнаружили, что риск рассеянного склероза увеличивается в 32 раза после заражения вирусом Эпштейна – Барр . Также учёные установили, что вероятность развития РАС не повышалась при инфицировании цитомегаловирусом и вирусом герпеса [17] .
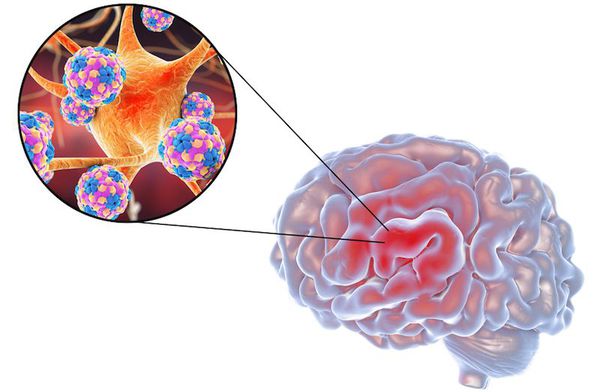
В основе демиелинизации (избирательного поражения головного мозга) лежит аутоиммунный процесс. Пути передачи инфекции не выяснены. Заражения непосредственно от больного не происходит. Возможность контактного пути распространения болезни следует считать маловероятным. [3] [4]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы рассеянного склероза
При всём многообразии и изменчивости расстройств, свойственных РС, можно выделить основную, наиболее частую, типичную его форму—цереброспинальную.
Обычно заболевание цереброспинальной формой РС начинается в молодом возрасте. Эта форма характеризуется:
- сочетанием пирамидных и мозжечковых расстройств;
- нередким поражением зрительных нервов;
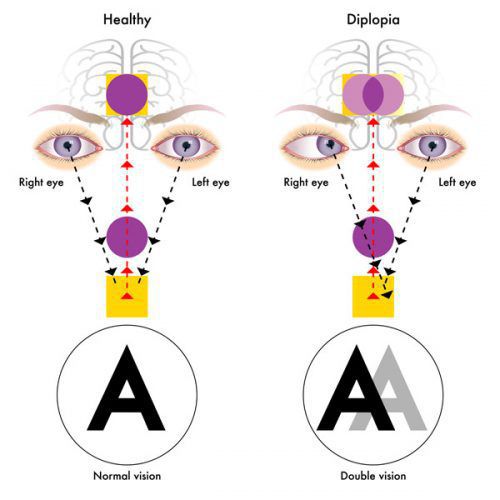
- иногда преходящей диплопией (раздвоение видимых объектов);
- ремиттирующим течением (повторные ремиссии).
Развитие пирамидных и мозжечковых расстройств обусловлено частым образованием очагов воспаления в боковых столбах спинного мозга, мозговом стволе и ножках мозжечка.
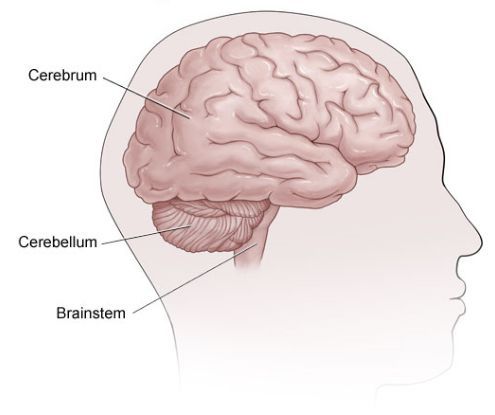
Наиболее ранними симптомами являются:
- утрата брюшных рефлексов;
- утомляемость и слабость ног;
- лёгкое интенционное дрожание в руках;
- нистагм (неконтролируемое ритмичное движение глаз).
Офтальмологические проявления
Нередко начальным изолированным расстройством является поражение зрения, развивающееся по типу так называемого ретробульбарного неврита (острое воспаление зрительного нерва). При этом возникает слепота или скотома (слепой участок в поле зрения) того или иного глаза.

Поскольку процесс локализуется не в соске зрительного нерва, а в его стволе (ретробульбарно), то на глазном дне в течение иногда довольно длительного срока изменений не обнаруживается.
При значительном поражении поперечника зрительного нерва утрачивается прямая реакция зрачка слепого глаза на свет при сохранённой реакции сужения его в случае освещения другого глаза (содружественная реакция зрачка).
Для ретробульбарного неврита при РС характерно выпадение центральных полей зрения (центральная скотома), так как бляшки развиваются обычно внутри ствола зрительного нерва. В отличие от этого при ретробульбарном неврите сифилитической этиологии или при воспалении придаточных полостей носа чаще наблюдается концентрическое сужение полей зрения, так как воспалительный процесс развивается с наружной поверхности зрительного нерва — с его оболочек.

Через известный срок при РС обнаруживаются изменения глазного дна — побледнение соска зрительного нерва (атрофия). Типичным для РС является преимущественное побледнение височных половин сосков зрительных нервов. Утрата зрения может быть полной или частичной, одно- или двусторонней. Через некоторое время обычно наступает улучшение, но процесс может и нарастать. Двусторонняя слепота отмечается редко.
Мозжечковые и пирамидные расстройства
Наиболее ранними мозжечковыми расстройствами является:
- интенционное дрожание в руках, обнаруживаемое при пальце-носовой пробе;
- расстройство почерка;
- нистагм глазных яблок при отведении в стороны.
Резко выраженный нистагм (иногда не только горизонтальный, но и вертикальный или ротаторный), зависящий от пораженпя мозжечка, расстройства речи (скандированная речь) и дрожание головы или туловища являются уже признаком далеко зашедшего процесса.
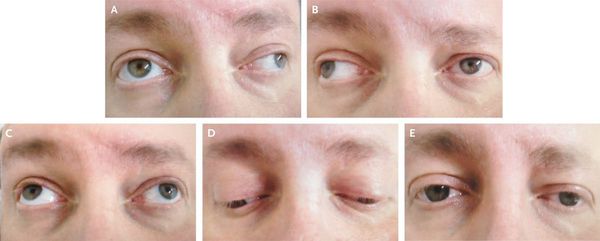
Развиваются и другие мозжечковые симптомы — адиадохокинез (невозможность быстрой смены противоположных движений — сгибания или вращения), шаткая походка и др.
Иногда, наряду с выраженными симптомами пирамидного поражения, отмечаются и симптомы поражения периферического двигательного неврона: утрата сухожильных рефлексов конечностей, атрофии мышц.
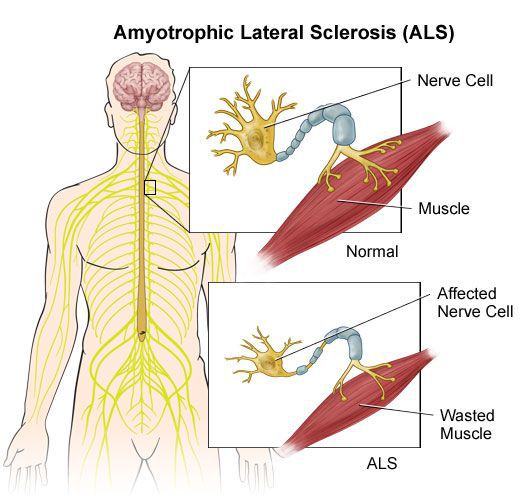
Нарушения чувствительности не столь выражены, как двигательные расстройства. Своеобразной парестезией (ощущение жжения, мурашек, покалывания) при РС является возникающее при резком сгибании головы к груди ощущение электрического тока, как бы пробегающего по позвоночнику вниз, с иррадиацией в ноги, иногда в руки. В некоторых случаях наблюдаются нарушения суставно-мышечного и вибрационного чувства в нижних конечностях. Значительно реже расстраивается поверхностная чувствительность.
Из черепномозговых нервов, кроме зрительных, чаще поражаются отводящий и глазодвигательный нервы. Паралич глазных мышц обычно имеет преходящий характер и выражается лишь диплопией, которая может быть начальным симптомом заболевания.
Нередки поражения тройничного, лицевого и подъязычного нервов. Развитие склеротических бляшек в надъядерных отделах кортико-нуклеарного пути может стать причиной возникновения псевдобульбарного синдрома, а в мозговом стволе — развития бульбарных симптомов (симптомы поражения черепных нервов).
Нарушения функций тазовых органов являются нередкими симптомами РС. Встречаются следующие нарушения:
- императивные (внезапные и неподавляемые) позывы, учащения, задержки мочи и стула;
- недержание, неполное опорожнение мочевого пузыря, приводящее к уросепсису — характерны для боле поздних стадий.
Нередки нарушения функции половой системы. Эти проблемы могут одновременно являться функциональными нарушениями тазовых органов, а также могут быть самостоятельными симптомами.
Психические нарушения редки. Деменция и выраженные формы психического расстройства свойственны лишь поздним периодам заболевания и обусловлены множественными и распространенными очагами в коре и подкорковых образованиях больших полушарий.
Патогенез рассеянного склероза
Для того, чтобы понять механизм развития РС, необходимо ознакомиться с патологической анатомией данного заболевания.
При микроскопическом исследовании обнаруживаются заметные и достаточно характерные изменения, выявляемые с наибольшим постоянством в спинном мозгу, мозговом стволе и полушариях головного мозга. Видны множественные бляшки различной величины (от точечных до весьма массивных, которые, к примеру, занимают весь поперечник спинного мозга), рассеянные преимущественно в белом веществе. Такая множественность и разбросанность очаговых изменений и определяет название болезни.
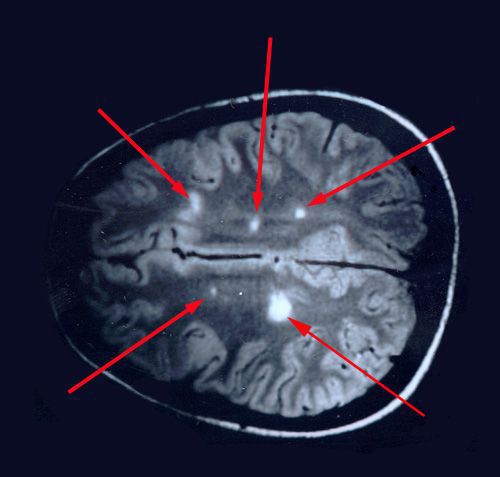
Отдельные бляшки имеют округлую форму, они нередко сливаются и создают изменения сложных очертаний. Цвет бляшек на разрезе розовато-серый (недавно образовавшиеся очаги) или серый, желтоватый (старые очаги).
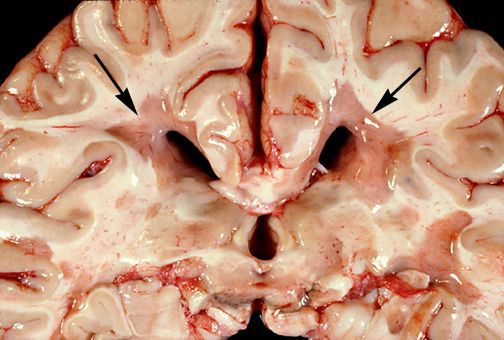
При разрезе бляшки определяется их большая плотность по сравлению с нормальной мозговой тканью. Эти уплотнения, склерозирование бляшек дало возможность охарактеризовать заболевание как склероз.
При микроскопии на первый план выступают изменения миелиновых волокон. В области очага, бляшки, в белом веществе наблюдаются в той или иной степени распад миелиновой оболочки, покрывающей нервные волокна центральных проводников, причём осевой цилиндр нередко остаётся неповреждённым.
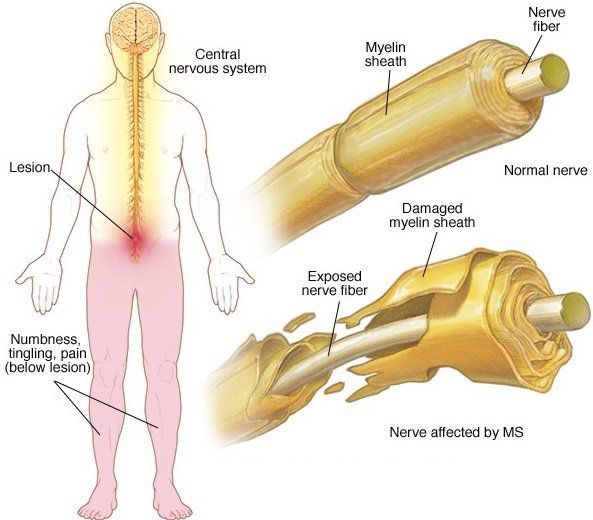
В остром периоде, при наличии отёка и инфильтрации, в очаге поражения нарушается проводимость по нервным волокнам. В дальнейшем, при условии гибели осевых цилиндров, возникают необратимые, стойкие выпадения.
После периода острого воспаления оказывается, что осевые цилиндры частично сохраняют свою целостность и проводимость, иногда даже наблюдается ремиелинизация нервных волокон. В результате наблюдается не только ремиссия, но даже и вполне удовлетворительное восстановление отдельных утраченных ранее функций, что очень характерно для РС.
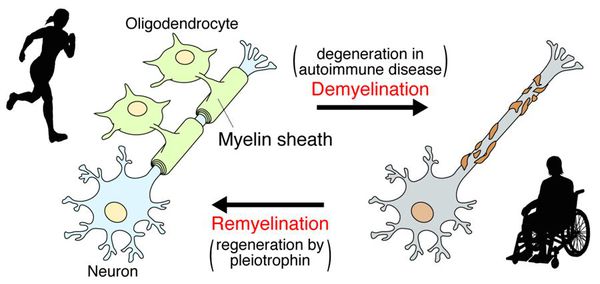
Образование новых воспалительных очагов определяет ухудшение и возникновение новых симптомов. [2] [5]
Классификация и стадии развития рассеянного склероза
Строгой и общепринятой классификации РС нет. Некоторые авторы предлагают подразделять РС по клиническому течению, другие по локализации процесса. [9]
По характеру течения выделяют:
- ремитирующую форму — характеризуется редкими обострениями, чередующимися с ремиссиями, иногда длящимися годами, причём поражённые участки мозга восстанавливаются как частично, так и полностью;
- первично прогрессирующую — незаметное начало и медленное, но необратимое нарастание симптоматики;
- вторично-прогрессирующую — сначала напоминает ремитирующую, но на поздних стадиях характерен переход в прогрессирующую форму;
- прогрессирующе-ремитирующую — редкая форма, когда заболевание, начинаясь с ремитирующего течения, переходит в первично-прогрессирующее.
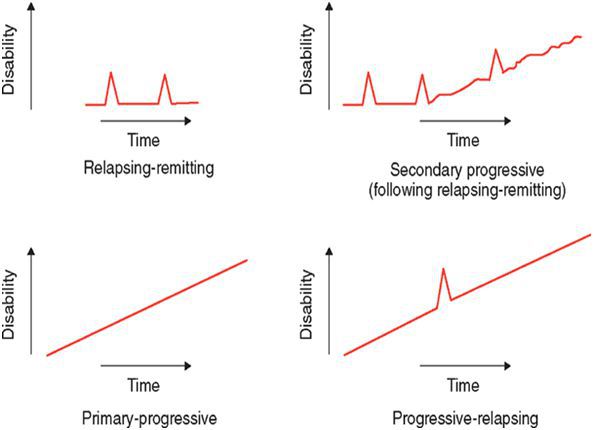
По локализации поражения мозга:
- церебральная — страдает пирамидная система;
- стволовая — наиболее тяжёлая форма РС, быстро приводящая больного к инвалидности;
- мозжечковая — церебеллярные нарушения, часто сочетается с поражением ствола мозга;
- оптическая — страдает зрительная система;
- спинальная — поражается спинной мозг, возникают тазовые расстройства и спастический нижний парапарез;
- цереброспинальная форма — наиболее распространённая, характеризуется большим количеством склеротических бляшек в головном и спинном мозге, клинически выявляются мозжечковые и церебральные нарушения, патология зрительной, вестибулярной и глазодвигательной систем.
По стадиям РС делят на:
- острую стадию, которая длиться первые две недели обострения;
- подострую, длящуюся два месяца от начала обострения и является переходной стадией к хроническому прогрессированию заболевания;
- стадию стабилизации, при которой в течение трёх месяцев не наблюдается обострений.
Осложнения рассеянного склероза
Серьёзными осложнениями, особенно при спинальных формах, являются пролежни и глубокие нарушения тазовых органов.
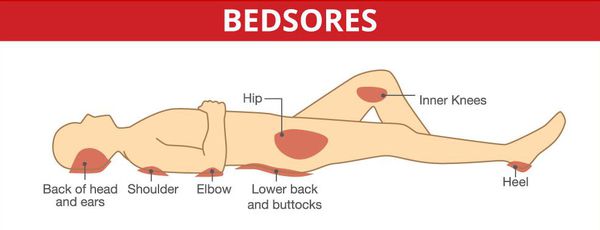
Неблагоприятно могут протекать также острые и подострые случаи с поражением жизненно важных отделов мозгового ствола.
Неврологический статус пациента напрямую зависит от его иммунитета. Зачастую появляется повышенная утомляемость, развивается мышечная слабость, головокружение. В стадии прогрессирования отмечается атаксия (нарушение координации и произвольных движений), значительное уменьшение физических и особенно двигательных возможностей конечностей с развитием спастики (двигательные нарушения в связи с повышенным тонусом мышц).
Весьма часто резко снижается острота зрения, теряется чёткость изображения, уменьшаются поля зрения, происходит искажение цветов, диплопия, развивается амблиопия и стабизм (косоглазие).
У пациентов зачастую возникает раздражительность, неустойчивость настроения, в некоторых случаях эйфория, неадекватное отношение к своему состоянию.
При РС нередки когнитивные нарушения — снижение памяти, концентрации внимания, нарушение пространственной ориентации.
Также при РС появляются тазовые нарушения — задержка мочеиспускания и длительные запоры, впоследствии больной теряет возможность контролировать процессы опорожнения кишечника и мочевого пузыря. В результате неполного опорожнения мочевого пузыря возникают урологические заболевания, вплоть до уросепсиса.
Вышеперечисленные осложнения требуют особого внимания, так как именно они могут стать причиной смертельного исхода для больного. [15] [16]
Диагностика рассеянного склероза
При вероятном РС, наряду с полным неврологическим осмотром, необходимо проводить исследование головного и спинного мозга при помощи МРТ. Этот способ исследования является наиболее информативным дополнительным методом диагностики. С его помощью можно обнаружить участки изменённой плотности в белом веществе головного мозга (очаги демиелинизации и глиоз). [10]
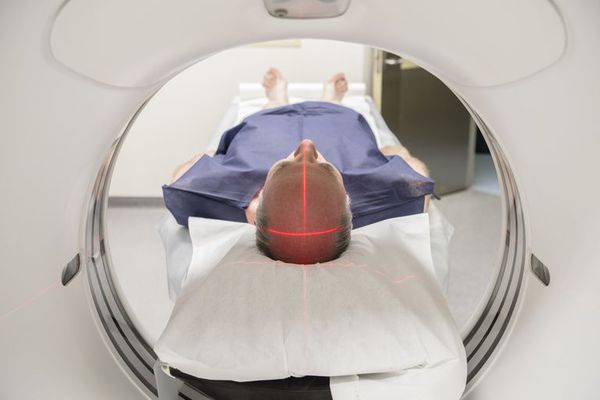
Исследование зрительных вызванных потенциалов, применяемое для определения степени сохранности некоторых проводящих путей, может также являться одним ранних диагностических критериев.
При изучении ликвора информативным считается метод изоэлектрического фокусирования спинномозговой жидкости, позволяющий выделить олигоклональные группы IgG.
Для диагностики РС широко используются критерии, предложенные Международной экспертной группой. [11]
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 35 лет.
Над статьей доктора Борисова Э. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
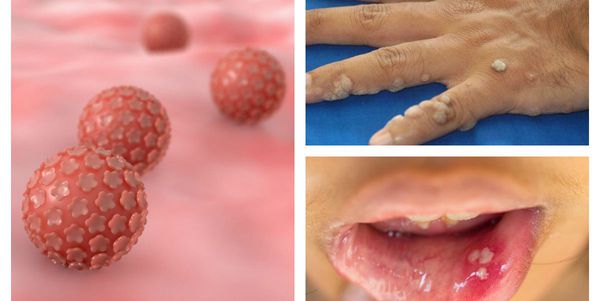
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
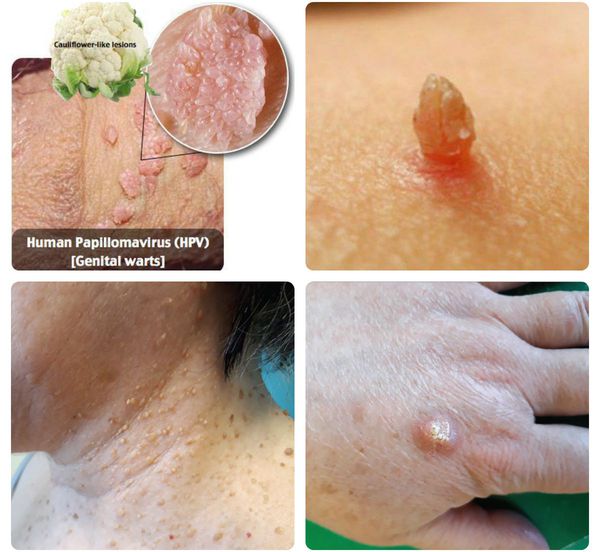
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
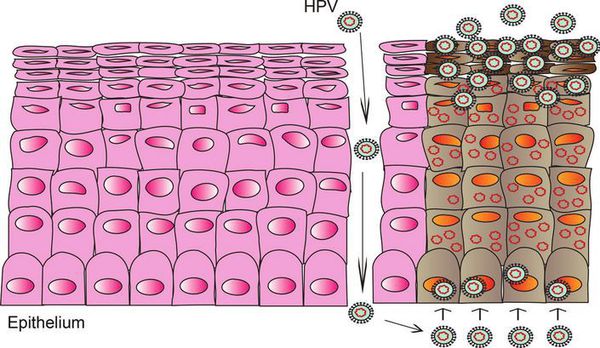
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
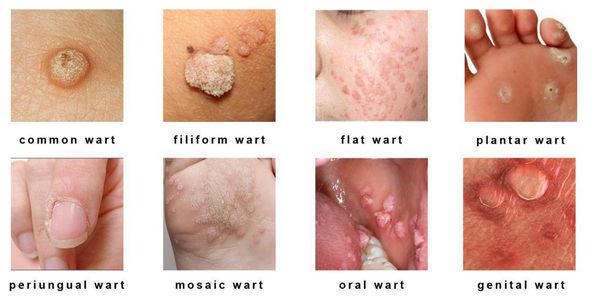
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
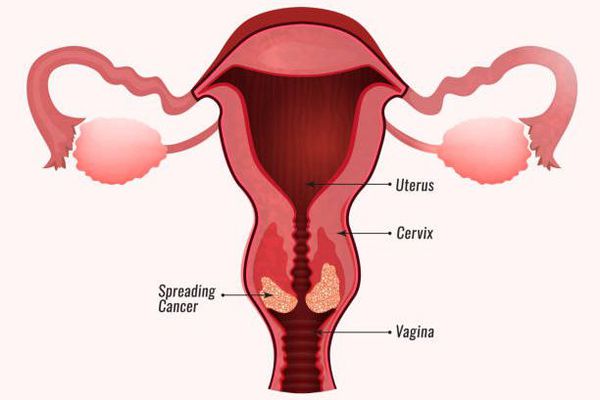
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
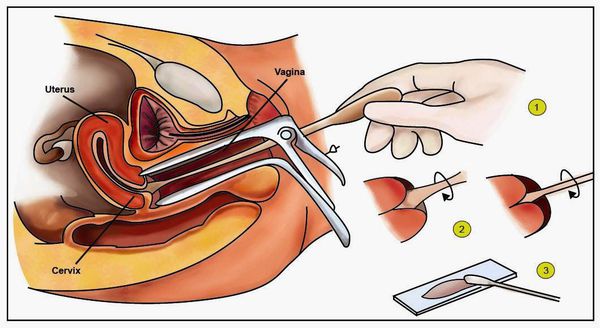
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
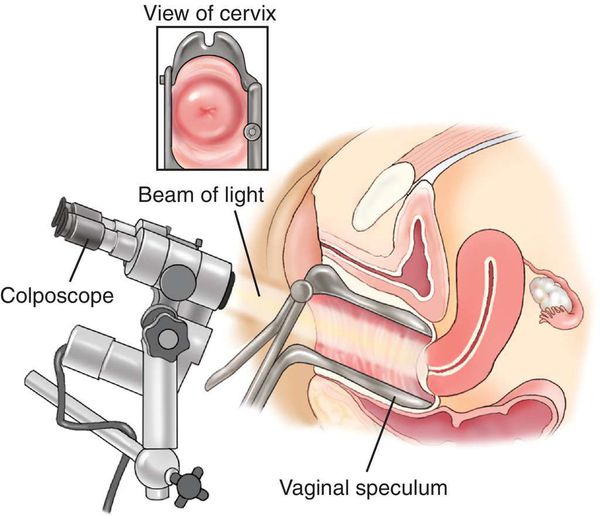
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
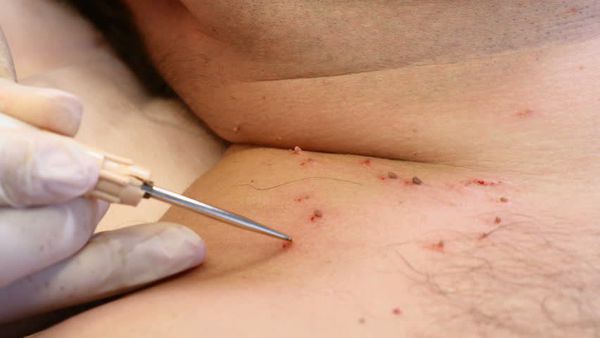
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
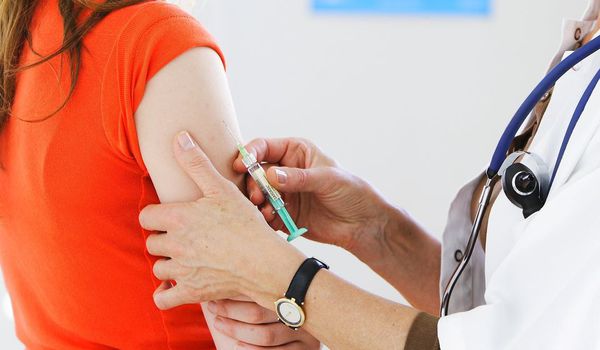
Рассеянный склероз (РС) – заболевание во многом загадочное. Ученые знают, что при этом расстройстве клетки иммунной системы человека атакуют вещество миелин, защитный слой которого покрывает нервные волокна головного и спинного мозга, а его разрушение приводит в итоге к серьезному расстройству нервной системы. Но что именно является триггером процесса, почему иммунная система начинает атаковать мозг, долгие годы оставалось неизвестным
Ученые работали с факторами риска рассеянного склероза. Среди них – низкий уровень витамина D в организме, курение, избыточный вес, женский пол (женщины заболевают РС в три раза чаще мужчин).
Также были исследования, которые демонстрировали корреляцию между рассеянным склерозом и вирусом Эпштейна – Барр (ЭБ), однако гипотеза, согласно которой РС есть последствие этой инфекции, до недавнего времени вызывало скепсис у большей части научного сообщества.
Долго не верил в нее и Билл Робинсон, ученый-иммунолог, профессор Стэнфордского университета (США). Дело в том, что вирус Эпштейна – Барр – одна из распространенных детских инфекций. Инфекционный мононуклеоз, вызываемый вирусом, протекает относительно нетяжело, ребенок поправляется, но ЭБ остается в организме в латентном (спящем) состоянии до конца жизни.
О его находках мы еще поговорим, но прежде всего следует обратить внимание на поистине прорывное исследование, выполненное научной группой Гарвардского университета под руководством профессора Альберта Ашерио. Результат изысканий его научной группы был опубликован в апреле 2022 года в журнале Science.
Что обнаружил профессор Ашерио?
Гарвардский проект длился более 20 лет. За это время были проанализированы медицинские данные 10 миллионов американских военнослужащих, включая 62 миллиона результатов анализов сданных ими образцов крови.
995 участников исследования на том или ином этапе своей жизни получили диагноз рассеянный склероз. Среди них оказался лишь один военнослужащий, не имевший вируса ЭБ в крови.
По подсчетам авторов исследования, после того как в образцах крови участника появляется этот вирус – а тех, кто получил его не в детстве, а непосредственно в период воинской службы было 34, – риск рассеянного склероза повышается в 32 раза.
Группа профессора Ашерио проверила соотношение РС с другими распространенными вирусами, в норме присутствующими в организме человека в латентном состоянии, например с цитомегаловирусом. Ни один из них не коррелировал с риском возникновения РС.
Исследователи наблюдали такую картину: сначала у военнослужащего появлялся в образце крови ЭБ, то есть происходило заражение, через какое-то время в крови появлялись нейрофибриллы, своеобразные обломки поврежденных клеток мозга, а через некоторое время – примерно через пять лет после инфицирования – такой военнослужащий получал диагноз РС.
Это исследование можно считать прорывным, так как на большой выборке участников связь вируса и РС оказалась, по словам Ашерио, кристально ясной.
Каков же биологический механизм, обеспечивающий причинно-следственную связь между вирусом ЭБ и рассеянным склерозом? Пока неясно, однако гипотеза имеется.
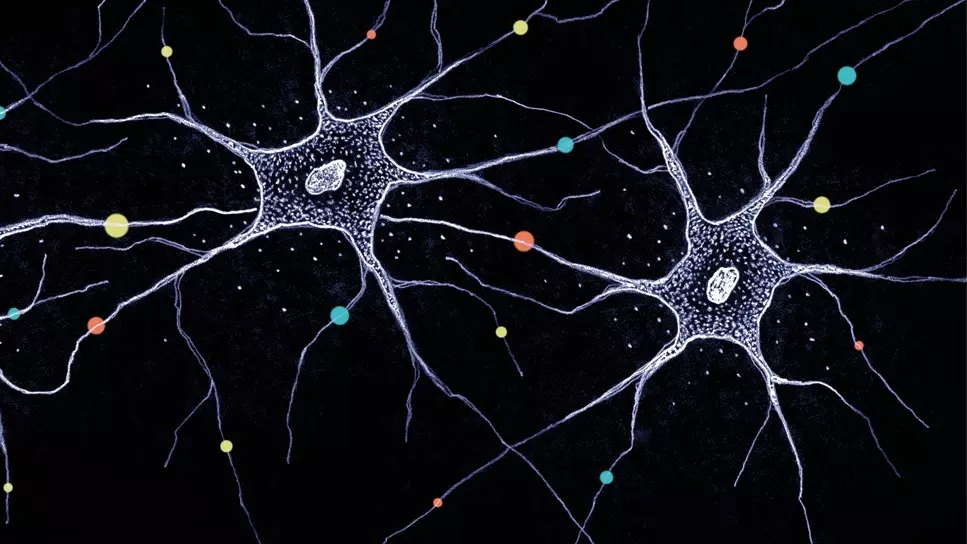
Нейрон. Фото: Biozentrum/University of Basel
Нейрон (клетка головного мозга) и его отростки покрыты защитным слоем миелина, как электрические провода покрыты изоляцией. Это позволяет проводить сигналы между нейронами со скоростью 100 метров в секунду. Когда миелин разрушается, передача электрического сигнала также нарушается, а постепенно гибнет и сам источник сигнала – нейрон.
В зависимости от того, в какой части головного или спинного мозга нарушено прохождение сигнала, больной может страдать от разнообразных симптомов: онемение, затуманенное зрение, нарушение двигательных функций, невнятная речь, а также когнитивные и эмоциональные нарушения.
Особенностью РС является одновременное поражение нескольких различных отделов нервной системы, что приводит к появлению у больных разнообразных неврологических симптомов, которые проявляются на продвинутой стадии болезни. Это включает нарушения зрения, неприятные ощущения в глазах (или в одном глазу), двигательные нарушения, частичные параличи и судороги мышц, нарушения чувствительности, сложности с мочеиспусканием и дефекацией, слабость и сонливость. В некоторых случаях возможны также когнитивные и эмоциональные нарушения. На ранних стадиях болезни объективные и субъективные неврологические симптомы могут не выявляться. Это связано с тем, что при поражении небольшого количества нервных волокон функция полностью компенсируется здоровыми нервными волокнами, и, лишь когда процент пораженных волокон приближается к 40–50%, появляются выраженные неврологические симптомы.
Робинсон и его коллеги в ходе лабораторного эксперимента рассмотрели, как функционируют клетки В-иммунной системы, которые отвечают за производство антител к инфекционным агентам. Они обнаружили, что антитела, атакующие один из белков вируса Эпштейна – Барр (а именно EBNA1) могут также атаковать один из близких к нему по структуре белков, входящих в состав миелина – GlialCAM. Такой эффект называется кросс-реактивностью и нередко встречается в мире живых организмов.
Например, при аллергии на пыльцу березы может возникать аллергическая реакция на яблоко и другие косточковые фрукты. Главный белок-аллерген березы сходен с определенными белками яблока, сельдерея, моркови, арахиса, фундука, сои, груши, клубники.
По словам профессора Робинсона, такая кросс-реактивность приводит к тому, что белок, входящий в состав миелиновой оболочки, разрушается.
Разумеется, такое случается далеко не с каждым из тех, кто болел инфекционным мононуклеозом: риск повышается у людей, перенесших в детстве психологические травмы, а также у тех, кто страдает недостатком витамина D в организме, так что у нас остаются шансы несколько снизить риски для себя и для своих детей.
Хотелось бы, однако, для профилактики и лечения РС иметь эффективные терапии.
Вакцина или лекарство?
Фото: MART PRODUCTION/Pexels
Казалось бы, есть очевидный выход: сделать вакцину против вируса Эпштейна – Барр и всех привить. Это, однако, не так легко осуществить.
Если большинство заражается инфекционным мононуклеозом в детстве, прививать от него нужно в очень раннем возрасте. При этом вакцина должна работать долгие годы и обеспечивать стерилизующий иммунитет, так чтобы попавший в организм вирус был уничтожен полностью и не осел в В-клетках.
Все это очень трудно проверить в реальной жизни, и, как говорит одна из авторов Гарвардского исследования доктор Марианна Кортезе, убедиться в том, что вакцина достигает цели, которой является предотвращение рассеянного склероза, мы сможем только через 30–40 лет после вакцинации. Это было бы чрезвычайно сложным и дорогим клиническим испытанием.
В свете новых изысканий логичным кажется создание противовирусного препарата, который воздействовал бы непосредственно на латентный вирус ЭБ.
Результаты первого этапа еще не опубликованы, однако руководство компании заявляет, что из 24 добровольцев, участвовавших в испытаниях, 20 продемонстрировали признаки улучшения или по крайней мере замедления регресса. Важно и то, что препарат не давал серьезных побочных эффектов.
Исследователи использовали донорские белые кровяные тельца, нацеленные на вирус ЭБ. До них подобная технология была опробована в 2018 году австралийскими учеными, которые использовали и перепрограммировали собственные Т-клетки пациентов с РС.
Использование не собственных, а донорских клеток позволяет сократить время производства препарата и удешевляет его.
Ученые надеются, что их препарат, пока что называемый АТА188, позволит контролировать симптомы, а донорский принцип его производства сделает его доступным для максимального числа пациентов с разнообразными формами РС.
Из 18 пациентов, которые согласились продолжать участие в испытаниях препарата, 9 сообщают о своем стабильном состоянии на протяжении года или более того, но, пожалуй, самым значительным достижением стало то, что у некоторых пациентов наблюдается восстановление миелинового защитного слоя нервных волокон.
Такие результаты с учетом маленькой выборки рано объявлять победой над рассеянным склерозом, однако основания для оптимизма определенно имеются.
Источники:
Читайте также:

