Вирус папилломы дыхательные пути
Обновлено: 25.04.2024
Для цитирования: Савельева И.В., Полянская И.Б., Иванова О.В. Опыт использования инозина пранобекса при ВПЧ-ассоциированных поражениях слизистых оболочек и кожи у женщин. РМЖ. Мать и дитя. 2015;23(20):1209.
Заболевания, ассоциированные с вирусом папилломы человека (ВПЧ), являются одной из важнейших проблем в акушерстве и гинекологии. Вирус вызывает целый ряд заболеваний кожи и слизистых оболочек. В настоящее время известно уже более 200 типов папилломавирусов, причем 40 из них поражают мочеполовые органы. Инфицированность населения Земли папилломавирусом впечатляет – им инфицировано около 600 млн жителей планеты, причем у 28% зараженных в процессе задействованы онкогенные типы вирусов [16, 17].
В связи с резким ростом инфицированности населения ВПЧ, значительной его контагиозностью и способностью вызывать злокачественную патологию диагностика и лечение заболеваний, ассоциированных с папилломавирусной инфекцией, привлекают особое внимание акушеров-гинекологов. Согласно данным ВОЗ, папилломавирусная инфекция является наиболее распространенной инфекцией, передающейся половым путем; в Европе инфицированность ею населения репродуктивного возраста составляет 20–60% [1, 3, 14].
На сегодняшний день доказано, что папилломавирусная инфекция является ведущей причиной рака шейки матки [2, 15, 18, 20]. При инвазивном раке шейки матки в 95–100% случаев выявляется ВПЧ.
Как показали исследования последних лет, большинство женщин на протяжении жизни инфицируются ВПЧ. Так, например, более 80% женщин заражаются ВПЧ уже через 2 года после начала половой жизни, при этом даже при наличии одного полового партнера 20% женщин являются зараженными ВПЧ [10, 13]. Благодаря работе иммунной системы первичное заражение ВПЧ в большинстве случаев остается незамеченным и не сопровождается какими-либо последствиями. Однако тем, у кого самоэлиминации вируса не произошло, приходится жить с ВПЧ и бороться с его разрушающим действием. ВПЧ обнаруживают у 99,7% женщин с гистологически подтвержденным диагнозом рака шейки матки. При этом нередко определяется инфицированность различными типами ВПЧ, в т. ч. у женщин с нормальной цитологией.
Рак шейки матки представляет собой важную социальную проблему. На сегодняшний день он является одной из основных причин смерти от злокачественных опухолей у женщин в возрасте 15–40 лет. Особенно заметный рост наблюдается в группе моложе 29 лет, где прирост этого показателя за прошедшее десятилетие составил 150% [4].
Папилломавирусы передаются только от человека к человеку. Основным путем заражения ВПЧ является половой (включая орогенитальные и анальные контакты). Доказана возможность передачи папилломавирусной инфекции от матери плоду с поражением гортани (ларингеальный папилломатоз) и появлением аногенитальных бородавок у новорожденного, а также способность поражать клетки трофобласта, что может являться причиной прерывания беременности [15, 20].
Инкубационный период при заражении ВПЧ составляет от 3 мес. до нескольких лет.
Факторами риска инфицирования ВПЧ являются:
• раннее начало половой жизни;
• наличие более 3-х половых партнеров;
• наличие одного полового партнера, у которого множество половых партнеров;
• курение;
• наличие других инфекций, передающихся половым путем;
• нарушение иммунитета;
• факторы окружающей среды, условия жизни и работы.
По онкогенной опасности для человека условно выделяют три группы типов папилломавирусов (табл. 1):
• неонкогенные папилломавирусы ‒ никогда не приводят к озлокачествлению вызванного ими процесса;
• онкогенные папилломавирусы низкого риска – при определенных условиях (достаточно редко) могут приводить к озлокачествлению вызванного процесса;
• онкогенные папилломавирусы высокого онкогенного риска ‒ под влиянием различных факторов приводят к озлокачествлению вызванного ими процесса и являются доказанным этиологическим фактором рака шейки матки.
Течение папилломавирусной инфекции во многом зависит от состояния иммунной системы. В 70–80% случаев оно может быть транзиторным, и тогда наблюдается спонтанное очищение пораженной ткани от ВПЧ. Данный благоприятный исход возможен у молодых женщин с нормальным состоянием иммунной системы.
Латентное течение ВПЧ-инфекции характеризуется отсутствием каких-либо клинических и морфологических изменений при обнаружении ДНК вируса. В данном случае требуется наблюдение и постоянный контроль за состоянием эпителия шейки матки, влагалища и вульвы [11, 19].
В 20–30% случаев при ВПЧ-инфекции наблюдается прогрессирование заболевания. После элиминации вируса у части женщин сохраняются субклинические проявления инфекции, которые могут переходить в клиническую фазу у женщин с нарушением иммунитета [12]. ВПЧ довольно долго персистирует в многослойном плоском эпителии, что способствует рецидивированию заболевания.
По варианту течения и глубине поражения ВПЧ-ассоциированные заболевания нижнего отдела гениталий делятся на следующие формы [11, 12]:
1. Клинические (видимые невооруженным глазом):
– экзофитные кондиломы (остроконечные типичные, папиллярные, папуловидные);
– симптоматические цервикальные интраэпителиальные неоплазии.
2. Субклинические (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом либо гистологическом исследовании):
– плоские кондиломы (типичная структура с множеством койлоцитов);
– малые формы (различные поражения многослойного плоского эпителия и метапластического эпителия с единичными койлоцитами);
– кондиломатозный цервицит/вагинит.
3. Латентные (отсутствие клинических, морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
4. Цервикальная интраэпителиальная неоплазия (CIN) или плоскоклеточные интраэпителиальные поражения (SIL) и рак шейки матки:
‒ CIN I – слабая дисплазия с койлоцитозом, дискератозом или без них;
‒ CIN II – умеренная дисплазия с койлоцитозом, дискератозом или без них;
‒ CIN III – тяжелая дисплазия или карцинома in situ с койлоцитозом, дискератозом или без них;
‒ микроинвазивная плоскоклеточная и железистая карцинома.
Субклинические формы – плоские кондиломы, вирусные цервициты и вагиниты – являются причиной частых обращений больных к врачам с жалобами на дискомфорт, обусловленный зудом, жжением, обильными выделениями, рецидивирующим бактериальным вагинозом и кандидозом. В большинстве случаев у таких пациенток возникают обострения клинических симптомов перед каждой менструацией. Клинические формы течения ВПЧ-инфекции – экзофитные кондиломы – могут быть незначительны по размерам и площади поражения, но вызывать нестерпимый зуд у пациенток, и наоборот, достаточно большие образования бывают врачебной находкой во время профилактического осмотра. Длительная персистенция ВПЧ в ткани органов нижнего отдела генитального тракта способна провоцировать развитие предраковых и раковых процессов.
Целый ряд онкологических заболеваний связан с высокоонкогенными типами ВПЧ, в первую очередь с 16 и 18 [19], в их числе рак шейки матки, прямой кишки, влагалища и вульвы, рак полового члена, гортани, ротовой полости.
Для диагностики ВПЧ-ассоциированных заболеваний применяются следующие методы исследования:
• клинические;
• цитологические (Pap-test);
• расширенная кольпоскопия;
• подтверждение наличия ДНК ВПЧ в цервикальном эпителии (ПЦР);
• определение вирусной нагрузки методом Hybride Capture (ВПЧ-Digene-тест), позволяющее выявить число копий ДНК онкогенных вирусов;
• ПЦР в режиме реального времени;
• жидкостная цитология;
• морфологическое исследование;
• определение онкомаркеров – онкобелков p16, Кi67;
• сканирование шейки матки в режиме реального времени (TruScreen) и др.
Клинико-визуальный метод является наиболее простым в диагностике ВПЧ-инфекции гениталий. С помощью рутинного осмотра вульвы, промежности, перианальной области, шейки матки и влагалища с использованием теста с раствором Люголя и 3–5% уксусной кислотой выявляется большинство клинических и субклинических форм инфекции. Однако данный метод не позволяет судить о характере и прогнозе течения патологического процесса [5].
Кольпоскопия представляет собой высокоинформативный и недорогой метод диагностики заболеваний шейки матки. Наиболее распространенной является расширенная кольпоскопия, которая включает осмотр и ревизию состояния слизистой оболочки шейки матки, влагалища и вульвы при увеличении микроскопа в 7–30 раз и применении некоторых эпителиальных тестов, при которых оценивается реакция тканей в ответ на их обработку различными медикаментозными средствами. Для более детального осмотра сосудистой сети применяются различные фильтры [5].
Диагностика типичных экзофитных кондилом не представляет особой сложности. Кольпоскопически они имеют характерный вид с пальцеобразными выпячиваниями и наличием петли сосуда в каждом из них. Большие трудности вызывает диагностика субклинических форм папилломавирусной инфекции и выявление кольпоскопических признаков, характеризующих вирусные поражения слизистой оболочки шейки матки, влагалища и вульвы. Это сложно еще и потому, что участки ВПЧ-инфекции могут сочетаться с другими доброкачественными и злокачественными образованиями эпителия. В связи с большим разнообразием проявлений субклинической инфекции специфического комплекса кольпоскопических признаков нет. Точно диагностировать внутриэпителиальные кондиломы с помощью одного кольпоскопического метода возможно только при выраженном ороговении или при сочетании плоских форм кондилом с экзофитными.
В настоящее время существует достаточно лекарственных средств для устранения симптомов заболевания, а также препаратов для повышения иммунитета, которые позволяют полностью избавиться от рецидивов и добиться такого результата, когда вирус не обнаруживается в анализах. Такой низкий уровень его концентрации поможет забыть о внешних проявлениях и предупредить развитие онкологических заболеваний, особенно часто встречающихся на фоне ВПЧ у женщин.
Выбор метода лечения при ВПЧ-ассоциированной патологии зависит от ряда факторов, включая морфологию, размеры, количество и локализацию кондилом, возраст больных и наличие беременности. В этом процессе немаловажную роль также играет собственный опыт врача и метод лечения, который он предпочитает. Основной целью терапии является элиминация кондилом, которые вызывают симптомы, сопряженные с физическим и психологическим дискомфортом. Тяжесть клинической манифестации ВПЧ-ассоциированной патологии слизистых оболочек и кожи урогенитальной и перианальной области широко варьирует, что требует тщательного выбора и обоснования целесообразности использования того или иного метода в каждом конкретном случае.
Доказательства преимущества какого-либо определенного метода перед остальными отсутствуют. Лечебное средство нужно выбирать индивидуально, исходя из того принципа, что лечебное воздействие не должно сопровождаться осложнениями, вызывающими более тяжелые страдания по сравнению с основной болезнью. При этом следует также учитывать выбор пациенток, исходя из стоимости и комфортности того или иного метода лечения для конкретного больного.
Арсенал средств:
• криодеструкция жидким азотом (пораженную область уничтожают замораживанием);
• радиоволновое удаление кандилом и лечение шейки матки;
• лазерная терапия – вариант, к которому желательно прибегать только в крайних случаях. Дело в том, что вирус, обработанный лазером, попадает в воздух и может заразить медперсонал, работающий без защитных масок;
• лекарственный метод – обработка пораженной области различными кремами, мазями, гелями, назначение иммуностимуляторов.
Целью настоящего исследования явилась оценка эффективности применения инозина пранобекса (Изопринозина) при остроконечных кондиломах, CIN, субклинических формах ВПЧ в комбинированном режиме.
Материал и методы. Проведен анализ эффективности применения и побочных эффектов инозина пранобекса (ИП) при ВПЧ-ассоциированных поражениях слизистых оболочек и кожи у 30 больных. ИП назначали 30 больным, из них 11 пациенток принимали ИП в монорежиме, а 19 – в комбинированном режиме. При этом сравнивали эффективность лечения ВПЧ-ассоциированных заболеваний по степени ликвидации жалоб на зуд и неприятные ощущения, по площади регрессии макроскопических изменений, при ВПЧ-ассоциированных заболеваниях шейки матки – по результатам ДНК ВПЧ-теста.
Далее побочные эффекты были проанализированы по результатам лечения пациенток, которые принимали ИП как в монорежиме, так и в комбинированном режиме.
Результаты исследования. Пациентки распределились по возрастным группам следующим образом: число пациенток до 20 лет составило 5; от 21 до 25 лет – 10; от 26 до 30 лет – 7; от 31 до 35 лет – 4; от 36 до 40 лет – 3; от 41 до 45 лет – 1.
Результаты визуальной оценки уменьшения площади ВПЧ-ассоциированных патологически измененных участков шейки матки, слизистых оболочек и кожи урогенитальной, анальной и перианальной областей после их лечения различными методами с и без применения ИП свидетельствуют, что наиболее значительное клиническое улучшение наступило после комбинированного лечения по сравнению с применением ИП в монорежиме (p <0,001). Результаты применения традиционных методов лечения оказались одинаковыми по эффективности с ИП в монорежиме (p<0,001) и ниже, чем таковые в группе с ИП в комбинированном режиме (p<0,001).
Результаты повторного анализа ПЦР ДНК ВПЧ-тестирования через 6 мес. у женщин, включенных в исследование, оказались положительными в среднем в 66,2±0,08% наблюдений, у женщин после традиционных методов лечения – в 52,6±0,09%, у пациенток после ИП в монорежиме – в 42,6±0,09%, у женщин после ИП в комбинированном режиме – в 25,3±0,08% наблюдений.
Анализ результатов свидетельствует, что применение ИП как в монорежиме, так и в комбинированном способствует существенной элиминации ВПЧ (p
Заключение. Инозин пранобекс (Изопринозин) – давно используемый в медицинской практике иммуностимулятор, который считается эффективным при различных вирусных инфекциях. ИП, по своей природе являясь производным пуринов и жизненно важным компонентом клеточного ядра, не дает выраженного токсического эффекта даже при назначении в высоких дозах. Обычно природные аналоги ИП поступают в организм из разнообразных пищевых продуктов. Поэтому при правильном назначении ИП в качестве иммуностимулятора с учетом противопоказаний к его применению частота побочных эффектов минимальна. Об этом свидетельствуют данные многолетнего использования ИП в медицинской практике во всем мире. Обнадеживающие результаты комбинированного применения ИП позволяют сделать вывод о целесообразности включения указанного иммуномодулятора в схемы традиционных методов лечения ВПЧ-ассоциированной патологии слизистых оболочек и кожи. Требуется дальнейшее изучение эффективности этого метода с точки зрения доказательной медицины.
Лучевая диагностика папилломатоза трахеи, бронхов на рентгене, КТ
а) Терминология:
1. Синонимы:
• Рецидивирующий респираторный папилломатоз (РРП)
2. Определение:
• Узелки вдыхательных путях (папилломы), обусловленные инфицированием вирусом папилломы человека (ВПЧ):
о Верхние отделы > нижние отделы дыхательных путей
• Инвазивный папилломатоз:
о Диссеминация в легких
б) Лучевые признаки трахеобронхиального папилломатоза:
1. Основные особенности:
• Оптимальный диагностический ориентир:
о Утолщение, в том числе узловое стенок дыхательных путей
о Множественные солидные и полостные узелки или объемные образования в легких
• Локализация:
о Чаще всего поражается гортань:
- Различная частота поражения дистальных отделов дыхательных путей
В 5-29% от всех случаев
о Инвазивный папилломатоз
- В коронарной плоскости центральная локализация или локализация в прикорневой зоне
- В аксиальной плоскости локализация в задних отделах
• Размер:
о Инвазивный папилломатоз:
- Различный размер
- Большинство узелков 1 -3 см в диаметре
• Морфологические особенности:
о Инвазивный папилломатоз
о Узелки меньшего размера обычно солидные
о Чем больше размер узелка, тем больше вероятность формирования в нем полости

(а) У пациента с трахеобронхиальным папилломатозом при прицельной рентгенографии органов грудной клетки в ПП проекции в правом легком определяются множественные накладывающиеся друг на друга кольцевидные затемнения, соответствующие кистам. В левом легком выявляются аналогичные затемнения (не показаны). Выявляется объемное уменьшение нижней доли правого легкого.
(б) У этого же пациента при нативной КТ визуализируются узелки в области бифуркации трахеи и в правом верхнедолевом бронхе, а также множественные кисты с тонкими неровными стенками в верхней и нижней долях правого легкого.
2. Рентгенография:
о Дыхательные пути:
- Утолщение, в том числе узловое, стенок дыхательных путей:
При рентгенографии может не визуализироваться
о Множественные узелки или объемные образования в легких:
- В структуре могут определяться полости
4. Рекомендации к проведению лучевых исследований:
• Оптимальный метод лучевой диагностики:
о КТ представляет собой оптимальный метод визуализации узелков в дыхательных путях, выявления инвазивного папилломатоза легких и плоскоклеточного рака

(а) При КТ с контрастным усилением в обоих легких определяются множественные полостные узелки. В нижней доле левого легкого выявляется полостное объемное образование с неровным контуром. Наблюдается преимущественное поражение задних отделов нижних долей легких вследствие диссеминации.
(б) У этого же пациента при КТ с контрастным усилением на реконструкции в коронарной плоскости в обоих легких визуализируются множественные солидные и полостные узелки и объемные образования. Чем больше размер узелка, тем больше вероятность формирования полости. Образование нижней доли левого легкого может соответствовать плоскоклеточному раку — известному осложнению папилломатоза.
в) Дифференциальная диагностика папилломатоза трахебронхиального дерева:
1. Остеохондропластическая трахеобронхопатия:
• Множественные мелкие узелки в дыхательных путях ± кальцифи каты
• Поражает переднебоковую стенку трахеи и стенки проксимальных бронхов
• Отсутствует поражение задней мембранозной стенки трахеи
• Асимметричный стеноз дыхательных путей
2. Гранулематоз с полиангиитом:
• Множественные полостные узелки или объемные образования в легких
• Стеноз подголосового отдела гортани
• Утолщение стенок дыхательных путей
3. Трахеобронхиальный амилоидоз:
• Кальцифицированные или некальцифицированные узелки в подслизистом слое трахеи, вызывающие сужение ее просвета
• Поражается задняя мембранозная стенка
4. Рецидивирующий полихондрит:
• Диффузное утолщение стенок трахеи и главных бронхов и сужение их просвета; отсутствие кальцификатов
• Поражение передней и боковой стенок трахеи, хрящей трахеи
6. Плоскоклеточный рак:
• Наиболее частая форма рака легких, при которой формируются полости
• Наблюдаются в 15% случаев
• Развитие тесно связано с курением
• Риск повышается при наличии инвазивного папилломатоза
7. Метастазы в легких:
• Множественные узелки или объемные образования в легких
• В метастазах плоскоклеточного рака и сарком могут формироваться полости
• Дыхательные пути поражаются не всегда
8. Септические эмболы:
• Узелки или объемные образования с нечетким контуром
• Количество полостей вариабельно

(а) У пациента с трахеобронхиальным папилломатозом при нативной КТ в нижней доле правого легкого определяется солидное объемное образование с дольчатым контуром, соответствующее плоскоклеточному раку. Плоскоклеточный рак встречается в 2% случаев. Ее наличие следует заподозрить при быстром росте узелка в легких.
(б) У этого же пациента при нативной КТ в нижней доле правого легкого визуализируются солидный и полостной узелки. У пациентов с трахеобронхиальным папилломатозом наличие узелков в легких служит признаком инвазивного папилломатоза.
г) Патоморфология папилломатоза трахеи и бронхов:
1. Основные особенности:
• Этиология:
о Инфицирование дыхательных путей ВПЧ:
- Передача ВПЧ от матери ребенку при прохождении через родовые пути:
Факторы риска: первые роды, роды через естественные родовые пути, возраст матери < 20 лет
- Чаще всего встречается инфицирование ВПЧ 6 и 11 типов
- Может поражаться любой отдел дыхательных путей:
В 95% случаев поражается гортань
Единичные папилломы чаще встречаются у курящих мужчин среднего возраста
- Диссеминация вдыхательных путях (инвазивный папилломатоз):
Менее чем в 1 % случаев наблюдается диссеминация в легких
Хирургические вмешательства на папилломах гортани повышают риск диссеминации
о Диссеминация в легких обычно наглядна у детей и лиц молодого возраста:
• Инфекция ВПЧ:
о Папилломы и остроконечные кондиломы
о Тропизм к кератиноцитам о Рак шейки матки
2. Макроскопические патоморфо логические и хирургические особенности:
• Папиллярные или на широком основании образования с васкуляризированной сердцевиной, покрытые плоским эпителием
• Папилломы дыхательных путей могут расти экзофитно или эндофитно
• Напоминают цветную капусту
3. Микроскопические особенности:
• Образования в гортани и легких, состоящие из плоских эпителиальных клеток
• Полости выстланы плоским эпителием
о Плоские эпителиальные клетки могут распространяться между альвеолами через поры Кона
д) Клинические аспекты:
1. Проявления:
• Наиболее частые признаки:
о При умеренном поражении симптомы могут отсутствовать
о Охриплость вследствие поражения гортани является наиболее частым симптомом
о При наличии хрипов и стридора может быть ошибочно принят за астму
о Другие симптомы зависят от размера, количества и локализации папиллом:
- Одышка, гемофтиз
- Постобструктивная пневмония
• Функциональные легочные тесты:
о Признаки обструкции верхних отделов дыхательных путей (до трахеи)
• Ларингоскопия:
о Непосредственная визуализация папиллом
о Выполнение биопсии, необходимой для определения типа ВПЧ
2. Демографические данные:
• Возраст:
о Взрослые: два случая на 100000 человек
о Двухуровневое распределение по возрасту:
- Дети: от 18 месяцев до трех лет
- Взрослые: четвертое десятилетие
• Пол:
о Дети: М =Ж
о Взрослые: М>Ж
3. Естественное течение заболевания и прогноз:
• У молодых лиц обычно купируется самостоятельно
• Узелки в легких обычно растут весьма медленно:
о При быстром росте следует подозревать плоскоклеточный рак
• Инвазивный папилломатоз:
о Летальный исход вследствие дыхательной недостаточности
о Уровень смертности достигает 50% о В 2% случаев выявляется плоскоклеточный рак:
- Обычно возникает спустя 15 лет после развития папилломатоза
- Карциномы часто характеризуются мультицентричным ростом
4. Лечение папилломатоза трахеи и бронхов:
• Если купируется самостоятельно, то лечение обычно не требуется
• При развитии обструкции дыхательных путей проводится хирургическое или медикаментозное лечение:
о Лазерная абляция образований дыхательных путей:
- Обычно требуется многократное повторение процедуры
- При поражении нижних отделов дыхательных путей выполнение процедуры сопряжено с техническими трудностями
- Меры предосторожности для медицинских работников, препятствующие передаче вируса:
Распространение аэрозольных вирусных частиц
о Трахеостомия:
- Устранение обструкции дыхательных путей
- Необходимость в проведении процедуры чаще возникает у пациентов молодого возраста
о Антивирусные препараты могут замедлить рост
о Интерферон может замедлить рост:
- Системное введение препарата либо непосредственное введение его внутрь образования
• Отказ от курения:
о Снижает риск развития плоскоклеточного рака о Канцерогенные вещества в табаке способствуют росту папиллом
5. Диагностические пункты:
1. Следует учитывать:
• У пациентов с множественными узелками в дыхательных путях следует подозревать трахеобронхиальный папилломатоз
2. Ключевые моменты при интерпретации изображений:
• Следует изучать легкие на предмет наличия инвазивного папилломатоза и патологических образований, которые могут соответствовать плоскоклеточному раку
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 35 лет.
Над статьей доктора Борисова Э. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
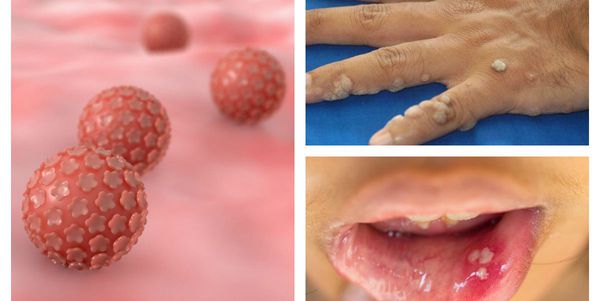
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
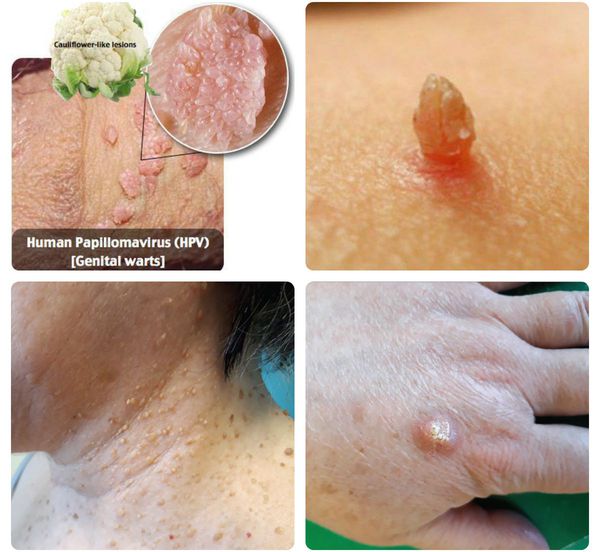
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
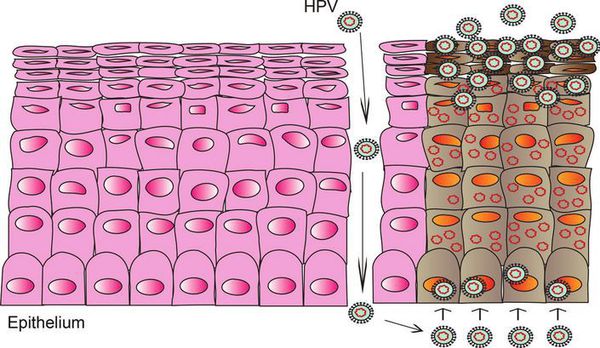
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
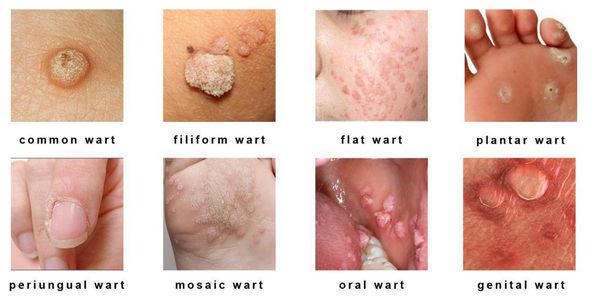
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
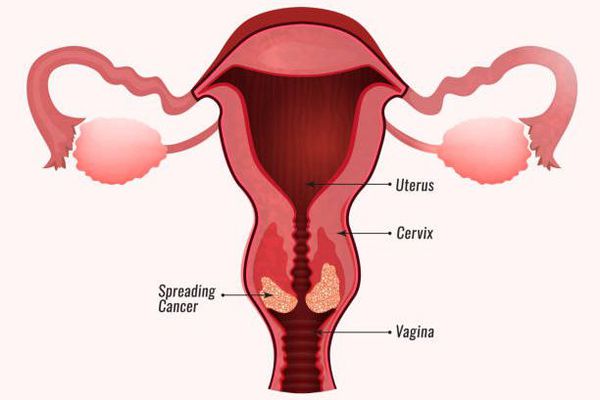
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
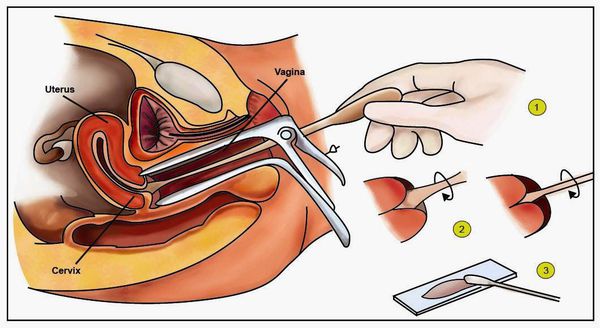
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
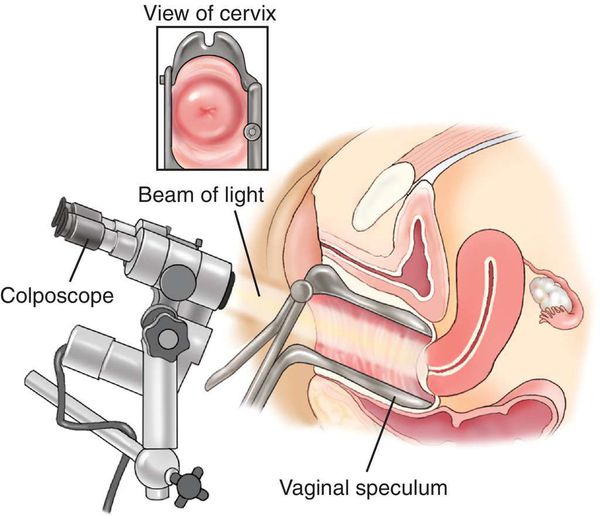
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
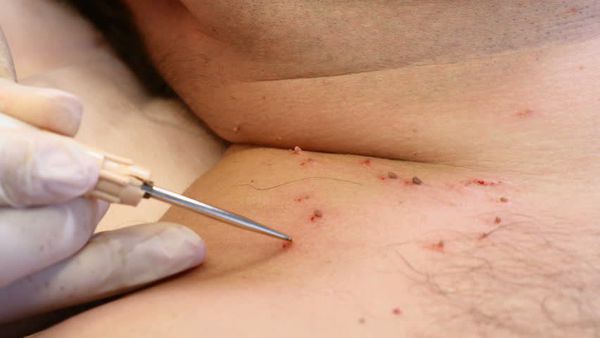
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
Папилломатоз гортани остается одной из неразрешимых проблем современной оториноларингологии. В статье отражается историческая последовательность изучения заболевания, приводятся варианты лечения и ре- зультаты собственного исследования, в ходе которого сравнивались 2 способа лечения больных папилломатозом гортани.
Для цитирования: Свистушкин В.М., Волкова К.Б. Современное состояние проблемы респираторного папилломатоза гортани. РМЖ. 2015;23:1377-1380.
В статье приведено современное состояние проблемы респираторного папилломатоза гортани
Для цитирования. Свистушкин В.М., Волкова К.Б. Современное состояние проблемы респираторного папилломатоза гортани // РМЖ. 2015. No 23. С. 1377 –1380.
Резюме: папилломатоз гортани остается одной из неразрешимых проблем современной оториноларингологии. В статье отражается историческая последовательность изучения заболевания, приводятся варианты лечения и результаты собственного исследования, в ходе которого сравнивались 2 способа лечения больных папилломатозом гортани.
Ключевые слова: папилломатоз гортани, вирус папилломы человека, противовирусная терапия.
1. Ашуров З.М., Зенгер В.Г. Респираторный папилломатоз у детей. М.: Медиа-сфера, 2004.
2. Солдатский Ю.Л., Киселев В.И., Онуфриева Е.К., Стеклов А.М., Шепин Н.В., Стрыгина Ю.В., Гаспарян С.Ф., Погосова И.Е. Анализ эффективности противорецидивной терапии ювенильного респираторного папилломатоза при помощи индинола // Вестник оториноларингологии. 2006. № 1. С. 46–48.
3. Best S.R., Friedman A.D., Landau-Zemer T., Barbu A.M., Burns J.A., Freeman M.W., Halvorsen Y.D., Hillman R.E., Zeitels S.M. Safety and dosing of bevacizumab (avastin) for the treatment of recurrent respiratory papillomatosis // Ann Otol Rhinol Laryngol. 2012 Sep. Vol. 121 (9). Р. 587–593.
4. Кучерова Л.Р. Клинико-иммунологическое обоснование местного применения рекомбинантного интерферона-альфа2 в терапии рецидивирующего респираторного папилломатоза: Дисс. … канд. мед. наук. М., 2011.
5. Carvalho C.M., Huot L., Charlois A.L., Khalfallah S.A., Chapuis F. Prognostic factors of recurrent respiratory papillomatosis from a registry of 72 patients // Acta Otolaryngol. 2009 Apr. Vol. 129 (4). Р. 462–470.
6. Свистушкин В.М., Мустафаев Д.М. Папилломатоз гортани: современное состояние проблемы // Вестник оториноларингологии. 2013. № 2. С. 79–85.
7. Derkay C.S., Volsky P.G., Rosen C.A., Pransky S.M., McMurray J.S., Chadha N.K., Froehlich P. Current use of intralesional cidofovir for recurrent respiratory papillomatosis // Laryngoscope. 2013 Mar. Vol. 123 (3). Р. 705–712. DOI: 10.1002/lary.23673. Epub 2012 Oct 15.
8. Abramson A.L., Levy A.S., Hirschfield L.S. The pathologic and thermal effects of gold vapour laser photodynamic therapy on the larynx. Experimental study // Arch. Otolaryngol. Head Neck Surg. 1990, Jun. Vol. 116. N 6. P. 687–691.
9. Bell R., Hong W.K., Itri L.M., McDonald G., Strong M.S. The use of cis-retinoic acid in recurrent respiratory papillomatosis of the larynx: a randomized pilot study // Am J Otolaryngol. 1988 Jul-Aug. Vol. 9 (4). Р. 161–164.
10. Hartnick C.J., Boseley M.E., Franco R.A. Jr, Cunningham M.J., Pransky S. Efficacy of treating children with anterior commissure and true vocal fold respiratory papilloma with the 585-nm pulsed-dye laser // Arch Otolaryngol Head Neck Surg. 2007 Feb. Vol.133 (2). Р. 127–130.
11. Bishai D., Haskins K. Keerti Shah The Cost of Juvenile-Onset Recurrent Respiratory Papillomatosis // Arch Otolaryngol Head Neck Surg. 2000. Vol. 126 (8). Р. 935–939.
12. Carney A.S., Evans A.S., Mirza S., Psaltis A. Radiofrequency coblation for treatment of advanced laryngotracheal recurrent respiratory papillomatosis // Journal of Laryngology and Otology. 2010. Vol. 124 (5). Р. 510–514.
13. Donne A.J., Hampsonb L. Homer J.J., Hampsonb I.N. The role of HPV type in Recurrent Respiratory Papillomatosis // International Journal of Pediatric Otolaryngology. 2010. Vol. 74 (1). Р. 7–14.
14. Kashima H., Mounts P., Leventhal B., Hruban R.H. Sites of predilection in recurrent respiratory papillomatosis // Ann Otol Rhinol Laryngol. 1993 Aug. Vol. 102 (8 Pt 1). Р. 580–583
15. Kashima H.K., Kessis T., Mounts P., Shah K. Polymerase chain reaction identification of human papillomavirus DNA in CO2 laser plume from recurrent respiratory papillomatosis // Otolaryngol Head Neck Surg. 1991 Feb. Vol. 104 (2). Р. 191–195.
16. Carvalho C.M., Huot L., Charlois A.L., Khalfallah S.A., Chapuis F. Prognostic factors of recurrent respiratory papillomatosis from a registry of 72 patients // Acta Otolaryngol. 2009 Apr. Vol. 129 (4). Р. 462–470.
17. Chadha N.K., James A. Adjuvant antiviral therapy for recurrent respiratory papillomatosis // Cochrane Database Syst Rev. 2012 Dec 12. Vol. 12. CD005053.
18. Derkay C.S., Hester R.P., Burke B., Carron J., Lawson L. Analysis of a staging assessment system for prediction of surgical interval in recurrent respiratory papillomatosis // Int J Pediatr Otorhinolaryngol. 2004 Dec. Vol. 68 (12). Р. 1493–1498.
19. Derkay C.S., Volsky P.G., Rosen C.A., Pransky S.M., McMurray J.S., Chadha N.K., Froehlich P. Current use of intralesional cidofovir for recurrent respiratory papillomatosis // Laryngoscope. 2013 Mar. Vol. 123 (3). Р. 705–712. DOI: 10.1002/lary.23673. Epub 2012 Oct 15.
20. Derkay C.S. Recurrent respiratory papillomatosis // Laryngoscope. 2001. Vol. 111 (1). Р. 57–69.
21. Derkay C.S., Wiatrak B. Recurrent respiratory papillomatosis: a review // Laryngoscope. 2008 Jul. Vol. 118 (7). Р. 1236–1247.
21. Mahnke C.G., Fröhlich O., Lippert B.M.,Werner J.A. Recurrent laryngeal papillomatosis. Retrospective analysis of 95 patients and review of the literature // Otolaryngol P. 1996. Vol. 50 (6). Р. 567–578.
22. Förster G., Boltze C., Seidel J., Pawlita M., Müller A. Juvenile laryngeal papillomatosis--immunisation with the polyvalent vaccine gardasil // Laryngorhinootologie. 2008. Vol. 87 (11). Р. 796–769.
23. Hallmo P., Naess O. Laryngeal papillomatosis with human papillomavirus DNA contracted by a laser surgeon // Eur Arch Otorhinolaryngol. 1991. Vol. 248 (7). Р. 425–427.
24. Hermann J.S., Pontes P., Weckx L.L., Fujita R., Avelino M., Pignatari S.S. Laryngeal sequelae of recurrent respiratory papillomatosis surgery in children // Rev Assoc Med Bras. 2012. Vol. 58 (2). Р. 204–208.
25. El-Bitar M.A.,Zalzal G.H. Powered instrumentation in the treatment of recurrent respiratory papillomatosis: an alternative to the carbon dioxide laser // Arch Otolaryngol Head Neck Surg. 2002 Apr. Vol. 128 (4). Р. 425–428.
26. Hester R.P., Derkay C.S., Burke B.L., Lawson M.L Reliability of a staging assessment system for recurrent respiratory papillomatosis // Int J Pediatr Otorhinolaryngol. 2003 May. Vol. 67 (5). Р. 505–509.
27. Larson D.A., Derkay C.S. Epidemiology of recurrent respiratory papillomatosis // APMIS. 2010 Jun. Vol. 118 (6-7). Р. 450–454.
28. McMurray J.S., Connor N., Ford C.N. Cidofovir efficacy in recurrent respiratory papillomatosis: a randomized, double-blind, placebo-controlled study // Ann Otol Rhinol Laryngol. 2008 Jul. Vol.117 (7). Р. 477–483.
29. Shikowitz M.J. Comparison of pulsed and continuous wave light in photodynamic therapy of papillomas: an experimental study // Laryngoscope. 1992 Mar. Vol. 102 (3). Р. 300–310.
30. Zeitels S.M., Akst L.M, Burns J.A., Hillman R.E., Broadhurst M.S., Anderson R.R. Office-based 532-nm pulsed KTP laser treatment of glottal papillomatosis and dysplasia // Ann Otol Rhinol Laryngol. 2006 Sep. Vol. 115 (9). Р. 679–685.
31. Lee R.G., Vecchiotti M.A., Heaphy J., Panneerselvam A., Schluchter M.D., Oleinick N.L., Lavertu P., Alagramam K.N., Arnold J.E., Sprecher R..C. Photodynamic therapy of cottontail rabbit papillomavirus-induced papillomas in a severe combined immunodeficient mouse xenograft system // Laryngoscope. 2010 Mar. Vol. 120 (3). Р. 618–624.
Читайте также:

