Вирус размножается в лимфоцитах
Обновлено: 24.04.2024
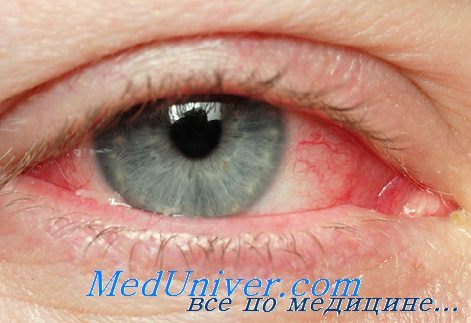
Поражение глаз при инфекционном мононуклеозе
Инфекционный мононуклеоз — острая инфекционная вирусная болезнь подросткового и юношеского возрастов, характеризующаяся лихорадкой, генерализованной лимфоаденопатией, тонзиллитом, увеличением печени и селезенки и появлением в крови атипичных мононуклеаров.
Возбудителем инфекционного мононуклеоза является вирус Эпштейна—Барр (ВЭБ), относящийся к семейству герпесвирусов. Он содержит ДНК, покрыт липидсодержащей оболочкой, обладает тропизмом к В-лимфоцитам. В них он пожизненно персистирует в виде латентной инфекции.
Воротами инфекции является эпителий ротоглотки и слюнных желез. Здесь вирус размножается, выделяется из клеток и проникает в В-лимфоциты, которые разносят его по всему организму. В В-лимфоцитах вирус не размножается, а вызывает трансформирующий эффект, повышая их способность к размножению, что наряду с активацией Т-лимфоцитов, атакующих зараженные В-лимфоциты, ведет к гиперплазии лимфоидной ткани в виде генерализованной лимфоаденопатии, увеличения печени и селезенки. ВЭБ также неспецифически стимулирует различные клоны В-лимфоцитов, что ведет к выработке гетерофильных антител.
Активация Т-лимфоцитов ВЭБ-трансформированными В-лимфоцитами проявляется атипичными мононуклеарами в периферической крови. Лизис ВЭБ-трансформированных В-лимфоцитов Т-киллерами ведет к развитию тонзиллита.
Инкубационный период при инфекционном мононуклеозе продолжается от 4 до 6 нед. Болезнь начинается подостро со слабости, головной боли, болей в мышцах и суставах, боли в горле при глотании, нарушения сна и аппетита, повышения температуры тела до 38—39° С, увеличения заднешейных и шейных боковых лимфатических узлов до 2—3 см. Указанные явления усиливаются в течение 2—4 дней с развитием тонзиллита, генерализованной лимфоаденопатии, увеличения печени и селезенки.
При инфекционном мононуклеозе могут поражаться глаза. Ранними признаками заболевания бывает отек век или периорбитальный отек (у 25—40%), боли в глазных мышцах (у 10—20%), фотофобия (у 5—10%). Часто развивается односторонний или двусторонний конъюнктивит, иногда пленчатый. Описаны дакриоцистит, увеит, неврит зрительного нерва, ретинальные кровоизлияния и экссудаты, хориоретинит.
Выделяют два типа поражения глаз при ЭБВ-инфекции: непосредственная инвазия вируса в глаз и патологические нарушения, связанные с поражением вирусом иннервирующих глаз нервов.
Кровь при инфекционном мононуклеозе характеризуется умеренным лейкоцитозом, относительным и абсолютным лимфоцитозом с наличием 10% и более атипичных мононуклеаров. Диагноз подтверждается наличием гетерофильных антител, выявляемых реакцией Хэнгенуциу-Дейхера— Пауля-Буннеля-Давидсона или реакцией Гоффа-Бауэра.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Разрушение эффекторных клеток иммунитета и макрофагов вирусами. Устранение действия цитокинов вирусами.
Многие вирусы размножаются продуктивно или абортивно в клетках лимфоидной или ретикуло—эндотелиальнои системы, которые, тем самым, участвуют в создании персистентной инфекции. Лимфоциты и макрофаги являются искушающими мишенями для любых вирусов, они разносят вирусы по организму, а также играют ключевую роль в иммунном ответе. Исключительным примером разрушения иммунной системы является вирус иммунодефицита человека, размножающийся в СД4 Т-лимфоцитах и клетках моноцит-макрофагального ряда и вызывающий глубокую иммунную депрессию и гибель от вторичных инфекций или от неоплазий.
Геном цирковируса анемии цыплят кодирует небольшой белок (13 кД), получивший название апотин, который сам по себе вызывает гибель Т-лимфоцитов и рассматривается как важный фактор патогенеза при данной инфекции у цыплят.
Подавление МНС-регуляции антигенной экспрессии
Т-клетки СД8 и СД4 различают вирусные пептиды во взаимодействии соответственно с МНС I, МНС II, а в присутствии вируса концентрация молекул МНС на клеточной поверхности уменьшается. Аденовирусы кодируют ранний протеин, который связывается с вновь синтезированным антигеном МНС I, препятствуя его нормальному процессингу и, тем самым, уменьшает его экспрессию на поверхности клеток.
Бетагерпесвирусы в дополнение к снижению регулирующей экспрессии МНС I исключают лизис хозяинных клеток Тц-лимфоцитами, синтез молекулподобных МНС I, которые действуют как ловушки, защищая от лизиса NK-клетки, которые сами лизируют клетки, не экспонирующие нормальные комплексы с МНС I.

Устранение действия цитокинов
Интерфероны играют важную роль как антивирусные агенты и как иммуномодуляторы. Однако некоторые вирусы содержат гены, которые блокируют антивирусное действие эффекторных молекул.
Избегание нейтрализации антителами (маскирование эпитопов и иммунные ловушки)
Все еще непонятно, каким образом филовирусы, аренавирусы и асфаровиру-сы устойчивы к нейтрализации сывороткой инфицированных людей и животных. Одной из особенностей вируса Эбола является использование иммунных ловушек для избежания нейтрализации; вирус образует 2 гликопротеина, один из которых формирует пепломеры на поверхности вириона, другой, а может быть, тот же самый, производится в большом количестве и секретируется из клеток. Этот белок, вероятно, связывает антитела и тем самым защищает вирус.
Индукция не нейтрализующих антител
Для многих персистентных инфекций характерно присутствие вирус-специфических антител в низком титре при высоком титре антител против не нейтрализуемых эпитопов вируса. В последнем случае комплекс вирус-антитела и вирусный антиген могут накапливаться на базальных мембранах почечных клубочков или в других местах, вызывая различную иммунную патологию или неопластические заболевания.
Например, при многих ретровирусных инфекциях, в том числе при Алеутской болезни норок, не нейтрализующие антитела часто, соединяясь с вирионами, блокируют присоединение нейтрализующих антител. Поэтому при создании новых вакцин против инфекционного перитонита кошек, PC- болезни, вирусной диареи КРС, инфекционной анемии лошадей, артрита-энцефалита коз и др. необходимо учитывать экспрессию естественных недоминантных нейтрализующих эпитопов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Особенности иммунитета при вирусных инфекциях. Патогенез противовирусного иммунного ответа.
Эффективная иммунизация организма против вирусных инфекций тесно связана с их пато- и иммуногенезом. Поэтому рациональное проведение вакцинации, а также максимальная ее эффективность требуют изучения иммунологических и патогенетических основ инфекционного процесса.
Выздоровление от вирусной инфекции обеспечивают, по крайней мере, три феномена:
1) подавление репродукции вируса и нейтрализация инфекционности вирионов;
2) разрушение инфицированных клеток;
3) образование интерферона.
Иммунный цитолиз инфицированных вирусом клеток является существенным фактором в выздоровлении от вирусной инфекции, в основе которого лежат различные процессы, включающие Тц-клетки (антителозависимая, комплементзависимая цитотоксичность). Циркулирующие антитела играют важную роль в выздоровлении от многих генерализованных инфекций (пикорна-, тога-, флави-, парвовирусной и других инфекций). Менее важная роль Т-лимфоцитов связана с тем, что иммунодоминантные Тц-детерминанты часто находятся на консервативных белках, локализованных внутри вириона или на неструктурных вирусных белках, которые находятся только в инфицированных клетках.

При генерализованных инфекциях вирус могут нейтрализовать только те антитела, которые связываются с рецепторами поверхности вириона, которыми они прикрепляются к клетке и блокируют адсорбцию и проникновение вируса в клетку. Некоторые моноклональные антитела, не обладающие нейтрализующей активностью, могут способствовать выздоровлению — предположительно, благодаря антитело-зависимой клеточной цитотоксичности, комплемент-зависимому лизису антителами. В присутствии антител макрофаги могут поглощать и переваривать инфицированные вирусом клетки.
NK-клетки активируются интерфероном или непосредственно вирусными гликопротеинами. Они не обладают иммунологической специфичностью, но преимущественно лизируют клетки, инфицированные вирусом.
Ниже приведены основные примеры стратегии вирусов, направленные на преодоление или снижение иммунологического прессинга со стороны хозяина.
1. Репликация без цитопатогенного действия
Аренавирусы и хантавирусы, например, вызывают хронические инфекции у грызунов без гибели клеток, в которых они размножаются. Инфекция, как правило, не сопровождается заметными изменениями в организме. Ретровирусы также не вызывают изменений в клетках-мишенях, тканях и органах естественных хозяев.
2. Распространение от клетки к клетке путем сплавления мембран
Лентивирусы, морбилливирусы и герпесвирусы (цитомегаловирусы) вызывают слияние клеток, обеспечивая передачу вирусного генома от клетки к клетке и избавляя его от влияния гуморальных иммунных механизмов хозяина.
3. Латентная непродуктивная инфекция непермиссивных клеток
Вирус может размножаться продуктивно в клетках одного типа и вызывать непродуктивную латентную инфекцию в клетках другого типа. Многие герпес-вирусы находятся в латентном состоянии в нервных ганглиях или В-лимфоцитах, но размножаются продуктивно и вызывают острые поражения эпителиальных клеткок слизистых. Пермиссивность клеток может зависеть от стадии дифференциации или активации. Например, папилломавирусы поражают базальные клетки эпителия в начале дифференцировки, но образуют инфекционные вирионы только в полностью дифференцированных клетках вблизи поверхности тела.
4. Частичная экспрессия вирусных генов
Латенция вирусов может поддерживаться ограниченной экспрессией генов, которая может убивать клетки. В течение латентной инфекции некоторые вирусы, такие как герпесвирусы, экспрессируют только ранние гены, которые необходимы для поддержания латенции. В течение реактивации, которую часто стимулирует иммуносупрессия и/или действие цитокинов или гормонов, полный вирусный геном транскрибируется снова. Эта стратегия в течение латентного состояния защищает вирус от всех иммунных механизмов организма.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Обзор
Автор
Редактор
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Исследования в области происхождения злокачественных опухолей, ежегодно уносящих миллионы человеческих жизней, ведутся с XIX века. Работая в области молекулярной вирусологии, Вармус совместно с Дж. М. Бишопом в исследованиях 1970-х гг. сделали открытие, которое по-новому осветило долго остававшуюся дискуссионной проблему этиологии опухолей у человека и животных. Согласно полученным результатам, неконтролируемый рост клеток, образующих опухоль, вызывается не только проникающим в клетку извне онковирусом, но и внутренними процессами в самой клетке. Вармус доказал, что нормальные гены роста клетки вследствие случайных спонтанных мутаций под воздействием химических канцерогенов или, порой, процесса старения могут изменять свою молекулярную структуру и таким образом превращаться в протовирусы онкогенной природы. За открытие клеточного происхождения онкогенных протовирусов Вармус совместно с Дж. М. Бишопом в 1989 г. были удостоены Нобелевской премии по физиологии и медицине [1].
Один из самых распространённых вирусов в человеческой популяции — вирус Эпштейна-Барр (рис. 1) — был открыт и описан в 1964 году двумя английскими вирусологами: Майклом Эпштейном и Ивонной Барр. Вирус Эпштейна-Барр (ВЭБ) — член семейства герпесвирусов [6, 7]. В инфицированных клетках вирусная ДНК, как правило, не встроена в клеточный геном, а находится в ядре в виде замкнутого кольца (эписомы). Биологическое значение интеграции ВЭБ в геном клетки остается неясным. Высказываются предположения, что эписомная ДНК необходима для реализации полноценной репликации ВЭБ, завершающейся формированием вирусных частиц [8].

В отличие от многих других герпесвирусов, вирус Эпштейна-Барр поражает в первую очередь эпителиальные клетки ротовой полости, глотки, миндалин. Здесь он размножается наиболее активно, и поэтому главным путём заражения вирусом являются поцелуи (вот и приехали). Наибольшее количество вирусных частиц находится в клетках эпителия около слюнных желез, и со слюной выделяется большое количество их. Не удивительно, что инфекционный мононуклеоз — самое распространённое заболевание, вызываемое вирусом Эпштейна-Барр, — называют ещё болезнью поцелуев [9].
После первой встречи человека с ВЭБ вирус в незначительном количестве сохраняется в организме хозяина в течение всей жизни. Однако если любой элемент иммунного ответа нарушен, даже незначительное количество ВЭБ-инфицированных клеток может преумножиться колоссально [12].
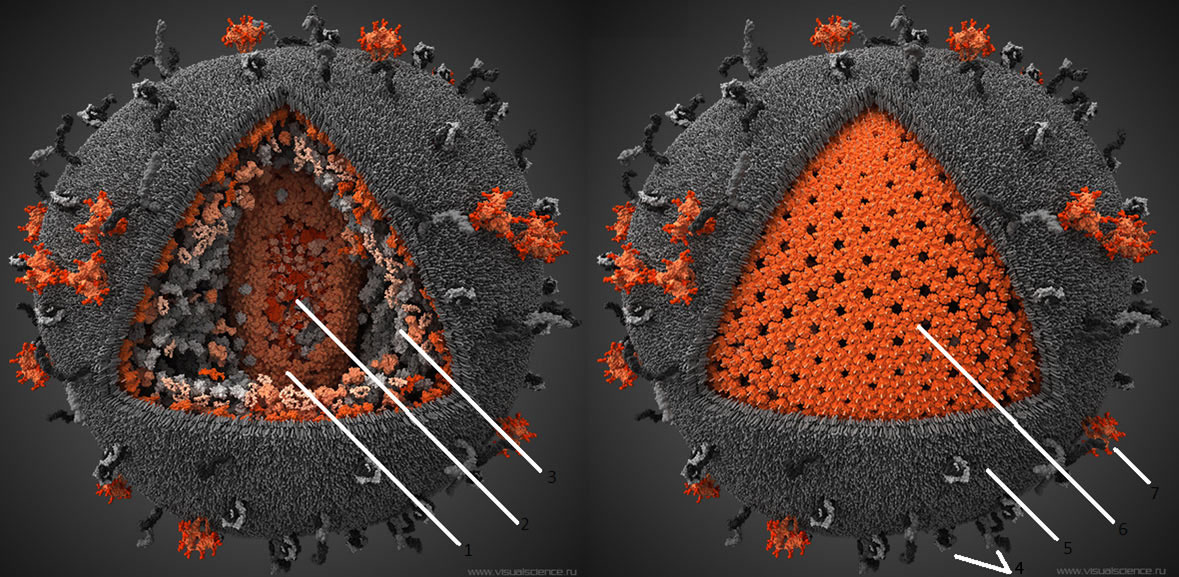
Инфицированные В-клетки могут значительное время находиться в миндалинах, что позволяет вирусу выделяться во внешнюю среду со слюной. С зараженными клетками ВЭБ распространяется по другим органам. В пораженных вирусом клетках возможно два вида развития: литический, приводящий к разрушению клетки-хозяина, и латентный (клетка заражена, но ничего не выдает нахождения вируса), когда число вирусных копий небольшое и клетка не разрушается. ВЭБ может длительно находиться в В-лимфоцитах, эпителии носоглотки и слюнных железах. Кроме того, он способен проникать и в другие клетки: Т-лимфоциты, NK-клетки, макрофаги, нейтрофилы, эпителиоциты сосудов (рис. 2а, 2б) [13].

Злокачественные лимфомы (например, увеличение лимфоузлов), согласно данным Международного агентства по изучению рака, составляют 3–4% среди всех регистрируемых в мире злокачественных новообразований [14]. Лимфомы делят на две основные группы: лимфома Ходжкина (20–30 % всех лимфом) и неходжкинские лимфомы (около 70%) [14, 15].
Неходжикинские лимфомы — это совокупность новообразований, в возникновении которых принимают участие различные агенты [18]. Первая группа — это вирусы, трансформирующие лимфоциты и другие клетки (ВЭБ, HHV-8). Вторая группа представлена факторами различной природы, вызывающими иммунодефицитные состояния. К таким факторам в первую очередь относится ВИЧ (вирус иммунодефицита человека), вызывающий у инфицированного лица подавление иммунитета в результате истощения пула Т-лимфоцитов CD4+ и возникновение СПИДа. В третью группу входят некоторые инфекции, (например, H. pylori), которые увеличивают риск возникновения лимфом на фоне вызываемой ими хронической стимуляции иммунной системы и постоянной активации лимфоцитов [17].
Исследования последних лет свидетельствуют о том, что в патогенезе ВЭБ-ассоциированных патологий чрезвычайно важную роль играет вредный LMP1 — латентный мембранный белок 1, кодируемый одноименным геном (LMP1). Он обладает свойствами онкобелка и функционирует как постоянно активный псевдорецептор. Он способен изменять В-лимфоциты человека [19].
Есть предположение, что аминокислотные замены, накапливающиеся в LMP1, по-видимому, также вносят свой вклад в возникновение опухолей. Механизм этого процесса окончательно не установлен, но предполагается, что усиленный трансформирующий эффект мутированных LMP1 может представлять важную составляющую этого процесса. При этом показано, что различия в последовательности гена LMP1 могут определять агрессивный географически локализованный генотип ВЭБ [21].
Из известных механизмов действия LMP-2 (второй из братьев семейства LMP), расположенного на противоположном конце линейного генома, упоминается лишь способность этих белков совместно повышать сигнальную трансдукцию в ВЭБ (+) клетках [19].
По данным Харальда цур Хаузена, связь между вирусом и раковым заболеванием считается установленной при определении следующих критериев:
- эпидемиологические доказательства того, что вирусная инфекция является фактором риска для развития специфической опухоли;
- присутствие и сохранение генома вируса в клетках опухоли;
- стимуляция пролиферации клеток после введения генома (или его части) вируса в ткани культуры клеток;
- демонстрация того, что геном возбудителя индуцирует пролиферацию и злокачественный фенотип опухоли [19].
Однако канцерогенность ВЭБ далеко не однозначна. Несмотря на то, что кодируемые вирусом продукты способны вызывать пролиферацию инфицированных клеток, ведущую к возникновению лимфом у больных с иммунодефицитом, эти клинически агрессивные опухоли довольно часто поликлональны и подвергаются регрессии при восстановлении иммунного ответа на ВЭБ. Такие опухоли как лимфома Беркитта (ЛБ) и лимфома Ходжкина (ЛХ) встречаются не только в ВЭБ-ассоциированных, но и в ВЭБ-неассоциированных вариантах, что говорит о том, что патогенез этих новообразований связан не только с ВЭБ. Кроме того, злокачественные клетки больных ЛБ и ЛХ отличаются фенотипически от клеток ЛКЛ, полученных под воздействием ВЭБ in vitro, и не экспрессируют ряд белков, необходимых для трансформирующего роста. Эти находки позволяют предположить, что опухолевые клетки могут возникать и под воздействием факторов невирусного происхождения, а также зависеть от различных усиливающих рост клеток стимулов [17].
Лабораторная диагностика ВЭБ-инфекции базируется на цитологическом исследовании крови или костного мозга, серологических исследованиях и ПЦР. С помощью метода ПЦР можно определить ДНК вируса в плазме до клинических проявлений болезни, а репликация вируса в организме является показанием к противовирусной терапии и критерием эффективности проведенного лечения. Материалом для исследования служат слюна или рото- и носоглоточная слизь, соскоб эпителиальных клеток урогенитального тракта, кровь, спинномозговая жидкость, ткани опухоли и костный мозг. Как у больных ВЭБ, так и у носителей может быть получен положительный результат в ПЦР. Поэтому для их дифференцировки проводится количественный ПЦР-анализ для определения количества копий вирусного генома. У маленьких детей (до 1–3-х лет) по причине недостаточно сформированного иммунитета диагностика по антителам затруднительна, поэтому в данной группе пациентов в помощь приходит именно ПЦР. Однако в силу того, что ПЦР-анализ информативен только при размножении (репликации) вируса, то существует и определенный процент ложноотрицательных результатов (до 30%), связанный именно с отсутствием репликации в момент исследования. При этом важно сопоставление результатов клинических, серологических и молекулярных обследований в определении ВЭБ-инфекции, как причины имеющегося заболевания [1].
Специфическая профилактика (вакцинация) против ВЭБ не разработана, но проводятся клинические испытания. Основной проблемой при разработке вакцины является большое отличие в белковом составе вируса на разных фазах его существования. Впрочем, в настоящее время разрабатывается вакцина, которая содержит рекомбинантный поверхностный антиген gp350. После вакцинации первичная инфекция протекает субклинически, но собственно инфицирование человека не предупреждается. Кроме того, вырабатывающиеся нейтрализующие антитела не влияют на течение различных форм латентной инфекции, в том числе опухолей. Профилактические меры сводятся к укреплению иммунитета, закаливанию детей, мерам предосторожности при появлении больного в окружении, соблюдение правил личной гигиены.
Заключение
Широкое распространение ВЭБ с выраженным трансформирующим потенциалом среди населения планеты и редкого возникновения в инфицированной популяции связанных с этим вирусом опухолей с преимущественной их локализацией в определенных географических регионах позволяет сделать важный вывод. Подобно большинству опухолей иной вирусной природы, в патогенезе ВЭБ-ассоциированных новообразований важную роль играют дополнительные факторы, и одного ВЭБ недостаточно для возникновения опухоли. ВЭБ лишь инициирует пролиферацию инфицированных им клеток, а последующие события влияют на гистопатологический спектр возникающих неоплазий. Одним из важнейших факторов, в значительной степени определяющих возникновение ВЭБ-ассоциированных опухолей, служит выраженная иммуносупрессия (врожденная, ятрогенная или индуцированная любой вирусной инфекцией, и в первую очередь ВИЧ), приводящая к утрате функции иммунного распознавания клеток, инфицированных ВЭБ.
Таким образом, несмотря на многолетнее изучение связи ВЭБ с опухолями человека, вопрос о роли вируса в их возникновении до конца не изучен. Раскрытие механизма злокачественной трансформации вирусом, персистирующим в латентном состоянии более чем у 90% населения планеты, — задача чрезвычайно сложная. Однако технические достижения последних лет, существенно повысившие специфичность исследований, позволяют надеяться, что детали ВЭБ-ассоциированного канцерогенеза будут выяснены.

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
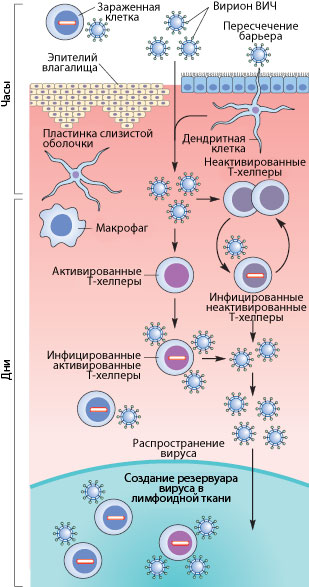
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Читайте также:

