Вирус в крови гемоглобин
Обновлено: 25.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Повышенный гемоглобин, или эритроцитоз: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
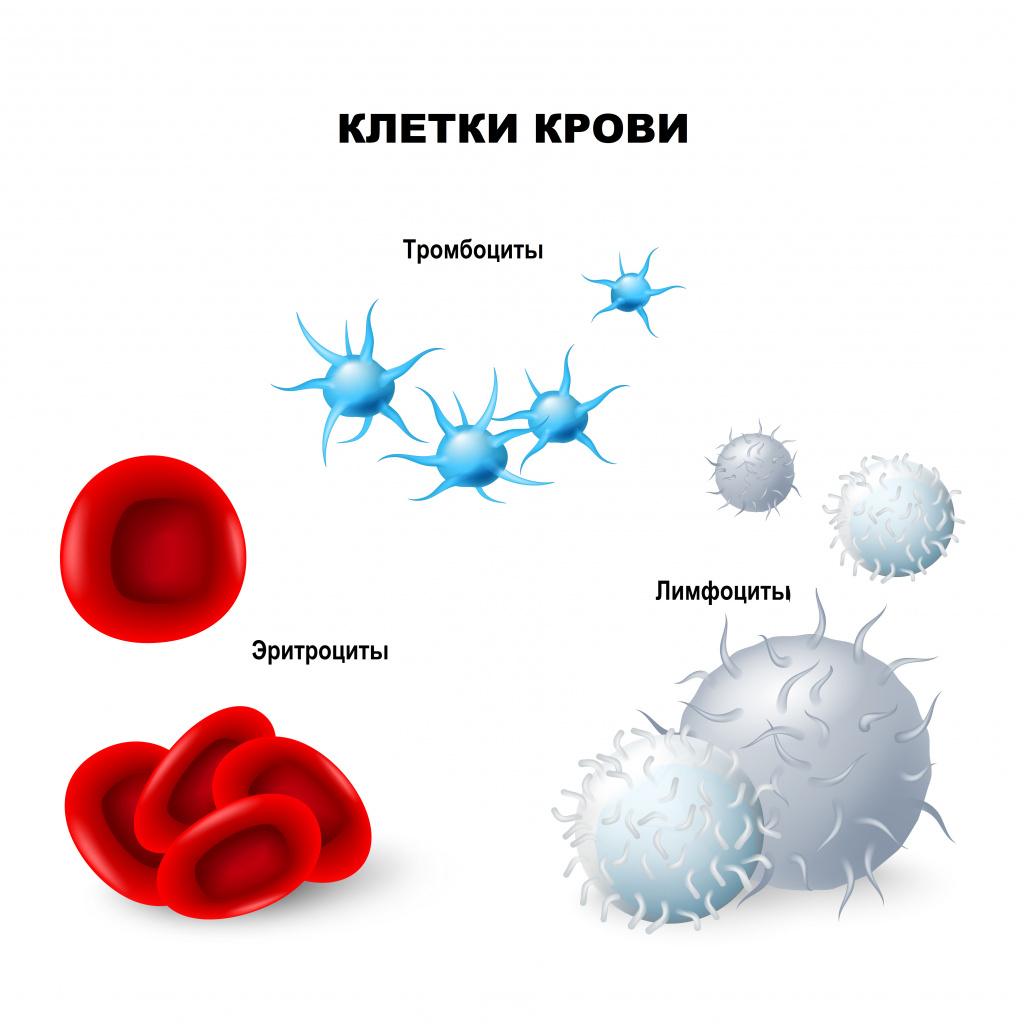
Эритроцитоз – увеличение содержания красных клеток в единице объема крови, сопровождающееся повышением уровня гемоглобина. Основными симптомами этих изменений являются головные, мышечные боли, головокружение, носовые кровотечения, быстрая утомляемость, более специфические симптомы зависят от соответствующего заболевания.
Разновидности эритроцитоза
Эритроцитоз может быть первичным и вторичным.
Первичный эритроцитоз рассматривается как самостоятельное заболевание системы кроветворения и имеет генетическую природу. В медицине он известен как врожденная полицитемия, или болезнь Вакеза. Данная патология провоцирует увеличение объема костного мозга и повышенную выработку эритроцитов и гемоглобина.
Вторичный эритроцитоз не считается отдельным заболеванием, а лишь симптомом острых или хронических болезней и состояний.
Относительный эритроцитоз является следствием обезвоживания организма, вызванного обильной диареей или рвотой.
Также повышение уровня гемоглобина может являться результатом передозировки лекарственных препаратов, курения, злоупотребления алкоголем и воздействия химических веществ (нитритов).
Абсолютный эритроцитоз является следствием усиленного эритропоэза – процесса образования красных кровяных клеток в костном мозге. Эта форма патологии всегда связана с болезнями внутренних органов или систем.
Возможные причины повышения гемоглобина
- Изменение структуры гена Jak2 V617F, отвечающего за выработку красных клеток крови.
- Неспособность крови связывать и переносить кислород к тканям.
- Снижение поступления кислорода к тканям почек (это приводит к тому, что они начинают усиленно вырабатывать гормон, отвечающий за образование эритроцитов (эритропоэтин)).
- Дефицит ферментов, отвечающих за выработку эритроцитов и их функцию переноса кислорода к тканям.
- Заболевания почек (гидронефроз, поликистоз почек, онкологические заболевания и стеноз почечной артерии).
- Заболевания легких (хронический обструктивный бронхит, бронхиальная астма, заболевания, поражающие легочную ткань, иногда неустановленной причины).
- Заболевания сердца (врожденные и приобретенные пороки сердца).
- Заболевания печени (опухоли печени).
- Заболевания головного мозга (в частности, опухоль мозжечка).
- Заболевания женской половой системы (онкологические заболевания яичников).
- Болезни эндокринной системы, поражающие надпочечники и способствующие повышению артериального давления, при которых обычно неэффективны основные препараты, используемые при гипертонической болезни (болезнь Иценко–Кушинга, феохромоцитома), а также заболевания щитовидной железы.
- Отравление угарным газом.
- Пребывание на больших высотах.
- Синдром обструктивного апноэ, характеризующийся временной остановкой дыхания во время сна.
При выявлении увеличения количества эритроцитов, гематокрита, гемоглобина в первую очередь необходимо в максимально короткие сроки обратиться к гематологу.
Для уточнения диагноза может потребоваться проведение стернальной пункции или трепанобиопсии костного мозга.
Исследование пунктатов, полученных из опухолей, предопухолевых, опухолеподобных образований различной локализации: печень, почки, лёгкие, забрюшинные опухоли, опухоли средостения, щитовидная железа, предстательная железа, яичко, яичники, лимфатические узлы, миндалины, мягкие ткани, кости. .
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Повышенный гемоглобин, или эритроцитоз: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Эритроцитоз – увеличение содержания красных клеток в единице объема крови, сопровождающееся повышением уровня гемоглобина. Основными симптомами этих изменений являются головные, мышечные боли, головокружение, носовые кровотечения, быстрая утомляемость, более специфические симптомы зависят от соответствующего заболевания.
Разновидности эритроцитоза
Эритроцитоз может быть первичным и вторичным.
Первичный эритроцитоз рассматривается как самостоятельное заболевание системы кроветворения и имеет генетическую природу. В медицине он известен как врожденная полицитемия, или болезнь Вакеза. Данная патология провоцирует увеличение объема костного мозга и повышенную выработку эритроцитов и гемоглобина.
Вторичный эритроцитоз не считается отдельным заболеванием, а лишь симптомом острых или хронических болезней и состояний.
Относительный эритроцитоз является следствием обезвоживания организма, вызванного обильной диареей или рвотой.
Также повышение уровня гемоглобина может являться результатом передозировки лекарственных препаратов, курения, злоупотребления алкоголем и воздействия химических веществ (нитритов).
Абсолютный эритроцитоз является следствием усиленного эритропоэза – процесса образования красных кровяных клеток в костном мозге. Эта форма патологии всегда связана с болезнями внутренних органов или систем.

Возможные причины повышения гемоглобина
- Изменение структуры гена Jak2 V617F, отвечающего за выработку красных клеток крови.
- Неспособность крови связывать и переносить кислород к тканям.
- Снижение поступления кислорода к тканям почек (это приводит к тому, что они начинают усиленно вырабатывать гормон, отвечающий за образование эритроцитов (эритропоэтин)).
- Дефицит ферментов, отвечающих за выработку эритроцитов и их функцию переноса кислорода к тканям.
- Заболевания почек (гидронефроз, поликистоз почек, онкологические заболевания и стеноз почечной артерии).
- Заболевания легких (хронический обструктивный бронхит, бронхиальная астма, заболевания, поражающие легочную ткань, иногда неустановленной причины).
- Заболевания сердца (врожденные и приобретенные пороки сердца).
- Заболевания печени (опухоли печени).
- Заболевания головного мозга (в частности, опухоль мозжечка).
- Заболевания женской половой системы (онкологические заболевания яичников).
- Болезни эндокринной системы, поражающие надпочечники и способствующие повышению артериального давления, при которых обычно неэффективны основные препараты, используемые при гипертонической болезни (болезнь Иценко–Кушинга, феохромоцитома), а также заболевания щитовидной железы.
- Отравление угарным газом.
- Пребывание на больших высотах.
- Синдром обструктивного апноэ, характеризующийся временной остановкой дыхания во время сна.
При выявлении увеличения количества эритроцитов, гематокрита, гемоглобина в первую очередь необходимо в максимально короткие сроки обратиться к гематологу.
Для уточнения диагноза может потребоваться проведение стернальной пункции или трепанобиопсии костного мозга.
Исследование пунктатов, полученных из опухолей, предопухолевых, опухолеподобных образований различной локализации: печень, почки, лёгкие, забрюшинные опухоли, опухоли средостения, щитовидная железа, предстательная железа, яичко, яичники, лимфатические узлы, миндалины, мягкие ткани, кости. .
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Анемии: причины появления, симптомы, диагностика и способы лечения.
Определение
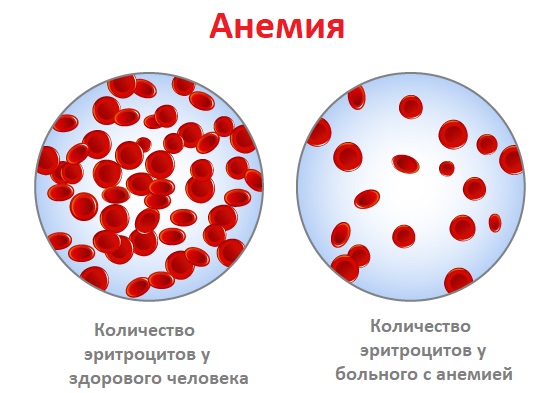
Анемия – это уменьшение содержания гемоглобина и/или снижение количества эритроцитов в единице объема крови, приводящее к снижению снабжения тканей кислородом.
Анемия встречается при ряде заболеваний (язвы и полипы желудочно-кишечного тракта, хроническая болезнь почек, онкологические, инфекционные заболевания, глистные инвазии и др). Чем ниже уровень гемоглобина, тем тяжелее протекает анемия.
Причины появления анемии
Анемия может возникнуть в результате нарушения образования эритроцитов, повышенного их разрушения или потери эритроцитов с кровью.
Статистика утверждает, что самой распространенной является анемия, возникшая после кровопотери (острой или хронической). Острой считается кровопотеря с объемом крови более 500-700 мл (у взрослых), которая происходит в течение короткого промежутка времени. Потеря крови может быть видимой (кровотечение из ран, кровавая рвота, маточное, носовое кровотечения) и первоначально скрытой (кровотечения в кишечник, в полость живота и/или плевры, большие гематомы).
Хронические кровопотери развиваются в результате незначительных, но длительных потерь крови (обильные и длительные менструации, язва желудка, рак, геморрой, проведение процедур гемодиализа и др.). С течением времени незначительные кровопотери приводят к истощению запасов железа в организме, когда количество теряемого организмом железа превышает его поступление с пищей. В результате дефицита железа нарушается синтез гемоглобина.
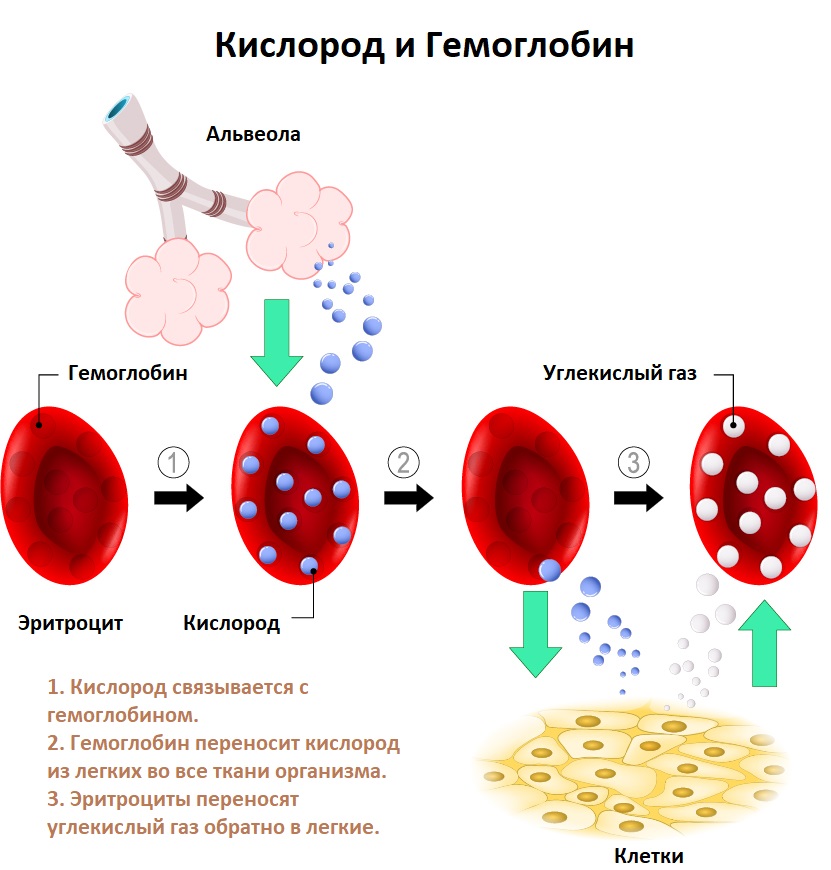
Дефицит железа может возникнуть из-за снижения всасывания железа в результате различных заболеваний двенадцатиперстной кишки и начальных отделов тонкой кишки (энтеритов, опухолей, состояний после оперативных вмешательств на данном участке кишечника). Состояния, приводящие к снижению уровня белков крови, являющихся переносчиками железа (нефротический синдром, нарушение белково-синтетической функции печени, синдром нарушенного всасывания, алиментарная недостаточность), также могут привести к его снижению и, как следствие, к анемии.
Железодефицитные анемии, связанные с исходно недостаточным уровнем железа (недостаток железа у матери в период беременности), наблюдаются у новорожденных и детей младшего возраста.
Анемии вследствие нарушенного кроветворения возникают:
- при недостаточном поступлении в организм или нарушении всасывания в желудочно-кишечном тракте компонентов, необходимых для образования эритроцитов (витамина В6, витамина В12, фолиевой кислоты и др.);
- поражении клеток костного мозга - предшественников эритроцитов токсическими веществами, ионизирующей радиацией;
- образовании вторичных очагов опухолевых клеток в костном мозге (метастазировании);
- нарушении синтеза небелковой части гемоглобина (гема) и накоплении его токсичных продуктов;
- нарушении регуляции образования эритроцитов (уменьшении продукции гормона, стимулирующего рост и размножение эритроцитов (эритропоэтин) или воздействии ингибиторов).
Развитие наследственных гемолитических анемий связано с генетическими дефектами (нарушением активности ферментов эритроцитов, нарушением структуры или синтеза гемоглобина, дефектами мембран эритроцитов).
Приобретенные гемолитические анемии могут быть обусловлены разрушением эритроцитов в результате воздействия на них антител, механических повреждений оболочки эритроцитов, химических повреждений эритроцитов, недостатка витаминов, разрушения эритроцитов паразитами.
Классификация анемий
1. Анемии, связанные с кровопотерей:
- анемии, связанные с нарушением образования гемоглобина;
- анемии, связанные с нарушением синтеза ДНК и РНК;
- анемии, связанные с нарушением процессов деления эритроцитов;
- анемии, связанные с угнетением пролиферации (размножения) клеток костного мозга.
- наследственные гемолитические анемии;
- приобретенные гемолитические анемии.
Существуют общие (неспецифические) проявления анемии и признаки, которые специфичны для определенного вида анемий.
Отсутствие этих признаков не исключает наличие анемии, поскольку при легкой и среднетяжелой форме заболевания, а также его медленном развитии клиническая картина может быть смазанной.
Клинические проявления недостатка железа в организме: сухость кожи, нарушение целостности эпидермиса, ломкость ногтей, волос, изъязвления и трещины в углах рта, мышечная слабость. Может наблюдаться чувство жжения языка, извращение вкуса в виде неукротимого желания есть мел, зубную пасту, землю, сырую крупу, сырое мясо, а также пристрастие к некоторым запахам (ацетона, бензина).
Дефицит витамина В12 также может проявляться поражением желудочно-кишечного тракта (атрофическим гастритом) и неврологической симптоматикой (парестезиями, нарушением чувствительности, онемением конечностей). При крайне тяжелом течении заболевания наблюдаются психические нарушения, бред, галлюцинации, приобретенное слабоумие и др.
Клиническая картина дефицита фолиевой кислоты очень похожа на дефицит витамина В12, но при фолиеводефицитных состояниях отсутствует неврологическая симптоматика и редко возникает воспаление языка. Дефицит фолиевой кислоты приводит к обострению шизофрении, учащению и утяжелению приступов эпилепсии.
Для гемолитических анемий характерны желтушность кожных покровов и слизистых, увеличение размера селезенки, склонность к образованию камней в желчных путях.
При массивном гемолизе эритроцитов (гемолитическом кризе) кроме анемии, желтухи и ухудшения общего состояния могут наблюдаться тошнота, рвота, расстройство сознания, судороги, развитие острой почечной и/или сердечно-сосудистой недостаточности.
При апластической анемии, которая возникает на фоне угнетения пролиферации клеток костного мозга, происходят кровоизлияния (преимущественно в области бедер, голеней, живота, в местах инъекций образуются гематомы). Часто диагностируются бронхиты, пневмонии.
Диагностика анемии
Анемия может возникать под влиянием самых разнообразных факторов. Чаще всего встречаются дефицитные анемии (железодефицитные, B12-дефицитные, фолиеводефицитные и др.).
Большую роль в выявлении причины анемии играют сведения, полученные при опросе пациента: возраст, наличие профессиональных вредностей, характер диеты, наличие сопутствующих заболеваний, прием лекарственных препаратов, информация о наследственности и др. Не менее важны данные осмотра: изменение цвета и состояния кожи; увеличение лимфатических узлов, печени, селезенки; наличие поражения нервной системы.
Первый этап диагностики анемии обычно включает следующие исследования:
-
клинический анализ крови: определение концентрации гемоглобина, количества эритроцитов, лейкоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC), лейкоцитарной формулы и СОЭ (с микроскопией мазка крови при наличии патологических сдвигов);
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
В организме здорового человека уровень железосодержащего белка находится в пределах от 120 до 135 г/л. После того как пациент переболел COVID-19, цифры иногда уменьшаются. Если упал гемоглобин после коронавируса – это типичное осложнение. В статье разберемся, почему развивается анемия, как её диагностировать и лечить.

Программы реабилитации после коронавирусной инфекции

Включает 30 исследований

Включает 29 исследований

Включает 3 исследования
Консультации: ведущего врача превентивной медицины

Включает 32 исследования
Консультации: Смольянинова Е.И.
Причины анемии после КОВИД-19
Пониженный гемоглобин после коронавируса – осложнение, причины которого до сих пор полностью не изучены. В 2020 году после проведенных исследований ученые выдвинули предположение, что инфекция взаимодействует в организме с железосодержащим белком и впоследствии разрушает его. Этот вывод был сделан потому, что в организмах пациентов с анемией был выявлен в большом количестве гем – составная часть гемоглобина. То есть происходил распад вещества, переносящего кислород по телу. Эта версия проверяется.

Проведенные исследования показали, что коронавирусная инфекция действует на компоненты крови таким образом, что в ней в большом количестве появляются мегакариоциты. Их задача – делать красную жидкость густой. Но при КОВИД-19 организму это не нужно. Тело, противодействуя вирусу, начинает совершать ошибки. Эритроцитам труднее перемещаться по густой крови. Возникает гипоксия. Анемия – одно из последствий описанных процессов.
Китайские ученые установили, что работу по обездвиживанию эритроцитов проводит не сам ковид, а белки ORF1ab, ORF10 и ORF3a, которые помогают вирусу закрепиться в организме. Именно они взаимодействуют с клетками, переносящими кислород по телу, лишая их возможности выполнять свои функции. Проще говоря, у инфекции есть помощники в деле разрушения человеческого организма.
Как распознать анемию после коронавируса
После ковида низкий гемоглобин у взрослого человека и ребенка выявляют по нескольким признакам:
- Сонливость и снижение работоспособности. Этот симптом характерен и для коронавируса без анемии.
- Нарушение концентрации.
- Появление проблем с памятью.
- Мышечная слабость. Ее часто списывают на обычную усталость. Если симптом держится долго, то это, скорее всего, проявление анемии.
- Головные боли.
- Выпадение волос.
- Ломкость ногтей.
- Окрашивание кожных покровов в бледно-желтый цвет.
- Ощущение жжения на языке. Вкусовые рецепторы начинают работать иначе.
- Сбой менструального цикла у женщин.
- Частая смена настроения.
- Ощущение недостатка витаминов. Это может проявляться в том, что пациенту хочется каких-то фруктов или овощей, например: лимонов, граната, клубники.
- Шум в ушах.
- Мушки перед глазами.
- Нарушение координации.
- Боли в сердце.
Это всё признаки анемии, как и низкий уровень гемоглобина. Название патологии и малое количество указанного вещества часто отождествляют. Также железодефицитная анемия может сопровождаться регулярной потерей сознания.
Необязательно, чтобы все многочисленные симптомы проявлялись вместе и сразу. Если несколько признаков присутствует, то это повод обеспокоиться и записаться на диагностику. Обследование можно пройти в медицинском центре La Salute.
Способы диагностики
Чтобы назначить лечение, врачу необходимо изучить результаты ряда исследований:
- общие клинические анализы;
- определение количества эритроцитов в крови и гемоглобина;
- выявление числа ретикулоцитов – предшественников клеток, названных в предыдущем пункте, появляющихся в процессе кроветворения;
- определение СОЭ;
- диагностика, направленная на установление гематокрита (выясняют, сколько красных кровяных телец находится в организме, в общем объеме);
- анализ по определению того, сколько гемоглобина в эритроците;
- выявление ферритина (если его уровень снижается в крови, это значит, что имеет место воспалительный процесс);
- диагностика числа лейкоцитов и тромбоцитов.
Не стоит опасаться, что назначается так много анализов. Количество заборов крови минимальное. По полученным в лаборатории результатам доктор может выявить эритроцитоз или анизоцитоз – проблемы с красными тельцами в организме.
Падение уровня гемоглобина и последующее возникновение анемии врачу помогает определить предварительный осмотр пациента. Медики принимают во внимание все признаки, о которых речь шла выше. Например, пожелтение кожных покровов. С помощью пальпации врач может определить, что увеличена селезенка. Также доктор проводит опрос больного, чтобы установить клиническую картину. Врача интересует: есть ли слабость в теле, терял ли пациент сознание и так далее.
Анемия ведет к тому, что уровень кислорода, переносимого кровью, падает. Это сказывается на работе внутренних органов. Пациентам назначают:
- фиброгастродуоденоскопию – изучают слизистую пищевода, стенки желудка, двенадцатиперстной кишки;
- УЗИ печени;
- исследование внутренних половых органов у женщин;
- УЗИ почек;
- рентген легких;
- компьютерную томографию.
Все виды описанных исследований проводятся в медицинском центре La Salute.

Железодефицитная анемия (IDA) и анемия хронических заболеваний (АСD) являются двумя наиболее распространенными причинами анемии во всем мире. Анемия может наблюдаться у 95% пациентов в критическом состоянии. Анемия имеет клиническое значение у пациентов в критическом состоянии, поскольку она связана с заболеваемостью и смертностью. Вследствие анемии до 40% пациентов получают переливание эритроцитарной массы во время пребывания в отделении интенсивной терапии. У пациентов с COVID-19 сообщалось о связи между статусом железа и риском неблагоприятных исходов, что свидетельствует о том, что пациенты с низким уровнем железа в сыворотке крови и другими показателями железодефицитной анемии, вероятно, будут страдать от тяжелых состояний при COVID-19. В другом исследовании было показано, что распространенность анемии высока (49%) у госпитализированных пациентов с COVID-19. Причина анемии часто связана с ограниченной доступностью железа (IDА) или нарушением обмена железа из-за воспалительного процесса (ACD). При IDA ферритин, насыщение трансферрина и ZnPP обычно являются достоверными маркерами запасов железа в организме. Снижение уровня ферритина ниже 30 нг/мл и уровней ZnPP выше 40 мкмоль/моль гема свидетельствует об абсолютной IDA. Из-за воспалительного статуса ACD связан со снижением уровня гемоглобина и железа, снижением насыщения трансферрина, но повышением уровня ферритина, а также повышением уровня CRP, IL-6 и гепсидина.
Причина анемии у пациентов в критическом состоянии связана со многими причинами, такими как дефицит питательных веществ, кровопотеря или воспаление. Железодефицитная анемия, определяемая снижением содержания железа в организме, является одной из основных нутритивных причин анемии и обычно развивается, когда всасывание пищевого железа в кишечнике не может компенсировать повышенную потребность в железе или потерю крови.
Анемия хронического заболевания также известна как функциональная железодефицитная анемия. ACD имеет более сложную патофизиологию и обусловлена различными клиническими состояниями, такими как инфекции и воспалительные заболевания, и , в частности , воспалительными цитокинами. Ее обычно определяют как перераспределение железа из ключевых мест его использования в места хранения, что приводит к снижению доступности железа, а не к абсолютному дефициту железа. Это приводит к внезапному возникновению анемии у пациентов в критическом состоянии.
При ковиде часто наблюдается анемия, особенно , у пациентов в критическом состоянии, таких как больные COVID-19. Например, Bellman-Weiler et al. показали, что Почти 25% больных здесь страдали анемией с высоким коэффициентом анемии воспаления. В том же цитируемом исследовании авторы указали, что анемия в значительной степени связана с внутрибольничной смертностью.
Часто IDA и АCD сосуществуют, что затрудняет интерпретацию показателей эритроцитов и параметров статуса железа. Однако дифференциация между обоими патологическими процессами важна для постановки диагноза и лечения. Диагноз IDA основывается на множестве лабораторных биомаркеров, связанных с метаболизмом железа, таких как гемоглобин, ферритин, растворимый рецептор трансферрина, протопорфирин цинка (ZnPP) и гепсидин. Нарушение регуляции гомеостаза железа по-разному влияет на эти биомаркеры. Наиболее важным является взаимодействие между дефицитом железа и воспалением. На многие биомаркеры влияет не только дефицит железа, но и воспаление; таких как ферритин - хорошо известный? как белок острой фазы. Однако было показано, что ZnPP менее чувствителен к воспалительному статусу.
У пациентов с COVID-19 затронуты некоторые маркеры железа. Появляется все больше доказательств того, что анемия также присутствует у пациентов с COVID-19 из-за общепринятых патофизиологических механизмов, возникающих у пациентов в критическом состоянии. Однако, судя по недавним публикациям, есть указания на возможные специфические взаимосвязи между патологиями крови и COVID-19, предполагающие сильное участие эритроцитов в патофизиологии COVID-19. Отмечено, что повышенные уровни ZnPP указывают на дефицит железа у пациентов с анемией с диагнозом COVID-19. Существует тесная связь между повышенными уровнями ZnPP и тяжестью заболевания и что отношение ZnPP/лимфоцитов (ZnPP/L) может иметь потенциал для прогнозирования тяжести COVID-19, особенно оцениваемого в первые пять дней. при поступлении больных в стационар.
Анемия хронического воспаления при ковиде
Многие из описанных в настоящее время изменений у пациентов с COVID-19 подтверждают развитие ACD. Уже в начале пандемии COVID-19 сообщалось об изменениях уровня гемоглобина. В ретроспективном исследовании делается вывод, что более низкие уровни гемоглобина при поступлении связаны с более неблагоприятным прогнозом. Сообщается, что анемия и нарушение гемостаза железа широко распространены у госпитализированных пациентов с COVID-19. Однако, как сообщалось, тяжесть заболевания не влияла на уровень гемоглобина . В недавнем систематическом обзоре и метаанализе Taneri et al. показали, что уровни гемоглобина были ниже у пожилых людей с диагнозом COVID-19. В одном исследовании 39% пациентов страдали анемией. В другом ретроспективном исследовании наблюдались более высокие значения 68%. На основании низкого уровня гемоглобина и высокого уровня ферритина было подсчитано, что более 56% случаев анемии у пациентов с COVID-19 связаны с АСD. В этом контексте наблюдаемое улучшение респираторных симптомов при приеме EPO ( эритропоэтина ) можно рассматривать как влияние на метаболизм железа . С другой стороны, было предложено использовать лишение железа в качестве многообещающего адъювантного терапевтического средства против выживания вируса. Это основано на потребности вируса в железосодержащих ферментах для завершения процесса репликации. Что касается нарушения метаболизма гемоглобина, то острый респираторный дистресс-синдром является одной из критических стадий COVID-19, приводящей к поражению легких и гемолизу. Это приводит к низкому уровню оксигенации, повышению уровня свободного железа и снижению активности гемоксигеназы-1 (HO-1). На основании этого наблюдения предполагается, что Hb, HO-1 и перегрузка железом являются возможными мишенями для лечения COVID-19 .
Ферритин
В недавней статье сообщается о чрезвычайно высоких уровнях ферритина у пациентов с COVID-19 в целом и особенно при гемодиализе. Эти повышенные уровни ферритина связаны с тем, что ферритин одновременно является маркером воспаления и статуса железа. Таким образом, увеличение в первую очередь связано с воспалением, связанным с инфекцией, что подтверждается аналогичным увеличением белков острой фазы СRP и IL-6 в этом и родственных исследованиях. Однако уровни ферритина у этих пациентов не коррелировали с классическим острофазным белком СRP. Это может указывать на то, что в данном случае ферритин указывает на изменение метаболизма железа. Однако предполагалось, что ферритин может также функционировать как сигнальная молекула как прямой медиатор иммунной системы.
Гепсидин
Недавно гепсидин был введен в качестве диагностического биомаркера для дифференциации между IDA и ACD, который находится в пределах нормы при IDA/ACD и повышен только при IDA, что указывает на ограничение железа в отношении супрессивного сигнала . У пациентов с COVID-19 повышенный уровень гепсидина предсказывал тяжесть течения COVID-19 . Несмотря на то, что уровни гепсидина были значительно выше у пациентов с тяжелым поражением, даже в сочетании с коэффициентом числа лимфоцитов гепсидин имел низкую прогностическую ценность. Эти различия касающимися ферритина или гепсидина, вероятно, объясняются неоднородностью пациентов, такой как сопутствующие заболевания пациентов и исходные демографические данные.
Протопорфирин цинка
Различные исследования идентифицировали ZnPP как биомаркер IDA, на который не влияют или мало влияют сопутствующие острые воспаления. Было показано, что при ACD ZnPP обнаруживает и количественно оценивает нарушения метаболизма железа, связанные с хроническими воспалительными заболеваниями, а также помогает контролировать успех терапии железом хронических воспалительных заболеваний. Диагностическая ценность ZnPP как индикатора IDА у госпитализированных пациентов показала, что ZnPP имеет относительно более высокую степень диагностической эффективности лучше, чем железо и ферритин для данной популяции пациентов. Таким образом, было предложено использовать ZnPP в качестве инструмента скрининга IDA у госпитализированных пациентов.
Возможность использования ZnPP в качестве биомаркера была подтверждена, особенно в условиях ограниченных ресурсов, в которых IDА часто связана с другой причиной воспаления. Когда эритропоэз становится железодефицитным, включение цинка вместо железа в протопорфирин-IX опосредуется эритроидным ферментом феррохелатазой. Повышенное соотношение ZnPP/гем указывает на IDА и наблюдается при различных формах анемии, таких как IDА и АCD. Можно подчеркнуть, что ZnPP является экономически эффективным и простым для анализа биомаркером для дефицита железа (ID), особенно в условиях стационара, если используется прямое измерение в капле капиллярной цельной крови вместо сложной экстракции из крови и последующего анализа HPLC.
Читайте также:

