Вирус вич нобелевская премия
Обновлено: 23.04.2024
Проведя тщательный анализ этого образца, группа ученых во главе с Майклом Уороби (Michael Worobey) из университета Аризоны показала, что этот мужчина был инфицирован ВИЧ — вирусом, вызывающим синдром приобретенного иммунодефицита.
При жизни ни сам мужчина, ни его лечащие врачи об этом не знали. Формально вирус будет открыт лишь 17 лет спустя.
Извлекая крошечные генетические фрагменты из образца ткани, команда Уороби практически полностью реконструировала геном ВИЧ в том виде, в котором он существовал в те годы. А сама работа ученого помогла пролить свет на возникновение того, что станет причиной одной из самых важных пандемий в истории человечества.
В погоне за образцами
Вирус иммунодефицита человека был выявлен в 1980-х, после того как таинственный новый синдром затронул жителей США, и, как казалось, тогда он появился из ниоткуда. На самом деле эпидемия зародилась за несколько десятилетий до этого, просто на совсем другом континенте. В Африке.
Теперь мы можем с уверенностью утверждать, что по мере распространения геном вируса претерпевал постоянные изменения: сравнивая накопившиеся мутации и оценивая время, за которое они произошли, ученые могут проследить историю эволюции вируса вплоть до самого момента возникновения.
по теме

Общество
Наиболее вероятное место его появления — южный Камерун. А приблизительное время — 1920-е годы. Именно там и тогда вирус от шимпанзе перешел к человеку, перед тем как вскоре перебраться в город, известный в наше время как Киншаса.
В густонаселенном и быстрорастущем регионе с множеством потенциальных реципиентов вирус и обосновался, чтобы затем распространиться по всему миру.
Очевидно, что огромное количество людей тогда было инфицировано ВИЧ еще прежде, чем кто-то узнал о его существовании. Образцы тканей некоторых из погибших сохранились до наших дней: они рутинно собирались для исследований патологоанатомами, обрабатывались химическим фиксатором, располагались на восковых подложках, изучались под микроскопом (скорее всего, безрезультатно), а затем отправлялись в хранилище.
Но поскольку вирус до своего появления на Западе не был идентифицирован, определить заранее, какой именно образец ткани, взятый в то время, может содержать его следы, невозможно. Искать следы вируса в таких условиях — все равно что искать иголку в тысяче стогов сена.
Более того, процесс обработки химическим фиксатором и условия хранения образцов, дошедших до нашего времени, были таковы, что негативно влияли на содержащиеся в них РНК — молекулы, составляющие геном ВИЧ.
Вирус ВИЧ под микроскопом. Компьютерная Модель.
Однако нет ничего странного в том, что за два десятилетия поисков ученым удалось найти лишь два образца со следами вируса, собранных в Киншасе в период до его открытия.
Дэвид Хо (David Ho) из университета Рокфеллера (Rockefeller University) нашел следы вируса в образце крови, взятой в 1959 году; Уороби обнаружил их в кусочке лимфатического узла из 1960 года.
В обоих случаях от молекул РНК в целом сохранилось около одного процента. Но даже этих крошечных кусочков оказалось достаточно, чтобы доказать: именно ВИЧ блуждал по Киншасе за десятилетия до его открытия, а также чтобы наметить основные вехи истории его эволюции.
В то же время, ввиду ненадежности фрагментарных свидетельств, Уороби хотел собрать геном полностью. Целиком.
Его коллеги Софи Грисилс и Том Уоттс (Sophie Gryseels and Tom Watts) для этого разработали более точную технологию извлечения РНК и применили ее к более чем 1600 образцам тканей из Университета Киншасы (University of Kinshasa). И один из них, как оказалось, действительно содержал следы вируса.
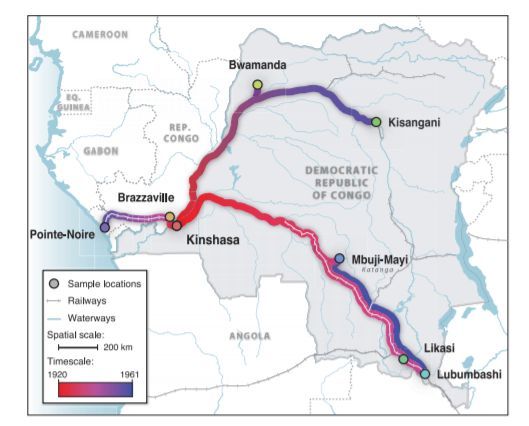
Скрытая эпидемия. Пути распространения ВИЧ в Африке до того, как вирус попал в США.
Место и время
Извлеченные образцы оказались больше всего похожи на подтип С, наиболее распространенный тип ВИЧ в Африке. Тот, что и сейчас доминирует в южной части континента.
На поверку генетический материал, попавший в руки ученых, является лишь малой частью того разнообразия, которое существовало в Киншасе в 1960-е.
А стало быть, из всех подтипов вируса лишь некоторые из тех, что в то время можно было обнаружить в городе, вырвались наружу, дабы стать общемировой проблемой.
История ВИЧ в датах
1930-е
Исследователи полагают, что приблизительно в 1930-х некая форма вируса иммунодефицита обезьян (SIV) перебралась к людям во время разделки или поедания мяса шимпанзе в Демократической Республике Конго. Этот вирус стали называть ВИЧ-1, и это самый распространенный тип вируса на сегодняшний день.
1959
Первый известный случай заболевания СПИДом выявлен при исследовании образцов плазмы крови мужчины, умершего в Демократической Республике Конго в 1959 году.
1960-е
ВИЧ-2, ареал распространения которого ограничен западной частью Африки, перешел к людям от обезьян вида дымчатый мангобей в Гвинее-Бисау в 1960-х.
Генетический анализ вируса, проведенный в 2003 году, говорит, что именно этот тип, вероятно, впервые перебрался в Соединенные Штаты примерно в 1968 году.
1970-е
На протяжении 1970-х вирус, оставаясь незамеченным, продолжает распространяться по США и остальному миру, начинается эпидемия.
1981
Высокая распространенность двух редких заболеваний — саркомы Капоши и пневмонии — отмечена среди молодых гомосексуальных мужчин в Нью-Йорке и Калифорнии в США. Это первый задокументированный случаи СПИДа. К концу года уже 121 человек умер от таинственного заболевания.
1982
Ученые центра по контролю и профилактике заболеваний (Centers for Disease Control and Prevention, CDC) в Атланте, США, предположили, что нарушение работы иммунной системы среди гей-сообщества вызвано инфекционным заболеванием. Они ввели термин Синдром приобретенного иммунодефицита (СПИД) и установили, что помимо геев в группу риска входят потребители инъекционных наркотиков, люди гаитянского происхождения и больные гемофилией. К концу 1982 года СПИД был обнаружен на пяти континентах.
1983
Эпидемия СПИДа бурно развивается в Европе: в первую очередь среди гей-сообщества, а также среди людей, имеющих тесные связи с центральной Африкой.
Начинается расследование случаев СПИДа в Руанде, Заире и других африканских странах.
1984
Используя недавно разработанные техники, в ходе нескольких исследований независимо друг от друга Люк Монтанье (Luc Montagnier) из Института Пастера в Париже (the Pasteur Institute in Paris), Франция, и Роберт Галло (Robert Gallo) из Национального института раковых заболеваний (the National Cancer Institute) в Вашингтоне, округ Колумбия, США, обнаруживают ретровирус, ответственный за развитие заболевания, известного как СПИД. Позднее он будет назван вирусом иммунодефицита человека (ВИЧ).
Случаи заболевания СПИДом все чаще начинают появляться в среде гетеросексуалов.
1985
В Атланте, США, проведена первая конференция, посвященная проблемам СПИДа.
Вслед за прошлогодним открытием вируса на рынке появляется первый метод тестирования на ВИЧ, одобренный Управлением по контролю за продуктами и лекарствами США (US Food and Drug Administration, FDA).
В США начинается тестирование крови в донорских пунктах.
1987
Азидотимидин (AZT), также известный как Зидовудин, первый противовирусный препарат, становится доступным для лечения ВИЧ после клинических испытаний. Препарат работает, блокируя действие обратной транскриптазы фермента ВИЧ, не давая вирусу размножаться в клетках. AZT замедляет развитие СПИДа, отдаляя смерть.
К 1987 году 16908 человек умерли от СПИДа в США. Всего Всемирная организация здравоохранения (ВОЗ) сообщила о 71571 случае заболевания СПИДом, из которых 47022 — в США.
По оценкам Всемирной организации здравоохранения, по всему миру носителями ВИЧ являются от 5 до 10 миллионов человек, ВОЗ запускает глобальную программу по борьбе со СПИДом.
1988
ВОЗ объявила 1 декабря всемирным днем борьбы с ВИЧ/СПИДом.
1991
Красная лента стала международным символом борьбы с ВИЧ/СПИДом.
1992
В США СПИД вышел на первое место среди причин смертности мужчин в возрасте от 24 до 44 лет.
Первые комбинированные лекарственные препараты для лечения ВИЧ появляются на рынке, после того как FDA наряду с AZT одобрило использование Zalcitabine (ddC), который также блокирует обратную транскриптазу.
Комбинированные препараты против ВИЧ оказываются более эффективными, а комплексное лечение замедляет развитие лекарственной резистентности.
1994
Использование AZT для предотвращения передачи ВИЧ от матери ребенку во время беременности рекомендовано в США. Исследование показало, что подобная терапия снижает шанс передачи вируса во время беременности до 8 %, в контрольной группе вероятность передачи составляла 25 %.
Через 12 лет после открытия вируса правительство США впервые запускает кампанию в медиа по пропаганде использования барьерных контрацептивов.
1995
ВОЗ объявила о достижении количеством зараженных миллионной отметки, всего же с начала эпидемии ВИЧ вирусом заразились более 19,5 миллиона человек.
1996
Международная инициатива по вакцинации против СПИДа (IAVI) — некоммерческая организация, базирующаяся в Нью-Йорке, — создана для ускорения поиска вакцины против ВИЧ.
90 % всех заболевших теперь проживают в развивающихся и развитых странах.
1997
Впервые благодаря появлению ВААРТ отмечено резкое падение смертности от СПИДа.
ООН объявляет, что к 2010 году 40 миллионов детей могут потерять одного или обоих родителей из-за СПИДа.
1998
Первые полномасштабные испытания вакцины против ВИЧ начинаются в США.
Две команды исследователей начинают разработку вакцин против штаммов ВИЧ, распространенных в странах Африки к югу от Сахары
В Сан-Франциско обнаружен штамм ВИЧ, устойчивый ко всем лекарственным средствам, подавляющим протеазу, которые в то время существовали на рынке. У некоторых пациентов, использующих для лечения ингибиторы протеазы, встречаются необычные побочные эффекты, такие как рост жировых отложений и проблемы с сердцем.
1999
33 миллиона человек инфицированы ВИЧ, а 14 миллионов умерли от СПИДа по всему миру.
СПИД становится одним из четырех самых массовых убийц современности.
2001
Индийская компания начинает продавать копии дорогих запатентованных лекарств против СПИДа через медицинскую благотворительную организацию в Африке. Этот шаг заставляет некоторые фармацевтические компании снижать цены.
2003
5 миллионов новых случаев СПИДа выявлены на протяжении 2003 года — самое большое количество с начала эпидемии. 3 миллиона человек умерли от СПИДа в этом же году.
2005
Около 40 миллионов человек инфицированы ВИЧ по всему миру.
Высокорезистивный штамм вируса, вызывающий быстрое развитие СПИДа, обнаружен в Нью-Йорке, США.
По оценкам ученых, сам ВИЧ возник где-то между 1896 и 1905 годом. Далеко не все вирусы так молоды. Когда ученые впервые обнаружили следы гепатита B времен Бронзового века, они подсчитали, что вирус менялся в 100 раз медленнее, чем предполагалось до этого. Открытие кардинально изменило предполагаемый период его возникновения. Даже ВИО (вирусы иммунодефицита обезьян), ближайшие родственники ВИЧ, поражающие шимпанзе, эволюционировали с разной скоростью в далеком прошлом и в новейшей истории, что делает оценку времени возникновения очень сложной.
В целом именно благодаря этому факту статистическими методами ученым удалось достаточно точно локализовать время и место начала пандемии. Установить, что с 1920-х годов именно Киншаса, ныне столица Демократической Республики Конго, стала центром первого очага эпидемии ВИЧ, а также положила начало эпидемии 1960-х годов в других частях континента.
Отсюда, из Киншасы, вирус прибыл на Гаити примерно в 1964 году. Причиной тому стало возвращение на родину жителей этого островного государства. До середины 60-х многие жители Гаити работали в только что получившем свою независимость Конго в качестве специалистов. И значительная часть гаитянских работников проживала именно в Киншасе.

Миграция из Гаити в США. Вторая половина 60-х тут наблюдается резкий рост. ВИЧ попадет в США именно в этот период.
Уже с Гаити вирус вместе с мигрантами перебрался на материк — в Соединенные Штаты Америки. Где очень быстро распространился среди гомосексуалов, воспользовавшись относительной уязвимостью перед ВИЧ именно этой группы.
Первые смерти от симптомов, крайне похожих на СПИД, будут зафиксированы здесь (преимущественно среди афроамериканских геев) уже в конце 60-х. Накануне знаменитых Стоунвольских бунтов, органично связанных с борьбой за права черного населения Америки и ставших отправной точкой эмансипации ЛГБТ-движения, завершившегося нынешней либерализаций законодательства относительной однополых браков и партнерств практически во всех западных странах.
Работа Уороби подтвердила эти и некоторые другие тезисы. Не на моделях, а на реальном генетическом материале.

Новость
Вирусы — неотъемлемый компонент живой природы, однако бороться с ними — дело благородное. По крайней мере, в случае ВПЧ и ВИЧ.
Автор
Редакторы
6 октября 2008 года Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Гарольду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки, и Франсуазе Барре-Синусси и Люку Монтанье за открытие вируса иммунодефицита человека.
Лауреаты
Гарольд цур Хаузен (Harald zur Hausen), родился в 1936 г. в Германии, на настоящий момент гражданин Германии, доктор медицины в Университете Дюссельдорфа. Заслуженный профессор и бывший заведующий и директор по науке Немецкого ракового центра в Гейдельберге.
Франсуаза Барре-Синусси (Françoise Barré-Sinoussi), родилась в 1947 г. во Франции, на настоящий момент гражданка Франции, кандидат наук (PhD) в области вирусологии. Профессор и директор подразделения ретровирусных инфекций Института Пастера в Париже. Кстати, Франсуаза стала восьмой женщиной в истории, удостоенной Нобелевской премии.
Люк Монтанье (Luc Montagnier), родился в 1932 г. во Франции, на настоящий момент гражданин Франции, кандидат наук (PhD) в области вирусологии. Почётный профессор и директор Мирового сообщества по изучению и предотвращению СПИДа в Париже.
Открытие вирусной природы рака шейки матки
Вопреки существовавшим в 1970-х представлениям о природе раковых заболеваний, Гарольд цур Хаузен (Harald zur Hausen) постулировал, что развитие рака шейки матки (по крайней мере, в некоторых случаях) связано с папилломавирусом человека (ВПЧ). Он предположил, что если опухолевые клетки содержат онкогенный вирус, то их геном должен включать и вирусную ДНК. Следовательно, активность вирусных генов, инициирующих злокачественный рост, может быть обнаружена при помощи специальных ДНК-тестов, ориентированных на вирусный генетический материал. Цур Хаузен более десяти лет продвигал свою идею и занимался поиском различных типов ВПЧ-инфекции, что затруднялось, в частности, тем обстоятельством, что вирусная ДНК лишь частично внедрялась в хромосомы хозяина (человека). В 1983 году ему удалось обнаружить ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16. Годом позже он клонировал ДНК ВПЧ-16 и ВПЧ-18 в пациентах, больных раком шейки матки. Эти типы вируса обнаруживаются примерно в 70% случаях рака шейки матки.

Рисунок 1. Вирус папилломы человека (ВПЧ). ВПЧ содержит двуцепочечную кольцевую молекулу ДНК, заключённую в капсид. Всего известно >100 видов ВПЧ. ВПЧ-16 и ВПЧ-18 являются причиной 70% случаев рака шейки матки.
Значение исследований вируса папилломы
Исследования Гарольда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые более чем в 95% случаев позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18. Это лечение позволит сократить объем хирургического вмешательства и в целом снизить угрозу, представляемую раком шейки матки.
Открытие ВИЧа
В 1981-м появились медицинские описания новой формы синдрома иммунодефицита. Франсуаза Барре-Синусси (Françoise Barré-Sinoussi) и Люк Монтанье (Luc Montagnier) выделили и исследовали культуры лимфатических клеток людей, которым был поставлен диагноз начальной формы приобретённого иммунодефицита. В этих культурах им удалось обнаружить следы работы фермента обратной транскриптазы — прямого свидетельства инфекции ретровирусом и его репликации в заражённых клетках. Кроме того, они обнаружили непосредственно ретровирусные частицы, отпочковывающиеся от заражённых клеток. Выделенный вирус — получивший название вируса иммунодефицита человека (ВИЧ) — заражал и убивал лимфоциты как здоровых, так и больных людей, а также реагировал с антителами инфицированных пациентов. По сравнению с уже известными на тот момент канцерогенными вирусами, ВИЧ не вызывал неконтролируемой пролиферации клеток; вместо этого он использовал активацию клеточного метаболизма Т-лимфоцитов для собственного размножения. Этот факт позволил объяснить причину приобретённого иммунодефицита, поскольку Т-клетки выполняют очень важную роль в иммунной защите. К 1984 году Барре-Синусси и Монтанье уже имели несколько образцов нового человеческого ретровируса (который они отнесли к подгруппе лентивирусов), полученных из пациентов, заразившихся половым путём, при переливании крови или больных от рождения (в случае, когда инфекция передаётся от матери к ребёнку). Значение проделанной ими работы трудно переоценить, учитывая почти повсеместное распространение ВИЧа и эпидемию СПИДа, охватившую почти 1% населения Земли.

Значение исследований вируса иммунодефицита
ВИЧ стал причиной глобальной пандемии. Никогда прежде медицина и наука не реагировали на угрозу так же быстро, идентифицируя причину нового заболевания и предлагая методики лечения. Пусть не совершенные, на сегодня они обеспечивают практически такую же среднюю продолжительность жизни пациентов, как и у здоровых людей. Многочисленные разработки в области вирусологии этой инфекции всё-таки позволяют надеяться, что однажды человечество сможет полностью победить вирус иммунодефицита.

Обзор
Автор
Редактор
Предполагала ли маленькая итальянская девочка из интеллигентной еврейской семьи Рита Леви, учась в гимназии для молодых особ, что судьба подготовила для нее статус старейшего лауреата Нобелевской премии по физиологии и медицине? Вряд ли. Под большим вопросом был даже факт ее будущей принадлежности к науке. Тем не менее, преодолев все многочисленные преграды, она добилась мирового признания итальянской науки — несмотря на то, что много лет жила и работала в Америке. А главное — открыла ученой общественности доступ в таинственный и неведомый прежде мир специфических молекул, которые необходимы для роста и развития высокоорганизованных тканей, — факторов роста. Не зря ее в 2001 году наградили почетным званием пожизненного сенатора Италии, чего могут удостоиться лишь бывшие президенты и граждане, прославившие страну достижениями в науке или искусстве.
С самого детства будущего нейробиолога окружала атмосфера высокой духовности, культуры и интеллигентности. Ее мать, Адель Монтальчини, была талантливой художницей из Асти (столица итальянской провинции Асти, ничего общего с молодой поп-исполнительницей ASTI и известным алкогольным напитком), а отец, Адамо Леви, — высокообразованным математиком и инженером-электриком из Казале-Монферрато (живописный город севера Италии). Они оба любили искусство, классическую музыку и книги. Вспомним другого нейробиолога — Чарльза Скотта Шеррингтона, о котором мы уже писали [1], — это идеальная колыбель для проявления и развития всех талантов. Так и вышло: трое из четырех детей в семье обрели признание и известность. Джино (Луиджи) Леви-Монтальчини стал известным архитектором, по мнению современников — одним из лучших. Сестра-близнец — Паола Леви-Монтальчини — добилась больших успехов в изобразительном искусстве. Ну а героиня нашей статьи и вовсе стала нобелевским лауреатом.


Но о них мы напишем позже. Интереса ради еще стоит добавить, что была у всех них одна общая черта, которая очень помешала работать именно в десятилетие между 1935 и 1945 годами. И учитель, и ученики были потомками Моисея, а попросту говоря, людьми еврейской национальности, что в те сложные годы фашизма ой как не приветствовалось.


Рисунок 4. Стэнли Коэн (род. 1922). Американский биохимик и зоолог, лауреат Нобелевской премии по физиологии и медицине 1986 года (совместно с Ритой Монтальчини) — за открытие ростовых факторов.

Фактор роста нервов вызвал неоднозначную реакцию со стороны ученых — многие критиковали исследование, ибо оно противоречило всем ранее установленным законам физиологии: нервная ткань не регенерирует и не растет. И точка. А согласие с очевидными результатами профессора Хамбургера и профессора Леви-Монтальчини (которым она стала в 1958 году) предполагало признание научным сообществом своей неправоты, чего не хотелось совсем. Дело еще в том, что вещество не обладало традиционными свойствами для уже известных в то время гормонов. Что делают гормоны? Вызывают временную метаболическую реакцию. А тут, оказывается, есть еще какие-то вещества, без которых организм и вовсе не может обойтись — постоянные регуляторы специфических типов клеток. Дальше грянул целый фейерверк исследований — подобно салюту на День Победы: миру один за другим открывались новые факторы роста, в том числе эпидермальный фактор (Коэна), тромбоцитарный фактор (PDGF), фактор роста фибробластов (FGF), колониестимулирующие факторы (например, гранулоцитарный, G-CSF), интерлейкины (IL-1, IL-2). А в 80-х годах и вовсе доказали, что онкогены (видоизмененные участки ДНК, ведущие к неправильному считыванию информации и таким образом становящиеся причиной онкологических заболеваний) несут код для производства белков, сходных по структуре с факторами роста и их рецепторами на поверхности клеток. Тут уж можно легко догадаться, что когда регуляция факторами роста нарушается, может возникнуть онкозаболевание.
Фактор роста нервов оказался не единственным для всей нервной системы: как в биологическом виде есть подвиды, так и здесь обнаружились факторы роста для различных видов нервных клеток. Практическое применение не заставило себя долго ждать: уже через какое-то короткое время NGF стал использоваться для восстановления поврежденных нервов, а EGF — для улучшения эффективности пересадки кожи. Но это были только первые скромные шажки в огромный мир непознанной молекулярной регуляции организма.
Вначале только одна лаборатория Леви-Монтальчини занималась исследованиями факторов роста, но благодаря ее усилиям в нейробиологической науке были открыты новые обширные отрасли, в освоении которых участвуют ученые многих стран и ныне.
До самого конца Рита Леви сохранила ясность и остроту мысли, даже на своем 100-летнем юбилее в созданном ею же Европейском исследовательском институте мозга (EBRI) заявляла, что ум ее остается таким же острым, как и 80 лет назад. Видимо, повлиял тот факт, что до конца жизни она посвящала несколько часов в день исследовательской работе. По словам племянницы, выдающийся нейробиолог умерла во сне. Наверное, именно такой смерти был достоин человек, всё свое время посвятивший изучению роста и жизни.

Президент Италии Джорджо Наполитано и пожизненный сенатор и нобелевский лауреат Карло Руббиа в гостях у Риты Леви-Монтальчини (2009).
Люк Монтанье с самого детства имел все шансы прославиться на исследовательском поприще — он был единственным ребенком в семье, и его отец прививал интерес к экспериментам.
В 21 год он стал бакалавром естественных наук в одном из старейших французских университетов — Университете Пуатье, затем продолжил образование в Париже, в Сорбонне. До защиты диссертации в 1960 году работал научным ассистентом и преподавателем, в позднее стажировался в Великобритании.

Люк Монтанье
Монтанье занялся глубоким изучением вирусологии и онкологии, и в 1964 году совместно с Яном Макферсоном он нашел идеальный субстрат для культивирования раковых клеток и дальнейшего исследования клеточных трансформаций.
Люк Монтанье занимался изучением ретровирусов в рамках исследования причин развития рака в Институте Пастера. Он доказал, что РНК ретровирусов способна синтезировать ДНК, чтобы встраиваться в ДНК хозяина. Ранее эта теория считалась спорной и несостоятельной.
1983 год стал для ученого знаковым. Совместно с коллегой Франсуазой Барре-Синусси ученый смог выделить из увеличенных лимфоузлов пациента со СПИДом новый вирус, который вначале связали с лимфаденопатией. Исследователи опубликовали 20 мая статью в журнале Science, но получили не самые восторженные рецензии, пока схожий вирус не обнаружил в независимом исследовании американский вирусолог Роберт Галло. Три года спустя было доказано, что открытый вирус действительно вызывает синдром приобретенного иммунодефицита. В 2008 году Люк Монтанье и Франсуаза Барре-Синусси были удостоены за это открытие Нобелевской премии.
Люк Монтанье всячески продвигал идеи честной, открытой и справедливой науки и сожалел, что не разделил почетную премию с Робертом Галло.
От великих открытий к спорным теориям

Люк Монтанье
Вскоре после публикации статьи о квантовом отпечатке ДНК Люк Монтанье дал интервью в поддержку Бенвениста.

Люк Монтанье
Авторитет ученого в научной среде пошатнулся после его пропаганды антинаучных методов лечения СПИДа — он предлагал использовать биодобавки и антиоксиданты. Зато он стал ключевой фигурой движения ВИЧ-диссидентов.
Цитаты ученого начали массово тиражировать не только отрицатели ВИЧ (притом, что именно он открыл ВИЧ), но и сторонники отказа от вакцинации. В 2012 году Монтанье участвовал в слете антивакцинаторов, где заявлял об опасности прививок. После этого 35 нобелевских лауреатов выступили с требованием отстранить ученого от руководства африканским центром борьбы со СПИДом.

Люк Монтанье
Также он принял активное участие в кампании против массовой вакцинации от COVID-19. Монтанье отмечал, что количество смертей увеличивается из-за эффекта ADE — антителозависимого усиления инфекции, когда антитела, которые формируются против вируса, повышают его возможность вызывать инфекцию вместо того, чтобы защищать организм. Никаких свидетельств возникновения этого эффекта при вакцинации нет.

Люк Монтанье
Вероятно, Люк Монтанье был искренне убежден, что борется против опасных вакцин от COVID-19, однако никаких клинических подтверждений этого получено не было.
Тем не менее Люк Монтанье сделал немало ценных открытий и вполне заслуженно носил звание нобелевского лауреата, хотя оно в последние годы и способствовало распространению ложных и опасных убеждений. Его вклад в доказательную науку останется в истории.
Родившийся дважды
В 1953 году Люк получил эквивалент степени бакалавра естественных наук в Университете Пуатье, а спустя два года окончил со степенью магистра Парижский университет. В 1960 году молодой ученый защитил в Сорбонне диссертацию на материале своих исследований клеток сердца эмбриона человека, и уехал на три с половиной года на стажировку в Англию, в лабораторию известного вирусолога Кингсли Сандерса.
У Сандерса молодой ученый сделал первое значительное открытие. Оно касалось РНК-вирусов, у которых наследственный материал хранится в форме не ДНК, как у всех остальных живых существ, а другой рибонуклеиновой кислоты — РНК. Монтанье удалось впервые показать, что РНК тоже способна удваивать себя. Некоторые вирусы, называемые ретровирусами, используют этот механизм, чтобы синтезировать на основе своей РНК ДНК, и встраивать ее в ДНК хозяина — например, человека. Такая модификация ДНК заставляет клетку быстро делиться, возникает раковая опухоль.
Спорное открытие
Изучение онкогенных ретровирусов стало основной темой исследований Монтанье. В 1972 году он основал и возглавил лабораторию вирусной онкологии в Институте Пастера в Париже. В том числе, лаборатория изучала интерфероны — белки, которые образуются в клетках высших животных в ответ на вторжение вируса и подавляют его размножение. Монтанье с коллегами смогли выделить гены, отвечающие за синтез этих белков.
Монтанье и Барре-Синусси опубликовали статью о своем открытии в журнале Science 20 мая 1983 года. А уже в следующем году в том же журнале вышла статья доктора Роберта Галло и его коллег из Национальных институтов здравоохранения США, которые независимо от французских коллег, открыли тот же вирус, и назвали его H.T.L.V.-III. Авторы этой статьи настаивали, что сделали открытие первыми. При этом оказалось, что оба научных коллектива использовали пробы из организма одного и того же французского пациента, и в институте Пастера заподозрили американских коллег в краже своего материала. Когда те попытались получить патент на свое открытие в США, французы подали на них в суд.
Разделенные награды
В 1986 году Монтанье получил вместе с Галло престижную международную Премию Альберта Ласкера за клинические медицинские исследования (теперь она носит имя американского кардиохирурга Майкла Дебейки, оперировавшего в том числе президента России Бориса Ельцина). Жюри премии приняло соломоново решение: Монтанье наградили за открытие вируса, Галло — за то, что он доказал его роль как возбудителя СПИДа. В 2002 году двое ученых публично заявили, что оставили свои разногласия в прошлом, и собираются вместе работать над созданием вакцины против этой смертельной болезни.
Однако в 2008 году Нобелевскую премию в области медицины и физиологии за открытие ВИЧ решили дать только Монтанье и Барре-Синусси. Третьим лауреатом в номинации в том году стал немецкий вирусолог Харальд цур Хаузен, показавший, что рак шейки матки вызывает вирус папилломы человека (ВПЧ). Галло оставили за бортом, однако он нашел мужество сказать, что все трое призеров полностью заслужили свои премии, и он рад, что Нобелевский комитет отметил важность исследований ВИЧ/СПИДа.
Скандальный нобелиат
Читайте также:

