Вирусное поражение черепных нервов
Обновлено: 25.04.2024
Невралгия тройничного нерва - методы диагностики, лечения по Европейским рекомендациям
Компрессионные синдромы включают сосудистую компрессию нервных структур, вызывающую гиперфункцию (гиперактивность). Наиболее распространенными являются компрессия тройничного и лицевого нервов, что приводит к невралгии тройничного нерва и гемифациальному спазму, соответственно. Но есть и другие, и мы обсудим их здесь следуя нумерации черепных нервов.
а) Симптомы невралгии тройничного нерва. Характерной особенностью невралгии тройничного нерва (НТН) является острая, как электрический ток, боль в лице с локализацией в одной или нескольких областях иннервации тройничного нерва. Боль длится всего от нескольких секунд до нескольких минут, но может возникнуть повторно сразу за предыдущим приступом, таким образом, как бы сливаясь из коротких вспышек, возникает мучительный болевой приступ, длящийся в течение нескольких часов или даже дней.
Боль, как правило, начинается после прикосновения, холодного ветра, разговора, приема пищи или бритья, а также может начаться самопроизвольно. Последнее может свидетельствовать о зубной боли, в результате чего многие пациенты в первую очередь обращаются за стоматологической помощью.
При типичной невралгии тройничного нерва (НТН) чувствительные и двигательные функции нерва не нарушаются. Частота заболеваемости составляет 4 на 100000 в год, а средний возраст возникновения чуть более 60 лет с небольшим женским перевесом (1,8:1). Правая сторона страдает чаще (60%), и только в 1% тройничная невралгия появляется с обеих сторон.
б) Причины невралгии тройничного нерва. Тригеминальная невралгия может быть симптоматической или идиопатической. Причина симптоматической невралгии может быть периферической, например, воспаление в верхнечелюстной или нижнечелюстной области (связанное с зубом), приводящее к раздражению ветвей тройничного нерва. При более центральном поражении, таком как травма или опухоль, может появляться невралгическая боль, но почти всегда с потерей функции нерва.
При отсутствии причин, описанных выше, тройничная невралгия называется идиопатической. Но после открытий Dandy, Gardner и Jannetta известно, что более 90% так называемой идиопатической НТН вызвано сосудистой (артериальной или венозной) компрессией нерва в зоне входа корешка. Аксоны тройничного нерва в этой зоне имеют переходную оболочку от шванновских клеток на периферии к олигодендроглиальным клеткам в центральном сегменте. Считается, что сосудистая компрессия приводит к латеральному распространению потенциала действия, в результате чего возникает аномальная активность в центральных путях и ядрах тройничной системы.
в) Дополнительная и дифференциальная диагностика. Обязательно неврологическое обследование: чувствительные и двигательные функции тройничного нерва должны быть нормальными, как описано выше. В некоторых случаях нейрофизиологические тесты могут выявить небольшие изменения, но в целом они не являются достаточно надежными. Необходимо выполнить МРТ, чтобы исключить другие заболевания, такие как PC, внутренние сосудистые поражения (кавернома) или опухоль.
МРТ может выявить вазо-невральный конфликт, который, как полагают, вызывает боль при тройничной невралгии. Чувствительность и селективность МРТ, однако, в целом не может подтвердить или опровергнуть определенную нервно-сосудистую компрессию. Таким образом, наиболее важным аспектом в диагностике являются точные анамнестические сведения. Типичная невралгия тройничного нерва (НТН) может быть дифференцирована от зубной боли, кластерной головной боли, коленчатой невралгии, языкоглоточной невралгии, постгерпетической невралгии/нейропатии или крылонебной невралгии.
При продолжительной невралгии тройничного нерва (НТН) ее характерные особенности (короткие атаки, триггеры) могут постепенно превращаться в более устойчивую боль. Поэтому иногда трудно определить, сохраняется ли типичная невралгия тройничного нерва (НТН) или же имеет место атипичная форма. Последняя включает в себя хроническую жгучую боль в лице без типичных триггеров, и не связана с сосудистой компрессией. Только тщательный сбор анамнеза поможет определить начальные симптомы этого заболевания.
г) Лечение невралгии тройничного нерва (НТН). Во всех случаях черепно-лицевых болей, напоминающих невралгию тройничного нерва (НТН) к первому выбору относится назначение карбамазепина (тегретол®). Почти во всех случаях типичной невралгии тройничного нерва (НТН) карбамазепин снимает боль при адекватной дозировке, т. е. одновременно появляется и диагностический показатель. Многие пациенты в течение определенного времени могут снижать исходную дозу и даже излечиваются. Основные недостатки этого препарата — это побочные эффекты (тошнота, головокружение), которые препятствуют продолжению применения препарата у достаточно большого процента пациентов. В этом случае заменить карбамазепин могут такие препараты как трилептал® или другие противоэпилептические препараты, как Dilantin® и габапентин.
При неудаче медикаментозного лечения из-за отсутствия эффекта или побочных действий обычно принимается решение о хирургическом лечении. Микроваскулярная декомпрессия (МВД), разработанная и рекомендуемая Jannetta et al, является наиболее логичным и этиологичным вариантом лечения. Это очень деликатная операция в важной области проводится под общей анестезией, в соотношении баланса между риском и пользой обязательно учитываются общее состояние пациента и опыт нейрохирурга.
При каких-либо противопоказаниях можно выбрать другие абляционные методы: радиочастотное поражение Гассерова ганглия, баллонная компрессия Гассерова узла; введение глицерола в полость Меккеля. В последнее время опыт работы с гамма-ножом или стереотаксической радиохирургией дал почти такие же положительные результаты как при традиционных абляционных процедурах, поэтому эти новые методы следует рассматривать в качестве реальной альтернативы.
При симптоматической невралгии тройничного нерва (НТН), особенно у пациентов с PC, описанное выше лечение является методом выбора, т. к причиной болей служат нарушения в ПНС, а не в зоне входа корешка. Таким образом, уменьшение сенсорной передачи каким-нибудь абляционным методом является логичным вариантом лечения.
д) Результаты. Наилучшие краткосрочные и долгосрочные результаты получены с помощью этиотропной терапии — микроваскулярной декомпресии (МВД). Краткосрочные результаты почти так же хороши при абляционном поражении ганглия или инъекциях глицерола в Меккелеву полость. Эти процедуры можно повторять, поэтому они являются хорошими методами второго выбора при подлинной невралгии тройничного нерва (НТН) и у больных с PC. Проведение процедур в молодом возрасте создает риск поздних серьезных осложнений в виде феномена болезненной анестезии. Это справедливо и для самых радикальных абляционных процедур, таких как операция Денди, которая предусматривает перерезку нерва у ствола мозга. Результаты приведены в таблице ниже.

Смертность, заболеваемость и показатели эффективности различных методов лечения невралгии тройничного нерва.
Учебное видео по анатомии тройничного нерва и его ветвей
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое невропатия (нейропатия)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Алексеевича Г. В., невролога со стажем в 16 лет.
Над статьей доктора Алексеевича Г. В. работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Невропатия, или нейропатия (Neuropathy) — повреждение одного или нескольких нервов периферической нервной системы. К ней относятся черепные и спинальные нервы, а также нервы и сплетения вегетативной нервной системы [2] [3] . Невропатия проявляется нарушением чувствительности, болью в поражённом участке, судорогами, мышечной слабостью и затруднением движений. Выделяют две основные группы невропатий:
- мононевропатия — повреждение отдельного нерва, например срединного.
- полинейропатия — множественные повреждения нервов при диабетической полинейропатии, диффузной нейропатии, полирадикулопатии, плексопатии.
Распространённость нейропатии среди населения составляет 2-7 %. Риск развития заболевания увеличивается с возрастом: в 40 лет патология встречается в 15 % случаев [4] [5] [6] .
Повреждение периферических нервов может вызывать множество причин. Даже после комплексного обследования выявить их удаётся не всегда. К основным факторам, приводящим к заболеванию, относят:
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы невропатии
Несмотря на то, что нейропатию вызывают различные причины, основные симптомы заболевания схожи [9] [14] [15] [16] [17] :
- Двигательные нарушения, слабость мышц. Пациент с трудом выполняет действия, связанные с мелкой моторикой, например застёгивание пуговиц. Возникают проблемы с ходьбой — больной может упасть из-за слабости мышц стопы.
- Сенсорные нарушения — онемение, повышенная тактильная чувствительность, резкая стреляющая боль, подобная удару электрическим током.
- Снижение и выпадение сухожильных рефлексов. Появляются трудности при выполнении повседневных действий, таких как надевание одежды, перемещение предметов.
- Расстройства сердечно-сосудистой системы. Выражается в нестабильности артериального давления и его снижении при резком вставании, проявляется головокружением и потемнением в глазах .
- Расстройства желудочно-кишечного тракта — запоры и кишечная непроходимость, вызванные ухудшением тонуса мышц кишечника.
- Боли в кистях и стопах.
- Нарушение равновесия и координации движений.
- Повышенная потливость.
- Задержка мочеиспускания.
- Сексуальная дисфункция.
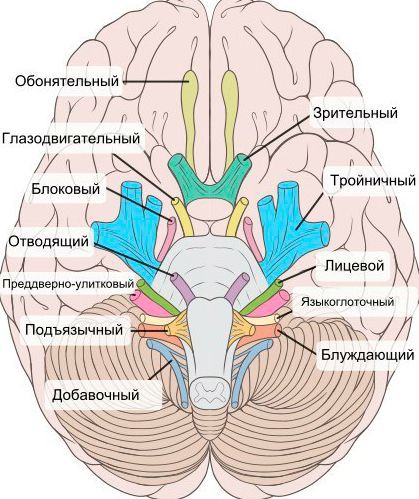
При нейропатии могут поражаться не только нервы конечностей, но и черепно-мозговые нервы:
- невропатия зрительного нерва (оптическая нейропатия) приводит к нечёткости, затуманенности зрения, нарушению цветового восприятия, слепоте;
- поражение глазодвигательного нерва проявляется опущением верхнего века и параличом глазных мышц;
- патология отводящего нерва вызывает сходящееся косоглазие, опущение верхнего века, двоение в глазах;
- лицевого нерва — паралич мимических мышц;
- преддверно-улиткового (слухового нерва) — потерю слуха;
- языкоглоточного нерва — нарушение подвижности языка;
- гортанного нерва — дыхательную недостаточность [15] .
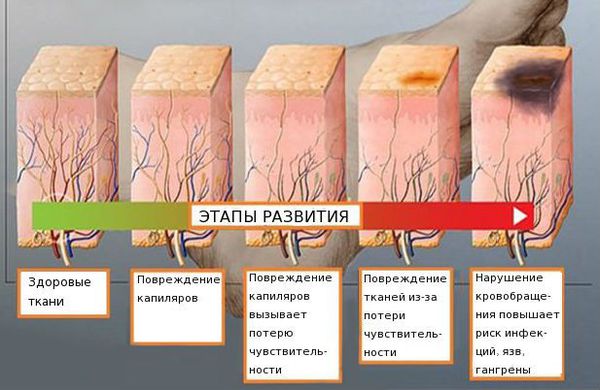
На начальных стадиях двигательные расстройства могут не проявляться. Но в дальнейшем нейропатия значительно ограничивает физическую активность пациента [5] [7] [16] [17] .
Для повреждения периферической нервной системы характерны основные синдромы:
- Поражение переднего корешка спинного мозга — приводит к ослаблению или параличу мышц. Возможны судороги и подёргивания.
- Поражение заднего корешка спинного мозга — проявляется повышенной тактильной чувствительностью, жжением, нарушением спинальных рефлексов, болью в области поражения.
- Поражение межпозвоночного узла — вызывает жжение, покалывание, снижение болевого порога, интенсивные жгучие боли, обострение герпесвирусной инфекции.
- Поражение спинального нерва — приводит к расстройствам чувствительности и двигательным нарушениям.
- Поражение сплетения периферических нервов — вызывает боль, но менее интенсивную, чем при повреждении корешков [16] .
Патогенез невропатии
К нейропатии могут приводить нарушения обмена веществ и иммунной системы, генетические факторы, инфекционное и токсическое воздействие [1] .
Развитие заболевания при обменных нарушениях, например при сахарном диабете, вызвано чрезмерным накоплением глюкозы в клетке. Гипергликемия приводит к отложению в нервных клетках продукта обмена — сорбитола. Избыток сорбитола нарушает функции клеток периферических нервов. При этом уменьшается выработка мио-инозитола — соединения, влияющего на передачу сигналов в мозге и защиту нервных клеток от повреждения. Всё это приводит к ухудшению регенеративных способностей нервной ткани и снижению её проводимости [9] .
В развитии нейропатии важная роль принадлежит митохондриям (органеллам, обеспечивающих клетку энергией) . Они повреждаются при гипергликемии и приёме противоопухолевых препаратов: паклитаксела, бортезомиба, оксалиплатина. Эти лекарства влияют и на другие внутриклеточные структуры (например микротрубочки, поддерживающие форму клетки ), негативно воздействуют на клеточные процессы и в результате активируют запрограммированную гибель нейронов [9] [15] [18] . Схожие нарушения возникают и у ВИЧ-инфицированных пациентов, принимающих антиретровирусные препараты [9] [15] .
Классификация и стадии развития невропатии
Попытки систематизировать различные виды нейропатии предпринимались многократно как отечественными, так и зарубежными авторами. Но ни одна из классификаций не удовлетворяет всем потребностям клиницистов. Это связано с тем, что к развитию заболевания приводит множество сложных и до конца не изученных факторов [16] .
По одной из классификаций, нейропатии разделяют на следующие группы: [19]
I. Мононевропатии (поражение одного нерва).
- Травматические мононевропатии — возникают при травмах, ранениях, электротравмах, химических повреждениях.
- Туннельные синдромы — это ущемление нерва при длительном сдавлении и травматизации в костно-мышечных каналах. К ним относятся: синдром карпального канала (сдавление нерва в области запястья), пронаторный синдром (поражение нерва в плече), синдром кубитального канала (в локте), синдром тарзального канала (сдавление большеберцового нерва), синдром ложа Гийона (сдавление глубокой ветви локтевого нерва) и др.
II. Множественные нейропатии (поражение нескольких отдельных нервов).
- Моторная мультифокальная нейропатия с блоками проведения — аутоиммунное заболевание, проявляющееся слабостью мышц стоп и кистей.
- Моторно-сенсорная невропатия с блоками проведения — вызывает поражение не только моторных, но и сенсорных волокон.
- Множественная невропатия при васкулитах.
III. Полиневропатии (множественные поражения нервной ткани).
1. Наследственные полиневропатии: Шарко — Мари — Тута, синдром Руси — Леви, Дежерина — Сотта и др.
2. Приобретённые полиневропатии.
2.1. Аутоиммунные полиневропатии — возникают при сбое в работе иммунной системы (синдром Гийена — Барре, синдром Миллера — Фишера, хроническая воспалительная демиелинизирующая полинейропатия, парапротеинемические полиневропатии, паранеопластические полинейропатии).
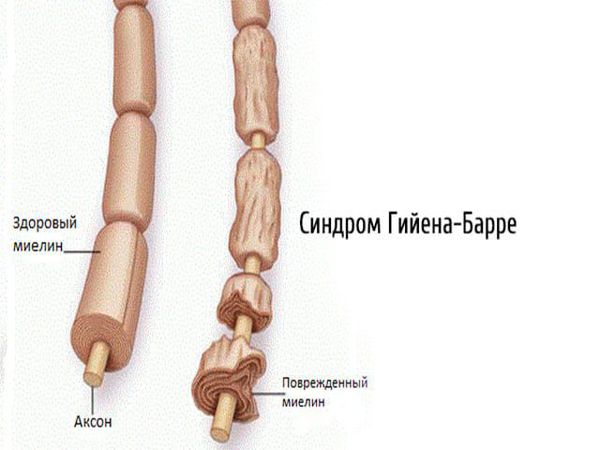
2.2. Метаболические полинейропатии — диабетическая, уремическая, печёночная, при системных заболеваниях. Наиболее часто встречается диабетическая нейропатия.
2.2 Вызванные дефицитом витаминов В1, В6, В12.
2.3 Токсические полинейропатии — вызванная алкоголем, лекарствами, отравлением тяжёлыми металлами. Препараты, способные приводить к нейропатии:
-
— крайне нейротоксичное средство. Развитие острой нейропатии возникает в 90 % случаев, а хронической — в 50 %. Приём оксалиплатина приводит к жжению, покалыванию, онемению рук, ног и области вокруг рта.
- Таксен (Палитаксел,Доцетаксел) — вызывает нарушение чувствительности, слабость и боль в мышцах, возможны редкие вегетативные симптомы.
- Препараты на основе алкалоидов барвинка (Винбластин, Винорелбин, Виндезин, Винкристин) — нарушают функции мочевого пузыря и кишечника, влияют на чувствительность в руках и ногах, ухудшают мелкую моторику, приводят к мышечной слабости и резкому снижению артериального давления.
- Бортезомиб — нарушает чувствительность, приводит к боли и вегетативным симптомам.
- Иммуномодулирующие препараты (Талидомид) — провоцирует сенсорные нарушения, преимущественно в нижних конечностях, лёгкие двигательные, желудочно-кишечные и сердечно-сосудистые расстройства [15][16][18] .
2.4 Инфекционно-токсические — после гриппа, кори, дифтерии, мононуклеоза, поствакцинальные, при ВИЧ-инфекции, лепре.
IV. Поражения сплетений (шейного, верхнего плечевого, нижнего плечевого, пояснично-крестцового).
V. Вертеброгенные поражения нервных корешков (радикулиты).
Несмотря на многообразие причин, вызывающих полинейропатии, по участкам поражения их можно разделить на два вида:
- Аксональные — вовлечены нервы с наиболее длинными отростками (аксонами), к ним относится большинство токсических полинейропатий, аксональный тип наследственной моторно-сенсорной полинейропатии. Характеризуются мышечными атрофиями.
- Демиелинизирующие — вызваны разрушением миелиновой оболочки, окружающей отростки нервных клеток. Проявляются выпадением сухожильных рефлексов, развитием мышечной слабости без мышечных атрофий [19] .
Осложнения невропатии
Зачастую нейропатия уже является осложнением какого-либо заболевания, например сахарного диабета. У некоторых пациентов, страдающих диабетом, может развиваться диабетическая амиотрофия — асимметричное поражение проксимальных (близких к туловищу) отделов ног с развитием болей и слабости в мышцах [16] [17] [19] .
Если лечение не начато вовремя, нейропатия стремительно прогрессирует. В результате снижается тонус мускулатуры, наступает атрофия мышц и инвалидность. На фоне мышечной слабости случаются падения и травмы. Пациенты утрачивают способность ходить и обслуживать себя. Иногда последствиями полинейропатии становятся полный паралич конечностей или дыхательная недостаточность.
Диагностика невропатии
Неврологи используют различные шкалы для оценки тяжести нейропатии. Универсального опросника, соответствующего всем потребностям клиницистов, не существует. Это связано с различным прогнозом, проявлениями и причинами нейропатии [21] .
Во время обследования оценивают проводимость нерва, учитывая временную динамику [17] . Для диагностики применяют следующие методы:
- Электромиография (ЭМГ) — регистрация электрической активности в мышце при её сокращении. Позволяет определить характер двигательных расстройств, уточняет степень разрушения нерва и выявляет заболевание до появления симптомов. ЭМГ позволяет провести дифференциальную диагностику невропатии с миастенией, миотонией, миоплегией, полимиозитом [16][17] .
- Электронейромиография (ЭНМГ) — оценивает прохождение импульса по нервному волокну. ЭНМГ поможет не только выявить расположение поражённых участков, но и определить момент начала патологического процесса [17] .
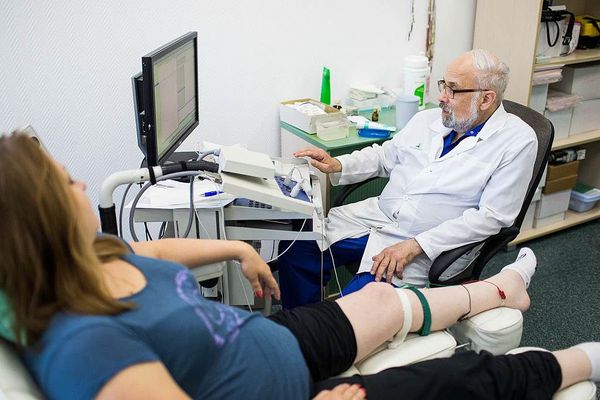
- УЗИ — распространённый метод визуализации периферических нервов. Ультразвук поможет выявить нарушения, которые незаметны при электродиагностике. Оценивается изменение диаметра нерва, непрерывность и ухудшение звукопроводимости. УЗИ позволяет обнаружить опухоли периферических нервов, травматические невромы, разрывы, воспаление, демиелинизирующие процессы.
- МРТ — визуализирует нервы и структуру мягких тканей, выявляет злокачественные опухоли и предоставляет информацию о мышечной атрофии и поражении нервов. МРТ выявляет повреждение нерва в областях, которые трудно исследовать при помощи электродиагностики или ультразвука.
Согласно статистике, УЗИ выявляет мононевропатии или плечевые плексопатии чаще, чем МРТ [20] .
Лечение невропатии
Выбор методов лечения нейропатии зависит от вызвавших её причин:
Прогноз. Профилактика
Невропатия зачастую развивается достаточно медленно. Пациенты сообщают о неврологических проявлениях врачу спустя годы после её формирования. О симптомах симметричной полинейропатии лечащий врач узнаёт в среднем через 39 месяцев. В таком случае лечение может быть запоздалым, а повреждение нерва необратимым [5] .
При синдроме Гийена — Барре прогноз ухудшают пожилой возраст, быстрое развитие заболевания, потеря аксонов. Восстановление может занять несколько месяцев и быть неполным. Приблизительно у 15 % пациентов с синдромом Гийена — Барре сохраняются остаточные параличи [16] [17] .
Васкулитная нейропатия развивается с разной скоростью. Заболевание может протекать как в прогрессирующей хронической форме, так и в рецидивирующей с длительными периодами ремиссии.
Прогноз при сахарном диабете зависит от поддержания оптимального уровня сахара в крови. Приверженность лечению позволяют замедлить развитие нейропатии.
Прогноз после травмы периферической нервной системы плохой. При повреждении эндоневральной трубки (внешнего слоя соединительной ткани, окружающей периферические нервы) пациенты редко восстанавливаются полностью [17] .
После терапии противоопухолевыми средствами нейропатия может сохраняться несколько лет [18] . Обратимость патологии остаётся под вопросом, особенно при приёме противораковых препаратов на основе платины и таксанов. Для уменьшения тяжести симптомов онкологи могут снизить дозировку или прекратить применение нейротоксических противоопухолевых препаратов [15] [18] .
Не все нейропатии можно предотвратить. Однако часть нарушений возможно избежать или отсрочить их появление на несколько лет. Это в первую очередь относится к эндокринным нейропатиям, например диабетической, и нейропатии, вызванной дефицитом витаминов в организме.
Что такое невралгия тройничного нерва? Причины возникновения, диагностику и методы лечения разберем в статье доктора Новиков Ю. О., остеопата со стажем в 41 год.
Над статьей доктора Новиков Ю. О. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Невралгия тройничного нерва (НТН, Neuralgia n. trigemini, Prosopalgia) — хроническое заболевание, для которого характерны интенсивные боли стреляющего и/или жгучего характера в области лица, при этом расстройств чувствительности не выявляется.
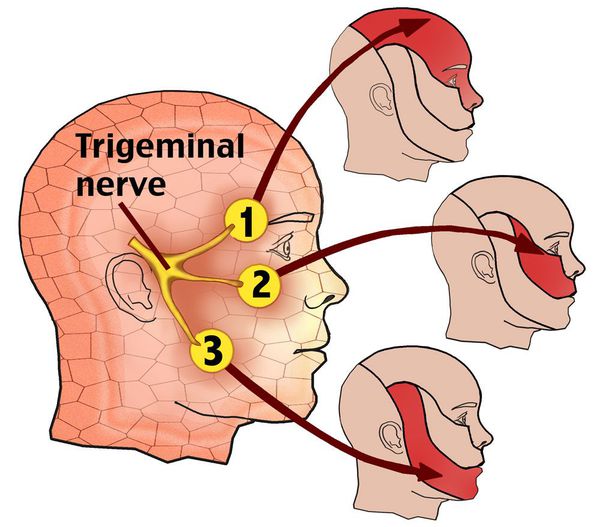
По данным Всемирной организации здравоохранения, распространённость заболевания находится в пределах 2-4 человек на 100 000 населения. Чаще встречается у женщин 50-69 лет. Преобладает правосторонняя локализация. [1] [2] Примерно в 3% случаев возможен двусторонний процесс, частота которого возрастает в ходе увеличения длительности заболевания. [3]
Причины невралгии тройничного нерва
Невралгия V нерва может быть проявлением как поражения отдельных ветвей, так и его ядер в области ствола головного мозга и продолговатого мозга.
Поражения отдельных ветвей V нерва возникают в связи с переломом черепа, менингитом или рассеянным склерозом, объёмными образованиями головного мозга, саркоидозом или аневризмами близлежащих сосудов.
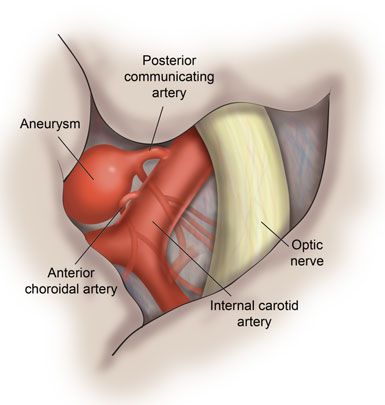
Поражение комплекса ядер также может быть связано с сосудистым процессом, объёмными образованиями, различными энцефалитами, рассеянным склерозом, сирингобульбией и сирингомиелией.
Кроме того, поражение V нерва может быть одним из признаков краниальной полиневропатии, связанной с отравлением трихлорэтиленом и другими химическими веществами, или ранним признаком некоторых заболеваний соединительной ткани, таких как склеродермия.
Некоторые проявления НТН возможны как сопутствующие признаки невропатии VII (лицевого) нерва. Это связано с единым кровоснабжением.
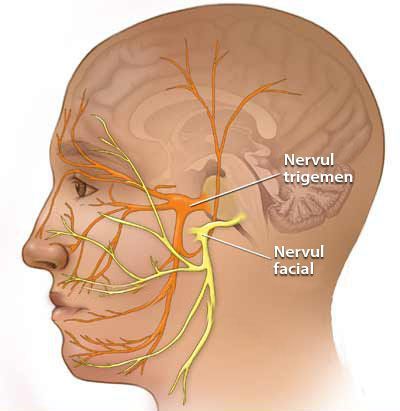
Также существует эссенциальная или идиопатическая НТН.
Факторы риска невралгии тройничного нерва
К факторам риска развития заболевания некоторые авторы относят:
- Генетический дефект в хромосоме 32Р, брахидактилию и наследственную форму гипертензии, которая передаётся от одно из родителей. Эти нарушения сочетаются с патологической извитостью или стенозом задней нижней мозжечковой или позвоночной артерий, что приводит к сдавлению переднебоковых отделов продолговатого мозга. , который снижает эластичность сосудов и увеличивает механическое воздействие пульсовой волны на корешок тройничного нерва.
- Сдавление ветвей тройничного нерва в костном канале, на месте которого повреждается оболочка, окружающая нервные волокна.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы невралгии тройничного нерва
Основной симптом невралгии тройничного нерва — это интенсивная боль в области лица. Боли при невралгии бывают двух видов:
- постоянные, тупые, периодически усиливающиеся боли без широкой иррадиации, возникающие в области распространения той или другой ветви нерва и не сопровождающиеся выраженными вегетативными реакциями;
- боли пароксизмального характера, длящиеся от нескольких минут до нескольких часов. [4][5]
Интенсивность приступов различна: от несильных, но частых, продолжающихся несколько секунд, до сильных и непереносимых, продолжающихся минутами и причиняющих сильные страдания.
Приступы нередко возникают спонтанно, без каких-либо раздражителей, либо в результате попадания твёрдой и холодной пищи в рот, прикосновений, сквозняков, переохлаждений под кондиционером, движений челюстями и т. п.
Приступ начинается обычно с болей в одной ветви нерва — месте первичного поражения, затем боль распространяется на другие ветви, нередко иррадиирует в затылок, к ушным нервам, в шею и даже в область грудных нервов.
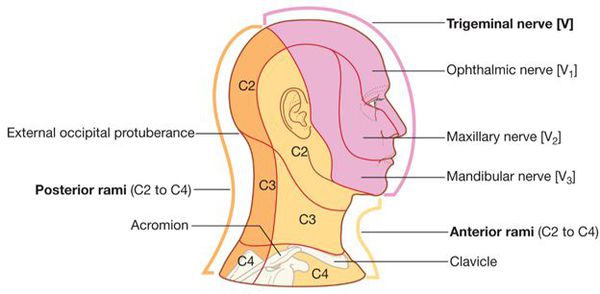
Сильные приступы обычно сопровождаются вегетативными рефлекторными реакциями: покраснением лица, слезотечением, жидкими выделениями из носа, слюнотечением, иногда отёком щеки, века, небольшим припуханием половины носа.
К симптомам воспаления тройничного нерва также относится общее беспокойство, потирание болевой зоны рукой, давление на эту зону, причмокивание. Это наслоение новых раздражений, очевидно, ускоряет момент возникновения тормозного состояния в центре болевых восприятий, которым обычно сменяется приступ.
В качестве двигательных проявлений в связи с болевым приступом возникают тикообразные подёргивания мышц или спазматические сокращения. Максимальные подёргивания или сокращения мышц соответствуют, в основном, зонам, с которых начинается боль, т. е. местам первичного поражения.
При длительном заболевании иногда отмечается поседение волос головы на поражённой стороне.
Иногда пароксизмальные невралгии сопровождаются высыпанием herpes zoster (опоясывающий герпес), располагающегося соответственно первичным поражениям тех или других ветвей, иногда поражающего слизистую роговицы.
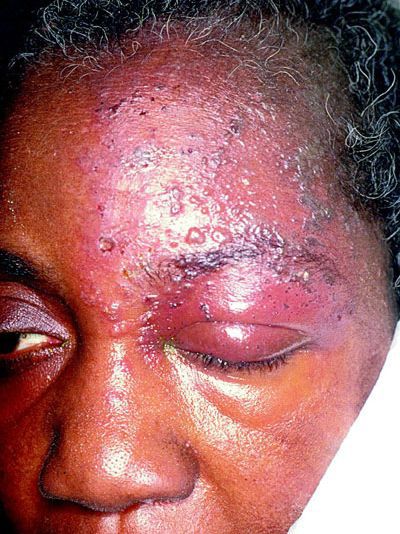
Периоды обострений могут чередоваться с периодами ремиссий, которые длятся месяцами, иногда годами.
Вне приступа обычно не наблюдается никаких расстройств: ни болевых точек, ни объективных расстройств чувствительности. Иногда можно отметить снижение болевой чувствительности главным образом в районе той ветви, которая являлась местом первичного поражения. Реже снижение чувствительности обнаруживается в области всех ветвей тройничного нерва. В отдельных случаях вне приступов больные испытывают лёгкие тупые боли. Болевые ощущения возникают в любое время, но чаще во сне. [6] [7]
Патогенез невралгии тройничного нерва
Патогенез невралгии тройничного нерва, как и локализация процесса, остаётся до конца неясным. Считается, что причиной данного страдания является сдавление корешка нерва в месте его выхода из моста изменёнными сосудами или опухолью, а причиной патологии у больных с рассеянным склерозом — образование бляшки в области чувствительного ядра тройничного нерва.
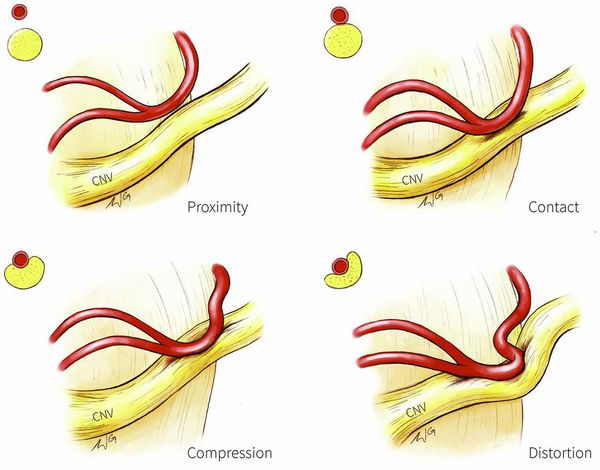
Предполагают центральную локализацию поражения на уровне понтобульбоспинальных центров, есть мнения о поражении в нисходящем корешке, связанном с ядром, или на уровне задних корешков. Имеющиеся патологоанатомические исследования, как правило, обнаруживали в гассеровых узлах изменения воспалительного или рубцового характера. Патологический очаг, изменяющий функцию узлов, влечёт за собой функциональные нарушения в расположенном выше зрительном бугре. Очаг раздражения в узле периодически под влиянием обычно внешних раздражений ведёт к возбуждению последнего с последующим возбуждением в расположенных выше центрах. Начавшись с одной точки, возбуждение затем распространяется по этим центрам. Далее сверхсильное возбуждение клеток сменяется торможением, которое распространяется в том же порядке, в каком происходила иррадиация болей. Результатом полного тормозного состояния является прекращение болей.
В этой схеме, объясняющей возникновение приступа пароксизмальной невралгии, имеется аналогия с эпилептическими припадками, только с той разницей, что реализация невралгических припадков ограничивается областью подкорки, и эти припадки никогда не ведут к последующему разлитому торможению коры головного мозга. Впрочем, это бывает иногда и при истинной парциальной эпилепсии. Если исходить из данного положения, то станет понятным, что наслаивание новых раздражений ускорит наступление тормозного состояния, т.е. конца приступа. К этим приёмам обычно и прибегают больные для купирования приступа. [8] [9]
Классификация и стадии развития невралгии тройничного нерва
Невралгия тройничного нерва бывает:
- первичной — истинной (эссенциальная или идиопатическая);
- вторичной — симптоматической:
- центральной;
- периферической (компрессионной).
Классификация по этиологическому фактору:
- травматическая НТН;
- инфекционная НТН;
- НТН в результате патологии обмена веществ в организме.
Классификация по уровню поражения:
- дентальная плексалгия;
- невралгия носоресничного нерва (синдром Чарлина);
- невралгия ушно-височного нерва (синдром Фрейя);
- синдром крылонебного узла (синдром Сладера);
- глоссофарингиальная невралгия;
- SUNCT-синдром;
- синдром поражения полулунного узла.
Классификация по нарушению функций:
- нарушение чувствительной функции тройничного нерва;
- нарушение двигательной функции тройничного нерва.
Осложнения невралгии тройничного нерва
Осложнения симптоматических вариантов НТН зависят в первую очередь от этиологии. При нейроинфекционных процессах, объёмных образованиях, аневризмах близлежащих сосудов, демиелинизирующих заболеваниях наиболее вероятны осложнения от основных заболеваний, вплоть до инвалидизации и летального исхода.
В случае идиопатической НТН чаще всего наблюдается переход в хроническую стадию: болезнь носит длительный характер, тянется непрерывно или с интервалами различной продолжительности, почти не поддаваясь окончательному излечению. Однако в некоторых случаях отмечают длительную ремиссию до 5-7 лет, но затем боли возобновляются. В периоды ремиссий типично щадящее поведение пациентов с НТН — они предпочитают жевать одной половиной рта, даже в тёплую погоду укрывают голову.
В начальных стадиях болезни, когда её причина установлена, соответствующее лечение может быстро ликвидировать воспалительный процесс без остаточных явлений в виде образования рубцов. Если рубцы образуются, рецидив болезни почти неизбежен — она приобретает хроническое течение.
В случае длительно протекающих невралгий нередки признаки нарушения трофики (питания) тканей в зоне иннервации нервного корешка, таких как сальность и истончение кожи. В случае НТН I ветви вероятны выпадение ресниц и бровей, вплоть до трофических язв роговицы. Кроме того в зоне иннервации снижается тактильная и/или температурная чувствительность.
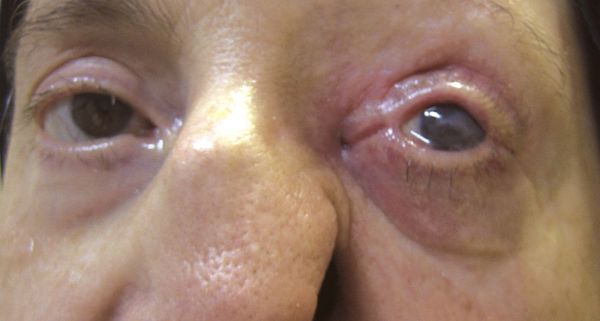
Диагностика невралгии тройничного нерва
Когда следует обратиться к врачу
При НТН посетить доктора нужно как можно раньше, так как в некоторых случаях боль может быть вызвана новообразованием, инфекцией или демиелинизирующим заболеванием.
Подготовка к посещению врача
Особая подготовка не требуется. Если у пациента есть результаты нейровизуализации, то снимки стоит взять с собой.
Инструментальная диагностика
В первую очередь при подозрении на НТН необходимо выполнить магнитную томографию или компьютерную томография головы с целью исключения серьёзной патологии.
Важно дифференцировать НТН с сирингомиелией и сирингобульбией, иногда начинающихся болями в области тройничного нерва, которые могут приобрести пароксизмальный характер. Наличие характерных для сирингомиелии симптомов и дефектов физического развития позволяют установить правильный диагноз.
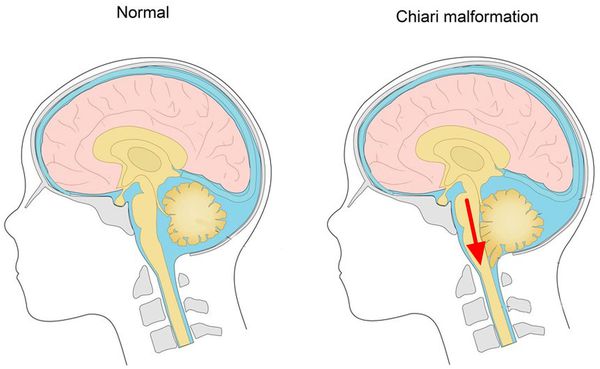
Иррадиирующие боли при заболеваниях придаточных полостей носа, зубов сравнительно легко дифференцируются от невралгии. Боли тупые, не носят пароксизмальный характер, исчезают бесследно после излечения вызвавших их заболеваний. Если после излечения боли не проходят, следует думать о невралгии. Смешение невралгии с болями, иррадиирующими из зубов, нередко ведёт к ошибочному диагнозу и удалению здоровых зубов.
Боли в районе первых ветвей тройничных нервов, наблюдаемые при тиреотоксикозах, необходимо относить к токсическим невралгиям. Они всегда двусторонние, часто сочетаются с затылочными болями, носят упорный характер. Специальное лечение обычно снимает эти боли.
Дифференциальная диагностика
Инфекционные невралгии тройничного нерва приходится дифференцировать с невралгиями неинфекционной этиологии. В пожилом возрасте такие невралгии могут быть обусловлены склеротическими изменениями отверстий, через которые проходят ветви тройничного нерва, с кровоизлияниями в нерв или гассеров узел.
Этиологический диагноз приходится ставить только на основании анамнестических данных. Клинические признаки могут быть сходны только при склеротическом поражении одной ветви, пароксизмы не так сильны и не приобретают широкой иррадиации. Невралгии, возникшие в результате оболочечных воспалительных процессов и неопластических процессов в области гассерова узла и корешков, тройничного нерва, кариозных заболеваний пирамидки распознаются сравнительно легко. При всех этих заболеваниях обычно в процесс вовлекаются другие черепные нервы: слуховой, лицевой, отводящий. [12] [13]
Лечение невралгии тройничного нерва
Медикаментозное лечение
Препаратами второго ряда являются баклофен, тизанидин и антидепрессанты, которые вначале назначаются в условиях стационара, а затем применяются в амбулаторных условиях с постепенной отменой при достижении улучшения.
Также дополнительно применяют витамины группы B и сосудистые препараты.
Используют блокады анестетиками в местах выходов соответствующих ветвей тройничного нерва, акупунктуру и остеопатические методы коррекции.
Физиотерапия
Из физиотерапевтических методов в остром периоде заболевания и во время приступа местно используют умеренное тепловое и/или ультрафиолетовое воздействие. Широко применяют курсовое воздействие диадинамическими токами, которые оказывают обезболивающее и противовоспалительное воздействие. В упорных случаях возможно использование анальгетиков типа прокаин, тетракаин, эпинефрин.
В подостром периоде положительно зарекомендовал себя эндоназальный электрофорез 4% раствора прокаина и 2% раствор витамина В1.
В случае хронических форм НТН показан массаж лица, грязевые или парафин-озокеритовые аппликации на воротниковую область.
Многообещающие перспективы сосредоточены на использовании ботулинического токсина. [18]
Хирургическое лечение
При неэффективности консервативной терапии показаны нейрохирургические методы лечения:
- невротомию или нервэктомию (перерезание или удаление нерва);
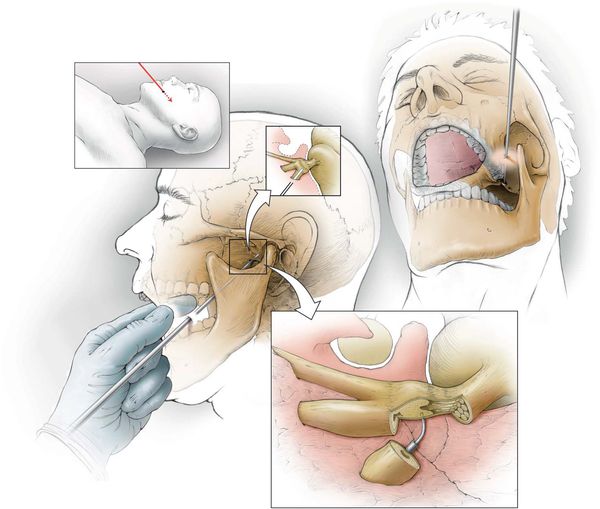
- клипирование аневризматически расширенных артерий — на мешотчатое расширение артерии накладывается металлическая скобка, прекращающая кровоток в этом расширении;
- ликвидация сдавления нерва в костных каналах внутри черепа — частично удаляются костные стенки канала;
- термическая коагуляция узла тройничного нерва;
- операции на гассеровом узле и чувствительном корешке тройничного нерва — электрокоагуляция, криодеструкция. [14][15][16][17]
Дополнительные методы лечения
Также используются когнитивно-поведенческая терапия, физические упражнения, релаксация, биологическая обратная связь, окклюзионные шины и трейнеры, массаж и многое другое как дополнительные методы помощи при хронических лицевых болях. [19]
Как снять боль при невралгии тройничного нерва
Самолечение при невралгии тройничного нерва может навредить пациенту. Уменьшить и предотвратить вероятность новых приступов можно, если своевременно лечить воспалительные и инфекционные заболевания, уменьшить психоэмоциональное перенапряжение, соблюдать режим труда и отдыха, не злоупотреблять алкоголем, острыми и горячими блюдами.
Прогноз. Профилактика
Прогноз эффективности лечения и длительности ремиссии зависит от степени нарушения тройничного нерва, своевременности начатого лечения, а также возраста пациента. Бесспорно, наилучший прогноз восстановительного лечения НТН можно ожидать при вторичных симптоматических проявлениях, когда причина не вызывает сомнения и хорошо поддаётся соответствующей терапии (например, одонтогенная или инфекционная НТН). При идиопатических НТН, этиология которых не ясна, курация наиболее затруднительна.
Профилактика прозопалгий имеет большое значение вследствие малых надежд на полное излечение хронических форм невралгий, поэтому профилактические мероприятия, в основном, сводятся к своевременному лечению заболеваний, которые могут провоцировать развитие НТН. Особое внимание необходимо уделить санации зубов, лечению ринитов и гайморита.
Важным условием профилактики является отсутствие переохлаждений и сквозняков. Необходимо избегать психотравмирующих факторов, закаляться. Немаловажная роль в профилактике принадлежит саногенезу, так как любое интеркуррентное заболевание как инфекционного, так и соматического плана, приводящее к ослаблению защитных сил организма, может привести к обострению НТН. [20] [21]
Кафедра оториноларингологии с клиникой Первого Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова, Санкт-Петербург, Россия, 197022
Городской клинический онкологический диспансер, Санкт-Петербург, Россия, 197044
Кафедра оториноларингологии с клиникой Первого Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова, Санкт-Петербург, Россия, 197022
Поражение тройничного нерва при герпетической инфекции в оториноларингологии
Журнал: Вестник оториноларингологии. 2016;81(4): 19‑21
Кафедра оториноларингологии с клиникой Первого Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова, Санкт-Петербург, Россия, 197022
Нейротропизм герпетической инфекции обусловливает разнообразный спектр ее клинических проявлений. Цель - исследование особенностей поражения тройничного нерва при герпетической инфекции. Проведено обследование и этиопатогенетическое лечение 36 больных с невропатией тройничного нерва, обусловленной ВПГ 1-го типа, и 21 больного с невропатией тройничного нерва, обусловленной Herpes zoster oticus. Помимо традиционных клинических методов использованы вирусологическая диагностика для верификации герпетической инфекции и электронейрография. Выздоровление отмечено у 23 больных 1-й группы и у 11 - 2-й группы.
Кафедра оториноларингологии с клиникой Первого Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова, Санкт-Петербург, Россия, 197022
Городской клинический онкологический диспансер, Санкт-Петербург, Россия, 197044
Кафедра оториноларингологии с клиникой Первого Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова, Санкт-Петербург, Россия, 197022
Герпетическая инфекция (ГИ) является одной из актуальных медицинских проблем 1. На территории России и стран СНГ различными формами герпетической инфекции ежегодно страдают 20 млн человек [1]. В Санкт-Петербурге регистрируется 23 000-25 000 случаев поражений нервной системы при герпетической инфекции ежегодно [1]. Нейротропизм Г.И. обусловливает разнообразный спектр ее клинических проявлений [1, 4-6]. Например, только при Herpes zoster oticus (ушной герпес) выделяют 12 клинических форм. Возможность поражения герпес-вирусами черепно-мозговых нервов и последующего периневрального распространения приводит к тяжелым функциональным, органическим и косметическим расстройствам. После инфицирования низковирулентные штаммы вируса простого герпеса (ВПГ) в организме человека переходят в латентное состояние и находятся в стадии провируса в чувствительных ганглиях ЦНС: тройничном, пояснично-крестцовом, крестцовом [1, 7-9].
В большинстве случаев распространение ВПГ начинается из самого крупного ганглия - гассерова узла, который расположен между листками твердой мозговой оболочки в одноименной выемке передней грани пирамиды височной кости. Общность строения сенсорных ганглиев, анатомические предпосылки, развитая сосудистая сеть и множественные коллатерали нервных волокон позволяют предполагать возможность распространения ВПГ с поражением вестибулярного, спирального, тройничного и коленчатого ганглиев [4-6, 10].
Цель - исследование особенностей поражения тройничного нерва при герпетической инфекции.
Среди проходивших обследование и лечение в клинике оториноларингологии Первого Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова за период с 2010 по 2015 г. поражение тройничного нерва было выявлено у 21 больного с Herpes zoster oticus и у 36 - с невралгией тройничного нерва, вызванной ВПГ 1-го типа. Всем пациентам проводились неврологическое обследование и лабораторная вирусологическая диагностика для верификации ВПГ 1-го и вируса герпеса человека (ВГЧ) 3-го типов. В исследование были включены пациенты с высоким (более 1:800) титром специфических IgG. Также проводилось исследование на авидность (определение высокоспециализированных и низкоспециализированных антител). У всех в последующем подтвердилась либо первичная герпетическая инфекция (положительная полимеразная цепная реакция (ПЦР) крови и слюны при показателе авидности <30%), либо рецидив хронической герпетической инфекции (положительная ПЦР крови и слюны при авидности >40%).
Из 36 пациентов с невралгией тройничного нерва (23 женщины и 13 мужчин в возрасте от 21 года до 68 лет) большинство пациентов обращались в начальной стадии заболевания в связи с выраженным болевым синдромом и с подозрением на острый синусит, острый отит. 26 больных связывали появление головных болей с перенесенным ОРВИ или переохлаждением. У 12 больных в этот период имелись признаки Herpes labialis, у 6 - Herpes nasalis. Как известно, при раздражении тройничного нерва возникают интенсивные приступообразные боли в лице. По своей локализации боли совпадают обычно с проекцией одной из трех ветвей нерва. Из 32 больных у 30 пациентов болевой синдром соответствовал поражению n. ophtalmicus и n. maxillaris, у 6 - n. mandibullaris.
Из 21 больного с Herpes zoster oticus было 11 женщин и 10 мужчин в возрасте от 32 до 70 лет. 11 пациентов обратились в течение первой недели от момента заболевания, остальные спустя 7-8 дней, когда появлялись первые симптомы неврита лицевого нерва. 13 больных связывали развитие заболевания с переохлаждением, 8 - со стрессовой ситуацией. Как правило, заболевание начиналось с появления везикулярных высыпаний на ушной раковине, головных болей, недомогания, в последующем появлялись симптомы поражения лицевого, тройничного и слухового нервов. Все пациенты обследовались в острой стадии заболевания и наблюдались до стойкой стабилизации состояния.
Больным проводилось исследование тригеминофациального рефлекса. Как известно, лицевой нерв, являясь преимущественно двигательным нервом, обеспечивающим мимические движения, имеет тесные связи с чувствительными центрами тройничного нерва. Это взаимодействие получило название тригеминофациального рефлекса (ТФР). Впервые, используя методику электронейрографии, данный рефлекс зарегистрировал E. Kugelberg в 1952 г., описав его как рефлекс мигания при раздражении нижнеглазничной ветви тройничного нерва (регистрация осуществлялась с круговой мышцы глаза). Позднее исследования были проведены и для других мимических мышц при электростимуляции ветвей тройничного нерва. В отличии от прямого ответа круговой мышцы глаза, регистрируемого при стимуляции лицевого нерва, ТФР является рефлекторным ответом и состоит из двух компонентов: раннего (R1) и позднего (R2).

Таблица 1. Параметры ТФР в контрольной группе, М±m

Таблица 2. Параметры ТФР у больных с невропатиями тройничного нерва герпетической этиологии, М±m
При сравнении параметров ТФР больных с невропатиями тройничного нерва с показателями в контрольной группе выявлено статистически достоверное увеличение значений латентного периода R1-ответа и ипсилатерального R2 (р<0,001) по сравнению с контрольной группой, что свидетельствует о нарушении проведения возбуждения по системе тройничного нерва. Таким образом, исследование ТФР при поражениях тройничного нерва позволяет выявлять нарушения нервной проводимости.
При лечении герпетических невропатий тройничного нерва была использована следующая схема комплексной терапии:
1. Ацикловир в течение 3 нед по 800 мг 4 раза в сутки или валтрекс по 500 мг 2 раза в день в течение 7 дней.
3. Ибупрофен по 200 мг 4 раза в день или карбамазепин 200 мг 2 раза в день.
4. Мильгамма по 2 мл внутримышечно ежедневно в течение 10 дней, затем мильгамма композитум - внутрь по 1 драже 3 раза в день в течение 6 нед.
Все больные с Herpes zoster oticus получали пролонгированный курс лечения ацикловиром. Пациенты с герпетической невропатией тройничного нерва, обусловленной ВПГ 1-го типа, получали недельный курс валтрекса (валацикловира) гидрохлорида. В организме человека валацикловир быстро и полностью превращается в ацикловир под воздействием валацикловиргидролазы. Ацикловир in vitro обладает специфической ингибирующей активностью в отношении вирусов Herpes simplex типа 1 и 2, Varicella zoster и Эпштейна-Бар, цитомегаловируса и вируса герпеса человека типа 6. У пациентов с сохраненным иммунитетом вирусы Herpes simplex и Varicella zoster с пониженной чувствительностью к валацикловиру встречаются крайне редко. Для лечения заболеваний, вызванных вирусом Herpes simplex, взрослым назначали валтрекс по 500 мг 2 раза в сутки в течение 7 дней.
Основная сложность лечения больных с герпетическими невропатиями тройничного нерва обусловлена недостаточной эффективностью применения обычных анальгетических средств (производные метамизола, ибупрофена), что нередко является показанием к применению препаратов иных групп, в частности - карбамазепина, габапентина или амитриптилина. Для купирования болевого синдрома при невропатиях тройничного нерва, обусловленных ВПГ 1-го типа, в основном назначался нурофен (ибупрофен) по 200 мг 4 раза в день. При невропатиях тройничного нерва, обусловленных Herpes zoster oticus, как правило, назначался карбамазепин. Карбамазепин на протяжении последних нескольких десятилетий остается наиболее эффективным и доступным лекарственным средством при лечении больных с невралгией тройничного нерва. При этом максимальная эффективность карбамазепина (в качестве средства монотерапии) проявляется в начальном периоде заболевания. Основным показанием к назначению карбамазепина является приступообразно возникающая боль, охватывающая область иннервации тройничного нерва. Суточная доза карбамазепина при тригеминальной невропатии обычно составляет 200 мг 2 раза в день. Дозу препарата можно увеличивать до 800 мг в сутки и в последующем переходить на поддерживающие дозы по 200 мг 2 раза в день по мере регресса невропатии. Лечение больных с поражением тройничного нерва включало также применение высоких доз витаминов группы В в форме поликомпонентных препаратов мильгамма и мильгамма композитум.
Результаты лечения больных с невропатией тройничного нерва, обусловленного ВПГ 1-го типа, оказались достаточно оптимистичными: из 36 больных у 23 пациентов на фоне противогерпетической терапии и приема ибупрофена болевой синдром претерпел обратное развитие в течение первых 10 дней. У 8 пациентов явления невропатии сохранялись в течение 11-17 дней, болевой синдром был купирован при переходе на лечение карбамазепином. У 5 больных лечение оказалось малоэффективным.
Из 21 больного с невропатиями тройничного нерва, обусловленными Herpes zoster oticus, полностью купировать болевой синдром удалось только у 11 пациентов, у 6 удалось достичь значительного улучшения, у 4 пациентов существенной динамики от проводимого лечения не было отмечено (пациенты были выписаны с рекомендацией продолжить прием карбамазепина).
Таким образом, несмотря на успехи в лечении герпетических поражений современными противогерпетическими препаратами, проблема постзостерной невропатии тройничного нерва остается актуальной, что, вероятнее всего, связано с демиелинизирующими процессами, которые происходят при Herpes zoster oticus как в стволе тройничного нерва, так и в гассеровом узле.
Особенности вирусной инфекции нервной системы у детей в зависимости от возбудителя
а) Паралитический полиомиелит. С широким распространением вакцинации случаи полиомиелита стали крайне редкими, и повсеместное уничтожение вируса остается приоритетной задачей ВОЗ. Около 90-95% инфекций полиовируса являются субклиническими, 5% проявляются в виде легкой формы заболевания с фебрилитетом и 1-2% в основном дают симптоматику поражения ЦНС либо менингоэнцефалита, либо полиомиелита.
При полиомиелите в патологический процесс вовлекаются клетки передних рогов, двигательные и чувствительные черепные ядра продолговатого мозга, ретикулярная формация, червь мозжечка и в меньшей степени, таламус и III и V слои моторной зоны коры. Нейроны подвергаются дегенеративным изменениям, сопровождающимся вначале полиморфноядерной реакцией, которая позднее становится мононуклеарной.
Клинические проявления возникают после инкубационного периода, который длится 3-35 дней. Первоначальные симптомы включают головную боль, тошноту и лихорадку, а вслед за ними в течение 2-5 дней менингеальные симптомы раздражения и сильную боль в нижней части спины и конечностях. В серьезных случаях паралич появляется в течение первых двух дней.
Обычный спинальный полиомиелит характеризуется асимметричным вялым параличом, затрагивающим ноги, руки и/или туловище с отсутствием сухожильных рефлексов. Задержку мочи при начале заболевания демонстрируют 20-30% пациентов. Бульбарная форма редко бывает изолированной, распространяясь по меньшей мере на шейный отдел спинного мозга в 90% случаев. Могут поражаться все мышцы, иннервируемые черепными нервами. Кроме того, дыхательная недостаточность и гипертензия может быть результатом повреждения стволовой ретикулярной субстанции. Заболевание может сопровождаться энцефалитическими признаками, но они могут также вызываться и дыхательной недостаточностью из-за паралича диафрагмальных и межреберных мышц.
В анализе СМЖ обнаруживают 30-200 клеток/мм3. Изначально преобладают полиморфноядерные клетки, затем через 5-7 дней сменяющиеся лимфоцитарным плеоцитозом. Содержание белка повышается поздно, достигая максимальных значений примерно на 25 день заболевания.
По данным МРТ описано развитие отека спинного мозга с патологическим сигналом от центральной его части (Kibeetal., 1996). До начала клиники вирус может выделяться из кала и ротоглотки первые 19 дней и до трех месяцев после первых клинических проявлений (в среднем пять недель). При типировании вируса определяют один из трех типов полиовируса. Серологический диагноз ставится на основании повышения титра нейтрализующих или комплемент-связывающих антител.
Прогноз паралитического полиомиелита зависит от степени вовлечения. Восстановление поврежденных мышц часто происходит в течение года и более, но если через месяц мышцы все еще остаются парализованными, то обычно окончательно. Прогрессирующая болезнь моторных нейронов (постполиомиелитный синдром), напоминающий амиотрофический склероз, иногда наблюдается у взрослых через 20 и более лет после острого начала заболевания (Dalakas et al., 1986).
Случаи паралитического полиомиелита, связанного с живой вакциной, могут встречаться у пациентов с иммунодефицитом, получивших вакцину или контактировавших с вирусом (Nkowane et al., 1987; Sen et al., 1989; Groom et al., 1994). При этом возможны атипичные проявления. Поскольку редкие случаи полиомиелита могут также возникать у детей без иммунодефицита после живой вакцины (Dussaix et al., 1987), с уменьшением уровня заболеваемости во всем мире, в большинстве развитых стран сейчас используют убитую инъекционную полиовакцину при плановой вакцинации для предупреждения этого осложнения.
Постановка диагноза не представляет трудностей при условии, если не упускать из вида именно это заболевание. Синдром Гийена-Барре отличается от полиомиелита по характеру начала, симметричности распределения слабости и по данным ликвора. Регистрировались редкие случаи паралитического заболевания, связанного с другими вирусами (Kylleman et al., 1993). Вирус Западного Нила вызывал эпидемии заболеваний, напоминающих паралитический полиомиелит.
Случаи интоксикации химикатами или укусов насекомыми также могут имитировать сходную клиническую картину (Gear, 1984).

б) Энтеровирусы. Первоначальная классификация энтеровирусов, до геномного анализа, была основана на цитопатическом эффекте различных культивируемых клеток и инфицированных животных. Были выделены три типа полиовирусов, 24 коксаки-вируса типа А и 6 коксаки-вирусов типа В вирусов и 34 типа ЕСНО-вирусов. Последующие выделенные энтеровирусы обозначались номером, начиная от энтеровируса 68 без дальнейшего подразделения. Позднее геномный анализ последовательности частично подтвердил первоначальную культуральную классификацию.
Эти вирусы внедряются в организм хозяина через желудочно-кишечный тракт, где реплицируются и вызывают виремию, способную привести к инфекции ЦНС. В большинстве случаев отмечается слабый желудочно-кишечный вирусный продром, а в анамнезе присутствуют данные о наличии у членов семьи схожих симптомов. Большая часть случаев протекает в легкой форме с быстрым выздоровлением. Микроорганизмы можно обнаружить с помощью ПЦР или выделить из ликвора, а также из крови, кала и ротоглотки. При экспресс-диагностике ПЦР результаты можно получить через несколько часов. Инфекция встречается в любом возрасте, включая первые недели жизни (Kaplan et al., 1983).
Энтеровирусы Коксаки В1-5 и Коксаки А7, 9 и 25, ЕСНО-вирусы 4,6,9,11,14,16,18,20 и 30, так же как полиовирусы обычно вызывают асептический менингит. Острый эпидемический конъюнктивит, связанный с энтеровирусом 70, может осложняться менингитом, параличом черепных нервов или поражением конечностей, изолированно или совместно. Характерны сильные боли и фасцикуляции (Wadia et al., 1983; Chopra et al., 1986).
Менингит, вызванный вирусом Коксаки группы А, может сопутствовать или предшествовать герпангине, респираторным инфекциям и паротиту. Среди заболеваний группы В могут встречаться плевродиния (болезнь Борнхольма или эпидемическая миалгия) или диарея. Осложнением менингита могут быть миокардит и энцефалит, особенно у детей раннего возраста (Kaplan et al., 1983). Инфекции ЕСНО-вирусов могут вызывать как спорадические случаи, так и эпидемии. Пятнистопапулезная сыпь особенно характерна при инфекциях вирусов ECHO 4, 9 и 16. Иногда сыпь появляется при Коксаки А9 и А23. Также может быть петехиальной.
В литературе сообщалось о последствиях энтеровирусных менингитов (Kaplan et al., 1983). Вероятней всего, они являются результатом развития энцефалита, сопутствующего менингиту. Они особенно характерны при неонатальном энтеровирусном менингите, который также представлен лихорадкой, плохим аппетитом, диареей, гепатомегалией и сыпью (Huang et al., 2003).
Энтеровирусы также могут быть причиной других проявлений заболеваний ЦНС, включая паралич нижних двигательных нейронов (вирус Коксаки А4, 7, 9, В5, вирус ECHO 70); синдром Гийена-Барре и поперечный миелит (Коксаки А9, В1, 4, ECHO 6, 70); церебральную атаксию (Коксаки А9, 4, 7, В3, 4, ECHO 6, 9, 71); периферический неврит (ECHO 9). Энтеровирусы обычно вызывают самопроходящие заболевания, которые, хотя и связаны с заболеваемостью, редко заканчиваются смертельным исходом. Однако в некоторых более уязвимых группах пациентов (например, у младенцев или детей с иммунодефицитом) энтеровирусы могут вызывать угрожающие жизни инфекции.
Плеконарил — антивирусный препарат, который встраивается в капсид пикорнавирусов, включая энтеровирусы, предупреждая прикрепление вирусов к клеточным рецепторам и высвобождение вирусной РНК в клетку. Клинические испытания плеконарила показали некоторую эффективность у пациентов с тяжелой формой заболевания (Rotbart и Webster, 2001); к сожалению, этот лекарственный препарат не выпускался в промышленном масштабе.
в) Вирус эпидемического паротита. Среди неиммунизированного населения свинка выявляется как наиболее частая причина вирусного асептического менингита. Классическая клиническая картина лептоменингита встречается у 0,5-2% пациентов, больных эпидемическим паротитом. Однако плеоцитоз наблюдался только у 56% таких пациентов с паротитом (Russell и Donald, 1958). Паротит в 30-40% случаев может отсутствовать (Levitt et al, 1970), и в таких случаях диагноз можно получить при ПЦР амплификации вирусного генома в СМЖ или серологическими методами. Симптомы менингита появляются с 8 по 20 день после начала паротита. Часто сопровождаются выраженной лихорадкой.
В ликворе наблюдается лимфоцитарный плеоцитоз, нередко значительный, с сотнями клеток/мм 3 . Содержание глюкозы может быть снижено (Wilfert, 1969). Хотя заболевание обычно протекает в легкой форме, плеоцитоз может присутствовать на протяжении нескольких месяцев с длительным сохранением специфических интратекальных олигоклональных IgG (Vandvik et al., 1978a).

г) Вирусы герпеса. Некоторые представители семейства герпесвирусов могут вызывать лимфоцитарный менингит.
• Вирус простого герпеса. ВПГ 2 типа (Nahmias et al., 1982) чаще отвечающий за болезнь, чем 1 тип, который главным образом вызывает энцефалит. Менингит, вызванный ВПГ-2, может быть проявлением первичной инфекции у сексуально активных подростков. Иногда, легкие случаи ВПГ-1 инфекции могут проявляться только в виде раздражения мозговых оболочек (Whitley et al„ 1982а) с выздоровлением пациентов через 7-14 дней.
• Вирус опоясывающего герпеса. Вирус может вызывать асептический менингит, а также более сложное поражение ЦНС, описанное в следующем разделе. Могут встречаться пре-эруптивные неврологические проявления (Tsolia et al., 1995). В этом исследовании, у двоих детей с энцефалитом сопутствующей патологией была атаксия. Другие очаговые неврологические дефициты, кроме атаксии, развились у семи детей: у троих паралич лицевого нерва, у одного сопровождающая гемиплегия, двое имели парез верхних конечностей, у одного был радикулит, перешедший в парез ноги, и у одного ребенка паралич отводящего нерва. У двоих детей наблюдался изолированный менингит. В этой группе только двое детей переживали длительные последствия: у одного наблюдался стойкий паралич руки, у другого паралич отводящего нерва.
Другие синдромы ЦНС, связанные с вирусом ветряной оспы, включают вирусный миозит, радикулопатию, миелит и отсроченный гемипарез после ветряной оспы (Kamholz и Tremblay, 1985; Ichiyama et al., 1990; Rosenfeld et al., 1993; Herrold и Hahn, 1994; Gilden, 2004; Mariotti et al., 2006). Сообщалось также о поражении базальных ганглиев (Silverstein и Brunberg, 1995) и латеральном медуллярном синдроме (Kovacs et al., 1993). Сосудистые явления ишемического характера, часто поражающие крупные мозговые артерии, нередко отмечаются после ветряной оспы (Amlie-Lefond et al., 1995; Tsolia et al., 1995; Lanthier et al., 2005; Losurdo et al., 2006).
Острые артериопатии, приводящие к ишемическим инсультам, могут быть причиной четверти случаев тромбоза мозговых артерий в детском возрасте; в исследовании Guillot et al. (2005) наиболее вероятным этиологическим фактором в 60% случаев определена ветряная оспа (Guillot et al., 2005). Вероятно, при постинфекционных состояниях действует несколько механизмов, а в некоторых случаях важны воспалительные процессы в стенке артерий, так же как повышенная секреция прокоагулянтов, таких как антикардиолипин (Kurugol et al., 2000, 2001).
Кроме того, иммунная реакция хозяина на вирус ветряной оспы включает образование антител, способные на перекрестную реакцию и инактивацию белка S, важного фактора антикоагуляции хозяина. Это может привести к состоянию гиперкоагуляции и развитию молниеносной пурпуры, также как к ишемическому инсульту после Varicella zoster (Josephson et al., 2001).
• Вирус Эпштейна-Барр (ЭБВ). Большинство инфекций ЭБВ в раннем периоде жизни протекает бессимптомно, неврологические осложнения редки; они могут включать в себя асептический менингит, проявления энцефалита и некоторые другие осложнения ЦНС (Hung et al., 2000). Менингит может предвещать некоторые другие неврологические осложнения, такие как инфекционный полиневрит (синдром Гийена-Барре), энцефаломиелит или поражение черепных нервов (Hausler et al., 2002) или паркинсонизм (Hsieh et al., 2002). Примерно у трети пациентов с инфекционным мононуклеозом при исследовании СМЖ обнаруживают >5 клеток/мм 3 и такие показатели могут сохраняться месяцами, часто после полного клинического выздоровления (Pejme, 1964). Полное выздоровление может откладываться на несколько недель и месяцев.
• Вирус герпеса человека (ВГЧ) 6 и 7. ВГЧ-6 инфекция является причиной внезапной экзантемы (exanthema subitum), и в редких случаях вызывает менингоэнцефалит у здоровых прежде детей (Asano et al., 1992; Jones et al., 1994). Хотя большинство первичных инфекций ВПГ-6 (и тесно связанного ВПГ-7) протекают бессимптомно, оба вируса причастны к более 30% фебрильных судорог, встречающихся в первые два года жизни (Hall et al., 1994; Barone et al., 1995; Ward, 2005).
г) Аденовирусные инфекции нервной системы. Выделено множество типов аденовирусов; большинство вызывает легкие инфекции желудочно-кишечного тракта, дыхательной системы или почек и только в редких случаях они являются причиной синдромов поражения ЦНС. Проявления включают асептический менингит, миелит, подострый очаговый энцефалит, Рейе-подобный синдром и преходящую энцефалопатию (Linssen et al., 1991; Straussberg et al., 2001).
д) Парвовирус В19. Большинство инфекций парвовируса В19 имеют бессимптомное течение, но симптоматическая инфекция у детей обычно проявляется в виде лихорадки и сыпи, а у взрослых могут быть артропатии. Также сообщалось о редких случаях ЦНС инфекции с признаками менингоэнцефалита и определением вирусной ДНК в ликворе (Barah et al., 2001, 2003). Иммунный ответ хозяина к парво В19 в ЦНС считается предположительной причиной воспаления с подтверждением повышенного уровня цитокинов в ликворе, так же как специфического HLA-генома хозяина (Kerr et al., 2002).
е) Вирус лимфоцитарного хориоменингита (вирус ЛХМ). Вирус ЛХМ является человеческим зоонозом, вызываемым распространяемым грызунами ареновирусом, поражающим полевых мышей. Вирус передается человеку после контакта с выделениями зараженных мышей, морских свинок и хомяков. Внутриутробная инфекция у человека может привести к поражению плода (Barton и Mets, 2001; Barton et al., 2002), тогда как постнатальное инфицирование обычно протекает бессимптомно или как простудное заболевание, но может встречаться и синдром вовлечения ЦНС (Barton и Hyndman, 2000).
ж) Другие и неопределенные вирусы. Они, вероятно, являются причиной многих случаев заболеваний — в действительности большинства, в которых не могут быть выделены патогенные микроорганизмы. Понятно, что число возможных вирусных агентов велико, и поскольку заболевание обычно протекает в легкой форме, сложные исследования не проводятся.
Читайте также:

