Вирусные гастроэнтериты у животных
Обновлено: 18.04.2024
Гастроэнтерит собак и кошек – довольно широкий термин, означающий наличие воспалительного процесса в желудке и кишечнике. Является распространенной причиной острой рвоты, анорексии и диареи, однако стоит понимать, что с подобными симптомами могут протекать и панкреатит, и гепатит, и непроходимость кишечника. Причин для воспаления ЖКТ множество, например, изменение диеты, инфекционные организмы, токсины, нарушения в работе иммунной системы, метаболические расстройства. Сбор анамнеза и физикальный осмотр иногда позволяют установить, почему началось воспаление, но в большинстве случаев специфическая причина так и не бывает обнаружена. Зачастую для полного исчезновения симптомов достаточно симптоматической терапии, включающей инфузионную поддержку, диету, противорвотные средства и гастропротекторы. Тем не менее, в некоторых случаях может произойти быстрая декомпенсация, обычно вторично к гиповолемии, потере жидкости и нарушениям КЩР.
Анатомия и физиология
Желудок – это участок ЖКТ между пищеводом и тонким кишечником, который выполняет функции накопительного резервуара для пищи, а также здесь происходит измельчение и перемешивание пищи, поступающей затем в тонкий кишечник. Желудок состоит из мышечных слоев, участков с железистой тканью и слизистой. С помощью движений мышц желудок измельчает пищу и продвигает ее через пилорический сфинктер в тонкий кишечник. Железистые участки не менее важны: пристеночные клетки секретируют соляную кислоту, основные клетки секретируют пепсиноген, слизеобразующие клетки также секретируют бикарбонат. Благодаря барьерной функции слизистой желудка соляная кислота и пищеварительные ферменты удерживаются в просвете желудка, что препятствует потере компонентов плазмы в желудок. Как только пища в желудке достаточно измельчилась, она через пилорический сфинктер продвигается в тонкий кишечник, начало которого называется двенадцатиперстной кишкой.
Энзимы щеточной каймы разрушают более крупные молекулы до более мелких, которые легче всасываются. Абсорбция обычно происходит с помощью специальных транспортных механизмов или пиноцитоза. Эпителиальные клетки также вовлекаются в процессы абсорбции и секреции воды и электролитов. Энтероциты плотно связаны между собой, чтобы ограничить всасывание между клетками и препятствовать обратному току питательных веществ – из интерстиция в просвет кишечника. Продолжительность жизни энтероцитов колеблется от 2ух до 5и дней; они стартуют от крипт (основа ворсинок) и мигрируют по направлению к просвету кишечника. Здоровая, неповрежденная слизистая оболочка играет большую роль в сохранении целостности кишечника. Любое воспаление, нарушающее целостность слизистой, может привести к серьезному заболеванию кишечника. Немаловажно помнить, что ЖКТ всасывает 99% воды, поступающей в него, следовательно, любые нарушения в работе ЖКТ могут приводить к серьезным расстройствам водного и электролитного баланса организма.
Анамнез и клинические признаки воспаления кишечника и желудка у собак
С особой тщательностью собранный анамнез при симптомах гастроэнтерита у собак и кошек – основа определения причины воспаления кишечника. Необходимо спросить, что пациент ест обычно, не менялась ли последнее время его диета, имелся ли в последнее время доступ к непривычной еде, инородным телам, мусору, токсинам. Необходимо также выяснить, общался ли пациент с другими животными, и если да, то не было ли у этих животных похожих симптомов или истории таковых. Кроме того выясните при сборе анамнеза вакцинальный статус пациента, историю дегельминтизаций и использования медикаментов.
Клинические признаки гастроэнтеритов различной этиологии похожи и мало зависят от причины заболевания. Диарея, рвота, анорексия – наиболее распространенные симптомы, и различные комбинации этих признаков могут в большей степени указывать на одну причину, чем на другую. Серьезное воспаление или изъязвление слизистой может приводить к гематемезису или мелене.
Физикальный осмотр, как правило, не помогает установить причину заболевания. Вы можете обнаружить у пациента разную степень дегидратации и абдоминальной боли. В тяжелых случаях, при парвовирусном энтерите или ГГЭ, у пациента можно обнаружить признаки гиповолемии и шока, вторичных по отношению к потере жидкости и нарушению КЩР.
Этиология воспаления желудка и кишечника у кошек и собак
Инфекционные гастроэнтериты у мелких домашних животных
ЖКТ поражает масса инфекционных агентов. Вирусы, бактерии, паразиты, грибы могут приводить к гастроэнтеритам различной степени тяжести. В таблице представлены возможные инфекционные причины гастроэнтерита, в тексте же описаны только самые распространенные.
Инфекционные причины гастроэнтеритов собак и кошек
Бактерии:
- Campylobacter spp
- Clostridium spp
- Escherichia coli
- Salmonella spp
- Helicobacter spp
Вирусы:
- Парвовирус
- Ротавирус
- Кишечный коронавирус - коронавирусный гастроэнтерит у кошек
- Инфекционный перитонит кошек
- Вирус чумы собак
- Коронавирусный гастроэнтерит у собак
- Вирус лейкемии кошек
- Вирус иммунодефицита кошек
Грибы, Водоросли и Оомицеты:
- Гистоплазмоз
- Прототекоз
- Питиоз
Паразиты:
- Аскариды (Toxocara canis, Toxocara cati, Toxascaris leonina)
- Нематоды (анкилостомоз, унцинариоз, стронгилоидоз)
- Власоглавы
- Кокцидии (изоспоры, токсоплазмы, криптоспоридии)
- Лямблии
- Трихомонады
- Кишечные балантидии
Риккетсии:
Вирусные энтериты собак и кошек
Одна из самых распространенных инфекционных болезней у собак – парвовирусный энтерит (CPV-2), который может приводить к тяжелому энтериту, рвоте, геморрагической диарее, шоку (глава 112). Также к сильному воспалению кишечника могут привести коронавирус и ротавирус, правда, поскольку эти вирусы поражают только верхнюю часть ворсинок, воспаление редко достигает таких масштабов как при парвовирусном энтерите, поражающем крипты. Таким образом короновирусный гастроэнтерит у кошек - это не редкость У кошек к тяжелому гастроэнтериту приводит панлейкопения, также вызываемая парвовирусом.
Бактериальные энтериты кошек и собак
Бактерии, чаще всего вызывающие острый гастроэнтерит у кошек и собак: клостридии, сальмонеллы, кампилобактерии, хеликобактер, энтеротоксигенная E. Coli. Однако в настоящее время считается спорным утверждение, что некоторые из этих микроорганизмов могут привести к клинически значимому энтериту. Пока вопрос о роли клостридий, кампилобактерий, хеликобактера считается открытым.
Паразитарные гастроэнтериты кошек и собак
Хотя большинство кошек и собак переносят инвазию паразитами без тяжелых расстройств, тем не менее, аскариды, нематоды и власоглавы могут стать причиной сильного воспаления, рвоты и диареи. Из простейших к гастроэнтеритам у животных чаще всего приводят лямблии, кокцидии и криптоспоридии.
Грибковые гастроэнтериты собак и кошек
Грибковые заболевания могут поражать ЖКТ как кошек, так и собак, хотя больше всего вероятность заболевания зависит от географического местоположения пациента. Гистоплазмоз – наиболее распространенное заболевание, которое может привести к тяжелой энтеропатии с потерей белка. Заражение питиозом, вызываемым оомицетом, тоже может привести к схожим последствиям.
Геморрагический гастроэнтерит
Геморрагический гастроэнтерит у собак и кошек – заболевание с неизвестной этиологией. Обычно геморрагический гастроэнтерит поражает собак небольших пород молодого и среднего возраста и характеризуется подострым началом клинических признаков, быстрым прогрессированием и без соответствующей терапии может привести к смерти. Заболевшие животные, как правило, не имели никаких жалоб до этого. Было предположено, что причиной начала заболевания может быть ненормальный иммунный ответ на бактерии, бактериальные токсины или ингредиенты диеты. Хотя C. perfringens была выделена из содержимого кишечника животных, больных геморрагическим гастроэнтеритом, ее точная роль в этиологии заболевания пока не установлена.
При данной патологии показана агрессивная терапия, так как может произойти очень быстрая декомпенсация. Более всего необходимо адекватное восполнение объема жидкости. Основные цели – быстро возместить объем жидкости, потерянной во время острой диареи и рвоты, а затем отрегулировать объем вводимой жидкости таким образом, чтобы постепенно достичь регидратации (подробнее на других страницах сайта). Необходимо помнить, что кишечник – шоковый орган у собак, и недостаточная перфузия может привести к ухудшению гастроэнтерита, транслокации бактерий, сепсису, ДВС. Из-за потерь протеинов плазмы в кишечник особое внимание следует уделить коллоидно-осмотическому давлению и при необходимости осуществлять коллоидную поддержку. Помимо инфузионной терапии может потребоваться введение противорвотных препаратов и антибиотиков (при подозрении на транслокацию). При своевременном и адекватном лечении прогноз на полное восстановление от геморрагического гастроэнтерита хороший.
Наушение диеты
Причиной гастроэнтеритов у собак (реже у кошек) может стать поглощение животным токсинов (например, фосфорорганика), инородных тел, мусора. Некоторые токсины напрямую приводят к воспалению ЖКТ, тогда как инородные тела могут привести к травматическому гастроэнтериту или осмотической диарее (из-за наличия неперевариваемой субстанции внутри ЖКТ). Поедание слишком жирной пищи может привести к панкреатиту. К возникновению рвоты и диареи могут приводить и медикаменты: антибиотики, антибластомные препараты, глистогонные препараты. Съеденный мусор может стать источником бактериальных токсинов. Наиболее часто нарушение диеты приводит к остро развившимся рвоте, диарее и анорексии. Внимательно собирайте анамнез: владельцы должны знать, имело ли животное доступ к специфическим токсинам или мусору. Диагноз этот, как правило, гипотетический и лечение – поддерживающее (инфузионная терапия, противорвотные, гастропротекторы по необходимости). Прогноз хороший и большинство животных восстанавливаются за 24-72 часа.
Энтеропатия с потерей белка (PLE)
Энтеропатия с потерей белка – общий диагноз, который включает в себя гастроэнтериты любой этиологии, приводящие к чрезмерной потере белка плазмы. Чаще всего с термином Энтеропатия с потерей белка ассоциируются следующие заболевания: тяжелые лимфоцитарно-плазмоцитарные, эозинофильные, гранулематозные воспалительные заболевания кишечника, лимфангиэктазия, диффузное грибковое поражение ЖКТ, диффузная неоплазия, например, лимфосаркома. Некоторые из вышеупомянутых заболеваний могут приводить к энтеропатии с потерей белка при достаточно сильной степени поражения слизистой кишечника.
Потеря белка может происходить по механизму воспалительного процесса или из-за нарушения гастроинтестинального барьера. Потеря протеинов очень часто возникает из-за ненормального функционирования энтероцитов, а также при нарушении проницаемости кишечной стенки между энтероцитами. Клинические признаки энтеропатии часто связывают с хроническим истощением из-за недостатка поступления питательных веществ в организм. Однако через кишечник могут теряться и такие белки как альбумин и антитромбин III, которые играют важную роль в процессах гемостаза. Альбумин (молекулярная масса 69.000 дальтон) имеет большое значение для поддержания онкотического давления. Потеря альбумина через ЖКТ может привести к снижению коллоидно-осмотического давления, что часто приводит к потере жидкости из внутрисосудистого пространства. Хотя обычно этот процесс происходит постепенно, тем не менее, он может привести к значимому перераспределению жидкости в организме пациента, и это следует учитывать при назначении инфузионной терапии. Возможно, помимо кристаллоидов потребуется переливание коллоидов или человеческого альбумина, чтобы предотвратить дальнейшие потери жидкости из сосудистого русла. Альбумин имеет дополнительные положительные свойства - антиоксидантные и противовоспалительные.
Антитромбин III играет важную роль в коагуляции и фибринолизе, инактивируя тромбин и другие факторы свертывания. Даже небольшое снижение уровня антитромбина III приводит к значимому увеличению риска тромбозов и тромбоэмболий. Пациенты с энтеропатией с потерей белка, теряющие большое количество белка, имеют предрасположенность к тромбозам сосудов в легких, мозге, портальной вены. Лечение энтеропатии часто включает глюкокортикоиды, которые также увеличивают риск тромбоэмболий. Поэтому в таких случаях часто оправдано использование антикоагулянтов и антиагрегантов.
Лечение энтеропатии основано на лечении основного заболевания. Пациенты с диффузной неоплазией, например, лимфосаркомой должны получать химиотерапию. Пациенты с воспалительными заболеваниями кишечника должны получать противовоспалительную терапию и гипоаллергенную диету. Лимфангиэктазия может быть первичной и вторичной, и кормление диетами с низким содержанием жира может быть более результативным, чем кормление гипоаллергенными кормами, в зависимости от степени воспалительного процесса.
Внекишечные заболевания
Частые внекишечные причины гастроэнтеритов у мелких животных – гипоадренокортицизм, заболевания почек или печени, острый панкреатит, перитонит.
Диагностика
Объем диагностических исследований, которые вы будете проводить собаке, поступившей с симптомами острого гастроэнтерита, зависит от анамнеза, наличия схожих проблем в прошлом и стабильности пациента. Анализ кала на паразитов и бактерии следует проводить всем животным с острым гастроэнтеритом. Помимо окраски по Граму можно выполнить культуральные исследования. Окончательно отрицательным результат считается, если проведено не менее трех исследований кала. Существуют тесты ELISA для выявления энтеротоксинов C. perfringens и токсинов А и В C. difficile. Антигенные тесты существуют и на лямблий, и на парвовирусный энтерит.
Обследование должно включать в себя клинический и биохимический анализы крови, анализ мочи. Обычно результаты этих исследований находятся в пределах нормы и никак не влияют на постановку окончательного диагноза. Однако в некоторых случаях, например, при ГГЭ (когда мы увидим повышение гематокрита при нормальном количестве общего белка) или при PLE (когда мы увидим снижение белка, альбумина, глобулина, холестерина) данные анализов могут помочь в диагностике. Электролиты следует проверять регулярно для назначения адекватной инфузионной терапии.
Рентген брюшной полости может быть не информативным, а может показать заполненные жидкостью петли кишечника. Тем не менее, всегда следует проводить рентгеновское исследование при подозрении на обструкцию кишечника (инородным телом или новообразованием). УЗИ – прекрасный способ обследовать органы брюшной полости, включая толщину и слоистость стенок желудка и кишечника. К сожалению, находки УЗ обследования могут быть неспецифичными, и оценивать их стоит только совместно с данными остальных исследований.
Наиболее распространенные клинические признаки гастроэнтерита – рвота, диарея, анорексия. Эти симптомы характерны для множества заболеваний, поэтому диагностика часто проводится методом исключения. Дифференциальные диагнозы при гастроэнтеритах животных включают в себя такие заболевания как почечная недостаточность, заболевания печени, гипоадренокортицизм, осложненный кетоацидозом сахарный диабет, вестибулярный синдром или другие неврологические отклонения, панкреатит, пиометра, простатит и перитонит. Из первичных заболеваний ЖКТ необходимо обязательно исключить инвагинацию, обструкцию инородным телом, инфильтративные заболевания (неоплазия, инфекции) и ишемию. Эти заболевания следует обязательно исключить, прежде чем ставить диагноз гастроэнтерит.
Лечение гастроэнтерита у собак и кошек
Гастроэнтерит у кошек - лечение должно быть комплексным и воздействовать на причину, патогенез, симптомы. Большинство гастроэнтеритов у кошек и собак хорошо отвечают на поддерживающую терапию. Агрессивность лечения зависит от степени выраженности симптомов и от первопричины заболевания. Поскольку наиболее частые симптомы гастроэнтерита вне зависимости от причины – рвота, диарея и анорексия, дегидратация является довольно распространенной находкой, и соответственно начальная терапия подразумевает нормализацию водного баланса пациента (смотри другие статьи нашего сайта).
Последующее лечение можно разделить на специфическое и симптоматическое. Специфические препараты используются для лечения первопричины заболевания. В большинстве случаев препараты, борющиеся с инфекционными причинами гастроэнтеритов, доступны. Паразитарные инфекции ЖКТ лечат фенбендазолом или другими ангельминтиками. Кампилобактер чувствителен к эритромицину, энрофлоксацину и цефокситину, клостридия – к метронидазолу и ампициллину. Выбор препарата зависит от множества причин, включая возраст пациента и его возможность принимать препараты перорально. В ветеринарной медицине существует крайне мало эффективных противовирусных препаратов, поэтому такие болезни как вирусный энтерит лечат симптоматически. Для лечения пациентов с PLE применяют терапию, воздействующую на причину заболевания, зачастую это смена диеты и противовоспалительные препараты.
Множество препаратов, применяемых для лечения гастроэнтеритов кошек и собак, не специфичны. Помимо инфузионной терапии рекомендуется голодная диета на 24-48 часов, а начинать кормление следует с влажных, хорошо усваиваемых кормов. Применение гастропротекторов и противорвотных средств может ускорить регенерацию энтероцитов. Антибиотики назначают при серьезных гастроэнтеритах, когда велик риск транслокации бактерий, например у щенков с парвовирусным энтеритом. Антибиотикотерапия должна включать препараты, хорошо действующие на грамотрицательные микроорганизмы и анаэробы (то есть на те микроорганизмы, присутствие которых в ЖКТ наиболее ожидаемо).
Прогноз при гастроэнтеритах собак и кошек
Для большинства легких и средней тяжести гастроэнтеритов у собак и кошек прогноз на выздоровление очень хороший. Тем не менее, для положительного результата очень важна ранняя диагностика и своевременная терапия.
Полезно знать
© VetConsult+, 2016. Все права защищены. Использование любых материалов, размещённых на сайте, разрешается при условии ссылки на ресурс. При копировании либо частичном использовании материалов со страниц сайта обязательно размещать прямую открытую для поисковых систем гиперссылку, расположенную в подзаголовке или в первом абзаце статьи.
Гастроэнтерит (gastroenteritis) – Одно из наиболее часто встречающихся заболеваний органов пищеварения у молодняка, характеризующееся воспалением желудка и кишечника, сопровождающееся нарушением пищеварения, интоксикацией и обезвоживанием организма.
Гастроэнтериты по происхождению бывают первичные и вторичные; по характеру воспаления – альтеративные (эрозивно-язвенные, некротические), экссудативные (серозные, катаральные, фибринозные, геморрагические и гнойные) и реже продуктивные; по локализации – очаговые и диффузные; по течению – острые и хронические. Наиболее часто встречаются экссудативные гастроэнтериты.
Этиология. Причины гастроэнтеритов разнообразны, ведущее место среди них принадлежит алиментарным факторам. К ним относятся недоброкачественные и несоответствующие возрастным группам корма, наличие в кормах остаточных количеств токсических веществ или появление их в процессе приготовления, нарушение режима кормления и поения, резкий переход от одного типа кормления к другому и др.
Симптомы. Угнетение, учащение дефекации (понос), жидкие водянистые фекалии. В зависимости от вида воспаления в фекалиях находят: при некротическом – обрывки тканей; эрозивно-язвенном – примесь крови; катаральном – тяжи слизи; геморрагическом – примесь крови; гнойном – серо-желтые комки из лейкоцитов и омертвевших тканей; при фибринозном – пленки фибрина. Животные много лежат, тяжело поднимаются, плохо принимают корм, отмечаются, особенно при воспалениях желудка, позывы к рвоте.
При длительном течении заболевания наступает истощение, анемия и обезвоживание, которые сопровождаются понижением температуры тела, развитием сердечной недостаточности, сгущением крови, западением глаз.
В крови больных животных первоначально увеличивается количество лейкоцитов, затем уменьшается за счет выброса с калом и угнетения кроветворения, возрастает активность трансаминаз, снижается количество гемоглобина, эритроцитов, альбуминов и при хроническом течении возрастает уровень иммуноглобулинов, появляются аутоантитела.
Диагноз и дифференциальный диагноз. Диагноз проводится с учетом глубокого анализа анамнестических данных по кормлению животных, условий содержания, эпизоотической обстановки, особенностей возникновения, развития и течения болезни, патологоанатомических изменений и результатов лабораторных исследований. Характерными клиническими признаками являются потеря аппетита, жажда, рвота, диарея, жидкие водянистые фекалии с примесью экссудата в зависимости от вида воспаления.
Для организации целенаправленного лечения и профилактики больных животных на основании комплексных исследований дифференцируют гастроэнтериты на алиментарные, токсические, аллергические (повторяющиеся на определенные корма), инфекционные и инвазионные.
Лечение. Больных животных выделяют и при необходимости изолируют. Устраняют причину, вызвавшую заболевание. Если гастроэнтериты обусловлены кормовыми токсикозами, отравлениями минеральными ядами, для удаления из желудочно-кишечного тракта принятого корма промывают желудок теплым изотоническим раствором натрия хлорида, 1-2%-ным раствором натрия гидрокарбоната и назначают солевые слабительные и растительные масла в принятых дозах.
С целью устранения дисбактериоза назначают курс антибиотиков, сульфаниламидов и нитрофуранов, к которым чувствительна микрофлора желудочно-кишечного тракта животных. Хороший эффект дают энтеросептол 30-40мг/кг, интестопан 5-10 мг/кг, йодинол 1-2 мг/кг, этоний 10 мг/кг, ЛЕРС 0,5 г/кг в виде 5%-ного раствора, а также трибрисен, тримеразин, трихопол и др., которые задают 2-3 раза в сутки до выздоровления животных.
После устранения причины показаны диетическое кормление и поддерживающая терапия. При назначении диеты необходимо учитывать, что у молодняка в первые 3-4 недели жизни отсутствует активность сахарозы, у телят слабо усваивается растительный белок.
В качестве жидкостей для питья используют чистую прохладную воду, изотонический раствор натрия хлорида, а также сложные растворы электролитов с добавлением 5% глюкозы и 1 % аскорбиновой кислоты. Проводят также регидратационную терапию путем введения изотонических электролитных растворов подкожно и внутрибрюшинно, а гипертонических - внутривенно. Внутрь дают слизистые отвары льняного семени, риса, ячменной и овсяной муки, настои лечебных трав и хорошего сена.
Для ослабления токсикоза и прекращения диареи назначают адсорбенты (гидрат окиси алюминия, уголь активированный, белую глину, лигнин, порошок кутикулы мышечного желудка птиц и др.) и вяжущие (отвары коры дуба, препараты танина, висмута) в принятых дозах. Для улучшения питания и снятия общего токсикоза применяют внутривенно раствор глюкозы, гемодез, полиглюкин, амидопептид, гидролизин, липофундин и других плазмозаменяющих растворов.
С целью повышения резистентности и усиления регенерации эпителия слизистой оболочки и других структур назначают витамины А, Е, C, U и группы В. Для снятия спазма и болей применяют но-шпу, белладонну (красавку), атропин, анестезин, анальгин и др.
После завершения антимикробной терапии для восстановления полезной микрофлоры желудочно-кишечного тракта назначают в течение трех дней внутрь пробиотики.
Профилактика гастроэнтеритов основана на недопущении скармливания молодняку недоброкачественных кормов, соблюдении режима кормления, постепенном переходе от одного типа рациона к другому, недопущении использования кормов не по физиологическому назначению, строгом соблюдении условий содержания, параметров микроклимата и технологии отъема молодняка.
Вирусный гастроэнтерит свиней (трансмиссивный гастроэнтерит свиней, болезнь Дойла и Хитчингса) – Transmisille gastroenteritis – высококонтагиозная вирусная болезнь, проявляющаяся рвотой, тяжелой диареей и высокой смертностью среди поросят до 2-недельного возраста.
Этиология. Возбудитель болезни РНК-содержащий вирус (Porcine transmissille gastroenteritis virus), относящийся к семейству Coronaviridae, роду Coronavirus. Вирус трансмиссивного гастроэнтерита имеет 1 серотип и не имеет связи с вирусом энзоотической диареи свиней, хотя с ним тесно родственны. Главным отличием вируса энзоотической диареи является исключительный пневмотропизм при отсутствии энтеропатогенности.
Возбудитель устойчив к замораживанию. При – 18 °С сохраняется до 18 месяцев, при -20 °Си ниже – до 365 дней. При нагревании до 56 °С инактивируется за 30 мин.
Эпизоотологические данные. Источником возбудителя являются больные или переболевшие свиньи вирусоносители, которые могут выделять вирус с испражнениями, мочой и носовыми истечениями в течение 2 – 3 месяцев после переболевания. Особенно высокая концентрация вируса отмечается в фекалиях в начале болезни, поэтому инфекция распространяется очень быстро. Вирус переносится с продуктами убоя больных и переболевших свиней, спецодеждой и обувью обслуживающего персонала, инфицированными кормами, водой, предметами ухода за животными и транспортными средствами, инфицированными вирусом. Заражение происходит через пищеварительный тракт и дыхательные пути. Если болезнь возникает в хозяйстве впервые, то она протекает в виде эпизоотии, которая в течение 2 – 4 дней охватывает все восприимчивое поголовье свиней. Если хозяйство продолжает оставаться неблагополучным по вирусному (трансмиссивному) гастроэнтериту, то болезнь протекает энзоотически и возникает при завозе новых восприимчивых свиней или при получении беспрерывных опоросов. В данном случае заболевают преимущественно поросята первых пяти дней жизни, смертность среди которых составляет не более 30%. При первичном заносе возбудителя смертность новорожденных поросят достигает до 100%. Болезнь возникает в любое время года, но наиболее часто регистрируется в холодное время.
Течение и симптомы. Инкубационный период весьма короткий и исчисляется часами. Иногда он длится до 3 дней. Болезнь у поросят в начале проявляется рвотой, сразу после приема молозива или молока. Затем появляется диарея. Фекалии водянистые, зелено-желтого цвета, неприятного запаха.
Поросята становятся малоподвижными, кожный покров у них влажный и они скучиваются под обогревательной лампой. По мере развития болезни диарея становится профузной, фекалии непроизвольно вытекают из анального отверстия. Температура тела обычно в пределах нормы. Гибнут поросята на 2 – 3 день с момента появления клинических признаков.
У лактирующих свиноматок внешние симптомы болезни обычно отсутствуют. У некоторых из них наблюдаются диарея, угнетенное состояние, резкое уменьшение или полнее прекращение молока и истощение. Выздоравливают свиноматки быстро, однако секреция молока не восстанавливается, что резко отражается на состоянии здоровья подсосных поросят.
Патологоанатомические изменения. Трупы поросят истощены, кожа темно-серого цвета, видимые слизистые оболочки цианотичны. Желудок растянут и заполнен свернувшимся молоком. Слизистая дна желудка гиперемирована. Тонкий отдел кишечника вздут, содержимое его водянистое, зеленовато-желтого цвета. Стенка кишечника истощена. Слизистая оболочка гиперемирована.
Встречается катаральное и десквамативно-некротическое воспаление. Толстый отдел кишечника катарально воспален. Сосуды брыжейки кровенаполнены, пакеты мезентериальных лимфатических узлов набухание, гиперемированные, на разрезе сочные. Под капсулой почек выявляют мелкоточечные кровоизлияния, граница между корковым и мозговым слоями сглажена. Иногда выявляют скопления экссудата желтоватого цвета или ураты в почечной лоханке. Сердце дряблое, сероватого цвета. В веночной бороздке сердце часто находят петехии. В селезенке могут обнаруживаться застойные явления, напоминающие инфаркты.
Диагноз. Ставят на основании эпизоотологических данных, симптомов болезни и результатов лабораторных исследований, включающих изоляцию вируса на первичных и перевиваемых линиях клеток поросят с последующей идентификацией вируса в РНФ, РН, ВИЭОФ, ELISA и определении титра антител в сыворотке крови реконвалесцентов.
В лабораторию направляют тонкую и подвздошную кишку с содержимым и мезентериальные лимфоузлы от поросят, взятые в первые часы после появления диареи. Материал необходимо брать от 8 – 9 поросят пораженных пометов (по 2 – 3 поросенка из помета). Доставляют патматериал в стеклянных сосудах помещенных в сосуд Дюара с жидким азотом или в термос с сухим льдом.
Дифференциальный диагноз. Дифференцируют вирусный (трансмиссивный) гастроэнтерит от ротавирусной инфекции, колибактериоза, анаэробной энтеротоксемии, сальмонеллеза.
Лечение. Эффективных лечебных средств нет. Используют сыворотку крови реконвалесцентов, аллогенную сыворотку, миксоферрон и симптоматические средства, направленные на борьбу с обезвоживанием, дезинтоксикацию организма и восстановление функционального состояния кишечника. Для подавления бактериальной микрофлоры применяют антибиотикотерапию. Подсосным свиноматкам вводят препараты, предупреждающие развитие агалактии.
Профилактика и меры борьбы. Общие профилактические мероприятия должны быть направлены на недопущение заноса возбудителя болезни, обеспечение свинопоголовья полноценными кормами, обращая внимание на их доброкачественности. Супоросным свиноматкам и новорожденным поросятам должны быть созданы условия, предусмотренные технологией.
При возникновении ВГЭС хозяйство объявляется неблагополучным, и в нем вводятся ограничения регламентированной инструкцией профилактике и мерам борьбы с этой болезнью.
Для специфической профилактики применяют свиноматкам аттенуированные, авирулентные и субъединичные вакцины орально, интраназально и внутримышечно. Поросят-сосунов целесообразно вакцинировать орально, чтобы индуцировать быструю защиту посредством интерференции или стимулирование локального иммунитета, обеспечивающего синтез секреторных Ig A.
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо).
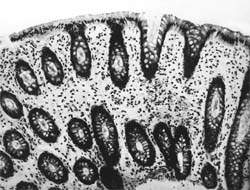 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
Методы диагностики ротавирусной инфекции
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
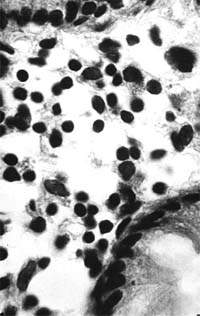 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
- заболевания, вызываемые неустановленным возбудителем (около 70% случаев);
- острые кишечные инфекции, вызываемые установленным возбудителем (около 20%);
- бактериальная дизентерия (около 10%).
Важно, что в наиболее обширную группу ОКИ неустановленной этиологии входят и большинство так называемых пищевых токсикоинфекций (ПТИ) — эту группу составляют приблизительно 20 этиологически разных, но патогенетически и клинически сходных заболеваний, не представляющих эпидемической опасности.
Более чем в половине случаев этиологию ОКИ не удается установить ни клинически, ни лабораторно. Эта задача, равно как и выбор патогенетического лечения, тем более не может быть решена (да и не ставится) на этапе догоспитальной помощи. Усилия врача скорой медицинской помощи (СМП) должны быть направлены на:
- коррекцию тяжелых нарушений жизненно важных функций организма больного;
- дифференцирование инфекционного, терапевтического или хирургического генеза заболевания;
- решение вопроса о необходимости госпитализации больного для специализированного лечения или проведения противоэпидемических мероприятий.
Клиническая картина ОКИ
ОКИ — заболевания различной этиологии и семиотики — объединяют общий для всех этих состояний, преимущественно фекально-оральный, способ передачи возбудителя и развитие вследствие этого характерного симптомокомплекса острой диареи (табл. 1).
ПТИ также относятся к БД, так как вызываются условно-патогенными бактериями и в ряде случаев имеют групповой, эксплозивный характер. Однако в подавляющем большинстве случаев ПТИ протекают спорадически с развитием острого гастрита, гастроэнтерита или гастроэнтероколита, с той или иной степенью обезвоживания и интоксикации и имеют благоприятный прогноз.
При диарее вирусной этиологии (ВД) целостность слизистой оболочки желудочно-кишечного тракта в большинстве случаев не нарушается и в процесс редко вовлекается толстая кишка. Инкубационный период, как правило, более короткий, чем при эпидемической БД. Острый вирусный гастроэнтерит, хотя и сопровождается лихорадкой и нарушением общего состояния больного, редко приводит к тяжелой интоксикации, развитию выраженной воспалительной реакции и дегидратации организма больного. К числу значимых дифференциальных критериев ВД можно отнести отсутствие при этих заболеваниях выраженной боли в животе, водянистый, а не слизисто-гнойный и кровавый характер испражнений. ВД нередко сопровождается острым респираторным заболеванием, особенно у детей. Продолжительность ВД редко превышает 3 дня, и в целом заболевание имеет благоприятный прогноз. Пациенты с относительно легким течением ВД в госпитализации не нуждаются.
Из ОКИ паразитарного происхождения (ПД) наибольшее клиническое значение имеют амебиаз и лямблиоз. Известно, что клиническая картина амебной дизентерии развивается приблизительно у 10% инфицированных амебой больных. Амебный колит характеризуется сильнейшей болью в животе, лихорадкой и кровавой диареей, которая чревата перфорацией толстой кишки. Генерализация амебиаза сопровождается септикопиемией с образованием абсцессов печени, легких или головного мозга и крайне неблагоприятным прогнозом для жизни больного. Заболевание носит эндемичный характер. Лямблиоз на территории России распространен очень широко и в 25-50% случаев приводит к развитию острого или хронического энтерита, сопровождающегося диареей. Наибольшую помощь в постановке доклинического диагноза при ПД может оказать тщательный сбор анамнеза настоящего заболевания и анамнеза жизни пациента, поскольку особую группу риска образуют лица, практикующие анальные сексуальные контакты.
В современной классификации ОКИ выделяют так называемые особые формы заболевания:
- диарея путешественников;
- диарея у мужчин-гомосексуалов;
- диарея у ВИЧ-инфицированных;
- антибиотико-ассоциированная диарея;
- синдром избыточного роста бактерий в желудочно-кишечном тракте.
Из особых форм ОКИ для практики врача СМП имеет значение лишь один из вариантов антибиотико-ассоциированной диареи — псевдомембранозный колит. Это заболевание развивается во время или значительно после приема антибактериальных препаратов и связано с колонизацией кишечника условно-патогенным микроорганизмом сlostridium difficile. Протекает псевдомембранозный колит с высокой лихорадкой, кровавой диареей, болью в животе и сопровождается существенной интоксикацией со всеми возможными осложнениями острой профузной диареи. При подозрении на псевдомембранозный колит больной должен быть госпитализирован в инфекционный стационар.
Доклиническая и дифференциальная диагностика ОД
Всестороннее изучение анамнеза настоящего заболевания является первым шагом в обследовании пациентов, имеющих характерные признаки ОКИ (табл. 1).
У больных необходимо выяснить:
- когда и как началось заболевание (например, внезапное или постепенное развитие заболевания, наличие инкубационного или продромального периода);
- характер испражнений (водянистые, кровянистые, с примесью слизи или гноя, жирные и т. д.);
- частоту стула, количество и болезненность испражнений;
- наличие симптомов дизентерии (лихорадка, тенезмы, примесь крови и/или гноя в испражнениях).
В беседе с больным очень важно установить наличие и, что особенно существенно, развитие субъективных и объективных проявлений обезвоживания (жажды, тахикардии, ортостатических реакций, уменьшения диуреза, вялости и нарушений сознания, судорог, снижения тургора кожи) и интоксикации (головной боли, тошноты, рвоты, мышечных болей).
На догоспитальном этапе ОКИ необходимо дифференцировать с рядом острых неинфекционных заболеваний хирургического, терапевтического, гинекологического и иного профиля. Единственной целью дифференциального диагноза в данном случае является выбор направления госпитализации больного. Основные критерии для проведения дифференциального диагноза отражены в предлагаемом нами алгоритме догоспитальной медицинской помощи (рис. 2).
Распространенность ошибочной диагностики ОКИ иллюстрируют данные DuPont H. L. (1997). Предоставленные автором данные анализа более 50 тысяч случаев госпитализации больных с ОКИ констатируют, что в 7,4% случаев этот диагноз был установлен при таких заболеваниях, как острый аппендицит, острый холецистопанкреатит, странгуляционная кишечная непроходимость, тромбоз мезентериальных сосудов, инфаркт миокарда, крупозная пневмония, декомпенсация сахарного диабета, гипертонический криз. Напротив, указанные выше заболевания были ошибочно диагностированы у больных с ОКИ в 11,1% случаев.
Догоспитальная терапия ОД
Наибольшую угрозу для пациентов с ОКИ представляет развитие дегидратации и ассоциированной с ней артериальной гипотензии на фоне интоксикации, провоцирующей падение артериального давления и нарушение функции центральной нервной системы. Объем догоспитальной терапии при ОКИ базируется на мониторинге жизненно важных функций организма больного: состоянии сознания и функции внешнего дыхания, уровне АД и гидратации пациента. При наличии соответствующего оснащения бригады СМП терапия клинически значимой гиповолемической и инфекционно-токсической артериальной гипотензии должна осуществляться под контролем центрального венозного давления. В соответствии со стандартными рекомендациями терапия на этом этапе направлена:
- на восстановление сердечного ритма;
- на оптимизацию объема циркулирующей крови;
- на устранение гипоксии и нормализацию кислотно-щелочного равновесия;
- на проведение инотропной/вазопрессорной терапии.
Для устранения гипоксии больному назначают оксигенотерапию газовой смесью с 35%-ным содержанием кислорода.
Регидратацию больного начинают с диагностики обезвоживания, тяжесть которой может варьировать от I до IV степени (табл. 2).
При дегидратации I и II степеней (85-95% больных ОКИ) восполнение потери жидкости может и должно осуществляться оральным путем. ВОЗ рекомендует применять для оральной регидратации растворы следующей прописи: 3,5 г NaCl, 2,5 г NaHCO3 (или 2,9 г цитрата натрия), 1,5 г KCl и 20 г глюкозы или ее полимеров (например, 40 г сахарозы, или 4 столовые ложки сахара, или 50-60 г вареного риса, кукурузы, сорго, проса, пшеницы или картофеля) на 1 л воды. Это позволяет получить раствор, содержащий приблизительно 90 ммоль Na, 20 ммоль K, 80 ммоль Cl, 30 ммоль HCO3 и 111 ммоль глюкозы. Можно с успехом использовать любой из готовых растворов для оральной регидратации (цитроглюкосалан, регидрон, гастролит). Количество выпитой жидкости должно в 1,5 раза превышать ее потери с испражнениями и мочой. Компенсация обезвоживания сопровождается очевидным уменьшением жажды, нормализацией диуреза и улучшением общего состояния больного.
Дегидратация III и IV степеней, выраженная тошнота или рвота, а также бессознательное состояние больного требуют неотложной инфузионной терапии. Для внутривенной регидратации используют полиионные кристаллоидные растворы: трисоль, квартасоль, хлосоль, ацесоль. Менее эффективно введение моноионных растворов (физиологического раствора хлорида натрия, 5%-ного раствора глюкозы), а также несбалансированных полиионных растворов (раствора Рингера, мафусола, лактасола). Коллоидные растворы (гемодез, реополиглюкин, рефортан) вводят только в случаях упорной гипотонии, после восстановления объема циркулирующей крови в целом. В тяжелых случаях инфузия водно-электролитных смесей начинается с объемной скоростью 70-90 мл/мин, при средней тяжести состояния больного — с объемной скоростью 60-80 мл/мин. В ряде случаев необходимая скорость инфузии обеспечивается путем одновременного вливания в 2-3 вены. После стабилизации артериального давления скорость инфузии снижается до 10-20 мл/мин. Для предотвращения прогрессирования обезвоживания, развития гемодинамической недостаточности, отека легких, пневмонии, ДВС-синдрома и острой почечной недостаточности объем жидкости, вводимой после стабилизации состояния больного, может составлять 50-120 мл на 1 кг веса.
Назначение антибактериальной терапии среднетяжелых и тяжелых ОКИ на доклиническом этапе не только не входит в задачи врача СМП, но и категорически противопоказано, поскольку может существенно ухудшить состояние больного и затруднить лабораторную верификацию возбудителя заболевания. Возрастающая угроза инфекций, вызванных антибиотико-резистентными штаммами микроорганизмов, наличие нежелательных реакций при применении антимикробных препаратов, суперинфекция, связанная с эрадикацией нормальной микрофлоры антибактериальными средствами, и возможность индукции антибиотиками некоторых факторов вирулентности у энтеропатогенов (например, индукция фторхинолонами фага, ответственного за продукцию шигеллезного токсина), заставляют тщательно взвешивать все за и против при решении вопроса об антимикробной терапии и назначать ее только после точной диагностики возбудителя ОКИ. В связи с вышеизложенным антибактериальные препараты особенно не рекомендуются при гастроэнтеритическом варианте ОД любой степени тяжести, при легком, стертом течении колитического варианта и в период реконвалесценции при любой форме кишечного заболевания.
Эмпирическое назначение антибиотиков возможно в случае легкопротекающей и среднетяжелой ОКИ любой этиологии, а также при диарее путешественников, наиболее вероятным возбудителем которой являются энтеротоксигенные штаммы E.coli или другие бактериальные патогены. В этом случае взрослым назначают фторхинолоны, а детям — ко-тримоксазол, применение которых позволяет сократить длительность заболевания с 3-5 до 1-2 дней. Этой категории больных, как правило, не нуждающихся в госпитализации, можно рекомендовать амбулаторный прием антисептиков кишечного действия: эрцефурила, интетрикса или энтероседива в стандартных дозах в течение 5-7 дней, а также препаратов неантимикробного действия, облегчающих течение диареи (табл. 3).
Столь же опасным, как антибиотики, в отношении усугубления интоксикации является применение при ОКИ любого клинического течения сильных противодиарейных препаратов (имодиума) и противотошнотных средств (церукала, торекана).
Особое значение при ОКИ имеет коррекция микробиоценоза кишечника пробиотиками, проводимая на различных этапах лечения: в остром периоде — в целях конкурентного вытеснения патогенной микрофлоры, у реконвалесцентов — для обеспечения реабилитационных процессов. Весьма эффективно раннее, не позже второго дня болезни, назначение бифидумбактерина форте в ударных дозах (по 50 доз 3 раза каждые 2 часа в первый день лечения) с последующим приемом поддерживающих доз (30 доз в день, по показаниям — до 6 дней).
Пробиотик IV поколения бифидумбактерин форте обеспечивает высокую локальную колонизацию слизистой оболочки кишечника, элиминацию патогенной и условно-патогенной микрофлоры. Положительный клинический эффект при сальмонеллезе средней тяжести отмечен через 1-2 дня, при тяжелом течении сальмонеллеза и дизентерии — к окончанию курса. Из пробиотиков, приготовленных на основе микроорганизмов рода Bacillus, препаратом выбора является биоспорин, назначаемый по 2 дозы 2-3 раза в день в течение 5-7 дней. Препарат обладает выраженным антибактериальным, антитоксическим и иммуномодуляторным действием, индуцирует синтез эндогенного интерферона, стимулирует активность лейкоцитов крови, синтез иммуноглобулинов. При преобладании энтеритического синдрома рекомендуется энтерол, получаемый из сахаромицетов Буларди. Он назначается по 250 мг 2 раза в день в течение 5 дней. В периоде реконвалесценции наряду с традиционными патогенетическими средствами (стимуляторами репарации, общего и местного иммунного ответа) целесообразно применение препаратов облигатной флоры, оптимально — бифидумбактерина форте, оказывающего стабилизирующее влияние на микробиоценоз кишечника и гомеостатические процессы.
Несмотря на расширение возможностей по верификации возбудителя и большой выбор методов этиопатогенетической терапии, появившихся в арсенале врача за последние 20 лет, ОКИ и сегодня по-прежнему сопряжены с высокой летальностью. Так, по данным Н. Д. Ющука, при ПТИ и сальмонеллезе летальность составляет около 0,1%, а при дизентерии — 1,4%, при этом причиной 20% летальных исходов при бактериальной дизентерии и 44,4% летальных исходов при всех остальных ОКИ является инфекционно-токсический шок. Причины столь высокой летальности, вероятно, кроются в неадекватной оценке прогноза и тяжести состояния больного ОКИ и неоказании ему, в том числе по причинам недостаточного инструментального, медикаментозного и информационного обеспечения, неотложной помощи именно на догоспитальном этапе. Хочется надеяться, что предложенный нами простой алгоритм догоспитальной медицинской помощи при ОД (рис. 2) окажется небесполезным для практикующих врачей и их пациентов.
Читайте также:

