Вирусный мононуклеоз при беременности
Обновлено: 19.04.2024
Инфекционный мононуклеоз – это острое вирусное заболевание (преимущественно вирус Эпштейна-Барр), которое характеризуется лихорадкой, поражением ротоглотки, лимфатических узлов, печени, селезенки и своеобразными изменениями состава крови (лимфомоноцитоз, атипичные мононуклеары).
Код(ы) МКБ-10:
| Коды МКБ-10 | |
| B27 | Инфекционный мононуклеоз |
| B27.0 | Мононуклеоз, вызванный гамма-герпетическим вирусом Мононуклеоз, вызванный вирусом Эпштейна-Барр |
| B27.1 | Цитомегаловирусный мононуклеоз |
| B27.8 | Другой инфекционный мононуклеоз |
| B27.9 | Инфекционный мононуклеоз неуточнённый |
| D82.3 | Иммунодефицит вследствие наследственного дефекта, вызванного вирусом Эпштейна-Барр |
Дата разработки/пересмотра протокола: 2017 год.
Сокращения, используемые в протоколе:
| EA | – | ранний антиген ВЭБ вируса Эпштейна-Барр |
| EBNA | – | ядерный антиген вируса Эпштейна-Барр |
| IgG | – | иммуноглобулины класса G |
| IgM | – | иммуноглобулины класса М |
| VCA | – | капсульный антиген вируса Эпштейна-Барр |
| ВИЧ | – | вирус иммунодефицита человека |
| ВОП | – | врач общей практики |
| ВЭБ | – | вирус Эпштейна-Барр |
| ДНК | – | дезоксирибонуклеиновая кислота |
| ЖКТ | – | желудочно-кишечный тракт |
| ИФА | – | иммуноферментный анализ |
| МКБ | – | международная классификация болезней |
| НПВС | – | нестероидные противовоспалительные средства |
| ОАК | – | общий анализ крови |
| ОАМ | – | общий анализ мочи |
| ПЦР | – | полимеразная цепная реакция |
| СОЭ | – | скорость оседания эритроцитов |
Пользователи протокола: врачи скорой неотложной помощи, фельдшеры, врачи общей практики, педиатры, детские инфекционисты, детские хирурги.
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
Классификация
| По типу: • типичный; • атипичный (бессимптомный, стертый, висцеральный). | По тяжести: • легкая форма; • среднетяжелая форма; • тяжелая форма. | По течению: • острое (до 3 мес.); • затяжное (3-6 мес.); • хроническое (более 6 мес.); • рецидивирующее (возврат клинических симптомов болезни через 1 месяц и более после перенесенного заболевания). |
Осложнения:
· ранние осложнения (1-3 недели болезни): разрыв селезенки, асфиксия, (вследствие фаринготонзиллярного отека), миокардит, интерстициальная пневмония, энцефалит, паралич черепных нервов, в том числе паралич Белла, менингоэнцефалит, полиневрит, синдром Гийена-Барре;
· поздние осложнения (позже 3 недели болезни): гемолитическая анемия, тромбоцитопеническая пурпура, апластическая анемия, гепатит, синдром мальабсорбции и др., как следствие аутоиммунного процесса.
Типичная форма характеризуется лихорадкой, поражением ротоглотки, лимфатических узлов, печени, селезенки и своеобразными изменениями состава крови (лимфомоноцитоз на фоне лейкоцитоза и атипичные мононуклеары в количестве 10% и более).
Атипичные формы инфекционного мононуклеоза:
· стертая форма: протекает со слабо выраженными и быстро проходящими формами, симптомами или под маской острых респираторных заболеваний, диагностируется преимущественно в эпидемических очагах;
· бессимптомная форма: протекает с отсутствием клинических симптомов, диагностируется на основании обследования гематологическими, серологическими методами и методом эпидемиологического анализа;
· висцеральная форма: отличается тяжелым течением с полиорганным поражением, с вовлечением сердечно-сосудистой, центральной и периферической нервной систем, почек, надпочечников и других жизненно важных органов.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии [1-5,9,12,15,16]:
| Признак | Характеристика |
| Лихорадка | Высокая, длительная |
| Синдром поражения рото-и носоглотки | Синдром тонзиллита с налетами или без, аденоидит, фарингит |
| Синдром поражения лимфатических узлов | Преимущественно увеличение передне- и/или заднешейных групп лимфоузлов, внутрибрюшных лимфоузлов, наиболее часто у ворот печени и селезенки, гипертрофия небных и глоточной миндалин |
| Синдром гепатоспленомегалии | Увеличение размеров печени и селезенки |
| Синдром цитолиза печеночных клеток и нарушения пигментного (билирубинового) обмена Печени | Повышение аланинаминотрансминазы, аспартатаминотрансминазы. Нарушение пигментного обмена печени, проявляющееся желтухой и повышением билирубина |
| Синдром экзантемы | Сыпь пятнисто-папулезная, реже геморрагическая с локализацией на лице, туловище, конечностях, чаще проксимальных отделов, яркая, обильная, местами сливная. Возможен кожный зуд, отечность лица. Появляется на 5-10 день болезни. |
Критерии оценки степени тяжести инфекционного мононуклеоза по клиническим признакам [1-5,9,12,15,16]:
| Признак | Характеристика признака | |||
| Легкая степень тяжести | Средняя степень тяжести | Тяжелая степень тяжести | ||
| Выраженность и длительность интоксикации | Отсутствует или легкая выраженность, 1-5 дней | Умеренной выраженности, 6-7 дней | Ярко выражена, более 8 дней | |
| выраженность и продолжительность лихорадки | повышение температуры до 38 ° С, длительность 1-5 дней | повышение температуры от 38,1 до 39 ° С, длительность 6-8 дней | повышение температуры более 39,0 ° С, длительность более 9 дней | |
| Характер воспалительных изменений в рото- и носоглотке | Воспалительные изменения катарального характера или с островчатыми, тонкими налетами, продолжительностью 1-3 дня; затруднение носового дыхания 1-4 дня | Воспалительные изменения с лакунарными налетами, продолжительностью 4-6 дней; затруднение носового дыхания 5-8 дней | ||
| ОАК | лейкопения/умеренный лейкоцитоз (12-25х109/л); лимфомоноцитоз до 70-80%; нейтропения; увеличение СОЭ до 20-30 мм/ч; атипичные мононуклеары (отсутствие или увеличение от 10 до 50%). | |
| Серологический (ИФА с определением показателя индекса авидности) | обнаружение специфических антител IgM VCA к ВЭБ и IgG VCA, IgG EA, IgG-EBNA к ВЭБ с определением показателя индекса авидности | |
Дополнительные лабораторные исследования: | ||
| Молекулярно-генетический метод (ПЦР) | обнаружение в крови ДНК вируса Эпштейна-Барр. | |
| Биохимический анализ крови (при гепатомегалии и желтухе) | определение концентрации билирубина и АЛАТ в крови: умеренная гиперферментемия, гипербилирубинемия. | |
| Бактериологическое исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы | для идентификации бактериальной этиологии острого тонзиллита. | |
| Признак | Критерии |
| Атипичные мононуклеары | Выявление атипичных мононуклеаров в периферической крови более10% (со 2-3 недели болезни) |
| Лимфомоноцитоз | Выявление лимфомоноцитоза в периферической крови |
| IgM VCA VCA, IgG-EBNA вируса Эпштейна- Барр | В острый период: IgM VCA с момента развития клинических признаков болезни и следующие 4-6 недель присутствуют и снижаются, IgG EA с первой недели болезни нарастают до нескольких лет после нее, персистируют на невысоком уровне, IgG VCA обнаруживаются через несколько недель после появления IgM VCA, нарастают, персистируют пожизненно на высоком уровне, IgG-EBNA-1, 2- отсутствуют или имеются в небольшом количестве. В период реконвалесценции: IgM VCA отсутствуют или имеются в малом количестве, IgG EA персистируют пожизненно на невысоком уровне, IgG VCA персистируют пожизненно IgG EBNA несколько недель после появления клинических признаков и персистируют обнаруживаются через пожизненно на невысоком уровне |
| Определение показателя индекса авидности | Обнаружение IgG с низкой авидностью при наличии или отсутствии IgM свидетельствует о первичной (недавней) инфекции. Присутствие высокоавидных антител IgG указывает на период реконвалесценции |
| ДНК вируса Эпштейна-Барр в крови и слюне | Выявление ДНК вируса методом ПЦР в крови (через 1-2 недели после появления клинических симптомов), слюне. |
Инструментальные исследования: нет.
Показания для консультации специалистов:
· консультация оториноларинголога: при аденоидите, формировании паратонзиллярного абсцесса, воспалительных процессах со стороны придаточных пазух носа;
· консультация гематолога: при прогрессировании гематологических сдвигов;
· консультация хирурга: при выраженном абдоминальном болевом синдроме.

Диагностический алгоритм: (схема)
Инфекционный мононуклеоз — это острое заболевание вирусной природы, которое проявляется повышением температуры тела, поражением небных миндалин, лимфатических узлов, увеличением печени и селезенки. Возбудитель – вирус Эпштейн-Барр (ДНК-содержащий вирус из группы герпесвирусов, вирус герпеса 4 типа). Особенность вируса в том, что он преимущественно поражает определенные клетки иммунной системы (в-лимфоциты), что обуславливает изменения в органах, которые их содержат (лимфатические узлы, селезенка и печень). После перенесенного мононуклеоза формируется стойкий иммунитет (повторные случаи заболевания не встречаются). В большинстве случаев это одиночная инфекция, редко бывают групповые вспышки (например, семейные).
Симптомы инфекционного мононуклеоза у беременной
- общее недомогание, слабость, вялость;
- небольшое повышение температуры тела;
- появление отделяемого из носа.
- начало острое, с высоким повышением температуры тела (39-40 ̊С);
- длительность лихорадки 1-3 недели;
- воспаление небных и носоглоточных миндалин (тонзиллит), что сопровождается болью при глотании, затруднением носового дыхания;
- увеличение лимфатических узлов (чаще передних и задних шейных, реже паховых и локтевых), которое сохраняется до 1 месяца;
- высыпания на коже различного характера (появляются в течение 3 дней от начала заболевания и через несколько дней проходят бесследно);
- увеличение печени и селезенки, что может сопровождаться желтушностью кожных покровов или протекать без нее.
- нормализация температуры тела;
- улучшение общего самочувствия;
- исчезновение признаков ангины;
- постепенно возвращаются к нормальным размерам лимфатические узлы, селезенка, несколько позже – печень;
- нормализуются показатели общего анализа крови;
- длительность от 2 недель до 1 месяца.
Инкубационный период инфекционного мононуклеоза у беременной
Инкубационный период (время от момента попадания вируса в организм человека до появления первых симптомов):
- составляет от 4 до 15 дней;
- наиболее часто 7-10 дней.
Формы инфекционного мононуклеоза у беременной
Выделяют типичную и атипичную формы заболевания.
- бессимптомная форма – нет симптомов (человек в данном случае просто носитель инфекции, заболевание можно выявить только лабораторными методами);
- стертая форма – слабо выраженные проявления инфекции, в дальнейшем быстро исчезающие;
- висцеральная форма - с преимущественным поражением внутренних органов, их увеличением.
- острый;
- затяжной;
- хронический;
- осложненный.
Причины инфекционного мононуклеоза у беременной
- Источник инфекции – больной человек (как в период разгара, так и вирусоноситель).
- Возможные пути передачи – воздушно-капельный, контактно-бытовой (с инфицированной слюной, при поцелуях).
- Прогрессированию заболевания способствует наличие любого другого заболевания, приводящего к угнетению иммунной системы человека (например, частые ангины).
- Наибольшее число случаев заболевания регистрируется в осенне-весенний период.
LookMedBook напоминает: что данный материал размещен исключительно в ознакомительных целях и не заменяет консультацию врача!
Врач терапевт поможет при лечении заболевания
Диагностика инфекционного мононуклеоза у беременной
- Анализ анамнеза заболевания и жалоб (уточнение у больного, когда появились симптомы заболевания, проводимое ранее лечение и эффект от него и т.д.).
- Общий осмотр (врачебный осмотр кожных покровов, оценка состояния больного и т.д.).
- Инфекционный мононуклеоз можно заподозрить на основании комплексной оценки симптомов заболевания.
- Характерным лабораторным признаком, помимо неспецифической реакции крови на воспаление (увеличение числа лимфоцитов, повышение СОЭ), является появление в общем анализе крови специфических клеток (мононуклеаров).
- Более точно диагноз может быть установлен на основании лабораторных тестов (обнаружение специфических антител – ИФА, обнаружение ДНК возбудителя методом ПЦР).
- Необходима консультация акушера-гинеколога.
- Возможна также консультация инфекциониста.
Лечение инфекционного мононуклеоза у беременной
Перед назначением лечения необходима консультация акушера-гинеколога.
Угрозу прерывания беременности может представлять ситуация, когда женщина ранее не болела инфекционным мононуклеозом (нет специфического иммунитета), что можно установить на основании лабораторных тестов.
Через кровь вирус не распространяется, однако возможна передача вируса от матери ребенку во время родов (вертикальный путь).
Вопрос о госпитализации решается индивидуально (чаще госпитализируют детей, другие возрастные группы — в случае тяжелого течения инфекции).
- Постельный режим необходим на время лихорадки.
- При тяжелом поражении печени с желтухой – диета №5 (с исключением жирного, жареного, специй, ограничением соли и т.д.), при всех формах заболевания – обильное питье.
- Полоскание ротоглотки различными антисептическими растворами.
- Противовирусная терапия – препараты интерферона и индукторы интерферона.
- Назначаются также противоаллергические препараты, жаропонижающие, витаминные комплексы.
- В случае тяжелого течения и угрозы развития осложнений возможны короткие курсы гормональной терапии.
- При наличии инфекционных осложнений – антибактериальная терапия.
Осложнения и последствия инфекционного мононуклеоза у беременной
- Угрозу прерывания беременности может представлять ситуация, когда женщина ранее не болела инфекционным мононуклеозом (нет специфического иммунитета), что можно установить на основании лабораторных тестов.
- Через кровь вирус не распространяется, однако возможна передача вируса от матери ребенку во время родов (вертикальный путь).
Профилактика инфекционного мононуклеоза у беременной
Специальных профилактических мероприятий не проводится.
- исключить контакт с больным инфекционным мононуклеозом;
- сбалансированное и рациональное питание (употребление в пишу продуктов с высоким содержанием клетчатки (овощи, фрукты, зелень), отказ от консервированной, жареной, острой, горячей пищи);
- лечение очагов хронической инфекции (кариозные зубы, лечение хронических ринитов (насморк), синуситов (воспаление придаточных пазух носа) и т.д.);
- регулярное посещение акушера-гинеколога (1 раз в месяц в 1-м триместре, 1 раз в 2-3 недели во 2-м триместре и 1 раз в 7-10 дней в 3-м триместре);
- своевременная постановка на учет беременной в женской консультации (до 12 недели беременности).
ИНФОРМАЦИЯ ДЛЯ ОЗНАКОМЛЕНИЯ
Необходима консультация с врачом
Певцова Анастасия Владимировна, врач-методист, акушер-гинеколог, медицинский редактор.
Подоляк Анжелика Алексеевна, редактор.
Что делать при инфекционном мононуклеозе?
- Выбрать подходящего врача терапевт
- Сдать анализы
- Получить от врача схему лечения
- Выполнить все рекомендации
Резюме
Актуальность Эпштейна - Барр вирусной инфекции объясняется широкой циркуляцией вируса Эпштейна - Барр среди детского и взрослого населения, его тропностью к иммунокомпетентным клеткам с пожизненной персистенцией после первичного инфицирования и полиморфизмом клинических проявлений от субклинических форм, инфекционного мононуклеоза до формирования онкологических, аутоиммунных гематологических заболеваний. Персистенция Эпштейна -Барр вируса приводит к подавлению клеточного звена иммунитета, снижению продукции интерферонов и факторов неспецифической защиты, что способствует реактивации персистирующей инфекции, чаще всего без мононуклеозоподобного синдрома, и появлению атипичных мононуклеаров в крови с формированием лимфопролиферативного, интоксикационного, астеновегетативного синдромов, длительного субфебрилитета, что диктует необходимость применения иммунокоррегирующей терапии. В статье приведен клинический случай, в котором изложены описание и анализ течения хронической Эпштейна - Барр вирусной инфекции у ребенка дошкольного возраста (5 лет 8 мес.) с отягощенным преморбидным фоном. Эпизоды реактивации хронической персистирующей инфекции протекали под маской острой респираторной инфекции с лимфопролиферативным синдромом, гнойного тонзиллита, гнойного аденоидита. Терапия, включавшая антибиотики, препараты с противовирусной активностью коротким курсом, бактериальные лизаты, физиотерапию, имела временный и непродолжительный эффект. В силу отсутствия полного мононуклеозоподобного синдрома в клинике и атипичных мононуклеаров в гемограмме обследование на Эпштейна - Барр вирусную инфекцию не проводилось до пятилетнего возраста, в связи с чем она не была верифицирована, и, соответственно, ребенок не получал адекватной иммунотропной терапии. Только в 5 лет 8 мес. при очередном эпизоде активации хронической Эпштейна - Барр вирусной инфекции в состав комплексной терапии был включен меглюмина акридонацетат, на фоне которого была достигнута хорошая клинико-лабораторная динамика. Описанный клинический случай демонстрирует эффективность включения в состав комплексного лечения Эпштейна - Барр вирусной инфекции меглюмина акридонацетата, обладающего противовирусным, иммуномодулирующим и противовоспалительным действиями, что позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем - и астеновегетативного синдрома и достигнуть перехода активной хронической Эпштейна - Барр вирусной инфекции в латентную форму.
Ключевые слова: острая респираторная инфекция, гнойный тонзиллит, гнойный аденоидит, лимфопролиферативный синдром, меглюмина акридонацетат, иммунотропная терапия.
Chronic Epstein-Barr viral infection in children: a clinical case
Svetlana P. Kokoreva, Veronika B. Kotlova®, Oleg A. Razuvaev
Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia
Abstract
The urgency of Epstein-Barr virus infection is explained by wide circulation of Epstein-Barr virus among children and adults, its tropism to immunocompetent cells with lifelong persistence after primary infection and polymorphism of clinical manifestations from subclinical forms, infectious mononucleosis to formation of oncological, autoimmune hematological diseases. Persistence of Epstein - Barr virus leads to suppression of cellular immunity, decreased production of interferons and nonspecific protection factors, which contributes to reactivation of persistent infection, most often without mononucleosis-like syndrome, and the appearance of atypical mononuclears in blood with the formation of lymphoproliferative, intoxication, astheno-vegetative syndrome, long-term subfebrile condition, which dictates the need for immunocorrective therapy. This article presents a clinical case describing and analyzing the course of a chronic Epstein-Barr virus infection in a preschool child (5 years 8 months) with a pre-morbid background. Episodes of reactivation of chronic persistent infection occurred under the mask of acute respiratory infection with lymphoproliferative syndrome, purulent tonsillitis, purulent adenoiditis. Therapy, including antibiotics, short-course antiviral agents, bacterial lysates, and physiotherapy, had a temporary and short-lived effect. meglumine acridonacetate. The described clinical case demonstrates the effectiveness of the inclusion of meglumine acridonacetate, which has antiviral, immunomodulatory and anti-inflammatory effects, in the complex treatment of Epstein-Barr virus infection, This allowed to obtain fairly rapid positive clinical dynamics of relieving intoxication and febrile and lymphoproliferative syndromes in the acute period, and subsequently - astheno-vegetative syndrome and achieve the transition of active chronic Epstein - Barr virus infection into a latent form.
Keywords: acute respiratory infection, purulent tonsillitis, purulent adenoiditis, lymphoproliferative syndrome, meglumine acridonacetate, immunotropic therapy.
Введение
Сегодня Эпштейна - Барр вирусная инфекция (ЭБВИ) представляет собой междисциплинарную проблему и активно изучается не только инфекционистами, но и врачами других специальностей: педиатрами, оториноларингологами, ревматологами, гематологами, онкологами, неврологами, иммунологами. Это объясняется тем, что вирус Эпштейна - Барр (ВЭБ) является одним из наиболее распространенных возбудителей, выявляемых как в детском возрасте, так и среди взрослого населения. По данным различных исследователей, инфицированность ВЭБ составляет 17,7% в периоде новорожденности и возрастает до 90% и выше у лиц старших возрастных групп 1. Являясь оппортунистической инфекцией, она в большинстве случаев протекает бессимптомно. Особенностью манифестных форм ЭБВИ является полиморфизм клинических симптомов, начиная от инфекционного мононуклеоза до фульминантных тяжелейших форм, аутоиммунных и онкологических заболеваний, реализующихся спустя годы после диагностированной ЭБВИ. Доказано, что манифестация клинических проявлений развивается при первичном инфицировании и реактивации персистирующей инфекции 4.
В случае адекватного иммунологического ответа первичное инфицирование приводит к формированию латентной формы инфекции - персистирующей неактивной ЭВБИ. Приравниваясь к здоровому носительству, она является естественным завершением иммунологических изменений. При снижении иммунитета происходит реактивация инфекции с манифестными проявлениями -активация персистирующей инфекции. При тяжелом течении могут формироваться органные поражения: менингоэнцефалит, миокардит, гепатит, гломерулонефрит и другие с возможным летальным исходом 10.
Но чаще в клинической практике встречаются варианты повторной реактивации ЭБВИ с неспецифической симптоматикой, когда при отсутствии остро развившегося полного мононуклеозоподобного синдрома и появления атипичных мононуклеаров в периферической крови, характерных для инфекционного мононуклеоза, возникают утомляемость, слабость, артралгии, головная боль, снижение памяти и внимания, депрессия, субфебрилитет. При этом принято говорить о хронической инфекции, если симптоматика сохраняется в течение полугода. Дети с хронической ЭБВИ имеют, как правило, отягощенный преморбидный фон, страдают хроническим тонзиллитом, хроническим аденоидитом; у них формируются различные варианты лимфопролиферативного синдрома, умеренно выраженный интоксикационный синдром, астенизация, может быть субфебрилитет; у этой категории больных отмечаются частые рекуррентные заболевания, что объясняется иммуносупрессивным воздействием ВЭБ 14.
Изучение форм ЭБВИ стало быстро развиваться благодаря возможностям современной лабораторной диагностики, которая позволяет оценить время инфицирования и активность инфекционного процесса [15, 16]. Для острой первичной инфекции типично появление ДНК вируса в крови и иммуноглобулинов М к капсидному антигену (аVCAJgM) и (или) иммуноглобулинов к раннему ЕА-антигену (аЕАIgG), которые циркулируют с третьей недели инфицирования, а также низкоавидных иммуноглобулинов к капсидному антигену (аVCAIgG). Со временем низкоавидные аVCAIgG трансформируются в высокоавидные, сохраняясь пожизненно. Начиная со второго месяца с момента заражения появляются антитела к ядерному антигену (аEBNAIgG). У части пациентов они сохраняются всю жизнь, у части -элиминируются. Положительный результат исследования полимеразной цепной реакции (ПЦР) крови не позволяет судить о форме инфекции, так как может регистрироваться как при первичном инфицировании, так и при реактивации персистирующей инфекции. На фоне высокоавидных аVCAIgG и (или) аEBNAIgG при реактивации персистирующей инфекции появляются капсидные антитела класса М и (или) ранние антитела. Давность инфицирования вне обострения инфекционного процесса подтверждается обнаружением высокоавидных аVCAIgG и аEBNAIgG. Положительные результаты ПЦР слюны могут быть у 15-25% здоровых серопозитивных людей. Это происходит в силу пожизненной персистенции вируса в В-лимфоцитах, которые, находясь в лимфоидной ткани миндалин при латентной инфекции или ее активации, дают положительный результат исследования [17].
Иммунокорригирующая терапия Эпштейна - Барр вирусной инфекции
На сегодняшний день общепринятых принципов этиотропного лечения ЭБВИ не разработано, так как препараты с противовирусной активностью не позволяют элиминировать возбудитель из организма, и основой лечения является симптоматическая и патогенетическая терапия. Однако длительная персистенция ВЭБ, приводящая к угнетению клеточного иммунитета, факторов неспецифической защиты, интерферон-продуцирующей функции лейкоцитов, свидетельствует о необходимости использования иммунокорригирующих препаратов [18, 23-26].
В педиатрической практике хорошо зарекомендовали себя индукторы эндогенного интерферона, в частности меглюмина акридонацетат (Циклоферон®), которые имеют ряд преимуществ по сравнению с экзогенными интерферонами. При их назначении не вырабатываются аутоантитела на собственный интерферон, время выработки стимулированных эндогенных интерферонов контролируется макроорганизмом, что не приводит к его передозировке. Кроме того, индукторы эндогенного интерферона имеют высокую биодоступность 30. Циклоферон® является низкомолекулярным индуктором интерферона и, соответственно, оказывает противовирусное, иммуномодулирующее, противовоспалительное действия, стимулируя синтез а- и у-интерферона, что способствует усилению Т-клеточного иммунитета - нормализации субпопуляций СD3-лимфоцитов, СD4-лимфо-цитов, NK-клеток и иммунорегуляторного индекса. Прямое действие меглюмина акридонацетата реализуется через нарушение репликации вируса, блокирование вирусной ДНК или РНК, увеличение дефектных вирусных частиц и снижение вирус-индуцированного синтеза белка [32, 33]. Его клиническая эффективность доказана у детей при острой респираторной вирусной инфекции (ОРВИ) и гриппе, так как на ранней стадии инфицирования он подавляет репликацию вируса, стимулирует и поддерживает уровень всех видов интерферона. Из всех индукторов интерферона Циклоферон является самым быстрым, вызывая продукцию интерферона через 2-72 ч после введения, реализуя таким образом противовирусный и иммуномодулирующий эффекты уже через 2-3 ч после приема 34. Наибольшую эффективность у детей препарат имеет при низком интерфероновом статусе 37. Доказано прямое противовирусное действие Циклоферона с подавлением размножения вируса на стадии репликации и вирусного потомства, его способность индуцировать синтез эндогенного интерферона в отношении герпетических вирусов, и показана его клиническая эффективность у детей при различных герпесвирусных инфекциях, в том числе и ЭБВИ 39. В качестве примера успешного использования иммуно-тропной терапии при герпесвирусной инфекции приводим клинической случай течения и исхода хронической ЭБВИ у ребенка дошкольного возраста.
Anamnesis vitae: ребенок от третьей беременности (в семье есть двое детей 8 и 10 лет), протекавшей с угрозой прерывания (терапия дюфастоном) на фоне хронической фетоплацентарной недостаточности, третьих срочных родов путем кесарева сечения. Вес при рождении -3260 г, оценка по Апгар - 7-8 баллов. По поводу конъюгационной гипербилирубинемии была переведена на второй этап выхаживания. С рождения находилась на искусственном вскармливании в связи с гипогалактией у матери. До года наблюдалась неврологом по поводу перинатального поражения нервной системы, профилактические прививки с 12 мес. Из перенесенных заболеваний мама отмечала нетяжелые ОРИ в 1,5 года и острую кишечную инфекцию в 2 года 4 мес.
Предварительный диагноз - острая респираторновирусная инфекция, осложненная аденоидитом. Синусит (?).
Динамика и исходы. В гемограмме лейкоцитоза нет -9,5 х 10 9 /л, абсолютный лимфомоноцитоз (п4%, с28%, л56%, м12%), СОЭ - 18 мм/час. Биохимические тесты без патологических изменений, СРБ - 3 мг (норма - 0-10). При рентгенологическом исследовании придаточных пазух носа данных по синуситу не выявлено. Получен отрицательный результат ПЦР-исследования мазков из носоглотки (респираторный скрин). Лор-врачом диагностирован гнойный аденоидит. По данным ультразвукового исследования органов брюшной полости выявлялись умеренная гепатомегалия, мезентериальная лимфаденопатия.
Терапия в отделении включала антибиотики (цефтриаксон парентерально), Виферон-1 per rectum 2 раза в сутки, симптоматические средства, физиолечение. На фоне проводимого лечения в течение трех суток состояние ребенка оставалось без убедительной клинической динамики: продолжала лихорадить, сохранялись интоксикационный и лимфопролиферативный синдромы. На четвертый день пребывания в стационаре результаты лабораторного обследования: ПЦР+ крови на ВЭБ, аVCAJgM+ и аVCAIgG+ авидность 100%, аEAIgG–, аEBNAIgG+, что позволило диагностировать реактивацию хронической ЭБВИ. К лечению добавлен Циклоферон в таблетках по схеме на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-е сутки. На третий день у девочки нормализовалась температура, восстановился аппетит, улучшилось самочувствие. Стал менее выраженным лимфопролиферативный синдром: носовое дыхание более свободное, уменьшился насморк. На 10-й день лечения ребенок жалоб не предъявлял. При объективном осмотре меньше выражены гипертрофия небных миндалин 1-й степени, шейная лимфаденопатия (размеры лимфоузлов уменьшились до 0,5 см), гепатомегалия 1,5 см. Выписана с клиническим улучшением с рекомендацией продолжить прием Циклоферона по схеме.
Клинический диагноз - хроническая Эпштейна - Барр вирусная инфекция, реактивация: лимфопролиферативный синдром, обострение хронического аденоидита, астеновегетативный синдром.
При объективном осмотре сохранялась умеренная гипертрофия небных миндалин, пальпировались мелкие, 0,3-0,5 см, безболезненные подчелюстные, передне-и заднешейные лимфоузлы, гепатомегалия отсутствовала, клинических проявлений астеновегетативного синдрома не отмечалось. Гемограмма соответствовала возрастной норме. В лабораторных тестах отсутствовали маркеры активной ЭБВИ: ПЦР крови - ДНК ВЭБ не обнаружено, аVCAJgM отрицательные, аEAIgG отрицательные, обнаружены аVCAIgG с авидностью 100% и аEBNAIgG.
Рисунок. Этапы формирования у пациентки хронической Эпштейна - Барр вирусной инфекции
Figure. Stages of chronic Epstein - Barr virus infection development in a patient
Заключение
Описанный клинический пример демонстрирует течение хронической ЭБВИ у больной в возрасте 5 лет 8 мес. с развитием лимфопролиферативного и астено-вегетативного синдромов. При реактивации хронической ЭБВИ, протекавшей с клиническими проявлениями ОРИ, гнойного тонзиллита, применялись антибиотики, препараты интерферона, глюкокортикостероиды интраназально, физиотерапия с временным эффектом. Назначение Циклоферона в составе комплексного лечения позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем -и астеновегетативного синдрома и достигнуть перехода активной хронической ЭБВИ в латентную форму, что подтверждается отсутствием маркеров активности хронической инфекции в течение года после использования Циклоферона.
Информация об авторах:
Кокорева Светлана Петровна, д.м.н., доцент, заведующая кафедрой инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Котлова Вероника Борисовна, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Разуваев Олег Александрович, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Information about the authors:
Svetlana P. Kokoreva, Dr. Sci. (Med.), Associate Professor, Head of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Veronika B. Kotlova, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Oleg A. Razuvaev, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Особенности течения и терапии респираторного микоплазмоза у детей в эпидемический сезон 2020-2021 гг.
Список литературы
References
Кафедра детских инфекционных болезней (зав. — проф. Е. В. Михайлова) ГОУ ВПО "Саратовский государственный медицинский университет имени В. И. Разумовского Федерального агентства по здравоохранению и социальному развитию", 410012, Саратов, ГСП, ул. Большая Казачья, 112.
В работе представлены результаты наблюдения за 80 пациентами в возрасте от 1 до 14 лет с первичной Эпштейна — Барр вирусной инфекцией. Выявлены гемореологи-ческие нарушения, возникающие при Эбштейна — Барр вирусном мононуклеозе. Проанализированы результаты использования реамберина в составе инфузионной терапии с целью коррекции гемореологических нарушений. Установлено, что реамберин снижает вязкость плазмы и уменьшает вязкость крови, под влиянием реамберина быстрее улучшалось состояние детей, восстанавливались гемодинамические нарушения. Применение реамберина способствовало сокращению продолжительности стационарного лечения больных тяжелой формой ЭБВ-мононуклеоза.
Ключевые слова: Эпштейна — Барр вирусная инфекция, гемореологические нарушения, вязкость крови, реамберин
ВВЕДЕНИЕ
Вирусная инфекция Эпштейна — Барр обнаруживается повсеместно и относится к одной из наиболее распространенных: 90 % населения в возрасте старше 40 лет имеют антитела к вирусу [4]. Эпидемиологические исследования показали, что к 6 годам антитела к вирусу появляются у 20 - 100 % детей [9].
Гемореологические нарушения возникают при различных инфекционных заболеваниях, имеют большое значение в патогенезе любого острого воспалительного процесса [1, 2, 6, 7].
Прогрессирование любого инфекционного заболевания сопровождается функционально-структурными изменениями тех или иных форменных элементов крови. От структурной организации мембран красных кровяных клеток во многом зависят их агрегационная активность и деформируемость, являющиеся важнейшими компонентами в микроциркуляции [5].
Бактерии, вирусы, токсины, циркулирующие иммунные комплексы (ЦИК), высокие концентрации ли-пидов и углеводов оказывают токсическое действие на эндотелий сосудов и нарушают стабильность эритроцитов [2].
Характер и глубина гемореологических нарушений имеют ряд особенностей в зависимости от этиологии, тяжести, клинической формы и характера течения заболевания [1].
Определение характера и глубины гемореологиче-ских нарушений при различных заболеваниях имеет важное значение для выяснения патогенеза возникающих изменений и осуществления рациональной патогенетической терапии [6, 10, 12]. Наличие тяжелых форм ЭБВ-мононуклеоза у детей, в патогенезе которых важную роль играют нарушения реологии крови, предполагает использование интенсивной инфузион-ной терапии для коррекции возникающих нарушений.
Существуют работы по исследованию нарушений гемореологических параметров крови и методов их коррекции с применением реамберина при ротавирус-ной инфекции у детей [15], послеродовом эндометрите [13].
Исследований гемореологических показателей при ЭБВ-мононуклеозе у детей в литературе не найдено.
Целью работы явилось изучение гемореологиче-ских нарушений при Эпштейна-Барр вирусном моно-нуклеозе у детей, повышение эффективности инфузи-онной терапии с учетом гемореологических нарушений и изменений показателей эндогенной интоксикации.
МЕТОДЫ ИССЛЕДОВАНИЯ
Проводилось клинико-лабораторное наблюдение за 80 пациентами в возрасте от 1 года до 14 лет. Основную группу составили 60 человек, получавших лечение по поводу первичной Эпштейн-Барр вирусной инфекции в условиях детской клинической инфекционной больницы № 5 Саратова с 2008 по 2010 г. В контрольной группе было обследовано 20 практически здоровых детей того же возраста с письменного согласия их родителей, проходивших плановую диспансеризацию в амбулаторных условиях на базе детской поликлиники № 3 Саратова.
Перед началом исследования получали информированное согласие законного представителя больного на участие в нем. Текст информированного согласия был одобрен локальным независимым этическим комитетом.
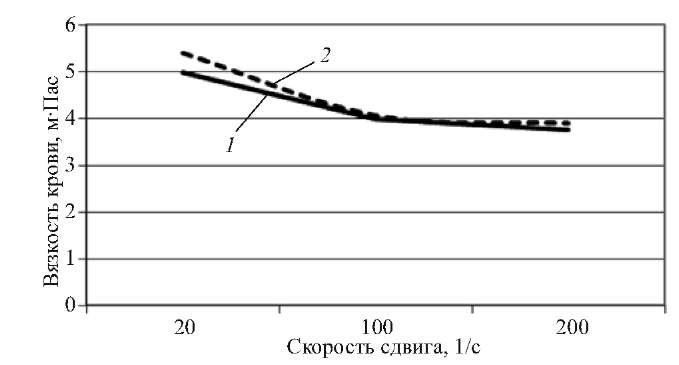
Рис. 1. Характер гемореологической кривой при среднетяже-лой форме ЭБВ-мононуклеоза у детей в острый период.
1 — контроль, 2 — больные со среднетяжелой формой ЭБВ-мононуклеоза.
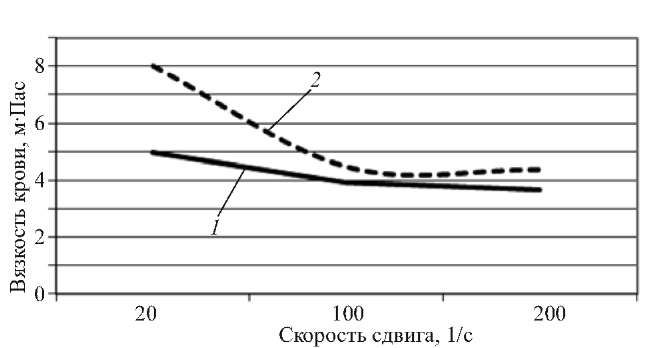
Рис. 2. Характер гемореологической кривой при тяжелой форме ЭБВ-мононуклеоза у детей в острый период
1 — контроль, 2 — больные с тяжелой формой ЭБВ-мононуклеоза.
В основной группе (60 больных) диагноз ставился на основании совокупности клинико-лабораторных данных в соответствии с классификацией МКБ-10. В 100 % случаев диагноз был подтвержден наличием IgM к VCA в исследовании крови методом иммуно-ферментного анализа с помощью диагностических наборов фирмы "Вектор-Бест", Россия. Форму тяжести болезни определяли по клинической классификации В. Ф. Учайкина [14].
В исследование включали детей со среднетяжелой и тяжелой формами заболевания. При оценке эффективности лечения использовали следующие клинические критерии: продолжительность тяжелого и сред-нетяжелого состояния, продолжительность симптомов интоксикации, гемодинамических нарушений, продолжительность инфузионной терапии, а также длительность сроков госпитализации. Кроме того, оценивали следующие лабораторные показатели: вязкость крови на различных скоростях сдвига, вязкость плазмы, индекс агрегации эритроцитов, индекс деформируемости эритроцитов, молекулы средней массы, Д-димеры при поступлении и на 5 - 6-й день лечения. Реологические свойства крови изучали на аппарате "анализатор крови реологический" (АКР-2) по методике, предложенной А. С. Парфеновым, Н. А. Добровольским [3]. Уровень Д-димеров определяли количественным экспресс-методом с использованием портативного прибора Cardiac Reader ("Hoffman La Roche", Швейцария). В качестве исследуемого материала использовали гепа-ринизированную венозную кровь. Время исследования — 8 мин. Диапазон линейности теста — 100 - 4000 нг/мл. Референтные значения — содержание Д-димера менее 500 нг/мл.
Оценку клинических симптомов заболевания проводили ежедневно во время всего периода заболевания.
У всех детей были выявлены клинические проявления симптомокомплекса эндогенной интоксикации: слабость, вялость, отсутствие аппетита, нарушение сна, температурная реакция, тахикардия.
Больные ЭБВ-мононуклеозом, включенные в исследование, распределились следующим образом: мальчики составили 36 человек (60 %), девочки — 24 человека (40 %). Дети в возрасте от 1 года до 7 лет — 40 человек (67 %), от 7 до 14 лет — 20 человек (33 %).
В большинстве случаев заболевание протекало на неотягощенном преморбидном фоне — 96 %, в 1,7 % случаев (1 человек) наблюдалось наличие малой мозговой дисфункции (синдром повышенной нервной возбудимости), в 5 % случаев (3 человека) — наличие патологии сердечно-сосудистой системы (стеноз легочной артерии, миокардиодистрофия), в 1,7 % (1 человек) — детский церебральный паралич, в 1,7 % (1 человек) — хронический пиелонефрит в стадии ремиссии.
Лечение было комплексным, пациенты получали патогенетическую и симптоматическую терапию согласно стандартам лечения. Всем больным с тяжелой формой ЭБВ-мононуклеоза с целью дезинтоксикации проводили инфузионную терапию.
В зависимости от метода лечения были сформированы две группы детей. В основной группе (20 пациентов с тяжелой формой ЭБВ-мононуклеоза) наряду с инфузионной терапией глюкозо-солевыми растворами в программу был включен реамберин в дозе 10 мл/кг внутривенно капельно. Состав реамберина: активный компонент: меглумина натрия сукцинат — 15 г (получен по следующей прописи: N-метилглюкамина (мег-лумина) — 8,725 г, янтарной кислоты — 5,28 г); вспомогательные вещества: натрия хлорид — 6 г, калия хлорид — 0,3 г, магния хлорид (в пересчете на безводный) — 0,12 г, натрия гидроксид — 1,788 г, вода для инъекций до 1 л.
Группу сравнения составили 20 пациентов с тяжелой формой ЭБВ-мононуклеоза, получавшие инфузи-онную терапию глюкозо-солевыми растворами без ре-амберина. Между изучаемыми группами не было существенного различия по возрасту, полу, основным клинико-лабораторным показателям.
Статистическую обработку полученных результатов проводили на персональном компьютере при использовании пакета электронных таблиц Microsoft Excel 2010 Beta, программы Statistica 6.0.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследования реологических показателей крови проводили дважды: при поступлении и на 5 - 6-й день лечения.
При среднетяжелой форме ЭБВ-мононуклеоза в острый период наблюдалось статистически достоверное повышение вязкости плазмы до 1,43 + 0,01 мПа • с, что на 18,2% выше, чем у здоровых детей (р < 0,05; табл. 1). Отмечено статистически достоверное повышение вязкости крови при малых скоростях сдвига, в большей степени (при скорости сдвига 20 1 /с)—на 7,2 % ( р 0,05; табл. 1), в меньшей степени при скорости сдвига 100 1 /с и 200 1 /с — на 2 % и 3,5 %, соответственно ( р 0,05; табл. 1).
Таким образом, при среднетяжелой форме ЭБВ-мо-нонуклеоза у обследованных больных регистрировалась повышенная вязкость крови в сосудах микроциркуляционного русла в большей степени, в сосудах среднего и крупного калибра — в меньшей степени.
Индекс агрегации эритроцитов (ИАЭ) увеличивался на 6,3%, достигая 1,35 + 0,01 усл. ед. (р < 0,05; табл. 1).
Индекс деформируемости эритроцитов (ИДЭ) достоверно не изменялся.
Таблица 1. Показатели реологических параметров крови при среднетяжелой форме ЭБВ-инфекции у детей в острый период и на фоне лечения (М + т, п = 20)
Основная группа, острый период,
n = 40
Основная груп па, 5 - 6-й день лечения,
n =4
Вязкость крови при скорости сдвига 20 1 /c, мПас
Вязкость крови при скорости сдвига 100 1 /c, мПас
Вязкость крови при скорости сдвига 200 1/c, мПас
Вязкость плазмы, мПа
Примечание. n — число наблюдений; * — отличия достоверны по сравнению с контролем, р < 0,05.
Таким образом, наиболее ранним диагностическим признаком нарушения гемореологических свойств крови при среднетяжелой форме ЭБВ-мононуклеоза является повышение вязкости крови преимущественно в сосудах микроциркуляционного русла, повышение агрегации эритроцитов.
Характер гемореологической кривой при среднетя-желой форме ЭБВ-мононуклеоза у обследованных детей в острый период заболевания показан на рис. 1.
Как видно из табл. 1 и рис. 1 при повторном обследовании при среднетяжелой форме ЭБВ-мононуклеоза у детей все реологические параметры крови восстанавливались и не имели достоверных отличий от контроля.
Детям со среднетяжелой формой ЭБВ-мононуклео-за в острый период заболевания проводилось исследование Д-димеров, являющихся фрагментами волокон фибрина, которые образуются в процессе фибриноли-за при расщеплении фибринового сгустка плазмином. По уровню Д-димеров можно судить о наличии или отсутствии ДВС-синдрома при инфекционной патологии [11]. Уровень данного показателя в острый период заболевания у обследованной группы детей не превышал допустимые значения (500 нг/мл), поэтому не определялся повторно, на 5 - 6-й день лечения (табл. 1).
В острый период при тяжелой форме ЭБВ-моно-нуклеоза наблюдали статистически достоверное повышение вязкости крови при всех скоростях сдвига ( р 0,05; табл. 2). Максимальное повышение вязкости крови регистрировали в сосудах микроциркуляторно-го русла. Так, при скорости сдвига 20 1 /с отмечено увеличение вязкости крови на 59,4 % выше по сравнению с группой контроля ( р 0,05, табл. 2). Выявлено статистически достоверное увеличение вязкости крови в сосудах среднего калибра — при скорости сдвига 100 1/с (р < 0,05) на 12,6 %ивсосудах крупного калибра на 16,5 % — при скорости сдвига 200 1 /с (р < 0,05, табл. 2).
Key words: Epstein - Barr virus infection, hemorheological disorders, blood viscosity, reamberine
Мононуклеоз является острым инфекционным заболеванием вирусной природы. Оно имеет несколько наименований: его называют моноцитарной ангиной, болезнью Филатова и доброкачественным лимфобластозом. Также это заболевание именуют инфекционным мононуклеозом или вирусным. Для заболевания характерны лихорадочные состояния и поражения ротоглотки и лимфоузлов. Более того, мононуклеоз влияет на печень, селезенку и кровь. Мононуклеоз больше распространен у детей. Чаще всего заболевание человека приходится на осень. Дети особенно подвержены заболеванию мононуклеозом в период стрессов и тяжелых физических нагрузок. Мононуклеоз, как правило, переносится людьми в подростковом возрасте. Так, у женского пола это приходится на возраст 14-16 лет, а у мужчин — на 16-18 лет. После сорокалетнего возраста болезнь встречается редко. Во время обострения заболевания вирус инфицирует здоровые клетки. Если иммунитет ослаблен, то развивается суперинфекция. Если вирус поражает лимфоидную и ретикулярную виды ткани, то у пациента наблюдается лимфоаденопатия и гипертрофия печени и селезенки.

Как правило, человеку достаточно переболеть мононуклеозом один раз, чтобы выработать пожизненный иммунитет к этому заболеванию.
Как действует вирус мононуклеоза
При попадании в дыхательные пути вирус мононуклеоза поражает эпителиальные покровы и лимфоидные структуры ротовой полости и глотки. Это приводит к отечности слизистой, гипертрофия миндалин и лимфоузлов. Внедряясь в лимфоциты группы Б, вирус распространяется по всему организму пациента. При распространении вируса Эпштейна-Барра в крови пациента обнаруживаются атипичные мононуклеары. Гистологические исследования показывают гиперплазию лимфоидной и ретикулярной тканей. У пациента наблюдается увеличение печени и селезенки, лимфоаденопатия, также возможны изменения функциональности клеток печени.
Причины мононуклеоза
Почему у людей появляется такое заболевание, как мононуклеоз? Для ответа на этот вопрос нам нужно ознакомиться с причинами развития и возбудителем мононуклеоза. Возбудитель мононуклеоза называется вирусом Эпштейна-Барра. Этот вирус назван в честь открывших его ученых: патолога М.А. Эпштейна и вирусолога И. Барра. Этот вирус является Б-лимфотропным вирусом человека и относится к вирусам группы герпеса. Люди остро восприимчивы к нему. Вирус Эпштейна-Барра может долгое время пребывать в организме в качестве скрытой инфекции. Источником такой инфекции для окружающих может стать носитель вируса и больной мононуклеозом яркой и стертой формы. Это заболевание передается воздушно-капельным, половым, контактно-бытовым путем. Мононуклеоз в простонародье называют болезнью поцелуев. Это связано со способностью заболевания передаваться через слюну. Также заразиться мононуклеозом можно во время родовой деятельности и во время переливания крови. Подхватить заболевание достаточно легко: это может произойти даже во время поездки на общественном транспорте. Иммунодефицит стимулирует развитие и распространение мононуклеоза. Инкубационный период мононуклеоза составляет от пяти дней до полутора месяцев.
Симптомы мононуклеоза

Мононуклеоз может протекать как с ярко выраженными симптомами, так и с их отсутствием. При неярком течении болезни у пациентов могут наблюдаться субфебрилитет, ослабленность с повышенной утомляемостью, гиперемия слизистой ротоглотки и миндалин, а также может быть затруднено носовое дыхание, наблюдаться сильные выделения слизи и першение в горле. Если мононуклеоз развился резко и остро, то температура тела будет высокой, появится болезненность при глотании, лихорадка и головная боль. Зачастую у людей ломит все тело. Так заболевание проявляется в течение первой недели. Далее уже проявляются более серьезные симптомы мононуклеоза, выражающиеся в виде увеличения печени и селезенки, ангины, лимфоаденопатии и сильной боли в области горла. Боль может распространиться на мышцы и суставы. При мононуклеозе нарушается носовое дыхание и появляется гнусавость, как при гайморите. Для заболевания характерно образование желтоватого налета на миндалинах, сыпи на мягком небе и фолликул на глоточной стенке. Еще одним ярким симптомом мононуклеоза является увеличение лимфоузлов до трех сантиметров. Надо сказать, что это, впрочем, безболезненно. Лимфоузлы увеличиваются в основном при детском мононуклеозе. В период мононуклеоза у пациентов может наблюдаться пожелтение кожи и слизистых. Такие симптомы ближе мононуклеозу у взрослых. Во время реконвалесценции симптомы ослабевают. Этот период происходит через пару-тройку недель после разгара заболевания. Периоды обострений заболевания сменяются временами ремиссии, а сама болезнь может протекать долго.
Тонзилит при мононуклеозе носит катаральный и лакунарный характер. Для катарального тонзилита характерна припухлость миндалин, а для лакунарного — воспалительный процесс в области миндалин с наличием язвенно-некротических поражений. На фоне мононуклеоза может развиться назофарингит. Так как это заболевание влияет на лимфоток, то на коже могут проявляться папулы и пигментные пятна. Такая сыпь может сохраняться до 5 дней, а потом самостоятельно исчезает.
Лечением мононуклеоза занимается врач-инфекционист. В случаях мононуклеоза у детей для начала следует обратиться к педиатру. Врач назначает необходимое лечение и режим. После мононуклеоза пациентам показано диспансерное наблюдение в течение полугода. В этот период нужно избегать физических нагрузок и стрессов.
Классификация мононуклеоза
Мононуклеоз может быть типичным и атипичным, острым и хроническим. Также отдельно выделяют мононуклеоз у пациентов с ВИЧ и при иммунодефиците. Типичный мононуклеоз протекает с проявлением симптомов заболевания, а атипичный мононуклеоз протекает бессимптомно.
Диагностика мононуклеоза

Для проведения диагностики заболевания врач после осмотра назначает лабораторные исследования. В первую очередь пациента отправляют сдавать кровь. По результату такого теста можно исключить иные патологии со схожими симптомами. На мононуклеоз указывает наличие в крови атипичных мононуклеаров и увеличенное количество лимфоцитов. Вирус мононуклеоза можно обнаружить в слюне. В скрытой форме вирус Эпштейна-Барра можно обнаружить в лимфоцитах группы Б и в слизистой рта и глотки. При получении положительного результата анализа можно говорить о наличии инфекции, о хронической форме заболевания или начале инфицирования. Отрицательный результат указывает на отсутствие инфекции, соответственно. ПЦР-диагностика позволяет найти ДНК вируса в сыворотке крови и в цельной. Постановке диагноза поможет выявление сывороточного иммуноглобулина М к VCA-антигенам. После выздоровления пациента иммуноглобулин М к VCA-антигенам исчезает. Переболев единожды мононуклеозом, организм человека сохраняет навсегда иммуноглобулин G к VCA-антигенам.
Чтобы следить за процессом развития мононуклеоза, нужно сдавать кровь на анализ каждые три дня. Это важно и потому, что начальная стадия ВИЧ может сопровождаться синдромом, подобным мононуклеозу.
Лечение мононуклеоза

Лечение мононуклеоза направлено на обезвреживание его возбудителя — вируса Эпштейна-Барра. Для этого назначаются специальные препараты, антибиотики, кортикостероиды (в особых случаях) и проводят симптоматическую терапию. Лечение направляется и на восстановление печени. Любознательные пациенты должны помнить, что при наличии налета на миндалинах нельзя пытаться удалить его подручными средствами, это навредит вашему здоровью и спровоцирует сепсис.В состав симптоматической терапии входят жаропонижающие средства от лихорадки и сосудосуживающие препараты для улучшения носового дыхания, антигистаминные средства, чтобы избежать аллергической реакции. В состав такого лечения входят средства, укрепляющие иммунную систему, и противовирусные лекарства. Для лечения горла назначаются полоскания фурацилином, содой и солью. Устранить боль и понизить температуру помогут ибупрофен или ацетаминофен. Кортикостероиды, помимо снятия боли, помогут ликвидировать отек. При лечении мононуклеоза пациенту зачастую показан постельный режим и специальная диета. Диета при мононуклеозе состоит из продуктов питания, не нагружающих печень. Само питание дробится на 4-5 приемов в день. Пациент должен получать в полноценном объеме белки, жиры растительного происхождения, углеводы и витамины. К продуктам, которые нужно употреблять при мононуклеозе, относят молочную продукцию, нежирную рыбу и мясо, фрукты и ягоды, овощи, каши, хлеб из муки грубого помола. К запрещенным продуктам при мононуклеозе относят сливочное масло, жареное, копченое, маринованное, острое, соленое и консервы. Физические нагрузки при мононуклеозе запрещены, за исключением лечебной физкультуры. Профилактика мононуклеоза на сегодняшний день не разработана.
Осложнения мононуклеоза
Осложнения на почве мононуклеоза не сильно распространены, но опасны. Но, так или иначе, к ним относят отит, паратонзиллит, синуситы. У детей чаще наблюдаются осложнения в виде пневмонии. Редко встречаются разрыв селезенки и гемолитическая анемия (высокий уровень разрушаемости эритроцитов), тромбоцитопения и гранулоцитопения. Смертельно опасными осложнениями мононуклеоза считаются непроходимость дыхательных путей и разрыв селезенки. Мононуклеоз способен вызывать осложнения неврологической системы: энцефалит, полиневрит и паралич мимических мышц. Помимо этого, последствиями заболевания могут стать психозы, осложнения работы дыхательной и сердечной систем.
На здоровье ребенка мононуклеоз оставляет след в виде повышенной утомляемости, необходимости отдыха в большом количестве и снижения нагрузки.
Инфекционный мононуклеоз может спровоцировать лимфому Беркитта и карциному носоглотки.
Особенности инфекционного мононуклеоза у детей

Заражению мононуклеозом наиболее подвержены дети до десяти лет. Дети могут заразиться, например, в детском садике воздушно-капельным путем, через поцелуи, пользование общей посудой и т.д. Это заболевание больше распространено у мальчиков. Чаще всего заболевание мононуклеозом у детей происходит в осеннее время и в период прихода зимы. Инфекционный мононуклеоз не всегда протекает с яркой симптоматикой, но знать его симптомы необходимо. Разберем их подробнее. Симптомами мононуклеоза у ребенка считаются признаки общей интоксикации, выражающиеся в виде озноба, утомляемости, появления сыпи и увеличения лимфатических узлов. К признакам инфекционного мононуклеоза можно добавить чувство першения в горле, субфебрильной температуры и заложенности носовых ходов. У детей также наблюдается гиперемия слизистых оболочек ротовой полости и глотки. При более ярком протекании болезни можно наблюдать у ребенка лихорадку, сонливость, повышенное потоотделение, болезненное глотание и боли в голове, горле и мышцах. В самый разгар заболевания развивается ангина, увеличение печени и селезенки, интоксикация и сыпь по телу. Сыпь, развившаяся на почве мононуклеоза, не вызывает зуда и не нуждается в специальном лечении. Яркими проявлениями мононуклеоза у детей становится гипертрофия лимфоузлов и разрастание лимфоидной ткани, а, следовательно, и полиаденит. На миндалинах маленького пациента легко заметить серо-бело-желтый налет, который легко устраняется. Что касается лимфатических узлов, то наиболее подвержены гипертрофии задние шейные лимфатические узлы. Прощупывание этих образований не вызывает болезненных ощущений у ребенка.
Лечение мононуклеоза у детей
Специального лечения мононуклеоза у детей нет. На сегодняшний день терапия детского инфекционного мононуклеоза включает симптоматическое и патогенетическое лечение, а также применение антисептических, десенсибилизирующих и общеукрепляющих лекарственных средств. При поражении печени врач назначает гепатопротекторы и специальную диету. Иммуноукрепляющие препараты эффективнее применять вместе с противовирусными средствами.
Антибиотики успешно используются для лечения вторичной инфекции. Их применение, как правило, совмещено с приемом пробиотиков.
При наличии риска удушья пациенту выписывают курс преднизолона. В случае сильной отечности гортани у детей медики прибегают к установке трахеостомы и использованию аппарата ИВЛ. В тех ситуациях, когда существует явная угроза разрыва селезенки, следует провести спленэктомию.
Детский инфекционный мононуклеоз, как правило, хорошо поддается лечению.
Мононуклеоз и беременность
Как правило, мононуклеоз не опасен для плода во время беременности женщины, но опасны сопровождающие его симптомы. Например, высокая температура у будущей мамы может оказать негативное влияние на плод. Чаще всего мононуклеоз у беременных проявляется повышением температуры, болезненными ощущениями в горле и гипертрофией лимфатических узлов. Общее состояние женщины сопровождается утомляемостью и сонливостью. В отдельных случаях вирусный мононуклеоз у беременных может сопровождаться более выраженными симптомами. При подозрении на мононуклеоз (болезнь Филатова) будущая роженица должна обратиться к инфекционисту за диагностикой и выявлением заболевания. Лечение мононуклеоза у беременных включает достаточное количество отдыха, недопускание высоких температур тела, и избегания обезвоживания организма. Обезвоживание может быть вызвано поднятием температуры и нарушением аппетита.
Если женщина заболела мононуклеозом в период планирования беременности, то зачатие лучше отложить до лучших времен. Пока состояние женщины не улучшится, следует пользоваться средствами контрацепции. Есть риск развития гепатита на почве мононуклеоза, что совсем не является положительным для будущей беременности. Медицинские специалисты пришли к выводу, что о вынашивании ребенка женщина может начать думать не раннее, чем через полгода, а то и целого года после мононуклеоза. Это же касается и случаев, когда мононуклеозом переболел будущий отец. Осложнения мононуклеоза могут помешать нормальному развитию беременности и спровоцировать выкидыш на раннем этапе. В большинстве случае медики настаивают на прерывании беременности при наличии инфекционного мононуклеоза. Лучше провести полноценное лечение заболевания, чтобы не дать перейти ему в хронический мононуклеоз. После успешного лечения и восстановления общего состояния здоровье женщины будет готово к удачной беременности.
Читайте также:

