Вирусный паралич у ребенка
Обновлено: 19.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Менингит: причины появления, симптомы, диагностика и способы лечения.
Определение
Менингит – это инфекционное воспаление мозговых оболочек головного и спинного мозга, сопровождающееся интоксикацией, лихорадкой, синдромом повышенного внутричерепного давления, менингеальным синдромом, а также воспалительными изменениями ликвора (спинномозговой жидкости).
Мозговые оболочки - это соединительнотканные пленчатые образования, покрывающие головной и спинной мозг. Различают твердую мозговую оболочку, паутинную и мягкую.
Твердая оболочка головного мозга имеет плотную консистенцию и толщину 0,2-1 мм, местами она срастается с костями черепа. Паутинная оболочка — тонкая, полупрозрачная, не имеющая сосудов соединительнотканная пластинка, которая окружает головной и спинной мозг. Мягкая оболочка — тонкая соединительнотканная пластинка, непосредственно прилежащая к головному мозгу, соответствует его рельефу и проникает во все его углубления. В ее толще располагается сосудистая сеть головного мозга.
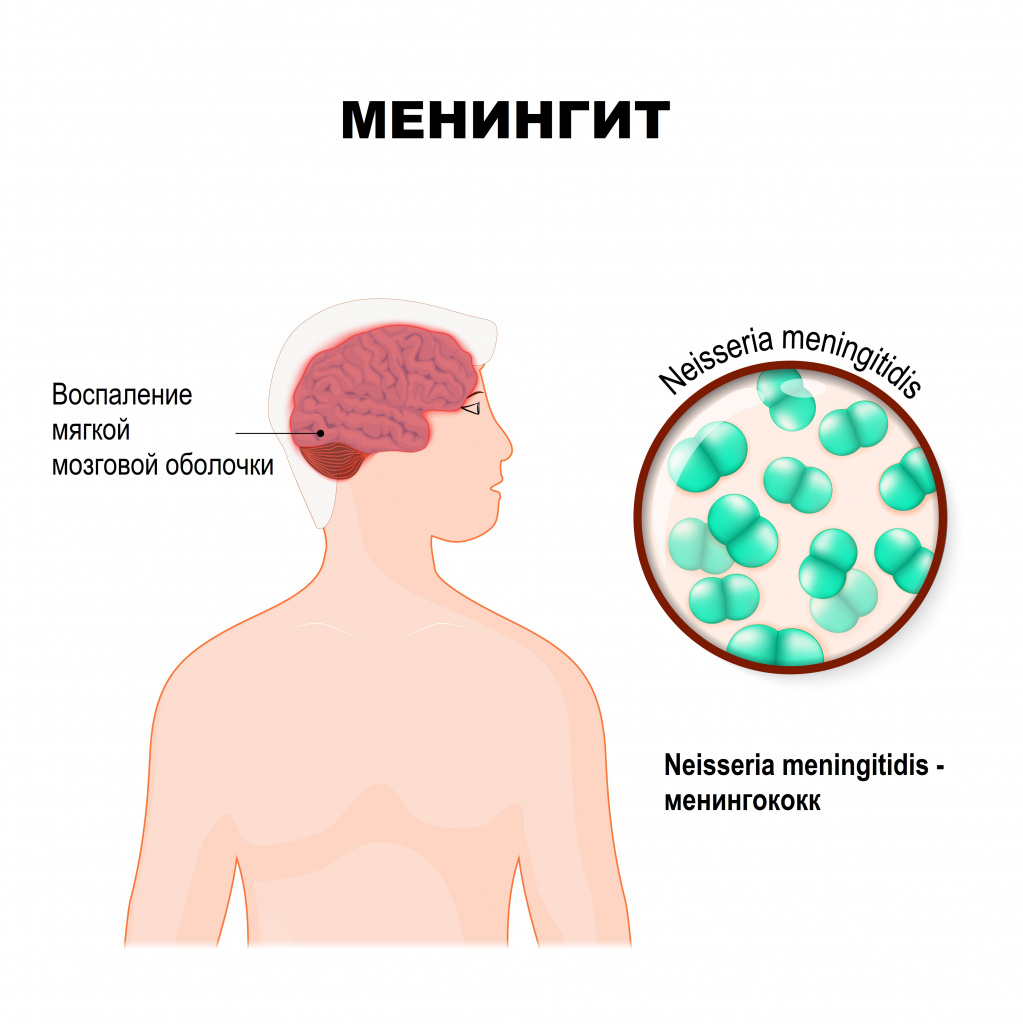
Причины появления менингита
Мозговые оболочки могут вовлекаться в воспалительный процесс первично и вторично. Менингит, возникший без предшествующей общей инфекции или заболевания какого-то другого органа, называется первичным. Вторичный менингит развивается как осложнение уже имеющегося инфекционного процесса. К вторичным относятся туберкулезный, стафилококковый, пневмококковый менингит. К первичным – менингококковый, первичный паротитный, энтеровирусные менингиты и другие.
Гнойное воспаление мозговых оболочек может быть вызвано различной бактериальной флорой (менингококками, пневмококками, реже - другими возбудителями). Причина серозных менингитов - вирусы, бактерии, грибы.
По прогнозу наиболее опасен туберкулезный менингит, который возникает при условии наличия в организме туберкулезного поражения. Развитие заболевания проходит в два этапа. На первом этапе возбудитель с током крови поражает сосудистые сплетения желудочков мозга с образованием в них специфической гранулемы. На втором – наблюдается воспаление паутинной и мягкой оболочек (как правило, поражаются оболочки основания головного мозга), которое вызывает острый менингиальный синдром.
Процесс развития менингококкового менингита также состоит из нескольких этапов:
- попадание возбудителя на слизистую оболочку носоглотки;
- попадание менингококка в кровь;
- проникновение возбудителя через гематоликворный барьер, раздражение рецепторов мягкой мозговой оболочки токсичными факторами и воспаление.
Течение инфекционного процесса зависит от патогенных свойств возбудителя (способности вызывать заболевание) и состояния иммунной системы человека.
Предшествующие вирусные заболевания, резкая смена климата, переохлаждение, стресс, сопутствующие заболевания, терапия, подавляющая иммунитет, - могут иметь существенное значение для возникновения и течения менингита.
Классификация заболевания
По типу возбудителя:
- Вирусный менингит (гриппозный, парагриппозный, аденовирусный, герпетический, арбовирусный (клещевой), паротитный, энтеровирусные ЕСНО и Коксаки).
- Бактериальный менингит (менингококковый, туберкулезный, пневмококковый, стафилококковый, стрептококковый, сифилитический, бруцеллезный, лептоспирозный).
- Грибковый (криптококковый, кандидозный и др.).
- Протозойный (токсоплазмозный, малярийный).
- Смешанный.
- Первичный.
- Вторичный.
- Острый.
- Подострый.
- Молниеносный.
- Хронический.
- Легкая.
- Среднетяжелая.
- Тяжелая.
- Генерализованный.
- Ограниченный.
- Осложненный.
- Неосложненный.
- менингеальный синдром – проявляется ригидностью (повышенным тонусом) затылочных мышц и длинных мышц спины, гиперстезией (повышенной чувствительностью) органов чувств, головной болью, рвотой, изменениями со стороны спинномозговой жидкости;
- общемозговой синдром – проявляется сонливостью, нарушением сознания, тошнотой, рвотой, головокружением, психомоторным возбуждением, галлюцинациями;
- астеновегетативный синдром – проявляется слабостью, снижением трудоспособности;
- судорожный синдром;
- общеинфекционный синдром - проявляется ознобом, повышением температуры.
Пневмококковый менингит, как правило, наблюдается у детей раннего возраста на фоне имеющегося пневмококкового процесса (пневмонии, синусита).
При стрептококковом менингите на первый план выступает гепатолиенальный синдром (увеличение печени и селезенки), почечная недостаточность, надпочечниковая недостаточность, петехиальная сыпь (кровоизлияния, вследствие повреждения капилляров, в результате чего, кровь, растекаясь под кожей, образует округлые пятна, размер которых не превышает 2 мм).
Гнойные менингиты, вызванные синегнойной палочкой, грибами встречаются редко. Диагноз устанавливается только после дополнительных лабораторных исследований.
Для серозного туберкулезного менингита характерно постепенное начало, хотя в редких случаях он может манифестировать остро. В дебюте заболевания больные жалуются на утомляемость, слабость, раздражительность, нарушение сна. Температура обычно не выше 38℃, отмечается непостоянная умеренная головная боль. На 5-6-й день болезни температура становится выше 38℃, усиливается головная боль, появляется тошнота, рвота, сонливость. Быстро развивается бессознательное состояние. Могут наблюдаться расходящееся косоглазие, низкое положение верхнего века по отношению к глазному яблоку, расширение зрачка.
Клинические проявления поражения мозговых оболочек могут развиваться еще до увеличения слюнных желез.
Для энтеровирусного менингита характерна двух- и трехволновая лихорадка с интервалами между волнами 1-2 и более дней. Почти всегда наблюдаются и другие проявления энтеровирусной инфекции (мышечные боли, кожная сыпь, герпангина).
Для диагностики коревого и краснушного менингитов большое значение имеет указание на контакт с больным этими заболеваниями, а также типичные клинические симптомы кори или краснухи.
Диагностика менингита
-
клинический анализ крови с определением концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC), лейкоформула и СОЭ (с микроскопией мазка крови при наличии патологических сдвигов);
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Острый вялый паралич - это сложный клинический синдром, характеризующийся остро возникшим нарушением активных движений (объѐма, силы, быстроты) в одной или нескольких конечностях, снижением мышечного тонуса, изменением рефлексов.
Острый вялый паралич (ОВП)- это любое заболевание у ребенка до 15 лет с острым вялым параличом, сходное с полиомиелитом заболевание у больного любого возраста. Таким образом, к ОВП причисляют все заболевания, которые протекают с быстрым развитием вялых параличей, но не более чем в течение 4 суток.
Основной причиной данной болезни считаются различные энтеровирусы.
Симптомы острого вялого паралича:
Острый вялый паралич характеризуется такими проявлениями:
- острое начало с общеинфекционных признаков,
- мышца не оказывает сопротивления движениям пассивного характера;
- атрофия выражена очень сильно;
- отмечается снижение либо полное отсутствие глубоких рефлексов;
- мышечная и нервная электровозбудимость меняется.
- очень короткий период нарастания двигательных нарушений: от нескольких часов до 2 - 3 дней.
У детей также проявляются симптомы этого заболевания – они выражаются в виде слабости либо дрожи в конечностях, а помимо этого в неправильном функционировании глотательной, а также дыхательной мускулатуры, потому как разрушаются нижние двигательные нейроны.
Профилактика.
Для профилактики заболевания следует придерживаться таких правил:
- Нужно вовремя лечить инфекционные патологии;
- Отказаться от всех вредных привычек и вести ЗОЖ – гулять на свежем воздухе, выполнять физические упражнения, соблюдать правильный рацион питания и пр.;
- В случае ухудшения здоровья без промедления обращаться к доктору;
- Контролировать уровень АД.
Острый полиомиелит относится к инфекционным заболеваниям вирусной этиологии и характеризуется разнообразием клинических форм. Часто, клиническая картина выражается развитием вялых и периферических парезов и/или параличей.
Источником инфекции является человек, больной или носитель.
Вирус полиомиелита выделяется у больного человека с фекалиями, а заражение происходит через воду, продукты питания, бытовые предметы. Возможен и воздушно-капельный и воздушно-пылевой путь передачи.
Естественная восприимчивость людей высокая, однако часто болезнь протекает бессимптомно. К сожалению, именно бессимптомные носители заболевания представляют большую эпидемиологическую опасность.
Наибольшему риску заболевания полиомиелитом в случае завоза дикого вируса полиомиелита подвержены дети, не привитые против этой инфекции (получившие менее 3 прививок против полиомиелита) или привитые с нарушением сроков иммунизации в возрасте до 7 лет.
Разработка эффективных вакцин для профилактики полиомиелита стала одним из наиболее крупных медицинских достижений XX века.
На сегодняшний день существуют два основных типа вакцин:
1. Оральная полиомиелитная вакцина (OПВ), содержащая ослабленный живой полиовирус в виде горьких капель, которая вводится через рот.
2. Инактивированная полиомиелитная вакцина (ИПВ), содержащая убитый полиовирус, которая вводится внутримышечно.
В России прививки против полиомиелита входят в Национальный календарь профилактических прививок, согласно которому всем детям первого года жизни необходимо сделать три прививки от полиомиелита (в 3; 4,5 и 6 месяцев) – вакцинацию, и последующие 3 ревакцинации: в 18, 20 месяцев и в 14 лет.
Первые две прививки делают инактивированной полиомиелитной вакциной (независимо от возраста, даже если по каким-то причинам ребенок начал прививаться в срок старше года), которая вводится с помощью инъекции.
Последующие прививки (3-я,4-ая,5-ая и 6-ая) – живой полиомиелитной вакциной, которая закапывается в рот. ИПВ считается высоко безопасной вакциной независимо от того, вводится ли она отдельно или в комбинации с другими вакцинами.
Многих родителей, бабушек и дедушек беспокоит вопрос, а не нанесет ли прививка против полиомиелита вред здоровью ребенка?
Спешим Вас успокоить, частота развития вакциноассоциированного полиомиелита невелика, по статистике около 10 случаев в год по стране. Приходится в основном на детей с выраженными нарушениями иммунитета и с тяжелыми хроническими заболеваниями.
Часто, у родителей происходит непонимание, почему после того, как в группе детского сада провели вакцинацию детей живой полиомиелитной вакциной, непривитых детей или получивших менее 3 доз полиомиелитной вакцины разобщают с детьми, на срок 60 дней с момента получения детьми последней прививки живой оральной полиовакциной.
На самом деле, такая мера направлена на защиту непривитых или прошедших не полный курс вакцинации детей, ведь после прививки живой вакциной, вирус полиомиелита выделяется с фекалиями ребенка и для сильно ослабленных детей и при несоблюдении правил гигиены может быть опасен. Хотя справедливости ради надо отметить, что такие случаи единичны.
Поэтому, если Ваш ребенок не имеет проблемы со здоровьем, проведенная вакцинация является единственным способом профилактики этого тяжелого заболевания и надежным барьером на пути его распространения.
Противопоказаниями к введению вакцин против полиомиелита являются:
Для ОПВ (оральная полиомиелитная вакцина):
Неврологические расстройства, сопровождавшие предыдущую вакцинацию полиомиелитной вакциной.
• Иммунодефицитное состояние (первичное), злокачественные новообразования, иммуносупрессия (прививки проводят не ранее, чем через 6 месяцев после окончания курса терапии).
• Плановая вакцинация откладывается до окончания острых проявлений заболевания и обострения хронических заболеваний. При легком течении ОРВИ, острых кишечных заболеваний и других нетяжелых состояниях прививки проводятся сразу же после нормализации температуры.
Для ИПВ (инактивированная полиомиелитная вакцина):
• Заболевания, сопровождающиеся повышением температуры тела, острые проявления инфекционного заболевания или обострение хронического заболевания. В этих случаях вакцинацию откладывают до выздоровления.
• Аллергическая реакция на предшествующее введение вакцины (аллергия может возникнуть на активные компоненты или к одному из вспомогательных веществ).
В обязательном порядке по эпидемическим показаниям прививку против полиомиелита проводят всем контактным лицам в очагах полиомиелита, в том числе вызванного диким полиовирусом (или при подозрении на заболевание):
- детям с 3 месяцев до 18 лет - однократно;
- медицинским работникам - однократно;
- детям, прибывшие из неблагополучных по полиомиелиту регионов (Пакистан, Афганистан), с 3 месяцев до 15 лет - однократно (при наличии достоверных данных о предшествующих прививках) или трехкратно (при отсутствии таких данных);
- лицам, контактировавшим с прибывшими из неблагополучных по полиомиелиту регионов, с 3 месяцев жизни без ограничения возраста - однократно;
- лицам без определенного места жительства с 3 месяцев до 15 лет - однократно (при наличии достоверных данных о предшествующих прививках) или трехкратно (при их отсутствии);
- лицам, работающим с живым полиовирусом, с материалами, инфицированными (потенциально инфицированными) диким вирусом полиомиелита без ограничения возраста - однократно при приеме на работу.
Вакцинация против полиомиелита по эпидемическим показаниям проводится в соответствии с постановлением главного государственного санитарного врача субъекта Российской Федерации, которым определяется возраст детей, подлежащих вакцинации, сроки, порядок и кратность ее проведения.
Единственным эффективным способом борьбы с полиомиелитом остается вакцинация!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Паралич: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Паралич – полная утрата движений в одной или нескольких частях тела, потеря мышцей или группой мышц мышечной силы, неспособность к выполнению движений. В некоторых случаях термин используется для описания нарушений сократительной способности мышц. Паралич не является самостоятельным заболеванием, но лишь одним из симптомов многих органических патологий нервной системы.
Разновидности паралича
Любое повреждение нервной системы может привести к нарушению двигательной функции. Различают органические, функциональные и рефлекторные параличи.
Органические параличи формируются из-за того, что на нервную систему (на любом ее уровне) воздействуют опухоли, травмы, инфекции или какие-либо другие факторы.
Функциональные параличи в большинстве случаев возникают в результате образования так называемой застойной области торможения в головном мозге, из-за чего к мышцам не поступает команда, чтобы те сокращались. В процессе развития заболевания не возникает патологических изменений, рефлексы остаются в норме, мышечный тонус поддерживается на должном уровне.
Рефлекторные параличи обусловлены поражением периферического двигательного нейрона, могут быть вызваны поражением любого участка нервного проводящего пути.
С анатомической точки зрения различают параличи, вызванные поражением центральной нервной системы (головного или спинного мозга), и параличи, связанные с поражением периферических нервов.
Многообразие причин параличей отражается на патоморфологических изменениях, которые могут иметь самые разные характер и локализацию.
Паралич подразделяют по степени выраженности, стойкости и распространенности. Он может быть полным или частичным, необратимым или преходящим, локализованным или распространенным.
Ни один из этих клинических типов не является самостоятельной патологией, однако существуют отдельные виды паралича, представляющие самостоятельные заболевания. К ним относятся болезнь Паркинсона (дрожательный паралич), полиомиелит (детский паралич), паралич Белла, бульбарный паралич, псевдобульбарный паралич, семейный периодический паралич, паралич вследствие поражения плечевого сплетения, детский церебральный паралич и другие.
Разрушение, дегенерация, воспаление, образование очагов (бляшек), склероз, демиелинизация – наиболее типичные варианты патологических изменений нервной ткани, выявляющихся при параличе. По своему развитию различают острый и вялый паралич. В первом случае симптоматика нарастает очень быстро, во втором обездвиживание развивается постепенно.
Выделяют следующую классификацию паралича, основанную на распространенности процесса:
- моноплегия – паралич одной конечности с одной стороны тела;
- параплегия – паралич двух конечностей одного типа, например, обеих рук;
- гемиплегия – паралич развивается в конечностях с одной стороны;
- тетраплегия – одновременно поражаются все четыре конечности;
- офтальмоплегия – паралич мышц, которые обеспечивают двигательную активность глаз.
При поражении периферических двигательных нейронов вместо повышения мышечного тонуса происходит его снижение. Поражаются отдельные мышцы, в которых выявляются атрофия и электрофизиологическая реакция перерождения. В парализованной конечности глубокие рефлексы снижаются или совсем пропадают, клонусы отсутствуют.
Психогенный паралич, не имеющий в своей основе органического поражения, может имитировать один из этих вариантов либо сочетать черты того и другого. Центральный паралич может проявляться в чистом виде или сочетаться с чертами периферического паралича. Как правило, ему сопутствуют сенсорные и трофические расстройства, а также изменения сосудистого тонуса.
Возможные причины паралича
Существуют разные причины паралича, но все они сводятся к поражению нервной системы, вызванному травмой, опухолью, абсцессом или воспалением. Кроме того, паралич может возникнуть как результат демиелинизирующих заболеваний, связанных с разрушением белка, который обеспечивает проведение нервного импульса по волокнам, – миелина. К таким заболеваниям относятся: рассеянный склероз, рассеянный энцефаломиелит и др.
Причинами паралича также могут являться:
Чтобы установить причину паралича, следует обратиться к врачу-терапевту , врачу общей практики или врачу-неврологу . При детском параличе необходимо срочно показать ребенка врачу-педиатру. Врач проведет необходимое обследование, консультации с профильными специалистами, назначит необходимое лечение.
Диагностика и обследования при параличах
Первым и самым частым проявлением паралича обычно является невозможность перемещаться и управлять опорно-двигательным аппаратом из-за отсутствия силы в мышцах или целой группе мышц, а именно:
- полное отсутствие мышечной силы в мышцах верхних конечностей, в результате чего становится невозможным выполнить такие действия, как захват предмета, поднятие, сгибание и разгибание руки;
- полное отсутствие мышечной силы в мышцах нижних конечностей, что сопровождается отсутствием активных движений в пораженной конечности;
- свисание головы вперед, что наблюдается при параличе задних мышц шеи.
При некоторых параличах нарушается функция тазовых органов, что сопровождается автоматическим рефлекторным опорожнением мочевого пузыря и недержанием кала.
Симптоматика паралича зависит и от его разновидности:
После общего осмотра назначаются лабораторные и инструментальные методы исследования. Для обнаружения признаков отравления необходим токсикологический анализ крови. Общий анализ крови позволяет выявить признаки воспаления.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Особенности вирусной инфекции нервной системы у детей в зависимости от возбудителя
а) Паралитический полиомиелит. С широким распространением вакцинации случаи полиомиелита стали крайне редкими, и повсеместное уничтожение вируса остается приоритетной задачей ВОЗ. Около 90-95% инфекций полиовируса являются субклиническими, 5% проявляются в виде легкой формы заболевания с фебрилитетом и 1-2% в основном дают симптоматику поражения ЦНС либо менингоэнцефалита, либо полиомиелита.
При полиомиелите в патологический процесс вовлекаются клетки передних рогов, двигательные и чувствительные черепные ядра продолговатого мозга, ретикулярная формация, червь мозжечка и в меньшей степени, таламус и III и V слои моторной зоны коры. Нейроны подвергаются дегенеративным изменениям, сопровождающимся вначале полиморфноядерной реакцией, которая позднее становится мононуклеарной.
Клинические проявления возникают после инкубационного периода, который длится 3-35 дней. Первоначальные симптомы включают головную боль, тошноту и лихорадку, а вслед за ними в течение 2-5 дней менингеальные симптомы раздражения и сильную боль в нижней части спины и конечностях. В серьезных случаях паралич появляется в течение первых двух дней.
Обычный спинальный полиомиелит характеризуется асимметричным вялым параличом, затрагивающим ноги, руки и/или туловище с отсутствием сухожильных рефлексов. Задержку мочи при начале заболевания демонстрируют 20-30% пациентов. Бульбарная форма редко бывает изолированной, распространяясь по меньшей мере на шейный отдел спинного мозга в 90% случаев. Могут поражаться все мышцы, иннервируемые черепными нервами. Кроме того, дыхательная недостаточность и гипертензия может быть результатом повреждения стволовой ретикулярной субстанции. Заболевание может сопровождаться энцефалитическими признаками, но они могут также вызываться и дыхательной недостаточностью из-за паралича диафрагмальных и межреберных мышц.
В анализе СМЖ обнаруживают 30-200 клеток/мм3. Изначально преобладают полиморфноядерные клетки, затем через 5-7 дней сменяющиеся лимфоцитарным плеоцитозом. Содержание белка повышается поздно, достигая максимальных значений примерно на 25 день заболевания.
По данным МРТ описано развитие отека спинного мозга с патологическим сигналом от центральной его части (Kibeetal., 1996). До начала клиники вирус может выделяться из кала и ротоглотки первые 19 дней и до трех месяцев после первых клинических проявлений (в среднем пять недель). При типировании вируса определяют один из трех типов полиовируса. Серологический диагноз ставится на основании повышения титра нейтрализующих или комплемент-связывающих антител.
Прогноз паралитического полиомиелита зависит от степени вовлечения. Восстановление поврежденных мышц часто происходит в течение года и более, но если через месяц мышцы все еще остаются парализованными, то обычно окончательно. Прогрессирующая болезнь моторных нейронов (постполиомиелитный синдром), напоминающий амиотрофический склероз, иногда наблюдается у взрослых через 20 и более лет после острого начала заболевания (Dalakas et al., 1986).
Случаи паралитического полиомиелита, связанного с живой вакциной, могут встречаться у пациентов с иммунодефицитом, получивших вакцину или контактировавших с вирусом (Nkowane et al., 1987; Sen et al., 1989; Groom et al., 1994). При этом возможны атипичные проявления. Поскольку редкие случаи полиомиелита могут также возникать у детей без иммунодефицита после живой вакцины (Dussaix et al., 1987), с уменьшением уровня заболеваемости во всем мире, в большинстве развитых стран сейчас используют убитую инъекционную полиовакцину при плановой вакцинации для предупреждения этого осложнения.
Постановка диагноза не представляет трудностей при условии, если не упускать из вида именно это заболевание. Синдром Гийена-Барре отличается от полиомиелита по характеру начала, симметричности распределения слабости и по данным ликвора. Регистрировались редкие случаи паралитического заболевания, связанного с другими вирусами (Kylleman et al., 1993). Вирус Западного Нила вызывал эпидемии заболеваний, напоминающих паралитический полиомиелит.
Случаи интоксикации химикатами или укусов насекомыми также могут имитировать сходную клиническую картину (Gear, 1984).

б) Энтеровирусы. Первоначальная классификация энтеровирусов, до геномного анализа, была основана на цитопатическом эффекте различных культивируемых клеток и инфицированных животных. Были выделены три типа полиовирусов, 24 коксаки-вируса типа А и 6 коксаки-вирусов типа В вирусов и 34 типа ЕСНО-вирусов. Последующие выделенные энтеровирусы обозначались номером, начиная от энтеровируса 68 без дальнейшего подразделения. Позднее геномный анализ последовательности частично подтвердил первоначальную культуральную классификацию.
Эти вирусы внедряются в организм хозяина через желудочно-кишечный тракт, где реплицируются и вызывают виремию, способную привести к инфекции ЦНС. В большинстве случаев отмечается слабый желудочно-кишечный вирусный продром, а в анамнезе присутствуют данные о наличии у членов семьи схожих симптомов. Большая часть случаев протекает в легкой форме с быстрым выздоровлением. Микроорганизмы можно обнаружить с помощью ПЦР или выделить из ликвора, а также из крови, кала и ротоглотки. При экспресс-диагностике ПЦР результаты можно получить через несколько часов. Инфекция встречается в любом возрасте, включая первые недели жизни (Kaplan et al., 1983).
Энтеровирусы Коксаки В1-5 и Коксаки А7, 9 и 25, ЕСНО-вирусы 4,6,9,11,14,16,18,20 и 30, так же как полиовирусы обычно вызывают асептический менингит. Острый эпидемический конъюнктивит, связанный с энтеровирусом 70, может осложняться менингитом, параличом черепных нервов или поражением конечностей, изолированно или совместно. Характерны сильные боли и фасцикуляции (Wadia et al., 1983; Chopra et al., 1986).
Менингит, вызванный вирусом Коксаки группы А, может сопутствовать или предшествовать герпангине, респираторным инфекциям и паротиту. Среди заболеваний группы В могут встречаться плевродиния (болезнь Борнхольма или эпидемическая миалгия) или диарея. Осложнением менингита могут быть миокардит и энцефалит, особенно у детей раннего возраста (Kaplan et al., 1983). Инфекции ЕСНО-вирусов могут вызывать как спорадические случаи, так и эпидемии. Пятнистопапулезная сыпь особенно характерна при инфекциях вирусов ECHO 4, 9 и 16. Иногда сыпь появляется при Коксаки А9 и А23. Также может быть петехиальной.
В литературе сообщалось о последствиях энтеровирусных менингитов (Kaplan et al., 1983). Вероятней всего, они являются результатом развития энцефалита, сопутствующего менингиту. Они особенно характерны при неонатальном энтеровирусном менингите, который также представлен лихорадкой, плохим аппетитом, диареей, гепатомегалией и сыпью (Huang et al., 2003).
Энтеровирусы также могут быть причиной других проявлений заболеваний ЦНС, включая паралич нижних двигательных нейронов (вирус Коксаки А4, 7, 9, В5, вирус ECHO 70); синдром Гийена-Барре и поперечный миелит (Коксаки А9, В1, 4, ECHO 6, 70); церебральную атаксию (Коксаки А9, 4, 7, В3, 4, ECHO 6, 9, 71); периферический неврит (ECHO 9). Энтеровирусы обычно вызывают самопроходящие заболевания, которые, хотя и связаны с заболеваемостью, редко заканчиваются смертельным исходом. Однако в некоторых более уязвимых группах пациентов (например, у младенцев или детей с иммунодефицитом) энтеровирусы могут вызывать угрожающие жизни инфекции.
Плеконарил — антивирусный препарат, который встраивается в капсид пикорнавирусов, включая энтеровирусы, предупреждая прикрепление вирусов к клеточным рецепторам и высвобождение вирусной РНК в клетку. Клинические испытания плеконарила показали некоторую эффективность у пациентов с тяжелой формой заболевания (Rotbart и Webster, 2001); к сожалению, этот лекарственный препарат не выпускался в промышленном масштабе.
в) Вирус эпидемического паротита. Среди неиммунизированного населения свинка выявляется как наиболее частая причина вирусного асептического менингита. Классическая клиническая картина лептоменингита встречается у 0,5-2% пациентов, больных эпидемическим паротитом. Однако плеоцитоз наблюдался только у 56% таких пациентов с паротитом (Russell и Donald, 1958). Паротит в 30-40% случаев может отсутствовать (Levitt et al, 1970), и в таких случаях диагноз можно получить при ПЦР амплификации вирусного генома в СМЖ или серологическими методами. Симптомы менингита появляются с 8 по 20 день после начала паротита. Часто сопровождаются выраженной лихорадкой.
В ликворе наблюдается лимфоцитарный плеоцитоз, нередко значительный, с сотнями клеток/мм 3 . Содержание глюкозы может быть снижено (Wilfert, 1969). Хотя заболевание обычно протекает в легкой форме, плеоцитоз может присутствовать на протяжении нескольких месяцев с длительным сохранением специфических интратекальных олигоклональных IgG (Vandvik et al., 1978a).

г) Вирусы герпеса. Некоторые представители семейства герпесвирусов могут вызывать лимфоцитарный менингит.
• Вирус простого герпеса. ВПГ 2 типа (Nahmias et al., 1982) чаще отвечающий за болезнь, чем 1 тип, который главным образом вызывает энцефалит. Менингит, вызванный ВПГ-2, может быть проявлением первичной инфекции у сексуально активных подростков. Иногда, легкие случаи ВПГ-1 инфекции могут проявляться только в виде раздражения мозговых оболочек (Whitley et al„ 1982а) с выздоровлением пациентов через 7-14 дней.
• Вирус опоясывающего герпеса. Вирус может вызывать асептический менингит, а также более сложное поражение ЦНС, описанное в следующем разделе. Могут встречаться пре-эруптивные неврологические проявления (Tsolia et al., 1995). В этом исследовании, у двоих детей с энцефалитом сопутствующей патологией была атаксия. Другие очаговые неврологические дефициты, кроме атаксии, развились у семи детей: у троих паралич лицевого нерва, у одного сопровождающая гемиплегия, двое имели парез верхних конечностей, у одного был радикулит, перешедший в парез ноги, и у одного ребенка паралич отводящего нерва. У двоих детей наблюдался изолированный менингит. В этой группе только двое детей переживали длительные последствия: у одного наблюдался стойкий паралич руки, у другого паралич отводящего нерва.
Другие синдромы ЦНС, связанные с вирусом ветряной оспы, включают вирусный миозит, радикулопатию, миелит и отсроченный гемипарез после ветряной оспы (Kamholz и Tremblay, 1985; Ichiyama et al., 1990; Rosenfeld et al., 1993; Herrold и Hahn, 1994; Gilden, 2004; Mariotti et al., 2006). Сообщалось также о поражении базальных ганглиев (Silverstein и Brunberg, 1995) и латеральном медуллярном синдроме (Kovacs et al., 1993). Сосудистые явления ишемического характера, часто поражающие крупные мозговые артерии, нередко отмечаются после ветряной оспы (Amlie-Lefond et al., 1995; Tsolia et al., 1995; Lanthier et al., 2005; Losurdo et al., 2006).
Острые артериопатии, приводящие к ишемическим инсультам, могут быть причиной четверти случаев тромбоза мозговых артерий в детском возрасте; в исследовании Guillot et al. (2005) наиболее вероятным этиологическим фактором в 60% случаев определена ветряная оспа (Guillot et al., 2005). Вероятно, при постинфекционных состояниях действует несколько механизмов, а в некоторых случаях важны воспалительные процессы в стенке артерий, так же как повышенная секреция прокоагулянтов, таких как антикардиолипин (Kurugol et al., 2000, 2001).
Кроме того, иммунная реакция хозяина на вирус ветряной оспы включает образование антител, способные на перекрестную реакцию и инактивацию белка S, важного фактора антикоагуляции хозяина. Это может привести к состоянию гиперкоагуляции и развитию молниеносной пурпуры, также как к ишемическому инсульту после Varicella zoster (Josephson et al., 2001).
• Вирус Эпштейна-Барр (ЭБВ). Большинство инфекций ЭБВ в раннем периоде жизни протекает бессимптомно, неврологические осложнения редки; они могут включать в себя асептический менингит, проявления энцефалита и некоторые другие осложнения ЦНС (Hung et al., 2000). Менингит может предвещать некоторые другие неврологические осложнения, такие как инфекционный полиневрит (синдром Гийена-Барре), энцефаломиелит или поражение черепных нервов (Hausler et al., 2002) или паркинсонизм (Hsieh et al., 2002). Примерно у трети пациентов с инфекционным мононуклеозом при исследовании СМЖ обнаруживают >5 клеток/мм 3 и такие показатели могут сохраняться месяцами, часто после полного клинического выздоровления (Pejme, 1964). Полное выздоровление может откладываться на несколько недель и месяцев.
• Вирус герпеса человека (ВГЧ) 6 и 7. ВГЧ-6 инфекция является причиной внезапной экзантемы (exanthema subitum), и в редких случаях вызывает менингоэнцефалит у здоровых прежде детей (Asano et al., 1992; Jones et al., 1994). Хотя большинство первичных инфекций ВПГ-6 (и тесно связанного ВПГ-7) протекают бессимптомно, оба вируса причастны к более 30% фебрильных судорог, встречающихся в первые два года жизни (Hall et al., 1994; Barone et al., 1995; Ward, 2005).
г) Аденовирусные инфекции нервной системы. Выделено множество типов аденовирусов; большинство вызывает легкие инфекции желудочно-кишечного тракта, дыхательной системы или почек и только в редких случаях они являются причиной синдромов поражения ЦНС. Проявления включают асептический менингит, миелит, подострый очаговый энцефалит, Рейе-подобный синдром и преходящую энцефалопатию (Linssen et al., 1991; Straussberg et al., 2001).
д) Парвовирус В19. Большинство инфекций парвовируса В19 имеют бессимптомное течение, но симптоматическая инфекция у детей обычно проявляется в виде лихорадки и сыпи, а у взрослых могут быть артропатии. Также сообщалось о редких случаях ЦНС инфекции с признаками менингоэнцефалита и определением вирусной ДНК в ликворе (Barah et al., 2001, 2003). Иммунный ответ хозяина к парво В19 в ЦНС считается предположительной причиной воспаления с подтверждением повышенного уровня цитокинов в ликворе, так же как специфического HLA-генома хозяина (Kerr et al., 2002).
е) Вирус лимфоцитарного хориоменингита (вирус ЛХМ). Вирус ЛХМ является человеческим зоонозом, вызываемым распространяемым грызунами ареновирусом, поражающим полевых мышей. Вирус передается человеку после контакта с выделениями зараженных мышей, морских свинок и хомяков. Внутриутробная инфекция у человека может привести к поражению плода (Barton и Mets, 2001; Barton et al., 2002), тогда как постнатальное инфицирование обычно протекает бессимптомно или как простудное заболевание, но может встречаться и синдром вовлечения ЦНС (Barton и Hyndman, 2000).
ж) Другие и неопределенные вирусы. Они, вероятно, являются причиной многих случаев заболеваний — в действительности большинства, в которых не могут быть выделены патогенные микроорганизмы. Понятно, что число возможных вирусных агентов велико, и поскольку заболевание обычно протекает в легкой форме, сложные исследования не проводятся.
Вирусные инфекции нервной системы у детей при ослабленном иммунитете
Оппортунистические инфекции ЦНС могут возникать у иммуноослабленных детей, и спектр инфекций зависит от особенностей нарушения клеточного иммунитета, врожденных или ятрогенных (Cunha, 2001). Все большее число детей появляется с ятрогенной этиологией иммунной недостаточности различной степени выраженности — от тяжелого иммунного подавления при трансплантации органов до хронического применения стероидов при воспалительных состояниях.
Инфицирование оппортунистическими возбудителями, обычно непатогенными для человеческого организма, может быть необычным нарушением, вторичным при обычных вирусных патогенах. В целом большему риску подвержены дети с Т-клеточной лимфоцитарной недостаточностью, у которых может встречаться широкий спектр вирусных, бактериальных, грибковых и протозойных инфекций. Дети с В-клеточным дефицитом в меньшей степени повержены риску инфицирования ЦНС, однако возможен общеизвестный синдром хронической энтеровирусной инфекции.
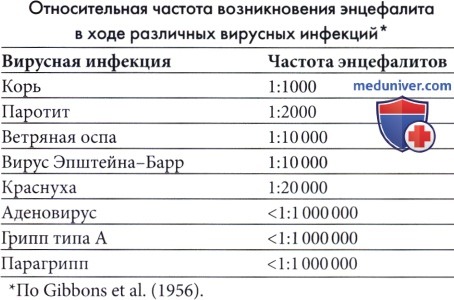
а) Замедленный тип острого коревого энцефалита при ослабленном иммунитете. Острый замедленный коревой энцефалит наблюдался в основном у пациентов с ослабленным иммунитетом (Murphy и Yunis, 1976), хотя изредка он встречается у детей с явно нормальными иммунными механизмами. В отличие от обычного постинфекционного энцефаломиелита, вирус кори в большом количестве выявляется в тканях мозга, а нуклеокапсиды видны при электронной микроскопии в ядрах глии и нейронах. Воспалительная реакция выражена в различной степени, но чаще слабая (Lacroix et al, 1995). Заболевание развивается через 2-6 месяцев после кори или контакта со случаями кори. Наиболее явным симптомом часто являются эпилептические припадки и во многих случаях первыми проявлениями является epilepsia partialis continua (Aicardi et al., 1977; Luna et al., 1990; Barthez Carpentier et al., 1992).
Быстро развивается прогрессирующее ухудшение с оглушенностью и комой и характерными очаговыми симптомами, особенно гемиплегией.
Продолжают появляться новые неврологические симптомы разной продолжительности. У некоторых пациентов отмечается ретинопатия (Haltia et al., 1977). Диагностика может быть затруднена, в связи с нормальными или слегка измененными показателями ликвора. В большинстве случаев отмечают интратекальный синтез специфических противокоревых антител и высокий титр антител против вируса кори в плазме крови и СМЖ. У детей с наиболее тяжелым подавлением иммунитета выработка антител, однако, может быть ослаблена.
б) Герпесвирусные инфекции человека. Все герпесвирусные инфекции могут стать причиной тяжелого заболевания у иммунодефицитных детей с ослабленной функцией Т-лимфоцитов, включая реципиентов органов при трансплантации, ВИЧ-инфицированных детей и детей с врожденным иммунодефицитом. Заболевание может возникать в результате первичной инфекции у неиммуннизированных детей или как результат реактивации латентной инфекции в период иммунной недостаточности. Болезнь может ограничиваться одним органом или распространяться, вовлекая многие органы с высоким уровнем вирусемии в плазме. Несмотря на доступность противовирусной терапии, полное выздоровление часто зависит от улучшения функции иммунной системы.
Нарушающие зрение вирусные ретиниты вызываются в первую очередь представителями семейства вирусов герпеса; в клинические синдромы входят острый ретинальный некроз (ОРН) (Bonfioli и Eller, 2005), прогрессирующий наружный ретинальный некроз (ПНРН) (Purdy et al., 2003), мультифокальный хориоидит, серпигинозный хориоидит и другие вирусные ретинопатии (ЦМВ ретинит, смотри ниже). При активном иммунитете наиболее распространенным считается ВПГ ретинит, тогда как вирус ветряной оспы в равной степени поражает пациентов с нормальным и ослабленным иммунитетом.
В связи с плохим проникновением лекарственных форм в ткани глаза при системной терапии из-за ограниченного кровоснабжения, при лечении тяжелых заболеваний необходимы как системные назначения, так и прямое внутриглазное введение противовирусных препаратов (Scott et al., 2002).
• Цитомегаловирус. При тяжелой иммунной депрессии может развиваться диссеминированная форма цитомегаловирусной инфекции. Обычно наблюдается высокий уровень вирусемии в крови. Инфекция может поражать головной мозг, сетчатку глаза, легкие, костный мозг, печень и кишечник. При лечении могут быть эффективны ганцикловир, фоскарнет или цидофовир; однако из-за их токсичности требуется тщательный метаболический контроль. Ганцикловир относится к средствам первого выбора после фоскарнета и цидофовира; для более долгосрочной поддерживающей иммуносупрессивной терапии подходит пероральный прием валганцикловира (Kimberlin, 2002; Griffiths, 2004).
ЦМВ ретинит хорошо распознается при прогрессировании ВИЧ-инфекции; при ее наличии у новорожденных, в отличие от взрослых или более старших детей, в первую очередь поражается макула, а не периферическая сетчатка, тем самым непосредственно угрожая центральному зрению (Wren et al., 2004). Другие проявления ЦМВ инфекции в центральной нервной системе у детей с иммунодефицитом включают очаговый или генерализованный энцефалит, паралич черепных нервов, поперечный миелит, радикулит и синдром Гийена-Барре. Успех терапии зависит от ответа вовлеченного органа, также как от уровня вирусемии. У ВИЧ-инфицированных пациентов цитомегаловирусное заболевание ЦНС, включая ретинит, может принять остро симптоматическое течение, в момент начала противовирусной терапии, как проявление синдрома восстановления воспалительного иммунитета (IRIS). IRIS наиболее характерен для пациентов, которые начали лечение в стадии прогрессирующей болезни и с очень низким уровнем CD4, что требует тщательного наблюдения при лечении ЦМВ, ВИЧ и иммунной перестройке для уменьшения симптомов (Griffiths, 2004).
• Вирус простого герпеса. Тяжелая инфекция ВПГ может иметь место у детей с ослабленным иммунитетом. Чаще всего поражаются ротовая полость, кожа, легкие и кишечник, в то время специфическое поражение ЦНС редко. Высокие дозы внутривенного ацикловира должны иметь эффект, хотя возможно развитие резистентности при повторной экспозиции, особенно при низких оральных дозах. ПЦР-исследование ликвора на ВПГ имеет важное значение в постановке диагноза и контроле лечения у иммуносупрессивных пациентов (Cinque et al., 1998).
• Вирус герпеса человека 6 и 7 типов. Реактивация ВГЧ-6 встречается приблизительно в 50% всех пересадок костного мозга и у 20-30% реципиентов паренхиматозных органов через 2-3 недели после процедуры. Клинические симптомы заключаются в лихорадке, кожной сыпи, пневмонии, подавлении костного мозга, энцефалите и отторжении трансплантата (Yoshikawa, 2003). Развитие лимбического энцефалита связано с высокой вирусной нагрузкой в крови ДНК ВГЧ-6 после трансплантации (Ogata et al., 2006). ВГЧ-7 виремия после пересадки стволовых клеток также была ассоциирована с энцефалитом (Chan et al., 2004). Эффект может быть от применения ганцикловира.
• Вирус Эпштейна-Барр. Инфекция ВЭБ способна вызывать тяжелые, часто заканчивающиеся смертью заболевания в некоторых семьях с потенциально фатальной чувствительностью к ВЭБ, передаваемой по наследству как Х-сцепленный ген. Это заболевание, известное как Х-сцепленный лимфопролиферативный синдром (ХЛС) (Grierson и Purtilo, 1987), может принимать форму смертельного инфекционного мононуклеоза, злокачественной лимфомы, приобретенной гипо- и агаммаглобулинемии и вирус-ассоциированного гемофагоцитарного синдрома (Tiab et al., 2000, Gilmour и Gaspar, 2003). Поврежденный ген XLP был определен и обозначен SH2D1A; он кодирует адаптерный белок SAP (белок сигнальной лимфоцитарной молекулосвязанной активации — SLAM-ассоциированный); измерение этого белка может быть использовано в диагностике состояния (Gilmour et al., 2000).
С XLP связан высокий уровень заболеваемости, и во всех случаях исход неблагоприятный. В настоящее время аллогенная трансплантация стволовых клеток остается единственным лечебным мероприятием (Lankester et al., 2005).
Похожий синдром моно- и поликлональной лимфоцитарной пролиферации, обусловленный ВЭБ, известный как посттрансплантационное лимфопролиферативное заболевание (ПТЛЗ), может развиваться при ослабленном иммунитете, особенно у реципиентов пересаженных органов (Randhawa et al., 1992). ПТЛЗ может проявляться полиорганными поражениями, нечасто вовлекая ЦНС. Поражение мозга у реципиентов с ПТЛЗ дает неблагоприятный прогноз; однако изолированное вовлечение ЦНС имеет лучший прогноз, чем одновременное поражение ЦНС и внечерепных органов (Buell et al., 2005). Исследование детей после трансплантации печени показало, что мониторинг вирусной нагрузки ВЭБ при раннем вмешательстве может уменьшить количество случаев ПТЛЗ (Lee et al., 2005).
Комбинированное лечение с иммунной модуляцией, противовирусными средствами и анти-В-клеточными моноклональными антителами ритуксимаба обеспечивает определенный эффект (Nozzoli et al., 2006).
У пациентов с более прогрессирующей ВИЧ-иммуносупрессией ВЭБ может привести к развитию лимфомы. Это может быть изолированная лимфома ЦНС или же поражение ЦНС при более распространенном заболевании (Nadal et al., 1994). В настоящее время проводится разработка более эффективного лечения вызываемой ВЭБ лимфомы у пациентов с ВИЧ, включая противовирусную терапию, химиотерапию и иммуномодулирующее лечение.
в) Полиомавирусная инфекция человека. JC-вирус — это человеческий нейротропный полиомавирус, который вызывает прогрессивную мультифокальную лейкоэнцефалопатию (ПМЛ), смертельное демиелинизирующее заболевание у иммунодефицитных пациентов. Сообщалось о случаях у детей с ВИЧ, после лечения злокачественных новообразований и у детей с врожденной иммунной недостаточностью (Redfearn et al., 1993; Bezrodnik et al., 1998; Angelini et al., 2001; Nuttall et al., 2004; Demir et al., 2005). Заболевание может начинаться медленно как расстройство с когнитивным нарушением или быстро прогрессировать с припадками, гемипарезом, нарушениями двигательных функций или с утратой зрения. На МРТ черепа могут быть распространенные повреждения белого и серого вещества. Исход без лечения и восстановления иммунитета обычно смертельный через несколько месяцев. Пациенты с прогрессирующей формой ВИЧ могут развить острую симптоматику ПМЛ вскоре после начала противовирусной терапии, что рассматривается как еще одно проявление синдрома воспалительного восстановления иммунитета (Nuttall et al., 2004).
г) Полиовирусная инфекция (дикий и поствакцинальный тип). Полиовирус у пациентов с ослабленным иммунитетом может вызвать развитие типичной картины паралитического полиомиелита. Имеются описания случаев при Х-сцепленной гипогаммаглобулинемии (Wright et al., 1977) и нарушении Т-клеточного звена иммунитета. В качестве исключения может иметь место более диффузное заболевание с вовлечением головного мозга и очагами кальцификации в зрительном бугре после вакцинации живым аттенуированным вирусом (Davis et al., 1977).
д) Хроническая энтеровирусная инфекция у детей с Х-сцепленной гипогаммаглобулинемией. Дети с Х-сцепленной гипогаммаглобулинемией (болезнью Брутона) часто страдают от вирусных инфекций ЦНС в сочетании с бактериальными осложнениями (гнойным менингитом). Наиболее распространенными возбудителями этих инфекций являются энтеровирусы (Cooper et al., 1983). Характерным клиническим проявлением является хронический лимфоцитарный менингит с различными признаками поражения мозга, такими как нарушение сознания и очаговые припадки или неврологический дефицит. Другие симптомы включают в себя прогрессирующую миелопатию, миелопатию, прогрессирующую до энцефалопатии, простую энцефалопатию, ретинопатию, нейросенсорную тугоухость и дерматомиозит (Rudge et al., 1996). Течение хроническое, нередко с летальным исходом. Диагностика по результатам ПЦР-исследования ликвора или же по биопсии ткани в некоторых случаях, а для контроля эффективности можно использовать количественную оценку ПЦР (Quartier et al., 2000).
Интратекальное и внутрижелудочковое введение гаммаглобулинов может помочь уменьшить симптомы, но не выводит инфекцию (Erlendsson et al., 1985; Johnson et al., 1985).
Читайте также:

