Вирусы могут быть дефектными
Обновлено: 19.04.2024
ПЕРСИСТЕНЦИЯ ВИРУСОВ (лат. persistere оставаться, упорствовать; вирусы) — длительное сохранение вируса в организме хозяина или в клеточной культуре.
При острой инф. болезни время пребывания вируса в организме определяется длительностью инкубационного периода и периода неосложненного клин, течения болезни. Сохранение вируса дольше этого срока представляет собой П. в.; в ряде случаев П. в. длится месяцами и годами, иногда всю жизнь.
В зависимости от наличия или отсутствия внешних проявлений феномена персистенции патогенных или потенциально патогенных вирусов различают: латентные вирусные инфекции (см.) с периодическими обострениями (или без них), в промежутках между ними вирус не обнаруживается; хронические вирусные инфекции с постоянно выделяющимся вирусом, более или менее выраженными признаками заболевания организма (или поражения клеток); медленные вирусные инфекции (см.), характеризующиеся длительным, иногда многолетним инкубационным периодом с последующим неуклонным развитием заболевания, приводящего к гибели организма. Ряд исследователей включает в эту классификацию группу персистентных вирусных инфекций, протекающих бессимптомно, не сопровождающихся постоянным выделением в окружающую среду вируса. П. в., протекающую без симптомов или с мало выраженными признаками поражения, называют также вирусоносительством (см. Носительство возбудителей инфекции). В 1963 г. Смит (W. Smith) выделил в качестве особой формы П. в. вирусный симбиоз — ассоциацию непатогенного вируса с клетками хозяина, представляющую взаимную выгоду для того и другого; существование этой формы П. в. признается не всеми. Границы между разными проявлениями феномена П. в. в значительной мере условны.
Определение П. в. и исследование механизмов персистенции являются основой для изучения этиологии и патогенеза ряда вирусных заболеваний, что позволяет разрабатывать эффективные меры их профилактики и лечения. П. в: может играть роль в формировании невосприимчивости организма к вирусной инфекции за счет интерференции вирусов (см.), продукции интерферона (см.) и антител (см.), повышения неспецифической резистентности организма (активизации фагоцитоза, специфической сенсибилизации организма). Особую эпидемиол, опасность представляют персистентные вирусные инфекции, при которых в окружающую среду выделяется вирус. В то же время П. в. имеет большое значение в экологии возбудителей, т. к. способствует сохранению вируса как вида.
П. в. зависит от степени резистентности организма (см.) или культивируемых клеток: чем менее восприимчив организм к данному вирусу, тем чаще наблюдаются скрытые формы инфекции. Относительная устойчивость организма (или клеток) к некоторым вирусам может быть обусловлена генетическими и иммунол, факторами. Важную роль при этом играют иммунол, толерантность, иммунодепрессивное действие вирусов, образование иммунных комплексов, в которых антитела нейтрализуют активность вируса, наличие иммунодефицитов, подавление выработки интерферона и исчезновение с поверхности зараженных клеток вирусных детерминант под влиянием антител. Нередко П. в. способствует происходящая в ходе вирусной инфекции селекция малочувствительных клеток из общей клеточной популяции. В процессе П. в. свойства вирусной популяции также могут изменяться: возможно снижение степени вирулентности, утрата гемагглютинирующей активности, изменение морфологии, а иногда и антигенной структуры вирионов.
В результате изменения реактивности клеток и свойств вирусов клин, проявления П. в. могут существенно отличаться от симптомов острой инфекции, вызванной тем же вирусом.
Изучение механизмов П. в. на уровне макроорганизма связано с большими трудностями, поэтому основные сведения получены на модельных системах в культурах клеток человека и животных. В зависимости от чувствительности клеток, от свойств вирусов и от условий постановки опытов наблюдаются различные реакции клеток на заражение вирусами: от острой инфекции с тотальной деструкцией клеток до П. в. с мало выраженным цитопатическим эффектом или его отсутствием с резкой активизацией клеточного деления — цитопролиферативным эффектом (см. Клетка, вирусная цитопатология).
П. в.— интеграция вирусного генома с клеточным в единую генетическую структуру. Этот феномен, являющийся результатом рекомбинационного механизма, был впервые обнаружен при изучении взаимодей-вия бактерий с умеренными фагами. Было установлено присутствие в клетках животных ряда ДНК-содержащих онкогенных вирусов, а также некоторых аденовирусов и вируса обычного герпеса. РНК-содержащие Онкогенные вирусы животных с помощью фермента — обратной транскриптазы (ревертазы) образуют ДНК-транскрипты, интегрирующие с клеточным геномом. В. М. Жданов предположил, что одним из возможных механизмов длительной персистенции в клетках неонкогенных РНК-содержащих вирусов является образование ДНК-транскриптов с помощью ревертазы онкогенного вируса, латентно пе репетирующего в той же клетке.
Как правило, при П. в. в клеточных культурах вирус присутствует лишь в отдельных клетках. Периодическая гибель инфицированных клеток и размножение клеток, сохранивших жизнеспособность, обусловливают смену циклов деструкции хронически инфицированных культур циклами репопуляции, т. е. восстановления клеточного слоя. Количество инфицированных клеток при П. в. в популяции может варьировать в зависимости от интенсивности продуцирования интерферона в клеточной популяции, а также от способности вируса в данной культуре передаваться от клетки к клетке, минуя выход в культуральную среду, от добавления в среду специфических антител, интерферона или ингибиторов. В целом для П. в. в клеточных культурах в отличие от острой инфекции, как правило, характерна пониженная продукция вируса.
Установление П. в. часто представляет значительные трудности, особенно при латентной инфекции. Кроме того, выявление П. в. затрудняется в связи с своеобразием клин, проявлений П. в., особенно при медленных вирусных инфекциях, изменением биол, свойств вируса в процессе персистенции, а также маскировкой вируса специфическими антителами.
Важным методом индикации П. в. служит электронная микроскопия (см.), позволяющая обнаружить в части клеток не только стандартные вирионы, но и ряд субвирусных структур. Косвенные указания на П. в. могут быть получены также с помощью цитологических, цитогенетических и цитохимических методов исследования.
Для выявления антигенов персистирующих вирусов применяют метод флюоресцирующих антител (см. Иммунофлюоресценция) и иммуноэнзимный метод, основанный на метке антител или антигенов пероксидазой, локализацию которой в клетке определяют цитохимически. Присутствие в клетке вирусоспецифических последовательностей нуклеотидов при интеграционном механизме П. в. обнаруживают методом молекулярной гибридизации очищенной клеточной ДНК с нуклеиновой к-той вируса. Кроме того, с целью индикации П. в. используют способность персистирующих вирусов интерферировать с индикаторными вирусами, феномен длительного сохранения IgM-антител в сыворотке крови при П. в. и др.
Библиография: Бочаров А. Ф. и Бочаров Е. Ф. Персистенция вирусов, Новосибирск, 1979; Гаврилов В. И., Семенов Б. Ф. и Жданов Б.М. Хронические вирусные инфекции и их моделирование, М., 1974; Зуев В. А. Лабораторная диагностика латентных, хронических и медленных вирусных инфекций, М., 1979; Соловьев В. Д., Хесин Я. Е, и Быковский А. Ф. Очерки по вирусной цитопатологии, М., 1979; Тимаков В. Д. и 3уев В. А. Медленные инфекции, М., 1977; H о t-ch i n J. Persistent and slow virus infections, Basel a. o., 1971.
Дефектные интерферирующие вирусные частицы. ДИ-частицы вирусов.
При обычной цитолитической инфекции значительную часть вирусного потомства представляют неинфекционные вирусные частицы, которые утратили способность к автономной репликации из-за дефектности их генома. Повреждения в важных для репликации генах чаще всего связаны с делеционными мутациями, хотя они могут быть и точечными. ДИ-частицы содержат дефектный геном, более короткий, чем геном стандартного инфекционного вируса.
Величина утраченной части родительского генома может достигать 90%. Обладающие большим разнообразием ДИ-частицы для своей репликации нуждаются в гомологичном инфекционном вирусе-помощнике, так как размножаются в зараженных им клетках, проявляя специфическую интерференцию.
Способность к интерференции заключается в том, что дефектные интерферирующие частицы препятствуют размножению инфекционного гомологичного вируса, который для них служит вирусом-помощником. ДИ-частицы используют для своей репродукции продукты генов инфекционного вируса и тем самым специфически подавляют его репродукцию. Способность ДИ-частиц к самообогащению особенно отчетливо проявляется при серийном пассировании вируса с высокой множественностью заражения. Использование неразведенного вирусного инокулята при серийных пассажах in vivo или in vitro является лучшим методом для накопления ДИ-частиц, а применение разведенных инокулятов позволяет снизить их концентрацию до минимального уровня и повысить выход инфекционного вируса.
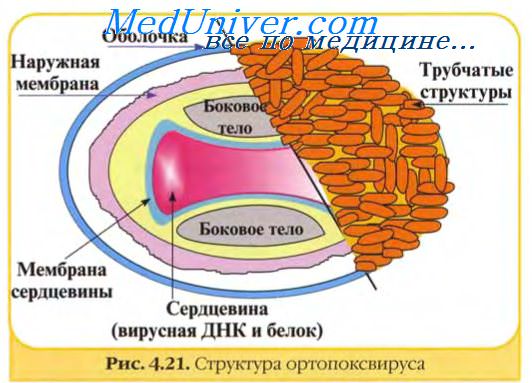
Дефектные интерферирующие частицы обнаружены практически у всех вирусов животных (кроме вирусов оспы). Следует отметить, что аутоинтерференция, обусловленная ДИ-частицами, у пикорнавирусов выражена слабо. Интерферирующая способность ДИ-частиц может зависеть от типа клеточных культур. ДИ-частицы играют определенную роль в инфекции и иммунитете. Они могут ослабить естественную вирусную инфекцию в результате интерференции с гомологичным инфекционным вирусом и влияют на установление и поддержание персистентной инфекции in vivo и in vitro. Высокое содержание ДИ-частиц в живых вакцинах может влиять на их эффективность.
В некоторых случаях большая доля неинфекционных частиц также может быть превращена в инфекционные при помощи различных обработок, что свидетельствует об их потенциальной инфекционности. Например, в препаратах пикорнавирусов концентрация вирионов может в 100—1000 раз превышать концентрацию инфекционных частиц. На 107—108 частиц вируса папилломы кролика приходится примерно одна опухолеобразующая единица.
Часто природа дефекта, делающего эти частицы неинфекционными, неизвестна. Такие частицы могут вызывать абортивную инфекцию, при которой осуществляется ряд вирусспецифических функций, но новый инфекционный вирус не образуется. Однако, даже инфекционные вирусные частицы с полным геномом могут быть дефектными для одной клеточной культуры и вызывать нормальную или абортивную инфекцию в клетках другого типа. Такие вирусы могут рассматриваться как мутанты, зависящие от хозяина. Они размножаются только в клетках, обладающих определенной генетической функцией, которой нет у самого вируса.
Вирусы-сателлиты относятся к вирусам, размножающимся за счет генных продуктов, образованных другими, часто неродственными им вирусами.
Очень часто РНК- или ДНК-геном вируса-помощника не имеет гомологии с геномом вируса-сателлита. Примером сателлитных вирусов человека могут служить аденоассоциированные вирусы (AAV), которые реплицируются только в ядрах клеток, одновременно зараженных аденовирусами. Сателлитоподобный вирус обнаружен у пчел, инфицированных вирусом хронического паралича пчел. Вирусы-сателлиты широко распространены у вирусов растений с разделенными геномами.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Персистентные инфекции в легких. Латентная инфекция в легких.
В последнее десятилетие в центре внимания исследователей различного профиля находятся сложные формы воспаления, явно отступающие от общепринятых канонов острых защитных реакций и характеризуемые своеобразными дисбалансами иммуноглобулинов и цитокинов. Эти формы воспаления характерны, прежде всего, для вирусной персистенции. Персистенция (постоянство, упорство) - понятие достаточно широкое и неоднозначное, которое, по современным представлениям, включает в себя несколько подвариантов: персистентная, латентная, хроническая и медленная инфекции, а также бессимптомное вирусоносительство.
Персистентными называют инфекции, при которых вирус либо его антигены в течение продолжительного времени обнаруживаются в организме человека. Указанное пребывание сопровождается определенными специфическими иммунологическими сдвигами. Клинические проявления заболевания могут быть выраженными, слабыми либо маскироваться симптомами общего хронического заболевания (кашель, слабость, субфебрилитет, одышка и т.д.), что нередко наблюдается у больных с хронической обструктивной болезнью легких и бронхиолите с облитерацией при нерсистенции респираторно-синцитиального вируса.
Латентная инфекция - это практически пожизненная инфекция, при которой вирус (чаще герпес) находится в наиболее тесном взаимодействии с геномом клетки и пребывает преимущественно то в дефектной (ДНК-транскрипт), то в полной инфекционной форме, что соответствует ремиссии и обострению. Активация латентной инфекции происходит, как правило, под влиянии других инфекций (чаще грипп), переохлаждения, перегрева, солнечной радиации, психических травм и т.д.
Наиболее типичным примером хронической инфекции является инфекция, вызываемая аденовирусами. Для нее характерна частая смена клинических ремиссий и обострений, но относительно благоприятный прогноз при своевременном и правильном лечении.
Медленная инфекция - имеет неизбежно летальный исход, характеризуется многомесячным или даже многолетним инкубационным периодом с последующим медленным, но неуклонным развитием симптомов заболевания (вирусы СПИД и спонгиозных энцефалитов).
Классификация вирусной персистенции весьма условна. При наличии отличительных свойств многие ее формы имеют общие черты: при всех вариантах весьма распространено формирование дефектных форм вируса, их тесное взаимодействие с геномом клетки-хозяина, чередование фаз обострения и клинической ремиссии. Вероятны переходы одной разновидности персистенция в другую, например персистентной инфекции в латентную или хроническую.
Как показали исследования, проведенные в Государственном научном центре пульмонологии (МЗ РФ), персистенция достаточно широко распространена не только при хронической, но и острой бронхолегочной патологии. При тяжелых полисегментарных пневмониях и острых абсцессах нередко отмечается замедленная элиминация респираторных вирусов и их компонентов из организма больного, что подтверждается и более длительными сроками образования специфических противовирусных иммуноглобулинов класса М и G. Персистенция сопровождается низкими показателями клеточного иммунитета (прежде всего Т-активные клетки), натуральной киллерной активности, всех видов интерферона. Иммуносупрессия, обусловленная вирусами, способствует более выраженной активации бактериальной флоры как аэробного, так и анаэробного плана.
При затяжных и рецидивирующих бронхитах, особенно с явлениями бронхоспазма, вирусы и вирусные компоненты удается обнаружить до 1,5-2 месяцев от начала заболевания. Их элиминация прямо коррелирует с исчезновением признаков воспаления бронхов.
При хронической обструктивной болезни легких и бронхиолите с явлениями облитерации у детей респираторно-синцитиальный вирус чрезвычайно часто выявляется как в период обострения, так и относительной клинической ремиссии.
У больных с ЛОР-патологией: аденоидитами, хроническими тонзиллитами и отитами основным персистирующим агентом является аденовирус. При одновременном наличии аденоидитов и шейных лимфоденитов чаще всего наблюдается ассоциация хронических аденовирусных и микоплазменных инфекций.
Особенности воспалительных реакций организма при вирусной персистенции чрезвычайно разнообразны, весьма вариабельны и зависят от громадного количества факторов, определяемых как макро-, так и микроорганизмами.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
На уровне макроорганизма основные формы вирусных поражений принципиально не отличаются от таковых, наблюдаемых при инфицировании вирусами отдельных клеток.
Продуктивная вирусная инфекция с образованием дочерних популяций и характерными клиническими проявлениями возможна лишь при наличии в заражённом организме чувствительных клеток, в которых осуществляется репродуктивный цикл возбудителя. Например, возбудитель полиомиелита может реплицировать только в клетках ЖКТ и ЦНС приматов и человека.
Абортивная инфекция развивается при проникновении возбудителя в нечувствительные клетки (например, при попадании вируса лейкоза коров в организм человека) либо в клетки, не способные обеспечить полный репродуктивный цикл (например, находящиеся в стадии клеточного цикла G0). Способность клеток к поддержанию вирусспецифических репродуктивных процессов также подавляет ИФН, противовирусный эффект которого направлен против самых различных вирусов.

Персистирующая вирусная инфекция возникает при таком взаимодействии между вирусом и заражённой клеткой, когда в последней продолжается выполнение собственных клеточных функций. Если заражённые клетки делятся, образуется инфицированный клон. Таким образом, увеличение числа заражённых клеток способствует увеличению общей популяции возбудителя в организме. Тем не менее персистирующие вирусные инфекции обычно нарушают функции клеток, что в конце концов приводит к клиническим проявлениям. У человека развитие персисти-рующих инфекций в определённой степени зависит от возраста. Например, внутриутробное заражение вирусом коревой краснухи или цитомегаловирусом (ЦМВ) приводит к ограниченному по времени персистированию возбудителя. Появление симптоматики связано с возможностью плода развивать иммунные реакции на инфекционный агент.
Латентная (скрытая) вирусная инфекция. В то время как персистирующие инфекции сопровождаются постоянным высвобождением дочерних вирусных популяций, при латентных поражениях они образуются спорадически. Репродуктивный цикл подобных возбудителей резко замедляется на поздних стадиях и активируется под влиянием различных факторов. Латентные инфекции характерны для большинства герпесвирусов, вызывающих рецидивирующие и обычно не прогрессирующие заболевания.

Дремлющая (криптогенная) вирусная инфекция — форма проявления вирусной инфекции при которой возбудитель в неактивном состоянии находится в отдельных очагах (например, в нервных ганглиях). Клинически инфекция проявляется лишь при резком ослаблении защитных сил организма. Например, вирус герпеса 3 типа, вызывающий при первичном заражении ветряную оспу, пожизненно сохраняется в организме. Рецидив заболевания в форме опоясывающего лишая возможен лишь при нарушениях иммунного статуса (наиболее часто в пожилом возрасте).
Медленные вирусная инфекции характеризуются длительным инкубационным периодом (месяцы и годы), в течение которого возбудитель размножается, вызывая всё более явные повреждения тканей. Первоначально возбудитель размножается в ограниченной группе клеток, но постепенно инфицирует всё большее их число. Заболевания заканчиваются развитием тяжёлых поражений и смертью больного. К медленным вирусным инфекциям относят подострый склерозирующий панэнцефалит, ВИЧ-инфекцию и др.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Поздняя стадия репродукции. На этом этапе происходит синтез нуклеиновых кислот вируса. Не вся вновь синтезированная вирусная ДНК упаковывается в вирионы дочерней популяции.
Поздние белки (L), большая часть которых представлена структурными полипептидами вируса, образуются при наличии вновь синтезированной ДНК вируса и ранних белков.
Поздние белки H1 и Н2 относятся к капсидным белкам. В частности, H1 является основным капсидным белкам, а белок Н2 – минорным капсидным белком с ДНК-связывающими функциями.
Большинство поздних белков, являются структурными. При их продукции ингибируется биосинтез сверхранних и ранних белков.
Когда инициируется инфекция клетки, репликация ДНК в клетке начинается, синтез ранних неструктурных белков прекращается, а синтез поздних белков еще продолжается. Поздние белки являются структурными, но иные из них также являются ферментами или белками, участвующими в сборке вирионов
В период транскрипции образуются ранние мРНК, кодирующие регуляторные (ранние) белки – альфа (сверхранние) и бета(ранние), а затем образуются поздние мРНК, кодирующие поздние (гамма) белки(структурные).
Репликация, транскрипция и этапы поздней сборки происходят в специальных участках цитоплазмы, называемых “фабриками“.
Вирусные протеазы: локализация и роль в репродукции.
Вирусная протеаза включается в работу на стадии воспроизведения вирионов. Аспартат-протеаза действует как ножницы, разрезая полоски белков на зрелые вирусные частицы, которые затем покидают инфицированную клетку-воспроизводителя ВИЧ.
Развитие ретровиорусов, в частности ВИЧ, включает расщепление вирусной протеазой образованного в процессе трансляции вирусной иРНК полипептида на функционально-активные фрагменты.
Дефектные вирусы и субвирусные частицы: общие свойства, классификация, происхождение.
Дефектные вирусы существуют как самостоятельные виды, которые репродуцируются лишь при наличии вируса-помощника (например, вирус гепатита D репродуцируется только в присутствии вируса гепатита В).
Дефектный вирус - Вирус, который самостоятельно не способен размножаться в зараженной им клетке хозяина, но может расти в присутствии другого вируса. Этот другой вирус обеспечивает необходимые молекулярные процессы, отсутствующие у дефектного вируса.
Дефектные Вирусы виды вирусов, не имеющих полной генетической информации для самовоспроизведения. Размножение их происходит в присутствии вирусов-помощников
Субвирусные частицы представляют собой промежуточные структуры при сборке вирионов.
Субвирусные частицы (subviral agents) - это частицы, значительно меньшие чем вирусы, но обладающие некоторыми их свойствами. К субвирусным частицам относят вирусы-сателлиты (satellite viruses), вироиды (viroids) и прионы (prions).
Читайте также:

