Вирусы с абортивным действием
Обновлено: 25.04.2024
Этот тип взаимодействия не завершается образованием вирусного потомства и может возникать при следующих обстоятельствах:
1) заражение чувствительных клеток дефектными вирусами или дефектными вирионами;
2) заражение стандартным вирусом генетически резистентных к нему клеток;
3) заражение стандартным вирусом чувствительных клеток в непермиссивных (нераз-решающих) условиях.
Различают дефектные вирусы, дефектные вирионы и псевдовирионы.
Дефектные вирусы существуют как самостоятельные виды, которые репродуцируются лишь при наличии вируса-помощника (например, вирус гепатита D репродуцируется только в присутствии вируса гепатита В).
Дефектные вирионы обычно лишены части генетического материала и могут накапливаться в популяции многих вирусов при множественном заражении клеток.
Псевдовирионы – это вирусы, в капсид которых заключена нуклеиновая кислота клетки хозяина, а не вирусная нуклеиновая кислота.
Абортивный типвзаимодействия чаще наблюдается при заражении нечувстви-тельных клеток стандартным вирусом. Механизм генетически обусловленной резис-тентности клеток к вирусам широко варьирует. Он может быть связан: с отсутствием на плазматической мембране специфических рецепторов для вирусов; с неспособностью данного вида клеток инициировать трансляцию вирусной иРНК; с отсутствием специ-фических протеаз или нуклеаз, необходимых для синтеза вирусных макромолекул, и т. д.
Абортивный тип взаимодействия может также возникать при изменении условий, в которых происходит репродукция вирусов: повышение температуры организма, изменение рН в очаге воспаления, введение в организм противовирусных препаратов и др. При устранении неразрешающих условий абортивный тип переходит в продуктивный тип взаимодействия вирусов с клеткой.
ІІІ. Интегративный тип взаимодействия вирусов с клеткой (вирогения).
Это взаимное сосуществование вируса и клетки в результате интеграции (встраивания) нуклеиновой кислоты вируса в хромосому клетки хозяина. При этом интегрированный геном вируса реплицируется ифункционирует как составная часть генома клетки.
Интегративный тип взаимодействия характерен для умеренных ДНК-содержащих бактериофагов, онкогенных вирусов и некоторых инфекционных вирусов как ДНК-содержащих (например, вируса гепатита В), так и РНК-содержащих (например, вируса иммунодефицита человека). Для интеграции с геномом клетки необходимо наличие кольцевой формы двунитевой ДНК-вируса. Геном ДНК-содержащих вирусов в кольцевой форме прикрепляется к клеточной ДНК в месте гомологии нуклеотидных последовательностей и встраивается в определенный участок хромосомы при участии ряда ферментов (рестриктаз, эндонуклеаз, лигаз). У РНК-содержащих вирусов процесс интеграции более сложный. Он начинается с механизма обратной транскрипции, который заключается в синтезе комплементарной нити ДНК на матрице вирусной РНК с помощью вирусоспецифического фермента обратной транскриптазы (ревертазы). После образования двунитевой ДНК и замыкания ее в кольцо происходит интеграция ДНК-транскрипта в хромосому клетки. Встроенная в хромосому клетки ДНК вируса называется провирусом, или провирусной ДНК. Провирус реплицируется в составе хромосомы и переходит в геном дочерних клеток, т.е. состояние вирогении наследуется. Однако под влиянием некоторых физических или химических факторов провирус может исключаться из хромосомы клетки и переходить в автономное состояние с развитием продуктивного типа взаимодействия с клеткой.
Дополнительная генетическая информация провируса при вирогении сообщает клетке новые свойства, что может быть причиной онкогенной трансформации клеток и развития опухолей, а также развития аутоиммунных и хронических заболеваний. Сохранение вирусной информации в виде провируса в составе клеточного генома и передача ее потомству лежит в основе персистенции (лат. persistentia — упорство, постоянство) вирусов в организме и развития латентных (скрытых) вирусных инфекций.
Культивировать вирусыможно только на биологических моделях: в организме лабораторных животных, в развивающихся куриных эмбрионах и культурах клеток.
На уровне макроорганизма основные формы вирусных поражений принципиально не отличаются от таковых, наблюдаемых при инфицировании вирусами отдельных клеток.
Продуктивная вирусная инфекция с образованием дочерних популяций и характерными клиническими проявлениями возможна лишь при наличии в заражённом организме чувствительных клеток, в которых осуществляется репродуктивный цикл возбудителя. Например, возбудитель полиомиелита может реплицировать только в клетках ЖКТ и ЦНС приматов и человека.
Абортивная инфекция развивается при проникновении возбудителя в нечувствительные клетки (например, при попадании вируса лейкоза коров в организм человека) либо в клетки, не способные обеспечить полный репродуктивный цикл (например, находящиеся в стадии клеточного цикла G0). Способность клеток к поддержанию вирусспецифических репродуктивных процессов также подавляет ИФН, противовирусный эффект которого направлен против самых различных вирусов.

Персистирующая вирусная инфекция возникает при таком взаимодействии между вирусом и заражённой клеткой, когда в последней продолжается выполнение собственных клеточных функций. Если заражённые клетки делятся, образуется инфицированный клон. Таким образом, увеличение числа заражённых клеток способствует увеличению общей популяции возбудителя в организме. Тем не менее персистирующие вирусные инфекции обычно нарушают функции клеток, что в конце концов приводит к клиническим проявлениям. У человека развитие персисти-рующих инфекций в определённой степени зависит от возраста. Например, внутриутробное заражение вирусом коревой краснухи или цитомегаловирусом (ЦМВ) приводит к ограниченному по времени персистированию возбудителя. Появление симптоматики связано с возможностью плода развивать иммунные реакции на инфекционный агент.
Латентная (скрытая) вирусная инфекция. В то время как персистирующие инфекции сопровождаются постоянным высвобождением дочерних вирусных популяций, при латентных поражениях они образуются спорадически. Репродуктивный цикл подобных возбудителей резко замедляется на поздних стадиях и активируется под влиянием различных факторов. Латентные инфекции характерны для большинства герпесвирусов, вызывающих рецидивирующие и обычно не прогрессирующие заболевания.

Дремлющая (криптогенная) вирусная инфекция — форма проявления вирусной инфекции при которой возбудитель в неактивном состоянии находится в отдельных очагах (например, в нервных ганглиях). Клинически инфекция проявляется лишь при резком ослаблении защитных сил организма. Например, вирус герпеса 3 типа, вызывающий при первичном заражении ветряную оспу, пожизненно сохраняется в организме. Рецидив заболевания в форме опоясывающего лишая возможен лишь при нарушениях иммунного статуса (наиболее часто в пожилом возрасте).
Медленные вирусная инфекции характеризуются длительным инкубационным периодом (месяцы и годы), в течение которого возбудитель размножается, вызывая всё более явные повреждения тканей. Первоначально возбудитель размножается в ограниченной группе клеток, но постепенно инфицирует всё большее их число. Заболевания заканчиваются развитием тяжёлых поражений и смертью больного. К медленным вирусным инфекциям относят подострый склерозирующий панэнцефалит, ВИЧ-инфекцию и др.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Вирусные инфекции. Особенности патогенеза вирусных инфекций. Основные этапы патогенеза вирусных инфекций.
В основе патогенеза вирусных инфекций лежит взаимодействие генома вируса с генетическим аппаратом чувствительной клетки. Исключая поражения, вызываемые вирусами, распространяющимися по нервной ткани, патогенез вирусных инфекций сопровождает вирусемия (виремия)— циркуляция возбудителя в крови. В кровоток возбудитель проникает прямым путем или из лимфатической системы. Многие вирусы (например, ВИЧ, вирусы гриппа, кори, герпеса) поражают иммунокомпетентные клетки, что чаще проявляется в нарушении функций и уменьшении числа Т-хелперов, увеличении содержания и активации Т-супрессоров или В-клеток. Некоторые возбудители образуют внутриядерные или цитоплазматические тельца включений (например, тельца Бабеша~Нёгри). имеющие диагностическое значение.
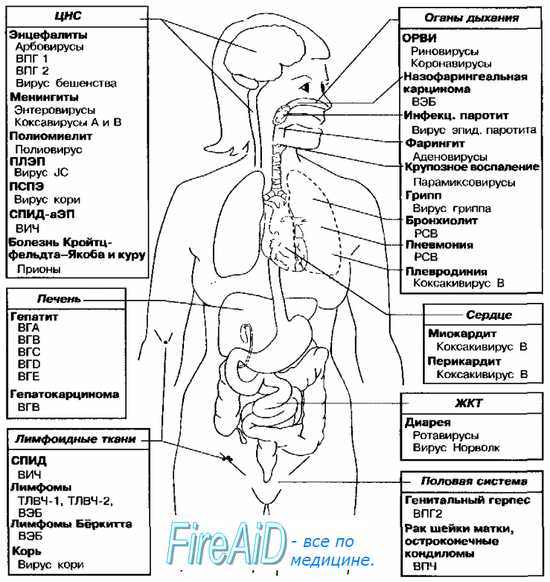
Рис. 5-9. Органы-мишени наиболее распространённых вирусных инфекций человека. ВЭБ — вирус Эпстайна-Барр, ВГА — вирус гепатита А, ВГВ — вирус гепатита В, ВГС — вирус гепатита С, BID — вирус гепатита D, ВГЕ — вирус гепатита Е, ВПЧ — вирус папилломы человека, ВПГ — вирус простого герпеса, ТЛВЧ — Т-пимфотропный вирус человека, ВИЧ — вирус иммунодефицита человека, ПЛЭП — прогрессирующая лейкоэнцефалопатия, РСВ — респираторно-синцитиальный вирус, ПСПЭ — подострый склерозирующий панэнцефалит, ОРВИ — острая респираторная вирусная инфекция, СПИД-аЭП — СПИД-ассоциированная энцефалопатия.
Основные этапы патогенеза вирусных инфекций
Проникновение вируса в организм. Основные входные ворота для возбудителей вирусных инфекции человека — дыхательные пути и ЖКТ, реже — кожные покровы. В некоторых случаях развиваются локальные поражения, но чаще в месте проникновения не возникает каких-либо проявлений или они носят стёртый характер, а возбудитель мигрирует в чувствительные ткани. Распространение возбудителя в организме может носить локальный или системный характер.
Локальные поражения вирусами типичны для возбудителей респираторных и кишечных инфекций, а также для некоторых кожных заболеваний. Продолжительность инкубационного периода большинства подобных инфекций составляет 2-3 сут. Первичную репликацию часто сопровождает вирусемия. Она обычно протекает бессимптомно или по типу продромальных явлений, но может возникать и на фоне выраженной клинической картины, не вызывая развития дополнительной симптоматики. Для подобных заболеваний характерно повторное заражение, так как циркулирующие AT не проявляют протективный эффект, а секреторный иммуноглобулин А (IgA) оказывает лишь кратковременное нейтрализующее действие на слизистой оболочке. Системные поражения. Из места проникновения возбудители попадают в кровоток, вызывая вирусемию, и постепенно фиксируются в чувствительных тканях. Первичное распространение обычно вызывает продромальные явления. Поскольку вирусемия предшествует поражению чувствительных тканей, то продолжительность инкубационного и продромального периодов подобных инфекций могут увеличиваться до 2-3 нед. Вирусемия при системных инфекциях обычно носит двухэтапный характер. Первый этап заканчивается поглощением циркулирующих вирусов клетками ретикулоэндотелиальной системы.
В дальнейшем возможно несколько вариантов:
• полная элиминация возбудителя (абортивная инфекция);
• размножение вирусов в фагоцитах с последующим выходом и развитием выраженной вторичной вирусемии, сопровождающейся появлением характерных клинических признаков заболевания (например, энцефалитов);
• некоторые вирусы (например, вирус гепатита В, пикорна- и тогавирусы) слабо поглощаются фагоцитами и могут циркулировать в крови в свободном состоянии, а возбудители колорадской клещевой лихорадки и лихорадки долины Рифт внедряются в эритроциты.
Основные органы-мишени наиболее распространённых вирусных инфекций представлены на рис. 5-9. Многие из указанных на рисунке возбудителей могут поражать, кроме названных, и другие ткани (так, полиовирусы способны вызывать поражения ЖКТ, а вирус эпидемического паротита обладает тропностью к эпителию извитых канальцев яичек).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Этот тип взаимодействия не завершается образованием вирусного потомства и может возникать при следующих обстоятельствах:

1) заражение чувствительных клеток дефектными вирусами или дефектными вирионами;
заражение стандартным вирусом генетически резистентных к нему клеток;
заражение стандартным вирусом чувствительных клеток в непермиссивных (неразрешающих) условиях.
. Различают дефектные вирусы и дефектные вирионы.
1. Дефектные вирусы существуют как самостоятельные виды, которые репродуцируются лишь при наличии вируса-помощника (например, вирус гепатита D репродуцируется только в присутствии вируса гепатита В).
2. Дефектные вирионы обычно лишены части генетического материала и могут накапливаться в популяции многих вирусов при множественном заражении клеток.
Абортивный тип взаимодействия чаще наблюдается при заражении нечувствительных клеток стандартным вирусом. Механизм генетически обусловленной резистентности клеток к вирусам широко варьирует. Он может быть связан: с отсутствием на плазматической мембране специфических рецепторов для вирусов; с неспособностью данного вида клеток инициировать трансляцию вирусной иРНК; с отсутствием специфических протеаз или нуклеаз, необходимых для синтеза вирусных макромолекул, и т. д.
Абортивный тип взаимодействия может также возникать при изменении условий, в которых происходит репродукция вирусов: повышение температуры организма, изменение рН в очаге воспаления, введение в организм противовирусных препаратов и др. При устранении неразрешающих условий абортивный тип переходит в продуктивный тип взаимодействия вирусов с клеткой.
3. Интегративный тип взаимодействия вирусов с клеткой (вирогения)
Это взаимное сосуществование вируса и клетки в результате интеграции (встраивания) нуклеиновой кислоты вируса в хромосому клетки хозяина. При этом интегрированный геном вируса реплицируется и функционирует как составная часть генома клетки.
Интегративный тип взаимодействия характерен:
для умеренных ДНК-содержащих бактериофагов,
и некоторых инфекционных вирусов как ДНК-содержащих (например, вируса гепатита В), так и РНК-содержащих (например, вируса иммунодефицита человека).
Для интеграции с геномом клетки необходимо наличие кольцевой формы двунитевой ДНК-вируса. Геном ДНК-содержащих вирусов в кольцевой форме прикрепляется к клеточной ДНК в месте гомологии нуклеотидных последовательностей и встраивается в определенный участок хромосомы при участии ряда ферментов (рестриктаз, эндонуклеаз, лигаз).
У РНК-содержащих вирусов процесс интеграции более сложный. Он начинается с механизма обратной транскрипции, который заключается в синтезе комплементарной нити ДНК на матрице вирусной РНК с помощью вирусоспецифического фермента обратной транскриптазы (ревертазы). После образования двунитевой ДНК и замыкания ее в кольцо происходит интеграция ДНК-транскрипта в хромосому клетки.
Встроенная в хромосому клетки ДНК вируса называется провирусом, или провирус -ной ДНК. Провирус реплицируется в составе хромосомы и переходит в геном дочерних клеток, т. е. состояние вирогении наследуется. Однако под влиянием некоторых физических или химических факторов провирус может исключаться из хромосомы клетки и переходить в автономное состояние с развитием продуктивного типа взаимодействия с клеткой.
Дополнительная генетическая информация провируса при вирогении сообщает клетке новые свойства, что может быть причиной онкогенной трансформации клеток и развития опухолей, а также развития аутоиммунных и хронических заболеваний. Сохранение вирусной информации в виде провируса в составе клеточного генома и передача ее потомству лежит в основе персистенции (лат. persistence — упорство, постоянство) вирусов в организме и развития латентных (скрытых) вирусных инфекций.

Культивирование вирусов
Культивирование вирусов человека и животных проводят с целью лабораторной диагностики вирусных инфекций, для изучения патогенеза и иммунитета при вирусных инфекциях, а также для получения диагностических и вакцинных препаратов.
Вирусы культивируют на трех биологических моделях:
в организме лабораторных животных,
в развивающихся эмбрионах птиц (чаще на куриных эмбрионах)
и культурах клеток (тканей).
Выращенные вирусы определяют с помощью методов:
Лабораторных животных (взрослых или новорожденных белых мышей, хомяков, кроликов, обезьян и др.) заражают исследуемым вируссодержащим материалом различными способами (подкожно, внутримышечно, интраназально, интрацеребрально и т. д.) в зависимости от тропизма вирусов. Использование животных для культивирования вирусов в диагностических целях весьма ограничено из-за видовой невосприимчивости животных ко многим вирусам человека, контаминации животных посторонними микробами, а также по экономическим и этическим соображениям.
О репродукции вирусов в организме животных судят по развитию у них видимых клинических проявлений заболевания, патоморфологическим изменениям органов и тканей, а также на основании реакции гемаг-глютинации (РГА) с суспензией из органов, содержащих вирусы. РГА основана на способности многих вирусов вызывать склеивание (агглютинацию) эритроцитов человека, птиц и млекопитающих в результате взаимодействия вирусных белков (гемагглютининов) с рецепторами эритроцитов.
Куриные эмбрионы (5-12-дневные) заражают путем введения исследуемого материала в различные полости и ткани зародыша. Таким образом можно культивировать вирусы гриппа, герпеса, натуральной оспы и др.
Достоинствами модели являются:
возможность накопления вирусов в больших количествах;
отсутствие скрытых вирусных инфекций;
доступность для любой лаборатории.
О репродукции вирусов в куриных эмбрионах свидетельствуют:
специфические поражения оболочек и тела эмбриона (оспины, кровоизлияния);
положительная РГА с вируссодержащей жидкостью, полученной из полостей зараженного зародыша.
Методику культивирования вирусов в развивающихся эмбрионах птиц используют при промышленном выращивании вирусов. Однако многие вирусы не размножаются в эмбрионах птиц; почти неограниченные возможности для культивирования вирусов появились после открытия метода культур клеток.
Культуру клеток (тканей) наиболее часто применяют для культивирования вирусов. Метод культур клеток разработан в 50-х годах XX века Дж. Эндерсом и соавт., получившими за это открытие Нобелевскую премию. Клетки, полученные из различных органов и тканей человека, животных, птиц и других биологических объектов, размножают вне организма на искусственных питательных средах в специальной лабораторной посуде. Большое распространение получили культуры клеток из эмбриональных и опухолевых (злокачественно перерожденных) тканей, обладающих, по сравнению с нормальными клетками взрослого организма, более активной способностью к росту и размножению.
При выращивании культур клеток необходимо выполнение ряда условий:
1) соблюдение правил асептики;
2) использование лабораторной посуды из нейтрального стекла (пробирки, флаконы, матрасы) или специальных реакторов для получения биотехнологической продукции;
3) использование сложных по составу питательных сред (среда 199, Игла), содержащих минеральные соли, аминокислоты, витамины, глюкозу, сыворотку крови животных или человека, буферные растворы для поддержания стабильного рН;
4) добавление антибиотиков к питательной среде для подавления роста посторонних микробов:
5) соблюдение оптимальной температуры (36— 38,5 °С) роста клеток.
В зависимости от техники приготовления различают
органные культуры клеток:
1. Однослойные культуры клеток — клетки способны прикрепляться и размножаться на поверхности химически нейтрального стекла лабораторной посуды в виде монослоя. Они получили наибольшее применение в вирусологии.
2. Суспензионные культуры клеток — клетки размножаются во всем объеме питательной среды при постоянном ее перемешивании с помощью магнитной мешалки или во вращающемся барабане. Их используют для получения большого количества клеток, например, при промышленном получении вирусных вакцин.
3.Органные культуры — цельные кусочки органов и тканей, сохраняющие исходную структуру вне организма.
Культуры клеток в процессе их культивирования способны проходить десятки генераций.
По числу жизнеспособных генераций культуры клеток подразделяют на: 1) первичные, или первично-трипсинизированные;
2) перевиваемые, или стабильные;
3) полуперевиваемые.
Первичные культуры способны размножаться только в первых генерациях, т. е. выдерживают не более 5—10 пассажей после выделения из тканей. В основе получения первичных культур лежит обработка кусочков тканей (эмбриональных, опухолевых или нормальных) протеолитическими ферментами, например трипсином, который разрушает межклеточные связи в тканях и органах с образованием изолированных клеток.
Перевиваемые, или стабильные, культуры клеток способны размножаться в лабораторных условиях неопределенно длительный срок (десятки лет), т. е. выдерживают многочисленные пассажи. Их получают преимущественно из опухолевых или эмбриональных тканей, обладающих большой потенцией роста. Перевиваемые культуры клеток имеют преимущества перед первичными культурами. К ним относятся: продолжительность их культивирования, высокая скорость размножения опухолевых и эмбриональных клеток, меньшая трудоемкость, способность культур сохранять свои свойства в замороженном состоянии в течение многих лет, возможность использования международных линий культур во многих лабораториях мира. Однако злокачественный характер клеток и соматические мутации, претерпеваемые нормальными клетками в гпоцессе многочисленных генераций, ограничивают использование этого вида культур, в частности невозможно их применение в производстве вирусных вакцин.
Полуперевиваемые культуры клеток имеют ограниченную продолжительность жизни и выдерживают 40—50 пассажей. Их обычно получают из диплоидных клеток эмбриона человека. В процессе пассажей эти куяьтуры сохраняют диплоидный набор хромосом, характерный для соматических клеток исходной ткани, и не претерпевают злокачественной тфодоЗдормавдод. Лзггстал> те>луперев\тааемые культуры клеток могут быть использованы как в диагностике, так и в производстве вакцин.
Внедрение в вирусологию метода культур клеток позволило выделить и идентифицировать многочисленные ранее неизвестные вирусы, так как почти к каждому вирусу можно подобрать соответствующие чувствительные клетки, в которых он способен репродуцироваться. Метод дал возможность изучать взаимодействие вирусов с клеткой на молекулярном уровне, получать высококачественные вакцинные и диагностические препараты, проводить вирусологические исследования в стандартных условиях.
О репродукции вирусов в культуре клеток, зараженных вируссодержащим материалом, можно судить на основании следующих феноменов:
цитопатогенного действия (ЦПД) вирусов, или цитопатического эффекта, образования внутриклеточных включений;
реакций гемадсорбции и гемагглютинации;
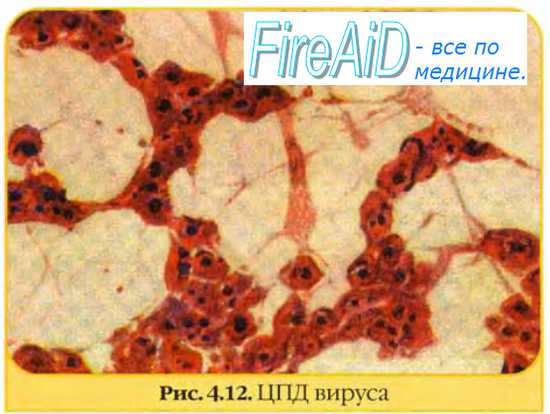
1. ЦПД — патологические изменения морфологии клеток, вплоть до их гибели, возникающие в результате репродукции вирусов, и наблюдаемые под микроскопом. В зависимости от особенностей репродуцирующихся вирусов ЦПД может отличаться. В одних случаях быстро вакуолизируется цитоплазма, разрушаются митохондрии, округляются и гибнут клетки, а в других — формируются гигантские многоядерные клетки (так называемые симпласты) или наблюдается явление клеточной пролиферации, которое в итоге заканчивается деструкцией клеток. Таким образом, характер ЦПД позволяет использовать этот феномен не только для индикации вирусов, но и для их ориентировочной идентификации в культуре клеток.
Некоторые вирусы можно обнаружить и идентифицировать по внутриклеточным включениям, которые образуются в ядре или цитоплазме зараженных клеток. Часто включения представляют собой скопления вирусных частиц или отдельных компонентов вирусов, иногда могут содержать клеточный материал. Выявляют включения с помощью светового или люминесцентного микроскопа после окрашивания зараженных клеток соответственно анилиновыми красителями или флюорохромами. Включения могут отличаться по величине (от 0,2 до 25 мкм), форме (округлые или неправильные) и численности (одиночные и множественные). Характерные цитоплазматические включения формируются в клетках, инфицированных вирусом натуральной оспы (тельца Гварниери), бешенства (тельца Бабеша—Негри), а внутриядерные включения — при заражении аденовирусами или вирусами герпеса.
3. В основе реакции гемадсорбции лежит способность культур клеток, инфицированных вирусами, адсорбировать на своей поверхности эритроциты. Целый ряд вирусов (гриппа, парагриппа и др.) обладают гемадсорбирующими свойствами, что позволяет использовать реакцию гемадсорбции для индикации этих вирусов даже при отсутствии выраженного ЦПД в культуре клеток. Механизмы реакции гемадсорбции и гемагглютинации сходны. Поэтому для обнаружения репродукции некоторых вирусов в культуре клеток можно использовать реакцию гемагглютинации с культуральной жидкостью, т. е. с питательной средой, содержащей размножившиеся вирусы.
Читайте также:

