Вирусы спасайся кто может
Обновлено: 18.04.2024
Главная задача биологии — это развитие представлений у человека о живых организмах, о многообразии видов, обо всех закономерностях развития живых существ, а также об их взаимодействии с окружающей природой. Предмет основы безопасности жизнедеятельности (ОБЖ) позволяет получить знания и умения, которые помогут сохранить жизнь и здоровье в опасных ситуациях. Эти ситуации всегда возникают неожиданно, но, тем не менее, большинство из них предсказуемы и к ним можно подготовиться заранее. ОБЖ учит нас предвидеть возможные опасности и минимизировать потери от той или иной ситуации. Сегодня мы сталкиваемся с новым видом вирусной опасности COVID-19,о котором поговорим с точки зрения биологии и ОБЖ.
Что такое вирус?
Вирус — это неклеточный инфекционный агент. Сегодня нам известно около 6 тысяч различных вирусов, но их существует несколько миллионов. Вирусы не похожи друг на друга и могут иметь как форму сферы, спирали, так и форму сложного асимметричного сплетения. Размеры вирусов варьируются от 20 нм до 300 нм.
Как устроен вирус?
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
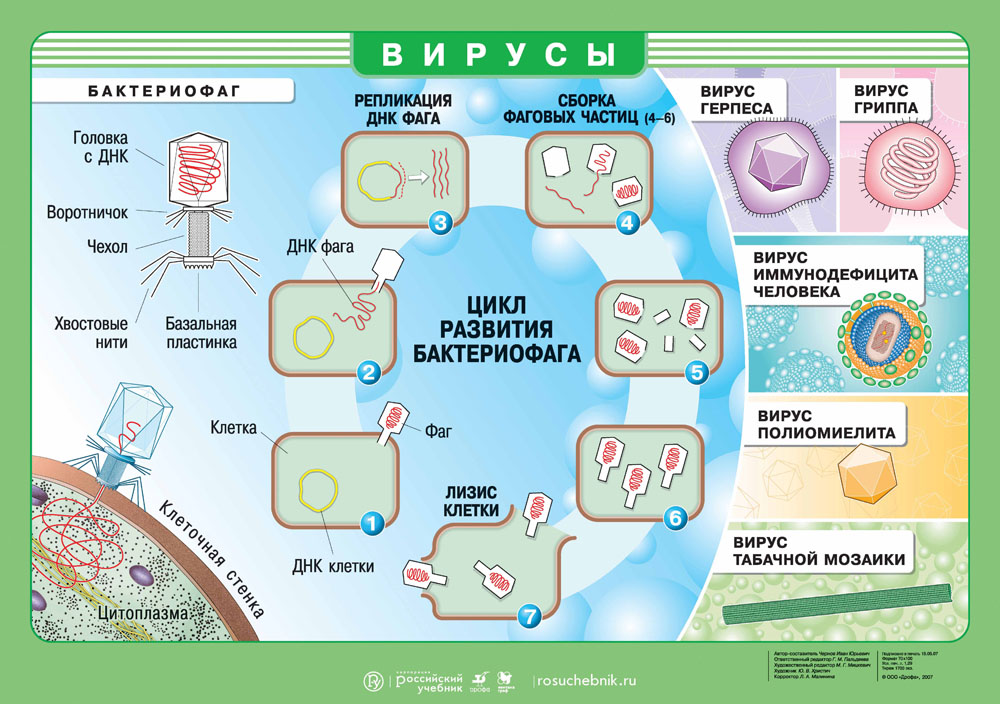
Как вирус попадает в организм?
- через физические повреждения (например, порезы на коже)
- путём направленного впрыскивания (к примеру, укус комара)
- направленного поражения отдельной поверхности (например, при вдыхании вируса через трахею)
- к эпителию слизистых оболочек (это например вирус гриппа)
- к нервной ткани (вирус простого герпеса)
- к иммунным клеткам (вирус иммунодефицита человека)

Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
Выход вируса
Вирус создал множество собственных копий, клетка оказывается изнуренной из-за использования ее ресурсов. Больше вирусу клетка не нужна, поэтому клетка часто погибает и новорожденным вирусам приходится искать нового хозяина. Это и есть заключительная стадию жизненного цикла вируса.
Скорость распространения вирусной инфекции
Размножение вирусов протекает с исключительно высокой скоростью: при попадании в верхние дыхательные пути одной вирусной частицы уже через 8 часов количество инфекционного потомства достигает 10³, а концу первых суток − 10²³.
Вирусная латентность
Как вирус распространяется?
- воздушно-капельный (кашель, чихание)
- с кожи на кожу (при прикосновениях и рукопожатиях)
- с кожи на продукты (при прикосновениях к пище грязными руками вирусы могут попасть в пищеварительную и дыхательную системы)
- через жидкие среды организма (кровь, слюну и другие)
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
Виновником эпидемии, распространяющейся сегодня по миру, стал коронавирус, вирусная частица в 0,1 микрона. Свое название он получил благодаря наростам на своей структуре, своеобразным шипам. Внутри вируса спрятан яд, с помощью которого он подчиняет себе зараженный организм. Этот вирус воздействует не только на человека, но и на птиц, свиней, собак и летучих мышей. В настоящий момент выделяют от 30 до 39 разновидностей коронавирусной инфекции. Но для человека патогенно всего 6. И как любой другой вирус COVID-19 мутирует.

К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Сколько же может жить этот вирус вне организма? Все зависит от типа вируса и от той поверхности, на которую вирусы попали. В качестве примера было рассмотрено 3 вируса, по которым велись исследования. Изучали время, на которое может задерживаться вирус на различных поверхностях. Данные приведены в таблице.

Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
- Соблюдение режима труда и отдыха, не допускающего развития утомления и переутомления.
- Выполнение условий, обеспечивающих здоровый и полноценный сон (свежий воздух, отсутствие шума, удобная постель, оптимальная продолжительность).
- Правильное здоровое питание в соответствии с потребностями организма.
- Комфортный микроклимат в жилище (температура, влажность и подвижность воздуха, естественная и искусственная освещенность помещений).
- Содержание в чистоте тела и тщательный уход за зубами.
- Спокойное и корректное поведение в конфликтных ситуациях.


Обзор
cGAS и виперины — редкие примеры известных противовирусных систем прокариот, унаследованных эукариотами
Автор
Редактор

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Что мы знаем об иммунитете прокариот?
Что объединяет грипп [1], оспу [2], бешенство [3], краснуху [4], геморрагическую лихорадку Эбола и COVID-19? Правильно, все эти заболевания человека вызываются вирусами. Есть названия и у некоторых вирусных инфекций других многоклеточных организмов: чума собак, паралич сверчка, табачная мозаика. Однако никто не придумал имена инфекционным заболеваниям прокариот. Между тем, вирусы и им изрядно досаждают. Разумеется, и прокариоты, и эукариоты обзавелись целым арсеналом средств для борьбы с паразитами, причем о защитных системах последних, а особенно об иммунной системе человека, науке известно куда больше, и информация о принципах работы врожденного и приобретенного иммунитетов давно вошла в школьный учебник.
А что у прокариот? Любой молекулярный биолог знает системы рестрикции-модификации и CRISPR-Cas, поскольку их компоненты нашли широкое применение в лабораторной практике [5], [6]. Однако это далеко не все антивирусные приспособления прокариот, известные ученым. Долгое время поиск был сосредоточен на Escherichia coli и еще нескольких модельных бактериях, но даже в такой узкой группе микроорганизмов удалось обнаружить несколько антивирусных систем с различными механизмами действия. Настоящую революцию в поиске новых антифаговых систем произвело обнаружение защитных островков (defence islands) — участков геномов прокариот, которые кодируют компоненты защитных систем [7]. Таким образом, если какой-то ген Х находится вблизи генов уже известных защитных систем в большом количестве прокариотических геномов, можно предположить, что Х тоже кодирует какой-то белок, участвующий в борьбе с вирусами. Поскольку количество прочитанных прокариотических геномов в последнее время растет как на дрожжах, этот подход позволяет ученым ежегодно находить новые гены, вовлеченные в защиту от вирусов . Так, в одной из статей 2018 года авторы описали сразу девять новых защитных систем [8], а в 2020 году одновременно две группы сообщили об обнаружении антифаговой активности у некоторых ретронов — крайне странных генетических элементов прокариот, казавшихся ранее абсолютно бесполезными [9], [10].
Еще в 2011 году обнаружили, что в защитных островках часто находятся гены, кодирующие белки-аргонавты , и с тех пор были получены убедительные свидетельства их роли в защите клеток от фагов [7], [15]. Эта находка интересна тем, что в отличие от остальных известных нам антивирусных систем прокариот, аргонавты широко распространены и среди эукариот. Странно, что до недавнего времени белки-аргонавты были единственным подобным примером. К счастью, два недавних открытия устранили это недоразумение.
cGAS — универсальный сигнальный компонент антивирусных систем
Узнавание вирусной нуклеиновой кислоты — важнейший этап активации врожденного антивирусного иммунитета у животных. Один из рецепторов, узнающих двунитевую ДНК в цитоплазме, получил название cGAS (cyclic GMP-AMP synthase), поскольку после связывания мишени начинает синтезировать циклический динуклеотид cGAMP (циклический гуанозинмонофосфат-аденозинмонофосфат, цГАМФ) из АТФ и ГТФ. cGAMP в свою очередь запускает сигнальный каскад, который активирует синтез интерферонов, необходимых в борьбе с вирусом [17].
Ученые из Weizmann Institute of Science в Израиле проанализировали 38 167 микробных геномов и обратили внимание, что из 637 прокариотических гомологов гена cGAS 417 (65,5%) находятся в защитных островках в составе оперона из 2–4 генов (рис. 1) [18]. Предположив, что такая локализация может указывать на антифаговую активность, они решили проверить, будет ли cGAS обеспечивать иммунитет штамму E. coli, в норме не содержащему такой системы. Для этого были выбраны два оперона: один из штамма E. coli TW11681, а другой из холерного вибриона Vibrio cholerae El Tor. Оказалось, что оба оперона повысили устойчивость лабораторного штамма E. coli к некоторым бактериофагам, то есть действительно функционируют как защитная система. Ученые дали этой системе название CBASS (cyclic-oligonucleotide-based antiphage signalling system).

Рисунок 1. Опероны, кодирующие cGAS, находятся в защитных островках. Желтым показаны известные системы противофаговой защиты.
Теперь предстояло понять механизм действия CBASS. Первым делом исследователи проверили, появляется ли cGAMP в клетках с CBASS в ответ на фаговую инфекцию. Для этого они проанализировали состав клеточных лизатов методом масс-спектрометрии. Как и предполагалось, cGAMP обнаружился только в клетках, содержащих систему CBASS, и только после заражения фагом.
Интересно, что в обоих исследованных оперонах ген cGAS соседствовал с геном фосфолипазы CapV, которая активируется cGAMP’ом и расщепляет липиды клеточной мембраны. Выходит, что зараженная вирусом бактерия включает систему самоубийства.
Такое поведение — не редкость в мире прокариот: известен целый класс антифаговых систем под названием Abi (abortive infection), принцип действия которых заключается в том, что клетка, обнаружив фаговую инфекцию, совершает суицид до того, как фаг успеет размножиться. Таким образом, ценой жизни одной клетки достигается защита целой популяции.
Для доказательства функционирования CBASS по механизму абортивной инфекции клетки смешали с разными концентрациями фаговых частиц. В случае, когда на пять бактериальных клеток приходилась одна фаговая частица (multiplicity of infection, MOI = 0,2), то есть зараженной оказывалась лишь часть клеток, популяция бактерий, обладающих CBASS, успешно справлялась с инфекцией, а когда концентрация фаговых частиц вдвое превышала концентрацию бактерий (MOI = 2), то есть заражались сразу все клетки, лизис культуры произходил еще быстрее, чем в штамме без CBASS (рис. 2). Это означает, что суицидальная система CBASS в первом случае спасла популяцию от полного уничтожения, а во втором спровоцировала немедленную гибель всех клеток в культуре.

Рисунок 2а. Графики роста культуры E. coli в зависимости от наличия CBASS и фаговой инфекции

Рисунок 2б. Схема действия CBASS: в ответ на заражение cGAS продуцирует cGAMP, который включает фосфолипазу, разрушающую клеточную мембрану
Хотя ученым и удалось обнаружить новую защитную систему прокариот, многое всё еще непонятно. Во-первых, остается загадкой, что является триггером для активации cGAS. Вряд ли это двунитевая ДНК, как у эукариот, ведь у прокариот ядра нет, и отличить геномную ДНК от вирусной не так-то просто. Во-вторых, неясно, во всех ли случаях CBASS ведет себя как система абортивной инфекции. Дело в том, что вместо фосфолипазы в состав CBASS могут входить другие белки с неизвестной активностью.
Так или иначе, cGAS заслужил место в ряду белков, вовлеченных в антивирусную защиту у представителей и прокариот, и эукариот.
Виперины — универсальная защита против вирусных РНК-полимераз
Виперин — один из белков, продуцируемый клетками животных в ответ на обработку интерферонами. Известно, что виперин подавляет репликацию многих вирусов за счет продукции ddhСTP (3′-deoxy-3′4′-didehydro-CTP, 3′-дезокси-3′4′-дидегидро-ЦТФ, ддгЦТФ) — производного одного из четырех нуклеотидов, из которых РНК-полимеразы строят РНК. ddhCTP узнается вирусными РНК-полимеразами и включается в состав РНК, но из-за отсутствия 3′-концевого гидроксила фермент не может продолжить синтез. Один из вирусов, с которым борется человеческий виперин — печально известный вирус Зика , [19].
Всё те же исследователи из Израиля заметили, что некоторые гомологи виперинов у прокариот кодируются генами, находящимися в защитных островках (рис. 3) [22]. Для подтверждения их участия в борьбе с вирусами ученые помещали гены 59 представителей прокариотических виперинов в лабораторный штамм E. coli и проверяли, придают ли они устойчивость к фаговым инфекциям. Около половины исследуемых белков показали хорошие результаты в защите от целого ряда фагов, что позволило заявить об открытии новой антивирусной системы прокариот.

Рисунок 3. Прокариотические виперины локализуются в защитных островках. Желтым выделены гены известных систем противофаговой защиты.
Для выяснения механизма работы виперинов ученые вновь прибегли к масс-спектрометрическому анализу клеточных лизатов после заражения фагом Т7. На этот раз искали ddhСTP, но нашли не только его: оказалось, что разные прокариотические виперины синтезируют производные разных нуклеотидов: ЦТФ, УТФ и ГТФ (рис. 4). Забавно, что среди продуктов виперинов не обнаружили производных АТФ. Сами авторы работы предполагают, что это связано с несовершенством системы детекции.

Рисунок 4. Филогенетическое дерево виперинов. Обозначены человеческий виперин и исследованные в работе прокариотические виперины, а также их субстратная специфичность.
Чтобы проверить эффект виперинов на работу фаговой РНК-полимеразы, исследователи экспрессировали под контролем промотора фага Т7 ген зеленого флуоресцентного белка GFP в клетках E. coli, кодирующих РНК-полимеразу фага Т7, и наблюдали, что клетки флуоресцируют. Но если в таких клетках экспрессировать один из генов виперинов, GFP не синтезируется (рис. 5).

Рисунок 5. Виперины подавляют активность РНК-полимеразы Т7 in vivo. МоаА — отрицательный контроль. В присутствии виперинов снижается экспрессия гена GFP, находящегося под контролем промотора Т7-РНК-полимеразы.
Полученные данные подтверждают, что прокариотические виперины борются с вирусами по тому же принципу, что и виперины животных. Хотя правильнее будет сказать, что виперины животных работают как прокариотические: филогенетический анализ свидетельствует о том, что эукариотические виперины — лишь небольшая веточка на разветвленном дереве этого белкового семейства (рис. 4).
Микробы — это модно
Людям свойственно интересоваться прежде всего собой, и уж если не видом Homo sapiens, то хотя бы животными или на худой конец растениями. Однако во все времена находились энтузиасты, исследующие необъятный мир микробов. Может, этим энтузиастам следует заняться какими-то действительно важными проблемами? Неужели мы уже все болезни научились лечить? Только вот без любителей микробов не было бы у нас ни эндонуклеаз рестрикции для клонирования, ни термофильных ДНК-полимераз для ПЦР, ни CRISPR-Cas для редактирования геномов. Если хорошенько поискать, то у прокариот непременно найдется еще много интересного и полезного! А искать сейчас удобно как никогда: информация о новых секвенированных геномах поступает непрерывным потоком, только успевай анализировать. Исследования в области прокариотических систем защиты от фагов — отличный пример такого поиска. Открытие новых антивирусных систем, общих для бактерий, архей и эукариот, показывает, что можно узнавать что-то новое про нас с вами, изучая захватывающе разнообразный мир микробов.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
В холода вирусы активизируются с большим удовольствием. Каждый год специалисты отмечают всплеск фарингитов, ларингитов, тонзиллитов, трахеитов, ринитов, ангин, гриппа, бронхита и даже пневмонии. Как себя защитить? Рассказывает врач-терапевт Елена Поклад.

— Хочу уточнить, что такого заболевания, как простуда, не существует. Да, может протянуть спину или шею (миозит), но это другое. Если вы начали чувствовать себя неважно, появились слабость и кашель, виной тому не сквозняк, а именно инфекция. Холод — лишь дополнительный фактор, проводник, который усугубляет ситуацию. Поэтому все равно важно одеваться по погоде.
Второй фактор — скученность. Дети учатся в школе, взрослые тоже, как правило, часто работают в коллективе, где есть переносчики вируса. Так может начаться и массовая эпидемия.
Как предотвратить?
— На самом деле оградить себя от вирусов со 100-процентной гарантией невозможно. Человека пришлось бы изолировать ото всех и поместить в специальный инкубатор. Но все же есть определенные правила профилактики:
1. Нужно соблюдать личную гигиену. Придя домой, обязательно хорошенько вымойте руки с мылом.
2. Неменьшего внимания требуют также фрукты и овощи. Тщательно мойте их перед едой. По возможности удаляйте кожуру.
3. Регулярно проветривайте помещение, в котором находитесь, чтобы вредоносные микроорганизмы не скапливались вокруг вас.

4. Дома почаще делайте влажную уборку, необязательно при помощи каких-то специальных средств. Хотя бы удаляйте поверхностную пыль — это любимое место обитания тех самых вредоносных организмов — и мокрой тряпкой протирайте полы.
5. Старайтесь избегать мест скопления людей. Большинство вирусов передаются воздушно-капельным путем.
6. Не списывайте со счетов старую добрую оксолиновую мазь. Обрабатывайте ею ноздри с внешней стороны (особенно актуально для деток), чтобы перекрыть хотя бы один путь проникновения инфекции в организм.
7. Делайте прививки от гриппа. Существуют три основных его вида: А, В и С. Последний штамм самый стабильный, и если им переболеть единожды, вряд ли он сможет побороть вас снова. А вот вирусы А и В изменчивы. Да, нет точной гарантии, но, по крайней мере, существует шанс, что болезнь как минимум будет протекать в более легкой форме.
Что делать при первых симптомах заболеваний?
- Начинайте принимать противовирусные препараты в профилактической дозировке. Пейте побольше теплой жидкости. Вспоминайте о малине и лимоне.
- Два-три раза в день полоскайте горло специальным раствором. Промывайте нос водой с морской солью (можно приобрести готовый спрей).
— При явных признаках интоксикации (ломота в костях, сильный озноб, повышение температуры, сильный кашель) сразу обращайтесь к врачу. Во-первых, чем раньше вы начнете лечение, тем лучше для вас, во-вторых, зараженный человек является переносчиком вирусов, которые могут быстро распространиться в коллективе.
Читайте также:

