Внутривидовой и межвидовой обмен генетическим материалом у вирусов
Обновлено: 24.04.2024
Генетические взаимодействия между вирусами. Рекомбинации и перераспределение генов вирусами. Обмен фрагментами генома вирусами. Антигенный шифт.
Заражение вирусами чувствительных к ним клеток носит множественный характер, то есть в клетку может проникнуть несколько вирионов, обычно идентичных или близкородственных. В подобных ситуациях геномы вирусных частиц в динамике репродуктивных циклов могут взаимодействовать или интерферировать. Независимо от типа нуклеиновой кислоты генетические взаимодействия между вирусами представлены несколькими формами: рекомбинация, обмена фрагментами генома, комплементация.
Генетические взаимодействия между вирусами. Рекомбинации и перераспределение генов вирусами
Рекомбинации и перераспределение генов между геномами приводят к перераспределении генетического материала в дочерних популяциях. Они отмечены во всех группах ДНК-содержащих вирусов, у всех РНК-содержащих вирусов с сегментированным геномом и лишь у немногих РНК-содержащих вирусов с несегментированным геномом (например, у полиовируса и вируса ящура).
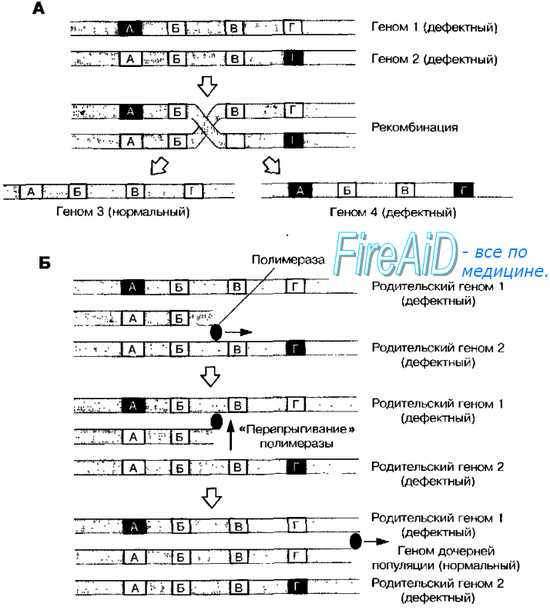
Рис. 5-5. Рекомбинация ДНК- (А) и РНК-содержащих (Б) вирусов
• У ДНК-содержащих вирусов с дефектными геномами можно наблюдать рекомбинации, приводящие к образованию нормального дочернего генома (рис. 5-5, А).
Обмен фрагментами генома вирусами. Антигенный шифт
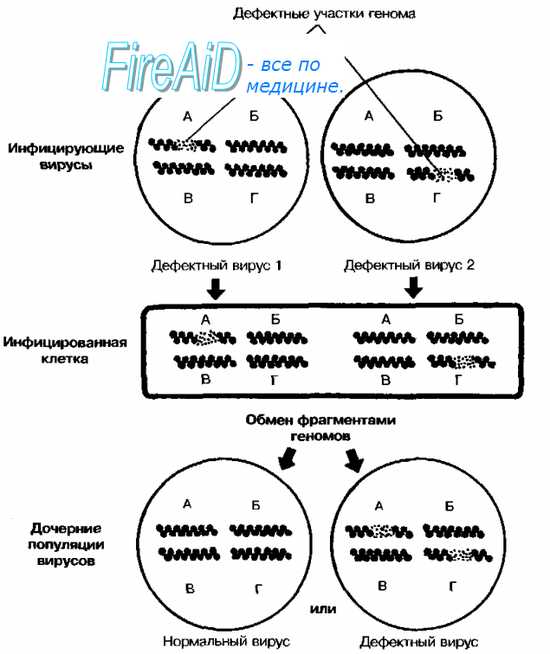
Рис. 5-6. Обмен фрагментами генома (А- Г) у РНК-содержащих вирусов
Обмен фрагментами генома наблюдают у РНК-содержащих вирусов с сегментированным геномом. Б отличие от рекомбинации суть процесса состоит в обмене крупных блоков наследственного материала. Например, при множественном заражении клетки мутантами вируса гриппа с изменениями, закреплёнными в различных сегментах генома, возможно появление нормального штамма вируса; в образовании популяции последнего принимают участие геномы обоих вирусов (рис. 5-6). В частности, передача двух фрагментов генома вирулентного для цыплят штамма вируса гриппа авирулентному влечёт за собой приобретение последним вирулентных свойств. В результате обмена вирус гриппа типа А может получить новые и селективно ценные типы поверхностных Аг гемагглютинина и нейраминидазы, что обеспечивает антигенный шифт [от англ. shift, перемещение] в динамике инфекционного процесса.
- Вернуться в оглавление раздела "Микробиология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Геном вирусов имеет простое строение и малую молекулярную массу. Число генов у вирусов колеблется от 4—6 (парвовирусы) до 150 генов и больше (вирус оспы). В основе изменчивости вирусов лежат мутации. Мутации носят случайный характер или могут быть направленными. Вирус, являясь облигатным внутриклеточным паразитом, реализует этот паразитизм на генетическом уровне. Присутствие нескольких типов вирусов в инфицированных клетках, т.е. смешанная инфекция, может приводить к таким генетическим взаимодействиям между ними, как множественная реактивация, рекомбинация, кросс-реактивация и др.; могут иметь место и не генетические взаимодействия — комплементация и др.
Множественная реактивация — процесс взаимодействия вирусов с поражением разных генов, в результате которого взаимодействующие вирионы дополняют друг друга благодаря генетической рекомбинации, образуя неповрежденный вирус. Рекомбинация — обмен генетическим материалом между вирусами — возможна в виде обмена генами (межгенная рекомбинация) или участками одного и того же гена (внутригенная рекомбинация). У вирусов рекомбинация происходит в процессе заражения двумя или более типами вирусов, отличающимися друг от друга по генетическим признакам. Вариантом рекомбинации является перекрестная реактивация, или кросс-реактивация, происходящая в том случае, когда у одного из штаммов вируса часть генома повреждена, а другой геном нормальный. При смешанной инфекции двумя такими вирусами в результате рекомбинации появляются штаммы вируса со свойствами родительских микроорганизмов.
В качестве примера негенетического взаимодействия вирусов может быть приведена комплементация: при смешанной инфекции стимулируется репродукция обоих участников взаимодействия или одного из них без изменения генотипов вирусов. Комплементация широко распространена среди вирусов и наблюдается между как родственными, так и неродственными вирусами. Обмен генетическим материалом при этом феномене не наблюдается.
Если геном одного вируса заключен в капсид другого вируса, этот феномен называется фенотипическим смешиванием, наблюдаемым при смешанной инфекции.
Возможны также генетические взаимодействия неродственных вирусов, изучаемые генетической инженерией.
Изучение генетики микроорганизмов не только имеет важное биологическое значение, но и способствует решению многих медицинских проблем, таких, как разработка патогенетических основ лечения и профилактики инфекционных болезней, способов диагностики (полимеразная цепная реакция, ДНК-зонды), создание профилактических, лечебных и диагностических препаратов.
44. Основные группы антимикробных химиопрепаратов, применяемых в терапии и профилактики инфекционных болезней.
В 1932 г. Г. Домагк синтезировал первый сульфаниламидный препарат — стрептоцид, явившийся родоначальником многочисленной группы сульфаниламидных соединений(табл. 8.1), к которым чувствительны ряд грамположительных и грамотрицательных бактерий, прежде всего пиогенные стрептококки, менингококки, гонококки, кишечная палочка и др.
Изучение механизма антибактериального действия сульфаниламидов привело к открытию антиметаболитов— соединений, имеющихьструктурное сходство с важнейшими метаболитами, участвующими в анаболических или катаболических реакциях. Включение антиметаболита в эти реакции приводит соответствующие бактерии к задержке размножения и последующей гибели. Сульфаниламиды оказывают бактериостатическое действие.
Помимо сульфаниламидов, к антиметаболитам относятся аналоги изоникотиновой кислоты, азотистых оснований и других соединений.
Однако антиметаболиты нашли сравнительно ограниченное применение в химиотерапии инфекционных заболеваний.
Это объясняется однотипностью многих биохимических реакций, протекающих в клетках бактерий и человека, поэтому один и тот же антиметаболит блокирует образование продуктов, необходимых для жизнедеятельности микробов и определенных клеток организма человека.
К препаратам, блокирующим процессы репликации и транскрипции относится группа хинолонов.
К препаратам, нарушающим энергетический метаболизм, относятся производные оксихинолина.
Из производных тиосемикарбазона применяется фарингосепт, обладающий бактериостатической активностью в отношении пиогенного стрептококка и других гемолитических стрептококков, встречающихся на миндалинах при ангинах, а также в полости рта при гингивитах и стоматитах.
Вирусы не способны размножаться на питательных средах - это строгие внутриклеточные паразиты. Более того, в отличие от риккетсий и хламидий, вирусы в клетке хозяина не растут и не размножаются путем деления. Составные части вируса - нуклеиновые кислоты и белковые молекулы синтезируются в клетке хозяина раздельно, в разных частях клетки - в ядре и в цитоплазме. При этом клеточные белоксинтезирующие системы подчиняются вирусному геному, его НК.
Репродукция вируса в клетке происходит в несколько фаз:
Первая фаза - адсорбция вируса на поверхности клетки, чувствительной к данному вирусу.
Вторая фаза - проникновение вируса в клетку хозяина путем виропексиса.
В зависимости от типа нуклеиновой кислоты этот процесс совершается следующим образом.
ДНК-содержащие (ДНК —> иРНК —>белок):
Репродукция происходит в ядре: аденовирусы, герпес, паповавирусы. Используют ДНК-зависимую РНК - полимеразу клетки.
Репродукция происходит в цитоплазме: вирусы имеют свою ДНК-зависимую РНК полимеразу.
РНК-содержащие вирусы:
Рибовирусы с позитивным геномом (плюс-нитиевые): пикорна-, тога-, коронавирусы. Транскрипции нет.
Рибовирусы с негативным геномом (минус- нитевые): грипп, корь, паротит, орто-, парамиксовирусы.
(-)РНК —> иРНК —> белок (иРНК комплементарная (-)РНК). Этот процесс идет при участии специального вирусного фермента - вирионная РНК-зависимая PHK-полимераза ( в клетке такого фермента быть не может).
(-)РНК -> ДНК —> иРНК —>белок (и РНК гомологична РНК). В этом случае процесс образования ДНК на базе (-)РНК возможен при участии фермента - РНК-зависимой ДНК-полимеразы (обратной транскриптазы или ревертазы)
Четвертая фаза - синтез компонентов вириона. Нуклеиновая кислота вируса образуется путем репликации. На рибосомы клетки транслируется информация вирусной иРНК, и в них синтезируется вирус-специфический белок.
Пятая фаза - сборка вириона. Путем самосборки образуются нуклеокапсиды.
Шестая фаза - выход вирионов из клетки. Простые вирусы, например, вирус полиомиелита, при выходе из клетки разрушают ее. Сложноорганизованные вирусы, например, вирус гриппа, выходят из клетки путем почкования. Внешняя оболочка вируса (суперкапсид) формируется в процессе выхода вируса из клетки. Клетка при таком процессе на какое-то время остается живой.
Описанные типы взаимодействия вируса с клеткой называются продуктивными, так как приводят к продукции зрелых вирионов.
Иной путь - интегративный - заключается в том, что после проникновения вируса в клетку и "раздевания" вирусная нуклеиновая кислота интегрирует в клеточный геном, то есть встраивается в определенном месте в хромосому клетки и затем в виде так называемого прови-руса реплицируется вместе с ней. Для ДНК- и РНК-содержащих вирусов этот процесс совершается по-разному. В первом случае вирусная ДНК интегрирует в клеточный геном. В случае РНК-содержащих вирусов вначале происходит обратная транскрипция: на матрице вирусной РНК при участии фермента "обратной транскриптазы" образуется ДНК, которая встраивается в клеточный геном. Провирус несет дополнительную генетическую информацию, поэтому клетка приобретает новые свойства. Вирусы, способные осуществить такой тип взаимодействия с клеткой, называются интегративными. К интегративным вирусам относятся некоторые онкогенные вирусы, вирус гепатита В, вирус герпеса, вирус иммунодефицита человека, умеренные бактериофаги.
Кроме обычных вирусов, существуют прионы - белковые инфекционные частицы, не содержащие нуклеиновую кислоту. Они имеют вид фибрилл, размером до 200 нм. Вызывают у человека и у животных медленные инфекции с поражением мозга: болезнь Крейтцфельда-Якоба, куру, скрепи и другие.
Методы индикации вирусов в исследуемом материале.
О репродукции вирусов в культурах клеток судят по их цитопатическому действию (ЦПД), которое носит разный характер в зависимости от вида вируса, по бляшкообра- манию на клеточном монослое, покрытом тонким агаровым слоем, гемадсорбции эритроцитов и другим тестам.
Таким образом, индикация вирусов производится микроскопически по наличию ЦПД, бляшкообразованию на клеточном монослое, гемадсорбции эритроцитов, добавленных к клеточной культуре вируса, а также в реакции гемагглютинации с исследуемым вируссодержащим материалом. Реакцию гемагглютинации вызывают вирусы, содержащие в составе своего капсида или суперкапсида гемагглютинин.
Наследственные изменения можно подразделить на изменения, возникающие в результате мутаций и рекомбинаций генетического материала.
Мутации представляют собой изменения в первичной структуре ДНК, которые выражаются в наследственно закрепленной утрате или изменении какого-либо признака (признаков).
Мутации можно классифицировать по происхождению, характеру изменений в первичной структуре ДНК, фенотипическим последствиям для мутировавшей бактериальной клетки и другим признакам.
По происхождению мутации можно условно подразделить на спонтанные и индуцированные. Первые составляют естественный, или спонтанный, фон, величина которого колеблется в зависимости от типа мутации и вида микробной популяции.
Индуцированными называют мутации, которые получают в эксперименте под влиянием каких-либо мутагенов.
По количеству мутировавших генов различают генные и хромосомные мутации. Первые затрагивают один ген и чаще всего являются точковыми, вторые распространяются на несколько генов.
Точковые мутации представляют собой замену или вставку пары азотистых оснований в ДНК, которая приводит к изменению одного кодона, вследствие чего вместо одной аминокислоты кодируется другая либо образуется бессмысленный кодон, не кодирующий ни одну из аминокислот. Последние называют нонсенс мутациями.
У микроорганизма, несущего точковую мутацию в одном гене, может возникнуть вторичная мутация в этом же гене, в результате которого произойдет восстановление дикого фенотипа. При этом первичную мутацию, которая привела к возникновению мутантного фенотипа, называют прямой, а мутацию, обусловившую возврат к дикому фенотипу, — обратной.
Хромосомные мутации носят характер крупных перестроек в отдельных фрагментах ДНК. Они возникают в результате выпадения меньшего или большего числа нуклеотидов (делеция), либо поворота участка ДНК на 180° (инверсия), либо повторения какого-либо фрагмента ДНК (дупликация). Один из механизмов образования хромосомных мутаций связан с перемещением Is-последовательностей и транспозонов из одного участка ДНК в другой или из репликона в репликон (из хромосомы в плазмиду и наоборот).
Рекомбинация (ре + лат. combinatio — соединение) — возникновение новых последовательностей ДНК в результате разрывов и последующих восстановлений ее молекул. В итоге таких изменений ДНК бактерий появляются так называемые рекомбинантные штаммы, или рекомбинанты
Наиболее изучены три типа передачи ДНК, отличающиеся друг от друга способом ее транспортировки: трансформация, трансдукция, конъюгация.
39-41. Генетические рекомбинации. Особенности рекомбинативной изменчивости у бактерий и эукариотов. Трансформация и ее стадии.
Генетические рекомбинации. Конъюгация, механизмы и этапы конъюгации. F и Hfr – факторы.
Генетические рекомбинации. Трансдукция, типы трансдукции.
Микроорганизмам, как и клеткам высших организмов свойственны генетические рекомбинации, которые имеют свои особенности. Они определяются прежде всего способом размножения и закономерностями передачи генетического материала. Известно, что генетические рекомбинации у клеток эукариот совершаются в ходе процессов, сопровождающих половое размножение путем реципрокного (взаимного) обмена фрагментами хромосом. При таком обмене генетическим материалом из двух рекомбинирующих родительских хромосом образуются две рекомбинантные хромосомы. Применительно к данным клеткам это означает, что в результате рекомбинаций возникают две рекомбинантные особи.
Прокариотам не свойственно половое размножение. Рекомбинация у них происходит в результате внутригеномных перестроек, заключающихся в изменении локализации генов в пределах хромосомы, или при проникновении в клетку реципиента части ДНК донора.
Последнее приводит к формированию неполной зиготы — мерозиготы. В результате рекомбинаций в мерозиготе образуется только один рекомбинат, генотип которого представлен в основном генотипом реципиента с включенным в него фрагментом ДНК донора. Вследствие этого реципрокность генетических рекомбинаций у бактерий не может быть выявлена.
Рекомбинации подразделяют на законные и незаконные. Законная рекомбинация требует наличия протяженных, комплементарных участков ДНК в рекомбинируемых молекулах. Она происходит только между близкородственными видами микроорганизмов.
Генетические рекомбинации происходят при участии ряда ферментов в пределах отдельных генов или групп сцеплений генов. Существуют специальные гес-гены, детермирующие рекомбинационную способность бактерий. Передача генетического материала (хромосомных генов) от одних бактерий к другим происходит путем трансформации, трансдукции и конъюгации, а плазмидных генов — путем трансдукции и конъюгации.
Трансформация— непосредственная передача генетического материала (фрагмента ДНК) донора реципиентной клетке.
Процесс трансформации бактерий можно подразделить на несколько фаз:
1) адсорбция ДНК-донора на клетке-реципиенте;
2) проникновение ДНК внутрь клетки-реципиента;
3) соединение ДНК с гомологичным участком хромосомы реципиента с последующей рекомбинацией.
После проникновения внутрь клетки трансформирующая ДНК деспирализуется. Затем происходит физическое включение любой из двух нитей ДНК донора в геном реципиента.
Переносимая ДНК взаимодействует с ДНК реципиента — происходит гомологичная рекомбинация.
Трансдукция (от лат. transductio — перенос, перемещение) — передача ДНК от бактерии-донора к бактерии-реципиенту при участии бактериофага. Различают три типа трансдукции: неспецифическую или общую, специфическую и абортивную.
Неспецифическая трансдукция. В процессе репродукции фага в момент сборки фаговых частиц в их головку вместе с фаговой ДНК может проникнуть какой-либо фрагмент ДНК бактерии-донора. При этом фаг может утратить часть своего генома и стать дефектным.
Принесенный фагом фрагмент ДНК бактерии-донора способен включаться в гомологическую область ДНК клетки-реципиента путем рекомбинации. Таким образом, при неспецифической трансдукции трансдуцирующие фаги являются только переносчиком генетического материала от одних бактерий к другим, поскольку сама фаговая ДНК не участвует в образовании рекомбинантов (трансдуктантов).
Специфическая трансдукция характеризуется способностью фага переносить определенные гены от бактерии-донора к бактерии-реципиенту. Это связано с тем, что образование трансдуцирующего фага происходит путем выщепления профага из бактериальной хромосомы вместе с генами, расположенными на хромосоме клетки-донора рядом с профагом.
При взаимодействии трансдуцирующих фагов с клетками реципиентного штамма происходит включение гена бактерии-донора вместе с ДНК дефектного фага в хромосому бактерии-реципиента. Бактерии, лизогенированные дефектным фагом, невосприимчивы, как и нее лизогенные клетки, к последующему заражению гомологичным вирулентным фагом.
Абортивная трансдукция. При абортивной трансдукции принесенный фагом фрагмент ДНК бактерии-донора не включается в хромосому бактерии-реципиента, а располагается в ее цитоплазме и может в таком виде функционировать. Во время деления бактериальной клетки трансдуцированный фрагмент ДНК-донора может передаваться только одной из двух дочерних клеток, т.е. наследоваться однолинейно и в конечном итоге утрачиваться в потомстве.
42. Плазмиды, их свойства и основные генетические функции. Генетический анализ, принципы составления генетических карт. Генная инженерия. Генетические методы диагностики инфекционных заболеваний. Молекулярная гибридизация, полимеразная цепная реакция.
Плазмиды — внехромосомные мобильные генетические структуры бактерий, представляющие собой замкнутые кольца двунитчатой ДНК. По размерам составляют 0,1—5 % ДНК хромосомы. Плазмиды способны автономно копироваться (реплицироваться) и существовать в цитоплазме клетки, поэтому в клетке может быть несколько копий плазмид. Плазмиды могут включаться (интегрировать) в хромосому и реплицироваться вместе с ней. Различают трансмиссивные и нетрансмиссивные плазмиды. Трансмиссивные (конъюгативные) плазмиды могут передаваться из одной бактерии в другую.
Среди фенотипических признаков, сообщаемых бактериальной клетке плазмидами, можно выделить следующие:
1) устойчивость к антибиотикам;
2) образование колицинов;
3) продукция факторов патогенности;
4) способность к синтезу антибиотических веществ;
5) расщепление сложных органических веществ;
6) образование ферментов рестрикции и модификации.
Некоторые плазмиды находятся под строгим контролем. Это означает, что их репликация сопряжена с репликацией хромосомы так, что в каждой бактериальной клетке присутствует одна или, по крайней мере, несколько копий плазмид.
Число копий плазмид, находящихся под слабым контролем, может достигать от 10 до 200 на бактериальную клетку.
Для характеристики плазмидных реплико-нов их принято разбивать на группы совместимости. Несовместимость плазмид связана с неспособностью двух плазмид стабильно сохраняться в одной и той же бактериальной клетке. Несовместимость свойственна тем плазмидам, которые обладают высоким сходством репликонов, поддержание которых в клетке регулируется одним и тем же механизмом.
Некоторые плазмиды могут обратимо встраиваться в бактериальную хромосому и функционировать в виде единого репликона. Такие плазмиды называются интегративными или эписомами.
У бактерий различных видов обнаружены R-плазмиды, несущие гены, ответственные за множественную устойчивость к лекарственным препаратам — антибиотикам, сульфаниламидам и др., F-плазмиды, или половой фактор бактерий, определяющий их способность к конъюгации и образованию половых пилей, Ent-плазмиды, детерминирующие продукцию энтеротоксина.
Плазмиды могут определять вирулентность бактерий, например возбудителей чумы, столбняка, способность почвенных бактерий использовать необычные источники углерода, контролировать синтез белковых антибиотикоподобных веществ — бактериоцинов, детерминируемых плазмидами бактериоциногении, и т. д. Существование множества других плазмид у микроорганизмов позволяет полагать, что аналогичные структуры широко распространены у самых разнообразных микроорганизмов.
Плазмиды подвержены рекомбинациям, мутациям, могут быть элиминированы (удалены) из бактерий, что, однако, не влияет на их основные свойства. Плазмиды являются удобной моделью для экспериментов по искусственной реконструкции генетического материала, широко используются в генетической инженерии для получения рекомбинантных штаммов. Благодаря быстрому самокопированию и возможности конъюгационной передачи плазмид внутри вида, между видами или даже родами плазмиды играют важную роль в эволюции бактерий.
Полимеразная цепная реакция позволяет обнаружить микроб в исследуемом материале (воде, продуктах, материале от больного) по наличию в нем ДНК микроба без выделения последнего в чистую культуру.
Для проведения этой реакции из исследуемого материала выделяют ДНК, в которой определяют наличие специфичного для данного микроба гена. Обнаружение гена осуществляют его накоплением. Для этого необходимо иметь праймеры комплементарного З'-концам ДНК. исходного гена. Накопление (амплификация) гена выполняется следующим образом. Выделенную из исследуемого материала ДНК нагревают. При этом ДНК распадается на 2 нити. Добавляют праймеры. Смесь ДНК и праймеров охлаждают. При этом праймеры, при наличии в смеси ДНК искомого гена, связываются с его комплементарными участками. Затем к смеси ДНК и праймера добавляют ДНК-полимеразу и нуклеотиды. Устанавливают температуру, оптимальную для функционирования ДНК-полимеразы. В этих условиях, в случае комплементарное™ ДНК гена и праймера, происходит присоединение нуклеотидов к З'-концам праймеров, в результате чего синтезируются две копии гена. После этого цикл повторяется снова, при этом количество ДНК гена будет увеличиваться каждый раз вдвое. Проводят реакцию в специальных приборах — амплификаторах. ПЦР применяется для диагностики вирусных и бактериальных инфекций.
Рекомбинация (ре + лат. combinatio — соединение) — возникновение новых последовательностей ДНК в результате разрывов и последующих восстановлений ее молекул. В итоге таких изменений ДНК бактерий появляются так называемые рекомбинантные штаммы, или рекомбинанты
Наиболее изучены три типа передачи ДНК, отличающиеся друг от друга способом ее транспортировки: трансформация, трансдукция, конъюгация.
39-41. Генетические рекомбинации. Особенности рекомбинативной изменчивости у бактерий и эукариотов. Трансформация и ее стадии.
Генетические рекомбинации. Конъюгация, механизмы и этапы конъюгации. F и Hfr – факторы.
Генетические рекомбинации. Трансдукция, типы трансдукции.
Микроорганизмам, как и клеткам высших организмов свойственны генетические рекомбинации, которые имеют свои особенности. Они определяются прежде всего способом размножения и закономерностями передачи генетического материала. Известно, что генетические рекомбинации у клеток эукариот совершаются в ходе процессов, сопровождающих половое размножение путем реципрокного (взаимного) обмена фрагментами хромосом. При таком обмене генетическим материалом из двух рекомбинирующих родительских хромосом образуются две рекомбинантные хромосомы. Применительно к данным клеткам это означает, что в результате рекомбинаций возникают две рекомбинантные особи.
Прокариотам не свойственно половое размножение. Рекомбинация у них происходит в результате внутригеномных перестроек, заключающихся в изменении локализации генов в пределах хромосомы, или при проникновении в клетку реципиента части ДНК донора.
Последнее приводит к формированию неполной зиготы — мерозиготы. В результате рекомбинаций в мерозиготе образуется только один рекомбинат, генотип которого представлен в основном генотипом реципиента с включенным в него фрагментом ДНК донора. Вследствие этого реципрокность генетических рекомбинаций у бактерий не может быть выявлена.
Рекомбинации подразделяют на законные и незаконные. Законная рекомбинация требует наличия протяженных, комплементарных участков ДНК в рекомбинируемых молекулах. Она происходит только между близкородственными видами микроорганизмов.
Генетические рекомбинации происходят при участии ряда ферментов в пределах отдельных генов или групп сцеплений генов. Существуют специальные гес-гены, детермирующие рекомбинационную способность бактерий. Передача генетического материала (хромосомных генов) от одних бактерий к другим происходит путем трансформации, трансдукции и конъюгации, а плазмидных генов — путем трансдукции и конъюгации.
Трансформация — непосредственная передача генетического материала (фрагмента ДНК) донора реципиентной клетке.
Процесс трансформации бактерий можно подразделить на несколько фаз:
1) адсорбция ДНК-донора на клетке-реципиенте;
2) проникновение ДНК внутрь клетки-реципиента;
3) соединение ДНК с гомологичным участком хромосомы реципиента с последующей рекомбинацией.
После проникновения внутрь клетки трансформирующая ДНК деспирализуется. Затем происходит физическое включение любой из двух нитей ДНК донора в геном реципиента.
Переносимая ДНК взаимодействует с ДНК реципиента — происходит гомологичная рекомбинация.
Трансдукция (от лат. transductio — перенос, перемещение) — передача ДНК от бактерии-донора к бактерии-реципиенту при участии бактериофага. Различают три типа трансдукции: неспецифическую или общую, специфическую и абортивную.
Неспецифическая трансдукция. В процессе репродукции фага в момент сборки фаговых частиц в их головку вместе с фаговой ДНК может проникнуть какой-либо фрагмент ДНК бактерии-донора. При этом фаг может утратить часть своего генома и стать дефектным.
Принесенный фагом фрагмент ДНК бактерии-донора способен включаться в гомологическую область ДНК клетки-реципиента путем рекомбинации. Таким образом, при неспецифической трансдукции трансдуцирующие фаги являются только переносчиком генетического материала от одних бактерий к другим, поскольку сама фаговая ДНК не участвует в образовании рекомбинантов (трансдуктантов).
Специфическая трансдукция характеризуется способностью фага переносить определенные гены от бактерии-донора к бактерии-реципиенту. Это связано с тем, что образование трансдуцирующего фага происходит путем выщепления профага из бактериальной хромосомы вместе с генами, расположенными на хромосоме клетки-донора рядом с профагом.
При взаимодействии трансдуцирующих фагов с клетками реципиентного штамма происходит включение гена бактерии-донора вместе с ДНК дефектного фага в хромосому бактерии-реципиента. Бактерии, лизогенированные дефектным фагом, невосприимчивы, как и нее лизогенные клетки, к последующему заражению гомологичным вирулентным фагом.
Абортивная трансдукция. При абортивной трансдукции принесенный фагом фрагмент ДНК бактерии-донора не включается в хромосому бактерии-реципиента, а располагается в ее цитоплазме и может в таком виде функционировать. Во время деления бактериальной клетки трансдуцированный фрагмент ДНК-донора может передаваться только одной из двух дочерних клеток, т.е. наследоваться однолинейно и в конечном итоге утрачиваться в потомстве.
42. Плазмиды, их свойства и основные генетические функции. Генетический анализ, принципы составления генетических карт. Генная инженерия. Генетические методы диагностики инфекционных заболеваний. Молекулярная гибридизация, полимеразная цепная реакция.
Плазмиды — внехромосомные мобильные генетические структуры бактерий, представляющие собой замкнутые кольца двунитчатой ДНК. По размерам составляют 0,1—5 % ДНК хромосомы. Плазмиды способны автономно копироваться (реплицироваться) и существовать в цитоплазме клетки, поэтому в клетке может быть несколько копий плазмид. Плазмиды могут включаться (интегрировать) в хромосому и реплицироваться вместе с ней. Различают трансмиссивные и нетрансмиссивные плазмиды. Трансмиссивные (конъюгативные) плазмиды могут передаваться из одной бактерии в другую.
Среди фенотипических признаков, сообщаемых бактериальной клетке плазмидами, можно выделить следующие:
1) устойчивость к антибиотикам;
2) образование колицинов;
3) продукция факторов патогенности;
4) способность к синтезу антибиотических веществ;
5) расщепление сложных органических веществ;
6) образование ферментов рестрикции и модификации.
Некоторые плазмиды находятся под строгим контролем. Это означает, что их репликация сопряжена с репликацией хромосомы так, что в каждой бактериальной клетке присутствует одна или, по крайней мере, несколько копий плазмид.
Число копий плазмид, находящихся под слабым контролем, может достигать от 10 до 200 на бактериальную клетку.
Для характеристики плазмидных реплико-нов их принято разбивать на группы совместимости. Несовместимость плазмид связана с неспособностью двух плазмид стабильно сохраняться в одной и той же бактериальной клетке. Несовместимость свойственна тем плазмидам, которые обладают высоким сходством репликонов, поддержание которых в клетке регулируется одним и тем же механизмом.
Некоторые плазмиды могут обратимо встраиваться в бактериальную хромосому и функционировать в виде единого репликона. Такие плазмиды называются интегративными или эписомами.
У бактерий различных видов обнаружены R-плазмиды, несущие гены, ответственные за множественную устойчивость к лекарственным препаратам — антибиотикам, сульфаниламидам и др., F-плазмиды, или половой фактор бактерий, определяющий их способность к конъюгации и образованию половых пилей, Ent-плазмиды, детерминирующие продукцию энтеротоксина.
Плазмиды могут определять вирулентность бактерий, например возбудителей чумы, столбняка, способность почвенных бактерий использовать необычные источники углерода, контролировать синтез белковых антибиотикоподобных веществ — бактериоцинов, детерминируемых плазмидами бактериоциногении, и т. д. Существование множества других плазмид у микроорганизмов позволяет полагать, что аналогичные структуры широко распространены у самых разнообразных микроорганизмов.
Плазмиды подвержены рекомбинациям, мутациям, могут быть элиминированы (удалены) из бактерий, что, однако, не влияет на их основные свойства. Плазмиды являются удобной моделью для экспериментов по искусственной реконструкции генетического материала, широко используются в генетической инженерии для получения рекомбинантных штаммов. Благодаря быстрому самокопированию и возможности конъюгационной передачи плазмид внутри вида, между видами или даже родами плазмиды играют важную роль в эволюции бактерий.
Полимеразная цепная реакция позволяет обнаружить микроб в исследуемом материале (воде, продуктах, материале от больного) по наличию в нем ДНК микроба без выделения последнего в чистую культуру.
Для проведения этой реакции из исследуемого материала выделяют ДНК, в которой определяют наличие специфичного для данного микроба гена. Обнаружение гена осуществляют его накоплением. Для этого необходимо иметь праймеры комплементарного З'-концам ДНК. исходного гена. Накопление (амплификация) гена выполняется следующим образом. Выделенную из исследуемого материала ДНК нагревают. При этом ДНК распадается на 2 нити. Добавляют праймеры. Смесь ДНК и праймеров охлаждают. При этом праймеры, при наличии в смеси ДНК искомого гена, связываются с его комплементарными участками. Затем к смеси ДНК и праймера добавляют ДНК-полимеразу и нуклеотиды. Устанавливают температуру, оптимальную для функционирования ДНК-полимеразы. В этих условиях, в случае комплементарное™ ДНК гена и праймера, происходит присоединение нуклеотидов к З'-концам праймеров, в результате чего синтезируются две копии гена. После этого цикл повторяется снова, при этом количество ДНК гена будет увеличиваться каждый раз вдвое. Проводят реакцию в специальных приборах — амплификаторах. ПЦР применяется для диагностики вирусных и бактериальных инфекций.
43. Генетика вирусов. Внутривидовой и межвидовой обмен генетическим материалом.
Геном вирусов имеет простое строение и малую молекулярную массу. Число генов у вирусов колеблется от 4—6 (парвовирусы) до 150 генов и больше (вирус оспы). В основе изменчивости вирусов лежат мутации. Мутации носят случайный характер или могут быть направленными. Вирус, являясь облигатным внутриклеточным паразитом, реализует этот паразитизм на генетическом уровне. Присутствие нескольких типов вирусов в инфицированных клетках, т.е. смешанная инфекция, может приводить к таким генетическим взаимодействиям между ними, как множественная реактивация, рекомбинация, кросс-реактивация и др.; могут иметь место и не генетические взаимодействия — комплементация и др.
Множественная реактивация — процесс взаимодействия вирусов с поражением разных генов, в результате которого взаимодействующие вирионы дополняют друг друга благодаря генетической рекомбинации, образуя неповрежденный вирус. Рекомбинация — обмен генетическим материалом между вирусами — возможна в виде обмена генами (межгенная рекомбинация) или участками одного и того же гена (внутригенная рекомбинация). У вирусов рекомбинация происходит в процессе заражения двумя или более типами вирусов, отличающимися друг от друга по генетическим признакам. Вариантом рекомбинации является перекрестная реактивация, или кросс-реактивация, происходящая в том случае, когда у одного из штаммов вируса часть генома повреждена, а другой геном нормальный. При смешанной инфекции двумя такими вирусами в результате рекомбинации появляются штаммы вируса со свойствами родительских микроорганизмов.
В качестве примера негенетического взаимодействия вирусов может быть приведена комплементация: при смешанной инфекции стимулируется репродукция обоих участников взаимодействия или одного из них без изменения генотипов вирусов. Комплементация широко распространена среди вирусов и наблюдается между как родственными, так и неродственными вирусами. Обмен генетическим материалом при этом феномене не наблюдается.
Если геном одного вируса заключен в капсид другого вируса, этот феномен называется фенотипическим смешиванием, наблюдаемым при смешанной инфекции.
Возможны также генетические взаимодействия неродственных вирусов, изучаемые генетической инженерией.
Изучение генетики микроорганизмов не только имеет важное биологическое значение, но и способствует решению многих медицинских проблем, таких, как разработка патогенетических основ лечения и профилактики инфекционных болезней, способов диагностики (полимеразная цепная реакция, ДНК-зонды), создание профилактических, лечебных и диагностических препаратов.
44. Основные группы антимикробных химиопрепаратов, применяемых в терапии и профилактики инфекционных болезней.
В 1932 г. Г. Домагк синтезировал первый сульфаниламидный препарат — стрептоцид, явившийся родоначальником многочисленной группы сульфаниламидных соединений(табл. 8.1), к которым чувствительны ряд грамположительных и грамотрицательных бактерий, прежде всего пиогенные стрептококки, менингококки, гонококки, кишечная палочка и др.
Изучение механизма антибактериального действия сульфаниламидов привело к открытию антиметаболитов— соединений, имеющихьструктурное сходство с важнейшими метаболитами, участвующими в анаболических или катаболических реакциях. Включение антиметаболита в эти реакции приводит соответствующие бактерии к задержке размножения и последующей гибели. Сульфаниламиды оказывают бактериостатическое действие.
Помимо сульфаниламидов, к антиметаболитам относятся аналоги изоникотиновой кислоты, азотистых оснований и других соединений.
Однако антиметаболиты нашли сравнительно ограниченное применение в химиотерапии инфекционных заболеваний.
Это объясняется однотипностью многих биохимических реакций, протекающих в клетках бактерий и человека, поэтому один и тот же антиметаболит блокирует образование продуктов, необходимых для жизнедеятельности микробов и определенных клеток организма человека.
К препаратам, блокирующим процессы репликации и транскрипции относится группа хинолонов.
К препаратам, нарушающим энергетический метаболизм, относятся производные оксихинолина.
Из производных тиосемикарбазона применяется фарингосепт, обладающий бактериостатической активностью в отношении пиогенного стрептококка и других гемолитических стрептококков, встречающихся на миндалинах при ангинах, а также в полости рта при гингивитах и стоматитах.
45. Антибиотики. Классификация. Механизмы действия антибактериальных препаратов на микробы.
Антибиотики — химиотерапевтические вещества, продуцируемые микроорганизмами, животными клетками, растениями, а также их производные и синтетические продукты, которые обладают избирательной способностью угнетать и задерживать рост микроорганизмов, а также подавлять развитие злокачественных новообразований.
За тот период, который прошел со времени открытия П.Эрлиха, было получено более 10 000 различных антибиотиков, поэтому важной проблемой являлась систематизация этих препаратов. В настоящее время существуют различные классификации антибиотиков, однако ни одна из них не является общепринятой.
Читайте также:

