Воздействие лазерного излучения на вирусы
Обновлено: 24.04.2024
О.Р. ШАНГИНА, Р.Д. ГАЙНУТДИНОВА
Всероссийский центр глазной и пластической хирургии МЗ РФ, г. Уфа
Контактная информация:
Шангина Ольга Ратмировна – заместитель Генерального директора, заведующая лабораторией консервации тканей, профессор
В статье представлен обзор данных литературы о медико-биологическом применении лазеров. Кроме того, разработана и предложена для внедрения в практику тканевых банков новая технология лазерного моделирования соединительнотканных трансплантатов, позволяющая сохранять их структуру и биомеханические свойства.
Ключевые слова: лазерное излучение, тепловые эффекты, связанные с взаимодействием между лазером и биологической тканью, лазеркоагуляция, лазерное моделирование.
O.R. SHANGINA, R.D. GAYNUTDINOVA
Russian Eye and Plastic Surgery Center, Ufa, the Republic of Bashkortostan, Russian Federation
Interaction of laser radiation with biological tissues
Contact details:
Shangina O.R. – Deputy General Director, Head of Tissue Conservation Laboratory, Doctor of Biological Sciences, Professor
The article presents a review of literature data on the biomedical application of lasers. In addition, a new technology for laser modeling of connective tissue grafts has been developed and proposed for introduction into the practice of tissue banks, which allows preserving their structure and biomechanical properties.
Key words: laser radiation, thermal effects associated with interaction between laser and biological tissueы, laser coagulation, laser modeling.
Уникальная способность лазера максимально концентрировать энергию в пространстве, во времени и в спектральном диапазоне делают этот прибор незаменимым средством во многих областях человеческой деятельности, и в частности в медицине [1]. Невозможно представить современную хирургию без лазерных скальпелей, с помощью которых проводят практически бескровные операции. Сфера применения лазерного излучения в медицине выходит далеко за пределы классических понятий о лазере как инструменте – заменителе скальпеля [2, 3].
Одно из направлений медико-биологического применения лазеров – использование их в качестве инструмента воздействия на биологические объекты. Можно выделить три типа такого воздействия. Первый тип – воздействие на ткани патологического очага импульсным или непрерывным лазерным излучением. Этому типу воздействия соответствует применение лазеров в дерматологии и онкологии для облучения патологических тканевых образований, которое приводит к их коагуляции. Второй тип – рассечение тканей, когда под влиянием излучения лазера непрерывного или импульсного действия часть ткани испаряется, и в ней возникает дефект. В этом случае плотность мощности излучения может превосходить используемую при коагуляции на два порядка (10 7 Вт/м 2 ) и более. Этому типу воздействия соответствует применение лазеров в хирургии. Третий тип – влияние на ткани и органы низкоэнергетического излучения (единицы или десятки ватт на квадратный метр), обычно не вызывающего явных морфологических изменений, но приводящего к определенным биохимическим и физиологическим сдвигам в организме, то есть воздействие физиотерапевтического типа. К этому типу следует отнести применение гелий-неонового лазера с целью биостимуляции при вяло текущих раневых процессах, трофических язвах и др. [4, 5, 6, 7]. Конечный фотобиологический эффект лазерного облучения проявляется ответной реакцией организма в целом, комплексным реагированием органов и систем. При лазерной терапии многими авторами отмечаются десенсибилизирующий, гипохолестеринемический эффекты, повышение активности общих и местных факторов иммунной защиты. В зависимости от длины волны лазерного облучения появляются бактерицидный или бактериостатический эффекты [8, 9, 10].
Сложность строения биологических объектов, разнообразие характера их взаимодействия со светом, обуславливают необходимость использования в хирургии большого количества разных типов лазеров и лазерных систем. Для повышения эффективности воздействия применяют разного рода фокусирующие устройства. Кроме того, существуют специальные насадки, позволяющие контролировать температуру в области взаимодействия [12].
С появлением новых областей применения лазерного излучения для обработки биологических тканей возникла острая необходимость выработки методик и критериев параметров лазерных излучателей. Для этих целей разрабатываются различные математические модели, призванные решить задачу оптимизации параметров лазерного излучателя и оценить результат, полученный при воздействии уже выбранным режимом на биологическую среду. При помощи модели, описывающей какой-либо конкретный процесс, на основе результата воздействия при определенных параметрах можно, последовательно изменяя исходные параметры, произвести оптимизацию спектральных и энергетических параметров лазерных излучателей для достижения необходимого в каждом конкретном случае нужного эффекта [13, 14, 15, 16, 17].
При выборе типа лазера либо лазерной системы должны учитываться оптические, термические и механические свойства биологической ткани. Лазерный луч, падая на ткань, может отражаться, рассеиваться и трансформироваться в другие виды энергии, и именно длина волны излучения определяет количественное соотношение между этими составляющими. Рассеянное отражение и рассеяние внутри ткани имеют место только для видимого и ближнего инфракрасного излучения, но не для среднего инфракрасного излучения. Инфракрасное излучение 10,6 мкм СО2-лазера имеет глубину проникновения от 1 до 20 мкм, в этом случае его рассеяние незначительно [5]. В этой области спектра излучение поглощается из-за возбуждения вращательного и колебательного состояния молекул. Посредством атомарного и молекулярного поглощения и последующей релаксации возбужденных частиц оптическая энергия преобразуется в тепловую энергию. Передаче возбуждения способствуют хромофоры ткани (молекулы, способные поглотить излучение и превратить его в тепло). Эффект воздействия зависит от соотношения целевых и конкурирующих хромофоров ткани. Целевыми для излучения СО2-лазера являются молекулы воды. Длина волны излучения этих лазеров позволяет достичь эффективного фотохимического испарения тканей, содержащих большое количество воды (эпителий, связки, мозг, мышцы). С другой стороны, энергия СО2-лазера плохо поглощается маловодными тканями (жировой, костной). В этих тканях происходит диффузное рассеяние энергии излучения, что приводит к ожогу или даже горению раньше, чем образуется кратер испарения. Данный факт может быть использован для удаления инфильтрата, сосредоточенного в объеме ткани, обедненного водой, который подвергается фотохимическому испарению излучением СО2-лазера [5, 19]. Высокое содержание воды в большинстве биологических тканей в значительной степени объясняет тот факт, что именно термический эффект имеет существенное значение в характеристике их повреждений, особенно при действии излучения в красной и инфракрасной областях спектра, так как поглощение в этой части спектра обусловлено практически полностью водой [20]. При плотностях потока излучения, превышающих указанные, происходит поглощение лазерной энергии молекулами воды, что приводит к их испарению и последующей коагуляции молекулы белка. Наблюдаемые при этом структурные изменения аналогичны результатам обычного термического воздействия. Однако лазерное излучение обеспечивает строгую локализацию поражения, чему способствует обводненность биообъекта и поглощение рассеивающейся энергии в пограничных с облучаемой областях. При импульсных термических воздействиях ввиду короткого времени воздействия и быстрого испарения воды наблюдается так называемый взрывной эффект: возникает выброс, состоящий из частиц ткани и паров воды [13].Известно, что фотофизические реакции обусловлены преимущественно нагреванием объекта до различной степени (в пределах 0,1–0,3 о С) и распространением тепла в биологических тканях. Разница температуры более выражена на биологических мембранах, что ведет к оттоку ионов Na+ и Ka+, раскрытию белковых каналов и увеличению транспорта молекул и ионов. Фотохимические реакции обусловлены возбуждением электронов в атомах поглощающего свет вещества. На молекулярном уровне это выражается в виде фотоионизации вещества, его восстановления или фотоокисления, фотодиссоциации молекул, в их перестройке – фотоизомеризации [18]. При взаимодействии лазерного излучения с биологическими тканями наблюдается целый ряд эффектов: термический (обусловленный селективным поглощением квантов света), возникновение волн сдавления и упругого удара в среде, действие мощных электромагнитных полей, сопровождающих в ряде случаев лазерное излучение, а также ряд других эффектов, обусловленных оптическими свойствами самой среды [3].
Эффективность лазерного моделирования соединительнотканных трансплантатов изучали и другие авторы [25]. Проведены исследования зоны лазерного реза трансплантатов, изготовленных из различных видов соединительной ткани: рыхлой волокнистой соединительной ткани (висцеральные оболочки внутренних органов, фасции), плотной неоформленной волокнистой соединительной ткани (дерма, твердая оболочка головного мозга), плотной оформленной волокнистой соединительной ткани (сухожилия различных локализаций). Анализ полученных данных показал следующее: у трансплантатов твердой мозговой оболочки и пяточного сухожилия в зоне лазерного реза происходит частичная гомогенизация пучков коллагеновых волокон, которая наиболее выражена у края трансплантата, то есть в зоне прохождения луча лазера. По мере отдаления от зоны реза степень гомогенезации пучков коллагеновых волокон уменьшается. Максимальная ширина зоны деструкции достигает 4 мкм. Подобная картина наблюдается и при исследовании трансплантатов дермы. У данных трансплантатов в зоне лазерного реза пучки коллагеновых волокон теряют структурную организацию и приобретают вид аморфной массы. Ширина зоны деструкции пучков коллагеновых волокон трансплантатов дермы достигает 5 мкм. У трансплантатов, изготовленных из фиброзной капсулы почки и глиссоновой капсулы печени, в зоне лазерного воздействия наблюдаются редкие очаги деструкции пучков коллагеновых волокон в виде набухания и частичной дезорганизации последних. Максимальная ширина таких очагов не превышает 1 мкм. В целом структурная организация в зоне лазерного реза у трансплантата фиброзной капсулы почки и глиссоновой капсулы печени не изменяется [25].
Обзор данных литературы по существующим на сегодняшний день результатам исследований воздействия лазера на биологическую ткань показал, что механизм воздействия до конца не выяснен. Опубликованных данных на эту тему не много. Таким образом, необходимо проведение дальнейших исследований по поиску оптимальных режимов лазерного излучения для повышения эффективности воздействия на биологические ткани.
Острые респираторные вирусные инфекции, знакомые всем как ОРВИ, – это инфекционное заболевание, вызываемое вирусами, передается воздушно-капельным путем и имеет массовое распространение. В простонародье его называют простудой. Причина заболевания: паравирусы, аденовирусы, риновирусы, респираторные коронавирусы и другие возбудители – насчитывается более 200 разновидностей вирусов. Провоцирующим фактором возникновения этих инфекций является переохлаждение. У заболевшего появляются и нарастают симптомы интоксикации: вялость, слабость, быстрая утомляемость, головная боль. В редких случаях, а особенно при отсутствии надлежащего лечения, появляются тошнота, рвота, судороги ног. Больных беспокоят боль в горле, мышцах, суставах, появляется осиплость голоса, затрудненное дыхание. И самое главное – подъем температуры тела. Если при ОРВИ все симптомы появляются и нарастают медленно, то для гриппа характерно бурное начало, резкий подъем температуры до высоких цифр, выраженная интоксикация. Правильное и адекватное лечение – залог успеха. В комплексной терапии и профилактике вирусных инфекций успешно применяется лазеролечение.
В течение последних 50 лет лазерная терапия (ЛТ) зарекомендовала себя как эффективный метод лечения и профилактики широкого круга заболеваний, включая вирусные инфекции. Метод направлен на повышение неспецифического иммунитета, повышение резистентности организма, и непосредственное локальное воздействие на органы, наиболее подверженные патологическому воздействию при вирусных инфекциях (Шамов В.Б., 2001). Эффективным средством профилактики вирусных инфекций в предэпидемический и эпидемический период является курс лазерной терапии с помощью аппаратов РИКТА. Наиболее часто проводят общесоматическую стимуляцию по В.И. Корепанову. Данная схема является общестимулирующей, укрепляющей, иммунокорригирующей, усиливающей любые другие методы воздействия.
На рисунке ниже приведена схема общесоматической стимуляции с использованием излучателя Т1 или излучателя Т2 аппаратов РИКТА.
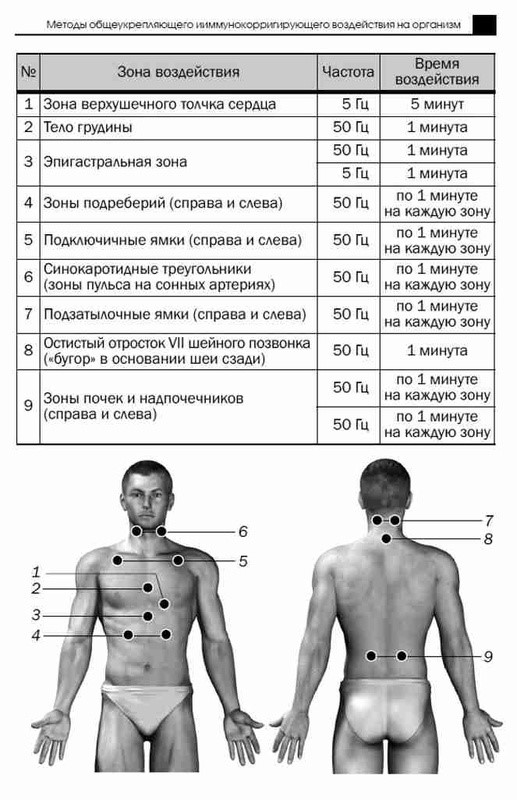
Общесоматическая стимуляция может проводиться и с помощью излучателя ДУШ 1. Воздействие проводится сканирующими движениями со скоростью 1 см в секунду, весь сеанс длится 15 минут. Реакция организма на лазерное воздействие является интегральной системной реакцией, включающей изменения на уровне клеток, тканей и органов и управляющих систем организма. Ответное реагирование организма может выражаться в следующем: - противовоспалительное действиe (активация микроциркуляции, изменение уровня РG, выравнивание осмотического давления, снижение отечности тканей, реактивация СОД и каталазы, снижение ПОЛ); - анальгезирующее действие (активация метаболизма нейронов, понижение порога болевой чувствительности); - стимуляция репаративных процессов (накопление АТФ, активизация метаболизма клеток, пролиферация фибробластов, эпителизация дефекта, синтез белка и калогена, быстрая васкуляризация за счет капилляров); - стимуляция иммунного ответа (усиление пролиферации иммунокомпетентных клеток, ускорение их созревания, увеличение продукции иммуноглобулинов); - рефлексогенное воздействие на функциональную активность различных органов и систем (раздражение нервных окончаний, возбуждение нервных центров, стимуляция биологических функций).
Важным средством профилактики вирусных инфекций является надвенное лазерное облучение крови (НЛОК). Данная методика рекомендуется в предэпидемический и в эпидемический период. НЛОК способствует повышению продукции интерферонов, относящихся к биорегуляторам с широким спектром биологического действия, повышению фагоцитарной активности макрофагов – клеток, которые пожирают зловредные микроорганизмы в крови. В организме интерферон продуцируется лейкоцитами крови в ответ на добавление вирусного или невирусного индуктора. Лазерное излучение является активным индуктором интерферона, причем, наиболее важное значение имеет эндогенный интерферон, у которого спектр свойств значительно шире. Исследователи отмечают, что максимальные показатели интерферона при однократном лазерном воздействии на кровь наблюдаются на 2-е сутки. Таким образом, НЛОК можно считать самостоятельным методом профилактики вирусных инфекций.
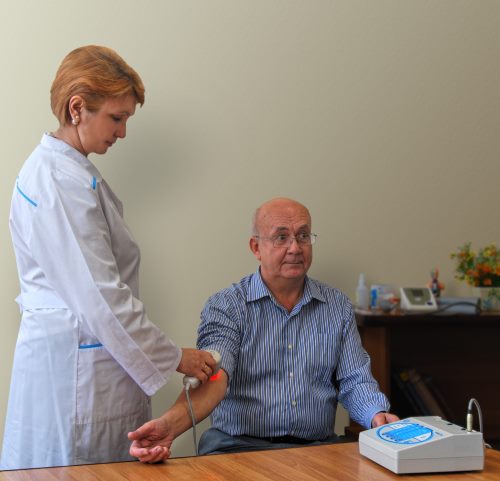
Методика проведения НЛОК: Излучателем Т1или Т2: НЛОК проводится на одну из пар симметричных зон, над крупными сосудистыми пучками (локтевые, подколенные, паховые, зона сонных и бедренных артерий), на частоте 50 Гц, время воздействия по 10 минут с каждой стороны. Время сеанса у взрослых 20 минут. Профилактический курс состоит из 5 ежедневных сеансов. При необходимости повторный профилактический курс проводят через 5-7 дней.
При проведении методики НЛОК излучателем ДУШ 1 время воздействия уменьшается: на каждую вену до 2 минут, курс состоит из 5-7 сеансов, по 1 сеансу в день. С целью профилактики вирусных инфекций рекомендуется проводить курсы НЛОК 2 раза в год – весной и осенью или в период предполагаемой эпидемии или в период эпидемических вспышек.
Для ликвидации явлений воспаления при таких заболеваниях, как ринит, отит, тонзиллит, фарингит, ларингит рекомендуются протоколы лечения с использованием внутриполостных насадок.
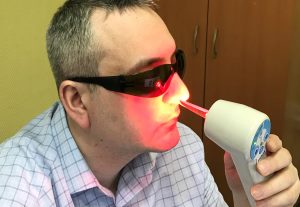
Лазерная терапия может использоваться как самостоятельный метод профилактики гриппа, так и в сочетании с медикаментозной терапией, гомеопатией, фитотерапией и физиотерапией.
- проводите профилактику и лечение вирусных инфекций аппаратами лазерной магнитно-инфракрасной терапии РИКТА;
- мойте руки с мылом, пользуйтесь одноразовыми спиртовыми салфетками для вытирания рук; - берегите окружающих
- пейте достаточно жидкости (не менее 1,5 литров в день, причем, если цвет мочи прозрачный – это говорит о том, что Вы принимаете достаточно жидкости, если цвет мочи насыщенно желтый – то Вы нуждаетесь в большем количестве жидкости);
- дышите свежим воздухом, проветривайте помещение, это позволит уменьшить концентрацию вирусов и снизить риск распространения инфекции;
- занимайтесь аэробными упражнениями, так как они способствуют ускорению обмена между легкими и кровеносной системой и при выполнении упражнений из организма с потом выводятся токсические вещества;
- употребляйте пищу, богатую витаминами (ешьте как можно больше темно-зеленых, красных и желтых овощей и фруктов), чаще пейте кисло-молочные напитки;
- посещайте сауну 1-2 раза в неделю, температура горячего воздуха в сауне более 80 градусов, при этой температуре вирусы погибают;
- расслабляйтесь (по 30 минут в день представляйте себе какой-нибудь приятный пейзаж), это повысит сопротивляемость организма к инфекциям;
ЛИТЕРАТУРА 1. Шамов В.Б. Грипп и другие ОРВИ. — Москва, 2001 2. Лазерная терапия и профилактика широкого круга заболеваний. Методическое пособие по применению аппарата лазерной терапии РИКТА® / под ред. к.м.н. Фёдорова Ю. Г. — 10-е изд., испр. и доп. — Москва, 2018. 3. Лазерная терапия и профилактика /под ред. А.В. Картелишева., А.Г. Румянцева, А.Р. Евстигнеева, А.В. Гейница, С.В. Усова. — Москва, 2012 – с. 326-327








Читайте также:

