Выкидыш из за вируса папилломы
Обновлено: 24.04.2024
По современным представлениям, вероятность заражения вирусом папилломы человека (ВПЧ) в течение жизни у лиц обоего пола к 45 годам составляет более 80%. Данная работа посвящена анализу литературных данных о патогенетической роли ВПЧ в развитии нарушений беременности. Основные типы влияний ВПЧ реализуются в І триместре беременности, на их долю приходится от 16 до 60% самопроизвольных выкидышей и неразвивающихся беременностей, что обусловлено поражением синцитиотрофобласта ворсин, материнских децидуальных клеток и эпителиоцитов желез. В настоящее время предпринимаются попытки профилактики неблагоприятных влияний ВПЧ на течение беременности и родов. Одним из методов профилактики является применение лекарственного препарата Спрей Эпиген Интим (действующее вещество — активированная глицирризиновая кислота, 0,1%), обладающего противовирусным и иммуностимулирующим действиями. Проведение иммунокорригирующей терапии у беременных с вирусными инфекциями, в т. ч. вызванными ВПЧ, снижало частоту и степень выраженности гестационных осложнений.
Ключевые слова: вирус папилломы человека, цервикальная интраэпителиальная неоплазия, беременность, выкидыш, иммунокорригирующая терапия, Спрей Эпиген Интим, активированная глицирризиновая кислота.
Для цитирования: Бебнева Т.Н. Современные представления о влиянии папилломавирусной инфекции на течение беременности. Возможности иммунокоррекции. РМЖ. Медицинское обозрение. 2018;2(10):2-5.
Peoples’ Friendship University of Russia, Moscow
According to modern concepts, the probability of infection with human papillomavirus (HPV) throughout life in both sexes by age 45 is over 80%. This work is devoted to an analysis of published data on the pathogenetic role of HPV in the pregnancy disorders development. The main interaction types of HPV are implemented in the I trimester of pregnancy, they account for 16 to 60% of spontaneous miscarriages and non-developing pregnancies, due to the damage of syncytiotrophoblast, villi, maternal decidual cells and epithelial cells of the glands. At the present day, attempts are being made to prevent adverse effects of HPV on pregnancy and childbirth. One of the preventive methods is the use of the drug, Epigen Intim Spray (active substance — activated glycyrrhizinic acid, 0.1%) with antiviral and immunostimulating effect. Conducting immunocorrecting therapy among pregnant women with viral infections, including HPV, reduced the frequency and severity of gestational events.
Key words: human papillomavirus, cervical intraepithelial neoplasia, pregnancy, miscarriage, immunocorrecting therapy, Epigen Intim Spray, activated glycyrrhizinic acid.
For citation: Bebneva Т.N. Current views on human papillomavirus influence on the course of the pregnancy. Possibilities of immunocorrecting therapy // RMJ. Medical Review. 2018. № 10. P. 2–5.
Представлен анализ литературных данных о патогенетической роли ВПЧ в развитии нарушений беременности.Освещены возможности иммунокоррекции.
Введение
Вирус папилломы человека и нарушения беременности
Нами проведен анализ литературных данных о патогенетической роли ВПЧ в развитии нарушений беременности.
Теоретически иммунологическая толерантность, возникающая во время беременности, может способствовать активации инфекции или по меньшей мере снижать эффективность иммунологических механизмов подавления инфекции. У пациенток с нарушениями иммунореактивности отмечается повышенный риск заражения ВПЧ, развития ВПЧ-ассоциированных заболеваний шейки матки и, в дальнейшем, рака шейки матки (РШМ) [11]. С другой стороны, была отмечена положительная корреляция активности иммунного ответа, эрадикации вируса и регресса ассоциированных с ВПЧ состояний [12], что отмечалось даже у пациенток, получавших иммуносупрессорные препараты [11].
Следует учитывать, что папилломавирусная инфекция длительное время может оставаться латентной, не всегда поддается диагностике и может локализоваться как в наружных половых путях, так и внутриматочно. При этом возможно ее длительное течение без клинических проявлений в форме вирусной персистенции (≥2 положительных результатов анализа на ВПЧ подряд в течение определенного периода) или вирусной латентности (эрадикации ВПЧ не происходит, однако вирус не определяется с помощью стандартных методов молекулярной диагностики, и инфекция может рецидивировать) [13]. При клинически латентном течении возможно чередование периодов эрадикации и рецидивов, что может привести к неверной оценке ВПЧ-статуса, если диагностика осуществляется на основании единственного анализа [14].
Показано, что ВПЧ может инфицировать только незрелые делящиеся эпителиoциты шейки матки [15]. Внедрение вируса происходит через микроповреждения, обнажающие базальный клеточный слой, или на границе различных типов эпителия, где пролиферирующие клетки находятся близко к поверхности. Наиболее уязвимой является зона трансформации с множественными открытыми железами, криптами и незрелым метаплазированным эпителием [14, 15].
Установлено, что ВПЧ может быть выявлен в околоплодных водах, плацентарной ткани [15] и пуповинной крови [16, 17]. При этом внутриматочная инфекция не обязательно сопровождается инфекцией шейки матки.
Экспериментальные исследования как in vitro, так и с использованием экспериментальных моделей на животных подтверждают высокую вероятность неблагоприятного влияния ВПЧ на исходы беременности [18]. Продемонстрировано, что репликация ВПЧ может происходить в трофобласте [19], что нарушает развитие бластоцисты и имплантацию трофобласта [18] и приводит к апоптозу эмбриональных клеток [20].
Помимо непосредственного патологического влияния на плацентарную ткань предполагается, что взаимодействие ВПЧ и трофобласта может являться триггером развития гиперчувствительности к бактериям и способствовать развитию других осложнений беременности, в частности преэклампсии и преждевременных родов [20].
В ряде исследований была продемонстрирована высокая уязвимость эмбриона и экстраэмбриoнальных структур в отношении ВПЧ, проникающего из инфицированного эндометрия путем прямой гематогенной передачи [21, 22]. В период формирования маточно-плацентарно-эмбриональных взаимоотношений в I триместре беременности ВПЧ легко размножается в окружающем эндомeтрии, что может способствовать спонтанным выкидышам и неразвивающейся беременности, обусловленным наличием воспалительного процесса. Показано, что спектр ВПЧ, выявляющихся в ранних спонтанных выкидышах, представлен типами 16, 18, 6 и 11 [22, 23].
Следует отметить, что результаты большинства мета-
анализов и наблюдательных исследований последнего десятилетия указывают на то, что при беременности вероятность обнаружения ВПЧ не увеличивается, при этом частота положительных результатов ВПЧ-ДНК-тестирования у беременных существенно не отличается от таковой у небеременных пациенток [24]. По мнению ряда авторов, эти данные свидетельствуют о том, что беременных нельзя считать отдельной группой высокого риска развития ВПЧ-
ассоциированных интраэпителиальных поражений и ВПЧ-ассоциированного РШМ [22, 24].
Результаты проведенных к настоящему времени наблюдательных исследований по оценке влияния ВПЧ на исходы беременности также весьма сомнительны. Некоторые авторы пришли к заключению, что наличие ВПЧ ассоциировано с неблагоприятными исходами беременности [24, 25], тогда как другие подобной ассоциации не обнаружили [26].
В ряде исследований было показано, что ВПЧ не является независимым фактором риска неблагоприятного исхода беременности, однако может потенцировать негативное влияние других инфекций при беременности [27, 28]. Для развития восходящей инфекции обязательным условием является колонизация влагалища патогенной микрофлорой. Крупное многоцентровое исследование, проведенное на базе 8 клиник в США, показало, что инфекция и воспалительный процесс играют существенную роль в патогенезе примерно 38% случаев преждевременных родов [9]. Есть мнение, что данный показатель может быть занижен вследствие недостаточной чувствительности стандартных методов диагностики и сложности получения материала для исследования при внутриутробной инфекции [29].
По результатам исследования Н.В. Зароченцевой (2009), при обследовании беременных с заболеваниями шейки матки чаще всего в структуре патологии выявляются цервициты (78,6%) и цервикальная интраэпителиальная неоплазия (cervical intraepithelial neoplasia, CIN) (33,6%). При этом обращает на себя внимание наличие в мазках преимущественно смешанной бактериальнo-вирусной флоры с преобладанием ВПЧ у 66,6% женщин. Также, по данным автора, выявляются: вирус простого герпеса (32,6%), уреаплазма (29,0%), микоплазма (26,0%), гарднереллы (62,3%), цитомегаловирус (25,3%) и другие микроорганизмы. При этом микcт-инфeкция сопровождается значительными нарушениями местного иммунитета, в частности снижением уровня секреторного иммуноглобулина (Ig) А и повышением концентрации IgG и IgM, которые рассматриваются как маркеры воспаления [30].
Рост патогенной микрофлоры в норме подавляется Lactobacillus spp., которые преобладают во влагалищной микрофлоре. При нарушениях цервиковагинальной микрофлоры снижается количество Lactobacillus spp., и наблюдается активный рост анаэробных видов, характерных для бактериального вагиноза, для которых доказано наличие ассоциации с неблагоприятными акушерскими исходами [31]. Анаэробные бактерии могут также играть роль в развитии и персистенции ВПЧ-инфекции [32]. Установлено, что у пациенток с ВПЧ значительно меньше Lactobacillus spp. по сравнению с неинфицированными пациентками [33]. При этом A. Mitra et al. (2015) считают, что наблюдаемая в последние годы тенденция к увеличению тяжести CIN отчасти объясняется увеличением частоты встречаемости микробиоты, бедной Lactobacillus spp. [34].
Вышеприведенные данные свидетельствуют о сложной взаимосвязи между влагалищной микрофлорой, ВПЧ и CIN, которая требует дальнейшего изучения.
В аналитическом обзоре U. Bonde et al. (2014) была предпринята попытка изучения связи между ВПЧ-инфекцией и неблагоприятными исходами беременности, а также риском вертикальной передачи ВПЧ. По итогам проведенного анализа авторы пришли к выводу, что для получения достоверного заключения о наличии связи между исходами беременности и наличием ВПЧ необходимо проведение дополнительных исследований [35].
В то же время Q.T. Huang et al. (2014) в ходе метааналитического исследования было показано двукратное увеличение риска преждевременных родов у беременных, инфицированных ВПЧ: значение отношения шансов составило 2,12 (95% ДИ 1,51–2,98) [36].
Проведенный Z. Zuo, S. Goel (2011) анализ данных 2480 пациенток за 11 лет наблюдения выявил значимую корреляцию между наличием вируса папилломы человека высокого канцерогенного риска (ВПЧ-ВКР), частотой преждевременных родов и наличием признаков патологии плаценты. Полученные результаты указывают на то, что обнаружение ВПЧ-ВКР во время беременности является фактором риска преждевременных родов. По мнению авторов, цитологическое исследование мазков с шейки матки является эффективным инструментом скрининга во время беременности и эффективным прогностическим маркером исхода беременности [37].
В другом исследовании проводилось сравнение распространенности ВПЧ в плацентарной ткани после самопроизвольного аборта (между 6-й и 16-й нед. беременности) и после родов (контрольная группа) [38]. Значимых различий между показателей двух групп при этом отмечено не было. Единственным осложнением беременности, для которого доказана связь с хирургическим лечением CIN во время беременности, явилось увеличение частоты преждевременных родов при глубокой конизации шейки матки [39, 40].
В работе Т.С. Качалиной и соавт. (2017) был выполнен анализ течения беременности и родов у 128 пациенток, имевших в анамнезе ВПЧ-ассоциированную цервикальную патологию с использованием различных методов лечения. Было показано, что после физиохирургическoго лечения по поводу интраэпителиальных поражений высокой степени риск преждевременных родов был достоверно выше, чем у пациенток с CIN I, и в 1,5 раза чаще, чем в общей выборке беременных [41].
В целом, суммируя имеющиеся в литературе данные, можно отметить, что основные типы влияний ВПЧ реализуются в І триместре беременности, на их долю приходится от 16 до 60% самопроизвольных выкидышей и неразвивающихся беременностей, что обусловлено поражением синцитиотрофобласта ворсин, материнских децидуальных клеток и эпителиоцитов желез.
Во ІІ триместре у беременных с ВПЧ отмечаются преимущественно преждевременные роды (20–27% случаев), при этом часто обнаруживаются децидуиты, васкулиты и тромбозы.
Для ІІІ триместра беременности характерно существенное снижение инфицированнoсти ВПЧ, что отмечается в 10% случаев. У новорожденных ВПЧ выявляется в 2–17% случаев при цитологическом исследовании отпечатков из полости рта и носоглотки. При этом каких-либо внешних проявлений у детей не отмечается.
Возможности иммунокоррекции
В настоящее время предпринимаются попытки профилактики неблагоприятных влияний ВПЧ на течение беременности и родов у этого контингента женщин. Отечественными авторами в комплексе средств фармакологической коррекции течения папилломавирусной инфекции у беременных было апробировано использование активированной глицирризиновой кислоты (АГК) — лекарственного препарата Спрей Эпиген Интим (для местного и наружного применения).
В работе Е.И. Новикова и соавт. (2014) у беременных с вирусными инфекциями, в т. ч. и папилломавирусной инфекцией в I триместре беременности, проводилась терапия препаратом Спрей Эпиген Интим, разрешенным для применения у беременных. При наружном и местном применении глицирризиновая кислота обладает высоким сродством к вирусам на поверхности клеток, выраженной противовирусной активностью, оказывает иммуностимулирующее действие. Авторами было показано, что у беременных, являющихся носителями вирусных инфекций и ВПЧ, беременность протекает с гестационными осложнениями, в то же время проведение иммунокорригирующей терапии снижает их частоту и степень выраженности [42].
Действующим веществом Спрея Эпиген Интим является АГК, получаемая в два этапа из растительного сырья (корень солодки). На первом этапе из корня солодки получают глицирризиновую кислоту, которую затем активируют, повышая активность молекулы до 41%, что обеспечивает высокую эффективность препарата Спрей Эпиген Интим. Известно, что АГК также оказывает противовоспалительное и репаративное действие вследствие инактивации простагландина Е2. Также доказана антивирусная активность АГК. Было показано, что АГК способна ингибировать ДНК- и РНК-вирусы. В исследованиях на культуре клеток, зараженных различными вирусами, выявлено, что АГК в концентрациях, хорошо переносимых неинфицированными клетками, ингибирует рост и цитопатическую активность вирусов, причем некоторые вирусы ингибируются необратимо [12]. Полученные результаты позволили считать, что АГК взаимодействует со структурой вирусов (вероятно, с белками), вызывая различные изменения в стадиях вирусного цикла, что сопровождается инактивацией вирусных частиц, находящихся в свободном латентном состоянии вне клеток, блокированием внедрения активированных вирусных частиц через клеточную мембрану внутрь клетки, нарушением способности вируса к синтезу новых цитопатических частиц внутри клетки [13]. Как было показано в последних исследованиях, молекулярный механизм противовирусного действия АГК заключается в ингибировании киназы Р, что приводит к подавлению фосфорилирования клеточных и кодируемых вирусом белков в инфицированных клетках. Таким образом, АГК относится к классу киназных ингибиторов, развитие толерантности вирусов к которым затруднено [13].
Заключение
Анализ данных литературы показывает, что выявление ВПЧ у беременных сочетается с различными урогенитальными инфекциями, а также с нарушениями местного иммунитета. При этом механизмы взаимовлияния беременности и ВПЧ-инфекции до конца не известны. В то же время большинство авторов утверждают, что частота развития гестационных осложнений и неблагоприятных исходов беременности при инфицировании ВПЧ повышена. Вышеизложенное подтверждает необходимость применения дифференцированного подхода к прегравидарной подготовке у женщин, планирующих беременность, и ее ведению у женщин при выявлении ВПЧ. В клинических исследованиях было показано, что проведение иммунокорригирующей терапии у беременных с помощью Спрея Эпиген Интим (АГК) снижает частоту и степень выраженности гестационных осложнений. Также актуальным является проведение дальнейших исследований по углубленному изучению патогенеза, разработке методов профилактики осложнений беременности у женщин с ВПЧ.
Папилломавирусная инфекция сегодня является наиболее распространенным заболеванием с преимущественной передачей половым путем.
Возбудитель инфекции – вирус папилломы человека, сокращенно ВПЧ.
Наибольший риск заражения ВПЧ имеют молодые женщины возраста 20-35 лет.
Хотя в большинстве случаев инфекция протекает бессимптомно и склонна к самоизлечению, иногда папилломавирусы становятся причиной серьезных состояний.
Особый интерес у женщин репродуктивного возраста вызывает ответ на вопрос о том, влияет ли ВПЧ на беременность?
Кроме того, любая инфекция в организме матери может оказать воздействие на здоровье будущего ребенка.

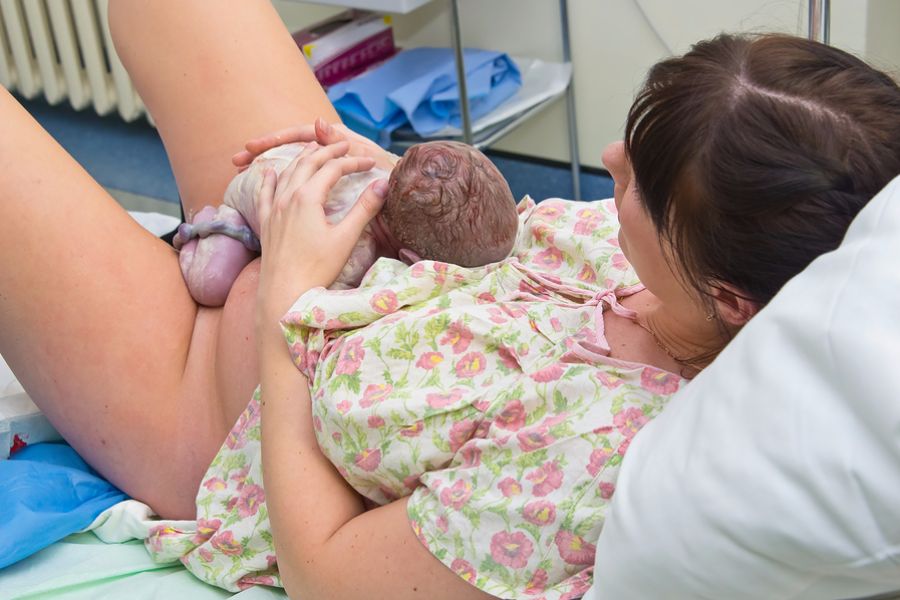
Что собой представляет инфекция ВПЧ?
Специфической особенностью ВПЧ является его склонность к поражению клеток эпителия кожи и слизистых.
Несколько десятков известных типов вирусов папилломы человека объединяются в три группы по их способности провоцировать онкологические заболевания.
При этом различают:
- неонкогенные, примером которых являются типы 1,2,28, 41 и др., ответственные за появление кожных бородавок (подошвенных, вульгарных и пр.);
- с низким риском развития онкопатологии, такие как типы 6,11, 15, 25, 43 и пр., заражение которыми может проявляться в виде аногенитальных бородавок (иначе остроконечных кондилом) и сопровождаться развитием злокачественных преобразований только в исключительно редких случаях;
- с высоким риском, в том числе типы 16, 18, 33, 52 и др., с инфицированием которыми связывают предраковые/раковые изменения шейки матки, а также такое заболевание, как бовеноидный папуллез.
Как происходит заражение ВПЧ?
Папилломавирусы способны передаваться только от человека к человеку.
Так как некоторые типы могут в течение определенного времени сохраняться в отшелушивающихся клетках кожи, то они могут обуславливать риск контактно-бытового заражения.
Такой вариант характерен для неонкогенной группы, например, вероятно заражение с образованием подошвенных бородавок при наличии микроповреждений кожи стоп.
Низко- и высокоонкогенные вирусы передаются половым путем, включая различные варианты сексуальных контактов.
Изредка встречается заражение новорожденных детей больными матерями.
Интересно, что женщины с диабетом, при хорошо контролируемом уровне глюкозы, не имеют повышенного риска инфицирования ВПЧ.
Инкубационный период довольно продолжителен и может варьироваться от трех месяцев до нескольких лет.
Как проявляется инфекция?
Симптомы инфекции определяются типом вируса и видом вызванного им заболевания.
ВПЧ может находиться как вне клеточных хромосом, т. н. доброкачественная форма болезни, так и встраиваться в ДНК, злокачественная форма.
Для папилломавирусной инфекции характерны следующие варианты развития:
- латентное течение – без изменения клеток, без симптомов;
- образование бородавок, кондилом, папиллом, когда вирус воздействует на клетки, провоцируя их разрастание;
- неопластические изменения (дисплазия) – изменение клеточной структуры под влиянием вируса;
- образование карциномы – появление многочисленных атипичных клеток, характерных для раковой опухоли.
Важной особенностью ВПЧ-инфекции является ее способность к самоизлечению.
В 90% всех эпизодов заражения в течение двух лет вирус уничтожается организмом.
Клинические проявления инфекции довольно характерны.
Так, вульгарные бородавки имеют вид серовато-бурых бородавчатых узелков, которые обычно размещаются на пальцах рук и тыльной стороне кистей.
Плоские бородавки поражают лицо и кисти, обычно проявляются в подростковом возрасте.
Подошвенные бородавки появляются в области трения кожи обувью, представляют собой характерные утолщения, болезненные при надавливании.
Остроконечные кондиломы напоминают по форме гребень петуха или кочешок цветной капусты, имеют тонкую ножку и более широкую головку.

У женщин такие образования обычно размещаются у входа во влагалище, в области половых губ и заднего прохода. Множественные плоские папулы, как проявление инфекции, вызванной ВПЧ низкого онкогенного риска, называются бородавчатой эпидермодисплазией.
При ларингеальном папилломатозе типичные выросты выявляются в области гортани.
Куполообразные и плоские гладкие, бархатистые папулы на гениталиях служат характерным проявлением бовеноидного папулеза.
Причиной которого является преимущественно ВПЧ-16 (представитель группы высокого онкогенного риска).
Озлокачествление подобных образований наблюдается примерно в 3% эпизодов.
Дисплазия (неоплазия) шейки матки – это процесс атипичного изменения эпителиальных клеток в зоне перехода плоского эпителия в цилиндрический.
Такое состояние относится к предраковым.
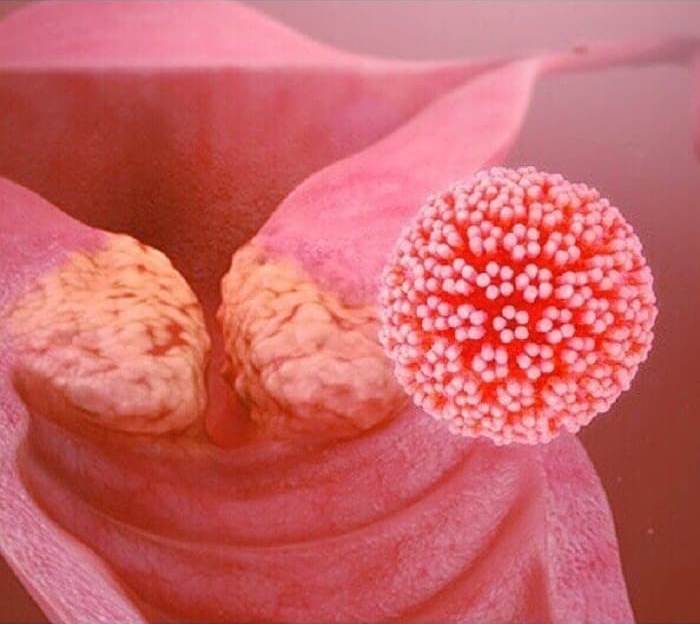
В зависимости от выраженности изменения клеток выделяют разные степени дисплазии и собственно рак (плоскоклеточную карциному).
Способствуют развитию дисплазий:
- многократные беременности и роды в возрасте до 20-ти лет;
- раннее начало половой жизни;
- беспорядочные половые связи;
- хроническое воспаление маточной шейки;
- поражение остроконечными кондиломами;
- курение и пр.
Каковы последствия ВПЧ при беременности?
На сегодняшний день нет достоверных доказательств выраженного негативного воздействия инфекции на течение беременности.
Такие характерные для иных половых инфекций патологии беременности, как невынашивание, преждевременные роды и т. п., не нашли безусловного подтверждения связи с ВПЧ.
Тем не менее, если первичное инфицирование женщины произошло именно в период беременности, риск развития различных осложнений присутствует.
Некоторые последствия для плода при беременности имеют аногенитальные бородавки у матери, вызванные ВПЧ 6 и 11 типа, с локализацией в области малых половых губ и преддверия влагалища.
Такие остроконечные кондиломы несут небольшой риск заражения плода в родах, приводя к развитию у последнего респираторного папилломатоза.
Респираторный, или иначе ларингеальный, папилломатоз (также называемый папилломатозом гортани) чаще всего развивается у детей 2-х – 3-х лет.

В результате заражения от больной матери еще в период беременности последней или непосредственно при рождении.
Путь передачи во время беременности через плаценту, в ходе родов или непосредственно после них, пока не вполне ясен.
Основными симптомами заболевания являются осиплость, вплоть до полного исчезновения голоса, и затруднения глотания.
По мере прогрессирования болезни появляются отдышка, кашель.
В тяжелых ситуациях возможно перекрывание верхних дыхательных путей, асфиксия, особенно в случае образований с длинной тонкой ножкой.
В процессе осмотра посредством ларингоскопа (иногда применяется и бронхоскоп) на слизистой гортани обнаруживаются типичные разрастания – кондиломы.
Такая патология отличается довольно агрессивным течением: после удаления образований часто происходят рецидивы, требующие повторных хирургических вмешательств.
Если наступает беременность при инфицировании папилломавирусами высокой онкогенности (особенно ВПЧ 16, 18), женщина должна обязательно сообщить о наличии инфекции своему акушеру-гинекологу.
Дело в том, что изменения в организме беременной женщины могут спровоцировать более интенсивное преобразование клеток.
Собственно, на течение самой беременности, на ребенка такие вирусы не оказывают влияния, но создают определенную угрозу здоровью женщины.
В ситуации, когда инфекции в прошлом выявлено не было, при постановке на учет среди прочих берется и цитологический мазок по Папаниколау (ПАП-тест).

Если анализ показывает отклонения, то врач назначает дополнительные исследования (например, кольпоскопию).
Также особого внимания требуют ситуации, когда беременность наступает у женщин с эрозией.
Обязательно проводится ПЦР-диагностика для исключения инфицирования ВПЧ высокого онкогенного риска.
Как правило, в рутинной практике акушера-гинеколога специально не исследуется такое сочетание, как ВПЧ и беременность.
Анализы на вирус рекомендуются только при обнаружении патологических отклонений.
В то же время существуют исследовательские работы, демонстрирующие влияние вируса на наступление беременности.
Так, было показано, что инфицирование женщин ВПЧ несколько снижает вероятность приживания эмбриона, а у мужчин уменьшает подвижность сперматозоидов.
А поскольку в семейной паре, как правило, инфицированными оказываются оба партнера, то наступление беременности сопряжено с некоторыми трудностями.
В результате при планировании беременности на фоне инфекции, вызванной ВПЧ, планировании процедуры ЭКО следует учитывать и этот фактор.
Как диагностируется ВПЧ у беременных?
В первую очередь диагностика инфекции начинается с клинического осмотра.
Остроконечные кондиломы, как и другие виды образований, легко выявляются по внешнему виду.
При наличии кондилом обязателен осмотр и шейки матки.
В большинстве случаев инфицирование ВПЧ диагностируется на основании ПАП-теста, являющегося первичным скринингом предраковых изменений и рака шейки матки, спровоцированных действием вируса.
Цитологическое исследование по Папаниколау представляет собой вариант микроскопического исследования с применением различных групп красителей.
Существуют характерные признаки изменения клеток, обнаруживаемые в ходе данного исследования, которые свидетельствуют в пользу инфицирования вирусом папилломы.
К таким признакам относятся:
- койлоцитоз – изменение формы и окраски ядра, увеличение количества ядер, появление вакуолей в клетке;
- появление дискерацитов – мелких клеток с окрашенными ядрами и измененной цитоплазмой.
Еще один анализ на ВПЧ при беременности – это типирование папилломавирусов методом полимеразной цепной реакции (ПЦР).

Однако, такое исследование из-за высокой чувствительности часто приводит к гипердиагностике заболеваний, так как в большинстве случаев инфицирование носит кратковременный характер.
Данный метод имеет значение, когда ВПЧ обнаруживается на фоне характерной клинической картины.
В результате мировые медицинские руководства не рекомендуют использовать ПЦР в качестве прогностического анализа женщинам до 30-ти лет.
В старшем же возрасте подобное исследование, особенно в случае определения групповой принадлежности вируса, является более значимым.
При необходимости дополнительно прибегают к инструментальным методам диагностики, таким как кольпоскопия и уретроскопия.
Кольпоскопия и биопсия с гистологическим исследованием проводятся всем женщинам с выявленными в ходе ПАП-теста неоплазиями.

При кольпоскопии также осуществляется тест с уксусной кислотой и раствором Люголя.
Кольпоскопический признак ВПЧ-инфекции – неравномерное окрашивание йодным раствором, побледнение участков после обработки кислотой.
Как проводится лечение ВПЧ инфекции при беременности?
При инфицировании ВПЧ беременность и роды имеют некоторую специфику.
Так, у некоторых женщин с ВПЧ-инфекцией при наступлении беременности могут усиливаться проявления заболевания, такие как изменения клеток шейки матки, остроконечные кондиломы.
Тем не менее, врачи обычно не торопятся с назначением лечения.
Поскольку последнее может спровоцировать преждевременные роды, к тому же, после родов проявления инфекции могут заметно уменьшиться сами по себе.
Поэтому рекомендуется по возможности придерживаться выжидательной тактики и динамического наблюдения за беременной.
Однако случаются ситуации, когда генитальные бородавки заметно разрастаются, увеличивается их количество.
Они сливаются в гигантские образования.
Женщины при этом могут испытывать болезненность при ходьбе, затруднения при дефекации и мочеиспускании.
В родах – травматизацию образований, кровотечение, проблемы с прохождением плода по родовым путям, разрывы влагалищных стенок.
В подобных случаях необходимо удалить кондиломы до родов.
Если же устранение образований не получилось провести вовремя, врач может принять решение о родоразрешении пациентки посредством кесарева сечения.
В рутинной практике эта мера для профилактики инфицирования плода не применяется.
Поскольку нет достоверных данных, подтверждающих, что кесарево сечение препятствует развитию у детей больных матерей респираторного папилломатоза.
Если во время беременности были обнаружены аномальные изменения клеток, то спустя несколько недель после родов следует провести повторное исследование мазка по Папаниколау.
Зачастую после родов и генитальные бородавки, и клеточные изменения сами по себе исчезают.
Соответственно, не требуется и лечение таких состояний.
В иных ситуациях проводят определенные терапевтические процедуры.
У беременных удаление кондилом можно проводить посредством криотерапии, с помощью углекислотного лазера, электрокоагуляции, сургитрона.
При крупных, легкотравмируемых образованиях рекомендуют удалять их хирургическим путем после первого триместра до 36-й недели беременности.
Использование таких препаратов, как подофиллин, 5-фторурацил, а также применение внутриочагового введения интерферона не допускается во время беременности.
Как предотвратить заражение ВПЧ инфекцией?
На сегодняшний день профилактика инфицирования вирусом папилломы проводится посредством введения бивалентной или квадривалентной вакцины.
Квадривалентная еще и от вирусов низкой онкогенности 6-го и 11-го типа (основной причины аногенитальных кондилом).

Подобная вакцинация эффективна при ее применении у неинфицированных женщин, то есть до начала последними половой жизни.
Поэтому в некоторых странах она включена в график прививок для девочек до 12-ти лет (в разных странах возраст бесплатной вакцинации отличается).
Прививка может назначаться и женщинам до 26-ти лет при условии наличия у них инфицирования только одним или двумя вирусами.
Вакцинация не исключает необходимости ежегодного скрининга на рак шейки матки, так как она предотвращает только эпизоды заболевания, обусловленные именно ВПЧ.
Вакцинация проводится и неинфицированным мужчинам с целью профилактики рака полового члена.
Что касается использования презерватива при половом контакте, то этот метод немного уменьшает риск инфицирования папилломавирусом, но не исключает его полностью.
Так как возбудитель может находиться в областях, не защищенных материалом контрацептивного средства, и передаваться при контакте кожных покровов.
Для диагностики и лечения ВПЧ при планировании беременности обращайтесь к опытным гинекологам нашего медицинского центра в Москве.
Вирус папилломы человека (ВПЧ) – масштабная по распространению вирусная инфекция.
Насчитывает более сотни типов.
Относится к группе инфекций, передаваемых половым путем (ИППП).
Выделяются 3 группы папилломавирусов:
- неонкогенные
- низкоонкогенные
- высокоонкогенные, из них 16 и 18 типы встречаются в 70%, тип 16 отмечается при онкологии в 41-54% вероятности

Основной способ передачи инфекции – сексуальный контакт.
Это обуславливает распространение среди жителей планеты, достигая цифры в 70%.
В процентном соотношении женское население более подвержено поражению вирусом.
Способы передачи:
- половая близость (вагинальный, оральный, анальный контакт, с проникновением и без)
- контактно-бытовой
- передача инфекции матерью ребенку при родах
Клиника ВПЧ
Поражение организма вирусом происходит на клеточном уровне.
В атакуемой клетке ПВЧ отмечается в двух формах:
- доброкачественная, вирус вне клеточной хромосомы человека
- злокачественная, ДНК вируса в геноме человеческой клетки, меняет его структуру, приводит к перерождению
При доброкачественном варианте человек не замечает болезни, чаще организм сам очищается от чужеродных вирусов.
Активация и переход к клиническим проявлениям наступает у ослабленных, и ВИЧ-инфицированных людей.
Симптомов, как правило, не наблюдается.
К клиническим проявлениям относят:
- Низкоонкогенные аногенитальные бородавки
- Респираторный рецидивирующий папилломатоз (РРП), редкая патология, папилломы локализуются в дыхательных путях (гортань, голосовые связки, носоглотка). Папилломатоз гортани характерен для младшего детского возраста, но бывает и у взрослых
- Онкологические патологии, вызванные папилломавирусом: рак шейки матки (РШМ), вульвы, вагины, ануса, полового члена, протекают долгое время без симптомов. При обнаружении проблемы преобладает симптоматика онкологии
Для РШМ на определенной стадии характерны вагинальные кровотечения между менструациями и после полового контакта. Боли в пояснице, ногах, в тазу, ухудшение состояния, потеря аппетита и веса. Раздражение во влагалище, выделения со специфическим запахом, отек одной ноги. С дальнейшим утяжелением проявлений.
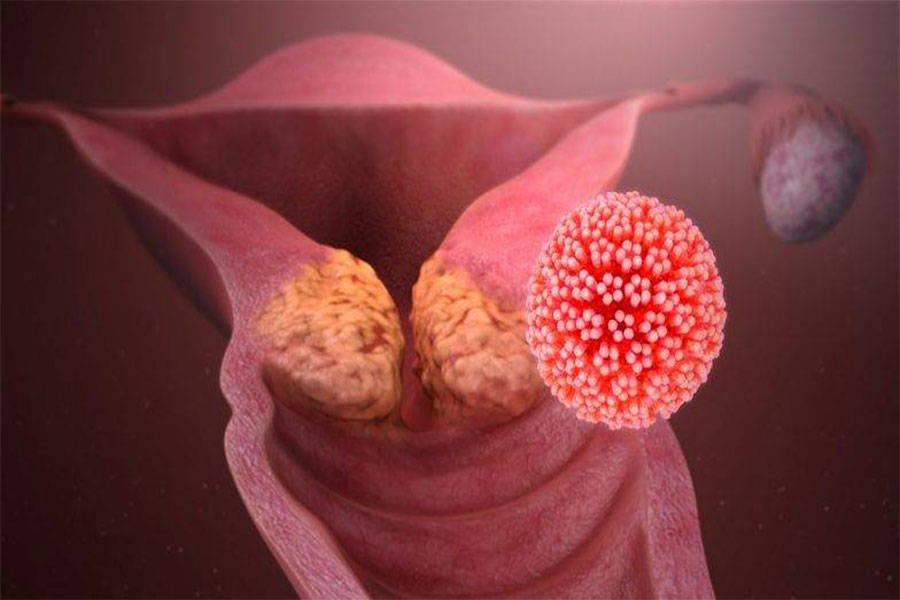
Опасен ли ВПЧ при беременности
ВПЧ при беременности не приговор, инфекция не влияет на плод и течение беременности.
Настороженность вызывают штаммы вирусов, вызывающие рост генитальных бородавок 6, 11, и типы повышенной онкогенности 16 и 18.
Лечение в период беременности требуется не всегда.
Пристальное наблюдение за проблемой (цитология, кольпоскопия), при необходимости применяют иммуномодуляторы для повышения защитных свойств организма.
Хирургическое вмешательство показано крайне редко, при угрозе для здоровья ребенка удаляются онкогенные образования.
Последствия ВПЧ у мужчин
Мужчина бывает вирусоносителем без явных проявлений клиники, или имеет проявления, например остроконечные кондиломы.
Если кондиломы появились у женщины, у ее полового партнера берется соскоб эпителия с головки полового члена, исследуется материал из ануса.
В некоторых странах мужчин на ПВЧ не обследуют в плановом порядке.
Взрослые люди независимо от пола одинаково подвержены возникновению таких патологий, как рак и предрак анальной области с участием ВПЧ.
Эпителий ануса так же атакуется вирусом, как и шейка матки.
Анальный рак отмечается у мужчин в 40% случаев, частота заболеваний растет, в частности в группе риска.
Отслеживается связь анального рака и предрака с ВИЧ-инфицированием по причине снижения иммунитета, анальных половых связей.
ВИЧ-положительные пациенты показывают более высокий процент заболевания.
ВПЧ активируется раньше, инкубационный период меньше, чем у здоровых людей.
ВПЧ для ВИЧ-позитивных пациентов является оппортунистической инфекцией и требует особого внимания.
К ранней диагностике анального рака относят:
Цитологический скрининг у мужчин проводит дерматовенеролог раз в 6 месяцев, если нет клинических проявлений при подтвержденном ВПЧ.
Если есть кондиломы, их удаляют.
Онкология как последствия ВПЧ
Взаимосвязь рака шейки матки с папилломавирусом 16 типа обнаружил Нобелевский лауреат 2008 года Гарольд цур Хаузен.
Научно установлено присутствие онкогенных ПВЧ при РШМ в 100% случаев.
Все больше данных подтверждает присутствие вирусов 16 и 18 типов при диагностике рака ануса, гениталий.
Связь этих заболеваний с ВПЧ имеет оптимистичный характер в плане предотвращения болезни путем первичной профилактики.
Она разработана для сокращения онкологического поражения женщин РШМ.
Рак шейки матки забирает 52% жизней женщин, это высокий показатель смертности.
Из них 85% женщины, из стран с низким и средним уровнем жизни.
Тяжелые последствия ВПЧ
Папилломавирус сопровождает такие заболевания:
- Верруциформная эпидермодисплазия – редкая патология, вызываемая некоторыми штаммами вируса. Проявляется изменением структуры клеток эпидермиса с характерными высыпаниями на пораженных участках в виде плоских бородавочных элементов или пятен, покрытых чешуйками. Имеет генетическую предрасположенность по рецессивному типу. Дисплазия эпидермиса может перейти в рак кожи, чаще всего при участии штаммов вируса 5, 8, 47
- Бовеноидный папулез (болезнь Боуэна) 16, 34, 35, 55 – редкая патология, протекает при участии 16 типа и сопутствующих типов, проявляется папулезным высыпанием в области мошонки, паха, полового члена, лобка, больших и малых половых губ. Папулы отдельные и слитые в бляшки до 2 см, с неоднородной поверхностью. Течение болезни затяжное, риск перерождения в онкологию 3%
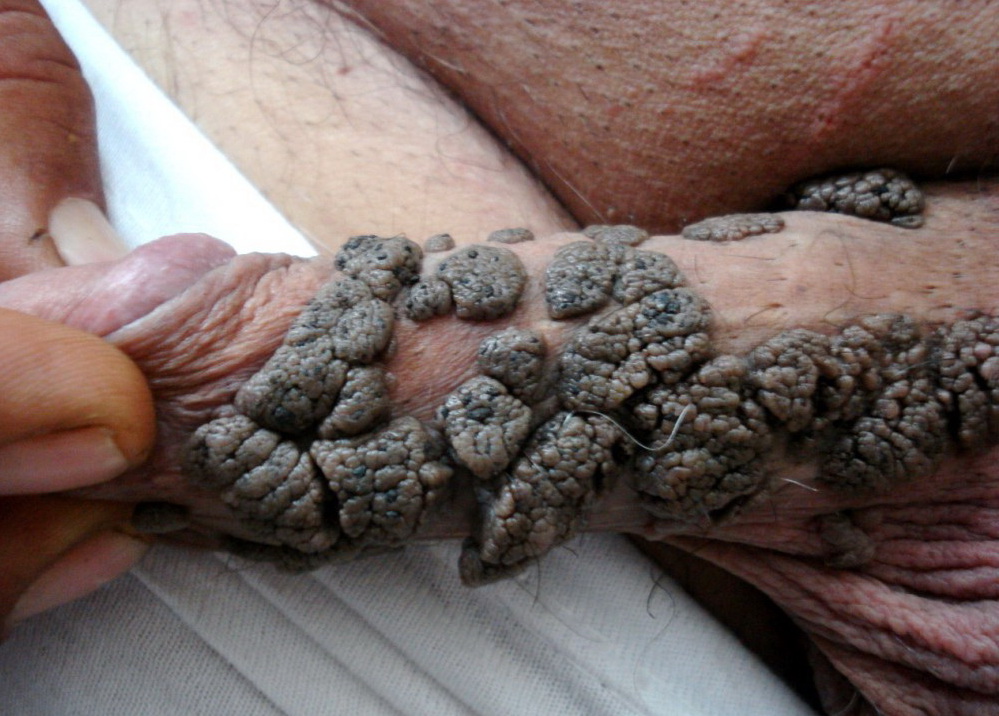
- Осложнения от папиллом и кондилом – редкое перерождение в злокачественные новообразования, при участии высокоонкогенных штаммов, чему способствует постоянное механическое повреждение, ослабленный иммунитет – чаще у мужчин, локализация половые органы, область ануса. Из узелков, растущих вширь и вглубь, образуется широкое основание, образование склонно к изъязвлению и деструкции, к рецидиву, относится к предраку. Необходимо глубокое хирургическое иссечение
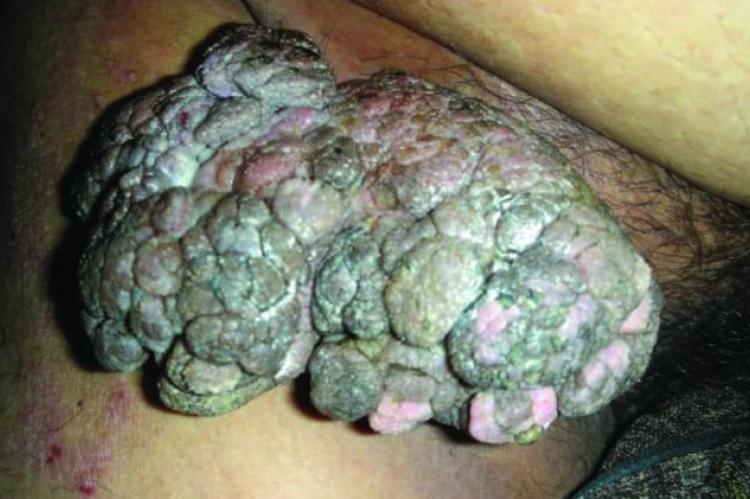
Диагностика ВПЧ

Современные методики обнаруживают вирус, определяют тип и потенциальную настороженность.
- Кольпоскопия – осмотр с использованием кольпоскопа.
- Цитология – микроскопия мазка. В результатах: норма 1, 2 класс, 3 класс дополняется гистологией, 4, 5 класс обнаружение злокачественных клеток. В мазках койлоциты и дискератоциты, измененные клетки.
- Гистология биопатов – микроскопическое изучение измененных клеток в тканях.
- Антитела к вирусу – отслеживаются в крови до появления клинических проявлений. Ранняя диагностика, но не устанавливает точно тип и концентрацию ПВЧ.
- Амплификационный (Digene-тест) – точное обнаружение ВПЧ. С указанием типов, концентрации. Материал – соскоб со слизистой оболочки вагины или уретры.
- Неамплификационный (ПЦР) – применяется для онкогенных штаммов. Материал: мазки, кровь, моча, амниотическая жидкость. Обнаруживается ДНК вируса.
- Дерматоскопия – характеризует новообразование при помощи оптики.
- Онкомаркер S-100 используется при определенных формах рака (рак кожи, меланома); осуществляют контроль над прогрессом заболевания, ответом на терапию. Диагностическая ценность низкая.
Лечение ВПЧ
Лечения инфекции, вызванной ВПЧ, на сегодня нет.
Большинство людей даже не подозревают о наличии заболевания.
Некоторые штаммы вируса изгоняются организмом самостоятельно.
Другие не приносят явных проблем и клинических проявлений.
Лечение заключается в устранении проявлений заболевания.

Проводят удаление генитальных бородавок, дисплазии, хирургическим или химическим путем.
- выжигание электрокаутером или лазером
- замораживание жидким азотом
- хирургическое удаление (кюретаж, иссечение)
- лечение химическими препаратами
- противовирусная и иммуномоделирующая терапия
- при диагностике рака – хирургическое вмешательство, радиотерапия и химиотерапия
Лечение позволяет не перейти из фазы предрак в более тяжелую стадию, не дает инфекции прогрессировать.
Показывает положительные результаты лечения при раннем обнаружении.
Профилактика ВПЧ
Разработана эффективная первичная профилактика РШМ, широко применяемая во многих странах современного мира.
Скрининг – тестирование на предраковые состояния и рак у здоровых женщин.
Эффективность методов для понижения смертности в глобальных масштабах, при раннем выявлении заболевания высока, как и вероятность излечения.
Проводится в возрасте 30-49 лет, учитывая длительную инкубацию.
Виды скрининга:
- визуальный осмотр с применением уксусной кислоты
- тесты на штаммы высокого риска
- цитологический тест окрашивание по Папаниколау шеечных и анальных мазков (РAP), цитология жидкости (LBC)
В странах, где применение скрининговых программ и раннее лечение предотвращает возникновение РШМ до 80%, реально виден результат.
При позднем, симптоматическом выявлении заболевания, лечение малоэффективное.
Вакцинация против ВПЧ
Вакцина против ПВЧ на 2013 год применялась уже в 55 странах ВОЗ.
Вакцинация не отменяет применение скрининга на РШМ, а дополняет его.
Проведение вакцинации для профилактики онкологии от ВПЧ 16 и 18 типов эффективно до внедрения вируса в организм человека.
Вакцины не излечат инфекцию и онкологию, вызванную папилломавирусом, поэтому их применяют до начала половых контактов.
В некоторых странах вакцинируют мальчиков, для сокращения аногенитального рака, вирусоносительства.
Одна из вакцин гарантирует перекрестное воздействие на вирус вызывающий рост генитальных кондилом у обоих полов.
Девочек по рекомендации ВОЗ вакцинируют в 9-13 лет, для минимизации затрат здравоохранения на эффективную профилактику РШМ.
Математическое моделирование прогнозирует при полном курсе первичного вакцинирования девочек 12-13 лет (3 дозы):
- значительное снижение рисков заболеваемости РШМ – на 63%
- предрака на 51%
- цитологические нарушения у женщин до 30 лет снижаются на 27%
Рекомендованный возраст для вакцинации: мальчики и девочки 9 – 17 лет, девушки 18 – 26 лет.
Ведутся исследования для вакцинации людей старше 30 лет.
Вакцины от ВПЧ
Наличие вакцины означает возможность первичной профилактики РШМ и других онкологических заболеваний.
Вакцины успешно применяются и показывают эффективность профилактических мер в США, Франции, Германии и других странах.

Вакцинация трехкратная, проводится с первым интервалом в 2 месяца и вторым в 4 месяца.
Возможна укороченная схема с первым интервалом в месяц и вторым в 2 месяца.
В случае наступления беременности вакцинация переносится в послеродовой период.
Проведение профилактики в течение 12 месяцев считается успешной и законченной вакцинацией.
Однако, отношение к вакцинации остается неоднозначным.
Вакцинация снижает риски от определенных штаммов вируса 16 и 18, но РШМ начинают вызывать штаммы, ранее признанные неонкогенными.
Прививка женщин, имеющих сексуальные контакты, практически нерезультативна.
Есть опасения, что вакцинация подростков вызовет пренебрежение к другим способам защиты.
При появлении признаков ВПЧ обращайтесь к автору этой статьи – дерматовенерологу в Москве с многолетним опытом работы.
Московский областной НИИ акушерства и гинекологии
НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи, Москва
Перинатальный центр Московской области
Московский областной НИИ акушерства и гинекологии
Родильный дом, г. Наро-Фоминск
Московский областной НИИ акушерства и гинекологии
Папилломавирусная инфекция у беременных
Журнал: Российский вестник акушера-гинеколога. 2011;11(6): 75‑78
Зароченцева Н.В., Малиновская В.В., Серова О.Ф., Метелёва Е.А., Кешьян Л.В., Торшина З.В. Папилломавирусная инфекция у беременных. Российский вестник акушера-гинеколога. 2011;11(6):75‑78.
Zarochentseva NV, Malinovskaia VV, Serova OF, Meteleva EA, Kesh'ian LV, Torshina ZV. Papillomavirus infection in pregnant women. Russian Bulletin of Obstetrician-Gynecologist. 2011;11(6):75‑78. (In Russ.).
Московский областной НИИ акушерства и гинекологии
На основании обследования 469 беременных с папилломавирусной инфекцией (ПВИ) представлены особенности течения этой инфекции во время беременности, ее распространенность среди беременных. Изложен алгоритм ведения беременных с ПВИ, включающий диагностику и тактику ведения во время беременности и после родов, а также методы лечения. Обращено внимание на применение иммунокорригирующей терапии - виферона.
Московский областной НИИ акушерства и гинекологии
НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи, Москва
Перинатальный центр Московской области
Московский областной НИИ акушерства и гинекологии
Родильный дом, г. Наро-Фоминск
Московский областной НИИ акушерства и гинекологии
В последнее время в России отмечается рост заболеваемости раком шейки матки (РШМ) у молодых женщин репродуктивного возраста, особенно в группе женщин моложе 29 лет. Как причина смерти женщин моложе 30 лет, рак шейки матки составляет 8,5% [4]. Среди онкологических заболеваний у беременных он составляет 45%. По данным С.И. Роговской [10], среди 1000 беременных в 1,3 случаев выявляют тяжелую дисплазию и рак in situ, в 0,45 случаев - инвазивный РШМ.
Основным этиологическим фактором РШМ является вирус папилломы человека (ВПЧ), что было подтверждено результатами как эпидемиологических, так и молекулярно-биологических исследований [2, 5, 8, 11, 14]. ВПЧ является также причиной дистрофических и злокачественных заболеваний вульвы и влагалища у женщин и полового члена у мужчин [6]. Вероятность самопроизвольной элиминации ВПЧ при носительстве и возможность спонтанной регрессии как субклинических, так и клинических форм папилломавирусной инфекции (ПВИ), склоняет ряд исследователей к наблюдательной тактике [1, 3, 12]. Однако ВПЧ не считается нормальным представителем влагалищного биотопа [7, 9].
В настоящее время нет единого мнения о влиянии ВПЧ на течение и исход беременности. Известно, что беременность является фактором риска развития ПВИ и способствует активной репликации и персистенции вируса папилломы человека. Исследования A. Schneider и соавт. (1987) показали, что частота развития ПВИ у беременных в 2,3 раза превышает таковую у небеременных женщин, при этом количество вирусной ДНК у беременных в среднем в 10 раз больше того же количества у небеременных. Число случаев передачи ВПЧ от матери плоду, по данным разных исследователей, составляет от 4 до 87%, что зависит от чувствительности использованных методов диагностики [10, 13].
Папилломатоз респираторного тракта, наиболее часто вызываемый 6-м и 11-м типами ВПЧ, имеет тяжелое течение у маленьких детей с наклонностью к рецидивированию. В 75-87% случаев признаки ювенильного респираторного папилломатоза регистрируются в первые 5 лет жизни, что, вероятно, связано с функциональной незрелостью иммунной системы [16].
Особенности течения ПВИ во время беременности. Эстрогены и прогестерон увеличивают экспрессию ВПЧ в цервикальном эпителии и способствуют клеточной пролиферации и канцерогенезу, а во время беременности отмечается чрезвычайно высокий выброс половых гормонов. Из-за усиления васкуляризации, активного метаболизма в тканях, изменения микробиоценоза влагалища, снижения компенсаторных возможностей систем иммунитета повышаются риск заражения и заболеваемость различными инфекциями. При этом латентная ПВИ может перейти в суб- и клинические формы [10].
Беременность может являться фактором риска развития ПВИ и способствовать активной репликации и персистенции ВПЧ. Во время беременности видимые кондиломы часто рецидивируют, имеют тенденцию к разрастанию, становятся рыхлыми, могут достигать гигантских размеров.
Распространенность ПВИ среди беременных. В Московском областном НИИ акушерства и гинекологии было проведено обследование 700 последовательно поступивших на специализированный прием по заболеваниям шейки матки беременных с целью выявления ПВИ. При скриннинговом обследовании этих беременных с использованием метода полимеразной цепной реакции клинико-лабораторные проявления ПВИ были выявлены у 46 (67%) беременных.
Результаты обследования беременных с различными заболеваниями шейки матки показали, что ПВИ чаще обнаруживается у пациенток с цервикальными интраэпителиальными неоплазиями (CIN) (95,5%), у беременных с осложненной эктопией (32,4%), с лейкоплакией (56%), после хирургического лечения CIN (42%), с полипами цервикального канала (38,8%). Следует отметить, что даже при неизмененной шейке матки ВПЧ выявляли у каждой третьей беременной (34%). Цитологические признаки папилломавирусного поражения шейки матки отмечались у 12% беременных с неизмененной шейкой матки только во II и III триместрах беременности. У беременных с осложненной эктопией койлоцитоз в сочетании с дискератозом многослойного плоского эпителия шейки матки был выявлен в I триместре у 7,4%, во II триместре - у 25,9% и в III триместре - у 31,5%. У беременных с полипами цервикального канала цитологические признаки папилломавирусного поражения шейки матки были обнаружены в 20,8% случаев.
Несмотря на хирургическое лечение CIN на этапе прегравидарной подготовки и последующее наблюдение за этими пациентками, число случаев рецидивов CIN у них во время беременности составило 4% на фоне ПВИ (наличие койлоцитов).
У беременных с лейкоплакией шейки матки койлоциты при цитологическом исследовании определялись в 56% случаев. Чаще всего признаки папилломавирусного поражения шейки матки были обнаружены у беременных с диагностированной CIN - в 73,3 и 77,7% случаев в I и II триместрах соответственно.
Представленные данные еще раз подтверждают, что цитологический метод исследования в настоящее время остается ведущим в диагностике заболеваний шейки матки. К сожалению, до сих пор среди гинекологов существует ошибочное мнение об опасности углубленного цитологического исследования шейки матки у беременных из-за возможных осложнений. В то же время высокая выявляемость заболеваний шейки матки во время беременности диктует необходимость обязательного цитологического исследования экто- и эндоцервикса у беременных при постановке их на учет.
Остроконечные кондиломы вульвы и влагалища были выявлены при кольпоскопическом исследовании у 62% беременных. Они представляли собой возвышающиеся над поверхностью слизистой оболочки фиброэпителиальные образования неправильной формы с пальцеобразными или конусовидными выступами на тонкой ножке, реже - на широком основании в виде одиночного узелка либо в форме множественных выростов, напоминающих цветную капусту или петушиные гребни. Поверхность кондилом была покрыта многослойным плоским эпителием и нередко кератинизирована. В подлежащей строме располагались сосуды. Возникающие в ряде случаев в строме воспалительные реакции, расстройство микроциркуляции и отек способствовали присоединению вторичной инфекции. У 5,3% беременных были выявлены кондиломы шейки матки в виде опухоли с почковидными сосочками, равномерно располагающимися по ее поверхности и образующими повторяющийся рисунок. У 9% беременных имелись гигантские кондиломы наружных половых органов и влагалища, величиной до 7 см.
Состояние местного иммунитета. Наличие доброкачественных заболеваний шейки матки и ПВИ сопровождалось резким снижением местного иммунитета, наиболее выраженным у беременных с CIN. Оно проявлялось уменьшением продукции секреторного иммуноглобулина А (sIgA), который является основным показателем иммунной защиты, и увеличением продукции иммуноглобулинов А, M и G (IgA, М, G). Наиболее выраженные изменения в содержании иммуноглобулинов всех изотипов были у беременных с CIN. Характерными для них являлись крайне низкая продукция sIgA (2,2±0,5 мкг/мл) и высокий уровень IgМ (24,8±0,9 мкг/мл), который рассматривают как маркер воспаления. Средние уровни IgA составили 24,2±1,6 мкг/мл, IgG - 1248,6±46,5 мкг/мл. У здоровых беременных уровень sIgA составил 12,2±0,5 мкг/мл, IgA - 36,5±0,5 мкг/мл, IgM - 2,6±0,5 мкг/мл, IgG - 456,5±35,5 мкг/мл.
Полученные результаты подтверждают связь между заболеваниями шейки матки и нарушением местного иммунитета, что имеет большое значение для выбора адекватной иммунокорригирующей терапии, и свидетельствуют о том, что степень нарушения местного иммунитета прямо пропорциональна тяжести заболевания шейки матки.
Алгоритм ведения беременных с ПВИ
I этап - обследование
- Диагностика и лечение других инфекций половых органов и дисбиоза влагалища.
- Обнаружение ДНК ВПЧ с типированием.
- Цитологическое исследование (РАР-тест).
II этап - определение тактики ведения
- Показания к наблюдению: латентная форма ПВИ, вестибулярный папилломатоз.
- Показания к лечению: остроконечные кондиломы вульвы, влагалища, шейки матки.
- Тактика ведения беременных с CIN I должна быть контролирующе-выжидательная с динамическим кольпоскопическим наблюдением и цитологическим контролем, с окончательным лечением шейки матки после родов.
- При наличии признаков ПВИ и CIN I-III проводится противовоспалительное лечение, коррекция микробиоценоза влагалища, после чего необходимо повторить РАР-тест.
- При наличии после лечения признаков ПВИ, CIN II-III у беременных или при ухудшении результатов кольпоскопического или цитологического исследования показаны биопсия шейки матки с гистологическим исследованием и консультация онколога.
- При выявлении CIN III необходима обязательная консультация онколога, в случае выявления CIN III во II-III триместрах возможно пролонгирование беременности при динамическом цитологическом и кольпоскопическом контроле 1 раз в 3 нед с последующим лечением после родоразрешения.
- Показаниями к биопсии шейки матки при беременности являются атипические цитологические и кольпоскопические картины, подозрительные на рак (неоднородная поверхность, экзофит, эрозия или изъязвления и атипичная васкуляризация).
III этап - комплексное обследование и определение тактики ведения в послеродовом периоде на основании данных кольпоскопии, цитогистологической переоценке предшествующих данных.
Лечение заболеваний, ассоциированных с ВПЧ, во время беременности необходимо проводить дифференцированно по показаниям в любые сроки, но предпочтительно в I триместре [10]. Перед использованием деструктивных методов лечения рекомендуется провести комплексное обследование, лечение сопутствующих воспалительных заболеваний гениталий.
Методами выбора для лечения остроконечных кондилом у беременных являются радиоволновая терапия и применение химических коагулянтов - солкодерма, трихлоруксусной кислоты. Возможно применение лазерной терапии, электрокоагуляции, хирургического метода.
В связи с риском неблагоприятного воздействия на плод во время беременности противопоказан прием цитостатических препаратов, которые, обладая антипролиферативной активностью, способствуют разрушению клеток, воздействуя как на поврежденные, так и на здоровые клетки.
Во время беременности применяются внутривлагалищные, ректальные и наружные средства, системные препараты. Интерферонотерапия проводится со второй половины беременности. Виферон является оптимальным препаратом для иммунокоррекции при беременности. Он содержит рекомбинантный α2-интерферон, а также мембраностабилизирующие компоненты - α-токоферола ацетат и аскорбиновую кислоту. Виферон является иммуномодулятором, влияющим на процессы дифференцировки, рекрутирования, функциональную активность эффекторных клеток иммунной системы, а также эффективность иммунного распознавания антигена и усиление фагоцитарной и цитолитической активности. Чтобы исключить развитие явлений рефрактерности эффекторных клеток к действию ИФН, системное введение препарата должно быть прерывистым. Кроме того, доказана протективная эффективность ИФН при заболеваниях, вызванных внутриклеточными микроорганизмами-паразитами (хламидии, микоплазмы и др.). Очевидно, эффект в данном случае также связан с подавлением синтеза белков и активацией фагоцитоза.
Виферон выпускается в виде суппозиториев 150 000 МЕ, 500 000 МЕ, 1 000 000 МЕ и 3 000 000 МЕ для ректального применения. Беременным назначаются обычно свечи по 150 000 или 500 000 МЕ 2 раза в день в течение 10 дней. При применении виферона создается высокая концентрация интерферона в очаге инфекции, что способствует быстрому купированию субъективных симптомов, снижению доз и длительности курса антибиотикотерапии. Применение виферона в комплексном лечении ИППП у беременных оказывает положительное влияние на состояние иммунитета и повышает эффективность противомикробной терапии.
У больных с ПВИ часто наблюдается нарушение микробиоценоза влагалища - резкий дефицит лактобацилл, избыток условно-патогенной микрофлоры. Отмечается значительная обсемененность дрожжеподобными грибами. В большом проценте случаев имеется инфицированность микроорганизмами, передающимися половым путем - хламидиями, генитальными микоплазмами и др. При наличии урогенитальной инфекции антибиотикотерапия проводится после 12 нед гестации. Коррекция микробиоценоза влагалища у беременных проводится с применением местных разрешенных препаратов. Во время беременности возможна терапия глицирризиновой кислотой, обладающей противовирусной активностью. Необходима также коррекция микробиоценоза влагалища с помощью эубиотиков.
Вопрос о родоразрешении у женщин с ПВИ решается индивидуально. Проведенные исследования свидетельствуют о том, что абдоминальное родоразрешение не снижает риск инфицирования плода (N. Sedlacek, S. Lindheim и соавт., 1989), описаны случаи рождения детей путем кесарева сечения с папилломатозом гортани.
Ввиду высокой частоты ПВИ у беременных, участия ВПЧ в процессах канцерогенеза, необходима оптимизация прегравидарной подготовки женщин, включающая комплексное обследование с целью выявления ВПЧ, проведение его типирования, а также лечение ВПЧ-ассоциированных заболеваний на этапе планирования беременности.
При планировании беременности субклинические формы инфекции, так же, как и CIN, должны быть вылечены еще до беременности.
Носительство ВПЧ не является противопоказанием к беременности.
Полностью излечить женщину от вирусоносительства не представляется возможным, поэтому адекватная прегравидарная подготовка является достаточной мерой профилактики обострения ПВИ при беременности.
Читайте также:

