Высокий ige при герпесе
Обновлено: 13.05.2024
Иммуноглобулин Е при вирусных инфекциях.
Что касается данных о выработке иммуноглобулина Е при вирусных инфекциях, то они немногочисленны и противоречивы. Большинство исследований посвящено определению уровня общего IgE. Так, имеются сведения о последовательном снижении уровней IgE (на 35-87%) в фазу выздоровления по сравнению с острой фазой респираторной вирусной инфекции у лиц без атонии. В то же время А. Курашвили и соавт. (1984) опубликовали данные о том, что острая фаза гриппа сопровождается снижением уровня общего IgE, а в период реконвалесценции у больных бронхиальной астмой этот уровень превышает нормальные показатели у здоровых доноров. По-видимому, указанные обстоятельства объясняются выраженным супрессорным воздействием вируса гриппа на гуморальный иммунитет.
Уровень общего IgE при частых рецидивах герпетической инфекции оказался повышенным независимо от наличия или отсутствия атопии.
Противоречивость данных об уровне IgE при вирусных инфекциях легко объяснима, учитывая неспецифичность изучаемых параметров иммуноглобулина, а также разнообразие вирусных агентов.

Наиболее детально проанализирован специфический IgE ответ при респираторно-синцитиачьной инфекции. Рядом зарубежных и отечественных исследователей показано, что при PC-инфекции возникает преимущественно местный, а не гуморальный IgE к вирусу (слизистая респираторного тракта, бронхоальвеолярный лаваж, бронхиальные и назофарингеальные смывы). При хронической обструктивной болезни легких и облитерирующем бронхиолите наиболее значительные уровни IgE к PC-вирусу регистрировали в жидкости бронхоальвеолярного лаважа, что соответствовало и основной локализации вируса (либо его антигенов) в глубоких отделах респираторного тракта, а не верхних дыхательных пугях. Следует отметить, что IgE-ответ на PC-вирус отмечался и у практически здоровых лиц, но преимущественно в смывах верхних дыхательных путей, при этом уровень специфического IgE и продолжительность его обнаружения значительно уступали показателям, полученным при наличии бронхоспазма и верифицированной бронхиальной астмы.
При сравнительном изучении уровней специфических IgE к различным респираторным вирусам было выяснено, что специфический ответ при PC-инфекции значительно выше, чем при гриппе, парагриппе и аденовирусе вне зависимости от наличия или отсутствия бронхоспазма. Объяснением подобного явления служат уникальные биологические свойства РСВ, который обладает слабо выраженной интерферониндуцирующей способностью (не только а, но и у-интерферон) в отличие от других респираторных вирусов. Слабая индукция интерферона-у (ИФ-у) - главного ингибитора IgE при респираторно-синцитиальной инфекции - естественно, ведет к длительной продукции указанного иммуноглобулина, тогда как при гриппе и парагриппе через неделю от начала инфицирования уровни ИФ-у оказывались в 10-12 раз выше и приостанавливали дальнейший синтез специфического IgE.
Оригинальные исследования были проведены сотрудниками Института вирусологии им. Д.И. Ивановского и НИИ пульмонологии МЗ РФ. Обследовали больных с различными вариантами бронхиальной астмы. В результате выявлены коррелятивные связи между подъемом уровней интерлейкина-4 (индуктора IgE), IgE и предшественника ИФ-у белка-неоптерина. Низким уровням неоптерина, как правило, сопутствовали высокие концентрации как общего, так и специфического IgE. Таким образом, PC-вирус в силу своих уникальных биологических свойств представляет особую опасность в плане развития аллергических реакций и атопических заболеваний, в том числе атопической бронхиальной астмы. Однако PC-вирус является наиболее частой причиной не только атонической, но и неатопической астмы. По мнению Н. Lindemann респираторные вирусы в 90,0% случаев обусловливают формирование инфекционно-аллергической астмы. Тогда как на долю бактериальной флоры остается всего 10,0%. Лидером среди респираторных вирусов является РСВ (60,0-70,0%). Чаще поражаются дети в возрасте 4-5 месяцев, при этом тотально поражается весь эпителий дыхательных путей, включая бронхиолы диаметром 75-300 мкм. Примерно у половины детей, перенесших PC-вирусный бронхиолит, по данным Zweimann et al., (1971) в течение ближайших 5 лет формируется либо хронический обструктивный бронхит, либо бронхиальная астма (особенно при наличии у родителей атопии).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Иммуноглобулин Е (IgE) - класс иммуноглобулинов, обнаруживаемый в норме в незначительных количествах в сыворотке крови и секретах. Впервые IgE был изолирован в 1960-х годах из сывороток больных атопией и множественной миеломой. В 1968 г. ВОЗ выделила IgE как самостоятельный класс иммуноглобулинов. Согласно ВОЗ 1 МЕ/мл (МЕ - международная единица) соответствует 2,4 нг. Обычно концентрация IgE выражается в МЕ/мл или кЕ/л (кЕ - килоединица).
В норме IgE составляет менее 0,001% от всех иммуноглобулинов сыворотки крови (см. табл.1).
Таблица 1: Содержание IgE в сыворотке крови здоровых людей
| Возрастные группы | IgE (кЕ/л) |
|---|---|
| До 1 года | 0 - 15 |
| 1 год-6 лет | 0 - 60 |
| 6 -10 лет | 0 - 90 |
| 10 -16 лет | 0 - 200 |
| Взрослые | 0 - 100 |
Структура IgE подобна структуре других иммуноглобулинов и состоит из двух тяжёлых и двух лёгких полипептидных цепей. Они сгруппированы в комплексы, называемые доменами. Каждый домен содержит приблизительно 110 аминокислот. IgE имеет пять таких доменов в отличие от IgG, который имеет только четыре домена. По физико-химическим свойствам IgE - гликопротеин с молекулярной массой примерно 190000 дальтон, состоящий на 12% из углеводов. IgE имеет самую короткую продолжительность существования (время полувыведения из сыворотки крови 2 - 3 суток), самую высокую скорость катаболизма и наименьшую скорость синтеза из всех иммуноглобулинов (2,3 мкг/кг в сутки). IgE синтезируется главным образом плазматическими клетками, локализующимися в слизистых оболочках. Основная биологическая роль IgE - уникальная способность связываться с поверхностью тучных клеток и базофилов человека. На поверхности одного базофила присутствует примерно 40000 - 100000 рецепторов, которые связывают от 5000 до 40000 молекул IgE.
Помимо участия в аллергических реакциях I (немедленного) типа, IgE принимает участие в защитном противогельминтном иммунитете, что обусловлено существованием перекрёстного связывания между IgE и антигеном гельминтов. Последний проникает через мембрану слизистой и садится на тучные клетки, вызывая их дегрануляцию. Медиаторы воспаления повышают проницаемость капилляров и слизистой, в результате чего IgG и лейкоциты выходят из кровотока. К гельминтам покрытым IgG присоединяются эозинофилы, которые выбрасывают содержимое своих гранул и таким образом убивают гельминтов.
IgE можно обнаружить в организме человека уже на 11-й неделе внутриутробного развития. Содержание IgE в сыворотке крови возрастает постепенно с момента рождения человека до подросткового возраста. В пожилом возрасте уровень IgE может снижаться.
В практике клинико-диагностических лабораторий определение общего и специфического IgE проводится с целью их использования в качестве самостоятельных диагностических показателей. В табл. 2 перечислены основные болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови.
Таблица 2: Болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови
| Болезни и состояния | Возможные причины |
| I. Повышенное содержание IgE | |
|---|---|
| Аллергические болезни, обусловленные IgE антителами: а) Атопические болезни · Аллергический ринит · Атопическая бронхиальная астма · Атопический дерматит · Аллергическая гастроэнтеропатия б) Анафилактические болезни · Системная анафилаксия · Крапивница - ангионевротический отек | Множественные аллергены: · пыльцевые · пылевые · эпидермальные · пищевые · лекарственные препараты · химические вещества · металлы · чужеродный белок |
| Аллергический бронхопульмональный аспергиллез | Неизвестны |
| Гельминтозы | IgE антитела, связанные с защитным иммунитетом |
| Гипер-IgE синдром (синдром Джоба) | Дефект Т-супрессоров |
| Селективный IgA дефицит | Дефект Т-супрессоров |
| Синдром Вискотт-Олдриджа | Неизвестны |
| Тимусная аплазия (синдром Ди-Джорджи) | Неизвестны |
| IgE - миелома | Неоплазия IgE-продуцирующих плазматических клеток |
| Реакция "трансплантат против хозяина" | Дефект Т-супрессоров |
| II. Сниженное содержание общего IgE | |
| Атаксия - телеангиэктазия | Дефекты Т-клеток |
Ниже приведены в качестве примеров диапазоны содержания общего IgE сыворотки крови (у взрослых) при некоторых патологических состояниях (табл. 3). Однако, несмотря на первоначально кажущуюся простоту использования определения общего и специфического IgE для диагностики, существуют некоторые сложности в интерпретации результатов. Их перечень приведён ниже.
Таблица 3: Значения общего IgE при некоторых патологических состояниях
| Патологические состояния | Содержание IgE (кЕ/л) |
|---|---|
| Аллергический ринит | 120 - 1000 кЕ/л |
| Атопическая бронхиальная астма | 120 - 1200 кЕ/л |
| Атопический дерматит | 80 - 14000 кЕ/л |
| Аллергический бронхолегочный аспергиллез: - ремиссия - обострение | 80 - 1000 кЕ/л 1000 - 8000 кЕ/л |
| Гипер - IgE синдром | 1000 - 14000 кЕ/л |
| IgE - миелома | 15000 кЕ/л и выше |
Особенности интерпретации и диагностические ограничения общего IgE
- Примерно 30% больных атопическими заболеваниями имеют уровень общего IgE в пределах значений нормы.
- Некоторые больные бронхиальной астмой могут иметь повышенную чувствительность только к одному аллергену (антигену), в результате чего общий IgE может быть в пределах нормы, в то время как кожная проба и специфический IgE будут положительными.
- Концентрация общего IgE в сыворотке крови также повышается при неатопических состояниях (особенно при глистной инвазии, некоторых формах иммунодефицитов и бронхопульмональном аспергиллезе) с последующей нормализацией после соответствующего лечения.
- Хроническая рецидивирующая крапивница и ангионевротический отёк не являются обязательными показаниями для определения общего IgE, так как обычно имеют неиммунную природу.
- Границы нормы, определённые для европейцев, не могут быть применены для представителей зон, эндемичных по гельминтозам.
Особенности интерпретации и диагностические ограничения специфического IgE
- Доступность определения специфического IgE не должна преувеличивать его диагностическую роль в обследовании больных с аллергией.
- Обнаружение аллергенспецифического IgE (к какому-либо аллергену или антигену) не доказывает, что именно этот аллерген ответственен за клиническую симптоматику; окончательное заключение и интерпретация лабораторных данных должны быть сделаны только после сопоставления с клинической картиной и данными развёрнутого аллергологического анамнеза.
- Отсутствие специфического IgE в сыворотке периферической крови не исключает возможности участия IgE-зависимого механизма, так как местный синтез IgE и сенсибилизация тучных клеток может происходить и в отсутствие специфического IgE в кровотоке (например, аллергический ринит).
- Антитела других классов, специфичные для данного аллергена, особенно класса IgG (IgG4), могут быть причиной ложноотрицательных результатов.
- Исключительно высокие концентрации общего IgE, например, у отдельных больных атопическим дерматитом, могут за счёт неспецифического связывания с аллергеном давать ложноположительные результаты.
- Идентичные результаты для разных аллергенов не означают их одинакового клинического значения, так как способность к связыванию с IgE у разных аллергенов может быть различной.
В заключении, учитывая всё выше изложенное, а также существующие сложности в постановке и интерпретации кожных проб, перечислим основные показания и противопоказания к назначению специфического аллергологического обследования in vitro - определения специфического IgE (табл. 4).
Таблица 4: Показания и противопоказания к определению специфического IgE
| Показания | |
|---|---|
| 1 | Дифференциальная диагностика между IgE-зависимым и не-IgE-зависимым механизмами аллергических реакций |
| 2 | Больные, у которых невозможно выявить аллерген анамнестически, при помощи дневника и т. д. |
| 3 | Больные с недостаточным эффектом специфической гипосенсибилизации, назначенной по результатам кожных проб |
| 4 | Дермографизм и распространённый дерматит |
| 5 | Больные детского и пожилого возраста с гипореактивностью кожи |
| 6 | Гиперреактивность кожи |
| 7 | Больные, которым невозможно отменить симптоматическую терапию препаратами, влияющими на результаты кожных проб |
| 8 | Отрицательное отношение больного к кожным пробам |
| 9 | В анамнезе системные аллергические реакции на кожные пробы |
| 10 | Несоответствие результатов кожных проб данным анамнеза и клинической картине |
| 11 | IgE-зависимая пищевая аллергия |
| 12 | Необходимость количественной оценки чувствительности и специфичности аллергена |
| 13 | Общий IgE сыворотки крови более 100 кЕ/л |
| Обследование нецелесообразно: | |
| 1 | При атопических заболеваниях в случаях удовлетворительных результатов специфической терапии по данным кожных проб |
| 2 | У больных с не-IgE-зависимым механизмом аллергических реакции |
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна–Барр: причины появления, симптомы, диагностика и способы лечения.
Вирус Эпштейна–Барр может инфицировать различные типы клеток, включая B-клетки иммунной системы (разновидность лейкоцитов – белых кровяных телец) и эпителиальные клетки слизистых оболочек.
ВЭБ является представителем ДНК-содержащих вирусов из семейства Herpesviridae (герпесвирусы), подсемейства гамма-герпесвирусов и рода лимфокриптовирусов. В процессе репликации (самокопирования) вируса экспрессируется свыше 70 различных вирусспецифических белков. В настоящее время выделены группы иммуногенных белков, определение антител к которым дает возможность дифференцировать стадию инфекции (ЕА – ранний антиген, ЕВNА-1 — ядерный антиген, VCA — капсидный антиген, LMP — латентный мембранный белок).
Другой способ заражения – контактно-бытовой (вирус передается через зубные щетки, столовые приборы, полотенца и т.д.). ВЭБ также может распространяться через кровь и сперму.
ВЭБ размножается в В-лимфоцитах и эпителиальных клетках, в связи с чем характерно многообразие клинических проявлений данной патологии. Важной отличительной чертой вируса является то, что он не тормозит и не нарушает размножение В-лимфоцитов, а, наоборот, стимулирует его. В этом заключается особенность возбудителя - он размножается в клетках иммунной системы, заставляя их клонировать свою, вирусную, ДНК.
Хронический воспалительный процесс, вызванный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии.
Классификация вируса Эпштейна-Барр
Единой классификации вирусной инфекции Эпштейна-Барр (ВИЭБ) не существует, к использованию в практической медицине предлагается следующая:
- по времени инфицирования – врожденная и приобретенная;
- по форме заболевания – типичная (инфекционный мононуклеоз) и атипичная: стертая, асимптомная, с поражением внутренних органов;
- по тяжести течения – легкая, средней степени и тяжелая;
- по продолжительности течения – острая, затяжная, хроническая;
- по фазе активности – активная и неактивная;
- смешанная инфекция – чаще всего наблюдается в сочетании с цитомегаловирусом.
- Инфекционный мононуклеоз (железистая лихорадка, болезнь Филатова) – распространенное инфекционное заболевание, основными проявлениями которого является подъем температуры до высоких значений, увеличение лимфатических узлов, воспаление слизистой оболочки глотки, увеличение печени и селезенки. ВЭБ в данном случае проникает через эпителий слизистых оболочек верхних дыхательных путей.
- Лимфогранулематоз (болезнь Ходжкина) и некоторые виды неходжкинских лимфом – группа заболеваний, объединенных злокачественной моноклональной пролиферацией лимфоидных клеток в лимфоузлах, костном мозге, селезенке, печени и желудочно-кишечном тракте.
- Синдром хронической усталости – состояние, характеризующееся длительным чувством усталости, которое не проходит после продолжительного отдыха.
- Синдром Алисы в стране чудес – состояние, клиническим проявлением которого является нарушение ощущения своего тела и отдельных его частей. Человек ощущает себя или части своего тела очень большими или очень маленькими по сравнению с действительностью.
- Гепатит, спровоцированный ВЭБ, часто является осложнением инфекционного мононуклеоза. Появляется слабость, тошнота, желтушность кожи и слизистых, увеличивается печень.
- Герпетическая инфекция в виде генитального или лабиального (на губах) поражения. Также возможен стоматит, вызванный ВЭБ. При активации инфекции появляется чувство жжения и боль, а затем множество маленьких пузырьков.
- Посттрансплантационная лимфопролиферативная болезнь – вторичное злокачественное заболевание, развивающееся после трансплантации гемопоэтических стволовых клеток (метод лечения, применяемый при онкологии, заболеваниях крови и др.), ассоциированное с ВЭБ-инфекцией.
- Рассеянный склероз – хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга. Характеризуется большим количеством симптомов и зависит от уровня поражения: часто снижается мышечная сила, угасают рефлексы, появляются параличи (обездвиженность) различных локализаций.
- Волосатая лейкоплакия – на слизистой оболочке языка по бокам, на спинке либо на его нижней части появляются белые участки с шероховатой поверхностью. Они безболезненны и не причиняют существенного дискомфорта. Основная опасность заключается в возможности озлокачествления измененных клеток слизистой.
- Назофарингеальная карцинома – злокачественное образование глотки. Среди его симптомов часто встречаются заложенность носа, потеря слуха, частые отиты, появление крови в слюне, кровянистые выделения из носа, увеличение лимфоузлов, головные боли.
- Аутоиммунный тиреоидит – хроническое заболевание щитовидной железы, при котором в организме образуются антитела к тканям щитовидной железы. При данном заболевании возможно появление зоба (увеличение щитовидной железы), развитие симптомов гипотиреоза: отеки, повышенная утомляемость, сонливость, запоры, сухость кожи, выпадение волос.
Лабораторное обследование включает:
-
вирус Эпштейна–Барр, определение ДНК в крови (Epstein Barr virus, DNA);
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Иммуноглобулин Е (IgE) - класс иммуноглобулинов, обнаруживаемый в норме в незначительных количествах в сыворотке крови и секретах. Впервые IgE был изолирован в 1960-х годах из сывороток больных атопией и множественной миеломой. В 1968 г. ВОЗ выделила IgE как самостоятельный класс иммуноглобулинов. Согласно ВОЗ 1 МЕ/мл (МЕ - международная единица) соответствует 2,4 нг. Обычно концентрация IgE выражается в МЕ/мл или кЕ/л (кЕ - килоединица).
В норме IgE составляет менее 0,001% от всех иммуноглобулинов сыворотки крови (см. табл.1).
Таблица 1: Содержание IgE в сыворотке крови здоровых людей
| Возрастные группы | IgE (кЕ/л) |
|---|---|
| До 1 года | 0 - 15 |
| 1 год-6 лет | 0 - 60 |
| 6 -10 лет | 0 - 90 |
| 10 -16 лет | 0 - 200 |
| Взрослые | 0 - 100 |
Структура IgE подобна структуре других иммуноглобулинов и состоит из двух тяжёлых и двух лёгких полипептидных цепей. Они сгруппированы в комплексы, называемые доменами. Каждый домен содержит приблизительно 110 аминокислот. IgE имеет пять таких доменов в отличие от IgG, который имеет только четыре домена. По физико-химическим свойствам IgE - гликопротеин с молекулярной массой примерно 190000 дальтон, состоящий на 12% из углеводов. IgE имеет самую короткую продолжительность существования (время полувыведения из сыворотки крови 2 - 3 суток), самую высокую скорость катаболизма и наименьшую скорость синтеза из всех иммуноглобулинов (2,3 мкг/кг в сутки). IgE синтезируется главным образом плазматическими клетками, локализующимися в слизистых оболочках. Основная биологическая роль IgE - уникальная способность связываться с поверхностью тучных клеток и базофилов человека. На поверхности одного базофила присутствует примерно 40000 - 100000 рецепторов, которые связывают от 5000 до 40000 молекул IgE.
Помимо участия в аллергических реакциях I (немедленного) типа, IgE принимает участие в защитном противогельминтном иммунитете, что обусловлено существованием перекрёстного связывания между IgE и антигеном гельминтов. Последний проникает через мембрану слизистой и садится на тучные клетки, вызывая их дегрануляцию. Медиаторы воспаления повышают проницаемость капилляров и слизистой, в результате чего IgG и лейкоциты выходят из кровотока. К гельминтам покрытым IgG присоединяются эозинофилы, которые выбрасывают содержимое своих гранул и таким образом убивают гельминтов.
IgE можно обнаружить в организме человека уже на 11-й неделе внутриутробного развития. Содержание IgE в сыворотке крови возрастает постепенно с момента рождения человека до подросткового возраста. В пожилом возрасте уровень IgE может снижаться.
В практике клинико-диагностических лабораторий определение общего и специфического IgE проводится с целью их использования в качестве самостоятельных диагностических показателей. В табл. 2 перечислены основные болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови.
Таблица 2: Болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови
| Болезни и состояния | Возможные причины |
| I. Повышенное содержание IgE | |
|---|---|
| Аллергические болезни, обусловленные IgE антителами: а) Атопические болезни · Аллергический ринит · Атопическая бронхиальная астма · Атопический дерматит · Аллергическая гастроэнтеропатия б) Анафилактические болезни · Системная анафилаксия · Крапивница - ангионевротический отек | Множественные аллергены: · пыльцевые · пылевые · эпидермальные · пищевые · лекарственные препараты · химические вещества · металлы · чужеродный белок |
| Аллергический бронхопульмональный аспергиллез | Неизвестны |
| Гельминтозы | IgE антитела, связанные с защитным иммунитетом |
| Гипер-IgE синдром (синдром Джоба) | Дефект Т-супрессоров |
| Селективный IgA дефицит | Дефект Т-супрессоров |
| Синдром Вискотт-Олдриджа | Неизвестны |
| Тимусная аплазия (синдром Ди-Джорджи) | Неизвестны |
| IgE - миелома | Неоплазия IgE-продуцирующих плазматических клеток |
| Реакция "трансплантат против хозяина" | Дефект Т-супрессоров |
| II. Сниженное содержание общего IgE | |
| Атаксия - телеангиэктазия | Дефекты Т-клеток |
Ниже приведены в качестве примеров диапазоны содержания общего IgE сыворотки крови (у взрослых) при некоторых патологических состояниях (табл. 3). Однако, несмотря на первоначально кажущуюся простоту использования определения общего и специфического IgE для диагностики, существуют некоторые сложности в интерпретации результатов. Их перечень приведён ниже.
Таблица 3: Значения общего IgE при некоторых патологических состояниях
| Патологические состояния | Содержание IgE (кЕ/л) |
|---|---|
| Аллергический ринит | 120 - 1000 кЕ/л |
| Атопическая бронхиальная астма | 120 - 1200 кЕ/л |
| Атопический дерматит | 80 - 14000 кЕ/л |
| Аллергический бронхолегочный аспергиллез: - ремиссия - обострение | 80 - 1000 кЕ/л 1000 - 8000 кЕ/л |
| Гипер - IgE синдром | 1000 - 14000 кЕ/л |
| IgE - миелома | 15000 кЕ/л и выше |
Особенности интерпретации и диагностические ограничения общего IgE
- Примерно 30% больных атопическими заболеваниями имеют уровень общего IgE в пределах значений нормы.
- Некоторые больные бронхиальной астмой могут иметь повышенную чувствительность только к одному аллергену (антигену), в результате чего общий IgE может быть в пределах нормы, в то время как кожная проба и специфический IgE будут положительными.
- Концентрация общего IgE в сыворотке крови также повышается при неатопических состояниях (особенно при глистной инвазии, некоторых формах иммунодефицитов и бронхопульмональном аспергиллезе) с последующей нормализацией после соответствующего лечения.
- Хроническая рецидивирующая крапивница и ангионевротический отёк не являются обязательными показаниями для определения общего IgE, так как обычно имеют неиммунную природу.
- Границы нормы, определённые для европейцев, не могут быть применены для представителей зон, эндемичных по гельминтозам.
Особенности интерпретации и диагностические ограничения специфического IgE
- Доступность определения специфического IgE не должна преувеличивать его диагностическую роль в обследовании больных с аллергией.
- Обнаружение аллергенспецифического IgE (к какому-либо аллергену или антигену) не доказывает, что именно этот аллерген ответственен за клиническую симптоматику; окончательное заключение и интерпретация лабораторных данных должны быть сделаны только после сопоставления с клинической картиной и данными развёрнутого аллергологического анамнеза.
- Отсутствие специфического IgE в сыворотке периферической крови не исключает возможности участия IgE-зависимого механизма, так как местный синтез IgE и сенсибилизация тучных клеток может происходить и в отсутствие специфического IgE в кровотоке (например, аллергический ринит).
- Антитела других классов, специфичные для данного аллергена, особенно класса IgG (IgG4), могут быть причиной ложноотрицательных результатов.
- Исключительно высокие концентрации общего IgE, например, у отдельных больных атопическим дерматитом, могут за счёт неспецифического связывания с аллергеном давать ложноположительные результаты.
- Идентичные результаты для разных аллергенов не означают их одинакового клинического значения, так как способность к связыванию с IgE у разных аллергенов может быть различной.
В заключении, учитывая всё выше изложенное, а также существующие сложности в постановке и интерпретации кожных проб, перечислим основные показания и противопоказания к назначению специфического аллергологического обследования in vitro - определения специфического IgE (табл. 4).
Таблица 4: Показания и противопоказания к определению специфического IgE
| Показания | |
|---|---|
| 1 | Дифференциальная диагностика между IgE-зависимым и не-IgE-зависимым механизмами аллергических реакций |
| 2 | Больные, у которых невозможно выявить аллерген анамнестически, при помощи дневника и т. д. |
| 3 | Больные с недостаточным эффектом специфической гипосенсибилизации, назначенной по результатам кожных проб |
| 4 | Дермографизм и распространённый дерматит |
| 5 | Больные детского и пожилого возраста с гипореактивностью кожи |
| 6 | Гиперреактивность кожи |
| 7 | Больные, которым невозможно отменить симптоматическую терапию препаратами, влияющими на результаты кожных проб |
| 8 | Отрицательное отношение больного к кожным пробам |
| 9 | В анамнезе системные аллергические реакции на кожные пробы |
| 10 | Несоответствие результатов кожных проб данным анамнеза и клинической картине |
| 11 | IgE-зависимая пищевая аллергия |
| 12 | Необходимость количественной оценки чувствительности и специфичности аллергена |
| 13 | Общий IgE сыворотки крови более 100 кЕ/л |
| Обследование нецелесообразно: | |
| 1 | При атопических заболеваниях в случаях удовлетворительных результатов специфической терапии по данным кожных проб |
| 2 | У больных с не-IgE-зависимым механизмом аллергических реакции |
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Клиника и диагностика поражений вирусом простого герпеса при иммунодефиците
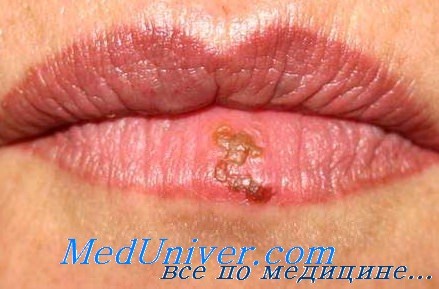
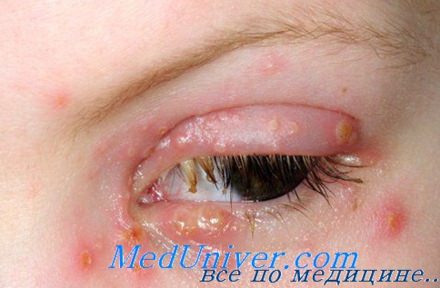
Поражение лица и ротоглотки наиболее типично для реактивации герпесвирусной инфекции. Морфология герпетических высыпаний зависит от типа пораженной эпителиальной ткани. На красной кайме губ и коже лица первичными элементами являются мелкие везикулы, которые возникают последовательно, имеют тенденцию к быстрому слиянию и формированию крупного вялого пузыря. Эти элементы умеренно болезненны, типично ощущение жжения.
После отторжения некротизированного эпителия обнажаются эрозированные кровоточащие поверхности, по краям которых появляются новые мелкие везикулы, и элемент начинает расти от центральной части к периферии.
Суперинфицирование элементов часто приводит к возникновению глубоких некрозов, заживающих с формированием рубца. Поражение лица вирусом герпеса следует дифференцировать от поражения зигомицетами (Absidia, Rhisopus, Mucor) и Aspergillus, которые вызывают тяжелые некрозы тканей лица, расплавление хрящей и костей лицевого скелета с быстрым обезображиванием внешнего облика пациента.
На слизистой оболочке рта наиболее типичным является возникновение нескольких одинаковых поверхностных некротических элементов диаметром 1—3 мм, которые затем углубляются и увеличиваются в размерах, часто сливаются. В самых тяжелых случаях значительная площадь полости рта поражена крайне болезненными глубокими некрозами серого цвета с кровоточащими участками эрозий.
В прошлом, до введения всеобщей профилактики ацикловиром, у больных после ТКМ герпетические поражения ротоглотки нередко становились причиной обструкции верхних дыхательных путей, в связи с чем возникала необходимость в протективной интубации трахеи.
Процесс заживления глубоких некрозов часто проходит стадию отторжения фибриновых пленок с обнажением ригидных сосудов десен, что может быть чревато значительной кровопотерей, особенно у детей младшего возраста. Мы наблюдали кровотечения из язв на деснах в объеме до 400 мл в сутки. Кроме того, заживление язв нередко сопровождается обильной саливацией: потерей до 700—900 мл слюны в сутки, что может стать причиной обезвоживания у детей.
Знание закономерностей развития герпетического стоматита позволяет сделать вывод, что при нейтропении лечение его нельзя ограничивать ацикловиром: необходимо назначать препараты, активные в отношении стрептококков, анаэробов, грамотрицательной флоры и грибов. Монотерапии, отвечающей таким требованиям, не существует, поэтому при фебрильной нейтропении, сопровождающейся стоматитом, мы наряду с ацикловиром всегда используем бета-лактам с расширенным спектром антианаэробной активности (пиперациллин/тазобактам, имипенем, амоксициллин/клавуланат) либо к другим бета-лактамам добавляем метронидазол.
Часто драматического улучшения удается добиться при использовании клиндамицина или пенициллина. Кроме того, мы рекомендуем и сами всегда используем системную противогрибковую терапию.
Поражение вирусом простого герпеса пищевода
При распространении инфекции из полости ротоглотки поражается верхний сегмент пищевода. Другой путь — контаминация инфицированной герпес-вирусом слюной эрозированного (в результате желудочно-пищеводного рефлюкса или рвоты) пищевода. В этом случае поражается нижний сегмент пищевода. Клиническая картина среднего и дистального эзофагита очень типична: больные жалуются на ощущение кома за грудиной, сильное жжение и боли, которые значительно усиливаются после глотания и рвоты.
Следует отметить, что последняя локализация — одно из самых опасных проявлений герпесвирусной инфекции, поскольку именно дистальный эзофагит служит воротами для развития инвазивных бактериальных и грибковых инфекций. По морфологической картине (язвенно-некротические элементы, захватывающие все слои пищевода) отличить герпетическое поражение от цитомегаловирусного, бактериального или грибкового не представляется возможным. Без проведения биопсии установить точный микробиологический диагноз невозможно.
Если принято решение выполнить эзофагоскопию и биопсию, то для диагностики герпес-вирусного поражения необходимо получить биоптат эпителия края язвы, а для диагностики ЦМВ-поражения — ее дна. Это связано с тем, что герпес-вирус поражает эпителий, а цитомегаловирус — строму.
При герпетическом эзофагите, как и при герпетическом стоматите, особенно больным с фебрильной нейтропенией, наряду с ацикловиром всегда следует назначать антимикотик системного действия (амфотерицин В внутривенно в дозе 0,3—0,5 мг/кг в сутки, флюконазол внутривенно или внутрь, возможно вориконазол и итраконазол) и системные антибиотики, обладающие антианаэробной активностью.
Важную роль играют антацидная и антирефлюксная (ранитидин или омепразол, дофаминовые антагонисты) терапия и адекватное обезболивание наркотиками.
Поражение бронхиального дерева и легких вирусом простого герпеса
Чаще всего герпетический трахеобронхит развивается у иммунокомпрометированных больных с герпетическим эзофагитом, которые интубированы и находятся на искусственной вентиляции легких. Наблюдаются также фокальные герпетические пневмонии. Диффузные пневмонии с развитием дыхательной недостаточности, напротив, являются следствием диссеминированной герпетической инфекции у больных с глубоким дефицитом клеточного или гуморального иммунитета.
Поражение вирусом простого герпеса центральной нервной системы
Герпетический энцефалит — очень редкое проявление реактивации герпесвирусной инфекции у онкогематологических больных. Он не отличается от энцефалита у иммунокомпетентного хозяина, т. е. характеризуется энцефалитическим синдромом и признаками воспаления и некроза на компьютерных и ядерно-магнитных томограммах. Поражение спинного мозга вирусом герпеса является казуистикой. Описаны случаи восходящего поперечного миелита.
Диагностика поражений вируса простого герпеса
Известно несколько методов быстрой и специфической диагностики герпесвирусной инфекции. Классическим методом является выделение вируса, основанное на его цитопатическом действии на чувствительные культуры клеток млекопитающих. Этот метод достаточно быстрый (90 % позитивных результатов в первые 3 дня, 100% —в первые 7 дней культивирования) и весьма специфичный.
Существует более быстрый метод (комбинация иммуноферментного и культурального методов), которым выявляют наличие вирусных антигенов в чувствительной клеточной культуре, зараженной исследуемым материалом. Этот метод аналогичен описанному ранее методу shell vial для ЦМВ и позволяет получить результаты в течение суток.
Следует отметить, что, как и при ЦМВ-инфекции, серологические данные (наличие специфического IgM или повышение титра IgG) и выделение вируса простого герпеса со слюной не несут полезной оперативной информации. Особенно важно это при диагностике герпесвирусного энцефалита. Нам доводилось наблюдать неадекватную интерпретацию серологических тестов у больных с энцефалитическим синдромом и необоснованное назначение ацикловира в высоких дозах. Единственным надежным методом диагностики является проведение биопсии ткани головного мозга и вирусологического исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

