Заболевание вызываемое вирусом кишечной и синегнойной палочкой
Обновлено: 24.04.2024
Эшерихиозы – это острые, преимущественно кишечные инфекции, вызываемые некоторыми сероварами бактерии Escherichia coli. Эшерихиозы проявляются в виде энтерита и энтероколита, могут генерализоваться и протекать с внекишечной симптоматикой. Путь передачи кишечной палочки фекально-оральный. Чаще заражение происходит при употреблении зараженных молочных и мясных продуктов. Возможен и контактно-бытовой путь передачи кишечной инфекции. Диагноз эшерихиоза устанавливается при выявлении эшерихий в рвотных и каловых массах, а при генерализации инфекции - в крови. Лечение эшерихиозов состоит из диеты, регидратационной терапии, применения противомикробных средств и эубиотиков.
МКБ-10
Общие сведения
Эшерихиозы (коли-инфекции) - группа инфекций, вызываемой кишечной палочкой и протекающих с поражением ЖКТ, мочевых путей, респираторного тракта, мозговых оболочек, бактериемией. Чаще встречаются у детей раннего возраста. Наиболее распространены кишечные инфекции, вызванные эшерихией: они являются самой частой причиной диареи у младенцев и взрослых. Некоторые штаммы и их токсины вызывают жизнеугрожающие поражения внутренних органов.
Причины эшерихиозов
Escherichia coli (кишечная палочка) представляет собой короткие полиморфные грамотрицательные палочковидные бактерии, непатогенные штаммы которых присутствуют в составе нормальной кишечной флоры. Эшерихиоз вызывают диареегенные серовары следующих групп:
- энтеропатогенные (ЭПКП);
- энтеротоксигенные (ЭТКП);
- энтероинвазивные (ЭИКП);
- энтерогеморрагические (ЭГКП);
- энтероадгезивные (ЭАКП).
Эшерихии устойчивы во внешней среде, могут сохранять жизнеспособность в почве, воде и фекалиях до нескольких месяцев. В пищевых продуктах (в особенности в молоке) размножаются, образуя многочисленные колонии, легко переносят высушивание. Кишечные палочки погибают при кипячении и действии дезинфицирующих средств.
Эпидемиология
Резервуаром и источником инфекции являются больные люди или здоровые носители. Наибольшее эпидемическое значение в распространении возбудителя имеют лица, больные эшерихиозами, вызванными видами ЭПКП и ЭИКП, остальные группы бактерий менее опасны. Больные эшерихиозами, обусловленными заражением ЭТКП и ЭГКП контагиозны только в первые дни заболевания, в то время как ЭИКП и ЭПКП группы кишечных палочек выделяются больными 1-2 (иногда 3) недели. Выделение возбудителя может продолжаться довольно долго, в особенности у детей.
Механизм передачи кишечной палочки – фекально-оральный, чаще всего реализуется пищевой путь заражения для ЭТКП и ЭИКП и бытовой для ЭПКП. Кроме того, заражение может осуществляться водным путем. Пищевое заражение в основном происходит при употреблении молочных продуктов, мясных блюд, напитков (квас, компоты) и салатов с вареными овощами.
В детских коллективах и среди лиц, пренебрегающих правилами гигиены, возможно распространение кишечной палочки контактно-бытовым путем через загрязненные руки, предметы, игрушки. Заражение возбудителями группы ЭГПК часто происходит в результате употребления недостаточно кулинарно обработанного мяса, сырого непастеризованного молока. Отмечены вспышки эшерихиозов, вызванных употреблением гамбургеров.
Реализация водного пути заражения в настоящее время мало распространена, заражение водоемов кишечной палочкой обычно происходит при сбросе сточных вод без предварительного обезвреживания. Естественная восприимчивость к эшерихиозам высокая, после перенесения инфекции формируется нестойкий группоспецифический иммунитет.
Классификация
Эшерихиозы классифицируются по этиологическому принципу в зависимости от группы возбудителя (энтеропатогенные, энтеротоксические, энтероинвазивные, и энтерогеморрагические).
- Эшерихии группы ЭПКП – преимущественно вызывают эшерихиозы у детей, в особенности на первом году жизни. Вспышки, обусловленные этой группой кишечных палочек, как правило, возникают в яслях, детских садах, роддомах и детских отделения больниц. Заражение обычно происходит контактно-бытовым путем.
- Палочки группы ЭИКП вызывают энтероколиты, протекающие по типу дизентерии у детей старше года и взрослых. Заражение происходит водным и пищевым путем, отмечается летне-осенняя сезонность. Преимущественно распространены в развивающихся странах.
- ЭТКП вызывают инфекции холероподобного течения, заражаются дети от двух лет и взрослые, заболеваемость высока в странах с жарким климатом и низкой гигиенической культурой. Заражение происходит пищевым и водным путем.
- Эпидемиологических данных в отношении инфекций, возникающих в результате поражения возбудителем группы ЭГКП, в настоящее время недостаточно для детальной характеристики. В эпидемиологии эшерихиозов основное значение играют гигиенические мероприятия, как общего, так и индивидуального характера.
Существует клиническая классификация, выделяющая гастроэнтерическую, энтероколитическую, гастроэнтероколитическую и генерализованную формы заболевания. Генерализованная форма может быть представлена коли-сепсисом или поражением кишечной палочкой различных органов и систем (менингит, менингоэнцефалит, пиелонефрит и др.). Эшерихиоз может протекать в легкой, среднетяжелой и тяжелой форме.
Симптомы эшерихиоза
Энтеропатогенный эшерихиоз
ЭПКП I класса развивается обычно у детей младшего возраста, инкубационный период составляет несколько дней, проявляется преимущественно рвотой, жидким стулом, выраженной интоксикацией и дегидратацией. Есть вероятность развития генерализованной септической формы. Взрослые заболевают ЭПКП II класса, болезнь протекает по типу сальмонеллеза.
Энтероинвазивный эшерихиоз
Для поражения ЭИКП характерно течение наподобие дизентерии или шигеллеза. Инкубационный период длится от одного до трех дней, начало острое, отмечается умеренная интоксикация (головная боль, слабость), лихорадка в пределах от субфебрильных до высоких значений, озноб. Затем появляются боли в животе (преимущественно вокруг пупка), диарея (иногда с прожилками крови, слизью). Пальпация живота отмечает болезненность по ходу толстой кишки. Нередко эшерихиоз этого вида протекает в легкой и стертой форме, может отмечаться среднетяжелое течение. Обычно длительность заболевания не превышает нескольких дней.
Энтеротоксигенный эшерихиоз
Поражение ЭТКП может проявляться клиническими симптомами, сходными с таковыми при сальмонеллезе, пищевой токсикоинфекции или напоминать легкую форму холеры. Инкубационный период составляет 1-2 дня, интоксикация слабо выражена, температура обычно не повышается, отмечается многократная рвота, обильная энтеритная диарея, постепенно нарастает дегидратация, отмечается олигурия. Имеют место боли в эпигастральной области, носящие схваткообразный характер.
Энтерогеморрагический эшерихиоз
ЭГКП развивается чаще всего у детей. Интоксикация при этом умеренная, температура тела субфебрильная. Имеет место тошнота и рвота, жидкий водянистый стул. При тяжелом течении к 3-4 дню, заболевания появляются сильные боли в животе схваткообразного характера, диарея усиливается, в испражнениях, утрачивающих каловый характер, могут отмечать примесь крови и гноя.
Чаще всего заболевание через неделю проходит самостоятельно, но при тяжелом течении (в особенности у детей младшего возраста) на 7-10 день, после исчезновения диареи, есть вероятность развития гемолитико-уремического синдрома (сочетание гемолитической анемии, тромбоцитопении и острой почечной недостаточности). Нередки нарушения мозговой регуляции: судороги конечностей, ригидность мускулатуры, нарушения сознания вплоть до сопора и комы. Летальность больных с развитием этой симптоматики достигает 5%.
Осложнения
Обычно эшерихиозы не склонны к осложнениям. В случае инфекции, спровоцированной возбудителем группы ЭГКП, есть вероятность возникновения осложнений со стороны мочевыделительной системы, гемолитическая анемия, церебральные расстройства.
Диагностика
Для диагностики эшерихиоза производится выделение возбудителя из кала и рвотных масс, в случаях генерализации – из крови, мочи, желчи или ликвора. После чего производится бактериологическое исследование, посев на питательных средах. В связи с антигенным сходством возбудителей эшерихиоза с бактериями, входящими в состав нормоциноза кишечника, серологическая диагностика малоинформативна.
Для лабораторной диагностики инфекций, вызванных ЭГКП, может применяться выявление бактериальных токсинов в испражнениях пациентов. При этом виде эшерихиозов в анализе крови могут быть отмечены признаки гемолитической анемии, повышение концентрации мочевины и креатинина. Анализ мочи обычно показывает протеинурию, лейкоцитурию и гематурию.
Лечение эшерихиоза
Лечение преимущественно амбулаторное, госпитализации подлежат больные с тяжелыми формами и высоким риском развития осложнений. Больным рекомендована диета. На период острых клинический проявлений (диареи) – стол №4, после прекращения – стол №13. Умеренная дегидратация корректируется приемом жидкости и регидратационных смесей перорально, при нарастании и выраженной степени обезвоживания производят внутривенное вливание растворов. Патогенетическое лечение выбирают в зависимости от вида возбудителя.
В качестве противомикробной терапии обычно назначаются препараты нитрофуранового ряда (фуразолидон), либо (при тяжелом течении инфекции, вызванной ЭИКП) фторхинолоны (ципрофлоксацин). Препараты назначают на 5-7 дней. Лечение эшерихиозов ЭПКП у детей целесообразно осуществлять с помощью комбинации сульфаметоксазола и триметоприма, антибиотикотерапии. Генерализованные формы лечат цефалоспоринами второго и третьего поколений.
В комплексную терапию при продолжительном течении заболевания для нормализации пищеварения и восстановления биоценоза кишечника включают ферментные препараты и эубиотики. Современные принципы лечения эшерихиозов, спровоцированных бактериями группы ЭГКП, включают применение антитоксических терапевтических мер (сыворотки, экстракорпоральная адсорбция антител).
Прогноз
Прогноз для взрослых и детей старшего возраста – благоприятный, при легком течении отмечаются случаи самостоятельного выздоровления. Дети раннего возраста могут страдать эшерихиозом в тяжелой форме, что ухудшает прогноз. Также заметно труднее идет выздоровление в случае генерализации и развития осложнений. Некоторые особо тяжелые формы эшерихиозов могут без должной медицинской помощи закончиться смертью.
Профилактика
Эшерихиозы – заболевания, связанные с низкой гигиенической культурой. Личная профилактика этих инфекций заключается в следовании гигиеническим нормам, в особенности при общении с детьми, мытье рук, пищевых продуктов, игрушек и предметов быта. Общая профилактика направлена на контроль соблюдения санитарно-гигиенического режима в детских учреждениях, предприятиях пищевой промышленности, лечебно-профилактических учреждениях, а также контроль над стоком канализационных отходов и состоянием источников воды.
Больные после перенесения эшерихиоза выписываются из стационара после клинического выздоровления, а также по результатам трехкратной бактериологической пробы. Допуск в коллектив детей, контактировавших с больным, также осуществляется после проведения бактериологической диагностики и подтверждения отсутствия выделения возбудителя. Лица, выделяющие патогенные эшерихии, подлежат изоляции на весь период контагиозности. Работники пищевой промышленности подвергаются регулярным обследованиям на предмет выделения возбудителя, в случае положительного теста – отстраняются от работы.
МКБ-10
B96.5 Pseudomonas (aeruginosa) (mallei) (pseudomallei) как причина болезней, классифицированных в других рубриках
Общие сведения
Синегнойная инфекция впервые была описана в 1850 году французским хирургом Седилем. В 1882-м французскому военному фармацевту Жессару удалось выделить чистую культуру возбудителя, а в 1916 году стала известна эпидемиология данного заболевания. Болезнь распространена повсеместно, бактерий обнаруживают в почве, воде и на растениях. Четкая сезонность отсутствует. В стационарах излюбленной локализацией считается физиотерапевтическое и реанимационное оборудование. Группами риска являются недоношенные новорожденные, дети до 3-х месяцев, пожилые, пациенты отделений гемодиализа, химиотерапии, нейрохирургии и реанимации, больные с муковисцидозом и иммуносупрессией.

Причины
Возбудитель заболевания – синегнойная палочка (Pseudomonas aeruginosa) и её штаммы, представляет собой условно-патогенный микроорганизм, способный вызывать поражение только при отсутствии адекватного ответа иммунной системы. Источником инфекции служат больные люди и животные, бактерионосители, преимущественная локализация микроорганизма – кожа, кишечник. Заражение происходит воздушно-капельным и пищевым путем. Путь инфицирования при госпитальном заражении чаще контактный – через нестерильный инструментарий, руки медицинского персонала и предметы ухода за больными. Бактерия погибает при кипячении, во время автоклавирования, а также при воздействии 3% перекиси водорода и хлорсодержащих дезинфектантов.
Патогенез
При попадании микробов на поврежденную кожу или слизистую оболочку возникает массивная деструкция тканей, обусловленная воздействием экзотоксинов и продуцируемых бактериями веществ. В норме слизистая организма способна нивелировать воздействие синегнойной палочки ввиду мукоцилиарного клиренса и механического барьера. Привлечение нейтрофилов и активный фагоцитоз усиливают образование множества антибактериальных цитокинов, ферментов и свободных радикалов, служат активаторами системы комплемента и других звеньев гуморального иммунитета.
От 33 до 83% штаммов синегнойной палочки имеют эволюционно обусловленный механизм защиты от иммунной системы – образование биопленок, состоящих из скопления пораженных клеток и внеклеточного матрикса, включающего фибрин, секреторное отделяемое слизистых, альгинат, полисахариды и липиды. Известно, что бактерии лизируют нейтрофилы, усиливая рост собственных биопленок.
Классификация
Поражения, вызываемые синегнойной палочкой, можно условно разделить на местные и генерализованные (септические). Некоторые виды, в том числе инфекции ЦНС, сердца и средостения развиваются вследствие диссеминации возбудителя. В зависимости от топологии воспалительного очага различают следующие формы синегнойной инфекции:
- Инфекция респираторного тракта. Пациенты, находящиеся на длительной искусственной вентиляции легких, в 30% случаев переносят трахеобронхит и в 24% – пневмонию синегнойной этиологии.
- Инфекция ЛОР-органов. Синуситы развивается редко, при этом до 40% хронических средних отитов приходится на долю синегнойной палочки.
- Инфекция ЖКТ. Проявляется в виде тяжелой диареи, нередко с летальным исходом среди детей до года. С возбудителем связывают около 16% послеоперационных перитонитов.
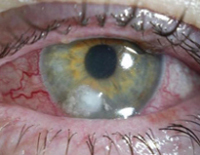
- Инфекция глаз. Связана с длительным применением контаминированных контактных линз и глазных капель, часто приводит к панофтальмиту.
- Инфекция мочевой системы. Наиболее вероятно развитие катетер-ассоциированного острого пиелонефрита. С данным возбудителем связывают до 13% случаев острого простатита.
- Инфекция кожи. Возникает после пребывания в бассейне со сниженной концентрацией дезинфицирующих средств, может поражать ногти, подкожную клетчатку, мышечные фасции с формированием некрозов.
- Раневая инфекция. Составляет до 10% всех боевых инфекционных осложнений, становится причиной около 30% гнойных процессов при ожоговой болезни. Считается поддерживающим фактором формирования трофических язв.
Симптомы синегнойной инфекции
Инкубационный период патологии крайне вариабелен, может составлять от нескольких суток до десятилетий, поскольку микроорганизм является одним из условно-патогенных компонентов микрофлоры человека. Клинические проявления зависят от пораженного органа. У взрослых при инвазии пищеварительного тракта первыми симптомами являются лихорадка (не более 38,5° C), снижение аппетита, озноб, слабость, тошнота, реже рвота, вздутие и болезненность живота, частый кашицеобразный стул с кровью и слизью.
Маленькие дети при поражении ЖКТ становятся вялыми, сонливыми, отказываются от еды и питья, срыгивают, гастроэнтероколит протекает с высоким риском кишечного кровотечения. Синегнойная патология ЛОР-органов проявляется лихорадкой 37,5° C и выше, резкой болью в ухе, снижением слуха, желто-зеленым обильным отделяемым, иногда с примесью крови. Поражение дыхательного тракта протекает в форме пневмонии – с повышением температуры тела более 38° C, нарастающей одышкой, кашлем с обильной слизисто-гнойной мокротой.
Псевдомонадная инфекция мочевыводящей системы характеризуется лихорадкой, болями в пояснице, частыми болезненными мочеиспусканиями, чувством неполного опорожнения мочевого пузыря, изменением цвета и запаха мочи. Глазные симптомы инвазии синегнойной палочки чаще выявляются в области одного глазного яблока, начинаются с появления рези, болей, чувства жжения, инородного тела, слезотечения, светобоязни и слизисто-гнойного обильного отделяемого. В дальнейшем может возникать снижение и помутнение зрения.
Поражение кожи проявляется высыпаниями в виде пятен и гнойничковых элементов по всему телу, включая сыпь на ладонях, подошвах и в носоглотке, увеличением лимфоузлов, постоянными головными болями (так называемая головная боль пловцов), зеленой окраской одной, реже двух ногтевых пластин, образованием болезненных уплотнений в подкожно-жировой клетчатке. Раневая инфекция возбудителя сопровождается появлением сине-зеленого гнойного отделяемого и гнойно-геморрагических корочек, увеличением зоны покраснения вокруг раны.
Осложнения
Мультисистемность и клиническое разнообразие симптомов синегнойной инфекции отражается на количестве осложнений данного состояния. К наиболее частым негативным последствиям относят генерализацию инфекционного процесса, инфекционно-токсический шок, у грудных детей – некротический колит. Высока вероятность абсцедирования и гангренозных изменений. Вялотекущее течение инфекции на слизистых уха, ротоглотки, носа, конъюнктивы и легких приводит к хронизации воспалительного процесса, формированию мезотимпанита, бронхоэктазов, ползучей язвы роговицы, частичной или полной глухоты, односторонней слепоты.
Диагностика
Диагноз выставляется на основании данных, полученных в ходе консультации инфекциониста. При возникновении обширных гнойных поражений обязательна консультация хирурга, по показаниям приглашаются другие профильные специалисты. Наиболее распространенными диагностическими методами подтверждения псевдомонадной этиологии болезни являются следующие инструментальные и лабораторные исследования:
- Физикальное обследование. При объективном осмотре обращают внимание на цвет раневого отделяемого, наличие сыпи. Поражение наружного уха, глаз проявляется гиперемией, обильным слизисто-гнойным отделяемым. В легких при пневмонии выслушивается ослабление дыхания, при перкуссии – притупление звука. В случае гастроэнтероколита обнаруживается болезненность по ходу кишечника, урчание; обязательно проводится визуальная оценка испражнений.
- Лабораторные исследования. Общеклинический анализ крови свидетельствует о наличии лейкоцитоза, палочкоядерного сдвига влево, ускорения СОЭ. В биохимических параметрах наблюдается увеличение АЛТ, АСТ, СРБ, снижение общего белка, гипоальбуминемия. В общем анализе мочи возможна протеинурия, гематурия. Анализ мокроты подтверждает большое число бактерий и лейкоцитов. В ликворограмме при поражениях головного мозга выявляется нейтрофильный плеоцитоз, клеточно-белковая диссоциация.
- Выявление инфекционных агентов. Золотым стандартом является бактериологическое исследование, осуществляемое в современных условиях методом масс-спектрометрии с обязательным определением антибактериальной чувствительности бактерии. Обнаружение возбудителя возможно с помощью ПЦР биологического материала из патологического очага. Серологическая диагностика (ИФА) выполняется неоднократно с промежутком не менее 10-14 суток для детекции роста титра антител.
- Инструментальные методики. Рентгенография органов грудной клетки, реже МРТ или КТ проводится с целью верификации легочных поражений, дифференциального диагноза. УЗИ органов брюшной полости, мочеполовой системы, мягких тканей, костей и забрюшинного пространства позволяет установить первичный очаг воспаления. Эхо-КГ показана при подозрении на инфекционный эндокардит. Колоноскопия, ФГДС назначаются с целью исключения новообразований пищеварительного тракта.
Дифференциальная диагностика синегнойной инфекции сложна ввиду многообразия клинических форм болезни. Наиболее распространенные поражения желудочно-кишечной системы дифференцируют с сальмонеллезом, шигеллезом и псевдомембранозным колитом. Кожные проявления отличают от гнойно-некротических поражений стрептококковой и стафилококковой этиологии. Инфекции дыхательной системы могут напоминать казеозную пневмонию при туберкулезе, саркоидоз, бактериальные воспаления легких. Причинами сепсиса могут быть различные вирусы, бактерии и грибы.
Лечение синегнойной инфекции
Стационарное лечение рекомендуется пациентам с органными поражениями, среднетяжелым и тяжелым течением болезни. Больные с нозокомиальной синегнойной инфекцией продолжают лечение в том отделении, где находились до манифестации инфекционного процесса, с обязательным проведением всех противоэпидемических мероприятий и санацией аппаратуры. Постельный режим необходим до устойчивого купирования лихорадки в течение 3-5 дней, его продолжительность зависит от степени инвазии, наличия осложнений и декомпенсации сопутствующих болезней. Специальная диета не разработана, рекомендован прием пищи с достаточным количеством белка, адекватный питьевой режим.
Средствами борьбы с инфекцией считаются гипериммунная антисинегнойная донорская плазма и противосинегнойный гамма-глобулин, Перечисленные препараты применяются реже в связи с возможным развитием сывороточной болезни, показаны при вялотекущем воспалительном процессе. Симптоматическое лечение включает дезинтоксикационную терапию, противовоспалительные и жаропонижающие средства. Хирургическое вмешательство необходимо при локализованных и разлитых гнойных процессах, заключается во вскрытии и дренировании гнойников, реже – ампутации конечности. Допускается местное применение раствора перекиси водорода, мазей с антибиотиками.
Прогноз и профилактика
Специфическая профилактика (поливалентная вакцина) показана медицинским работникам, ожоговым больным, пациентам с открытыми переломами и глубокими ранами, лицам с иммунным дефицитом, людям старческого возраста. Неспецифические меры сводятся к строгому соблюдению правил обработки медицинских инструментов и оборудования, контролю контаминации синегнойной палочкой персонала. Важны общеукрепляющие методы – закаливание, нормальный сон, полноценная еда, прогулки, физическая активность, неукоснительное соблюдение личной гигиены и своевременная санация гнойных очагов.
1. Pseudomonas aeruginosa: патогенность, патогенез и патология / Лазарева А.В., Чеботарь И.В.// Клиническая микробиология и антимикробная химиотерапия – 2015 – Т.17, №3.
3. Эпидемиология и профилактика синегнойной инфекции. Федеральные клинические рекомендации / Егорова О.Н., Брусина Е.Б. и др. – 2014.
Знакомьтесь с героиней нашего сегодняшнего повествования – синегнойной палочкой или Pseudomonas aeruginosa (P.aeruginosa).
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач-клинический фармаколог Трубачева Е.С.
Знакомьтесь с героиней нашего сегодняшнего повествования – синегнойной палочкой или Pseudomonas aeruginosa (P.aeruginosa).
.jpg)
И, воспользовавшись ситуацией, мы поговорим о микробиологической безопасности лечебных учреждений, ведь именно этот возбудитель до сих является одним из лидеров внутрибольничных инфекций, особенно в условиях реанимационных, хирургических, онкологических и ожоговых отделений, и, казалось бы, эта проблема не решаемая. О том, как победить этого зверя-убийцу и не разорится, мы сегодня и поговорим.
Микробиологические аспекты
Pseudomonas aeruginosa – это аэробная грамотрицательная палочка, с одним или двумя полярно расположенными жгутиками, которая может расти и размножаться и в анаэробных условиях.
Это один из немногих возбудителей, который угадывается в прямом смысле носом – инфицированная рана издает совершенно неповторимое амбрэ, которое не перепутаешь ни с чем, если услышал хотя бы один раз. Причем больной обнаруживается в прямом смысле по запаху от двери не то, что палаты, а от входа в лечебное отделение. Для тех, кто пока ни разу не сталкивался, – он слышится как запах сладкой карамели с аммиаком, вызывающий отчетливые рвотные позывы (хотя последнее строго индивидуально). Некоторые ощущают его как аромат жасмина в аммиаке. Запах очень специфический и способен играть серьезную диагностическую роль, а уж если к нему в дополнение идут сине-зеленые повязки, и это не вылитый ранее флакон зеленки, то перед вами на 99,9% рана, инфицированная P.aeruginosa. Согласитесь, это важно, особенно в условиях как недостатка микробиологических лабораторий, так и широкого распространения возбудителя в стационарах.
Дикая почвенная синегнойка, являющаяся родоначальницей всех внутрибольничных форм, будет выглядеть следующим образом. Как вы можете видеть, убить ее можно абсолютно всем с применением обычных терапевтических дозировок. (картинка 1)
В природе синегнойная палочка обитает в почве и воде, при этом она непривередлива в плане питательных веществ (в дистиллированной воде растет и размножается до 2,5 месяцев, хотя и снижает свою активность в десять раз). Поэтому идеальной средой ее обитания будет та локализация в организме, где темно, тепло и сыро, а именно – раны, нижние дыхательные пути, мочевыводящие пути и все те полости, в которые можно установить катетеры. Конечно, самостоятельно палочка туда не заползет, у нее нет ножек, зато мы – медицинский персонал, не соблюдая правила обработки рук и имея единственного больного в отделении, к концу смены обсеменим всех, особенно если в ординаторских и сестринских используются общие, а не одноразовые бумажные, полотенца.
P.aeruginosa очень любит, когда вокруг нее тепло (30 – 37 0 С), темно и сыро. Соответственно, самое чистое время года с точки зрения риска принести дикую уличную палочку в стационар – это зима. И если зимой в вашем на 100% чистом стационаре с внутренним микробиологическим контролем вдруг пациент, простите, завонял – ищите любителя-огородника с рассадой на подоконнике. Достаточно такому садоводу-огороднику один раз по приходу на работу не отмыть правильно руки и пойти на перевязку – больной с синегнойной (или ацинетобактерной, а то и вообще микст) инфекцией на ровном месте будет обеспечен. А если все остальные так же правильно не помыли руки или вытерлись общим полотенцем – чистый стационар очень быстро станет стационаром с синегнойкой.
Синегнойная палочка является активным пленкообразователем. В этом процессе участвует вырабатываемая микробом внеклеточная слизь, покрывающая саму клетку тонким слоем. Процесс пленкообразования условного возбудителя наглядно показан на данном видео. Как мы обсуждали ранее, микробы – это не статичные существа, которые всю жизнь питаются и размножаются, они способны вести достаточно бурную социальную жизнь, и синегнойная биопленка тому наглядный пример, поэтому о ней стоит поговорить поподробнее. Когда палочка прикрепляется к поверхности, она тут же образует монослой из микроколоний, покрытых экзополисахаридом. Затем бактерии образуют множество пилей, которыми скрепляются в том числе и друг с другом и вся структура образует полисахаридную матрицу. Когда биопленка созреет (это занимает в среднем неделю), то она становится эластичной и упругой, напоминая резину или силиконовую стельку, и точно так же обеспечивает защиту включенных в нее микроорганизмов от воздействий антибиотиков, антисептиков, дезенфектантов и иммунных клеток организма хозяина. При этом внутри самой биопленки бактерии активно обмениваются факторами вирулентности и антибиотикорезистентности и отшнуровывающиеся в последующем от пленки новые палочки будут обладать всем набором факторов защиты, характерным для материнской биопленки. Так выглядит один из способов получения вооруженной до зубов внутрибольничной микрофлоры, которая убивает пациентов и которую фактически невозможно убить в пациентах в виду как недоступности для действующих агентов (биопленка), так и в виду наличия механизмов антибиотикорезистентности, вплоть до металло-бета-лактамаз, разрушающих все до одного существующих антибиотика и большое число антисептиков и дезенфектантов.
Почему же P.aeruginosa так полюбила больницы? Да потому что здесь, в отличие от дикой среды обитания, для нее созданы идеальные условия, как в плане климата и питательных веществ, так и в плане окружения – зверю практически не требуется бороться за свое выживание с другой микрофлорой, фактически всегда за счет своих свойств синегнойка получает селективное преимущество перед другими возбудителями, которых успешно травят антисептиками, антибиотиками, заключительной дезинфекцией и УФ-излучением, оставляя сегодняшней героине расчищенную от конкурентов территорию.
Где же в стационаре создаются условия для размножения и распространения инфекции? Для этого необходимо знать следующие свойства P.aeruginosa:
Таким образом, исходя из вышесказанного, любимыми местами обитания в стационарах являются все то, что создает оптимальную для обитания теплую и влажную среду, а именно:
- краны, раковины, кафель и стыки между ними у раковин и моек, сан. узлы, тряпочные общие полотенца ординаторских и сестринских
- медицинское оборудование, создающее теплую и влажную среду (аппараты ИВЛ, наркозные аппараты, аппараты для проведения диализа, испарители всех типов)
- кондиционеры открытого типа, хотя и за сплит-системами необходим постоянный уход и дезинфекция
- посуда для сдачи анализов
- руки мед. персонала
- общие, а не одноразовые полотенца
То есть любимыми отделениями для обитания в стационаре будут ожоговые и хирургические (практически все, а не только гнойная хирургия и травматология), отделения реанимации и интенсивной терапии и хирургический блок. Особняком стоят пульмонологические отделения с пациентами с муковисцидозом и онкологические стационары. При этом синегнойка может оказаться совершенно в любом отделении, переехав туда на руках медицинского персонала и разбежавшись по больным уже через тамошнее общее полотенце. Поэтому первый и главный шаг на пути борьбы с распространением синегнойной инфекции – это наши руки, точнее, правильная их обработка. После КАЖДОГО пациента. И не протирание полотенчиком на обходе, а полноценное мытье, после которого хотя бы самому себе можно сказать, что уж ты-то точно сделал все, что было возможно.
Клинические аспекты
Какие пациенты более всего чувствительны к P.aeruginosa и когда вообще ждать именно ее:
Какую патологию чаще всего вызывает (а лучше сказать, осложняет) P.aeruginosa
То есть почти любая область поражения и это говорит нам о крайней необходимости микробиологической диагностики, так как почти точно такой же набор может вызвать нозокомиальный золотистый стафилококк или ацинетобактер.
Эпидемиологические аспекты
Как уже выше было неоднократно сказано – P.aeruginosa умеет поражать практически все, до чего сможет добраться, а уж убивать, да в своих нозокомиальных формах, когда из биопленок вылупились и распространились супермутанты, тем более. Вопрос в том, что делать, ведь ситуация кажется безнадежной. Но это не так.
Вылечить больных мы, конечно, можем, но только в том случае, если перед нами дикая и непуганая P.aeruginosa с улицы. Если случилось так, что в вашем стационаре она живет годами и смогла инфицировать пациента (а сама она не может, ее надо донести на чьих-то медицинских руках или до пациента, или до аппарата, который используется у этого пациента), то тут фармакология почти бессильна, так как внутрибольничные палочки умеют разрушать все до одного антибиотика, имеющегося на рынке, а новых уже лет 10 не было, и неизвестно когда будут, если вообще будут. Поэтому единственным барьером встает эпидемиологический надзор. Причем синегнойку, в отличие от фекальной микрофлоры, из стационара выбить можно полностью, так как в норме она не является элементом нормальной микрофлоры человека, как та же кишечная палочка, клебсиелла или энтерококки, то есть в людях в норме она не живет.
Почему в этой статье нет антибиотикограмм устойчивых форм? Ответ до банальности прост – автор долгое время проработала в стационаре, свободном от синегнойки. Это достижимо, и от P.aeruginosa можно освободится даже в самом запущенном случае, что не будет стоить колоссальных денег, при том, что в перспективе высвобождаются действительно серьезные средства, которые ежегодно тратятся на тушение пожара антибиотиками, что в случае внутрибольничных инфекций равноценно тушению бензином. Для достижения полного антисинегнойного эффекта необходимо:
- Правильно мыть руки после каждого пациента
- Менять перчатки после каждого пациента (вместе с мытьем рук)
- Прекратить практику использования общих полотенец и полотенец на обходе
- Ввести тотальный микробиологический мониторинг
- Если есть эпидемиолог, с него требовать доступ к антисептикам и дезенфектантам нескольких видов, а также постоянное наличие одноразовых расходных материалов (это его вопрос, как он будет с начальством договариваться, но все одноразовое обязано быть одноразовым и в достаточных количествах – так как отодрать синегнойную пленку обычными методами, как вы видели, фактически нереально)
- В идеале всю группу антисинегнойных препаратов необходимо вывести из общебольничного оборота и назначать только специально обученным клиническим фармакологом. Таким образом, удастся снизить антимикробную нагрузку на внутрибольничную флору, уменьшить ее селективность и снизить вероятность селекции нозокомиальных штаммов самой P.aeruginosa
В заключении хотелось бы отметить еще раз – данная статья не про то, как победить синегнойку голыми руками антибиотиками. Этого еще пока никому не удавалось, так как проблема не в одном больном с диким возбудителем. От антибиотиков в этом деле зависит процента два в лучшем случае (приблизительно столько диких форм к вам может прийти за год). Проблема носит глубокий системный характер, и без усилий по освобождению всего стационара от P.aeruginosa, использование только и исключительно антибиотиков на каждый случай, особенно внутрибольничного инфицирования, будет сизифовым трудом с соответствующим печальным результатом.
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С.,
врач – клинический фармаколог
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Микробиологические аспекты
E.coli относится к типичным представителям семейства Enterobacteriaceae, являясь грамотрицательной бактерией, факультативным анаэробом в составе нормальной кишечной микрофлоры человека. Но тут же становится патогеном, выбравшись из среды нормального обитания, хотя отдельные штаммы являются патогенными и для желудочно-кишечного тракта. То есть кишечная палочка относится к кишечным комменсалам, кишечным патогенам и внекишечным патогенам, каждый из которых мы кратко разберем.
К штаммам E.coli, действующим как кишечные патогены и встречающимся чаще других, относятся:
- Штамм серотипа O157:H7 (STEC O157) или так называемый энтерогеморрагический штамм E.coli, который является причиной 90% случаев геморрагических колитов и 10% случаев гемолитико-уремического синдрома. Встречается достаточно часто, а если вы работаете в стационарах плановой помощи, то это один из обязательных анализов для принятия решения о госпитализации, так что так или иначе он на слуху. Проблема инфицирования этим возбудителем связана с употреблением плохо термически обработанной пищи и передачи штамма контактным путем от человека к человеку, проще говоря, через руки.
- Второй крайне опасный высоко-патогенный штамм кишечной палочки – O104:H4, вызвавший в Германии 2011 году эпидемию с высоким уровнем смертности среди пациентов с пищевыми токсико-инфекциями вследствие развития гемолитико-уремического синдрома. Если помните, это была очень громкая история с перекрытиями границ для испанских огурцов, потом вообще для всей плодоовощной продукции из Европы в Россию, пока искали хотя бы источник, не говоря уж о виновнике тех событий. Окончательно виновными тогда были обозначены листья салата, в поливе которых использовалась вода с признаками фекального заражения, а затем речь пошла уже о пророщенных семенах, которые так же полили фекально-зараженной водичкой. Так вышли на конкретный штамм E.coli – O104:H4, который, подвергшись санации антибиотиком, выплескивает эндотоксин, вызывающий гемолиз и острую почечную недостаточность. В итоге – массовая летальность пациентов, получавших антибиотики.
Затем тот же штамм обнаружился при вспышке ПТИ в Финляндии, но к тому времени пациентов с диареями до появления микробиологических результатов перестали лечить бактерицидными антибиотиками и ситуация была купирована в зародыше.
И третий громкий (для нашей страны) случай – это массовое заболевание питерских школьников в Грузии, где так же был выявлен этот штамм (пресс-релиз Роспотребнадзора по данному случаю лежит здесь).
Когда кишечная палочка выступает внекишечным патогенном? Почти всегда, когда обнаруживается вне места своего нормального обитания.
- Заболевания мочевыводящий путей. Здесь E.coli является абсолютным лидером и играет ведущую роль в развитии:
- Острых циститов
- Пиелонефритов
- Абсцессов почек и
- Простатитов
Этот факт объясняется близким анатомическим расположением двух систем и огрехами в личной гигиене, что позволяет на этапе эмпирической терапии вышеперечисленных заболеваний сразу же назначать препараты, активные в отношении кишечной палочки.
- Заболевания желудочно-кишечного тракта:
- Диарея путешественников
- Интраабдоминальные абсцессы и перитониты, чаще всего носящие вторичный характер (прободение кишки в результате первичного заболевания, либо при дефектах оперативного вмешательства)
- Инфекции центральной нервной системы у очень ослабленных пациентов, результатом чего будет развитие менингитов. Встречается в основном у лиц старческого возраста и новорожденных. Кроме того, в случае внутрибольничного заражения менингит может развиться в результате плохой обработки рук медицинского персонала перед оперативным вмешательством или перевязками.
- Инфекции кровотока, а именно сепсис, как продолжение развития заболеваний мочевыводящих путей, ЖКТ и билиарного тракта вследствие метастазирования очага инфекции. Лечению поддается крайне тяжело, особенно если задействованы внутрибольничные штаммы, летальность чрезвычайно высокая.
- Инфекции кожи и мягких тканейкак следствие раневых инфекций после вмешательств на органах брюшной полости.
- Внутрибольничные пневмонии, вызванные устойчивыми штаммами кишечной палочки, целиком связаны с дефектами ухода за пациентом и фактором чистоты, точнее ее отсутствия, рук медицинского персонала или ухаживающих родственников. Факт внутрибольничного заражения доказывается элементарно, что будет наглядно продемонстрировано в следующем разделе.
- Послеродовые (и не только) эндометриты. Вынуждены упомянуть и эту патологию, так как инфицирование кишечной палочкой встречается все чаще и чаще, а большой настороженности нет. Как результат, можно очень сильно промахнуться с антибактериальной терапией и, как следствие, прийти к экстирпации органа в виду неэффективности антибиотикотерапии. Натолкнуть на мысль может более позднее, чем обычно, поступление и более агрессивное, чем обычно течение. Дополнительный осмотр прианальной области так же может натолкнуть на вероятность развития именно такого инфицирования.
(часть вторая) Практические вопросы диагностики и лечения.
Когда мы можем заподозрить, что перед нами пациент с инфекцией, вызванной кишечной палочкой?
- Пациенты с диареей, приехавшие из отпуска и все-таки смогшие прийти на прием (диарея путешественников или энтеротоксигенные штаммы E.coli).
- Пациенты со всеми заболеваниями мочевыделительной системы, в том числе беременные, но строго с наличием симптоматики (не надо лечить бессимптомную бактериурию, иначе вырастите резистентные штаммы и создадите проблему и себе, и женщине, и роддому в последующем).
- В стационарах – нозокомиальные пневмонии, послеоперационные менингиты, перитониты, сепсисы и т. д., носящие вторичный характер.
Подтвердить или полностью исключить кишечную палочку из возбудителей может только микробиологическое исследование. Конечно, в современных условиях микробиология уже становится практически эксклюзивом, но мы пришли учиться, а учится надо на правильных примерах, поэтому далее будет рассмотрен ряд антибиотикограмм, выполненных автоматизированными системами тестирования. Вдруг вам повезет, и в вашем лечебном учреждении все уже есть или в ближайшее время будет, а вы уже умеете с этим всем работать?
Если вы читаете данный цикл по порядку, то в базовом разделе по микробиологии был выложен ряд антибиотикограмм некоего микроорганизма в контексте нарастания антибиотикорезистентности, и это была наша сегодняшняя героиня – кишечная палочка.
- Начнем с дикого и крайне симпатичного штамма E.coli, который живет в кишечнике и обеспечивает синтез витамина К. С ним сталкиваются доктора амбулаторной службы у пациентов с инфекциями мочевыводящих путей или в случае госпитализации у пациентов, которые не получали антибиотики около года. И именно такую чувствительность мы имеем в виду, когда назначаем эмпирическую антибиотикотерапию
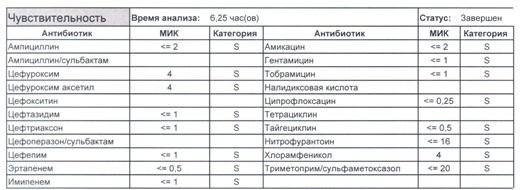
- Как видите, зверь чувствителен абсолютно ко всему, и это как раз тот случай, когда можно свободно пользоваться табличными материалами справочников или клинических рекомендаций, так как механизмы резистентности полностью отсутствуют.
- Если в ваши руки попал пациент, которого в течение последнего полугодия лечили антибиотиками пенициллинового ряда, то антибиотикограмма может выглядеть следующим образом.
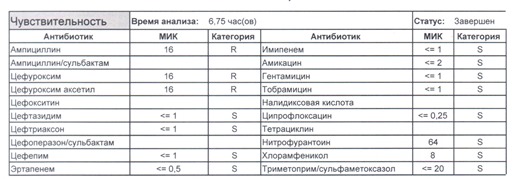
Если такая кишечная палочка окажется внекишечным патогенном, и перед вами будет беременная и ИМП (самый частый случай), то нам необходимо преодолеть резистентность к пенициллинам, то есть подавить деятельность пенициллиназ. Соответственно высокую эффективность продемонстрируют препараты с ингибиторами бета-лактамаз, чаще всего амоксициллина/клавуланат, как наиболее безопасный и эффективный. Единственное, пациентку необходимо предупредить, что в результате стимуляции рецепторов кишечника может развиться антибиотик-ассоциированная диарея.
- Отдельно хотелось бы обратить внимание на следующий штамм E.coli, как типичного обладателя бета-лактамаз расширенного спектра. И эти БЛРС чаще всего вырабатываются в результате неуемного использования цефалоспоринов третьего поколения и совершенно конкретного его представителя – цефтриаксона.
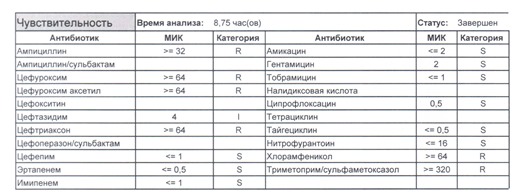
В каких ситуациях мы можем увидеть (или подумать) о таком звере:
- Пациент сам рассказывает, что получал цефтриаксон в промежутке полугодия
- Пациент был переведен из другого стационара (хотя там можно будет и следующую картинку обнаружить)
- Пациент ничего не получал, и вообще в больнице не лежал, но возбудитель попал с рук медицинского персонала, вызвав внутрибольничную инфекцию
- И самый простой случай – посев был взят в момент проведения терапии цефтриаксоном
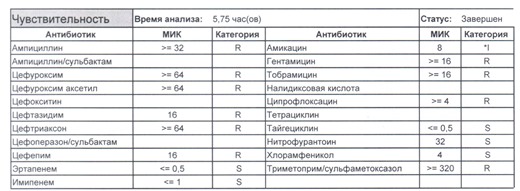
Подобный пациент не придет к вам своими ногами, его не увидит амбулаторная служба, это абсолютно стационарные больные, и если их привезут, то только из другого лечебного учреждения. Чаще всего это пациенты палат интенсивной терапии или реанимации, и такой возбудитель носит на 100% нозокомиальный характер.
Когда можем его обнаружить:
- вторичные перитониты,
- нозокомиальные пневмонии,
- пиелонефриты,
- послеоперационные менингиты,
- сепсис и т. п.
- Для эрадикации такого возбудителя нужен не просто отдельный обученный специалист и имеющая весь набор препаратов резерва аптека, но и напряженная работа эпидемиологической службы, так как подобный пациент должен быть изолирован в отдельную палату, а лучше изолятор (не подумайте, что бред – при правильной организации такие вещи вполне реальны) с проведением карантинных мероприятий, так как основная проблема появления подобного рода возбудителей в том, что они очень быстро разбегаются по всему корпусу (или стационару, если корпуса не изолированы) и обсеменяют все и вся, нанося вред другим ослабленным тяжелой болезнью пациентам и заселяя кишечники всего медицинского персонала.
- И еще одно крайне мерзкое свойство таких возбудителей – они умеют осуществлять горизонтальный перенос механизмов резистентности с другой флорой семейства Enterobacteriaceae, и даже если вы избавились от E.coli, неприятным сюрпризом может стать ее подруга клебсиелла, наносящая еще больший вред и по сути добивающая больного. Избавится полностью от этих возбудителей невозможно, для этого надо избавится от медицинского персонала как основных носителей, но контролировать можно – мероприятия подробно расписаны в действующих СанПиН 2.1.3.2630-10. Так что в случае выявления подобного возбудителя речь пойдет не только о лечении того пациента, у которого он обнаружен, но и проведения мероприятий по недопущению инфицирования всех остальных пациентов (а это, напомню, почти всегда ПИТ или ОРИТ), находящихся рядом.
- И в заключение необходимо упомянуть о панрезистентной E.coli, вооруженной полным спектром механизмов резистентности. В антибиотикограмме будут тотальные R, а МПК возбудителей пробьют все возможные потолки. К счастью для автора, она с таким зверем пока не сталкивалась, что связано с наличием работающей системы эпиднадзора, поэтому картинки не будет, хотя ее несложно представить. Такие пациенты, если кишечная палочка окажется патогеном, а не колонизатором (мало ли с чьих рук, например, в рану упала), к сожалению, почти не выживают, так как изначально являются крайне тяжелыми соматически, а кишечная палочка обычно подводит черту к их существования на бренной земле.
- Не допускать развития такой, не побоюсь этого слова, зверюги в ваших стационарах, а если появилась – гонять эпидемиологическую службу, чтобы избавляла руки и поверхности от такого рода заражения, что возможно только при условии наличия достаточного количества расходных материалов, перчаток и дезинфицирующих средств.
А теперь подведем небольшой итог нашего непростого разговора:
- Кишечная палочка – возбудитель очень серьезный и не следует его недооценивать. В ее типах также необходимо четко ориентироваться.
- В первую очередь о ней мы думаем при лечении инфекций мочевыводящих путей, особенно у беременных.
- Если перед нами пациент с признаками кишечной инфекции, то подход к терапии антибиотиками должен быть сугубо индивидуальным, и если состояние позволяет, то до получения микробиологии – вообще без антибиотиков. Если не позволяет – это должны быть бактериостатики.
- Мы никогда не лечим только анализ, и даже микробиологическое заключение, мы всегда лечим пациента со всем комплексом его симптомов и синдромов. Но микробиология помогает решить как дифференциально-диагностические задачи, что и позволяет отделить безусловный патоген от мирно живущего комменсала.
- Микробиологическая диагностика носит ключевое значение как для подтверждения самого возбудителя, так и для выбора необходимого антибиотика
- В случае выявления резистентных и панрезистентных возбудителей, помимо лечения самого пациента должна в полной мере задействоваться эпидемиологическая служба лечебного учреждения
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Врага, как известно, надо знать в лицо. Просторы интернета принесли вот такое симпатичное фото нашего противника.
Данного возбудителя невозможно перепутать ни с чем, особенно, когда процесс зашел далеко. Практически все отделение будет в курсе наличия такого больного из-за непередаваемого аромата, разносящегося из его пораженных областей.
Pseudomonas aeruginosa бывает дикой, ее нам приносят пациенты из внешнего мира и нашей, госпитальной, которая живет внутри больничных отделений (чаще хирургических и реанимационных) и вызывает тот самый суеверный ужас практически у всех, обремененных медицинским образованием.
Синегнойная палочка является вольным жителем тех мест, где тепло и влажно. Она живет в прудах (дикая), в раковинах, в банках с фурацилином и другими дезенфектантами, диализных жидкостях и наркозных аппаратах в стационарах.
А потому, если в отделение что-то такое выросло, борьба с синегнойной инфекцией должна начинаться со смены сантехники (старой на новую) и линолеума вокруг раковины. С отказа от фурацилина, со сроком изготовления более суток и с просушивания трубок аппаратуры для вентиляции легких.
Больной у нас тоже теплый и, как и любой человек, на 70% состоит из воды. А еще у него множество вольных открытых пространства – мокнущие раневые поверхности, ожоговые раны, свищевые ходы, пролежни, цистостомы, трахеостомы, катетеры. То есть все те условия, которые палочка очень любит. А еще теплой и влажной поверхностью у нас является роговица глаза и если промедлить с лечением – этот самый глаз можно потерять за несколько часов.
- Гангренозную пневмонию
- Эмпиему
- Наружный отит
- Инфекции глаз (особенно после травм и хирургических вмешательств)
- Фурункулез (после горячих ванн)
- Септицемию
- Эндокардит
- Менингит
- Часто инфицирует ожоговые поверхности, свищевые ходы, изъязвленные пролежни.
Синегнойная инфекция развивается чаще всего на фоне иммуносупрессии или массированной антимикробной терапии, так как сам возбудитель природно устойчив абсолютному большинству антибактериальных препаратов, а массовая гибель конкурентов, дает ей селективное преимущество. Кстати, основными препаратами, селектирующими в отделениях Pseudomonas aeruginosa являются цефалоспорины третьего и четвертого поколений.
- на руках
- на общих полотенцах в ординаторских, процедурных и манипуляционных (многоразовых)
- на фонендоскопах
- на мобильных телефонах
- на авторучках, которые у нас торчат из карманов и т.д.
И достаточно в отделении появиться одному пациенту с этим возбудителем, а персоналу забыть о путях распространения – к вечеру все 100% пациентов будут обсеменены этим возбудителем. А дальше как повезет… пациентам…
Если инфицирование все-таки произошло, и у пациента возникла синегнойная инфекция, чем же мы будем ее лечить?
В этом списке нет цефоперазона и цефоперазона/сульбактама, о которых нам с института говорят, что они антисинегнойные. Дело в том, что единственным действительно антисинегнойным цефалоспорином является цефтазидим, а данные о якобы высокой чувствительности к цефоперазону и цефоперазону сульбактаму существуют только в России, так как нет ни одной рекомендации по использованию этих препаратов ни в США, ни на medscape.com, ни на EUCAST. Более того, эти источники не дают даже критериев определения чувствительности Pseudomonas aeruginosa к этим препаратам. И откуда взялись наши российские выводы о высокой чувствительности вообще не понятно. Более того, комбинация Цефоперазон/сульбактам существует только в 2-х странах – России и Турции. FDA в свое время очень быстро отменила его регистрацию.
Цефалоспорин третьего поколения. Препарат с явной и очень высокой антисинегнойной активностью. Первые несколько лет после появления он был самым мощным препаратом против грам(-) флоры. Однако в связи с увеличением количества как госпитальных, так и внебольничных беталактамаз расширенного спектра (БЛРС), его значение было пересмотрено и сейчас он используется в качестве индикатора для выявления БЛРС у грам(-) бактерий. Проще говоря, если кишечная палочка или клебсиелла устойчивы к цефтаздиму, то любой, сколь угодно большой диаметр зоны на чашке Петри вокруг диска с цефотаксимом или цефтриаксоном в расчет уже не принимаются.
Если антибиотикограммы еще нет, но есть пациент предлеченный цефтазидимом без эффекта, то не нужно выбирать ему препарат среди III генерации цефалоспоринов, по причине того, что использование их будет бесполезным, при этом, если пациента с грамотрицательной инфекцией лечили цефалоспоринами 2-3-й генерации, то вполне допустима терапия цефтазидимом, потому что, во-первых, он активен против синегнойки, а во вторых бета-лактамаза цефуроксимаза, рушит все цефалоспорины, но не цефтазидим.
Еще одной особенностью цефтазидима является его возможность создавать высокие концентрации в ликворе, проникая через гематоэнцефалический барьер, поэтому его используют для лечения менингитов, вызванных грамотрицательной микрофлорой, при условии чувствительности к нему возбудителей.
3. Карбопенемы обладают антисинегнойной активностью, но она слабее чем у цефтазидима и анисинегнойными они стали только из-за того, что существует Эртапенем, у которого нет никакой антисинегнойной активности. Да, применять можно, но только в комбинации с другими антисинегнойными препаратами.
4. Амикацин, как и все аминогликозиды, обладает более мощным бактерицидным действием, чем бета-лактамы и минимальным количеством аллергических реакций. Но он должен нами рассматриваться, как и другие антисинегнойные препараты, как препарат резерва и не использоваться широко в стационаре. Другие аминогликозиды прекрасно отработают Гр (-) флору и без него, нам важно сохранить чувствительность нашей, местной синегнойки к нему как можно дольше.
Дозируем амикацин, как вы помните, на килограмм массы тела и детям и взрослым и обязательно с учетом клиренса креатинина. (подробнее о дозировании смотрите обзорную статью по аминогликозидам, которая располагается по этой ссылке /vracham/Informatsiya-dlya-spetsialistov/Antibiotikoterapiya/Obzory-antibiotikov-razlichnyh-grupp/Obzory-antibiotikov-razlichnyh-grupp_411.html)
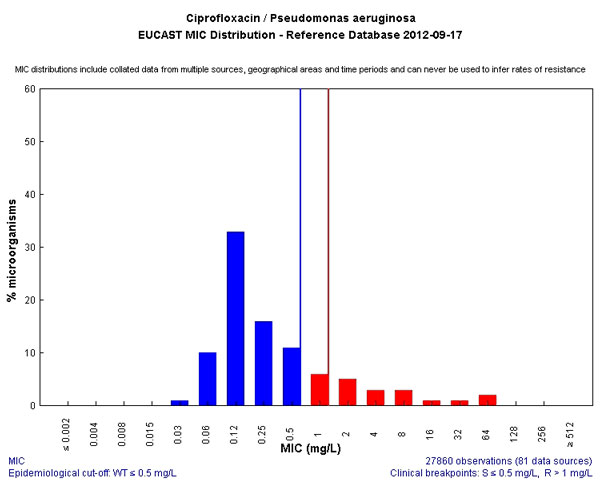
И, к сожалению, препарат, который нам скоро уничтожат коллеги из поликлинического звена, потому что назначают его направо и налево. Да и в стационарах коллеги грешат его необоснованным назначением, так как он относительно дешев и более чем доступен из-за огромного количества дженериков. Как результат, нам уже приходится использовать дозировки не 400 мг в сутки, а 800-1200 мг. И, слава богу, что механизм резистентности нам это еще позволяет. Является одним из самых безопасных антисинегнойных препаратов, а потому беречь его мы должны как самое дорогое.
Он может использоваться в стационаре в случаях не синегнойной инфекции только тогда, когда другим способом помочь пациенту невозможно.
Это препарат такого же глубокого резерва как амикацин. И может использоваться только под контролем клинического фармаколога в отличие от других фторхинолонов.
И один из самых страшных моих, и не только моих, кошмаров – это панрезистентная синегнойная палочка. Это та палочка которая устойчива абсолютно ко всем известным на данный момент антимикробным средствам и здесь мы совершенно бессильны. А потому наша основная цель состоит в том, чтобы не дать ей у нас в стационаре появиться. Для этого требуется соблюдать несложные правила асептики, а именно, мыть и обрабатывать руки после каждого пациента, менять перчатки, обрабатывать фонендоскопы и к пациентам с гнойным воспалением не заходить с мобильниками и чем либо еще, что мы можем схватить руками, сами того не замечая. Ну и никаких общих полотенец в ординаторских и сестренских.
Читайте также:

