Заболевания вызываемые днк-содержащими вирусами
Обновлено: 18.04.2024
1. Аденовирусы. Имеют наиболее важное клиническое значение, так как способны вызывать острые заболевания органов дыхания и конъюнктивы. Аденовирусы вступают во взаимодействие с клетками организма хозяина, вызывая три вида повреждений: 1) могут проходить в клетках полный цикл репликации, вызывая их гибель (например, в эпителиальных клетках); 2) в лим-фоидных клетках могут существовать в виде латентной или хронической инфекции. При этом за пределы клеток выделяется незначительное количество вирусов; ?) могут участвовать в онко-генной трансформации клеток.
Аденовирусные инфекции человека убиквитарны. Первичное инфицирование человека происходит обычно в первые годы жизни. Серотип аденовируса и характер заболевания тесно связаны с возрастом больного.
В неэпидемический период примерно в половине случаев инфицирование аденовирусом не приводит к заболеванию. В то же время возникновение 10 % респираторных заболеваний у детей связано с аденовирусом. Эти заболевания протекают в форме фарингита или трахеита.
В летний период аденовирусная инфекция у детей может протекать в форме фарингоконъюнктивальной лихорадки, которая характеризуется острым началом, развитием конъюнктивита, фарингита, ринита и тонзиллита. Продолжительность заболевания 3—5 дней.
Кератоконъюнктивит встречается у взрослых и протекает как эпидемическая вспышка. Инкубационный период может достигать 4—24 дней, а продолжительность заболевания — 1—4 нед.
Аденовирусы могут также вызывать развитие геморрагического цистита, диарею у детей, энцефалит и минингоэнцефалит, однако эти формы инфекции встречаются значительно реже.
2. Вирусы герпеса. Представляют собой одно из самых боль-ших семейств вирусов и включают около 80 разновидностей. Ви русы герпеса делятся на три подсемейства: а-вирусы герпеса бы стро растут и быстро разрушают ткани хозяина; В-вирусы герпе-са растут медленно и лишь в определенном типе клеток; у -виру-сы герпеса растут медленно и почти исключительно в лимфойд ных клетках их естественного хозяина.
Вирусы герпеса способны заражать клетки различных типов, Например, вирус herpes simplex растет в эпителиальных клетках и фибробластах человека, обезьяны, кролика, мыши и многих других животных. Вирус varicella/zoster лучше всего растет в эпителиальных клетках и фибробластах человека. Цитомегаловирус хорошо растет только в культуре фибробластов человека. Вирус Эпштейна—Барра можно культивировать только в В-лимфоци-тах.
Все вирусы герпеса вызывают продолжительную латентную инфекцию. Вирусы герпеса неустойчивы и не могут длительное время выживать в окружающей среде, поэтому заражение обычно происходит при попадании на чувствительные к вирусу ткани хозяина свежей, содержащей вирусы жидкости из тела больного. Чувствительностью к вирусу герпеса обладают слизистая оболочка ротовой полости, глаза, половых органов, заднего прохода, дыхательных путей, а также эндотелий сосудов.
Вирус герпеса вызывает развитие заболевания путем разрушения тканей, провоцируя иммунопатологический ответ, а также вызывая неопластическую трансформацию клеток. Цитопато-генный механизм действия вируса представлен энцефалитом, пневмонитом и гепатитом. Мультиформная эритема, гемолитическая анемия и тромбоцитопения являются иммунологически обусловленными. Известна связь вируса Эпштейна—Барр с некоторыми В-клеточными лимфомами и назофарингеальной карциномой.
Вирус герпеса вызывает развитие множества заболеваний, которые могут быть условно сгруппированы в болезни кожи и слизистых оболочек, органов, центральной нервной системы и реактивные синдромы.
Herpes simplex virus (HSV). Инфекции, вызываемые вирусом простого герпеса (herpes simplex), являются одними из самых распространенных у человека. Заражение HSV-1 происходит через секрет слизистой оболочки полости рта, a HSV-2 — через секрет слизистой оболочки половых органов.
В случае, если входными воротами инфекции является кожи. репликация вируса происходит в парабазальных и промежуточ ных эпителиальных клетках, которые затем подвергаются лизи су, а в месте повреждения развивается воспалительный процесс образуются тонкостенные пузырьки, появляются многоядерные
клетки, отек. Лимфатические узлы набухают. Дальнейшая репликация вируса может привести к виремии и висцеральной диссе-минации в зависимости от иммунного статуса больного. Впоследствии включаются защитные механизмы, такие как продукция интерферонов, естественные киллеры, защитные антитела.
После первичного инфицирования вирус простого герпеса может локализоваться в нейронах нервных узлов (ганглиев). Реактивированный вирус движется к кожным покровам и слизистым оболочкам по периферическим нервам.
Первичная инфекция HS V-1 часто бессимптомна, но может протекать в виде гингивостоматита и фарингита. Инкубационный период 2—12 дней. Заболевание начинается с лихорадки, болей в горле с отеком глотки и эритемы. Вскоре после начала заболевания на слизистой оболочке глотки и полости рта появляются мелкие пузырьки, которые быстро изъязвляются. Процесс часто затрагивает также мягкое небо и язык. Продолжительность заболевания 10—14 дней. Необходимо провести дифференциальную диагностику со стрептококковым и дифте-ритическим фарингитом, афтозным стоматитом и инфекционным мононуклеозом.
Поражение глаз HSV-1 сопровождается фотофобией, хемо-зом, отеком век. При первичном инфицировании развивается односторонний фолликулярный конъюнктивит и/или блефарит с пузырьками по краям век.
Первичную генитальную инфекцию вызывает HSV-2 (в 70—95 %). Инкубационный период 2—7 дней. У мужчин везикулярные повреждения возникают на головке полового члена и крайней плоти, а у женщин — на вульве, ягодицах, шейке матки и во влагалище. Пузырьки быстро изъязвляются, особенно у женщин. Проводится дифференциальный диагноз с сифилисом, генитальными проявлениями мультиформной эритемы и локальным кандидозом.
Для герпетической инфекции характерно рецидивирующее течение. Осложнения относительно редки. К ним относят герпетический энцефалит, герпетическое поражение новорожденного.
Герпетическая инфекция нередко возникает после пересадки органов и тканей, у больных СПИДом. Кроме того, генитальный герпес рассматривают в качестве фактора риска заражения вирусом иммунодефицита человека.
Для диагностики герпетической инфекции используют цито-патическое действие HSV на культуру клеток эмбриональной почки, почки кролика и амниона человека. Для типирования и идентификации индивидуального антигена HSV используют мо-ноклональные антитела. Для экспресс-диагностики мазки, полученные с поврежденных участков кожи или слизистых оболочек, окрашивают по Романовскому—Гимзе. Обнаружение в мазках
многоядерных гигантских клеток свидетельствует о наличии инфекции HSV или вируса varicella/zoster.
ДНК-вирусы как причина развития рака - вирусный канцерогенез
В канцерогенезе также могут участвовать ДНК-содержащие вирусы. Наиболее крупные ДНК-содержащие вирусы принадлежат к группе герпесвирусов. Первым вирусом, выделенным из культуры опухолевых клеток, был вирус Эпштейна-Баррра (ЭБВ).
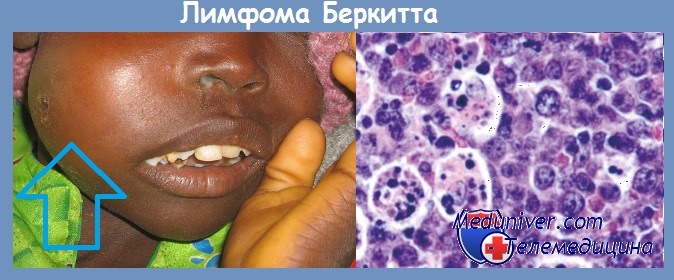
Вирус был получен из культуры опухолевых клеток больных лимфомой Беркита. В культуре in vitro ЭБВ вызывает бесконечную пролиферацию человеческих В-лимфоцитов. Вирусные гены, встраиваясь в геном этих клеток, инициируют пролиферацию путем активации клеточных генов-регуляторов роста (онкогенов).
В крови больных лимфомой Беркита обнаруживается более высокий, чем у здоровых людей, титр антител к антигенам вирусной оболочки и к мембранным антигенам. В то же время в африканских странах среди множества детей, инфицированных этим вирусом, лимфома развивается только в единичных случаях.
Механизм онкогенеза этого заболевания не может быть объяснен только вирусным заражением. К тому же, за пределами африканского континента регистрируются случаи заболевания лимфомой Беркита, абсолютно не связанные с инфицированием вирусом ЭБВ. По-видимому, ЭБВ также может принимать участие в патогенезе карциномы носоглотки, так как клетки этой опухоли экспрессируют вирусные антигены EBNA-1.
При исследованиях саркомы Капоши, развивающейся у больных СПИДом, в 1994 г. из ее клеток был выделен новый герпесвирус. Первоначально вирус получил название герпес-вируса саркомы Капоши (ГСК), впоследствии он был переименован в герпесвирус человека серотип 8 (ГВЧ 8). Вирус обнаруживается в веретеновидных клетках саркомы Капоши практически при всех случаях заболевания.
ГВЧ 8 был также найден в опухолевых клетках первичной эффузионной лимфомы и в клетках многоочаговой болезни Кастлемана. Данный вирус кодирует синтез циклина, который является промотором клеточного деления, чем и объясняется высокая пролиферативная активность инфицированных клеток.
Человеческие папилломавирусы (ПВЧ) вызывают кожные бородавки и ряд доброкачественных папиллом. Это весьма обширный класс вирусов, и некоторые его представители могут в той или иной степени участвовать в развитии злокачественных опухолей. Большинство вирусов вызывает лишь ограниченную пролиферацию клеток, но ряд серотипов может вызвать и развитие злокачественных новообразований.
Наибольшую опасность с точки зрения онкологии представляют серотипы 16, 18, 31 и 33. Более 90% опухолей карциномы шейки матки in situ обнаруживают в своих клетках генные последовательности вирусов ПВЧ. Эти вирусы также играют значительную роль в возникновении инвазивных и многоочаговых плоскоклеточных раков кожи, которые часто развиваются у больных после долгосрочных курсов иммуносупрессивной терапии.
Механизмы вирусного канцерогенеза в этом случае изучены недостаточно. В исследованиях доказано, что существует вероятность включения вирусной ДНК в клетки базального эпителия. Обычно в клеточную ДНК внедряются восемь ранних и два поздних гена. Ранние гены Е6 и Е7 вызывают пролиферацию клеток.
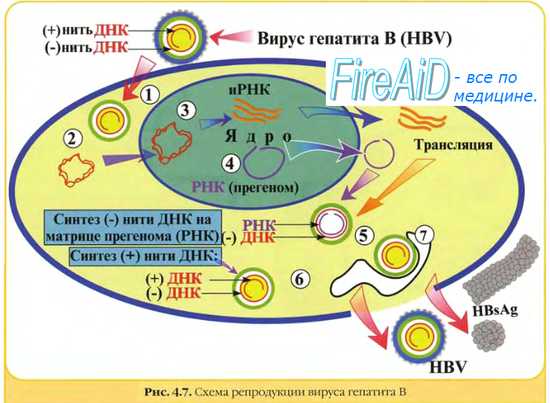
Вирус гепатита В четко связывают с развитием печеночно-клеточного рака. Риск развития этого заболевания у инфицированных вирусом в 200 раз превышает таковой у неинфицированных людей. Механизмы зарождения рака не до конца понятны: считается, что вирус вызывает бесконечную пролиферацию клеток, хотя зараженные вирусом клетки уничтожаются иммунной системой организма. Возможно, что пролиферирующие клетки становятся чувствительными к другим канцерогенам, например к афлатоксину.
Подытоживая вышесказанное, можно заключить, что основным механизмом канцерогенного воздействия является повреждение молекул ДНК и нарушения процессов ее репарации. Если не происходит исправления первичных повреждений ДНК, ошибки со временем начинают накапливаться, что ведет к дестабилизации структуры хромосом и к соматическим мутациям. Большинство таких мутаций летальны для клетки.
Однако, если часть клеток выживает, происходит постепенное накопление клеточной массы с опухолевым фенотипом, что в итоге приводит к клиническим проявлениям. Большой вклад в понимание этого процесса внесли современные исследования механизмов регулировки клеточного цикла и недавнее открытие регуляторных белков, которые запрещают клетке делиться, если ее геном сильно поврежден.
Для развития опухоли может быть недостаточно единичных мутаций в генах-регуляторах деления, но накопление массы ошибок в регуляторных генах может привести к фатальным последствиям. Особенно критичны мутации в генах, регулирующих клеточное деление, так называемых онкогенах. Очень опасны также мутационная инактивация генов, подавляющих клеточное деление — генов-подавителей опухоли, и мутации в генах, кодирующих белки, запрещающие деление при повреждении клеточного генотипа.
Накопление числа жизнеспособных мутаций по одному или нескольким из этих генов приводит к общей клеточной дезорганизации и к потере контроля над клеточным делением. В следующем разделе мы рассмотрим механизмы действия онкогенов и наиболее важные моменты контроля над клеточным циклом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
РНК-вирусы как причина развития рака - вирусный канцерогенез
Открытие вирусов, вызывающих злокачественные опухоли у животных, произошло еще на рубеже XIX и XX веков. В 1910 г. Пейтон Рауш обнаружил, что бесклеточный фильтрат из тканей птичьей саркомы может вызывать развитие аналогичной саркомы у цыплят. Примерно в это же время была доказана вирусная природа птичьего миелобластоза. Позднее было обнаружено, что часто проходит весьма значительный латентный период между инфицированием вирусом и развитием рака.
Тем не менее вплоть до 1960-х годов не существовало четких доказательств того, что инкорпорация вирусной ДНК в геном клетки является необходимым условием развития злокачественной трансформации, как не было и случаев выделения вирусной ДНК из раковых клеток.
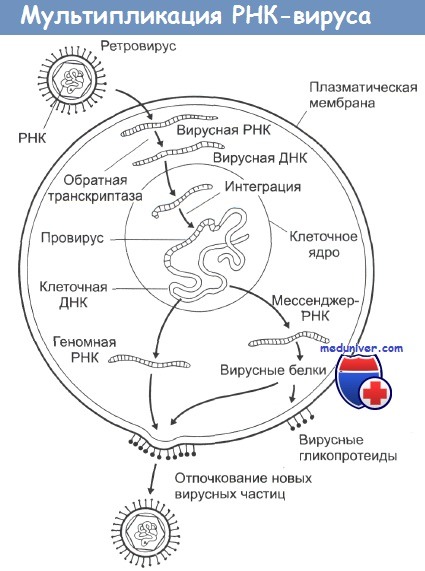
РНК-содержащие вирусы вызывают развитие целого ряда различных опухолей у животных, при этом наиболее распространена индукция этими вирусами лимфом, лейкемий и сарком. Типичная структура таких вирусов - это две идентичные цепочки молекул РНК в сочетании с ферментом обратная транскриптаза, одетых в гликопротеиновую оболочку. При инфицировании вирусом его обратная транскриптаза заставляет клетки синтезировать ДНК, комплементарную вирусной РНК.
Эта ДНК затем встраивается в клеточные хромосомы, и на ее основе клетка уже сама начинает синтез новых вирусных белков, вирусных обратных транскриптаз и элементов гликопротеиновой оболочки. Из-за механизма их действия этот тип вирусов получил название ретровирусы. Все они имеют весьма схожий внешний вид на электронных микрофотографиях и являются самыми маленькими из известных вирусов.
Некоторые из ретровирусов (например, вирусы птичьего лейкоза, кошачьей и мышиной лейкемии) содержат в себе только три гена и обладают очень длительным инкубационным периодом с момента заражения до возникновения опухоли. Другие вирусы (например, вирус саркомы Рауса (ВСР)) вызывают очень быструю злокачественную трансформацию и могут быть выделены из культуры опухолевых клеток.
Показано, что вирус ВСР содержит особый ген (v-src), способный вызывать трансформацию фибробластов in vitro. Этот ген кодирует наработку протеинкиназы, которая фосфорилирует тирозин. К сожалению, действие этой протеинкиназы запускает целый каскад различных метаболических процессов, и очень сложно оценить, какой именно из них ведет к злокачественной трансформации.
В настоящее время известно, что и нормальные, и злокачественные клетки содержат в своем генотипе участки ДНК, сходные или идентичные ряду последовательностей онкогенных РНК-содержащих вирусов. Такие участки получили название клеточных прото-онкогенов (чтобы отличать их от вирусных онкогенов). Постулируется, что активация этих участков, возникающая в результате канцерогенного воздействия, запускает целую цепочку событий, ведущую в итоге к злокачественной трансформации клетки. Считается также, что ретровирусы инкорпорировали эти клеточные участки в свой геном в процессе эволюции.
В настоящее время мы лучше понимаем механизмы действия продуктов вирусной активации. Примером такого продукта является протеинкиназа, активируемая геном sre, а также целый ряд других вирус-индуцированных канцерогенов. Это и рецепторы к эпидермальному фактору роста, продуцируемые геном v-erb, и тромбоцитарный фактор роста (ТФР), кодируемый фрагментами гена v-sis, и целый ряд связывающихся с ядром клетки белков, продукцию которых вызывает вирус птичьей лейкемии.
Как нормальные, так и раковые клетки содержат в себе участки последовательностей ДНК, гомологичные РНК онкогенных вирусов. Если происходит экспрессия или активация под действием канцерогенов этих клеточных онкогенов, это ведет к злокачественной трансформации клеток.
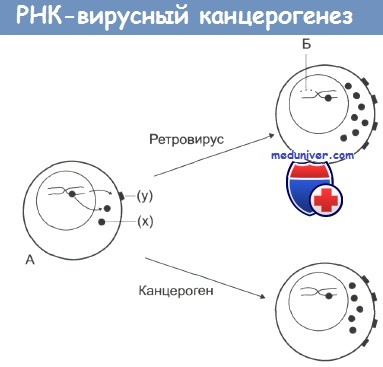
Онкогенная и злокачественная трансформация.
На стадии А нормальная клетка, которая характеризуется низкой протоонкогенной активностью, продуцирует фактор роста (х) или белки дифференцировки или рецепторы (у).
Канцерогены повышают активность протоонкогенов, что дает начало неопластической трансформации.
По другому механизму: при заражении ретровирусом происходит внедрение в ДНК клетки вирусных промоторов или онкогенов (Б), что также ведет к увеличению онкогенной активности и последующей злокачественной трансформации.
Первым ретровирусом, для которого была однозначно доказана связь со злокачественными новообразованиями, был вирус Т-клеточной лейкемии человека (ВТКЛ-1), выделенный из клеток хронической кожной Т-лимфомы. Этот вирус довольно широко распространен, может передаваться половым путем, через кровь, особенно в среде наркоманов, и от беременной женщины к плоду. Первоначально эндемический ареал циркуляции данного вируса был в основном представлен тропическими странами, однако в настоящее время в США серопозитивная реакция на вирус обнаруживается у каждого из 4000 человек населения. Кроме Т-клеточной лейкемии вирус вызывает тропический спастический паралич.
После 20 лет наблюдения за серопозитивными пациентами оценено, что риск развития последнего заболевания составляет около 5%. Один из вирусных генов, а именно tax-ген, вызывает увеличение продукции клеточного интерлейкина-2 (ИЛ-2) и его рецепторов, что является основным фактором, стимулирующим деление Т-клеток.
Ретровирусы могут вызывать опухолевые заболевания не напрямую, а опосредованно, как это было показано для вируса иммунодефицита человека (ВИЧ-1), вызывающего развитие СПИДа. Случаи развития рака у ВИЧ-инфицированных рассмотрены в одном из обзоров. Отмечается, что у ВИЧ-инфицированных наиболее часто развиваются три типа опухолей: мгновенная или высокозлокачественная В-клеточная лимфома; саркома Капоши (СК, которую вызывает другой вирус — герпесвирус ГСК, или герпесвирус 8); карцинома шейки матки.
До разработки эффективных методов терапии ВИЧ-инфицированных более 40% из них заболевали тем или иным видом рака. Тем не менее связь этого вируса с развитием онкологических заболеваний скорее всего косвенная и опосредована развитием общей хронической иммунодепрессии организма, которая и позволяет другим канцерогенным вирусам вызывать рак. В-клеточные лимфомы также характеризуются довольно сложным патогенезом. Хотя В-клетки не поражаются вирусом ВИЧ-1, они могут быть мишенью для других типов вирусов, например для вируса Эпштейна-Барра (ВЭБ). Рак шейки матки у женщин также развивается на основе вторичной вирусной инфекции — вируса папилломы человека (ВПЧ), на фоне общей иммунодепрессии, вызванной ВИЧ-1. По причине общего снижения иммунных реакций организма все эти опухоли развиваются особенно быстро и агрессивно.
Показано, что РНК-содержащий вирус гепатита С значительно увеличивает риск заболевания гепатоклеточной карциномой. У больных, инфицированных этим вирусом, риск развития раковой опухоли возрастает в 100 раз, но механизмы его канцерогенного действия в настоящее время почти не изучены. Если больной заражен еще и вирусом гепатита В, риск развития рака печени возрастает многократно. На земном шаре одним или обоими из этих вирусов заражено около миллиарда человек.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
В заражённых вирусом клетках возможны патологические проявления разностороннего характера.
Морфология патологических эффектов. Зараженные вирусом клетки. Основные реакции зараженных вирусом клеток.
Характерные проявления взаимодействий между вирусом и чувствительными клетками-видимые поражения заражённых клеток вплоть до их гибели, а также присутствие возбудителей в исследуемом материале.
Альтерация и воспаление зараженных вирусом тканей. При вирусных инфекциях на первый план выступает картина повреждения клеток и воспалительных изменений тканей, при различных инфекциях их соотношение и выраженность варьируют. В противоположность бактериальным инфекциям (где доминируют полиморфноядерные лейкоциты), при вирусных поражениях среди клеточных элементов воспалительных реакций доминируют мононуклеары (лимфо- и моноциты). На этапах, предшествующих разрушению клеток, можно визуально наблюдать их дегенеративные и некротические изменения.
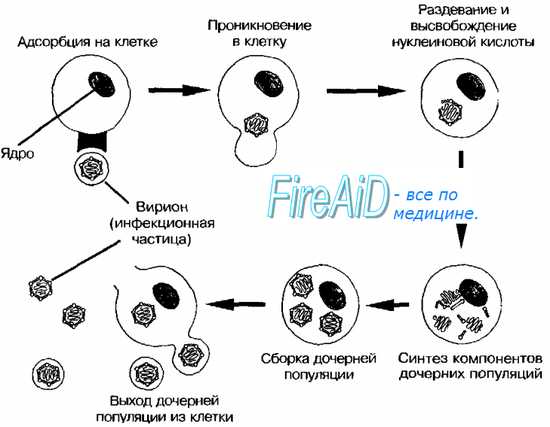
Тельца включений зараженных вирусом клеток. Микроскопия заражённых клеток часто позволяет выявить тельца включений — характерный, но не абсолютный признак вирусных поражений. Тельца значительно крупнее, чем отдельные вирионы, и часто окрашиваются кислыми красителями (например, эозином).
• При заражении клеток ДНК-содержащими вирусами тельца включений располагаются в ядре; исключение — тельца включений поксвирусов (тельца Гварнери).
• При заражении клеток РНК-содержашими вирусами тельца включений располагаются в цитоплазме (например, тельца Бабеша-Нёгри, выявляемые в цитоплазме клеток головного мозга при бешенстве).
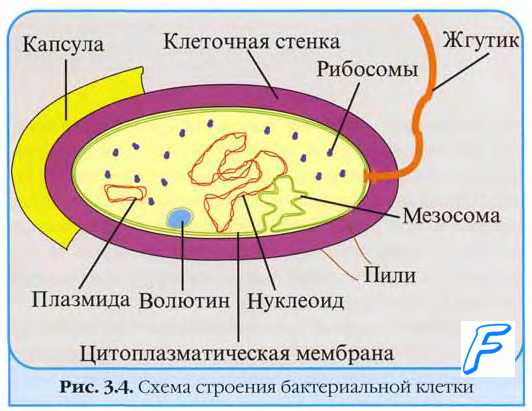
Причины гибели зараженных вирусом клеток. Размножаясь в клетке, вирусы индуцируют синтез вирусспецифических белков, в той или иной степени подавляющих метаболизм клетки. Нарушение синтеза макромолекул вызвано нарушением трансляции клеточной мРНК. Среди РНК-геномных вирусов наиболее быстрое и глубокое подавление макромолекулярных синтезов в клетке вызывают пикорнавирусы, среди ДНК-геномных — покс- и герпесвирусы. Действие указанных вирусов реализуется на ранних этапах (до появления морфологических признаков цитопатического эффекта). Ингибирование синтеза РНК и ДНК обычно вторично по отношению к воздействию на белки, контролирующие экспрессию генов и пролиферацию клетки. Значительно реже нарушения вызывают вирусные белки, напрямую ингибирующие синтез нуклеиновых кислот. Среди РНК-геномных вирусов наиболее быстрое и глубокое подавление синтезов нуклеиновых кислот вызывают пикорнавирусы, среди ДНК-геномных — покс- и герпесвирусы.
Во время репродукции вируса в клетке накапливаются вирусные компоненты, оказывающие токсическое и повреждающее действие на клеточные структуры. Например, цитотоксические свойства проявляют капсомеры некоторых аденовирусов, гликопротеины парамиксовирусов. В процессе вирусной инфекции также происходит повреждение мембран лизосом, содержимое которых высвобождается и осуществляет аутолиз клетки. Таким образом, гибель клеток наступает в результате сочетания раннего подавления синтеза клеточных компонентов, накопления токсических вирусных продуктов и повреждения лизосом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
1. Аденовирусы. Имеют наиболее важное клиническое значение, так как способны вызывать острые заболевания органов дыхания и конъюнктивы. Аденовирусы вступают во взаимодействие с клетками организма хозяина, вызывая три вида повреждений: 1) могут проходить в клетках полный цикл репликации, вызывая их гибель (например, в эпителиальных клетках); 2) в лим-фоидных клетках могут существовать в виде латентной или хронической инфекции. При этом за пределы клеток выделяется незначительное количество вирусов; ?) могут участвовать в онко-генной трансформации клеток.
Аденовирусные инфекции человека убиквитарны. Первичное инфицирование человека происходит обычно в первые годы жизни. Серотип аденовируса и характер заболевания тесно связаны с возрастом больного.
В неэпидемический период примерно в половине случаев инфицирование аденовирусом не приводит к заболеванию. В то же время возникновение 10 % респираторных заболеваний у детей связано с аденовирусом. Эти заболевания протекают в форме фарингита или трахеита.
В летний период аденовирусная инфекция у детей может протекать в форме фарингоконъюнктивальной лихорадки, которая характеризуется острым началом, развитием конъюнктивита, фарингита, ринита и тонзиллита. Продолжительность заболевания 3—5 дней.
Кератоконъюнктивит встречается у взрослых и протекает как эпидемическая вспышка. Инкубационный период может достигать 4—24 дней, а продолжительность заболевания — 1—4 нед.
Аденовирусы могут также вызывать развитие геморрагического цистита, диарею у детей, энцефалит и минингоэнцефалит, однако эти формы инфекции встречаются значительно реже.
2. Вирусы герпеса. Представляют собой одно из самых боль-ших семейств вирусов и включают около 80 разновидностей. Ви русы герпеса делятся на три подсемейства: а-вирусы герпеса бы стро растут и быстро разрушают ткани хозяина; В-вирусы герпе-са растут медленно и лишь в определенном типе клеток; у -виру-сы герпеса растут медленно и почти исключительно в лимфойд ных клетках их естественного хозяина.
Вирусы герпеса способны заражать клетки различных типов, Например, вирус herpes simplex растет в эпителиальных клетках и фибробластах человека, обезьяны, кролика, мыши и многих других животных. Вирус varicella/zoster лучше всего растет в эпителиальных клетках и фибробластах человека. Цитомегаловирус хорошо растет только в культуре фибробластов человека. Вирус Эпштейна—Барра можно культивировать только в В-лимфоци-тах.
Все вирусы герпеса вызывают продолжительную латентную инфекцию. Вирусы герпеса неустойчивы и не могут длительное время выживать в окружающей среде, поэтому заражение обычно происходит при попадании на чувствительные к вирусу ткани хозяина свежей, содержащей вирусы жидкости из тела больного. Чувствительностью к вирусу герпеса обладают слизистая оболочка ротовой полости, глаза, половых органов, заднего прохода, дыхательных путей, а также эндотелий сосудов.
Вирус герпеса вызывает развитие заболевания путем разрушения тканей, провоцируя иммунопатологический ответ, а также вызывая неопластическую трансформацию клеток. Цитопато-генный механизм действия вируса представлен энцефалитом, пневмонитом и гепатитом. Мультиформная эритема, гемолитическая анемия и тромбоцитопения являются иммунологически обусловленными. Известна связь вируса Эпштейна—Барр с некоторыми В-клеточными лимфомами и назофарингеальной карциномой.
Вирус герпеса вызывает развитие множества заболеваний, которые могут быть условно сгруппированы в болезни кожи и слизистых оболочек, органов, центральной нервной системы и реактивные синдромы.
Herpes simplex virus (HSV). Инфекции, вызываемые вирусом простого герпеса (herpes simplex), являются одними из самых распространенных у человека. Заражение HSV-1 происходит через секрет слизистой оболочки полости рта, a HSV-2 — через секрет слизистой оболочки половых органов.
В случае, если входными воротами инфекции является кожи. репликация вируса происходит в парабазальных и промежуточ ных эпителиальных клетках, которые затем подвергаются лизи су, а в месте повреждения развивается воспалительный процесс образуются тонкостенные пузырьки, появляются многоядерные
клетки, отек. Лимфатические узлы набухают. Дальнейшая репликация вируса может привести к виремии и висцеральной диссе-минации в зависимости от иммунного статуса больного. Впоследствии включаются защитные механизмы, такие как продукция интерферонов, естественные киллеры, защитные антитела.
После первичного инфицирования вирус простого герпеса может локализоваться в нейронах нервных узлов (ганглиев). Реактивированный вирус движется к кожным покровам и слизистым оболочкам по периферическим нервам.
Первичная инфекция HS V-1 часто бессимптомна, но может протекать в виде гингивостоматита и фарингита. Инкубационный период 2—12 дней. Заболевание начинается с лихорадки, болей в горле с отеком глотки и эритемы. Вскоре после начала заболевания на слизистой оболочке глотки и полости рта появляются мелкие пузырьки, которые быстро изъязвляются. Процесс часто затрагивает также мягкое небо и язык. Продолжительность заболевания 10—14 дней. Необходимо провести дифференциальную диагностику со стрептококковым и дифте-ритическим фарингитом, афтозным стоматитом и инфекционным мононуклеозом.
Поражение глаз HSV-1 сопровождается фотофобией, хемо-зом, отеком век. При первичном инфицировании развивается односторонний фолликулярный конъюнктивит и/или блефарит с пузырьками по краям век.
Первичную генитальную инфекцию вызывает HSV-2 (в 70—95 %). Инкубационный период 2—7 дней. У мужчин везикулярные повреждения возникают на головке полового члена и крайней плоти, а у женщин — на вульве, ягодицах, шейке матки и во влагалище. Пузырьки быстро изъязвляются, особенно у женщин. Проводится дифференциальный диагноз с сифилисом, генитальными проявлениями мультиформной эритемы и локальным кандидозом.
Для герпетической инфекции характерно рецидивирующее течение. Осложнения относительно редки. К ним относят герпетический энцефалит, герпетическое поражение новорожденного.
Герпетическая инфекция нередко возникает после пересадки органов и тканей, у больных СПИДом. Кроме того, генитальный герпес рассматривают в качестве фактора риска заражения вирусом иммунодефицита человека.
Для диагностики герпетической инфекции используют цито-патическое действие HSV на культуру клеток эмбриональной почки, почки кролика и амниона человека. Для типирования и идентификации индивидуального антигена HSV используют мо-ноклональные антитела. Для экспресс-диагностики мазки, полученные с поврежденных участков кожи или слизистых оболочек, окрашивают по Романовскому—Гимзе. Обнаружение в мазках
многоядерных гигантских клеток свидетельствует о наличии инфекции HSV или вируса varicella/zoster.
Читайте также:

