Желчные протоки при гепатите
Обновлено: 18.04.2024
Холангит – это неспецифическое воспалительное поражение желчных протоков острого или хронического течения. При холангите отмечается боль в правом подреберье, лихорадка с ознобами, диспепсические расстройства, желтуха. Диагностика холангита включает анализ биохимических показателей крови, проведение фракционного дуоденального зондирования с бакисследованием желчи, УЗИ, чрескожной чреспеченочной холангиографии, РХПГ. В лечении холангита используется антибиотикотерапия, дезинтоксикационная терапия, назначение ферментов, ФТЛ (грязелечение, хлоридно-натриевые ванны, парафино- и озокеритотерапия, УВЧ, диатермия), иногда – хирургическая декомпрессия желчных путей.
МКБ-10
Общие сведения
При холангите могут поражаться внутри- или внепеченочные желчные протоки. Заболевание чаще возникает у женщин в возрасте 50—60 лет. Изолированный холангит развивается редко. В практической гастроэнтерологии холангит, как правило, диагностируется совместно с гастродуоденитом, холециститом, гепатитом, желчнокаменной болезнью, панкреатитом. Заболевание может носить острое или хроническое течение.
Причины холангита
В этиологическом отношении различают инфекционный и асептический холангит. Инфекционные холангиты могут иметь бактериальную, вирусную, паразитарную этиологию:
- Бактериальные холангиты. Большая часть холангитов обусловлена попаданием в желчные протоки микробных возбудителей (чаще - кишечной палочки, протея, стафилококков, энтерококков, неклостридиальной анаэробной инфекции, реже — микобактерий туберкулеза, брюшнотифозной палочки, бледной спирохеты). Микроорганизмы проникают в желчные ходы преимущественно восходящим путем из просвета 12-перстной кишки, гематогенным – через воротную вену, лимфогенным – при холецистите, панкреатите, энтерите.
- Вирусные холангиты. Мелкие внутрипеченочные желчные протоки, как правило, воспаляются при вирусном гепатите.
- Паразитарные холангиты. Чаще всего развиваются при сопутствующем описторхозе, аскаридозе, лямблиозе, стронгилоидозе, клонорхозе, фасциолезе.
Асептический ферментативный холангит может развиваться в результате раздражения стенок желчных ходов активированным панкреатическим соком, имеющим место при панкреатобилиарном рефлюксе. В этом случае вначале возникает асептическое воспаление, а присоединение инфекции происходит вторично, в более позднем периоде. По асептическому типу также протекает склерозирующий холангит, обусловленный аутоиммунным воспалением желчных протоков. При этом, наряду со склерозирующим холангитом, часто отмечаются неспецифический язвенный колит, болезнь Крона, васкулит, ревматоидный артрит, тиреоидит.
Предрасполагающие факторы
Предпосылками для развития холангита служит холестаз, встречающийся при:
- дискенезии желчевыводящих путей;
- аномалиях желчных ходов;
- кисте холедоха;
- раке желчных путей;
- холедохолитиазе;
- стенозе фатерова сосочка.
Предшествовать началу холангита могут ятрогенные повреждения стенок протоков при эндоскопических манипуляциях (ретроградной панкреатохолангиографии, установке стентов, сфинктеротомии), оперативных вмешательствах на желчных путях.
Классификация
Течение холангита может быть острым и хроническим. В зависимости от патоморфологических изменений острый холангит может принимать катаральную, гнойную, дифтеритическую или некротическую форму.
- Катаральный холангит. Характеризуется гиперемией и отеком слизистой желчных протоков, лейкоцитарной инфильтрацией их стенок, десквамацией эпителия.
- Гнойный холангит. Происходит расплавление стенок желчных ходов и образование множественных абсцессов.
- Дифтеритический холангит. Протекает тяжело, характеризуется образованием фибринозных пленок на стенках желчных ходов
- Некротический холангит. Крайне тяжелый вариант с появлением очагов некроза.
Наиболее часто встречается хронический холангит, который может развиваться как исход острого воспаления или с самого начала приобретать затяжное течение. Выделяют следующие формы хронического воспаления:
- латентная;
- рецидивирующая;
- длительно текущая септическая;
- абсцедирующая;
- склерозирующая. При склерозирующем холангите в стенках желчных ходов разрастается соединительная ткань, что вызывает стриктуры желчных протоков и еще большую их деформацию.
По локализации воспаления различают холедохит (воспаление холедоха – общего желчного протока), ангиохолит (воспаление внутрипеченочных и внепеченочных желчных ходов), папиллит (воспаление фатерова сосочка).
Симптомы холангита
Острый холангит
Клиника острого холангита развивается внезапно и характеризуется триадой Шарко: высокой температурой тела, болями в правом подреберье и желтухой.
В тяжелых случаях к триаде Шарко могут присоединяться нарушения сознания и явления шока – в этом случае развивается симптомокомплекс, называемый пентадой Рейнолдса.
Хронический холангит
Клинические проявления хронического холангита носят стертый, но прогрессирующий характер. Заболевание характеризуется тупыми болями в правом боку слабой интенсивности, ощущением дискомфорта и распирания в эпигастрии. Желтуха при хроническом холангите развивается поздно и свидетельствует о далеко зашедших изменениях. Общие нарушения при хроническом холангите включают субфебрилитет, утомляемость, слабость.
Осложнения
В половине случаев наблюдаются неосложненные формы холангита, у 40% пациентов развиваются осложнения, у 10% - полиорганная недостаточность. Осложнениями холангита могут стать холецистопанкреатит, гепатит, биллиарный цирроз печени, печеночная недостаточность. Септические осложнения представлены множественными абсцессами печени, перитонитом, сепсисом, инфекционно-токсическим шоком.
Диагностика
Заподозрить холангит, как правило, удается на основании характерной триады Шарко; уточняющая диагностика осуществляется на основании лабораторных и инструментальных исследований.
- Лабораторные анализы. Биохимические пробы косвенно свидетельствуют о холестазе; при холангите отмечается увеличение уровня билирубина, щелочной фосфатазы, трансаминаз, aльфа-амилазы. С целью исключения паразитарной инвазии показано исследование кала на яйца гельминтов и простейшие.
- Дуоденальное зондирование. Для выявления возбудителей холангита проводится фракционное дуоденальное зондирование с бактериологическим посевом желчи. В 60% случаев при холангите имеет место смешанная бактериальная флора.
- Ультразвуковая диагностика. К визуализирующим методам диагностики холангита относятся УЗИ брюшной полости и печени, ультрасонография желчных путей. С их помощью удается получить изображение желчных протоков, выявить их расширение, определить наличие структурных и очаговых изменений в печени.
- Лучевая диагностика. Среди инструментальных методов диагностики холангита ведущая роль отводится эндоскопической ретроградной панкреатохолангиографии, магнитно-резонансной панкреатохолангиографии (МРПХГ), чрескожной чреспечёночной холангиографии. На полученных рентгенограммах и томограммах хорошо визуализируется структура желчевыводящих путей, что позволяет выявить причину их обструкции.
Дифференциальная диагностика холангита необходима с ЖКБ, некалькулезным холециститом, вирусным гепатитом, первичным билиарным циррозом, эмпиемой плевры, правосторонней пневмонией.
Лечение холангита
Важнейшими задачами при холангите являются купирование воспаления, дезинтоксикация и декомпрессия желчных путей. В зависимости от причин и наличия осложнений лечение холангита может проводиться консервативными или хирургическими методами.
Консервативная терапия
Консервативное ведение пациента с холангитом заключается в обеспечении функционального покоя (постельного режима, голода), назначении спазмолитических, противовоспалительных, антибактериальных, противопаразитарных средств, инфузионной терапии, гепатопротекторов.
Этиотропное лечение холангита проводится с учетом обнаруженных возбудителей: при бактериальной флоре обычно применяются цефалоспорины в комбинации с аминогликазидами и метронидазолом; при выявлении глист или простейших - противопаразитарные средства. При выраженной интоксикации показано проведение плазмафереза.
В период ремиссии холангита широко используется физиотерапевтическое лечение: индуктотермия, УВЧ, микроволновая терапия, электорофорез, диатермия, грязевые аппликации, озокеритотерапия, парафинотерапия, хлоридно-натриевые ванны.
Хирургическое течение
Поскольку лечение холангита невозможно без нормализации функции желчеотведения, довольно часто приходится прибегать к различного рода хирургическим вмешательствам. С целью декомпрессии желчных протоков могут проводиться:
- эндоскопическая папиллосфинктеротомия;
- экстракция конкрементов желчных протоков;
- эндоскопическое стентирование холедоха;
- чрескожное транспеченочное дренирование желчных протоков;
- наружное дренирование желчных протоков и др. вмешательства.
Наиболее эффективным методом лечения склерозирующего холангита служит трансплантация печени.
Прогноз и профилактика
При холангите, осложненном абсцедированием, циррозом, печеночно-почечной недостаточностью, генерализованным септическим процессом, прогноз неудовлетворительный. Своевременная терапия катарального холангита позволяет добиться излечения; при гнойной, дифтеритической и некротической форме - прогноз более серьезный. Длительное течение хронического холангита может привести к стойкой инвалидизации.
Профилактика холангита диктует необходимость своевременного лечения гастродуоденита, бескаменного холецистита, ЖКБ, панкреатита, глистных и протозойных инвазий; наблюдения у гастроэнтеролога после перенесенных хирургических вмешательств на желчных путях.
В статье представлены данные о нарушении билиарного статуса у пациентов с хроническими гепатитами В и С. При хронических гепатитах В и С имеют место выраженные изменения функционального состояния билиарного тракта, как в работе сфинктерного аппарата, так
The article presents data on disorders in biliary status in patients with chronic hepatitis B and C. In chronic hepatitis B and C, there are pronounced changes in the functional state of the biliary tract, both in the sphincter apparatus and in the gallbladder, as well as duodenal hypertension and increased hepatic choleresis. The revealed changes in the microscopic composition of bile also indirectly indicate the presence of inflammatory process in the biliary tract in patients with chronic hepatitis B and C.
В глобальном масштабе вирусный гепатит перешел на седьмое место причин смертей в 2013 г., по сравнению с 10-й ведущей причиной в 1990 г. [1]. Во всем мире вирусный гепатит А, по оценкам, поражает 1,4 млн человек в год [2]. Около 2 млрд человек в мире имеют доказательства прошлой или текущей инфекции гепатита В (HBV), из них 240 млн хронических носителей HBsAg [3]. Гепатит В, наряду с ассоциированной инфекцией вирусом гепатита D, является одним из наиболее распространенных патогенов, поражающих людей [4]. HBV ежегодно приводит к 650 000 смертей в результате гепатита, вызванного этим вирусным поражением печени [3].
Невозможно оценить ежегодную распространенность острой инфекции гепатита С (HCV) в мире, поскольку она протекает чаще бессимптомно. По оценкам экспертов, около 71 млн человек хронически инфицированы HCV во всем мире [2]. 55–85% этих людей имеют хроническую прогрессирующую HCV-инфекцию с 15–30-процентнным риском развития цирроза печени в течение двух десятилетий [5]. Китай, США и Россия имеют самую большую популяцию потребителей инъекционных наркотиков, которые инфицированы HCV.
HCV-инфекция характеризуется высокой частотой и разнообразием внепеченочных поражений. По результатам исследования 230 больных с хроническим гепатитом С (ХГС) в клинике им. Е. М. Тареева 47% пациентов имели внепеченочные поражения, что превышало частоту таковых при HBV-инфекции — 22–35% [6]. Как известно, печень и желчевыводящие пути анатомически функционально тесно взаимосвязаны. Поэтому патология печени может сопровождаться заболеваниями желчевыводящих путей. Поражения билиарного тракта, в том числе и функциональные расстройства, в какой-то степени обусловливают клинические проявления хронических гепатитов В и С.
В зарубежных исследованиях существуют единичные работы, в которых определена взаимосвязь ХГС и поражений желчевыводящих путей. Гепатит С стал прототипическим вирусным гепатитом с холангитовыми поражениями, которые представляют собой преимущественно интраэпителиальные лимфоцитарные инфильтрации [7] и лимфоидные агрегаты или образования фолликулов, обычно без повреждения канала. Эти ассоциированные с вирусом холангитовые поражения являются обратимыми и не приводят к прогрессированию процесса или кровотечению. Прогноз и ответ на терапию не связаны с наличием желчных поражений [8].
Среди гепатотропных вирусов вирус гепатита С чаще ассоциируется с холангитом. Развившийся холангит при вирусных гепатитах В и С является обратимым и не оказывает вредного влияния на течение заболевания или на эффективность терапии. При гепатите С в основе холангита лежит интраэпителиальная лимфоцитарная инфильтрация, как правило, без повреждения протоков. Несмотря на то, что вирус-индуцированный холангит является обратимым, все же происходят структурные повреждения, в том числе формирование дивертикулов, ассоциированных с воспалением. У этих пациентов обычно не регистрируется повышение уровня щелочной фосфатазы. Развитие холангита не ухудшает ответ на противовирусную терапию. Некоторые исследователи обнаружили частицы вируса гепатита в холангиоцитах [9, 10].
При HBV-инфекции описываемые гистологические изменения в желчных протоках существенно не отличаются от таковых при вирусном гепатите С, но встречаются в меньшем проценте случаев. Примерно в 25% случаев при HBV-инфекции биопсия показала наличие лимфоидных скоплений и в менее 10% случаев выявила повреждение желчных протоков. Поверхностный и ядерный антигены вируса гепатита В также были обнаружены в холангиоцитах [8].
K. S. Kumar с соавт. (2001) подтвердили влияние хронического холангита на течение гепатита С. В исследовании участвовали 620 пациентов с ХГС с повышенным уровнем щелочной фосфатазы сыворотки крови. У больных были исключены первичный билиарный цирроз печени и первичный склерозирующий холангит. Но у части пациентов морфологически было выявлено поражение внутрипеченочных желчных протоков. Авторы считают, что наличие холангита у данной группы пациентов связано с HCV-инфекцией [11].
В ряде других исследований также можно предположить роль НСV-инфекции в развитии поражения желчевыводящей системы (ЖВС). S. S. Sharma и соавт. выявили наличие функциональных расстройств сфинктера Одди у наркоманов с продолжительным стажем внутривенного введения наркотических веществ. Моторно-кинетические нарушения сфинктера Одди были подтверждены манометрией. Маркеры вирусных гепатитов у этих пациентов исследованы не были. Однако известно, что наркоманы составляют основную группу риска инфицирования HCV- и/или HBV-инфекцией. И именно этим вирусам, по-видимому, принадлежит роль в развитии дисфункциональных нарушений сфинктера Одди у данной категории пациентов [12].
Существуют работы, посвященные изучению возможной репликации вируса в желчном эпителии. M. A. Loriot с соавт. удалось in vitro инфицировать вирусом гепатита С клетки желчного эпителия у пациентов без НСV-инфекции. Это исследование, бесспорно, расширяет представление о клеточном тропизме вируса гепатита С и доказывает чувствительность желчного эпителия к данному вирусу [13].
К выводу о том, что билиарная система тесно связана с HCV-инфекцией и что желчь также инфицирована, как и сыворотка крови, пришли японские ученые. У 12 больных хроническим гепатитом С (у 8 была выявлена HCV PHK методом полимеразной цепной реакции) во время операции была аспирирована желчь тонкой пункционной иглой из желчного пузыря. У 5 больных с высоким содержанием РНК в сыворотке крови была обнаружена HCV PHK и в желчи. При сравнении уровней содержания вируса в сыворотке и желчи выявлено, что уровни РНК были одинаковыми. С помощью иммунопатологических исследований обнаружен вирус гепатита С в эпителиальных клетках у этих больных. В то же время у больных с отрицательной реакцией на HCV PHK вирус не был обнаружен ни в желчи, ни в желчных протоках [14].
Некоторые отечественные авторы также придерживаются точки зрения, что основной причиной расстройств ритмической деятельности билиарной системы являются воспалительные процессы в печени, приводящие к нарушению синтеза желчи, заметному уменьшению давления в протоковой системе и желчном пузыре, а в связи с этим и к постоянному спастическому сокращению сфинктера Одди [15–17].
По данным Н. Б. Волошиной (2004) у 89,6% пациентов с хроническим гепатитом В (ХВГ) диагностируются функциональные нарушения билиарного тракта. Среди них у 46,3% выявлено сочетание дисфункции сфинктера Одди по билиарному типу и гиперкинезии желчного пузыря, у 18,7% — изолированный гипертонус сфинктера Одди, 12,6% — имели гиперкинез желчного пузыря, 2,7% — гипокинез желчного пузыря и 1,6% — гипотонус сфинктера Одди. Было установлено, что функциональные нарушения билиарного тракта не зависят от типа вируса и ассоциированы с уровнем биохимической активности процесса [18].
Согласно исследованию В. А. Неронова (2010), у больных с хроническим HBV-поражением печени выявлен синдром хронической билиарной недостаточности, клинически проявляющийся жалобами на дискомфортные и (или) болевые ощущения в правом подреберье, непереносимость жирной пищи, метеоризм и обстипацию. Со стороны моторики билиарного тракта нарушен процесс работы сфинктерного аппарата желчевыводящих путей (гипертонус сфинктера Одди в 65,2% случаев — в стадии репликации, в 46,9% — в фазу интеграции вируса; гипертонус сфинктера Люткенса у 58,1% в фазу репликации и 47,2% в фазу интеграции вируса), также изменены физико-коллоидные свойства желчи с повышением плотности пузырной и печеночной порций, нарушен биохимический состав желчи, в виде снижения суммарного дебита холевой кислоты и фосфолипидов, а также холатохолестеринового и фосфолипидно-холестеринового коэффициентов. Что касается больных с хроническим HCV-поражением печени, билиарная недостаточность также имеет клинические проявления в виде непереносимости жирной пищи, метеоризма и обстипации. Со стороны моторики билиарного тракта выявлены следующие изменения: гипертонус сфинктера Одди в 79,6% у пациентов с высоким уровнем репликации и в 73,7% у пациентов с минимальной активностью. Гипертонус сфинктера Люткенса у 67,6% и у 69,3% соответственно. При изучении физико-коллоидных и биохимических свойств порций желчи установлены изменения в виде снижения дебита холевой кислоты и холатохолестеринового коэффициента. Выявлено, что хроническая билиарная недостаточность у больных с вирусными поражениями печени не специфична по отношению к возбудителю, а степень ее тяжести носит прямо пропорциональный характер степени активности вирусного процесса [19].
В работе В. Л. Останко (2010) проведено исследование состояния желчевыводящей системы (ЖВС) у пациентов с ХГС. Выявлено, что у 99% пациентов с ХГС наблюдаются изменения функционального состояния ЖВС в виде дисфункции желчного пузыря (гипотонически-гипокинетический тип у 82% и у 18% — гипертонически-гиперкинетический тип) и сфинктерного аппарата (гипертонус сфинктера Одди выявлен у 55,5% пациентов с гипертоническим типом дисфункции и у 1/3 пациентов при гипотонической дисфункции; также выявлены единичные больные с дисфункцией сфинктера Одди по гипокинетическому типу — 4%), сочетающиеся с нарушением коллоидного состава желчи в виде повышения степени литогенности (у 100% пациентов с ХГС). Причем обнаружена прямая корреляционная связь между стадией фиброза и риском развития желчекаменной болезни [20].
В своей работе К. В. Жданов и соавт. обследовали лиц молодого возраста с ХГС. У всех пациентов с помощью ультразвукового исследования, дуоденального зондирования, томографии было подтверждено наличие хронического холецистита. У 80% больных в желчи обнаружена патогенная микрофлора. В результате выполнения данной работы авторы сделали вывод, что успешная противовирусная терапия хронического гепатита С возможна только после проведения санации билиарного тракта [21].
Материалы и методы исследования
В нашей работе получены данные обследования 119 человек с хроническими гепатитами В и С в возрасте от 18 до 61 года (средний возраст составил 36,94 ± 11,2 года). Среди них — 45 женщин (37,8%) и 74 мужчины (62,2%). Согласно задачам исследования все пациенты разделены по этиологии заболевания на две группы: 1-я группа — 63 пациента с ХГС, 2-я группа — 56 пациентов с ХГВ. Контрольную группу составили 30 практически здоровых добровольцев аналогичного пола и возраста.
Всем больным проведено клиническое обследование, включающее сбор жалоб, анамнеза, объективный осмотр пациента. Клиническое обследование включало: общий анализ крови, общий анализ мочи, биохимический анализ крови, исследование уровней тканевых магния и цинка (в ногтях) методом масс-спектрометрии, иммунологическую диагностику маркеров вирусных гепатитов методами иммуноферментного анализа, полимеразной цепной реакции, эзофагогастродуоденоскопию, ультразвуковое исследование органов брюшной полости, электрокардиографию. Моторная функция ЖВС исследовалась путем проведения фракционного хроматического минутированного дуоденального зондирования с исследованием полученной желчи по методике В. А. Максимова [22].
Исследование проведено в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации (в редакции 2000 г. с разъяснениями, данными на генеральной ассамблее ВМА, Токио, 2004), с правилами Качественной клинической практики Международной конференции по гармонизации (ICH GCP), этическими принципами, изложенными в Директиве Европейского Союза 2001/20/ЕС и требованиями национального российского законодательства. Протокол исследования был одобрен Комитетом по этике ФГБОУ ВО КемГМУ МЗ РФ; процедуры рассмотрения и одобрения исследования соответствовали требованиям национального законодательства. Каждый больной подписал информированное согласие на участие в исследованиях.
При характеристике качественных показателей строились таблицы сопряженности и вычислялись частоты, для количественных показателей рассчитывались средние величины и стандартное отклонение (M ± SD). При оценке различий качественных показателей использовался хи-квадрат Пирсона, критерий Z Стьюдента. При оценке связи между двумя количественными показателями использовался ранговый корреляционный анализ Спирмена. Для изучения влияния нескольких факторов на зависимую переменную (степень фиброза печени, индекс гистологической активности) применялся линейный регрессионный анализ. Достоверность различий абсолютных и относительных показателей оценивалась с использованием критериев Манна–Уитни, Крускалла–Уоллеса. Различия между параметрами сравнения считались статистически значимыми при р ≤ 0,05.
Моторно-эвакуаторная функция билиарного тракта у пациентов с хроническими гепатитами В и С оценивалась путем анализа данных, полученных при проведении фракционного хроматического минутированного дуоденального зондирования. Результаты хроматического минутированного дуоденального зондирования пациентов с хроническими гепатитами В и С представлены в табл. 1.
Учитывая выявленные нарушения моторно-эвакуаторной функции билиарного тракта, были выделены следующие группы больных (табл. 2).
Клинические проявления функциональных нарушений ЖВС у пациентов с ХВГ соответствовали хорошо известным признакам. Так, гипомоторная дисфункция ЖП сопровождалась болью тупого характера, чувством давления, распирания в правом подреберье, эпигастральной области, усиливающихся при смене положения тела, возникающих после погрешности в питании (жирная, жареная пища). При гипермоторной дисфункции ЖП больные жаловались на коликообразные боли в правом подреберье с иррадиацией в спину, под правую лопатку, правое плечо, эпигастральную область. Боли провоцировались приемом жирной, жареной пищи, физической нагрузкой, а также стрессовой ситуацией. Часть больных отмечала чувство горечи, особенно в утренние часы, тошноту, метеоризм.
Всем пациентам с ХВГ проведено исследование микроскопического состава желчи, результаты отражены в табл. 3.
Анализируя данные, представленные в табл. 3, видно, что у пациентов с ХВГ регистрировались изменения микроскопического состава желчи во всех порциях, что косвенно указывало на наличие воспалительного процесса в ЖВС. Так, в группе ХГС выявлены следующие изменения микроскопического состава желчи: слизь в порции А обнаружена у 57 человек (90,5%), в порции В — у 46 (73%) и в порции С — у 55 человек (87,3%). Эпителий цилиндрический в большом количестве в порции А встречался у чуть более половины группы (55,5%), в порции В — у 1/3 группы (20 человек), в порции С — у 28 человек (44,4%). Присутствие лейкоцитоидов более 10 в поле зрения в порции А выявлено у 10 человек (15,8%), в пузырной порции — у 6 человек (9,5%) и в печеночной порции — у 12 человек (19%). Обнаружение цилиндрического эпителия и слизи в значительном количестве, а также избыточного количества лейкоцитоидов свидетельствовало о наличии воспалительного процесса ЖВС. У небольшой части пациентов выявлены желчные соли в большом количестве: в порции А — у 3 человек (4,8%), в порциях В и С — у 6 человек в каждой (9,5%), что указывало на высокую литогенность желчи. Паразиты и простейшие не выявлены ни в одном случае.
В группе ХГВ регистрировались следующие изменения в микроскопическом составе желчи: в порции А слизь обнаружена у 38 человек (67,8%), в порции В — у 29 (51,8%), в порции С — у 39 (69,6%). Эпителий в значительном количестве выявлен в порции А — у 24 человек (42,8%), в порции В — у 12 (21,4%) и в порции С — у 5 человек (8,9%). Лейкоцитоиды более 10 в поле зрения присутствовали в порции А у 7 человек (12,5%), в порции В — у 6 человек (10,7%) и в порции С — у 5 человек (8,9%). Желчные соли в избыточном количестве выявлены в порции А у 8 человек (14,3%), в пузырной порции — у 4 (7,1%), в порции С желчные соли встречались единичные у пятой части группы (21,4%). Паразитов и простейших также, как и в группе ХГС, выявлено не было.
Выводы
Итак, анализируя данные, полученные в результате хроматического минутированного дуоденального зондирования, можно сделать вывод, что при хронических гепатитах В и С имеют место выраженные изменения функционального состояния билиарного тракта как в работе сфинктерного аппарата, так и в работе ЖП, а также дуоденальная гипертензия и повышение печеночного холереза. Выявленные изменения микроскопического состава желчи также косвенно указывают на наличие воспалительного процесса в ЖВС у пациентов с хроническими гепатитами В и С. Данные изменения билиарного статуса часто требуют уточнения и коррекции, но игнорируются лечащими врачами, снижая качество жизни пациентов.
Литература
Е. Ю. Плотникова* , 1 , доктор медицинских наук, профессор
М. С. Карягина**
М. А. Шамрай**
Е. Н. Баранова*, кандидат медицинских наук
* ФГБОУ ВО КемГМУ МЗ РФ, Кемерово
** ГАУЗ КО ОКБСМП им. Подгорбунского, Кемерово
В статье описано течение холестатического варианта врожденной цитомегаловирусной инфекции у детей с оценкой акушерско-гинекологического анамнеза матерей и особенностей неонатального периода у новорожденных. Беременность у женщин протекала с признаками фет
Abstract. The article describes the course of the cholestatic variant of congenital cytomegalovirus infection in children with an assessment of the obstetric and gynecological history of mothers and the characteristics of the newbornneonatal period. Pregnancy in women proceeded with signs of fetal-placental insufficiency, which led to the birth of children with a low gestational age, since cytomegalovirus infection developed in an acute form. The newborns had a low Apgar score and signs of hypotrophy of I-II degrees. The clinical picture of congenital cytomegalovirus hepatitis was characterized by a protracted course and had an undulating character, a complete recovery of mass-growth parameters, a symptom of jaundice took place within 3 months. It was revealed that a longer cholestasis syndrome was observed in children who had both congenital cytomegalovirus infection and impaired bilirubin uptake, in particular, Gilbert's syndrome. Ursodeoxycholic acid is the only generally accepted starting drug for the drug effect on cholestasis syndrome in children with liver disease. Complex therapy with the use of the drug Ursodeoxycholic acid at a dose of 15-20 mg/kg per day, at the early stages of treatment, this infectious pathology made it possible to stabilize the clinical and laboratory parameters. In the absence of complaints and clinical manifestations, the levels of ALT, AST and ALP were restored for a long period within 5-6 months, while the cholesterol values returned to normal by 3 months. The chosen scheme of therapy with Ursodeoxycholic acid at a dose of 15-20 mg/kg per day contributed to the prevention of severe complications from the biliary tract, such as chronic cholecystocholangitis, primary biliary cirrhosis. The use of therapeutic tactics, taking into account the individual characteristics of young children, was not accompanied by the presence of side effects. For citation: Pervishko O. V., Soboleva N. G., Baum T. G., Volik D. V., Kalinovskya D. Yu. Congenital cytomegalovirus hepatitis: cholestatic syndrome and its correction // Lechaschi Vrach. 2022; 2 (25): 20-24. DOI: 10.51793/OS.2022.25.2.003
Резюме. В статье описано течение холестатического варианта врожденной цитомегаловирусной инфекции у детей с оценкой акушерско-гинекологического анамнеза матерей и особенностей неонатального периода у новорожденных. Беременность у женщин протекала с признаками фетоплацентарной недостаточности, что обуславливало рождение детей с низким сроком гестации, так как цитомегаловирусная инфекция развивалась в острой форме. Новорожденные имели низкую оценку по шкале Апгар и признаки гипотрофии I-II степени. Клиническая картина врожденного цитомегаловирусного гепатита характеризовалась затяжным течением и носила волнообразный характер, полное восстановление весоростовых показателей, симптома желтухи проходило в течение 3 месяцев. Выявлено, что более длительный синдром холестаза отмечался у детей, которые имели одновременно врожденную цитомегаловирусную инфекцию и нарушение захвата билирубина, в частности синдром Жильбера. Единственным общепринятым стартовым препаратом для медикаментозного воздействия на синдром холестаза при заболеваниях печени у детей является урсодезоксихолевая кислота. Комплексная терапия с применением препарата урсодезоксихолевой кислоты в дозе 15-20 мг/кг в сутки на ранних этапах лечения данной инфекционной патологии позволила стабилизировать клинико-лабораторные показатели. При отсутствии жалоб и клинических проявлений уровни аланинаминотрансферазы, аспартатаминотрансферазы и щелочной фосфатазы восстанавливались в течение 5-6 месяцев, тогда как показатели холестерина нормализовались к 3 месяцам. Выбранная схема терапии препаратом урсодезоксихолевой кислоты в дозе 15-20 мг/кг в сутки способствовала профилактике тяжелых осложнений со стороны желчевыводящих путей, таких как хронические холецистохолангиты, первичный билиарный цирроз. Применение лечебной тактики с учетом индивидуальных особенностей детей раннего возраста не сопровождалось побочными эффектами.
В зарубежных и отечественных литературных источниках наиболее исследованной инфекцией раннего детского возраста была и остается одна из герпетических, а именно цитомегаловирусная (ЦМВИ). Влияние вирусного агента на различных этапах внутриутробного и внеутробного периода формирует основную клиническую картину. Вариантами течения заболевания являются:
- острый приобретенный ЦМВ-гепатит с полным выздоровлением;
- первично-хронический приобретенный ЦМВ-гепатит умеренной степени активности;
- врожденный ЦМВ-гепатит с формированием порока развития (атрезии) желчевыводящих путей;
- формирующийся билиарный цирроз печени 2.
Механизм формирования отличных друг от друга патологий печени при ЦМВИ до конца не изучен [5]. В то же время с помощью нецелевой газовой хроматографии – масс-спектрометрии активно исследуются изменения аминокислотного, азотного и энергетического обмена у детей с инфантильной холестатической гепатопатией и внепеченочной билиарной атрезией [6]. Современные клинические характеристики ЦМВ-гепатита связаны с синдромом длительной желтухи, гиперферментемией, холестазом, а также с формированием аплазии/гипоплазии желчных протоков 8.
Современная лабораторная диагностика позволяет установить причину заражения гепатотропным вирусом и определить вовлеченность паренхимы в патологический процесс [9]. Холестатический вариант течения болезни является наиболее распространенным. Он характеризуется наличием желтухи у 62% детей. Основным биохимическим показателем холестаза у новорожденных и детей раннего возраста является повышение в сыворотке крови щелочной фосфатазы (ЩФ), 5-нуклеотидазы (5-НТ), гаммаглутамилтранспептидазы (ГГТ) [10]. В этом случае показатели аланинаминотрансферазы (АЛТ)/аспартатаминотрансферазы (АСТ) повышаются одновременно в 1,5-2 раза, но с преобладанием уровня АСТ [11].
Длительное хроническое течение заболевания требует назначения гепатопротекторов комбинированного воздействия, в частности, обладающих желчегонным, цитопротективным, антифибринолитическим действием. Единственным общепринятым стартовым препаратом для медикаментозного воздействия на синдром холестаза при заболеваниях печени у детей является урсодезоксихолевая кислота (УДХК) [12]. В литературных источниках широко описаны области ее применения, в частности в составе комплексной терапии холестаза у новорожденных и детей раннего возраста 16, при вирусных гепатитах В и С, а также с целью проведения дифференциальной диагностики билиарной атрезии и неонатального гепатита у 101 ребенка [17]. Основное холеретическое действие УДХК обусловлено несколькими механизмами, в частности конкурентной борьбой с токсичными желчными кислотами за рецепторы в подвздошной кишке, влиянием на гидрофобные желчные кислоты с целью их выведения, активацией транспортных белков [18].
На основании вышесказанного целью нашей работы явилось изучение эффективности применения УДХК при врожденном ЦМВ-гепатите у детей с признаками холестатического синдрома.
Материалы и методы исследования
Под наблюдением находились 34 ребенка в возрасте от 28 дней до 12 месяцев с висцеральной формой врожденной ЦМВИ, протекавшей с синдромом холестаза. Среди них было 19 мальчиков и 15 девочек, выписанных из родильного дома или со второго этапа выхаживания. Ежемесячно при проведении объективного осмотра измеряли антропометрические параметры, оценивали динамику результатов лабораторно-инструментальных обследований.
При выявлении синдрома холестаза всем обследуемым назначали суспензию УДХК (Урсофальк) в вечернее время (19-22 часа) в дозе 15-20 мг/кг в сутки в 1 прием в течение первого месяца с последующим ежемесячным динамическим контролем.
Результаты и обсуждение
У большинства наших пациентов акушерско-гинекологический анамнез был отягощен. В частности, угроза прерывания беременности на ранних сроках отмечалась у 21 женщины; признаки хронической фетоплацентарности – у 67%.
Проведение скрининга на TORCH-инфекции показало, что ЦМВ выявлялся у 7 из 34 обследуемых женщин во время беременности с помощью метода ПЦР-диагностики в крови. После консультации инфекциониста женщины получали лечение интерфероном α-2b по схеме, с последующим динамическим контролем. Остальные беременные на герпетические инфекции не обследовались, 2 женщины на учете не состояли. При сборе акушерского анамнеза обращало на себя внимание наличие контактов внутри семьи с детьми, посещающими детский сад и школу, при этом 9 детей получали лечение по поводу приобретенной ЦМВИ.
Большинство детей родились в срок, но 6 из них имели низкий срок гестации от 32 до 36 недель. Путем кесарева сечения родились 11 детей, при этом отмечен длительный безводный период продолжительностью более 14 часов. При рождении большинство детей имели низкую оценку по шкале Апгар: 6-7 баллов – 21 ребенок; 5-7 баллов – 9 новорожденных; 3-5 баллов – 4 пациента. Оценка весоростовых показателей выявила у 19 новорожденных признаки гипотрофии I–II степени. Признаки врожденной пневмонии отмечались у 12 детей (35%), синдром дыхательных расстройств – у 11 пациентов (32%). Неврологическая симптоматика с момента рождения у 14 (41%) наблюдаемых была представлена синдромом двигательных нарушений, 18 (53%) имели признаки вегетовисцеральных нарушений, 2 (6%) – гипертензионно-гидроцефальный синдром.
Продолжительность лабораторных изменений в биохимических анализах и их показатели перед началом и после терапии представлены в табл. 2.
Прием Урсофалька позволил нормализовать уровень общего и прямого билирубина, содержание холестерина в течение первых 2-3 месяцев лечения, тогда как максимально долго сохранялись высокими уровни АЛТ, АСТ, ГГТ, ЩФ. Особенностями ОАК крови при висцеральной форме ЦМВИ были лейкоцитоз до 13,6 ± 3,1 × 10 9 г/л со сдвигом влево у 2/3 больных; увеличение лимфоцитов – у 55,8% детей; нейтропения – у 41,2%; гипохромная анемия – у 50% обследуемых. Стабилизация показателей тромбоцитов происходила в течение двух месяцев.
По данным ультразвукового обследования органов брюшной полости определялись увеличение печени у 2/3 детей, которое держалось более 6 месяцев, и спленомегалия – до 5 месяцев. Толщина стенки желчного пузыря нормализовалась на фоне применения препарата Урсофальк в течение 2 месяцев у большинства пациентов.
При проведении контроля ПЦР-диагностики на ЦМВ в крови, моче, слюне динамика отрицательных результатов выявилась следующая: в крови вирус перестал определяться в течение 2,5 месяцев. Вирус продолжал сохраняться в слюне (до 2000 копий/ мл) в течение 10 месяцев, в моче (до 1500 копий/ мл) – 9 месяцев при отсутствии клинических проявлений, переводя данное заболевание в стадию стабилизации.
Комплексное лечение позволило нормализовать показатели биохимического анализа крови, в частности показатели общего и прямого билирубина, уровней ферментов печени и холестерина (табл. 2). Применение препарата УДХК (Урсофальк) в дозировке 15-20 мг/кг в лечении синдрома холестаза показало высокую эффективность данной лекарственной формы, а также не позволило развиться осложнениям в виде холецистохолангитов, внутридолькового холестаза, холангита, цирроза печени.
Лечение холестатического варианта врожденной ЦМВИ с использованием препарата УДХК (Урсофальк) в суспензии проводилось длительно, за время наблюдения родители не отмечали побочных эффектов терапии, а ее эффективность оценивали положительно.
Выводы:
- Формирование холестатического варианта врожденной ЦМВИ происходило при первичном инфицировании женщины во время беременности.
- Источниками инфекции для женщины явилось эпидокружение, в частности, дети дошкольного и школьного возраста, посещающие организованные коллективы.
- Холестатический синдром при ЦМВ-гепатите протекает длительно и носит волнообразный характер.
- На формирование длительного синдрома холестаза также оказывали влияние наследственные заболевания, связанные с нарушением захвата билирубина (в частности, синдром Жильбера).
- Назначение препарата УДХК (Урсофальк) приводило к нормализации клинико-лабораторных и инструментальных показателей у детей с синдромом желтухи и холестаза при ЦМВ-гепатите.
- Длительность терапии препаратом УДХК (Урсофальк) определяется индивидуальными особенностями пациента.
- Антихолестатическая терапия препаратом Урсофальк при его длительном приеме направлена на профилактику осложнений при врожденном ЦМВ-гепатите.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
1 Федеральное государственное бюджетное образовательное учреждение высшего образования Кубанский государственный медицинский университет Министерства здравоохранения Российской Федерации; 350063, Россия, Краснодар, ул. Седина, 4
2 Клиника G8 Centre, 350062, Россия, Краснодар, ул. Совхозная, 1, корп. 7
Сведения об авторах:
Information about the authors:
Врожденный цитомегаловирусный гепатит: холестатический синдром и его коррекция/ О. В. Первишко, Н. Г. Соболева, Т. Г. Баум, Д. В. Волик, Д. Ю. Калиновская
Для цитирования: Первишко О. В., Соболева Н. Г., Баум Т. Г., Волик Д. В., Калиновская Д. Ю. Врожденный цитомегаловирус¬ный гепатит: холестатический синдром и его коррекция // Лечащий Врач. 2022; 2 (25): 20-24. DOI: 10.51793/OS.2022.25.2.003
Теги: новорожденные, цитомегаловирус, желтуха, холестаз
Холестатический гепатит – это заболевание, в развитии которого ключевое значение имеет затруднение тока желчи, а также накопление составляющих ее компонентов в печени. Клинически болезнь проявляется зудом, дискомфортом в зоне правого подреберья, интенсивной желтухой, диспепсией, увеличением печени и появлением ксантелазм на коже. В диагностике основное значение имеют общеклиническое и биохимическое исследования крови с определением печеночных проб, УЗИ печени и желчного пузыря, сонография поджелудочной железы, МРТ органов брюшной полости. Терапия направлена на улучшение оттока желчи и нормализацию функции органа.
МКБ-10
Общие сведения
Холестатический гепатит представляет собой достаточно редкую патологию, в основе патогенеза которой лежит внутрипеченочный холестаз с ухудшением экскреторной функции клеток и повреждением протоков. Частота выявления заболевания не превышает 10% среди всех гепатитов с хроническим течением. Холестатический гепатит преимущественно встречается у людей пожилого возраста.
Несмотря на свою относительно низкую распространенность, заболевание плохо поддается лечению в связи с тем, что не всегда возможно четко установить его причину. Изучением этиологии и патогенеза, а также разработкой новых методов терапии холестатического гепатита занимается клиническая гастроэнтерология.

Причины
Данная патология может быть обусловлена внутрипеченочным или внепеченочным застоем желчи. В первом случае нарушение оттока желчи возможно как на уровне клеток печени, так и на уровне внутрипеченочных протоков. Причинами внутрипеченочного холестаза с последующим развитием гепатита может выступать:
- переход острого вирусного гепатита В, С или других типов в хроническую форму;
- поражение печени вирусами Эбштейна-Барра, герпеса, цитомегаловирусом, микоплазменная инфекция;
- прием различных препаратов, таких как аминазин, некоторые диуретики, антибиотики, анаболические стероиды, контрацептивы;
- воздействие токсинов, алкоголя, ядов;
- эндокринные заболевания.
Внепеченочный холестаз является следствием обструкции крупных протоков. В этом случае его возможными причинами служат:
- закупорка камнем общего желчного протока;
- хронический калькулезный холецистит;
- хронический панкреатит;
- рак головки поджелудочной железы и опухоли других органов гепатобилиарной системы.
На фоне холестаза в печени происходит деструкция гепатоцитов с последующим нарушением функции органа. В некоторых случаях установить причину развития заболевания не удается, что трактуется как идиопатический холестатический гепатит.
Симптомы холестатического гепатита
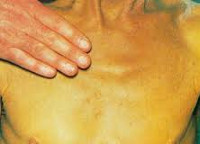
Симптоматика холестатического гепатита похожа на проявления других хронических заболеваний печени. Отличительными особенностями являются более выраженная желтуха и кожный зуд, который часто выступает первым проявлением болезни. Зуд в данном случае обусловлен попаданием в кровь желчных кислот вследствие застоя желчи в печени. Также у больных холестатической формой гепатита часто возникают ксантомы, которые имеют вид желтых пятен.
Цвет кала, как правило, становится более светлым, а моча темнеет. Пальпаторно определяется увеличение размеров и повышение плотности печени без спленомегалии. В период обострения возможно повышение температуры и неяркие симптомы интоксикации. Тяжесть клинической картины зависит от выраженности холестаза.
Диагностика
В диагностике заболевания важную роль играют лабораторные и инструментальные методы исследования. Из лабораторных методик основным для постановки диагноза холестаза считают биохимический анализ крови.
- Печеночные пробы. При биохимическом исследовании отмечается увеличение уровня билирубина за счет прямой фракции, повышение уровня трансаминаз, щелочной фосфатазы (более чем в 5 раз), гамма-глутаминтрансферазы и холестерина. Также можно определить повышенное количество в крови фосфолипидов, В-липопротеидов и желчных кислот.
- Серологическая и ПЦР-диагностика. Для подтверждения вирусной этиологии заболевания проводится исследование специфических маркеров методами ИФА и ПЦР. Характерным серологическим маркером внутрипеченочного холестаза является определение антимитохондриальных антител.
Из инструментальных методов используется эхографическая, рентгеновская, магнитно-резонансная, инвазивная диагностика:
- УЗИ печени и желчного пузыря. При ультразвуковом исследовании выявляются признаки хронического гепатита. УЗИ желчных путей, желчного пузыря и поджелудочной железы позволяет подтвердить или исключить внепеченочный холестаз.
- Рентгенография. При наличии сложностей в диагностике холестаза проводится ретроградная холангиопанкреатография, чрескожная чреспеченочная холангиография или холецистография, которые позволяют обнаружить камни в желчных путях в тех случаях, когда они не видны на УЗИ.
- МРТ. Современными неинвазивными методами выявления причин холестатического гепатита являются МР-панкреатохолангиография и МРТ гепатобилиарной зоны.
- Биопсия с гистологией. Для изучения морфологических изменений может проводиться пункционная биопсия печени, хотя она и не играет решающей роли в диагностике холестаза.
Лечение холестатического гепатита
Лечение хронического гепатита с холестатическим синдромом должно быть основано на устранении причины, которая привела к холестазу. Если причиной заболевания является воздействие токсических факторов или медикаментозных препаратов, то необходимо прекратить их поступление в организм. Всем больным рекомендуется придерживаться диеты №5, которая предусматривает исключение острой, жирной и жареной пищи. Обязательно минимизировать употребление алкоголя, который негативно влияет на клетки печени. Также рекомендовано полноценное питание с достаточным содержанием белка.
Медикаментозная терапия
На любой стадии заболевания желателен прием жирорастворимых витаминов А, Е, а также В12. Для улучшения функции гепатоцитов могут назначаться гепатопротекторы, эссенциальные фосфолипиды и липоевая кислота. При наличии внутрипеченочного холестаза с высокой активностью воспалительного процесса показано назначение небольших доз преднизолона для уменьшения выраженности патологических изменений.
Если больного беспокоит сильный зуд, необходимо применение препаратов для нейтрализации желчных кислот, таких как холестирамин или лигнин. Самым эффективным средством для лечения внутрипеченочного холестаза считается урсодезоксихолевая кислота, которая улучшает отток желчи. Препарат рекомендован всем больным с холестатическим гепатитом.
Хирургическое лечение
Если гепатит вызван внепеченочным холестазом, необходимо устранить его причину. Для этого используются различные оперативные методы:
- лапароскопическая или открытая холецистэктомия;
- резекция головки поджелудочной железы;
- экстракция конкрементов желчных протоков при РПХГ;
- эндоскопическая баллонная дилатация сфинктера Одди и др.
Прогноз и профилактика
При правильном лечении и устранении причины холестаза прогноз при холестатическом гепатите в целом благоприятный. Профилактика заболевания сводится к прекращению поступления в организм алкоголя и других гепатотоксических веществ, а также своевременному лечению патологии печени.
Читайте также:

