Анализ на икб инфекция
Обновлено: 26.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Исследование иксодового клеща: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показание к назначению исследования
Показанием для выполнения исследование является присасывание клеща к телу человека.
Для Российской Федерации наибольшее эпидемиологическое значение имеют иксодовые клещи (относящиеся семейству Ixodidae).
Для инфекций, передающихся иксодовыми клещами, характерна весенне-осенняя сезонность с апреля по октябрь, однако в регионах с теплым климатом отмечается круглогодичная активность иксодовых клещей. Группами риска по заболеваемости инфекциями, передающимися иксодовыми клещами, являются жители городской и сельской местности, посещающие очаги обитания клещей. Передача возбудителей инфекций происходит при присасывании зараженных клещей к телу человека.

К инфекциям, передающимся иксодовыми клещами, относятся клещевой вирусный энцефалит, иксодовые клещевые боррелиозы, клещевой гранулоцитарный анаплазмоз человека, моноцитарный эрлихиоз человека и другие (лихорадка Ку, крымская геморрагическая лихорадка, туляремия, риккетсиозы).
Возбудитель клещевого энцефалита - РНК-содержащий вирус рода Flavivirus. Инкубационный период заболевания составляет, как правило, 7–14 дней от момента присасывания клеща, но может длиться до 25 дней. Инфекция поражает клетки головного и спинного мозга с последующим развитием парезов и параличей.
Выявление возбудителя клещевого вирусного энцефалита в клеще позволяет своевременно провести экстренную профилактику инфекции. В случае получения положительного результата показано экстренное введение специфического иммуноглобулина - не позднее 72 часов от момента укуса. Максимальная эффективность препарата наблюдается при его введении в течение первых суток после укуса.
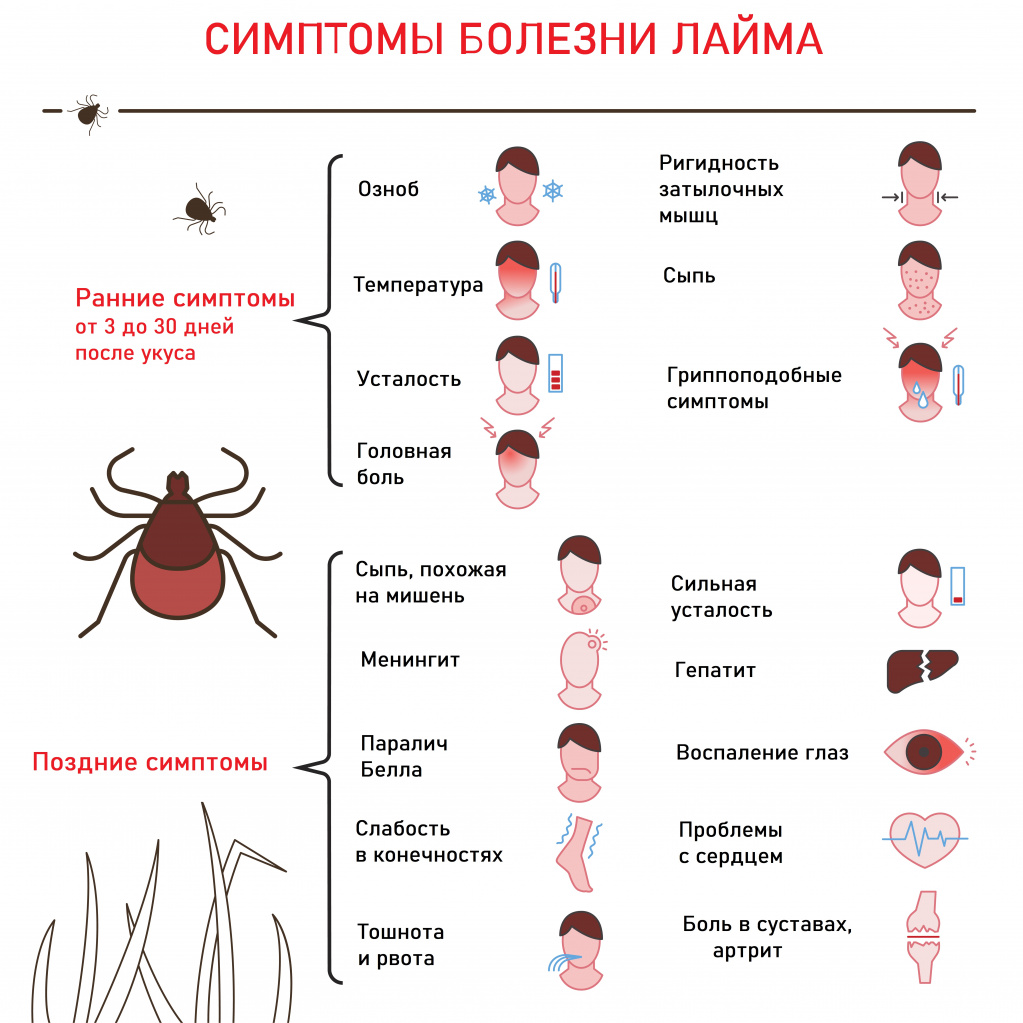
Возбудитель болезни Лайма - спиралевидная бактерия рода Borrelia. Заболевание развивается в 20% случаев после присасывания клеща, инфицированного боррелиями. У 50-80% больных отмечается местное кожное воспаление – клещевая мигрирующая эритема (покраснение), диаметр которой не превышает 5 см. При распространении по крови боррелии поражают внутренние органы, клетки нервной системы, в результате чего могут развиться менингит, менингоэнцефалит, радикулоневрит, неврит черепных нервов.
Возбудитель гранулоцитарного анаплазмоза человека - бактерия Anaplasma phagocytophilum, которая поражает гранулоциты – белые клетки крови, содержащие гранулы (нейтрофилы, эозинофилы, базофилы). Заражение происходит при укусе клеща, инфицированного бактериями - анаплазмами.
Среди симптомов заболевания отмечают длительную лихорадку, слабость, головную боль, потливость, кашель, тошноту, рвоту, диарею, боль в мышцах и суставах. Увеличиваются лимфатические узлы, могут наблюдаться поражения почек, печени, селезенки. Реже диагностируется воспаление оболочек головного и спинного мозга. Инкубационный период в среднем составляет 14 дней.
Возбудителями моноцитарного эрлихиоза являются бактерии, относящиеся к роду Ehrlichia. Они попадают в организм человека со слюной клеща, по лимфатическим путям проникают в кровь и начинают размножаться в клетках внутренней поверхности сосудов, в белых клетках крови - моноцитах. После разрушения клетки микроорганизмы выходят из нее и инфицируют другие. Поражаются внутренние органы (печень, центральная нервная система, костный мозг, кожа) с развитием инфекционных гранулем. Клиническая картина эрлихиоза схожа с гранулоцитарным анаплазмозом.
Гранулоцитарный анаплазмоз человека, моноцитарный эрлихиоз и боррелиоз являются показанием к назначению антибактериальной терапии. При своевременном выявления заболевания и лечении прогноз благоприятный.
Подготовка к процедуре
При обнаружении присосавшегося клеща для его удаления из тела необходимо обратиться в травматологический пункт. Если такой возможности нет, клеща следует удалить самостоятельно. Для этого нужно перехватить тело клеща обернутыми марлей пальцами или пинцетом строго перпендикулярно поверхности тела, как можно ближе к его ротовому аппарату. Затем, поворачивая тело клеща вокруг оси, извлечь его. Не рекомендуется смазывать место укуса и самого клеща маслом. Клеща с кусочком влажной ваты необходимо поместить в плотно закрываемую емкость (специальный контейнер с крышкой для исследования биоматериала, банку, пробирку или др.). Нельзя помещать в одну емкость клещей, снятых с разных людей.
Ранку на коже продезинфицировать антисептиком (спиртом, йодом, зеленкой), руки после извлечения клеща тщательно вымыть с мылом. Контейнер с клещом доставить в ближайший медицинский офис в день снятия. В настоящее время можно приобрести специальные устройства для удаления клеща, которые продаются в аптеке.

Живого клеща до исследования допускается хранить в холодильнике при +2 +8 о С до 1 мес. Исследование мертвого клеща допускается при условии хранения его после снятия в холодильнике при температуре +2 +8 о С не более 5 суток. С учетом риска развития клещевого энцефалита и продолжительности исследования (до 3 рабочих дней) лучше отдать клеща на исследование в день снятия с тела.
Срок исполнения
Что может повлиять на результат
Сроки выполнения ПЦР-исследований могут быть увеличены при проведении подтверждающих тестов.
Лабораторное исследование клеща для выявления РНК/ДНК возбудителей инфекций, передаваемых иксодовыми клещами: клещевого энцефалита, боррелиоза (болезни Лайма), анаплазмоза, эрлихиоза
Синонимы: ПЦР-диагностика клещевого энцефалита, боррелиоза, анаплазмоза и эрлихиоза. Tick-borne diseases, polymerase chain reaction, PCR, tick-borne encephalitis, Lyme disease, human anaplasmosis, human ehrlichiosis. Краткое описание теста «Лабораторное исследование клеща для выявления РНК.
В статье представлены основные сведения, касающиеся клинико-эпидемиологических особенностей клещевых боррелиозов у детей, проживающих на территории Новосибирской области. Наблюдения за показателями заболеваемости фиксируют отчетливый тренд в повышении кол
Иксодовые клещевые боррелиозы (ИКБ) (синонимы: болезнь Лайма, Лайм-боррелиоз) в настоящее время рассматриваются как группа природно-очаговых инфекций, с трансмиссивным механизмом передачи, характеризующаяся полисистемным поражением и большим полиморфизмом клинических проявлений.
До открытия возбудителя ИКБ проявления болезни описывались как отдельные синдромы или самостоятельные заболевания с неясной этиологией: лимфоцитарный менингорадикулит (синдром Баннварта), серозный менингит, хронический артрит, клещевая эритема, лимфоцитома и т. д. (A. Bannwarth, V. Sedlacek и др.). В России нозологическую самостоятельность иксодовые клещевые боррелиозы получили с 1991 года, а с 1992 года — были введены в форму статистической отчетности по инфекционным заболеваниям [1, 2].
Проводимые исследования в самих природных очагах как на территории Российской Федерации, так и в странах Европы показывают увеличение численности клещей и усиление активности циркуляции самого возбудителя [1, 5], что определяет тенденцию к повышению заболеваемости клещевыми боррелиозами в настоящее время.
Этиология клещевых боррелиозов
Сегодня известно (Johnson и соавт., 1984), что спирохеты, вызывающие клещевые боррелиозы, относятся к роду Borrelia. Данный род представляет собой гетерогенную популяцию микроорганизмов и подразделяется на две большие подгруппы:
1) возбудители возвратной клещевой лихорадки: B. recurrentis, B. duttoni, B. parkeri, B. turicatae, B. hermsii, B. miyamotoi и др.;
2) возбудители Лайм-боррелиозов: B. burgdorferi sensu stricto, B. garinii, B. afzelii, B. usitaniаe, B. valaisiana, B. andersonii, B. bissettii, B. japonica, B. tanukii, B. turdi, B. inica.
Указанные виды боррелий вследствие высокого фенотипического и генетического сходства были объединены в единый комплекс B. burgdorferi sensu lato [7]. Хотя этот комплекс сегодня включает до 18 видов Borrelia, только три из них являются явно патогенными: B. afzelii, B. burgdorferi и B. garinii (в том числе B. garinii OspA, тип 4, или B. bavariensis) [8, 9]. Зараженность клещей боррелиями в природных очагах варьирует от 10% до 80% [7, 10, 11]. В Новосибирской области как в природном очаге, так и у больных иксодовыми клещевыми боррелиозами чаще выявляется ДНК Borrelia garinii и Borrelia afzelii.
Основной механизм заражения при ИКБ — трансмиссивный, боррелии попадают в организм человека со слюной инфицированных клещей при кровососании. Пути передачи: трансмиссивный, алиментарный, контактный (через микротравмы кожных покровов при снятии и раздавливании клеща) и трансплацентарный. Сезонность заболевания — весенне-летняя, обусловленная периодом активности клещей. Иммунитет нестерильный, возбудитель способен к длительной персистенции в организме, возможны супер- и реинфекции [11]. После укуса клеща вероятность сероконверсии у человека находится в диапазоне от 3% до 6%. Клинически манифестные формы заболевания возникают в 0,3–1,4% случаев от всех укусов клещей.
Учитывая, что входными воротами инфекции при клещевых боррелиозах является кожа, где происходит размножение возбудителя с последующим лимфогенным распространением его в ближайшие лимфатические узлы и развитием регионарного лимфаденита, в месте присасывания клеща возникает первичный аффект с образованием эритемы [11–13]. Согласно статистическим данным, по мнению и отечественных и зарубежных авторов [3, 14], эритемные формы заболевания наблюдаются в клинической картине ИКБ в 40–70% случаев. При анализе заболеваемости трансмиссивными клещевыми инфекциями 125 детей в возрасте от 1 до 18 лет, проживающих в Новосибирской области, за 13 лет (период с 1999 по 2011 годы), было установлено, что иксодовыми клещевыми боррелиозами заболели 78,5% из них (95 человек). Заболевание протекало в эритемной форме у 94 больных ИКБ (98,9%). Диагноз выставлялся в соответствии с МКБ 10-го пересмотра на основании клинико-эпидемиологических, общеклинических, специфических (серологического — иммуноферментный анализ (ИФА), молекулярно-генетического — полимеразная цепная реакция (ПЦР)) и биохимических методов обследования.
Поражением кожи — мигрирующей эритемой — характеризуется период ранних локализованных проявлений (стадия локальной инфекции) при ИКБ. Эритема обычно возникает через 7–14 дней от момента укуса клеща (от 3 до 30 дней), локализуется вокруг места укуса, имеет округлую или овальную форму и тенденцию к распространению. В месте эритемы возможно возникновение кожного зуда, парестезий, повышение местной температуры. В отсутствие антибактериальной терапии эритема спонтанно угасает в сроки от нескольких дней до нескольких недель (в среднем — около 4 недель). У 10–30% больных мигрирующая эритема сопровождается неспецифическими симптомами, такими как недомогание, субфебрильная температура, кратковременные мигрирующие боли в мышцах и небольших суставах, утомляемость [15].
По нашим данным, в 44 случаях (46,3%) первыми признаками заболевания при ИКБ у детей явилось именно покраснение в месте укуса клеща. При наблюдении за детьми с эритемной формой иксодовых клещевых боррелизов, эритема появлялась в месте укуса клеща в срок до 45 дней (максимально) от момента присасывания клеща к коже, в среднем — на 11 ± 7 день. Размеры эритемы составляли от 1,5 до 20 см (в среднем — 6,6 ± 4 см). В редких случаях отмечался рост эритемы в размерах за период наблюдения. Эритема сохранялась на коже максимально до 36 дней, в среднем 8 ± 5 дней, с момента начала антибактериальной терапии угасала в среднем через 7 ± 4 дней. В 11 случаях (11,6%) эритема угасала с последующим шелушением. В двух случаях отмечалась эритема в виде двойного кольца, у троих детей отмечалось повышение местной температуры в области мигрирующей эритемы. В 5 случаях (5,3%) кожные проявления были представлены экзантемой (петехиальные, крупно- и среднепятнистые элементы сыпи), в сочетании с эритемой в месте присасывания клеща. Во всех пяти случаях сочетания эритемы и сыпи на туловище, у больных отмечалась лихорадка до фебрильных цифр и довольно интенсивные проявления интоксикации.
Наличие мигрирующей эритемы является патогномоничным симптомом клещевого боррелиоза. В последующем происходит диссеминация возбудителя: гематогенно, лимфогенно и периневрально боррелии распространяются на другие участки кожи, во внутренние органы (печень, селезенку, почки, сердце), суставы, оболочки мозга, центральную и периферическую нервную системы.
Генерализация инфекции (стадия диссеминации боррелий) у взрослых наиболее часто характеризуется поражением нервной системы в виде менингорадикулоневрита (синдрома Баннварта): сочетание серозного менингита, радикулита и поражения черепномозговых нервов (чаще всего в виде одно- или двустороннего периферического паралича лицевого нерва). Генерализованная стадия заболевания может протекать также с формированием кардита, лимфоцитомы (доброкачественная опухоль красно-фиолетового цвета), которая обычно локализуется на мочке уха у детей, а у взрослых в области ареол, мошонки, носа и предплечий.
К поздним и персистирующим клиническим проявлениям ИКБ (стадия органных поражений) относятся хронический атрофический акродерматит (acrodermatitis chronica atrophicans of Herxheimer, ACA) и хронический артрит, а также полинейропатии, хронический прогрессирующий менингоэнцефалит и мультифокальный церебральный васкулит, которые характеризуются необратимым неврологическим дефицитом и прогредиентным течением болезни. Обычно такие проявления развиваются не более чем у 5% пациентов, перенесших нейроборрелиоз. Также редко описываются случаи экстрапирамидных нарушений на фоне хронической боррелиозной инфекции. Суставные поражения могут возникать отсроченно, при отсутствии терапии, через несколько месяцев и даже лет после укуса клеща и обычно протекают в виде хронического олигоартрита, с ассиметричным поражением одного из суставов (чаще коленных и локтевых). Хронические формы иксодовых клещевых боррелиозов являются наиболее сложными с точки зрения диагностики и лечения. Это связано с тем, что заболевание имеет неспецифические симптомы, которые могут быть характерны также для заболеваний другой этиологии (например, артрит, энцефаломиелит или периферическая невропатия), которые не позволяют уточнить диагноз при отрицательных или сомнительных лабораторных и клинических критериях.
У детей в течении ИКБ можно выделить следующие клинические особенности.
- Наиболее часто ИКБ заболевают дети в возрасте от 3 до 10 лет.
- Мигрирующая эритема развивается у детей в 70–80% случаев и у большинства больных имеет кольцевидную форму.
- Характерной локализацией эритемы у детей является волосистая часть головы, околоушная область, лицо, верхняя часть туловища.
- Общеинфекционный синдром наблюдается у 60–70% больных ИКБ детей и обычно более выражен, чем у взрослых.
- У большинства больных детей наблюдается увеличение регионарных к месту укуса клеща лимфатических узлов.
- У 10% больных детей с острым течением ИКБ наблюдается вовлечение в патологический процесс мозговых оболочек с развитием серозного менингита.
- Развитие хронического течения после перенесенных острых ИКБ у детей наблюдается в 15–20% случаев.
Диагностика ИКБ
Для постановки диагноза ИКБ необходимо учитывать сведения эпидемиологического анамнеза (присасывание клеща, посещение мест с высокой вероятностью нападения клеща — выезд на природу, выход в лес) с учетом времени года (весенне-осенний период), клинические проявления: появление мигрирующей кольцевидной эритемы, увеличение регионарных лимфоузлов, наличие неврологической, суставной и кардиальной симптоматики.
Более доступны в практическом применении серологические методы диагностики. К наиболее распространенным методам определения антиборрелиозных антител относят иммуноферментный анализ (ИФА и ELISA), метод непрямой иммунофлюоресценции, реакция связывания комплемента, реакция пассивной гемагглютинации, а также иммуноблоттинг.
При ИКБ антитела класса IgM в максимальном количестве вырабатываются к 3–4 неделе болезни, ко второму месяцу появляются антитела класса IgG. У некоторых больных синтез IgM может задерживаться или отсутствовать вообще [3, 7, 11, 16]. Сероконверсия наблюдается у 20–50%, а по некоторым данным, у 80% больных ранним боррелиозом [8]. Наличие IgM-антител к боррелиям в сыворотке крови, как правило, указывает на раннюю инфекцию. Наличие IgG-антител указывает на диссеминацию боррелий или на переход в стадию хронического персистирования. Оба класса антител могут определяться в течение длительного времени (до 10 лет), в том числе и после успешно проведенной антибактериальной терапии [17–19].
С целью повышения диагностической точности американским Центром контроля болезней было предложено проверять положительные или пограничные результаты скрининговых тестов с помощью иммунноблоттинга, используя стандартизированные критерии серопозитивности метода [20]. Основным скрининг-тестом в этой схеме является ИФА. Исследуемые образцы с положительными или сомнительными результатами в ИФА обязательно дополнительно тестируют методом иммунного блоттинга [3, 7, 20, 21]. Согласно этим рекомендациям, серологическое тестирование на болезнь Лайма считается положительным, если в одной сыворотке как скрининговый метод, так и иммунноблоттинг дали положительные результаты. В РФ не имеется таких стандартизированных критериев диагностики, однако, учитывая сложный иммунопатогенез при боррелиозах, не следует основываться для постановки диагноза лишь на одном диагностическом тесте. Расширенное обследование с использованием всех доступных методов дает преимущество, особенно в диагностике безэритемных форм и поздних стадий заболевания, а также позволяет избежать диагностических ошибок, связанных с ложноположительными реакциями.
Своевременная диагностика и раннее назначение этиотропных препаратов являются эффективным средством предупреждения развития органных поражений и хронизации заболевания. Раннее назначение антибактериальной терапии при иксодовых клещевых боррелиозах позволяет достоверно снизить риск развития неврологических, суставных и кардиальных осложнений.
Лечение и профилактика ИКБ
В настоящее время стандартом терапии иксодовых клещевых боррелиозов считается использование у детей старше 8 лет и взрослых пациентов доксициклина (100 мг 2 раза в сутки) или амоксициллина (500 мг 3 раза в сутки) в течение 14 дней при острых ИКБ. При генерализованных формах (нейроборрелиоз) терапия проводится парентеральным введением пенициллина или препаратов группы цефалоспоринов (цефотаксим, цефтриаксон) не менее 14 дней. Эффективность антибактериальной терапии оценивается по характеру клинических проявлений.
Попытки создания вакцин против клещевого боррелиоза были предприняты в США, но оказались неэффективными в связи с большим разнообразием геновидов возбудителя. В настоящее время работы по созданию вакцин продолжаются [22].
Наиболее эффективными профилактическими мерами являются мероприятия по защите от укусов инфицированных клещей при посещении мест их вероятного обитания: специальная одежда, использование защитных репеллентов, акарицидные обработки лесопарковых зон, само- и взаимоосмотры [23]. Укусов клещей также можно избежать путем тщательного осмотра и удаления клещей с домашних животных [24].
При обнаружении клеща необходимо как можно скорее удалить его с помощью пинцета, избегая раздавливания насекомого. Удалять клеща необходимо полностью, поскольку оставшиеся в коже части насекомого могут привести к аллергическим реакциям и вторичной бактериальной инфекции. Использование вазелина при удалении клеща для нарушения функции дыхания у насекомого не является эффективным, поскольку клещи имеют низкую частоту дыхания (3–15 вдохов в час) и время, требуемое для гибели насекомого, может быть достаточным для передачи возбудителя человеку [25].
Возможность и необходимость превентивной антибиотикопрофилактики после укуса инфицированного клеща в настоящее время широко обсуждается отечественными и зарубежными авторами. В США антибиотикопрофилактика после укуса инфицированного клеща проводится, если:
- клещ находился на коже более 72 часов;
- продолжительность питания клеща неизвестна;
- клещ отпал сам после насыщения.
Превентивная антибиотикотерапия не показана, если:
- укус клеща случился вне эндемичных территорий;
- клещ находился на коже менее 24 часов;
- с момента укуса прошло более 72 часов.
Если клещ находился на коже от 24 до 72 часов, вопрос решается в индивидуальном порядке, например, если сделан анализ клеща и он заражен боррелиями. Для антибиотикопрофилактики используется доксициклин 200 мг — однократный прием. Для детей старше 8 лет доза составляет 4 мг/кг массы тела до максимальной 200 мг. Беременным и кормящим женщинам, детям до 8 лет назначают амоксициллин. Время до начала приема антибиотика должно составлять не более 72 часов после удаления клеща.
В России предлагаются следующие варианты антибактериальной профилактики:
- доксициклин в дозе 0,1 г 2 раза в день курсом от 3 до 5 дней, альтернативными препаратами с целью терапии и профилактики ИКБ могут быть ампициллин, азитромицин (Н. Н. Воробьева, Э. И. Коренберг) [12];
- тетрациклин по 0,5 г 4 раза в сутки 5 дней, бензатина бензилпенициллин + бензилпенициллин прокаина + бензилпенициллин 1,2–2,4 млн ЕД внутримышечно однократно, бензатина бензилпенициллин в дозе 2,4 млн ЕД внутримышечно однократно, доксициклин по 0,1 г 2 раза в сутки в течение 10 дней, амоксициллин + клавулановая кислота по 0,375 г 4 раза в сутки в течение 5 дней. Лечение проводят не позже 5-го дня от момента укуса. Риск возникновения заболевания уменьшается до 80% (Ю. В. Лобзин, С. С. Козлов, А. Н. Усков) [26].
Если говорить о выборе оптимального препарата для профилактики ИКБ, то антибиотик, используемый в этих целях, должен обладать, с одной стороны, высокой активностью в отношении боррелий даже при однократном приеме, с другой — благоприятным спектром безопасности. Доксициклин является наиболее часто применяемым для профилактики ИКБ препаратом, так как отвечает обоим требованиям. В целях минимизации риска побочных явлений предпочтительно использовать доксициклин в форме его нейтральной соли — моногидрата, который практически не ассоциирован с развитием кислотозависимых заболеваний ЖКТ (таких, как эзофагит, язва пищевода). Кроме того, доксициклина моногидрат, представленный в форме солютаб, характеризуется максимальным удобством применения, что немаловажно для пациентов, получающих антибиотик без отрыва от повседневной активности.
Резюмируя вышесказанное, можно заключить, что тактика ведения пациентов с риском развития клещевого боррелиоза должна предусматривать рациональное назначение эффективного антибактериального препарата, позволяющего предотвратить заболевание и его потенциальные осложнения.
Литература
И. В. Куимова 1 , доктор медицинских наук, профессор
О. А. Радионова
Е. И. Краснова, доктор медицинских наук, профессор
ГБОУ ВПО НГМУ МЗ РФ, Новосибирск
Abstract. The article reveals the basic information on the clinical and epidemiological characteristics of tick-borne borreliosis in children living in the Novosibirsk region. Observation has indicated a certain tendency of increasing the amount of Ixodes tick-bore borrelioses.
Возбудители боррелиозов относятся к порядку Spirochaetales, семейству Spirochaetaceae, роду Borrelia. В группу иксодовых клещевых боррелиозов (ИКБ) входят заболевания, вызываемые в большинстве случаев тремя представителями комплекса Borrelia burgdorferi sensu lato: B.burgdorferi, B.garinii и B.afzelii. Изучается патогенный потенциал других боррелий комплекса: B.valaisiana, B.lusitaniae, B.bissettii, B.sinica. Ареал распространения этих видов боррелий в основном совпадает с территорией обитания клещей I.persulcatus и I.ricinus, играющих одновременно роль переносчика и резервуара инфекции. Спонтанная инфицированность боррелиями клещей вида:
I. ricinus составляет в среднем 20%, клещей I.persulcatus – 40%. Сезон активности иксодовых клещей начинается в последней декаде апреля и продолжается в средней полосе России до октября, а в Приморье – до ноября. ИКБ распространен в России на 69 административных территориях, наибольшая заболеваемость регистрируется в Кировской, Томской и в последние годы – Вологодской и Ярославской областях. Клинически выраженное заболевание развивается приблизительно в 20% случаев после присасывания инфицированных боррелиями клещей. В результате попадания боррелий в кожу у 50–80% больных отмечается местное кожное воспаление – клещевая мигрирующая эритема, диаметр которой, как правило, превышает 5 см. В 20–50% случаев заболевания эритема отсутствует в начале заболевания и таким образом сразу развивается диссеминированная стадия ИКБ, которая носит название безэритемной формы. В случае гематогенного распространения боррелии поражают внутренние органы, что сопровождается развитием общеинфекционного синдрома и клиническими проявлениями со стороны висцеральных органов (печени, селезенки, сердца, почек). В случае поражения нервной системы возникают менингит (менингоэнцефалит), радикулоневрит, неврит черепных нервов. Наиболее часто поражается VII пара черепных нервов, нередко с парезом лицевых мышц, что является еще одним, кроме эритемы, характерным признаком ИКБ. В ряде случаев, особенно при поздно начатом лечении, заболевание переходит в третью – хроническую – стадию, для которой в настоящее время доказана только одна клиническая форма – хронический атрофический акродерматит. Следует отметить, что у определенной части больных не наступает полное выздоровление в течение длительного времени после острого периода, может до двух лет сохраняться субфебрилитет, длительно – артриты, прогрессирующий энцефаломиелит, энцефалопатии, патологические изменения со стороны сердечно-сосудистой системы.
Показания к обследованию
- Обращение пациента за медицинской помощью с апреля по октябрь;
- факт присасывания клеща или пребывание на природе: в лесной, лесопарковой зоне, в загородных домах и прилегающих к ним территориях;
- развитие общеинфекционного синдрома;
- появление мигрирующей эритемы.
Дифференциальная диагностика. Инфекционные заболевания, передаваемыми иксодовыми клещами; рожистое воспаление; склеродермия; артрит ревматоидный или иной этиологии; миокардит; заболевания ЦНС иного генеза.
Материал для исследований
- Биоптаты кожи – микроскопические исследования, изоляция боррелий культуральным методом, обнаружение ДНК;
- цельная кровь – изоляция боррелий культуральным методом, обнаружение ДНК;
- сыворотка крови – выявление специфических АТ;
- СМЖ – выявление специфических АТ (при развитии серозных менингитов), изоляция боррелий культуральным методом, обнаружение ДНК;
- моча – обнаружение ДНК;
- синовиальная жидкость – выявление специфических АТ (при артритах), изоляция боррелий культуральным методом, обнаружение ДНК.
Этиологическая лабораторная диагностика включает выявление возбудителя методом микроскопии, изоляцию боррелий с использованием культурального метода, обнаружение ДНК боррелий, выявление специфических АТ.
Сравнительная характеристика методов лабораторной диагностики. Обнаружение специфических АТ IgM и IgG – наиболее часто используемый метод лабораторной диагностики ИКБ. Применение РНИФ позволяет обнаружить АТ у 40–50% больных в первые 2–4 недели заболевания, а при исследовании образцов крови в динамике, взятой с интервалом в 1–3 месяца, удается подтвердить ИКБ в 60–70% случаев. Диагностически значимым титром в данной реакции считается положительный результат при разведении сыворотки 1:40, а также четырехкратное нарастание титра АТ во второй из взятых проб относительно первой.
При определении АТ методами ИФА, ИХЛА и т. п. в основном используются несколько (от 4 до 8) рекомбинантных АГ боррелий, относящихся к разным геновидам. Методы обладают большей диагностической чувствительностью в сравнении с РНИФ. АТ IgM начинают обнаруживаться к концу второй недели заболевания, АТ IgG – на 3–4-й неделе заболевания. Обнаружение АТ IgM отмечают у 50% больных с хронической формой ИКБ, что, видимо, связано с изменением антигенных детерминант во время персистенции боррелий в организме больного. Данные о диагностической чувствительности выявления АТ на разных стадиях заболевания приведены в таблице.
Диагностическая чувствительность определения специфических антител при ИКБ
| Стадия заболевания | АТ IgM | АТ IgG | АТ IgM+IgG |
|---|---|---|---|
| Острая (I) | 45–70% | 40–80% | 90% |
| Подострая (II) | 30–60% | 65–100% | 90–100% |
| Хроническая (III) | 5–50% | до 100% | до 100% |
При лабораторном подтверждении нейроборрелиоза для определения наличия интратекального синтеза АТ проводится выявление специфических АТ в сыворотке крови и СМЖ. Относительное увеличение концентрации специфических IgG в ЦНС можно определить путем вычисления ликвор-сывороточного индекса (ЛСИ). Для этой цели определяют концентрацию специфических Ig (титр) и общих Ig (г/л) в сыворотке крови и СМЖ.
ЛСИ = (специфические IgG (СМЖ) * общие IgG (сыворотка)) / (общие IgG (СМЖ) * специфические IgG (сыворотка))
Значения ЛСИ больше 2-х расцениваются как положительные и указывают на наличие синтеза специфических иммуноглобулинов клетками глиальной ткани.
Ложноположительные результаты при выявлении АТ методами РНИФ и ИФА могут быть получены у больных с другими спирохетозами: сифилисом и лептоспирозом, у пациентов с ревматоидным артритом неборрелиозной этиологии и другими системными заболеваниями, у пациентов с герпес-вирусной инфекцией, вызванной ЦМВ и вирусом Эпштейн-Барр, а также у беременных.
Для подтверждения специфичности результатов выявления АТ методами РНИФ и ИФА используют метод ИБ, который позволяет обнаружить специфические АТ к определенным белкам возбудителя. В качестве АГ в основном используются рекомбинантные белки p83-100, p58, p41i, p39 (BmpA), OspC (p20-25), p17 (DbpA), BBK32, VlsE, полученные для двух, а иногда и для трех видов боррелий.
Микроскопия (световая, фазовоконтрастная, темнопольная, электронная) биологического материала (СМЖ, кровь, синовиальная жидкость, биоптаты тканей) не имеет широкого применения из-за низкой концентрации возбудителя (в среднем концентрация боррелий в 1 мл биологического материала не превышает 10 000 микробных клеток), за исключением биоптатов кожи. В основном микроскопические исследования используются при контроле культуральных методов и как один из методов при оценке инфицированности боррелиями иксодовых клещей.
При применении для изоляции боррелий культурального метода в качестве среды для культивирования используется модифицированная среда BSK (BarbourStoenner- Kelly). Важным условием является получение образцов биологического материала до начала антибиотикотерапии. Из кожных биоптатов удается изолировать боррелии в 50–60% случаев при наличии клещевой мигрирующей эритемы и в 90% – при хроническом атрофическом акродерматите. При исследовании крови, СМЖ, синовиальной жидкости процент положительных результатов ниже – в среднем 20%. Этот метод не имеет широкого практического применения как диагностический в виду его длительности (от 3–4 до 10 недель) и высокой стоимости.
Выявление ДНК боррелий с использованием молекулярно-биологических методов (преимущественно ПЦР) целесообразно применять в комплексе с выявлением АТ. Прямым показанием для применения ПЦР являются боррелиозные менингиты, менингоэнцефалиты, наличие атипичной эритемы, рефрактерные артриты у пациентов с наличием АТ к боррелиям. Диагностическая чувствительность данного метода составляет от 20 до 35% при исследовании крови в остром периоде на первой неделе заболевания, от 20 до 80% при исследовании синовиальной жидкости при развитии Лайм-артрита и около 10–30% – при исследовании СМЖ при нейроборрелиозе. Метод позволяет также идентифицировать вид боррелий, вызвавших заболевание. Обнаружение ДНК и РНК боррелий методом ПЦР может быть выполнено во всех видах биологического материала (кровь, моча, биоптаты тканей, цереброспинальная и суставная жидкости и др.).
Особенности интерпретации результатов лабораторных исследований. Обнаружение ДНК патогенных боррелий комплекса B.burgdorferi sl в крови, СМЖ, синовиальной жидкости или моче пациента является основанием для предварительной постановки диагноза ИКБ. Выявление специфических АТ в образцах крови, взятых в динамике (сероконверсия в парных сыворотках крови) служит подтверждением этиологии заболевания.
Интерпретация результатов ИБ в основном сводится к алгоритму, представленному в таблицах .
Оценка результатов при выявлении антител IgM методом иммуноблота
| Отрицательный | Положительный | Неопределенный |
|---|---|---|
| Не выявлены АТ ни к одному из АГ. Выявлены АТ только к АГ p83-100 | Выявлены АТ к белку OspC. Выявлены АТ как минимум к двум АГ из группы: p41, VlsE, p17 | Выявлены АТ только к одному АГ из группы p41, VlsE, p17 в сочетании или без АТ к АГ р58, p39, BBK32 или выявлены АТ к любому количеству АГ р58, p39, BBK32 |
Оценка результатов при выявлении антител IgG методом иммуноблота
| Отрицательный | Положительный | Неопределенный |
|---|---|---|
| Не выявлены АТ ни к одному из АГ. Выявлены АТ только к АГ p17 | Выявлены АТ к белку VlsE. Выявлены АТ как минимум к двум АГ из группы: p83-100, p58, p41, p39, BBK32, OspC, p17 | Выявлены АТ только к одному АГ из группы: p83-100, p58, p41, p39, BBK32, OspC |
Комплекс антител, выявляемый на разных стадиях
| Стадия заболевания | АГ, к которым выявлены АТ IgM | АГ, к которым выявлены АТ IgG |
|---|---|---|
| Острая (I) | OspC, p41, p17, VlsE | P41, BBK32, p17, OspC, VlsE |
| Подострая (II) | OspC, p41, p17, BBK32, VlsE | p17, p41, VlsE, OspC, BBK32, p58 |
| Хроническая (III) | OspC, p41, VlsE, P39, p58 | p17, BBK32, p41, p58, VlsE, p83-100, OspC, p39 |
Определенные сложности использования для диагностики ИКБ методов выявления специфических иммуноглобулинов связаны с присутствием анамнестических АТ у большой части населения, проживающего на эндемичной территории, и низкой скоростью роста уровня АТ, что является особенностью боррелиозной инфекции. Очень медленные изменения уровня АТ к боррелиям (как повышение, так и снижение) также не позволяют использовать оценку уровня АТ для контроля эффективности терапии. Учитывая замедленное образование АТ при боррелиозах, при получении однократного отрицательного результата повторяют исследование в пробе крови, взятой через месяц.

В природных ландшафтах Черноморского побережья широко распространены кровососущие членистоногие, переносчики трансмиссивных инфекций вирусной и бактериальной этиологии. При эпизоотологических исследованиях в последние годы особое внимание уделяли отлову клещей, преимущественно I.ricinus, при исследовании которых выявили возбудителей туляремии, листериоза, клещевого боррелиоза, а так же возбудителей клещевого энцефалита (3,4).
Материалы и методы. Материалом для исследования служили суспензии клещей ( нимфы, имаго) голодных и напитавшихся, суспензии органов экспериментально зараженных белых мышей, сыворотки крови КРС и МРС. От больных поступали кровь, сыворотка, плазма крови, ЦСЖ с диагнозами: лихорадка неясной этиологии, КЭ, КМЭ, менингит, энцефалит, менингоэнцефалит, энцефаломиелит, миеломная болезнь, серозный менингит, энцефалопатия, лимфоцитома, ХАД, заболевания опорнодвигательной системы и другие.
Результаты и обсуждение. Анализ результатов клинико-эпидемиологического обследования позволил установить, что на территории Краснодарского края и Р.Адыгея встречаются разнообразные нозологические формы ИКБ и включают все основные, характерные для этой инфекции синдромы: общеинфекционный, поражения кожи, нервной, сердечно-сосудистой системы и опорно-двигательного аппарата (4,5).
Следует отметить, что курируемая территория не входит в перечень регионов по распространению КЭ. Однако данные, полученные в нашей лаборатории, позволяют говорить о расширяющемся ареале распространения иксодовых клещей, носителей ВКЭ, и, по-видимому, о расширении территории заболеваемости клещевым энцефалитом. Комплексное исследование полевого материала на зараженность возбудителями природноочаговых инфекций позволило установить, что в суспензии клещей обнаруживается ДНК боррелий методом ПЦР и в этих же пробах выявили антиген вируса КЭ. Таким образом, на территории края циркулируют возбудители ИКБ и КЭ, что может привести к развитию микст-инфекции у людей. Следует отметить, что еще в 1989 - 2000гг. антиген ВКЭ был обнаружен у диких млекопитающих в 24 случаях, у клещей - 37 пробах. Антитела к ВКЭ обнаружили в трех сыворотках с/х животных и в тридцати сыворотках людей. В 2004 году антитела к ВКЭ обнаружены в пяти сыворотках людей с диагнозом ЛНЭ (лихорадка неясной этиологии).
По данным различных авторов (2,7,8,10) частота возникновения микст-инфекций (МИ) ИКБ и КЭ в разных регионах страны колеблется в широких пределах - до 4,8 %.
Нами в 2004 году подтверждена МИ (ИКБ+ КЭ) у больного из Вологды, где произошел укус клеща, а так же в 2005 году у больной г.Краснодара. Следует отметить, что положительные результаты были получены в НРИФ, ПЦР, а ИФА результаты были отрицательные. Определение вирусной РНК в плазме крови больной и ЦСЖ и отрицательный результат ИФА вероятно указывает на серонегативную форму болезни КЭ. Положительные результаты на ИКБ получены у этой больной методом ПЦР и НРИФ. Антитела к боррелиям выявлены в титре
1: 320. В НРИФ при поиске антигена в ЦСЖ наблюдали специфическое свечение клеток боррелий как с положительной антиборрелиозной сывороткой, так и с гомологичной плазмой больной. Клиническое распознавание ИКБ и КЭ на первом этапе основывается на известных клинико-эпидемиологических данных. При КЭ в анамнезе также выявляется укус клещей или употребление сырого инфицированного молока коров или коз. А клинические исследования выявляют нейроинфекционный характер болезни. При МИ (ИКБ+ КЭ) прослеживаются три основных синдрома: общий инфекционный, менингеальный и очаговое поражение нервной системы.
Заключение. Опыт работы последних лет указывает на необходимость проведения исследований по клещевым инфекциям на территории края по совершенствованию эпизотолого - эпидемиологического надзора, оснащения лабораторий современными диагностическими тест-системами, совершенствования методов профилактики и проведения акарицидных обработок. Проведение этих мероприятий невозможно без поддержки централизованных и местных бюджетных средств. Очень актуальным является решение вопроса о комплексной серологической диагностике, позволяющей обнаруживать антитела и антигены к различным возбудителям клещевых инфекций, особенно МИ, и своевременном назначении сочетанной противовирусной терапии с антибиотиками в остром периоде болезни. В целях улучшения качества диагностической помощи, её унификации, совершенствования необходимо разработать и внедрять единую информационную систему слежения с помощью компьютерной обработки специальных тематических карт, заполняемых лечащими врачами на каждого больного (11).
С целью прогнозирования заболеваемости клещевыми инфекциями необходимо динамичное слежение за распространением клещей, их вирусофорностью, определения зон прокормителей клещей, территории риска. Следует проводить работу с населением через СМИ. Необходимо уделять особое внимание совершенствованию уровня подготовки врачей и средних медицинских работников по диагностике, лечению и реабилитации больных ИКБ, КЭ и других клещевых инфекций.
Читайте также:

