Антибиотик при ангине инфекционный мононуклеоз
Обновлено: 25.04.2024
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ).
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ). Практикующие врачи в своей повседневной практике чаще сталкиваются с клинически манифестными формами первичной Эпштейна–Барр-вирусной инфекции (ЭБВИ) в виде острой, как правило, не верифицированной респираторной инфекцией (более 40% случаев) или инфекционным мононуклеозом (около 18% всех заболеваний) [1, 2]. В большинстве случаев эти заболевания протекают доброкачественно и заканчиваются выздоровлением, но с пожизненной персистенцией ВЭБ в организме переболевшего [1, 3–5].
Однако в 10–25% случаев первичное инфицирование ВЭБ, протекающее бессимптомно, и острая ЭБВИ могут иметь неблагоприятные последствия [6–9] с формированием лимфопролиферативных и онкологических заболеваний, синдрома хронической усталости, ВЭБ-ассоциированного гемофагоцитарного синдрома и др. [7, 9, 11–14].
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Перед врачом, к которому обращается пациент с острой ЭБВИ, всегда встает вопрос: что предпринять в каждом конкретном случае, чтобы максимально снизить риск развития хронической ЭБВИ и ВЭБ-ассоциированных патологических состояний Этот вопрос не праздный, и ответить на него действительно очень трудно, т. к. до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся рекомендации часто противоречат друг другу.
По мнению многих исследователей, лечение ЭБВИ-мононуклеоза (ЭБВИМ) не требует назначения специфической терапии [15–17]. Лечение больных, как правило, проводится в амбулаторных условиях, изоляция пациента не требуется. Показаниями к госпитализации следует считать длительную лихорадку, выраженный синдром тонзиллита и/или синдром ангины, полилимфаденопатию, желтуху, анемию, обструкцию дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, гематологических, со стороны сердечно-сосудистой и дыхательной системы, синдром Рейе).
При легком и среднетяжелом течении ЭБВ ИМ больным целесообразно рекомендовать палатный или общий режим с возвращением к обычной деятельности на адекватном для каждого конкретного больного физическом и энергетическом уровне. Проведенное многоцентровое исследование показало, что необоснованно рекомендуемый строгий постельный режим удлиняет период выздоровления и сопровождается длительным астеническим синдромом, требующим нередко медикаментозного лечения [18].
При легком течении ЭБВ ИМ лечение больных ограничивается поддерживающей терапией, включающей адекватную гидратацию, полоскание ротоглотки раствором антисептиков (с добавлением 2% раствора лидокаина (ксилокаина) при выраженном дискомфорте в глотке), нестероидные противовоспалительные препараты, такие как парацетамол (Ацетаминофен, Тайленол). По мнению ряда авторов назначение блокаторов Н2 рецепторов, витаминов, гепатопротекторов и местная обработка миндалин различными антисептиками являются малоэффективными и необоснованными способами лечения [19, 20]. Из экзотических методов лечения следует упомянуть рекомендуемое Ф. Г. Боковым и соавт. (2006) применение мегадоз бифидобактерий при лечении больных острым мононуклеозом [21].
Мнения о целесообразности назначения антибактериальных препаратов при лечении ЭБВИМ весьма противоречивы. По мнению Gershburg E. (2005) тонзиллит при ИМ часто асептический и назначение антибактериальной терапии не оправдано. Также нет смысла в применении антибактериальных средств при катаральной ангине [4]. Показанием для назначения антибактериальных препаратов является присоединение вторичной бактериальной инфекции (развитие у больного лакунарной или некротической ангины, таких осложнений, как пневмония, плеврит и др.), о чем свидетельствуют сохраняющиеся более трех суток выраженные воспалительные изменения показателей крови и фебрильная лихорадка. Выбор препарата зависит от чувствительности микрофлоры на миндалинах больного к антибиотикам и возможных побочных реакций со стороны органов и систем.
По данным H. Fota-Markowcka et al. (2002) у больных чаще выделяют гемофильную палочку, стафилококк и пиогенный стрептококк, реже — грибы рода Candida [22], поэтому следует признать обоснованным назначение этим больным препаратов из группы цефалоспоринов 2–3 поколения, линкосамидов, макролидов и противогрибковых средств (флуконазол) в терапевтических дозах на 5–7 дней (реже — 10 дней) [4]. Некоторые авторы при наличии некротической ангины и гнилостном запахе изо рта, вызванных, вероятно, ассоциированной анаэробной флорой, рекомендуют использовать метронидазол по 0,75 г/сут, разделенных на 3 приема, в течение 7–10 дней.
Противопоказаны препараты из группы аминопенициллинов (ампициллин, амоксициллин (Флемоксин Солютаб, Хиконцил), амоксициллин с клавуланатом (Амоксиклав, Моксиклав, Аугментин)) из-за возможности развития аллергической реакции в виде экзантемы. Появление сыпи на аминопенициллины не является IgE-зависимой реакцией, поэтому применение блокаторов Н1 гистаминовых рецепторов не имеет ни профилактического, ни лечебного эффекта [19].
По мнению ряда авторов до настоящего времени сохраняется эмпирический подход к назначению глюкокортикостероидов больным с ЭБВИ [23]. Глюкокортикостероиды (преднизолон, преднизон (Делтазон, Метикортен, Оразон, Ликвид Пред), Солу Кортеф (гидрокортизон), дексаметазон) рекомендуются больным с тяжелым течением ЭБВИМ, с обструкцией дыхательных путей, неврологическими и гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [4, 24]. Суточная доза преднизолона составляет 60–80 мг в течение 3–5 дней (реже 7 дней) с последующей быстрой отменой препарата. Одинаковой точки зрения на назначение этим больным глюкокортикостероидов при развитии миокардита, перикардита и поражениях ЦНС нет.
При тяжелом течении ЭБВИМ показана внутривенная дезинтоксикационная терапия, при разрыве селезенки — хирургическое лечение.
Наиболее дискуссионным остается вопрос о назначении противовирусной терапии больным с ЭБВИ. В настоящее время известен большой перечень препаратов, являющихся ингибиторами ВЭБ репликации в культуре клеток [4, 25–27].
I. Подавляющие активность ДНК-полимеразы ВЭБ:
- ациклические аналоги нуклеозидов (ацикловир, ганцикловир, пенцикловир, валацикловир, валганцикловир, фамцикловир);
- ациклические аналоги нуклеотидов (цидофовир, адефовир);
- аналоги пирофосфатов (Фоскарнет (фоскавир), фосфоноацетиловая кислота);
- 4 оксо-дигидрохинолины (возможно).
II. Различные соединения, не ингибирующие вирусной ДНК-полимеразы (механизм изучается): марибавир, бета-L-5 урацил йододиоксолан, индолокарбазол.
Однако проведенный метаанализ пяти рандомизированных контролируемых испытаний с участием 339 больных ЭБВИМ, принимавших ацикловир (Зовиракс), показал неэффективность препарата [28, 29].
Одна из возможных причин кроется в цикле развития ВЭБ, в котором ДНК вируса имеет линейную либо циркулярную (эписома) структуру и размножается в ядре клетки хозяина. Активная репликация вируса происходит при продуктивной (литической) стадии инфекционного процесса (ДНК ВЭБ линейной формы). При острой ЭБВИ и активации хронической ЭБВИ происходит цитолитический цикл развития вируса, при котором он запускает экспрессию собственных ранних антигенов и активирует некоторые гены клеток макроорганизма, продукты которых участвуют в репликации ВЭБ. При латентной ЭБВИ ДНК вируса имеет вид эписомы (круговой суперспиральный геном), находящейся в ядре. Циркулярный геном ДНК ВЭБ характерен для CD21+ лимфоцитов, в которых даже при первичном инфицировании вирусом практически не наблюдается литической стадии инфекционного процесса, а ДНК воспроизводится в виде эписомы синхронно с клеточным делением инфицированных клеток. Гибель пораженных ВЭБ В лимфоцитов связана не с опосредованным вирусом цитолизом, а с действием цитотоксических лимфоцитов [4].
При назначении противовирусных препаратов при ЭБВИ врач должен помнить, что их клиническая эффективность зависит от правильной трактовки клинических проявлений болезни, стадии инфекционного процесса и цикла развития вируса на этой стадии. Однако не менее важным является и тот факт, что большинство симптомов ЭБВИ связаны не с прямым цитопатическим действием вируса в инфицированных тканях, а с опосредованным иммунопатологическим ответом ВЭБ-инфицированных В лимфоцитов, циркулирующих в крови и находящихся в клетках пораженных органов. Именно поэтому аналоги нуклеозидов (ацикловир, ганцикловир и др.) и ингибиторы полимеразы (Фоскарнет), подавляющие репликацию ВЭБ и уменьшающие содержание вируса в слюне (но не санирующие ее полностью [4], не оказывают клинического эффекта на тяжесть и продолжительность симптомов ЭБВИМ.
Показаниями для лечения ЭБВИМ противовирусными препаратами являются: тяжелое, осложненное течение болезни, необходимость профилактики ВЭБ-ассоциированной В-клеточной лимфопролиферации у иммунокомпрометированных пациентов, ВЭБ-ассоциированная лейкоплакия. Bannett N. J., Domachowske J. (2010) рекомендуют применять ацикловир (Зовиракс) внутрь в дозе 800 мг внутрь 5 раз в сутки в течение 10 дней (или 10 мг/кг каждые 8 часов в течение 7–10 дней). При поражениях нервной системы предпочтителен внутривенный способ введения препарата в дозе 30 мг/кг/сут 3 раза в сутки в течение 7–10 дней.
По мнению E. Gershburg, J. S. Pagano (2005), если под действием каких-либо факторов (например, иммуномодуляторов, при ВЭБ-ассоциированных злокачественных опухолях — применение лучевой терапии, гемцитабина, доксорубицина, аргинина бутирата и др.) удается перевести ДНК ВЭБ из эписомы в активную репликативную форму, т. е. активировать литический цикл вируса, то в этом случае можно ожидать клинический эффект от противовирусной терапии.
В комплексной терапии рекомендуется внутривенное введение иммуноглобулинов (Гаммар-П, Полигам, Сандоглобулин, Альфаглобин и др.) 400 мг/кг/сут, № 4–5.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные альфа-интерфероны (Интрон А, Роферон-А, Реаферон-ЕС) по 1 млн ME в/м в течение 5–7 дней или через день; при хронической активной ЭБВИ — 3 млн ME в/м 3 раза в неделю, курс 12–36 недель.
Медикаментозная коррекция астенического синдрома при хронической ЭБВИ включает назначение адаптогенов, высоких доз витаминов группы В, ноотропных препаратов, антидепрессантов, психостимуляторов, препаратов с прохолинергическим механизмом действия и корректоров клеточного метаболизма [30–32].
Залогом успешного лечения больного с ЭБВИ являются комплексная терапия и строго индивидуальная тактика ведения как в стационаре, так и во время диспансерного наблюдения.
Литература
И. В. Шестакова, доктор медицинских наук, доцент
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
МГМСУ, Москва

Выбор антибактериального препарата при гнойных осложнениях инфекционного мононуклеоза у детей в амбулаторных условиях ограничен необходимостью перорального способа введения. Проведенное клиническое наблюдение показало, что антибактериальная терапия препаратом Сумамед® сопоставима по эффективности с цефалексином, но имеет более высокий профиль безопасности. Широкий спектр антимикробного действия препарата Сумамед®, наименьшая кратность введения и длительность курса могут повышать приверженность пациентов к антибактериальной терапии.
Несмотря на то что в основе патогенеза инфекционного мононуклеоза лежит поражение лимфоидной ткани, немаловажную роль в течении заболевания играет вторичная инфекция. Повреждение и десквамация эпителиальных клеток нёбных и носоглоточной миндалин при проникновении вируса Эпштейна -- Барр создают благоприятные условия для реактивации эндогенной бактериальной и грибковой флоры и развития осложнений (тонзиллит, аденоидит, риносинусит).
Воспалительный процесс нёбных миндалин вначале имеет катаральный или фолликулярный характер. С 3--4-го дня заболевания в лакунах появляется воспалительный экссудат (лакунарный тонзиллит). Очень часто при инфекционном мононуклеозе у детей на нёбных миндалинах появляются различной величины и характера налеты, которые могут иметь частично фибринозный характер. Острый тонзиллит характеризуется длительным течением (до 7--14 дней) [1, 2].
В проведенном в Санкт-Петербурге (2010 г.) исследовании было показано, что гнойный процесс на миндалинах при инфекционном мононуклеозе у госпитализированных детей, как правило, обусловлен наслоением транзиторной (патогенной) микрофлоры: пиогенных стрептококков (23%), синегнойной палочки (15%), золотистого стафилококка (13%), реже высеваются клебсиелла (6%) и пневмококк (5%). В то же время достаточно часто в роли этиологического фактора выступают условно-патогенные микроорганизмы -- дрожжеподобные грибы (18%) и гемофильная палочка (17%), количество которых возрастает до патогенных значений в результате дисбиотических изменений на фоне Эпштейна -- Барр вирусной инфекции. В 10% случаев причиной острого тонзиллита при инфекционном мононуклеозе являются бактериальные и бактериально-грибковые ассоциации [2].
Уже в ранние сроки инфекционного мононуклеоза отечная и инфильтрированная носоглоточная миндалина создает препятствие в просвете хоан, что приводит к затруднению прохождения воздушной струи через носовые ходы. Снижение воздушного потока и нарушение мукоцилиарного транспорта при аденоидите способствует застою секрета в задних отделах полости носа. В этих условиях значительно возрастает вероятность развития острого гнойного риносинусита [3].
Антибактериальная терапия не влияет на течение Эпштейна -- Барр вирусной инфекции и показана только при наличии гнойных осложнений. В амбулаторных условиях выбор препарата в большинстве случаев проводится эмпирически с учетом сведений о ведущих патогенах, их чувствительности к антибиотикам, способности лекарственного средства создавать адекватные концентрации в очаге инфекции. Кроме того, в большинстве случаев для лечения на дому используются пероральные антибиотики.
В качестве стандарта лечения инфекций верхних дыхательных путей у амбулаторных детей рекомендуются аминопенициллины, высоко эффективные в отношении основных возбудителей -- Streptococcus pyogenes, Streptococcus рneumoniae, Haemophilus influenzae, Moraxella сatarrhalis (включая штаммы, продуцирующие b-лактамазы) [4, 5]. В то же время при инфекционном мононуклеозе они могут инициировать развитие иммунокомплексного васкулита [6]. Так называемая ампициллиновая сыпь, описанная в литературе еще в 1960-х гг., возникает у 75--100% больных обычно через 5--10 дней от начала терапии ампициллином. При этом состояние ребенка может значительно ухудшаться, что требует госпитализации, а в ряде случаев назначения глюкокортикоидных гормонов [2, 7, 8].
Согласно данным Chovel-Sella А. et al. (2013), на фоне применения амоксициллина, полученного путем химической модификации 6-аминопенициллиновой кислоты на основе структуры ампициллина, у детей с инфекционным мононуклеозом экзантема наблюдается значительно реже (29,5% случаев) [9]. Однако в инструкции к препарату инфекционный мононуклеоз указан как противопоказание [10]. Поэтому в домашних условиях при осложненной Эпштейна -- Барр вирусной инфекции средством выбора являются антибиотики из группы макролидов или цефалоспоринов.
В последние годы вновь возросло внимание педиатров к макролидным антибиотикам. В литературе появились новые данные о роли атипичной патогенной микрофлоры (микоплазмы, хламидии) и золотистого стафилококка в инфекционной патологии лимфоглоточного кольца у детей, в отношении которых активны макролиды [11, 12]. Кроме того, появились сведения о наличии противовоспалительного и иммуномодулирующего эффекта макролидов, их способности разрушать структуру биопленок [13].
В отличие от других представителей группы, азитромицин при приеме внутрь характеризуется хорошей биодоступностью (38%) и способностью к созданию высоких длительно сохраняющихся концентраций в тканях (особенно нёбных и носоглоточной миндалин). Препарат в существенно большем количестве накапливается внутриклеточно, благодаря чему его концентрации во многих тканях организма намного превышают МПК для большинства бактериальных патогенов и обеспечивают бактерицидный эффект в отношении внутриклеточных возбудителей [14]. Кроме того, среди всех макролидов азитромицин проявляет максимальную активность в отношении Haemophilus influenzae, включая штаммы, продуцирующие b-лактамазы [15]. С помощью фагоцитов препарат в большом количестве транспортируется в очаг воспаления, где происходит постепенное его высвобождение. Эффективная концентрация азитромицина в тканях сохраняется в течение 5--7 дней после последнего приема, что дает основание применять его при большинстве инфекций дыхательных путей и ЛОР-органов у детей один раз в сутки в виде коротких курсов (3--5 дней) в суммарной дозе от 30 до 60 мг/кг [16].
Поскольку все данные об эффективности и безопасности азитромицина получены при исследовании оригинального препарата, именно он использовался в клиническом наблюдении по сравнению с различными видами антибактериальной терапии бактериальных осложнений при инфекционном мононуклеозе у детей.
Цель исследования -- изучить современные особенности микробного пейзажа слизистой оболочки зева и сравнить эффективность азитромицина и цефалексина при лечении детей с острым инфекционным мононуклеозом в амбулаторных условиях.
ПАЦИЕНТЫ И МЕТОДЫ
К критериям исключения относились: развитие осложнений, непереносимость препарата, отказ пациента или родителей от дальнейшего участия в наблюдении, развитие нежелательных явлений.
Все пациенты получали стандартную терапию, которая включала препараты человеческого рекомбинантного интерферона-альфа-2b, антибактериальные средства, промывание слизистых зева и полости носа физиологическим раствором поваренной соли или морской воды, топические деконгестанты. По показаниям назначались жаропонижающие (парацетамол, ибупрофен), гепатопротекторы растительного происхождения.
Методом случайной выборки были сформированы 2 группы наблюдения. Пациенты 1-й группы (42 человека) в качестве антибактериального препарата получали препарат Сумамед® в зависимости от возраста виде суспензии (10 мг/кг массы тела в сутки 3 дня или 10 мг/кг массы тела в первый день и 5 мг/кг массы тела в последующие 4 дня) или капсул (500 мг) однократно в течение 3 дней или 500 мг в первый день и 250 мг в последующие 4 дня. Пациентам 2-й группы (23 человека) назначался цефалексин в суточной дозе 25--50 мг/кг массы тела в сутки, разделенной на 3 приема. Длительность антибактериальной терапии составила 7 дней.
Обе группы сформированы однородно по возрасту (средний возраст -- 6,4 ± 4,68 лет и 6,7 ± 4,52 лет в 1-й и 2-й группах соответственно), полу (20 мальчиков и 23 девочки в 1-й группе и 11 мальчиков и 12 девочек во 2-й группе) и начальным клиническим проявлениям, что допускает проведение сравнительной оценки результатов наблюдения и определения достоверности результатов. Размер выборки был достаточным для формирования выводов.
Осмотр проводился ежедневно до окончания курса антибактериальной терапии и включал: сбор и анализ анамнеза болезни, субъективную оценку пациентом выраженности симптомов (симптомы интоксикации, боль в горле), объективную оценку врачом наличия и выраженности симптомов (фарингоскопия, характер выделений из носовых ходов). Выраженность симптомов оценивали по 4-балльной шкале, где: 0 -- отсутствие симптома, 1 -- слабая выраженность симптома, 2 -- умеренная выраженность симптома, 3 -- сильная выраженность симптома. Все результаты фиксировали в индивидуальной регистрационной карте (ИРК).
Эффективность терапии определяли по срокам уменьшения выраженности и полного исчезновения изучаемых клинических проявлений, наличия и тяжести осложнений инфекционного мононуклеоза. Критериями оценки эффективности являлись: выздоровление -- полное исчезновение симптомов заболевания, улучшение -- значительное уменьшение выраженности клинических симптомов заболевания, отсутствие эффекта -- отсутствие положительной динамики, прогрессирование симптомов заболевания.
На протяжении всего наблюдения проводился мониторинг нежелательных явлений, при возникновении которых применение препаратов могло быть прекращено.
Статистическая обработка результатов проведена на персональном компьютере с помощью программы Microsoft Excel 2010. Для параметрических переменных определяли среднее значение показателя по группе пациентов (М), стандартного отклонения (s). Различие средних величин считалось достоверным при уровне значимости p < 0,05, соответствующим достоверной вероятности 0,95 и более.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При первичном осмотре частота и выраженность начальных клинических проявлений инфекционного мононуклеоза статистически не различалась в обеих группах (табл. 1). Так, выраженность боли в горле на момент обращения пациенты обеих групп оценивали в среднем на 3,8 ± 0,78 балла и 3,9 ± 0,86 балла соответственно, затруднение носового дыхания -- на 4,1 ± 0,96 балла и 4,2 ± 0,85 балла соответственно. Аналогичные результаты были получены при фарингоскопии: выраженность гиперемии составила в среднем 4,9 ± 0,30 балла и 4,8 ± 0,46 балла, а небные миндалины были увеличены до 2,4 ± 0,40 степени и 2,3 ± 0,53 степени соответственно (р > 0,05). Гнойный выпот в лакунах с одинаковой частотой наблюдался в обеих группах (80,9 и 86,6% соответственно), в остальных случаях -- фибринозные наложения на поверхности миндалин. Таким образом, на момент обращения группы были сопоставимы не только по основным демографическим, но и по клиническим признакам.
Анализ динамики клинических проявлений показал, что продолжительность основных симптомов инфекционного мононуклеоза и фарингоскопических признаков воспалительного процесса в зеве достоверно не зависели от применяемого антибактериального препарата (табл. 2).
Среди наблюдаемых нами детей с инфекционным мононуклеозом, получавших системные антибиотики с широким спектром антимикробного действия, ни в одном случае не отмечалось бактериальной суперинфекции со стороны слизистых оболочек носовых ходов и придаточных пазух.
Анализ результатов бактериологического исследования отделяемого со слизистой оболочки нёбных миндалин и задней стенки глотки до начала антибактериальной терапии показал, что в настоящее время произошли изменения этиологической структуры острых гнойных тонзиллитов, осложняющих течение Эпштейна -- Барр вирусной инфекции. На современном этапе наиболее частым возбудителем являлся Staphylococcus aureus (32%), который высевался в патогенных значениях (105--108 КОЕ/мл), реже выявлялся Streptococcus pneumoniae (18%), тогда как Streptococcus рyogenes (4%) и Haemophylus influenzae (3%) не относились к причинно-значимым патогенам (рис. 1). Высокая частота выявления дрожжеподобных грибов (18%), возможно, обусловлена иммуносупрессивным действием вируса Эпштейна -- Барр.

При повторном обследовании, проведенном через 10 дней от начала антибиотикотерапии, у всех пациентов наблюдалась полная санация слизистых зева от патогенных возбудителей, у 20% обследованных детей обнаружена условно-патогенная флора: Streptococcus viridans, Staphylococcus еpidermidis, непатогенные нейссерии и Staphylococcus аureus, степень обсемененности которым снизилась до условно-патогенных значений (102--103 КОЕ/мл).
Мониторинг нежелательных явлений показал, что на фоне терапии цефалексином у 2 детей (8,7%) отмечался кашицеобразный стул, у 1 ребенка (4,3%) на 7-й день от начала лечения появилась необильная пятнисто-папуллезная сыпь, которая быстро купировалась после приема антигистаминных средств. В то же время в группе детей, получавших препарат Сумамед®, нежелательных явлений не выявлено.
Хорошая переносимость в совокупности с выраженным клиническим эффектом и удобством применения (один раз в сутки, короткий курс) объясняют высокую комплаентность препарата Сумамед®.
Таким образом, проведенное клиническое наблюдение показало, что в настоящее время произошли изменения в этиологической структуре гнойных тонзиллитов, осложняющих течение Эпштейна -- Барр вирусной инфекции: доминирующими патогенами являются золотистый стафилококк и пневмококк, тогда как пиогенные стрептококки и гемофильная палочка не являются значимыми причинами бактериальных процессов в зеве у детей с инфекционным мононуклеозом.
Продолжительность основных симптомов инфекционного мононуклеоза и фарингоскопических признаков воспалительного процесса в зеве достоверно не отличаются при терапии азитромицином (Сумамед®) и цефалексином. Поэтому при прочих равных условиях для лечения в амбулаторных условиях рационально использовать Сумамед®, который, в отличие от цефалоспоринов, не только имеет меньшую кратность и длительность применения, но и активен в отношении внутриклеточных возбудителей (микоплазм и хламидий).
Полученные результаты позволяют рекомендовать препарат Сумамед® для лечения бактериальных осложнений при инфекционном мононуклеозе у детей. Применение препарата с широким спектром действия и высоким профилем безопасности позволяет повысить приверженность пациентов к терапии в амбулаторных условиях.

Пациентка жаловалась на боль в горле, заложенность носа, сильную потливость, слабость, тяжесть в правом подреберье, высокую температуру, сыпь на груди, увеличенные лимфоузлы на шее.
Анамнез
Пациентка заболела 4 дня назад, когда отметила днём резкий подъём температуры до 39 °C, затем присоединилась слабость, головная боль, небольшое першение в горле. Девушка расценила состояние как начало обычного ОРВИ. Стала принимать ибупрофен, температура снижалась на пару часов и повышалась снова.
На следующий день боль в горле усилилась появились налёты, температура была 38,5 °C. Пациентка вызвала врача на дом. После осмотра поставлен диагноз "лакунарная ангина", взят мазок на BL (возбудителя дифтерии). Назначено лечение:
- полоскание зева раствором фурацилина; ; ;
- ибупрофен.
На фоне данного лечения состояние не улучшалось, нарастали симптомы интоксикации, на приёме терапевт направил пациентку на общий анализ крови с пометкой "cito" (т. е. срочно) и на приём к инфекционисту.
Девушка учится на 3 курсе Рязанского государственного радиотехнического университета, вредные привычки отрицает, живёт в нормальных условиях с родителями и младшей сестрой.
Обследование
При физикальном осмотре: кожные покровы влажные, с мелкоточечной сыпью на груди. По ходу грудино-ключично-сосцевидной мышцы пальпируются два увеличенных лимфоузла диаметром 4 х 4 см, лимфоузлы мягкие, неспаянные с кожей, болезненные. При осмотре зева: миндалины отёчные, гиперемированные, рыхлые, увеличены, виден белый налёт в лакунах.
Дыхание в лёгких везикулярное (хрипов нет), частота дыхательных движений 22 в минуту. Тоны сердца ясные, ритм правильный, частота сердечных сокращений 96 ударов в минуту, артериальное давление 110/70 мм рт. ст. Живот мягкий, безболезненный. Печень + 2 см из под края рёберной дуги, край мягкий эластичный. Стул и диурез (объём мочи) в норме.
В анализе крови моноцитоз (увеличение числа моноцитов в крови) и лимфоцитоз (увеличение числа лимфоцитов в крови):
- лейкоциты — 18,9 x 10^9/л;
- СОЭ — 30 мм/ч;
- эритроциты — 3,9 х 10^12/л;
- гемоглобин — 128 г/л.
Инфекционистом пациентка была направлена на анализы: биохимический анализ крови (АЛТ, АСТ, билирубин общий, прямой, непрямой, глюкоза, холестерин, щелочная фосфатаза), ВИЧ, RW (сифилис), гепатиты В и С, антитела к вирусу Эпштейна — Барр (ВЭБ).
- гепатиты В и С, ВИЧ, RW — отрицательно;
- обнаружены антитела IgM (иммуноглобулин М) к вирусу Эпштейна — Барр.
- АЛТ — 425 ЕД/л;
- АСТ — 308 ЕД/л;
- билирубин общий — 26 мкмоль/л;
- непрямой — 6 мкмоль/л;
- прямой — 20 мкмоль/л;
- щелочная фосфатаза — 280 Ед/л;
- глюкоза — 5,4 ммоль/л;
- холестерин 4,2 — ммоль/л.
Диагноз
Лечение
- Полупостельный режим.
- Обильное питьё.
- Диета № 5 (рекомендована для людей с заболеваниями печени и желчного пузыря). — по 2 таблетке 3 раза в день в течение 10 дней. 500 мг — по 1 таблетке 2 раза в день в течение 10 дней 400 мг — по 1 таблетке 2 раза в день в течение 10 дней. — по 1 таблетке 4 раза в день рассасывать.
- Ибупрофен 400 мг — при температуре выше 38,5 °C.
- Полоскание зева раствором фурацилина.
На фоне лечения улучшилось общее самочувствие, нормализовалась температура тела, исчезли воспалительные изменения в горле, уменьшились лимфоузлы. Общий анализ крови практически нормализовался, оставались повышены моноциты, биохимический анализ крови нормализовался в течение двух месяцев.
Лечение длилось 21 день, закончилось выздоровлением. Далее пациентка в течение года находилась на диспансерном наблюдении.
Заключение
Данный клинический случай показывает типичное течение инфекционного мононуклеоза, вызванного ВЭБ. Этим заболеванием часто болеют молодые люди — студенты, которые постоянно контактируют с большим количеством людей, часто испытывают стресс и не имеют строгого режима дня и питания.
Что такое ангина? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
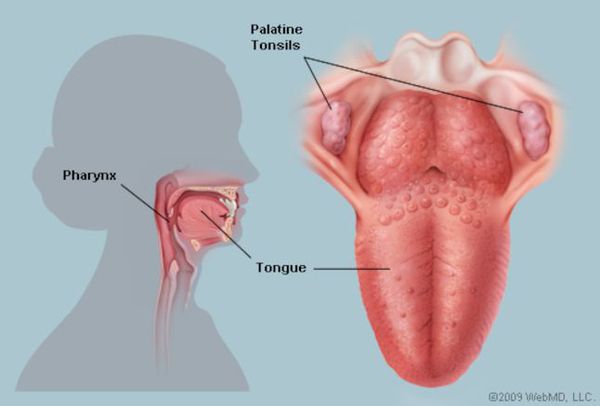
Этиология (причина ангины)
Впервые стрептококк был обнаружен т. Бильротом в 1874 году.
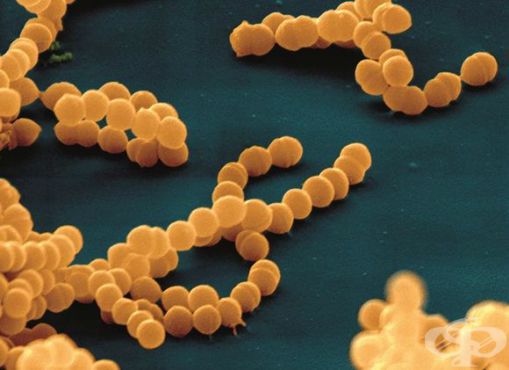
Стрептококки являются неподвижными грамположительными бактериями. Они располагаются парами, цепочками. Их таксономическое деление основано на различиях строения А-липополисахарида (обеспечивает сродство к соединительной ткани).
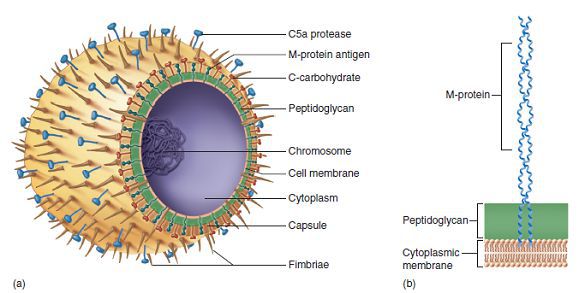
Строение стрептококка:
- Протеины клеточной стенки:
- М — подавляет фагоцитоз, имеет сродство к соединительной ткани сердца;
- Т — фактор типоспецифичности;
- R — нуклеопротеид;
- Протеиназа — вызывает набухание соединительной ткани сердца;
- Стрептокиназа — участвует в переводе плазмина в плазминоген, т. е. вызывает фибринолиз
- Липотейхоевая кислота — обладает сродством к эпителию лимфоидного аппарата глотки, обеспечивает фиксацию стрептококка, т. е. является рецептором;
- Гиалуроновая кислота — входит в состав капсулы, препятствует фагоцитозу возбудителя и расщепляет гликозаминогликаны;
- Стрептолизины:
- S (гемолиз эритроцитов, иммуносупрессия);
- О (кардиотоксичен — воздействует на митохондрии, блокирует тканевое дыхание в сердечной мышце и нарушает проведение сердечных импульсов);
- Эритрогенный экзотоксин — т. н. токсин Дика, вызывающий типичные проявления скарлатины, а в совокупности с другими факторами патогенности поражает капилляры, вызывая точечную сыпь. Первичная инфекция, как правило, протекает по типу скарлатины, а все повторные заражения — по типу ангины, так как к токсину Дика вырабатывается иммунитет. Однако следует помнить, что проявления жизни на Земле весьма обширны и многообразны, и не всегда подчиняются правилам — иногда скарлатина не проявляется, например, при субклинической форме, когда первичное заболевание протекает скрыто, а иммунитет к токсину формируется, или конкретный штамм стрептококка является нетоксигенным, т. е. не вырабатывает токсин, и первая встреча с возбудителем будет типичной ангиной. Также возможна повторная скарлатина, вызванная различными антигенными вариантами стрептококка).
При реакции организма на разные типы стрептококков выделяют однородный иммунитет (стойкий полииммунитет), который защищает от заражения, а также моноиммунитет (обусловленный бактериальными типоспецифичными М-антигенами), который не предохраняет от заболевания другими типами.
Возбудитель чувствителен к высыханию, погибает при нагревании до 60°C за 30 минут, высокочувствителен к антибиотикам пенициллинового и цефалоспоринового рядов. Стрептококки размножаются на кровяном агаре (вызывают гемолиз эритроцитов), могут расти в молочных продуктах, мясном фарше и салатах. [2] [3] [4]
Эпидемиология
Антропоноз. Источник инфекции — больные ангиной, скарлатиной и другими формами стрептококковой инфекции (бета-гемолитический стрептококк группы А) и носители стрептококка.
Механизм передачи: аэрозольный (путь передачи воздушно-капельный), возможен алиментарный (связанный с неполноценным питанием) и контактный пути передачи, особенно у детей раннего возраста.
Восприимчивость к инфекции высокая, сезонность осенне-зимняя. Значительную роль в распространении заболевания имеет повышенная скученность населения. [1] [3] [5]
Факторы риска
Чаще всего ангиной заболевают:
- дети от 5 до 15 лет;
- родители ребёнка школьного возраста;
- взрослые, часто контактирующие с детьми.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы ангины
Инкубационный период — до 2-х суток. Начало острое.
- общей инфекционной интоксикации;
- тонзиллита (острый, гнойный);
- углочелюстного лимфаденита.
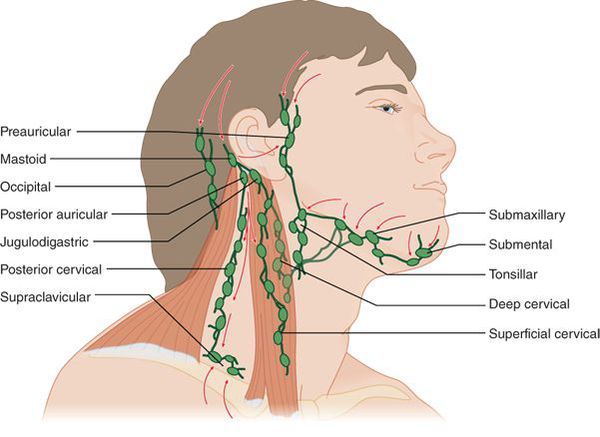
Повышение температуры, озноб и общая утомляемость
Головные боли и ломота в мышцах
При ангине появляется головная боль (тупая, без чёткой локализации) и выраженная ломота в мышцах и суставах.
Боли в горле
В первые сутки заболевания боли в горле проявляются при глотании, затем переходят в постоянное проявление и могут отдавать в ухо.
Увеличение и болезненность лимфатических узлов
Увеличиваются углочелюстные лимфоузлы, становятся очень болезненными, плотноэластической консистенции, не спаяны между собой и окружающими тканями.
Очень характерными являются данные, получаемые при фарингоскопии:
- открывание рта свободное;
- нёбные дужки, язычок, миндалины и мягкое нёбо в первые дни ярко гиперемированы.
Основные проявления тонзиллитов
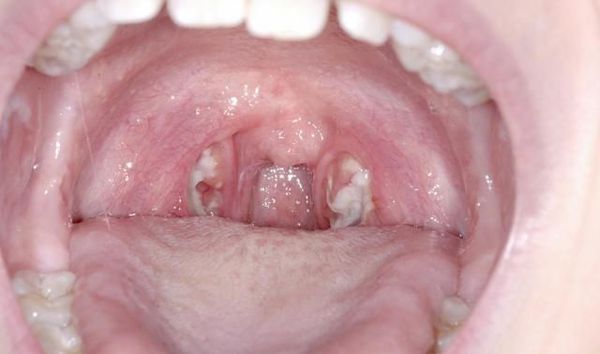
С третьего дня в лакунах появляется отделяемое жёлто-белого цвета (гной) — фолликулярно-лакунарный тонзиллит.
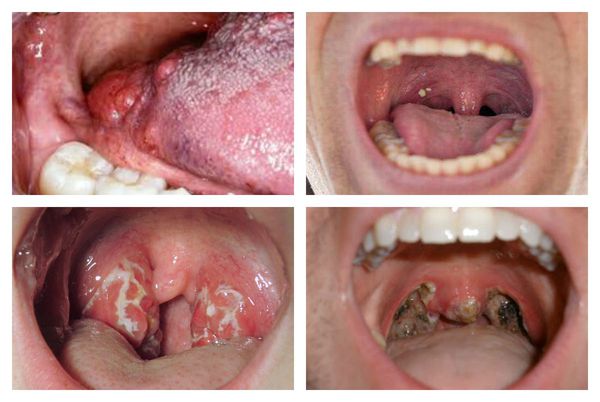
Как выглядит горло при ангине:
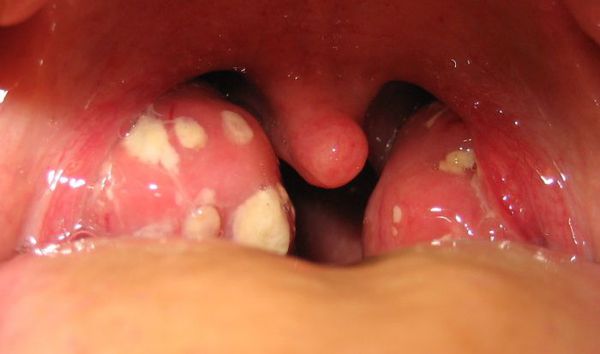
Далее при тяжёлых формах возникает некротический тонзиллит: тёмно-серый цвет миндалин, после отторжения гнойно-некротических масс остаются дефекты ткани.
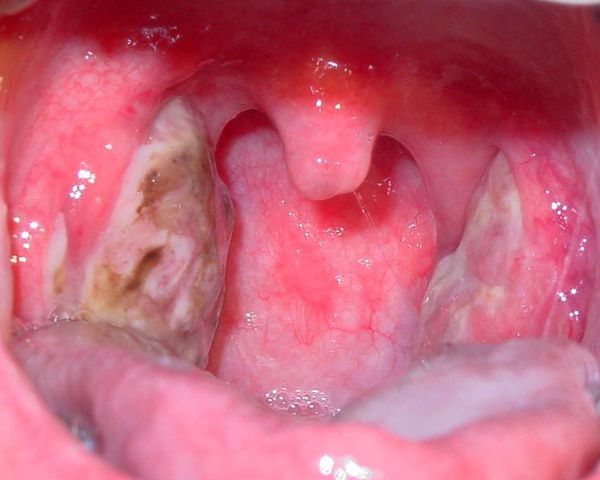
Необходимо помнить, что гнойный налёт при ангине не распространяется за пределы миндалин, легко снимается, не тонет в воде — появление каких-либо других вариантов течения является поводом для сомнения в диагнозе. [2] [3] [5] [6]
Флегмонозный тонзиллит
Флегмонозный тонзиллит — наиболее тяжёлая форма ангины. Характеризуется развитием в ткани миндалин чаще одностороннего гнойного очага без чётких границ. Резко усиливается интоксикация, возникает выраженная болезненность на стороне поражения и отёк, становится сложно открыть рот. Заболевание требует срочного хирургического лечения.
Язвенно-плёнчатая форма тонзиллита
При язвенно-плёнчатой форме ангины возникают изъязвления на поверхности ткани миндалин, сильная болезненность и налёт, который легко снимается шпателем.
Как протекает вирусная и герпесная ангина
"Вирусные ангины" не имеют ничего общего с классической стрептококковой ангиной. Они являются лишь отдельными синдромами при вирусных заболеваниях: аденовирусной, цитомегаловирусной и энтеровирусной (герпангина) инфекции и множестве других. Термин "ангина" применим только к заболеваниям, вызванным бета-гемолитическим стрептококком группы А. Все остальные воспаления ткани миндалины следует называть острым или хроническим тонзиллитом.
По этой причине выделять герпетическую ангину, ангину при дифтерии, гриппе, скарлатине и инфекционном мононуклеозе некорректно.
Как протекает ангина у детей
У детей симптомы ангины более выражены, чем у взрослых. Сильнее интоксикация, ребёнок вялый, отказывается от еды, возможны боли в животе, сильные головные боли, тошнота и рвота.
При каких симптомах ангины стоит бить тревогу
Когда обратиться к врачу:
- при подъёме температуры свыше 37,5 °C;
- сильной и мучительной боли в горле;
- выраженной интоксикации;
- болезненности углочелюстных лимфатических узлов.
Патогенез ангины
Ворота инфекции — лимфоидные образования кольца Пирогова — Лангханса. Происходит проникновение в них стрептококков, воспалительная реакция и дальнейшее распространение возбудителя, его токсинов и продуктов распада бактерий и клеток организма по лимфатическим путям в углочелюстные лимфоузлы (углочелюстной лимфаденит).
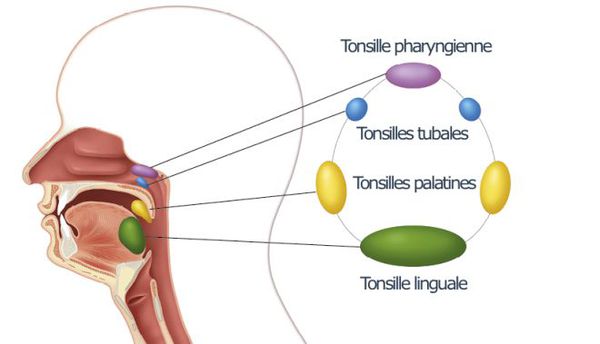
При благоприятном течении этим процесс ограничивается. При барьерной недостаточности стрептококки проникают в околоминдаликовую клетчатку (паратонзиллит, паратонзиллярный абсцесс), вызывают токсическое поражение всего организма. При проходе через слуховую трубу в среднее ухо возбудитель способен вызвать развитие отита и синусита. Достаточно редко при выраженном иммунодефиците развивается сепсис.
В ответ на проникновение бактериальных антигенов в организме больного образуются антитела, которые при взаимодействии с антигенами образуют циркулирующие иммунные комплексы антиген-антитело (АГ-АТ). В норме они разрушаются путём фагоцитоза, комплементом и не вызывают иммунопатологических реакций. Однако бывают ситуации, когда механизмы элиминации не срабатывают.
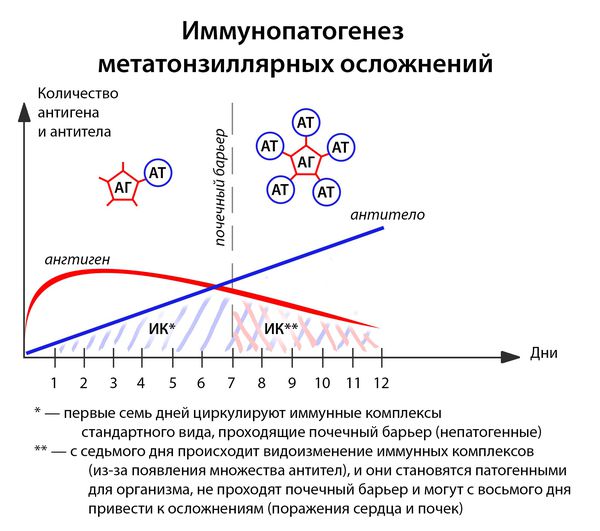
Иммунные комплексы оседают на базальной мембране сосудов (почек) и разрушают её. Далее происходит разрушение подлежащей соединительной ткани. Условиями для этого являются:
- большое количество образующихся иммунных комплексов (при сильном иммунитете, например, у подростков до 17 лет);
- массивная антигенемия (при несвоевременном лечении, высокой вирулентности возбудителя);
- частые повторные заболевания (2 года после перенесенной ангины — это период повышенного риска).
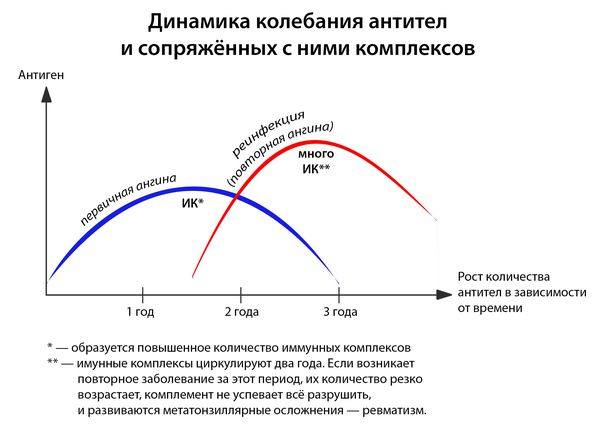
Иммунитет развивается с третьего дня: макрофаги подготавливают антигены, образуется суперантиген, и лишь затем передают его Т- и В-лимфоцитам, вырабатывающим специфические антитела. [1] [3] [4]
Классификация и стадии развития ангины
По степени тяжести ангина бывает:
- лёгкой;
- среднетяжёлой;
- тяжёлой.
По клинической форме:
- первичная — возникшая впервые или не раньше двух лет после ангины, перенесённой ранее);
- повторная — результат реинфицирования людей с повышенной восприимчивостью в течении двух лет от первичной ангины.
По характеру воспаления миндалин:
- катаральная ангина — покраснение и отёк миндалин;
- фолликулярная ангина — фолликулы белого цвета в ткани миндалин;
- лакунарная ангина — гнойное отделяемое из лакун миндалин;
- некротическая ангина — некроз ткани миндалин;
- гнойно-некротическая ангина — некроз и гнойное расплавление ткани миндалин.
- ангина язычной миндалины;
- ангина гортанных валиков;
- ангина нёбных миндалин;
- комбинированная ангина. [3][4]
Осложнения ангины
Осложнения ангины включают пара и метатонзиллярные процессы.
В острый период могут возникнуть:
- паратонзиллит, паратонзиллярный абсцесс (усиление лихорадки, односторонний характер болей, гиперсаливация, болезненность при открывании рта, асимметрия язычка, односторонний отёк, выраженная гиперемия мягкого нёба);
- инфекционно-токсический миокардит (боли в сердце, перебои в его работе, изменение размеров сердца, появление шумов, одышка, повышение ЛДГ на 1-2 нормы); (воспаление придаточных пазух носа);
- медиастенит (воспаление органов средостения — появление боли за грудиной, одышка);
- заглоточный абсцесс (нагноение лимфатических узлов и клетчатки заглоточного пространства — затруднение глотания, одышка, усиление инотоксикации);
- сепсис (полиорганное заражение, циркуляция возбудителя в крови).
В период выздоровления:
Диагностика ангины
Подготовка к посещению врача
При повышении температуры свыше 37,5 °С, сильной и мучительной боли в горле, болезненности углочелюстных лимфатических узлов и выраженной интоксикации нужно как можно скорее посетить терапевта. Специальная подготовка для этого не требуется.
Лабораторная диагностика
К методам лабораторной диагностики относятся:
- клинический анализ крови (нейтрофильный лейкоцитоз со сдвигом влево, повышение СОЭ);
- общий анализ мочи (мочевой синдром при осложнениях);
- ЭКГ (выполняется в день поступления и при выписке, могут быть признаки гипоксии, нарушения проводимости);
- бактериальный посев с миндалин (мазок) на бета-гемолитический стрептококк (и дифтерию);
- биохимия крови (АСЛО, РФ, СРБ). [3][4]
Дифференциальная диагностика
Боли в горле и повышение температуры тела являются достаточно частыми симптомами множества заболеваний, поэтому вопросы отличия ангины от других патологий являются основополагающими в практике любого врача:
Как отличить ангину от ОРЗ или фарингита
При остром респираторном заболевании поражается не паренхима миндалин, а в основном слизистая оболочка ротоглотки и других отделов респираторного тракта, отсутствует углочелюстной лимфаденит. При фарингите затрагиваются поверхностные слои гортани (слизистая оболочка).
Лечение ангины
Как долго лечится ангина
Режим и диета. Рекомендации и противопоказания для заболевших
Лечение осуществляется в домашних условиях, тяжёлые и осложнённые формы ангины лечатся в стационаре.
Режим палатный, диета — общий стол, при выраженном болевом синдроме показана механически и химически щадящая пища, обильное питьё.
Народные методы терапии. Лечение ангины народными способами и средствами недоказательной медицины недопустимо — это опасно для жизни и здоровья.
Антибиотики — лекарства для лечения ангины
Несмотря на длительное и широкое применение антибактериальных препаратов первого поколения бета-гемолитический стрептококк остаётся высокочувствителен к пенициллиновой и аминопенициллиновой группе антибиотиков, которые и являются препаратами первого выбора терапии — к концу вторых суток применения антибиотиков возбудитель уже погибает. При невозможности использования препаратов данных групп возможна замена на цефалоспориновый или макролидный ряд антибиотиков.
Уход на дому
При лечении ангины на дому первые три дня показано активное ежедневное наблюдение врача в целях своевременного выявления развития осложнений и исключения дифтерии зева.
В качестве патогенетической и симптоматической терапии широко используется:
- антисептические растворы — орошение ротоглотки и миндалин;
- полоскания горла;
- антигистаминные препараты;
- общеукрепляющие средства для повышения иммунитета;
- дезинтоксикационная парентеральная инфузионная терапия — при выраженном синдроме общей инфекционной интоксикации.
Основа лечения ангины — это высокоэффективная антибактериальная терапия. Поэтому применение трав, снимающих боль в горле, и ингаляций при болезни являются лишь вспомогательными. Противогрибковые препараты и компрессы при патологии не используются.
Выписка больных
Выписка пациентов осуществляется не ранее семи дней нормализации температуры тела при условии нормальных анализов крови, мочи и ЭКГ. [2] [3] [6]
Лечение гнойной ангины
В большинстве случаев ангина — это гнойно-воспалительное заболевание, которое требует скорейшего применения антибиотиков и при необходимости нестероидных противовоспалительных и противоаллергических средств.
Лечение простой и хронической ангины
Ангина — это острое заболевание без хронических форм. Однако есть термин "стрептококковое носительство" — отсутствие болезни как таковой, чаще на фоне хронической ЛОР-патологии. В этом случае проводят санирование очага, применяют антибиотики с учётом чувствительности к ним и аппаратно промывают миндалины.
Стоит ли удалять гланды
При ангине не удаляют миндалины. Хирургическое лечение возможно лишь при флегмонозной форме ангины и при редких случаях тяжёлого течения заболевания. При развитии осложнений, например, паратонзиллярного абсцесса производится вскрытие гнойника под местной анестезией и его санация.
Прогноз. Профилактика
Прогноз обычно благоприятный. У людей с тяжёлым иммунодефицитом повышенный риск развития осложнений в острый период болезни.
Поможет ли профилактика
Методы профилактики ангины не разработаны. Основное значение при возникновении очага заболевания имеют:
- изоляция больного и его лечение;
- обследование и санация контактных лиц (бактерионосителей);
- при частых повторных заболеваниях — бициллинопрофилактика, по показаниям — удаление миндалин (решение принимает ЛОР-врач);
- здоровый образ жизни, закаливание, приём витаминов.[reference:] [4]
Кормление грудью при болезни
Грудное вскармливание при ангине можно продолжить. Однако необходимо соблюдать меры профилактики заражения ребёнка:
- не дышать и не кашлять на него;
- чаще мыть руки;
- пользоваться защитной маской, не забывать постоянно менять её;
- регулярно проветривать помещение.
Также следует принимать индивидуально подобранный антибиотик, разрешённый при грудном вскармливании.
Читайте также:

