Бактериальные инфекции сахарного диабета
Обновлено: 11.05.2024
Нарушения иммунитета у пациентов с СД значительно повышают риск развития COVID-19. Согласно последним клиническим рекомендациям, тактика лечения зависит от тяжести инфекционного процесса, а ключевое звено терапии – строгий гликемический контроль
За время пандемии COVID-19 многие крупные исследования подтвердили прямую взаимосвязь между тяжестью течения инфекционного заболевания и наличием в анамнезе сахарного диабета. Мета-анализ 8 исследований с участием почти 50 тысяч пациентов с COVID-19 показал, что сахарный диабет (СД) занимает второе место среди наиболее распространенных сопутствующих заболеваний после артериальной гипертензии [1].
По мнению специалистов, высокий риск развития инфекции у пациентов с СД объясняется нарушениями иммунитета в связи с гипергликемией и ее острыми и хроническими последствиями. Кроме того, повышенный уровень цитокинов увеличивает риск развития тяжелой формы инфекции. [2]Исследования китайских ученых выявили, что сахарный диабет чаще встречается среди пациентов именно с тяжелым течением COVID-19, чем среди пациентов с нетяжелой формой заболевания: 16,2% против 5,7%, и прогноз COVID-19 у пациентов СД был хуже [3].
Согласно данным ряда работ, диабет выступает и как фактор риска смертности у пациентов с COVID-19. Большое национальное выборочное исследование показало, что смертность пациентов с диабетом была значительно выше, чем у пациентов без него: 10% против 2,5% [3]. Показатель летальности больных без коморбидных состояний в Китае составлял 0,9%, в то время как у пациентов с СД он достиг 7,3%. [4] Исследование клинических характеристик случаев смерти с COVID-19 выявило, что одной из причин смертности пациентов является диабетический кетоацидоз [5].
Потенциальные механизмы развития тяжелых форм СOVID-19 при СД
У пациентов с сахарным диабетом в сыворотке крови выявляется высокий уровень IL-6, TNF-a и других воспалительных цитокинов [6], и эксперименты на животных моделях заставили предположить, что СД приводит к усиленной выработке TLR4-индуцированного IL-6 [7]. Коронавирус, включая SARS, вероятно активирует TLR3 и TLR4, что приводит к неконтролируемому иммунному ответу и IL-6-доминантному цитокиновому шторму. Именно он, по всей видимости, и является одной из ведущих причин смерти от коронавирусной пневмонии. [8]
Чрезмерная активация TLR4 сигнального пути у пациентов с СД может способствовать прогрессированию заболевания до тяжелых форм и даже летального исхода.
Взаимное влияние COVID-19 на сахарный диабет: порочный круг
Если СД ухудшает прогноз и повышает степень тяжести инфекционного процесса, то и вирус SARS-CoV-2 повышает уровень гликемии и ухудшает течение СД.
В исследовании с участием пациентов с SARS было обнаружено, что даже при легкой форме COVID-19 у больных был высокий уровень гликемии натощак. В другом исследовании было показано, что вирусный белок ACE2 демонстрирует сильное иммуноокрашивание в островках поджелудочной железы, но слабое в экзокринных тканях. Предполагается, что вирус SARS-CoV-2 серьезно повреждает островковые клетки поджелудочной железы и способствует развитию диабета или ухудшению его течения. [9]
Колебания уровня глюкозы у больных СД и COVID-19
Неконтролируемые колебания гликемии у пациентов с сахарным диабетом при COVID-19 являются неблагоприятным прогностическим фактором и увеличивают риск развития осложнений обоих этих заболеваний.
Среди причин данного явления можно отметить [9]:
- Нерегулярное питание и снижение физической активности. К нарушению питания могут приводить и желудочно-кишечные симптомы COVID-19.
- Увеличение секреции глюкокортикоидов на фоне стресса и прием глюкокортикоидов в рамках терапии.
- Случайный или вынужденный перерыв в приеме ПССП в стационарах и выбор неоптимальной альтернативной сахароснижающей терапии.
- Прямое влияние вируса на поджелудочную железу. COVID-19 может тоже стимулировать выработку большого количества воспалительных цитокинов и привести к экстремальному стрессу у некоторых тяжелых и критических пациентов.
Принципы терапии СД при COVID-19
Согласно новейшим рекомендациям по диагностике, профилактике и лечению коронавирусной инфекции, ведение пациентов с сахарным диабетом зависит от тяжести инфекционного процесса, и в обязательном порядке требует более ответственного гликемического контроля. [9]
Легкая степень тяжести
Если температура тела больного ниже 38 °C, и при наличии кашля, слабости и боли в горле отсутствуют критерии среднетяжелого и тяжелого течения, лечение проводится в домашних условиях. Необходимости слишком сильно изменять исходный режим нет, и терапию ПССП или плановую инсулинотерапию можно продолжать.
Однако прогрессирование COVID-19 может быть быстрым, особенно на фоне гипергликемии. Поэтому больным диабетом с COVID-19, даже легкой степени, настоятельно рекомендуется увеличить частоту измерения глюкозы.
При повышении гликемии необходимо усилить терапию СД. При гликемии выше 13-15 ммоль/л нужно оценить уровень кетонов в моче и добавить генно-инженерный инсулин или аналог инсулина длительного действия.
Критериями среднетяжелого течения являются:
- Лихорадка выше 38 °C
- ЧДД более 22/мин
- Одышка при физических нагрузках
- Пневмония (подтвержденная с помощью КТ легких)
- SpO2
- СРБ сыворотки крови более 10 мг/л
У пациентов с СД среднетяжелое течение является показанием к госпитализации. Отечественные рекомендации предписывают отменить прием метформина, агонистов рецепторов ГПП-1 (арГПП-1), ингибиторов натрий-глюкозного котранспортера 2 типа (иНГЛТ-2), препаратов сульфонилмочевины. При гликемии выше 15,0 ммоль/л показано назначение инсулина короткого действия или базис-болюсной инсулинотерапии.
Для пациентов, которые находятся в процессе непрерывного почечного диализа, пропорция глюкозы и инсулина во вводимом растворе должна быть изменена в зависимости от результатов мониторинга глюкозы, во избежание серьезной гипогликемии или гипергликемии.
Каждые 3-4 часа требуется проводить контроль гликемии, 1-2 раза в день – контроль кетонов в моче.
При тяжелом течении отмечается
- ЧДД более 30/мин
- SpO2 ±
- PaO2 /FiO2 ≤300 мм рт. ст.
- Прогрессирование изменений в легких по данным рентгенографии и/или КТ
- Появление признаков других патологических состояний
- Снижение уровня сознания, ажитация.
- Нестабильная гемодинамика (систолическое АД менее 90 мм рт. ст. или диурез менее 20 мл/час)
- Лактат артериальной крови > 2 ммоль/л
- qSOFA> 2 баллов
Внутривенное введение короткого инсулина с помощью инфузомата следует рассматривать как терапию первой линии. Все другие сахароснижающие препараты должны быть отменены.
Целевая гликемия определяется тяжестью состояния пациента. Контроль показателей проводится каждые три часа при уровне ниже 13,0 ммоль/л и каждый час при превышении данного порога. Дважды в день необходимо также контролировать содержание кетонов в моче и лактата в крови.
Особенности лечения коронавирусной инфекции
При назначении терапии COVID-19 необходимо учитывать некоторые физиологические аспекты пациентов с сахарным диабетом, их ослабленный иммунный статус и влияние некоторых препаратов на уровень глюкозы.
Ведение пациентов с СД и COVID-19 после выписки из стационара
На время самоизоляции требуется предусмотреть обеспечение пациентов препаратами инсулина и антикоагулянтами. Возобновление сахароснижающей терапии другими препаратами возможно после полного выздоровления.
Из-за высокой уязвимости пациентов с СД требуется максимально ограничить их посещение лечебных учреждений. Для этого стоит рекомендовать больным пользоваться услугами телеконсультаций, пролонгировать период выписки рецептов и средств самоконтроля, обеспечить доставку лекарственных средств на дом.
Роль инсулинов в лечении СД при COVID-19
Согласно всем российским и международным рекомендациям, инсулины являются препаратами выбора у пациентов с коронавирусной инфекцией.
При СД1 оптимальным режимом служит инсулиновая помпа или базис-болюсная инсулинотерапия. При СД2 инсулины рекомендуются при любой степени тяжести: средние или длительного действия при легкой степени тяжести на фоне гипергликемии; короткого действия или базис-болюсная инсулинотерапия при средней степени тяжести; внутривенное введение инсулинов короткого действия при тяжелом состоянии. Стоит отметить, что и при глюкокортикоид-ассоциированном диабете инсулин также является препаратом первого выбора.
Современные препараты инсулинов ультракороткого сверхбыстрого, ультракороткого, короткого, среднего, длительного и сверхдлительного (инсулин деглудек) действия, а также комбинированные инсулины (ИДегАсп) позволяют подобрать оптимальный режим терапии СД на фоне COVID-19 при любых индивидуальных гликемических целях и состоянии любой степени тяжести.
У больных сахарным диабетом (СД) развитию инфекций мочевых путей способствуют не только общие, но и специфические факторы. С учетом высокой предрасположенности больных СД к мочевым инфекциям желательна ежегодная долговременная профилактика последних.
Patients with diabetes mellitus (DM) develop urinary tract infections which are due not only to common, but to specific factors. Taking into account the fact that DM patients are highly prone to urinary tract infections, it is desirable to annually make long-term prevention of the latter.
М.В. Шестакова — Эндокринологический научный центр РАМН, Москва
M.V. Shestakova — Endocrinology Research Center, Russian Academy of Medical Sciences, Moscow
И нфекции мочевых путей (цистит, уретрит, пиелонефрит) нередко осложняют течение сахарного диабета (СД) и ассоциируются с высоким риском быстрого ухудшения функционального состояния почек, особенно у больных, имеющих клинические признаки диабетической нефропатии. По данным некоторых авторов, частота мочевых инфекций у больных СД достигает 40%, что в 2 - 3 раза выше, чем в общей популяции [1]. Столь высокая частота инфицирования мочевого тракта при СД вполне объяснима, поскольку при этом заболевании имеются не только общие для всех лиц факторы, способствующие развитию мочевой инфекции, но и специфические факторы риска, обусловленные именно наличием СД и его осложнений (табл. 1).
• Глюкозурия - неизбежный спутник СД - несомненно способствует более частому развитию мочевых инфекций, поскольку глюкоза сама по себе является благоприятной питательной средой для размножения бактерий.
• Нейропатия мочевого пузыря - осложнение СД, заключающееся в нарушении его иннервации, вследствие чего у больных исчезают позывы к мочеиспусканию, развивается застой мочи и как следствие – мочевая инфекция.
• Снижение иммунной защиты, практически всегда имеющее место при СД, нередко приводит к тому, что даже непатогенная флора, присутствующая в моче в невысоких титрах, может привести к появлению симптомов инфекции мочевых путей.
Мочевые инфекции при СД не всегда протекают типично, очень часто (в 70% случаев) отмечается малосимптомное или бессимптомное течение. Классическая клиническая картина острого пиелонефрита или обострений хронического пиелонефрита, характеризующаяся ознобами, лихорадкой, дизурией, может отсутствовать. При этом заподозрить обострившуюся мочевую инфекцию у больного СД нередко можно на основании необъяснимой декомпенсации углеводного обмена и появления кетонурии.
С учетом подобной атипичности (бессимптомности) мочевых инфекций при СД рекомендуется проводить активное выявление инфицирования мочевых путей. Для этого необходимо регулярно – 2 - 3 раза в год проводить общеклинический анализ мочи и анализ мочи по Нечипоренко. Лабораторными показателями, характерными для обострения мочевых инфекций, являются:
• лейкоцитурия более 4 - 6 лейкоцитов в поле зрения в общем анализе мочи или более 2 - 4.103/ мл в пробе по Нечипоренко;
• эритроцитурия (более 103/мл в пробе по Нечипоренко), которая обычно развивается при цистите или при сочетании мочевой инфекции с уролитиазом;
• протеинурия, как правило, минимальна и не превышает 1 г/сут;
• бактериурия;
• посев мочи, выявляющий не менее 105 микробных клеток на 1 мл мочи (при отсутствии клинической картины) или 102 - 104 при обнаружении E.Coli, Proteus, Klebsiella, S.Saprophiticus.
В последние годы среди основных возбудителей мочевых инфекций у амбулаторных больных лидируют E. coli (70%), Proteus (5%) и Streptococci (2%); у больных обычных отделений к перечисленным добавляются Klebsiella, Enterobacter и Enterococci (по 15%) [2]. Однако необходимо помнить, что у 15% больных посев мочи отрицателен даже при наличии других лабораторных признаков мочевой инфекции. В ряде случаев такой ложноотрицательный результат может быть обусловлен наличием L-форм бактерий или микоплазм.
Обнаружение мочевой инфекции у больного СД требует немедленного назначения терапии . Основными принципами лечения неосложненной мочевой инфекции при СД являются:
• тщательная компенсация углеводных нарушений;
• соблюдение режима регулярных мочеиспусканий (каждые 3-4 ч) и массаж области живота после мочеиспусканий - для предотвращения застоя мочи;
• применение препаратов, всстанавливающих моторику мочевого пузыря;
• антибиотикотерапия.
Выбор оптимального антибактериального препарата для лечения мочевой инфекции при СД не всегда прост и требует соблюдения определенных правил. В частности, препарат должен быть подобран с учетом чувствительности патогенной микрофлоры, реакции мочи (кислая или щелочная), возраста, и наконец, имеющихся при СД осложнений (патологии почек или печени).
Таблица 1. Факторы риска развития мочевой инфекции при СД
Специфические
При невозможности произвести посев мочи с определением чувствительности микрофлоры лечение начинают с препаратов широкого спектра действия: цефалоспоринов, фторхинолонов, комбинированных пенициллинов. В щелочной среде наиболее эффективны сульфаниламиды, аминогликозиды, цефалоспорины; в кислой - ампициллин, фторхинолоны, нитрофураны. В детском возрасте предпочтительнее назначать полусинтетические пенициллины, цефалоспорины и макролиды, фторхинолоны и тетрациклины нежелательны. При СД, осложненном патологией почек (диабетической нефропатией) с нарушенной азотовыделительной функцией, противопоказаны аминогликозиды, тетрациклины, цефалоспорины I поколения (цефалексин, цефрадин). При мочевой инфекции, развившейся на фоне беременности, безопасно применение пенициллинов, но противопоказаны тетрациклины, аминогликозиды, фторхинолоны и сульфаниламиды.
Важно помнить также о длительности курсов антибактериального лечения. У больных СД длительность антибиотикотерапии при мочевой инфекции должна быть несколько больше, чем у больных, не страдающих диабетом. Это связано с трудностью достижения полного излечения, высокой частотой реинфекций и более частым развитием осложнений мочевой инфекции при СД. Лечение острого цистита должно продолжаться не менее 3 - 5 дней, острого пиелонефрита - 3 - 4 нед, обострений хронического пиелонефрита - до 3 мес; антибактериальные препараты следует чередовать [3].
Необходимость более тщательного пролечивания бактериальной мочевой инфекции у больных СД во многом обусловлена высокой опасностью развития тяжелых осложнений с вовлечением верхних отделов мочевыводящей системы. Наиболее грозными из этих осложнений являются [4]:
| · папиллярный некроз ; · перинефральный абсцесс; · эмфизематозный пиелонефрит; · эмфизематозный пиелит; |
• Папиллярный некроз развивается преимущественно у больных СД с непрерывно рецидивирующей мочевой инфекцией. Характеризуется чередованием эпизодов обострения пиелонефрита и /или почечных колик. При исследовании мочи выявляют микро- или макрогематурию, пиурию (часто в отсутствие симптомов), некротические почечные массы, протеинурию - не более 2 г/сут. При внутривенной урографии обнаруживают “изъеденные молью” чашечки и “кольцевидные тени” – следы отторжения некротизированных почечных сосочков. Опасность данного осложнения связана с возможностью быстрого развития острой почечной недостаточности вследствие обструкции мочевыводящих путей некротизированными почечными массами. Лечение заключается в немедленном восстановлении пассажа мочи и проведении антибактериальной терапии.
• Перинефральный абсцесс - острое гнойное воспаление почечной ткани. Может быть как одно- , так и двусторонним. Клинически характеризуется упорной лихорадкой с ознобами, однако при этом посевы мочи могут быть отрицательными. При пальпации области почек отмечается болезненность. Подтверждение диагноза получают, как правило, при проведеннии компьютерной томографии. Это осложнение требует проведения длительной антибиотикотерапии.
• Эмфизематозный пиелонефрит характеризуется скоплением пузырьков газа вдоль почечных пирамид и под почечной фасцией. Это осложнение вызывают анаэробные газобразующие бактерии. Наиболее типичными клиническими признаками эмфизематозного пиелонефрита являются упорная лиходардка, боли в животе, тошнота, рвота, при исследовании мочи - пиурия. В 85% случаев диагноз можно поставить на основании ультразвукового исследования или внутривенной урографии, при которых выявляются скопления газа вдоль почечных пирамид и под фасцией. Это тяжелейшее осложнение в 60-80% случаев приводит к смерти больного. Метод лечения - нефрэктомия.
• Эмфизематозный пиелит по клиническим проявлениям схож с эмфизематозным пиелонефритом. Отличие заключается в том, что скопления газа локализуются только вдоль собирательного тракта мочевыводящей системы. Антибиотикотерапия достаточно эффективна , однако смертность от этого осложнения составляет около 20%.
С учетом высокой предрасположенности больных СД к развитию инфекции мочевыводящей системы у этой категории пациентов желательно проводить ежегодную долговременную профилактику мочевой инфекции с помощью антибактериальной терапии. Возможно профилактическое применение котримоксазола (триметоприм + сульфаметоксазол), нитрофурантоина или одного триметоприма ежедневно или 3 раза в неделю в периоды высокого риска обострения хронической мочевой инфекции (при простудах, переохлаждениях, после полового акта). Однако всегда необходимо помнить, что только в условиях хорошего метаболического контроля СД возможны успешное лечение и профилактика мочевой инфекции.
1. Kasinath BS, Musais SK, Spargo BH, Katz AI. Non-diabetic renal disease in patients with diabetes mellitus // Am. J. Med.-1983;75:613-17.
2. Кузнецова О.П., Воробьев П.А., Яковлев С.В. Инфекции мочевыводящих путей // Русский медицинский журнал - 1997;№1:4-13.
3. Calvin M K. Urinary tract infection. In: Cur rent therapy in nephrology and hypertension. - ed. by Glassock B., Decker BC. INC Toronto, Philadelphia, 1987;61-7.
4. Viberti GC., Walker JD., Pinto J. Diabetic nephropathy in International Textbook of Diabetes Mellitus. ed. by Alberti KG., John Wiley & Sons, Chichester, New York.-1992;1267-1328.
Что такое сахарный диабет 2 типа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Хитарьяна Александра Георгиевича, диабетолога со стажем в 31 год.
Над статьей доктора Хитарьяна Александра Георгиевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Эпидемия сахарного диабета (СД) длится уже достаточно долго. [9] По данным Всемирной организации здравоохранения (ВОЗ) в 1980 году на планете было около 150 миллионов человек, страдающих от СД, а в 2014 году — около 421 миллионов. К сожалению, тенденция к регрессу заболеваемости за последние десятилетия не наблюдается, и уже сегодня можно смело заявить, что СД является одним из распространённых и тяжёлых болезней.
Сахарный диабет II типа (Type 2 diabetes) — хроническое неинфекционное, эндокринное заболевание, которое проявляется глубокими нарушениями липидного, белкового и углеводного обменов, связанного с абсолютным или же относительным дефицитом гормона, производимого поджелудочной железой.
У пациентов с СД II типа поджелудочная железа продуцирует достаточное количество инсулина — гормона, регулирующего углеводный обмен в организме. Однако из-за нарушения метаболических реакций в ответ на действие инсулина возникает дефицит этого гормона.
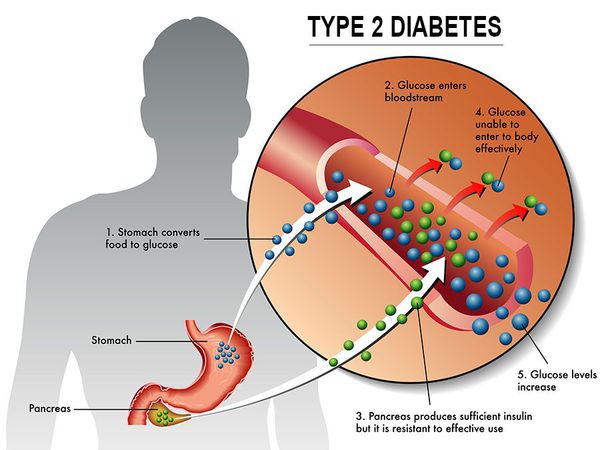
Инсулиннозависимый СД II типа имеет полигенную природу, а также является наследственным заболеванием.
Причиной возникновения данной патологии является совокупность определённых генов, а её развитие и симптоматика определяется сопутствующими факторами риска, такими как ожирение, несбалансированное питание, низкая физическая активность, постоянные стрессовые ситуации, возраст от 40 лет, бессонница. [1] [10]
Нарастающая пандемия ожирения и СД II типа тесно связаны и представляют основные глобальные угрозы здоровью в обществе. [3] Именно эти патологии являются причинами появления хронических заболеваний: ишемической болезни сердца, гипертонии, атеросклероза и гиперлипидемии.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы сахарного диабета 2 типа
Чаще всего симптоматика при СД II типа выражена слабо, поэтому данное заболевание можно обнаружить благодаря результатам лабораторных исследований. Поэтому людям, относящимся к группе риска (наличие ожирения, высокого давления, различных метаболических синдромов, возраст от 40 лет), следует проходить плановое обследование для исключения или своевременного выявления болезни.
К основным симптомам СД II типа следует отнести:
- перманентную и немотивированную слабость, сонливость;
- постоянную жажду и сухость во рту;
- полиурию — учащённое мочеиспускание;
- усиленный аппетит (в период декомпенсации (прогрессирования и ухудшения) болезни аппетит резко снижается);
- кожный зуд (у женщин часто возникает в области промежности);
- медленно заживающие раны;
- затуманенное зрение;
- онемение конечностей.
Период декомпенсации заболевания проявляется сухостью кожи, снижением упругости и эластичности, грибковыми поражениями. В связи с аномально повышенным уровнем липидов возникает ксантоматоз кожи (доброкачественные новообразования).
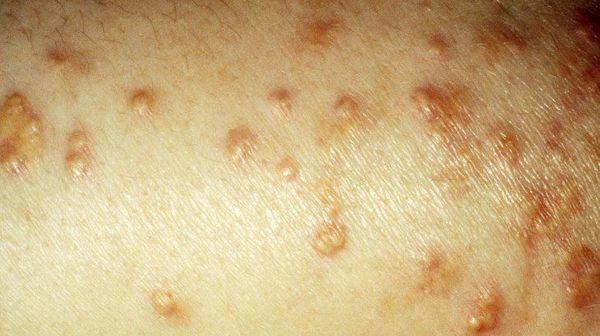
У больных СД II типа ногти подвержены ломкости, потере цвета или же появлению желтизны, а 0,1 – 0,3% пациентов страдают липоидным некробиозом кожи (отложения жиров в разрушенных участках коллагенового слоя).
Помимо симптомов самого СД II типа дают о себе знать также симптомы поздних осложнений заболевания: язвы на ногах, снижение зрения, инфаркты, инсульты, поражения сосудов ног и другие патологии.
Патогенез сахарного диабета 2 типа
Основная причина возникновения СД II типа — это инсулинорезистентность (утрата реакции клеток на инсулин), обусловленная рядом факторов внешней среды и генетическими факторами, протекающая на фоне дисфункции β-клеток. Согласно исследовательским данным, при инсулинорезистентности снижается плотность инсулиновых рецепторов в тканях и происходит транслокация (хромосомная мутация) ГЛЮТ-4 (GLUT4).
Повышенный уровень инсулина в крови (гиперинсулинемия) приводит к уменьшению количества рецепторов на клетках-мишенях. Со временем β -клетки перестают реагировать на повышающийся уровень глюкозы. В итоге образуется относительный дефицит инсулина, при котором нарушается толерантность к углеводам.
Дефицит инсулина приводит к снижению утилизации глюкозы (сахара) в тканях, усилению процессов расщипления гликогена до глюкозы и образования сахара из неуглеводных компонентов в печени, тем самым повышая продукцию глюкозы и усугубляя гимергликемию — симптом, характеризующийся повышенным содержанием сахара в крови.
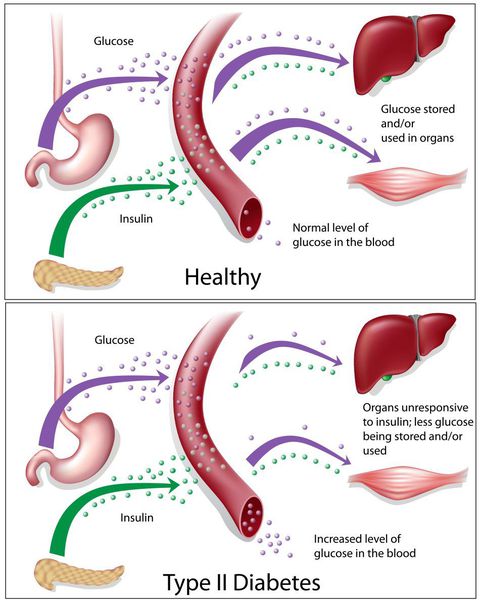
Окончания периферических двигательных нервов выделяют кальцитонин-подобный пептид. Он способствует подавлению секреции инсулина путём активизации АТФ-зависимых калиевых каналов (K+) в мембранах β-клеток, а также подавлению поглощения глюкозы скелетными мышцами.
Избыточный уровень лептина — главного регулятора энергетического обмена — способствует подавлению секреции инсулина, приводя к возникновению инсулинорезистентности скелетных мышц к жировой ткани.
Таким образом инсулинорезистентность включается в себя различные метаболические изменения: нарушение толерантности к углеводам, ожирение, артериальная гипертензия, дислипопротеидемия и атеросклероз. Главную роль в патогенезе этих нарушений играет гиперинсулинемия, как компенсаторное следствие инсулинорезистентности. [6]
Классификация и стадии развития сахарного диабета 2 типа
В настоящее время российские диабетологи классифицируют СД по степени тяжести, а также по состоянию углеводного обмена. Однако Международная Федерация диабета (МФД) довольно часто вносит изменения в цели лечения диабета и классификации его осложнений. По этой причине российские диабетологи вынуждены, постоянно изменять принятые в России классификации СД II типа по тяжести и степени декомпенсации заболевания.
Существуют три степени тяжести заболевания:
- I степень — наблюдаются симптомы осложнений, дисфункция некоторых внутренних органов и систем. Улучшение состояния достигается путём соблюдения диеты, назначается применение препаратов и инъекций.
- II степень — достаточно быстро появляются осложнения органа зрения, происходит активное выделение глюкозы с мочой, появляются проблемы с конечностями. Медикаментозная терапия и диеты не дают эффективных результатов.
- III степень - происходит выведение глюкозы и белка с мочой, развивается почечная недостаточность. В этой степени патология не поддаётся лечению.
По состоянию углеводного обмена выделяют следующие стадии СД II типа:
- компенсированная — нормальный уровень сахара в крови, достигнутый с помощью лечения, и отсутствие сахара в моче;
- субкомпенсированая — уровень глюкозы в крови (до 13,9 ммоль/л) и в моче (до 50 г/л) умеренный, при этом ацетон в урине отсутствует;
- декомпенсированная — все показатели, характерные для субкомпенсации, значительно повышены, в моче обнаруживается ацетон.
Осложнения сахарного диабета 2 типа
К острым осложнениям СД II типа относятся:
- Кетоацидотическая кома — опасное состояние, при котором происходит тотальная интоксикация организма кетоновыми телами, а также развивается метаболический ацидоз (увеличение кислотности), острая печёночная, почечная и сердечно-сосудистая недостаточность.
- Гипогликемическая кома — состояние угнетения сознания, развивающееся при резком уменьшении содержания глюкозы в крови ниже критической отметки.
- Гиперосмолярная кома — данное осложнение развивается в течение нескольких дней, в результате которого нарушается метаболизм, клетки обезвоживаются, резко увеличивается уровень глюкозы в крови.
Поздними осложнениями СД II типа являются:
- диабетическая нефропатия (патология почек);
- ретинопатия (поражение сетчатки глаза, способное привести к слепоте);
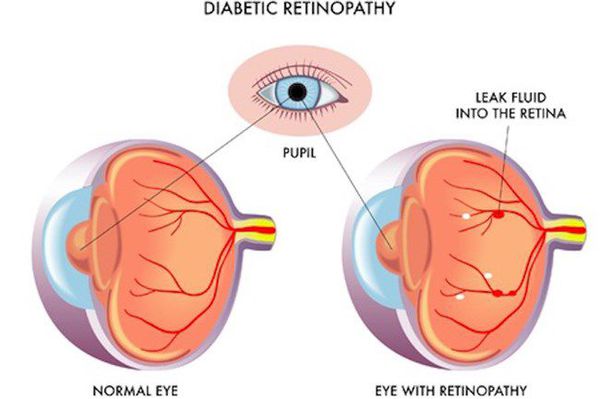
- полинейропатия (поражение периферических нервов, при котором конечности теряют чувствительность);
- синдром диабетической стопы (образование на нижних конечностях открытых язв, гнойных нарывов, некротических (отмирающих) тканей).
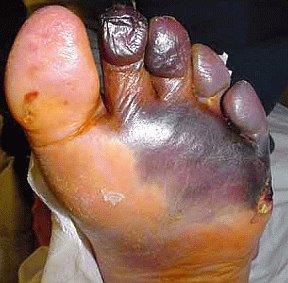
Диагностика сахарного диабета 2 типа
Для того чтобы диагностировать СД II типа необходимо оценить симптомы болезни и провести следующие исследования:
Лечение сахарного диабета 2 типа
Лечение СД II типа предполагает решение основных задач:
- компенсировать недостаток инсулина;
- скорректировать гормонально-метаболические нарушения;
- осуществление терапии и профилактики осложнений.
Для их решения применяется следующие методы лечения:
- диетотерапия;
- физические нагрузки;
- применение сахароснижающих препаратов;
- инсулинотерапия;
- хирургическое вмешательство.
Диетотерапия
Диета при СД II типа, как и обычная диета, предполагает оптимальное соотношение основных веществ, содержащихся в продуктах: белки должны составлять 16% суточного рациона, жиры — 24%, а углеводы — 60%. Отличие диеты при диабете II типа заключается в характере потребляемых углеводов: рафинированные сахара заменяются медленно усваиваемыми углеводами. Так как данное заболевание возникает у полных людей, потеря веса является важнейшим условием, нормализующим содержание глюкозы в крови. В связи с этим рекомендована калорийность диеты, при которой пациент еженедельно будет терять 500 г массы тела до момента достижения идеального веса. Однако при этом еженедельное уменьшение веса не должно превышать 2 кг, в противном случае это приведёт к избыточной потере мышечной, а не жировой ткани. Количество калорий, необходимое для суточного рациона пациентов с СД II типа, рассчитывается следующим образом: женщинам нужно умножить идеальный вес на 20 ккал, а мужчинам — на 25 ккал.
При соблюдении диеты необходимо принимать витамины, так как во время диетотерапии происходит избыточное выведение их с мочой. Нехватку витаминов в организме можно компенсировать при помощи рационального употребления полезных продуктов, таких как свежая зелень, овощи, фрукты и ягоды. В зимние и весенние периоды возможен приём витаминов в дрожжевой форме.
Физическая нагрузка
Верно подобранная система физических упражнений, с учётом течения заболевания, возраста и присутствующих осложнений, способствует значительному улучшению состояния больного СД. Эта методика лечения хороша тем, что необходимость применения инсулита практически отпадает, так как во время физических нагрузок глюкоза и липиды сгорают без его участия.
Лечение сахароснижающими препаратами
На сегодняшний день используют производные сахароснижающих препаратов:
- сульфонилмочевины (толбутамид, глибенкламид);
- бигуаниды, снижающие глюконеогенез в печени и повышающие чувствительность мышц и печени к инсулину (метформин);
- тиазолидиндионы (глитазоны), схожие по свойствам с бигуанидами (пиоглитазон, росиглитазон);
- ингибиторы альфа-глюкозидаз, снижающие темпы всасывания глюкозы в желудочно-кишечном тракте (акарбоза);
- агонисты рецепторов глюкагоноподобного пептида-1, стимулирующие синтез и секрецию инсулина, снижающие продукцию глюкозы печенью, аппетит и массу тела, замедляющие эвакуацию пищевого комка из желудка (эксенатид, лираглутид);
- ингибиторы депептидил-пептидазы-4, также стимулирующие синтез и секрецию инсулина, снижающие продукцию глюкозы печенью, не влияющие на скорость эвакуации пищи из желудка и оказывающие нейтральное действие на массу тела (ситаглиптин, вилдаглиптин);
- ингибиторы натрий-глюкозного котранспортера 2 типа (глифлозины), снижающие реабсорбцию (поглощение) глюкозы в почках, а также массу тела (дапаглифлозин,эмпаглифлозин).
Инсулинотерапия
В зависимости от тяжести болезни и возникающих осложнений врач назначает приём инсулина. Данный метод лечения показан примерно в 15-20% случаев. Показаниями к применению инсулинотерапии являются:
- быстрая потеря веса без видимой на то причины;
- возникновение осложнений;
- недостаточная эффективность других сахароснижающих препаратов.
Хирургическое лечение
Несмотря на множество гипогликемических препаратов, остаётся не решённым вопрос об их правильной дозировке, а также о приверженности пациентов к выбранному методу терапии. Это, в свою очередь, создаёт трудности при достижении длительной ремиссии СД II типа. Поэтому всё большую популярность в мире получает оперативная терапия данного заболевания — бариатрическая или метаболическая хирургия. МФД считает данный метод лечения пациентов с СД II типа эффективным. В настоящее время в мире проводится более 500 000 бариатрических операций в год. Существует несколько видов метаболической хирургии, самыми распространёнными являются шунтирование желудка и мини гастрошунтирование. [4]
Шунтирование желудка по Ру
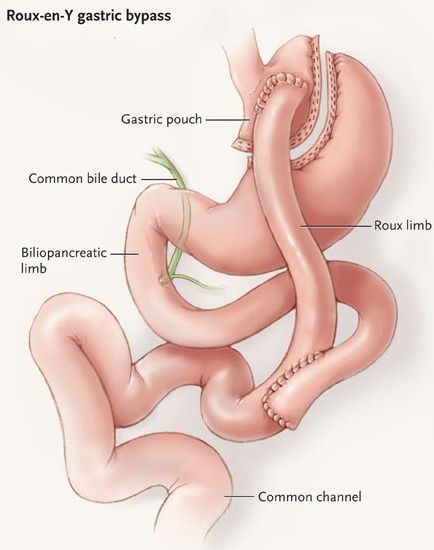
Во время шунтирования, желудок пересекается ниже пищевода таким образом, чтоб его объём сократился до 30 мл. Оставшаяся большая часть желудка не удаляется, а заглушается, предотвращая попадание в неё пищи. [5] В результате пересечения образуется маленький желудок, к которому затем пришивается тонкая кишка, отступив 1 м от её окончания. Таким образом пища будет прямиком попадать в толстую кишку, при этом обработка её пищеварительными соками снизится. Это, свою очередь, провоцирует раздражение L-клеток подвздошной кишки, способствующее снижению аппетита и увеличению роста клеток, синтезирующих инсулин.
Мини шунтирование желудка
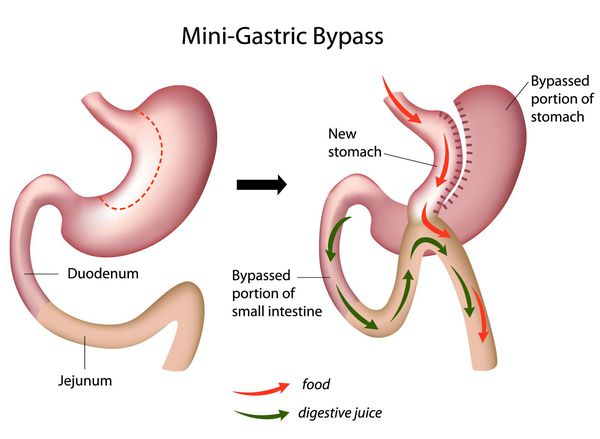
Главное отличие минигастрошунтирования от классического шунтирования желудка — сокращение количества анастомозов (соединений отрезков кишки). [2] При выполнении традиционной операции накладывается два анастомоза: соединение желудка и тонкой кишки и соединение разных отделов тонкой кишки. При минигастрошунтировании анастомоз один — между желудком и тонкой кишкой. Благодаря малому объёму вновь сформированного желудка и быстрому поступлению еды в тонкую кишку у пациента возникает чувство насыщения даже после приёма незначительных порций пищи.
К другим видам бариатрической хирургии относятся:
- гастропликация — ушивание желудка, предотвращающее его растягивание; [8]
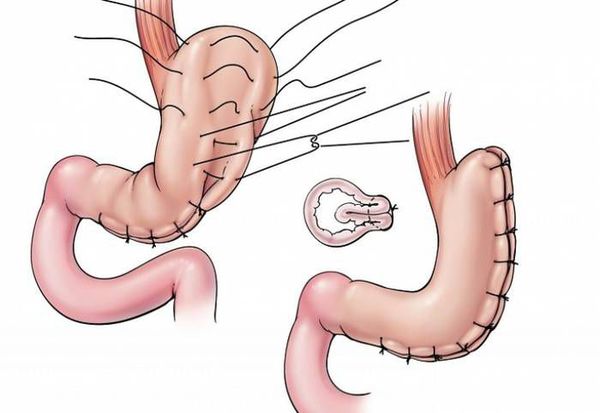
- рукавная гастропластика (иначе её называют лапароскопической продольной резекцией желудка) — отсечение большей части желудка и формирование желудочной трубки объёмом 30 мл, которое способствует быстрому насыщению, а также позволяет избежать соблюдения строгой диеты;
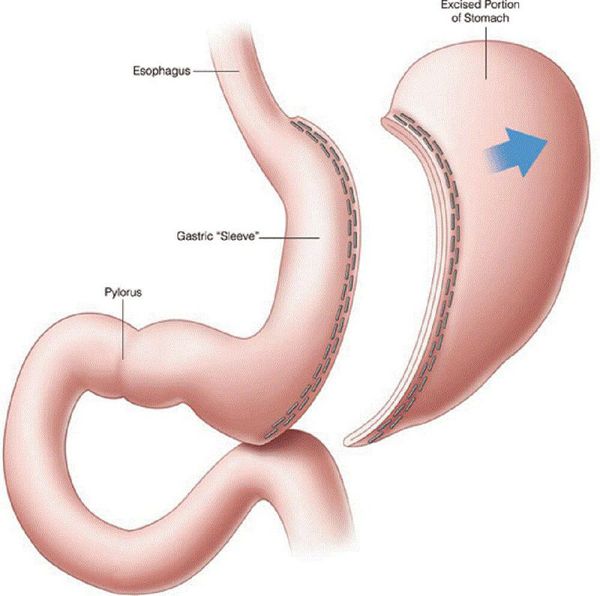
- бандажирование желудка — уменьшение объёма желудка с помощью специального кольца (бандажа), накладывающегося на верхнюю часть желудка (данное вмешательство обратимо).
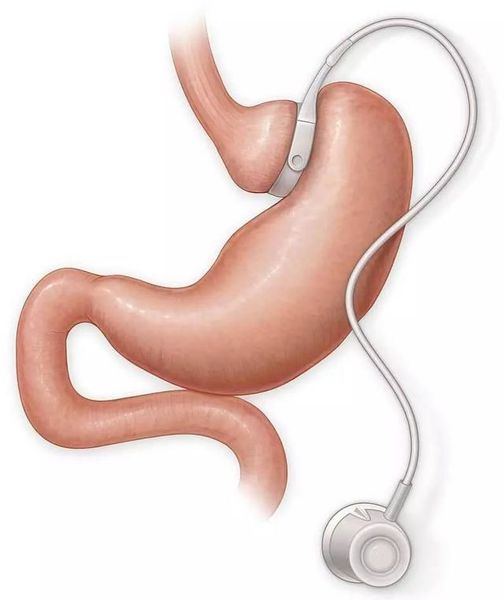
Противопоказания к проведению хирургического лечения — наличие у пациента эзофагита (воспаления слизистой оболочки пищевода), варикозного расширения вен пищевода, портальной гипертенззи, цирозща печени, язвенной болезни желудка или двенадцатиперстной кишки, хронического панкреатита, беременности, алкоголизма, тяжёлых заболеваний сердечно-сосудистой системы или психических расстройств, а также длительное применение гормональных препаратов.
Прогноз. Профилактика
К сожалению, полностью излечиться от СД II типа невозможно. Однако существуют способы улучшения качества жизни пациентов с данным заболеванием.
На сегодняшний день существует большое количество “баз”, где специалисты-эндокринологи объясняют пациентам, каким должен быть их уклад жизни, как правильно питаться, какие продукты не следует употреблять, какими должны быть ежедневные физические нагрузки.
Также создано огромное количество сахароснижающих препаратов, которые ежегодно совершенствуются. Для того, чтобы они оказывали положительное влияние на организма, медикаменты необходимо принимать регулярно.
Практика показывает, что соблюдение всех рекомендаций эндокринологов улучшает процесс лечения СД II типа.
Оперативным методом, повышающим качество жизни при СД II типа по мнению МФД, является бариатрическая хирургия.
Значительно улучшить состояние пациентов с данным заболеванием позволяет проведение гастроинтестинальных операций (терапия морбидного ожирения), вследствие которой нормализуется уровень гликогемоглобина и глюкозы в крови, теряется необходимость применения антидиабетических препаратов и инсулина.
Бариатрическая хирургия может привести к значительной и устойчивой ремиссии, а также к улучшению течения СД II типа и других метаболических факторов риска у тучных пациентов. Хирургическое вмешательство в течение 5 лет после установления диагноза чаще всего приводит к долговременной ремиссии.
Для предупреждения возникновения СД II типа необходимо соблюдать следующие меры профилактики:
Цистит и урогенитальные инфекции при сахарном диабете

Сахарный диабет в анамнезе пациента ведет к сильному ослаблению иммунитета. На фоне слабого иммунного ответа повышается риск возникновения и развития заболеваний, вызываемых вирусами, грибковой и бактериальной флорой. К подобным патологиям относится цистит, пиелонефрит, кандидоз и некоторые урогенитальные инфекции. Положение пациента усугубляется с возрастом – чем старше больной, тем чаще он страдает заболеваний, вызванных бактериями и грибами, на фоне прогрессирующего сахарного диабета. Инфекции мочевыводящих путей и мочевого пузыря встречаются чаще у людей с некомпенсированным сахарным диабетом.
Цистит: причины развития, патогенез, симптомы
Циститом называют воспалительное заболевание мочевого пузыря и мочевыводящих путей, вызванное стремительным развитием микробной флоры. Люди пожилого и старческого возраста страдают этим заболеванием в силу сниженного иммунитета, частых переохлаждений, недостаточно тщательной гигиены интимных зон. Сахарный диабет значительно повышает риск развития цистита, т.к. повышенный уровень глюкозы в моче диабетиков повреждает стенки мочевого пузыря и мочеточников, а также служит питательной средой для обитающих там условно патогенных микроорганизмов. Из-за анатомических особенностей женщины болеют чаще мужчин.
- тянущую боль внизу живота;
- частые позывы к мочеиспусканию при малом количестве выходящей мочи;
- боль при мочеиспускании;
- наличие в моче лейкоцитов, высокого содержания глюкозы, прожилок крови;
- повышение температуры тела, общую слабость, отсутствие аппетита;
- у пожилых людей возможно неконтролируемое подтекание мочи.
Цистит относится к инфекциям нижних мочевыводящих путей, обычно протекает в острой форме. Без адекватного лечения цистит переходит в пиелонефрит – воспаление канальцев, чашечек и лоханки почки. Он встречается в острой, хронической и хронической с периодическими обострениями форме.
Встречается бессимптомная форма обсеменения мочевыводящих путей, не сопровождающаяся воспалением. Обнаруживается при анализе мочи. Лечения не требует.
- контроль уровня сахара в крови, рациональное лечение;
- устранение всех очагов инфекции, включая кариес, хронический тонзиллит, холецистит и другие.
Кандидоз: этиология, патогенез заболевания
Кандидоз известен как молочница, встречается в равной степени и у мужчин, и у женщин. Может возникать на фоне низкой иммунной сопротивляемости, передаваться половым путем. Риск возникновения молочницы повышает пожилой возраст, дисбактериоз, хронические заболевания эндокринной системы, к которым относится сахарный диабет.
- чувство жжения в половых органах;
- белые комкообразные выделения;
- обнаружение грибов рода Кандида в мазке и моче;
- болезненное мочеиспускание, помутнение мочи;
- повышение температуры тела.
При отсутствии лечения дальнейшее размножение грибков вызывает генерализованный кандидоз с поражением слизистых оболочек, расстройством пищеварения на фоне дисбактериоза.
Диагностика и лечение урогенитальных инфекций
Предварительная постановка диагноза и его уточнение осуществляется с помощью нескольких методов: опросного, лабораторных (анализ мочи на лейкоцитоурию, сахар, бак.посев), инструментальных (УЗИ почек, биопсия).
После подтверждения диагноза врач назначает схему лечения, включающую в себя антибактериальные препараты, к которым чувствительна обнаруженная флора, антигистаминные, пробиотики, иногда и противогрибковые для исключения развития грибковой флоры в период вызванного антибиотиками дисбактериоза. Для людей пожилого и старческого возраста применение пробиотиков обязательно.
При молочнице назначаются противогрибковые препараты местного или общего действия (таблетки, свечи). Параллельно обязателен прием пробиотиков и контроль уровня сахара в крови.
В последние десятилетия отмечается повышенный интерес клиницистов к проблеме сепсиса как в хирургической, так и в терапевтической клинике. Это в значительной мере связано с увеличением числа случаев развития септического процесса и высокими показателями летальности.
Для координации исследований по теме "Сепсис" в 2002 г. было основано международное движение за выживаемость при сепсисе - "Surviving Sepsis Campaign" (SSC), объединившее 15 известных международных ассоциаций, в том числе Общество критической медицины, Европейское общество интенсивной терапии, Общество хирургической инфекции и др. Это движение регулярно выпускает рекомендации по диагностике и лечению сепсиса, которые периодически пересматриваются. В 2012 г. опубликованы новые рекомендации SSC, они стали логическим продолжением действовавших с 2008 г. [8].
Основы классификации сепсиса были заложены в 1992 г. на согласительной конференции Американского колледжа пульмонологов (АССР) и Общества специалистов критической медицины (SCCM). В перечне согласованных определений, лежащих в основе систематизации сепсиса, выделены последовательные понятия: "синдром системной воспалительной реакции" - ССВР (Systemic Inflammatory Response Syndrome - SIRS), "сепсис", "тяжелый сепсис" и "септический шок". В настоящий момент проходит обсуждение новой классификации сепсиса, предпринятое с целью более раннего начала патогенетического лечения. Предлагается выделять следующие клинические состояния: инфекция, сепсис и септический шок. В группу "инфекция" предлагают включать пациентов с ССВР и ССВР на инфекцию (сепсис, по старой классификации). Категория "сепсис" подразумевает сочетание ССВР и органной дисфункции, связанной с инфекцией. Понятие "септический шок" предлагается оставить в прежней трактовке [33]. Инициированная J. Vincent и соавт. дискуссия нашла активное продолжение на посвященном проблемам сепсиса конгрессе, который прошел 3-5 декабря 2014 г. в Париже (Франция). Продолжение обсуждения и окончательное формирование новой классификации ожидаются на последующих конференциях (Брюссель - март 2015 г. и Берлин - сентябрь 2015 г.).
Сепсис и нарушение углеводного обмена
Установлено, что прогноз при сепсисе зависит от сроков начала патогенетической терапии, эффективности санации очага инфекции, наличия сопутствующих заболеваний. Пристальное внимание при сепсисе уделяют также уровню глюкозы. Высказывают различные мнения. Так, G. van den Berghe и соавт. [31] у пациентов с сепсисом рекомендовали в качестве целевых значений показатели глюкозы в интервале 4,4-6,1 ммоль/л. Такие значения глюкозы ассоциировали со снижением смертности. Позднее была опубликована работа, продемонстрировавшая, что достижение этих показателей глюкозы сопровождалось увеличением летальности [12]. Согласно последним рекомендациям SSC, инсулин назначают лишь при превышении в двух последовательных анализах значения глюкозы 9,9 ммоль/л [8]. Неблагоприятные эффекты гипергликемии связаны с возникновением осмотического диуреза, потерей электролитов и развитием гиповолемии. Пороговыми для уровня глюкозы являются цифры около 10 ммоль/л, при превышении этих показателей реабсорбирующая способность почек истощается и глюкоза попадает в мочу [2]. Отдельной проблемой является развитие гипергликемии при проведении нутритивной поддержки. Этому вопросу посвящен ряд публикаций, в которых обсуждаются способы предупреждения и коррекции гипергликемии [5].
Нарушение гомеостаза глюкозы особенно актуально при развитии сепсиса у больных сахарным диабетом (СД). С одной стороны, имеются не всегда корригированные нарушения углеводного обмена, с другой - септический процесс, при котором наблюдается выброс контринсулярных гормонов. Таким образом, можно ожидать увеличения числа осложнений и летальности при сочетании этих двух процессов. В литературе имеются противоречивые и весьма ограниченные сведения о влиянии СД на течение сепсиса [4, 35]. В связи с этим представляется актуальным обсудить вопросы патогенеза и лечения больных с сепсисом на фоне СД.
Особенности этиопатогенеза сепсиса при СД
Увеличение числа случаев сепсиса при СД обусловлено целым рядом причин: с одной стороны, наблюдаются нарушения иммунитета, способствующие более частому возникновению инфекционных заболеваний, с другой - нарушения метаболизма, препятствующие полноценному проникновению препаратов к очагам инфекции. При СД у больных не только чаще наблюдаются инфекционные заболевания и более тяжелое их течение. Справедливо и обратное утверждение: инфекция является причиной декомпенсации СД, а в 20-25% наблюдений служит первым его признаком [6]. У пациентов с СД риск развития инфекции и сепсиса значительно повышен [21]. Имеются данные, согласно которым у 20,1-22,7% больных с сепсисом имеется СД [12, 28].
На взаимосвязь между инфекцией и СД впервые обратил внимание Авиценна (980-1027 гг. н.э.), который заметил, что течение диабета часто осложняется возникновением туберкулеза [26].
При обсуждении проблем сочетания СД и сепсиса на этиологии и типе диабета (1-й или 2-й тип) внимание обычно не акцентируют. При этом все осложнения рассматривают как производные от гипергликемии [16]. Высказывается и противоположное мнение: при СД 2-го типа наблюдается более тяжелое течение инфекции. Это объясняется особенностями фармакокинетики антимикробных препаратов при сопутствующем ожирении, проявляющимися изменениями их распределения, выведения и метаболизма [1].
Часть инфекций характерна только для больных СД и практически не регистрируются у лиц без нарушений углеводного обмена. К ним относятся злокачественный наружный отит, риноцеребральный мукоромикоз, эмфизематозный холецистит, эмфизематозный пиелонефрит и др. [1, 16], однако они встречаются редко, гораздо чаще клиницисту приходится сталкиваться с обычными инфекциями.
В исследовании, проведенном в Канаде, сравнили частоту развития инфекционных заболеваний у больных СД и у здоровых добровольцев, в каждую группу включили по
513 749 человек. Установили, что при СД повышается риск возникновения пневмонии (risk ratio - соотношение рисков) - 1,46-1,48, цистита - 1,39-1,43, туберкулеза - 1,12-1,21 и флегмоны подкожной жировой клетчатки - 1,81-1,85. Одновременно повышался риск возникновения инфекционных заболеваний, требующих госпитализации, - 2,10-2,23 [27]. В другое исследование, длившееся 12 мес, включили 705 пациентов с СД 1-го типа, 6712 больных - с СД 2-го типа и 18 911 больных артериальной гипертензией. Обнаружили, что у больных СД была выше вероятность развития инфекции нижних дыхательных путей - отношение шансов 1,42 для СД 1-го типа и 1,32 для СД 2-го типа, а также мочевого тракта - 1,96 и 1,24 соответственно, кожи и мягких тканей - 1,59 и 1,33 [21]. Таким образом, СД ассоциируется с увеличением вероятности развития и количества инфекционных осложнений. Вместе с тем данные о смертности при сочетании СД и сепсиса противоречивы. Ряд авторов сообщают об увеличении летальности, другие исследователи не обнаружили различий в исходах заболеваний. Приводятся сведения и об увеличении выживаемости на фоне этого заболевания [13].
В другом изыскании, продолжавшемся 7 лет и включавшем 29 900 пациентов с внебольничной пневмонией, отмечено, что сопутствующий СД приводил к увеличению риска летального исхода [17].
Риск развития септических осложнений при СД связан как с дефектами иммунитета, так и с макро- и микрососудистыми осложнениями и автономной невропатией.
В экспериментальных и клинических работах было показано, что при СД изменения фиксируются как в клеточном, так и в гуморальном звене иммунитета. При диабете наблюдается повышение уровня маркеров, характерных для воспаления (С-реактивного белка, фактора некроза опухоли альфа, интерлейкинов 6 и 8), однако при развитии сепсиса уровень провоспалительных цитокинов у больных СД не отличался от такового у пациентов без нарушения углеводного обмена [23, 24]. Таким образом, выраженность воспалительной реакции, оцениваемая по биохимическим маркерам, не определялась сосуществующим СД. Исследования in vitro демонстрируют, что у больных СД скомпрометирована функция нейтрофилов, моноцитов и лимфоцитов, а гуморальная антиинфекционная защита подавлена [16].
Макро- и микрососудистые поражения, автономная невропатия обусловливают повышенную склонность к инфекциям определенной локализации. Нарушение микроциркуляции приводит к замедленному ответу на микробную инвазию и ухудшает заживление дефекта кожи и слизистых оболочек, повреждая их барьерную функцию. В результате этого повышается частота инфицирования кожи и подлежащих мягких тканей [7]. Кроме того, присоединение на этом неблагоприятном фоне нарушений чувствительности нижних конечностей вследствие сенсорной невропатии сопровождается бессимптомным течением микротравм этой локализации и увеличивает риск инфекции. Наиболее типичным примером такого развития событий являются формирование диабетической стопы. Другим примером может служить дисфункция мочевого пузыря вследствие автономной невропатии. Развивающаяся задержка мочи и пузырно-мочеточниковый рефлюкс являются причиной колонизации микроорганизмами мочевых путей. При этом повышенная концентрация глюкозы в моче способствует росту сапрофитной и патогенной флоры, чем и объясняется характерная локализация инфекции при СД в мочевыводящих путях и развитие уросепсиса [22].
При СД наблюдаются и значимые нарушения функции органов дыхания. У больных СД происходит утолщение альвеолярно-капиллярной и бронхиально-капиллярной базальных мембран, что сопровождается нарушением диффузии газов и снижением респираторных резервов. Установлено, что при СД происходит неэнзимное гликозилирование структурных компонентов легких и грудной клетки, богатых коллагеном и эластином, обусловливающее снижение эластичности легких и повышение упругости грудной клетки. В результате формируется рестриктивный тип нарушения дыхания. Дополнительно наблюдаются микроваскулярные нарушения в легких, аналогичные изменениям в почках и в сетчатке. Диабетическая полинейропатия ухудшает респираторное нервно-мышечное функционирование, нарушая объемы вентиляции. Одновременно происходит снижение тонуса диафрагмы за счет потери аксональных окончаний диафрагмального нерва [32]. Все перечисленные выше нарушения приводят к увеличению частоты инфекций респираторного тракта.
Возникновение инфекции и развитие сепсиса напрямую связаны с показателем гликемии. Приводятся данные о том, что риск развития инфекции у больных СД зависит от степени компенсации нарушений углеводного обмена [25].
В исследовании у 55 408 больных СД, оперированных по поводу различных заболеваний (были исключены кардиохирургические вмешательства), установлено, что превышение в послеоперационном периоде показателя уровня гликемии 8,3 ммоль/л сопровождалось увеличением количества септических осложнений [15].
СД и инфекции мягких тканей
В настоящий момент самой распространенной по локализации инфекцией мягких тканей является диабетическая стопа [30]. Это связано с особенностями патогенеза септического процесса при СД, что отмечалось выше. В зависимости от тяжести инфекционного поражения выделяют нетяжелые (не угрожающие ампутации конечностей) и тяжелые (угрожающие ампутацией конечностей) формы.
В настоящее время все бактериальные инфекционные процессы мягких тканей, протекающие с некрозом их различных слоев, относят к некротизирующим инфекциям. К этой группе тяжелых хирургических инфекций относят клостридиальную и неклостридиальную формы, представленные клостридиальным и неклостридиальным целлюлитом, фасцитом, миозитом или целлюлофасциомиозитом (мионекроз) [3, 10].
Анаэробная инфекция мягких тканей - термин скорее хирургический, чем микробиологический, так как в это понятие входят гнойно-воспалительные заболевания мягких тканей, вызываемые анаэробно-аэробными ассоциациями микроорганизмов с преобладанием анаэробного компонента микрофлоры или чисто спорообразующих форм. Клинически анаэробная инфекция мягких тканей обычно выражается в виде флегмоны, тяжесть и течение которой в значительной степени зависят от объема пораженных тканей. Инфекция может локализоваться преимущественно в подкожной жировой клетчатке, в фасции и в мышцах или одновременно поражать эти анатомические образования.
Учитывая полимикробный характер инфекции, S. Finegold [11] выделил следующие клинические формы анаэробной неклостридиальной инфекции: неклостридиальный крепитирующий целлюлит, синергический некротический целлюлит, прогрессирующую синергическую бактериальную гангрену, некротический фасцит (НФ) и анаэробный стрептококковый миозит. Эти формы различаются сроком распространения заболевания, выраженностью местных симптомов и степенью интоксикации. Различна и частота их выявления: НФ и крепитирующий целлюлит регистрируются в 38%, синергическая бактериальная гангрена - в 19%, стрептококковый миозит - в 5% наблюдений.
При поражении подкожной жировой клетчатки кожа над этой зоной обычно мало изменена: отмечаются лишь ее плотный отек и гиперемия без четкой отграниченности процесса, но с выраженной тенденцией к распространению. Сравнительно небольшие изменения кожи, как правило, не отражают истинный объем поражения подлежащих тканей. Патологический процесс при этом может распространяться по подкожной жировой клетчатке и фасции далеко за пределы раны. Подкожная жировая клетчатка при этом имеет очаги расплавления, характерный серый или грязно-серый цвет, пропитана серозно-гнойной буроватого цвета жидкостью, часто с резким неприятным запахом, свободно стекающей в рану.
Выявление очагов плотной инфильтрации подкожной жировой клетчатки и участков потемнения или некроза кожи нередко свидетельствует о переходе патологического процесса на фасцию. Присутствие в ране расплавленных и грязно-серых участков некротизированной фасции, буроватого экссудата позволяет считать диагноз неклостридиальной инфекции несомненным. Необходимо подчеркнуть, что ее течение может осложниться тромбофлебитом поверхностных и глубоких вен.
Возможно также сочетанное поражение фасций, подкожной жировой клетчатки и мышц. При этом воспалительный процесс по межфасциальным пространствам может распространяться на значительное расстояние за пределы раны. Пораженные мышцы имеют тусклый, вареный вид, пропитаны серозно-геморрагическим экссудатом. При поражении фасций в процесс вовлекаются лишь поверхностные слои мышц, а при поражении мышц - вся их толща или вся группа мышц, при этом внешний вид раны обычно не соответствует распространенности поражения.
Возникновение тяжелых инфекций стопы при СД ассоциировано с развитием сепсиса. Обычно в области стопы имеются глубокие язвы с распространением на подкожную жировую клетчатку в сочетании с явлениями интоксикации и гипергликемией. Чаще всего наблюдается полимикробный характер инфекции с ассоциацией грамположительных (S. aureus), анаэробных (B. fragilis) и грамотрицательных (E. coli) микроорганизмов. При прогрессировании и распространении процесса характерно возникновение множественных абсцессов и развитие остеомиелита. По данным литературы, остеомиелит развивается у 50-60% больных с тяжелой инфекцией стопы, подтверждением диагноза является выделение возбудителей из костной ткани [19]. Антимикробная терапия обычно проводится препаратами широкого спектра действия с учетом высеянного возбудителя. Часто определяется метициллинрезистентный S. aureus, что требует назначения ванкомицина или линезолида. Длительность антибактериальной терапии зависит от наличия признаков остеомиелита и необходимости ампутации и может достигать 4-6 нед [7].
НФ встречается преимущественно у больных СД и сопровождается высокой летальностью. Первоначально инфекция развивается в подкожной клетчатке, далее быстро распространяется по фасциальным поверхностям, чаще всего вовлекаются верхние и нижние конечности, передняя брюшная стенка [3, 34]. При генерализации течение НФ осложняется возникновением септического шока. Выделяют два вида НФ. Первый вариант встречается чаще, составляя 90% всех наблюдений НФ, для него характерна смешанная анаэробная (Peptostreptococcus spp., Prevotella spp., Clostridium spp.) и аэробная (S. aureus, E. coli) флора. При втором варианте НФ (10% всех наблюдений) обычно высевают стрептококк группы А и различные виды стафилококков. Лечение НФ подразумевает оперативное вмешательство и мощную антибактериальную терапию.
Возбудители инфекции и СД
Характер высеваемых микроорганизмов у больных СД при развитии инфекции и сепсиса во многом определяется особенностями локальной микрофлоры. Вместе с тем имеются определенные закономерности. Так, по данным литературы, среди взрослых пациентов с бактериемией, вызванной стрептококками группы В, больные СД составляют 27,5%. Среди пациентов, у которых обнаружены бактерии Klebsiella spp., доля больных СД колеблется от 30 до 60%. Также чаще, чем в обычной популяции, септические осложнения у больных СД обусловлены S. aureus [14].
В проведенных исследованиях было установлено, что при развитии сепсиса у больных СД повышается риск бактериемии, являющейся неблагоприятным прогностическим фактором. Риск пневмококковой бактериемии у больных СД повышается в 1,5 раза [29]. Считается, что у больных СД имеются отличия от пациентов с нормальным показателем гликемии по характеру возбудителей пневмонии. Прежде всего повышается этиологическая значимость S. aureus и S. pneumoniae. Кроме того, пневмония, вызванная S. pneumoniae, протекает тяжелее [14]. Одновременно увеличивается риск развития кетоацидоза, несмотря на проводимую терапию [18].
Таким образом, у больных сахарным диабетом риск развития септических осложнений выше, чем у пациентов без нарушений углеводного обмена. Патогенез септических осложнений у таких больных связан с депрессией как клеточного, так и гуморального звена иммунитета. Доказаны большая частота и более тяжелое течение у этих больных пневмонии и инфекций мягких тканей. Все же полноценных исследований, отражающих исходное нарушение углеводного обмена и течение послеоперационного периода, не выполнено. Кроме того, не разработаны диагностические критерии риска развития септических осложнений у хирургических больных. Спорными остаются рекомендации по антибактериальной терапии при сочетании сахарного диабета и сепсиса. Все эти проблемы требуют дальнейшего детального изучения.
Читайте также:

