Цефтриаксон или левофлоксацин стафилококк
Обновлено: 25.04.2024
В данном обзоре анализируются преимущества и недостатки различных классов антибактериальных препаратов, в частности эффективность и безопасность препарата левофлоксацина (Леволет ® Р) для лечения инфекционно-воспалительной патологии верхних дыхательных путей. Подробно рассматривается фармакодинамика левофлоксацина, приводятся результаты исследований по его использованию и изучению эффективности применения по сравнению с другими классами антибактериальных препаратов. Авторы акцентируют внимание на последних тенденциях по назначению коротких курсов левофлоксацина, которые с успехом стали применять при лечении ряда инфекций. Приводятся исследования по назначению коротких курсов левофлоксацина в высокой дозе (750 мг 1 р./сут), которая повышала комплаентность пациентов, снижала риск развития устойчивости возбудителя к антибиотику. Приводятся актуальные сведения об эффективности и удобстве новой дозировки с выраженным терапевтическим результатом. В заключение авторы делают вывод, что Леволет ® Р по своим свойствам эффективен при лечении больных c острыми заболеваниями и обострением хронических заболеваний ВДП. Доказанная эффективность составляет 93,8–100%.
Ключевые слова: антибактериальные препараты, левофлоксацин, Леволет ® Р, инфекции верхних дыхательных путей.
Для цитирования: Рязанцев С.В., Сапова К.И. Высокодозовые фторхинолоны в лечении острого синусита. РМЖ. 2017;23:1734-1738.
High-dose fluoroquinolones in the treatment of acute sinusitis
Ryazantsev S. V., Sapova K.I.
Saint Petersburg Research Institute of Ear, Throat, Nose and Speech
Key words: antibacterial drugs, levofloxacin, Levolet ® R, upper respiratory tract infections.
For citation: Ryazantsev S. V., Sapova K.I. High-dose fluoroquinolones in the treatment of acute sinusitis // RMJ. 2017. № 23. P. 1734–1738.
Статья посвящена возможностям использования высокодозовых фторхинолонов в лечении инфекции верхних дыхательных путей - острого синусита. Анализируются преимущества и недостатки различных классов антибактериальных препаратов, в частности эффективность и безопасность препарата левофлоксацина (Леволет Р)
В последние годы появилось значительное количество публикаций, посвященных анализу результатов лечения инфекционно-воспалительной патологии верхних дыхательных путей (ВДП) респираторными фторхинолонами.
Респираторными фторхинолонами называют группу антибиотиков, используемых для лечения заболеваний дыхательных путей. Данный класс антимикробных препаратов был разработан на основе классических фторхинолоновых средств, но обладает неоспоримыми преимуществами перед своими предшественниками – это повышенная активность в отношении Streptococcus pneumoniae, основного возбудителя респираторных инфекций, а также существенная активность в отношении Mycoplasma pneumoniae и Chlamydophila pneumoniae. Так, классический фторхинолоновый антибиотик ципрофлоксацин в настоящее время обладает крайне низкой активностью в отношении S. pneumoniae [1].
На данный момент группа фторхинолонов в России пополнилась новым аналогом левофлоксацина – препаратом Леволет ® Р производства компании Dr. Reddy’s.
По химической структуре Леволет ® Р является фторхинолоном ІІІ поколения и представляет собой оптически активный левовращающий изомер офлоксацина. В химической структуре левофлоксацина существенную роль играют две основные группы: 4-метилпиперазинильная кислота, обусловливающая усиление всасывания при приеме препарата внутрь, повышение его активности в отношении грамотрицательных бактерий, удлинение периода полувыведения, и оксазиновое кольцо, обусловливающее расширение спектра активности в отношении грамположительных бактерий, а также удлинение периода полувыведения. Левофлоксацин характеризуется в 2 раза большей активностью, чем офлоксацин [2].
Леволет ® Р (левофлоксацин) – фторхинолон, противомикробное бактерицидное средство широкого спектра действия. Левофлоксацин активен в отношении большинства штаммов микроорганизмов in vitro и in vivo. Антибактериальный эффект этого препарата обеспечивает блок ДНК-гиразы (топоизомеразы II) и топоизомеразы IV, что приводит к нарушению суперспирализации и сшивки разрывов ДНК с последующим прекращением ее синтеза. В связи с тем что возбудители инфекционно-воспалительных заболеваний ВДП высокочувствительны к левофлоксацину, а также принимая во внимание характерные для фторхинолонов быструю всасываемость при приеме внутрь и способность хорошо проникать в слизистую оболочку респираторного эпителия, вовлеченного в воспалительный процесс, левофлоксацин наряду с другими фторхинолонами включен в первую линию терапии у больных острым риносинуситом (ОРС) [3].
Данные исследований
Выбор курса терапии
Заключение
Исходя из результатов вышеприведенных исследований можно сделать следующие выводы.
1. Леволет ® Р по своим свойствам является эффективным при лечении больных c острыми заболеваниями и обострением хронических заболеваний ВДП. Его эффективность составляет 93,8–100%.
2. Левофлоксацин хорошо переносится больными и обладает минимальными побочными эффектами (6,3%), что свидетельствует о терапевтической ценности препарата Леволет ® Р.
3. Доказана эффективность препарата Леволет ® Р (левофлоксацина) по сравнению с другими классами антибактериальных препаратов, используемых в лечении острых заболеваний и обострений хронических заболеваний ВДП.
4. Длительность пребывания препарата в организме делает возможным его прием 1 р./сут в дозировке 750 мг на протяжении 5 дней.
1. Козлов Р.С., Сивая О.В., Кречикова О.И. Динамика резистентности Streptococcus pneumoniae к антибиотикам в России за период 1999–2009 гг. // Клиническая микробиология и антимикробная химиотерапия. 2010. № 12(4). С. 329–341 [Kozlov R.S., Sivaja O.V., Krechikova O.I. Dinamika rezistentnosti Streptococcus pneumoniae k antibiotikam v Rossii za period 1999–2009 gg. // Klinicheskaja mikrobiologija i antimikrobnaja himioterapija. 2010. № 12(4). S. 329–341 (in Russian)].
2. Горпинченко И.И. Изучение эффективности использования препарата Леволет (левофлоксацин) у больных острым риносинуситом // Здоровье Украины. 2011. № 2. С. 137–140 [Gorpinchenko I.I. Izuchenie jeffektivnosti ispol'zovanija preparata Levolet (levofloksacin) u bol'nyh ostrym rinosinusitom // Zdorov'e Ukrainy. 2011. № 2. S. 137–140 (in Russian)].
3. Корнеев И.А. Применение препарата Леволет Р у пациентов с острым риносинуситом в реальной клинической практике // Эффективная фармакотерапия. 2014. Т. 5. С. 28–30 [Korneev I.A. Primenenie preparata Levolet R u pacientov s ostrym rinosinusitom v real'noj klinicheskoj praktike // Jeffektivnaja farmakoterapija. 2014. T. 5. S. 28–30 (in Russian)].
4. Лещенко С.И. Применение левофлоксацина в практике пульмонолога // Український пульмонологічний журнал. 2009. Т. 4. С. 54–57 [Leshhenko S.I. Primenenie levofloksacina v praktike pul'monologa // Ukraїns'kij pul'monologіchnij zhurnal. 2009. T. 4. S. 54–57 (in Russian)].
5. Анготоева И.Б. Эффективность и безопасность препарата Леволет для пациентов с острым бактериальным риносинуситом и обострением хронического гнойного риносинусита // Фарматека. 2011. № 10. С. 60–64 [Angotoeva I. B. Jeffektivnost' i bezopasnost' preparata Levolet dlja pacientov s ostrym bakterial'nym rinosinusitom i obostreniem hronicheskogo gnojnogo rinosinusita // Farmateka. 2011. № 10. S. 60–64 (in Russian)].
6. Крюков А.И., Кунельская Н.Л., Гуров А.В. и др. Исследование эффективности и безопасности левофлоксацина и амоксициллина клавуланата у больных острым бактериальным синуситом // Медицинский Совет. 2014. № (15). С. 6–9. doi:10.21518/2079-701X-2014-15-6-9 [Krjukov A.I., Kunel'skaja N.L., Gurov A.V. i dr. Issledovanie jeffektivnosti i bezopasnosti levofloksacina i amoksicillina klavulanata u bol'nyh ostrym bakterial'nym sinusitom // Medicinskij Sovet. 2014. № (15). S. 6–9. doi:10.21518/2079-701X-2014-15-6-9 (in Russian)].
7. Maezawa K., Yajima R., Terajima T. et al. Dissolution profile of 24 levofloxacin (100 mg) tablets // Journal of Infections. 2013. Vol. 19(5). P. 996–998.
8. Белоусов Ю.Б., Зырянов С.К., Камаев А.В. Эффективность применения левофлоксацина – слагаемые успеха // Клиническая микробиологическая и антимикробная химиотерапия. 2012. Т. 14. № 1. С. 34–37 [Belousov Ju.B., Zyrjanov S.K., Kamaev A.V. Jeffektivnost' primenenija levofloksacina – slagaemye uspeha // Klinicheskaja mikrobiologicheskaja i antimikrobnaja himioterapija. 2012. T. 14. № 1. S. 34–37 (in Russian)].
9. Пальчун В.Т., Кафарская Л.И., Кунельская Н.Л. и др. Анализ эффективности различных антибактериальных препаратов при остром экссудативном гаймороэтмоидите // Лечебное дело. 2010. № 3. С. 44–48 [Pal'chun V.T., Kafarskaja L.I., Kunel'skaja N.L., i dr. Analiz jeffektivnosti razlichnyh antibakterial'nyh preparatov pri ostrom jekssudativnom gajmorojetmoidite // Lechebnoe delo. 2010. № 3. S. 44–48 (in Russian)].
10. Zhang Z.C., Jin F.S., Liu D.M. et al. Safety and efficacy of levofloxacin for the treatment of chronic polyposis rhynosinusitis in European patients // European Journal of Otorhynolaryngology. 2012. Vol. 14(6). P. 870–874.
11. Michael Poole. A Trial of High-Dose, Short-Course Levofloxacin for the Treatment of Acute Bacterial Sinusitis // Otolaryngology – Head and Neck Surgery. 2006. №134. P. 10–17.
12. Paglia M., Peterson J., Fisher A.C. et al. Safety and efficacy with levofloxacin 500 mg for 4 weeks in treating chronic respiratory tract infections // Curr. Med. Res Opin. 2010. Vol. 26(6). P. 1433–1441.
Антибактериальные препараты из группы фторхинолонов занимают одно из ведущих мест в лечении различных бактериальных инфекций, в том числе в амбулаторных условиях. Однако столь популярные в настоящее время ципрофлоксацин, офлоксацин, ломефлоксацин
Антибактериальные препараты из группы фторхинолонов занимают одно из ведущих мест в лечении различных бактериальных инфекций, в том числе в амбулаторных условиях. Однако столь популярные в настоящее время ципрофлоксацин, офлоксацин, ломефлоксацин, пефлоксацин обладают высокой активностью в отношении грамотрицательных возбудителей, умеренной активностью против атипичных возбудителей и малоактивны в отношении пневмококков и стрептококков, что значительно ограничивает их применение, особенно при респираторных инфекциях.
В последнее десятилетие в клиническую практику стали входить новые препараты из этой группы — т. наз. новые фторхинолоны, которые сохраняют высокую активность против грамотрицательных возбудителей, свойственную их предшественникам, и при этом значительно более активны против грамположительных и атипичных микроорганизмов. Одним из таких препаратов является левофлоксацин (таваник). По химической структуре он представляет собой левовращающий изомер офлоксацина. Широкий спектр антибактериальной активности, высокая безопасность, удобные фармакокинетические свойства обусловливают возможность его широкого применения при различных инфекциях.
Механизм действия
Левофлоксацин обладает быстрым бактерицидным действием, поскольку проникает внутрь микробной клетки и подавляет, так же как и фторхинолоны первого поколения, ДНК-гиразу (топоизомеразу II) бактерий, что нарушает процесс образования бактериальной ДНК. Ферменты клеток человека не чувствительны к фторхинолонам, и последние не оказывают токсического действия на клетки макроорганизма. В отличие от препаратов прежнего поколения новые фторхинолоны ингибируют не только ДНК-гиразу, но и второй фермент, ответственный за синтез ДНК, — топоизомеразу IV, выделенную у некоторых микроорганизмов, прежде всего грамположительных. Считается, что именно воздействием на этот фермент объясняется высокая антипневмококковая и антистафилококковая активность новых фторхинолонов.
Левофлоксацин обладает клинически значимым дозозависимым постантибиотическим эффектом, достоверно более длительным по сравнению с ципрофлоксацином, а также длительным (2-3 часа) субингибирующим действием.
Под действием левофлоксацина отмечено повышение функции полиморфноядерных лимфоцитов у здоровых добровольцев и ВИЧ-инфицированных пациентов. Показано его иммуномодулирующее воздействие на тонзиллярные лимфоциты у больных хроническим тонзиллитом. Полученные данные позволяют говорить не только об антибактериальной активности, но и о синергическом противовоспалительном и антиаллергическом действии левофлоксацина.
Спектр антимикробной активности
Левофлоксацин характеризуется широким антимикробным спектром, включающим грамположительные и грамотрицательные микроорганизмы, в том числе внутриклеточные возбудители (табл. 1).
При сравнении эффективности различных антибактериальных препаратов в отношении возбудителей респираторных инфекций было выявлено, что левофлоксацин в отношении противомикробной активности превосходит остальные препараты. К нему оказались чувствительны все штаммы пневмококка, в том числе пенициллинрезистентные, при сравнительно более низкой чувствительности пневмококков к препаратам сравнения: офлоксацин — 92%, ципрофлоксацин — 82%, кларитромицин — 96%, азитромицин — 94%, амоксициллин/клавуланат — 96%, цефуроксим — 80%. К левофлоксацину оказались также чувствительны все штаммы моракселлы катаралис, гемофильной палочки и метициллин чувствительного золотистого стафилококка, 95% штаммов клебсиеллы пневмонии.
Резистентность
Возможность широкого клинического использования левофлоксацина и других новых фторхинолонов заставляет задуматься об опасности развития резистентности к ним. Хромосомные мутации являются основным механизмом, обеспечивающим устойчивость микробов к фторхинолонам. При этом происходит постепенное накопление мутаций в одном или двух генах и ступенчатое снижение чувствительности. Развитие клинически значимой резистентности пневмококков к левофлоксацину наблюдается после трех мутаций, а следовательно, представляется маловероятным. Это подтверждается и экспериментальными данными: левофлоксацин вызывал спонтанные мутации в 100 раз реже, чем ципрофлоксацин, независимо от чувствительности тестируемых штаммов пневмококка к пенициллину и макролидам. Широкое использование препарата в последние годы в США и Японии не привело к росту резистентности к нему. По данным K. Yamaguchi et al., 1999, чувствительность бактерий к левофлоксацину за пять лет, т. е. с момента начала его широкого применения, не изменилась и превышает 90% как для грамотрицательных, так и для грамположительных возбудителей.
Больший риск развития антибиотикорезистентности связан не с пневмококками, а с грамотрицательными бактериями. В то же время, по некоторым данным, применение левофлоксацина в отделениях интенсивной терапии не сопровождается значимым ростом резистентности грамотрицательной кишечной флоры.
Фармакокинетика
Левофлоксацин хорошо всасывается в желудочно-кишечном тракте. Его биодоступность составляет 99% и более. Так как левофлоксацин почти не подвергается метаболизму в печени, это способствует быстрому достижению максимальной его концентрации в крови (значительно более высокой, чем у ципрофлоксацина). Так, при назначении добровольцам стандартной дозы фторхинолона значения его максимальной концентрации в крови при приеме левофлоксацина составляли 2,48 мкг/мл/70 кг, ципрофлоксацина — 1,2 мкг/мл/70 кг.
После приема разовой дозы левофлоксацина (500 мг) его максимальная концентрация в крови, равная 5,1 ± 0,8 мкг/мл, достигается через 1,3-1,6 часа, при этом бактерицидная активность крови против пневмококков сохраняется до 6,3 часа независимо от их чувствительности к пенициллинам и цефалоспоринам. Более длительное время, до 24 часов, сохраняется бактерицидное действие крови на грамотрицательные бактерии семейства Enterobacteriacae.
Период полувыведения левофлоксацина составляет 6-7,3 часа. Около 87% принятой дозы препарата выделяется с мочой в неизмененном виде в течение последующих 48 часов.
Левофлоксацин быстро проникает в ткани, при этом уровни тканевых концентраций препарата выше, чем в крови. Особенно высокие концентрации устанавливаются в тканях и жидкостях респираторного тракта: альвеолярных макрофагах, слизистой бронхов, бронхиальном секрете. Левофлоксацин также достигает высоких концентраций внутри клеток.
Длительный период полувыведения, достижение высоких тканевых и внутриклеточных концентраций, а также наличие постантибиотического действия — все это позволяет назначать левофлоксацин один раз в сутки.
Лекарственные взаимодействия
Биодоступность левофлоксацина снижается при одновременном приеме с антацидами, сукральфатом, препаратами, содержащими соли железа. Интервал между приемом этих лекарственных средств и левофлоксацина должен составлять не менее 2 часов. Других клинически значимых взаимодействий левофлоксацина выявлено не было.
Клиническая эффективность
Существует много публикаций, посвященных результатам клинических исследований эффективности применения левофлоксацина. Ниже представлены наиболее значимых из них.
В многоцентровом рандомизированном исследовании, включившем 590 пациентов, сравнивалась эффективность и безопасность двух режимов лечения: левофлоксацина в/в и/или перорально в дозе 500 мг в сутки и цефтриаксона в/в 2,0 г в сутки; и/или цефуроксима перорально 500 мг два раза в сутки в комбинации с эритромицином или доксициклином у больных с внебольничной пневмонией. Длительность терапии 7–14 дней. Клиническая эффективность составила 96% в группе левофлоксацина и 90% в группе, получавшей цефалоспорины. Эрадикация возбудителей была достигнута соответственно у 98 и 85% больных. Частота нежелательных действий в группе левофлоксацина составляла 5,8%, а в группе сравнения 8,5%.
В другом большом рандомизированном исследовании сравнивалась эффективность лечения больных с тяжелой пневмонией левофлоксацином 1000 мг в сутки и цефтриаксоном — 4 г в сутки. Первые дни левофлоксацин назначили в/в, затем перорально. Результаты лечения в обеих группах оказались сопоставимы, но в группе цефтриаксона наблюдалась достоверно более частая смена антибиотика в первые дни лечения — из-за недостаточного клинического эффекта.
Сопоставимые результаты были получены и при сравнении групп пациентов, получавших лечение левофлоксацином и коамоксиклавом.
Эффективность монотерапии левофлоксацином изучалась у более чем 1000 пациентов с внебольничной пневмонией. Клиническая и бактериологическая эффективность составляли здесь 94 и 96% соответственно.
Фармакоэкономические исследования показали, что общие затраты на лечение пациентов левофлоксацином и комбинацией цефалоспорина и макролида сопоставимы или даже несколько ниже в группе левофлоксацина.
У пациентов с обострением хронического бронхита сравнивалась эффективность лечения левофлоксацином в дозе 500 мг в сутки перорально и цефуроксимом аксетила внутрь 500 мг два раза в сутки. При этом клиническая и бактериологическая эффективность не различалась в зависимости от групп и составляла 77–97%.
Таким образом, в настоящее время можно считать доказанной высокую эффективность левофлоксацина при респираторных инфекциях нижних дыхательных путей. Результаты проведенных исследований позволили включить левофлоксацин как препарат первого ряда или альтернативный в схему лечения пациентов с внебольничной пневмонией и обострениями хронического бронхита (табл. 2).
Среди возбудителей урологических инфекций наблюдается рост резистентности к широко используемым антибактериальным препаратам. Так, за период с 1992 по 1996 год отмечено увеличение устойчивости E. Coli и S. saprophyticus к котримоксазолу — на 8–16% и к ампициллину — на 20%. Устойчивость к ципрофлоксацину, нитрофуранам и гентамицину возрасла за этот же период на 2%. Применение левофлоксацина у пациентов с осложненными мочевыми инфекциями в дозе 250 мг в сутки оказалось эффективным у 86,7% пациентов.
Выше приводились фармакокинетические показатели высокого содержания левофлоксацина в тканях. Это наряду с антимикробным спектром препарата послужило основанием для его использования с целью профилактики инфекционных осложнений при эндоскопических методах лечения и диагностики, например при ретроградной холангиопанкреатографии и для периоперационной профилактики в ортопедии.
Применение левофлоксацина в этих ситуациях представляется перспективным и требует дальнейшего изучения.
Безопасность
Левофлоксацин считается одним из самых безопасных антибактериальных препаратов. Однако при его назначении существует ряд ограничений.
У пациентов с нарушением функции печени корригировать дозу препарата не нужно, но нарушение функции почек при снижении клиренса креатинина (менее 50 мл/мин) требует уменьшения дозы препарата. Дополнительный прием левофлоксацина после проведения гемодиализа или амбулаторного перитониального диализа не требуется.
Левофлоксацин не применяется у беременных и кормящих женщин, у детей и подростков. Препарат противопоказан пациентам, у которых в анамнезе имеются нежелательные реакции на лечение фторхинолонами.
У больных пожилого и старческого возраста при приеме левофлоксацина не выявлено повышенного риска развития нежелательных побочных реакций и не требуется коррекции доз.
Контролируемые клинические исследования показали, что побочные реакции при применении левофлоксацина возникают редко и большей частью не являются серьезными. Существует зависимость между дозой препарата и частотой развития НД: при суточной дозе 250 мг их частота не превышает 4,0–4,3%, при дозе 500 мг/ сут. — 5,3–26,9%, при дозе 1000 мг/сут. — 22–28,8%. Наиболее часто наблюдались симптомы желудочно-кишечной диспепсии — тошнота и диарея (1,1–2,8%). При внутривенном введении возможно покраснение места инъекции, иногда наблюдается развитие флебитов (1%).
Дозирование
Левофлоксацин выпускается в двух формах: для внутривенного введения и приема внутрь. Применяется по 250-500 мг один раз в сутки, при тяжелых инфекциях возможно назначение по 500 мг два раза в сутки. При внебольничной пневмонии длительность лечения составляет 10-14 дней, при обострении хронического бронхита — 5-7 дней.
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказыва
 |
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказывается недостаточно. Фактор удобства приема препарата и, что особенно непривычно для нашего понимания, вопросы цены и стоимости лечения в условиях серьезного ограничения финансирования здравоохранения часто могут оказаться определяющими. На приобретение лекарственных средств лечебные учреждения тратят 15–20% своего бюджета, причем 50–60% этих расходов приходится на долю антибактериальных препаратов, что заставляет пересмотреть существующие и искать новые подходы к их применению.
ЦА занимают одно из важных мест в лечении инфекций верхних и нижних дыхательных путей. Наиболее ответственным этапом в антибактериальной терапии данной категории пациентов является выбор первоначального препарата. От адекватности выбора зависит эффективность и безопасность лечения, а также его комфортность, переносимость, стоимость, эпидемиологическая ситуация.
Анализ имеющихся данных об использовании ЦА в России за 1997–1998 гг. позволяет выявить предпочтения врачами того или иного препарата (группы препаратов) и определенных методов его введения. Как видно из рис. 1, при назначении цефалоспориновых антибиотиков подавляющее большинство врачей выбирают парентеральные препараты.
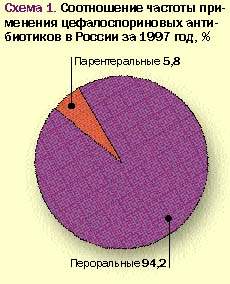 |
Данный факт лишь подтверждает, что в нашей стране пероральные лекарственные средства, и особенно пероральные цефалоспорины, очень мало популярны и практически не используются. Такое отношение к таблетированным формам отражает некоторый консерватизм практических врачей, связанный с тем, что еще 15-20 лет назад существовавшие тогда пероральные средства не выдерживали сравнения с парентеральными препаратами ни по эффективности терапии, ни по ее переносимости. Лишь последние десятилетия с момента создания первого перорального цефалоспорина — цефалексина и появления новых пероральных бактерицидных препаратов эта лекарственная форма несколько укрепила свои позиции не только в амбулаторной, но и в стационарной практике. Однако радикально на положении дел это не сказалось.
Очевидно, что такая форма назначения препаратов имеет безусловные преимущества. Это проявляется и в возможности амбулаторного ведения больного, и в удобстве приема препарата, и в снижении риска постинъекционных осложнений и длительности пребывания в стационаре, и даже в избавлении от психологического дискомфорта, связанного с инъекциями.
Наличие антибактериальных препаратов в двух формах — для парентерального и перорального применения — делает возможным их использование для проведения так называемой ступенчатой терапии. Суть такого лечения состоит в назначении внутривенного или внутримышечного препарата и в последующем, через двое-трое суток после достижения клинического эффекта, переводе на пероральный прием. Возможность проведения ступенчатой терапии одним и тем же препаратом является существенным преимуществом данного лекарственного средства перед его аналогами. Ступенчатая терапия предоставляет клинические и экономические преимущества как пациенту, так и лечебному учреждению.
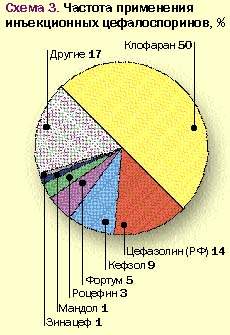
На основании приведенных данных трудно понять логику выбора цефалоспоринового антибиотика того или иного поколения и принципы, которыми руководствуется врач при назначении препарата. Анализ использования цефалоспориновых антибиотиков по поколениям (см. рис. 2 и 3) свидетельствует о предпочтительном назначении препаратов I и III поколений, причем из препаратов III поколения (61%) половина приходится на цефотаксим, а из препаратов I поколения большая часть приходится на цефазолин.
 |
Таким образом, ориентировочная этиология бронхолегочной инфекции служит основанием для выбора среди ЦА конкретного препарата (или поколения препаратов) с соответствующей антимикробной активностью.
При обострениях хронического бронхита особое значение приобретают препараты, высокоустойчивые к действию b-лактамаз, продуцируемых как грамотрицательными, так и грамположительными микроорганизмами (цефуроксим аксетил), и обладающие высокой активностью против Н.influenzae (цефтибутен).
 |
Общие принципы выбора первоначального ЦА сохраняются и у больных пневмонией на фоне тяжелых сопутствующих заболеваний (ХОЗЛ, сердечная недостаточность, сахарный диабет, алкогольная интоксикация и др.) и в возрасте старше 60 лет. Этиологическое значение в данной клинической ситуации приобретают Н.influenzae, S.аureus, некоторые грамотрицательные микроорганизмы (Е.соli, Сlebsiella), возрастает частота бета-лактамазопродуцирующих бактерий. В связи с этим возрастает значение препаратов, активных в отношении названных возбудителей. Известно, что противомикробное действие ЦА при переходе активности от первого поколения к последующим характеризуется снижением противостафилококковой активности и преобладанием активности против некоторых грамотрицательных микроорганизмов. Ценным свойством является устойчивость ЦА II поколения к b-лактамазам. В связи с этим врач должен ориентиро-ваться в данной ситуации на цефалоспорины II или по крайней мере III поколения.
| Цефалоспорины, открытые более 50 лет тому назад, продолжают занимать прочные позиции в лечении различных бактериальных заболеваний, несмотря на появление новых антимикробных средств. Цефалоспориновые антибиотики подразделяются на четыре поколения, отличающиеся по спектру действия, антибактериальной активности, стабильности в присутствии b-лактамаз, фармакокинетическому профилю. Все это наряду с многообразием лекарственных форм и стоимостью определяет их различные показания. Очевидно, что по мере появления новых поколений цефалоспориновых антибиотиков в клинической практике возникает немаловажная проблема дифференцированного назначения препарата с учетом свойств как самого антибиотика, так и особенностей инфекционно- воспалительного процесса у конкретного больного |
Таким образом, рациональный выбор первоначального ЦА для лечения инфекций верхних и нижних дыхательных путей определяется в первую очередь вероятностью этиологической роли того или иного микроорганизма в конкретной клинической ситуации. Такой подход требует от практического врача (а именно от него зависит адекватный выбор препарата) умения выявлять особенности каждого случая пневмонии (эпидемиологическую обстановку, фоновую патологию, факторы риска и др.) и ориентировки в антимикробном спектре назначаемого антибиотика. Однако в клинической практике при выборе ЦА, как, впрочем, и других антибиотиков, приходится наряду с ориентировочной этиологией бронхолегочной инфекции учитывать и другие факторы. Среди последних имеет значение фармакокинетика препарата, наличие разнообразных лекарственных форм, риск развития побочных эффектов, стоимость и др.
В настоящее время не окончательно определено место пероральных препаратов III поколения в клинической практике, так как их сравнительная клиническая и бактериологическая эффективность мало отличается от препаратов II поколения. Более того, как было сказано выше, преимущество цефалоспоринов III поколения состоит в их высокой активности в отношении b-лактамазопродуцирующих бактерий, наиболее часто вызывающих серьезные стационарные инфекции. Но поскольку в этом случае больные находятся в стационаре, то уже более обоснованно получают парентеральную терапию. В то же время ввиду сниженной активности в отношении грамположительных бактерий, часто являющихся причиной именно амбулаторной инфекции, назначение препаратов III поколения имеет меньше преимуществ перед препаратами II поколения.
Цель антибактериальной терапии состоит не только в достижении клинического эффекта, но и в полной эрадикации возбудителя, т. е. бактериологической эффективности. Это в основном определяется адекватным дозированием препарата для достижения необходимой концентрации в очаге инфекции. Высокая степень накопления препарата в тканях является необходимым требованием к лекарственному веществу.
ЦА первого поколения хуже проникают в ткани, что уменьшает степень бактериальной эрадикации.
Данные о биодоступности оральных ЦА следует иметь в виду при дифференцированном назначении их больным с сопутствующей патологией кишечника, связанной с нарушением всасывания, а также при одновременном приеме антисекреторных препаратов, антацидов, с учетом влияния пищи на всасывание ЦА.
Знание путей элиминации ЦА наряду с оценкой функционального состояния печени и почек (возраст, сопутствующая патология) также может определять выбор более адекватного для данной ситуации препарата. Выбирая ЦА для лечения тяжелых госпитальных пневмоний, например, у новорожденных и стариков или у больных с патологией почек, при наличии почечной недостаточности предпочтение следует отдать цефоперазону с учетом его преимущественно билиарной экскреции.
При дифференцированном выборе ЦА необходимо учитывать риск развития побочных эффектов. Наиболее типичны реакции гиперчувствительности (лихорадка, кожная сыпь), гематологические синдромы (цитопения, эозинофилия), нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея), печени (повышение активности трансаминаз), почек (повышение уровня креатинина), ЦНС (головная боль), флебиты при внутривенном введении. Поэтому анамнестические и клинико-лабораторные данные о наличии у больных какой-либо патологии должны влиять на выбор соответствующего препарата.
Флебиты часто возникают при введении цефалотина, цефотаксима, цефепима. Цефуроксим, цефоперазон, цефтибутен могут вызывать анемию (чаще гемолитическую), а при назначении цефалотина, цефамандола, цефотаксима, цефтазидима иногда выявляются фиксированные на эритроцитах антитела. Повышение активности печеночных ферментов возможно на фоне лечения цефоперазоном, цефтриаксоном, цефтазидимом, цефуроксимом. Уровень креатинина может повышаться при лечении цефалексином и цефподоксимом. Оральные цефалоспорины чаще всего вызывают нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея). При лечении парентеральными ЦА отмечено увеличение протромбинового времени, за исключением цефтазидима, не влияющего на синтез факторов протромбинового комплекса и показатели свертываемости крови. Возможны реакции гиперчувствительности (кожная сыпь, лихорадка, эозинофилия) на фоне применения почти всех ЦА III поколения.
Таким образом, дифференцированный выбор ЦА для лечения инфекций верхних и нижних дыхательных путей должен базироваться на учете и адекватной оценке многих факторов, включающих как особенности клинической ситуации, так и антимикробную активность и фармакокинетические характеристики назначаемого препарата.
Для цитирования: Цой А.Н., Архипов В.В. Место левофлоксацина в фармакотерапии внебольничной пневмонии. РМЖ. 2003;4:164.
ММА имени И.М. Сеченова
П о существующим оценкам, в нашей стране ежегодно отмечается 1,5 млн. случаев пневмонии [1], что позволяет рассматривать это заболевание, как одно из наиболее проблемных для отечественного здравоохранения. Необходимость регулярного обращения к теме фармакотерапии внебольничной пневмонии (ВП) можно объяснить, по крайней мере, двумя причинами – изменениями спектра и резистентности возбудителей ВП и появлением в клинической практике новых антибактериальных препаратов (АБП).
В частности, в последние годы отмечается снижение чувствительности основного возбудителя ВП – S.pneumoniae к АБП, часто применявшимся в рутинной практике. Так, по данным исследования ПеГаС–1, доля пневмококка, резистентного к тетрациклину и ко–тримоксазолу, составляет соответственно 34% и 38%. Примерно 4% штаммов этого микроорганизма резистентны к макролидам (в том числе к азитромицину). Наибольшую тревогу вызывает рост устойчивости этого возбудителя к пенициллину (и одновременно снижение эффективности других b –лактамов) – 7,5% у детей и до 9% у взрослых, причем максимальный уровень резистентности к пенициллину (до 20% в некоторых стационарах) наблюдается в Москве и крупных городах [2].
С другой стороны, фармакотерапия ВП в нашей стране по–прежнему далека от оптимальной. По данным крупного (778 амбулаторных больных в 7 городах России, включая Москву и Санкт–Петербург) фармакоэпидемиологического исследования [3], врачи общей практики при лечении ВП наиболее часто применяют гентамицин (29,3%), ко–тримоксазол (22,7%), ампициллин (20,3%) и ципрофлоксацин (17,2%).
При этом наиболее перспективным препаратам для амбулаторной терапии респираторных инфекций – респираторным фторхинолонам – вообще не нашлось места в числе назначений.
Между тем с середины 90–х годов респираторные фторхинолоны (левофлоксацин, спарфлоксацин) заняли прочное место в алгоритмах выбора АБП, построенных на принципах доказательной медицины (рекомендации Общества инфекционных болезней, США, 1998 [4]; Руководство Американского торакального общества, 2001 [5]; рекомендации Британского торакального общества, 2001 [6]). В качестве примера можно указать на значительный рост использования фторхинолонов в США (рис. 1), где с конца 90–х годов эти АБП применяются в клинической практике значительно чаще, чем цефалоспорины III поколения и аминогликозиды.
Рис. 1. Тенденции в применении АБП в США (1989-99 гг.) [7]
-
респираторные фторхинолоны – препараты широкого спектра, потенциально активные по отношению ко всем наиболее часто встречающимся возбудителям ВП (см. табл. 1) – грамположительным микроорганизмам (пневмококки, стафилококки), большинству грамотрицательных и внутриклеточных возбудителей, а также микобактериям туберкулеза и некоторым анаэробам;
Рис. 2. Динамика резистентности S.pneumoniae к фторхинолонам (данные Cross-Canada Surveillance Study)
Но наряду с этим приходиться констатировать, что стоимость респираторных фторхинолонов существенно выше стоимости АБП, применяемых в рутинной практике, кроме того, сохраняется запрет на использование препаратов этой группы для лечения детей и беременных.
Фармакокинетика/фармакодинамика левофлоксацина
Левофлоксацин практически полностью всасывается в кишечнике (биодоступность при приеме внутрь 99%). Период его полувыведения – 6–8 часов, что позволяет применять левофлоксацин 1 раз в день (суточная доза – 500 мг). Равновесная концентрация в плазме при приеме 1 раз в сутки устанавливается через 48 часов после начала лечения. Препарат хорошо проникает в ткани (объем распределения – 89–112 л), после его однократного приема концентрация в ткани легкого в 2–5 раз превышает концентрацию в крови [9]. В жидкости на поверхности эпителия нижних дыхательных путей левофлоксацин накапливается в концентрации в 12 раз большей, чем минимальная ингибирующая концентрация (МИК) для S.pneumoniae (см. рис. 3).
Рис. 3. Отношение концентрации фторхинолонов в жидкости на поверхности эпителия бронхов к величине МИК для S.pneumoniae [9]
В целом фармакокинетические параметры левофлоксацина не уступают аналогичным показателям других фторхинолонов III–IV поколения – гатифлоксацина и моксифлоксацина.
Для оценки фармакодинамики и эффективности фторхинолонов решающее значение имеет отношение величины площади под фармакокинетической кривой (AUC) к величине минимальной ингибирующей концентрации МИК90% возбудителя (рис. 4) [10]. Эффекта от применения препаратов следует ожидать только в том случае, когда величина AUC/МИК90%
Рис. 4. Соотношение фармакокинетических (Сmax, AUC24) и фармакодинамических (МИК90%) параметров, определяющих эффективность фторхинолонов [10]
Следует отметить, что левофлоксацин эффективен в отношении большинства возбудителей респираторной инфекции, хотя в отношении S.pneumoniae его прогнозируемая эффективность меньше, чем у фторхинолонов IV поколения.
Кроме того, благодаря высокой концентрации в крови левофлоксацин демонстрирует очень высокую эффективность у больных с бактериемией. Спектр антимикробного действия левофлоксацина представлен в таблице 2.
Клинические исследования левофлоксацина
В крупном многоцентровом рандомизированном клиническом исследовании (РКИ) [12] у 590 больных ВП оценивалась эффективность в/в введения и перорального приема левофлоксацина по сравнению с цефалоспоринами III поколения (цефтриаксон ВВ и цефуроксим внутрь). Эрадикация возбудителей при применении левофлоксацина была достигнута в 98% случаев (при использовании цефалоспоринов – 85%). Исследуемые препараты не отличались по эффективности в отношении пневмококка, однако левофлоксацин оказался более эффективным у больных с H.influenzae и атипичными возбудителями (табл. 3).
В крупном многоцентровом рандомизированном клиническом исследовании (РКИ) [12] у 590 больных ВП оценивалась эффективность в/в введения и перорального приема левофлоксацина по сравнению с цефалоспоринами III поколения (цефтриаксон ВВ и цефуроксим внутрь). Эрадикация возбудителей при применении левофлоксацина была достигнута в 98% случаев (при использовании цефалоспоринов – 85%). Исследуемые препараты не отличались по эффективности в отношении пневмококка, однако левофлоксацин оказался более эффективным у больных с и атипичными возбудителями (табл. 3).
В другом исследовании у госпитализированных больных с ВП (умеренное и тяжелое течение пневмонии) [13] левофлоксацин (500 мг в/в 2 раза в день) и цефтриаксон (4,0 г ВВ 1 раз в день) продемонстрировали одинаковую микробиологическую эффективность (эрадикация возбудителей в 83% при применении обоих АБП).
В одном из последних исследований (2002) левофлоксацин при в/в применении у больных с тяжелой ВП, получавших лечение в условиях стационара, сравнивался с комбинированной в/в терапией азитромицином и цефтриаксоном ( Сочетание цефалоспоринов III поколения и макролидов поддерживается рекомендациями по терапии ВП, опубликованными Американским торакальным обществом и Европейским пульмонологическим обществом, и является одним из стандартов терапии тяжелой пневмонии в условиях стационара. ) в/в [14]. Результаты этого исследования (всего 236 больных) оказались несколько неожиданными, так как монотерапия левофлоксацином оказалась по меньшей мере столь же эффективной ( В группах, получавших левофлоксацин и кларитромицин/цефтриаксон, клиническая эффективность оценивалась, как 94,1% и 92,3%, а микробиологическая эффективность - 89,5% и 92,3% соответственно. 3 ) , что и комбинированное лечение, кроме того, левофлоксацин лучше переносился больными.
От современных макролидов (кларитромицин) левофлоксацин статистически значимо не отличался как по клинической, так и по микробиологической эффективности [15].
По результатам одного из РКИ [16] левофлоксацин и гатифлоксацин обладают одинаковой эффективностью при лечении ВП легкой и средней тяжести, однако при терапии ВП тяжелого течения гатифлоксацин был несколько более эффективным (табл. 4).
В целом мета–анализ 5 крупных РКИ (1067 больных ВП) показал, что эффективность левофлоксацина при пневмонии составляет 83–100% (для препаратов сравнения – 90–95%) [17].
Основной нежелательной лекарственной реакцией (НЛР) левофлоксацина является его проаритмогенное действие, проявляющееся удлинением интервала QT на ЭКГ (в среднем, по данным РКИ, на 5 мс). Однако в этом отношении левофлоксацин представляется более безопасным, чем спарфлоксацин (аналогичная величина 13–15 мс) или эритромицин (8–15 мс). По общей частоте НЛР и частоте отмены препарата вследствие НЛР (рис. 5,6) левофлоксацин является одним из наиболее безопасных фторхинолонов [18,19].
Рис. 5. Частота НЛР при приеме фторхинолонов (%) [18,19]
Рис. 6. Необходимость отмены фторхинолонов из-за развития НЛР (%) [18,19]
Зарубежные рекомендации по применению левофлоксацина
Респираторные хинолоны рассматриваются целым рядом авторов в качестве препаратов выбора для лечения пневмонии, вызванной пенициллинрезистентными штаммами пневмококка (ПРП) [20–23]. Администрация пищевых продуктов и лекарственных средств США (FDA) одобрила левофлоксацин в качестве средства для терапии респираторных инфекций, вызванных ПРП, при этом учитывались суммарные данные 8–ми РКИ, в которых приняли участие более 3900 больных [24]. Из этого большого количества больных ПРП был возбудителем пневмонии в 18 случаях, а эффективность левофлоксацина удалось оценить только у 15 больных. Во всех этих случаях левофлоксацин оказался клинически эффективным.
Респираторные хинолоны рассматриваются целым рядом авторов в качестве препаратов выбора для лечения пневмонии, вызванной пенициллинрезистентными штаммами пневмококка (ПРП) [20–23]. Администрация пищевых продуктов и лекарственных средств США (FDA) одобрила левофлоксацин в качестве средства для терапии респираторных инфекций, вызванных ПРП, при этом учитывались суммарные данные 8–ми РКИ, в которых приняли участие более 3900 больных [24]. Из этого большого количества больных ПРП был возбудителем пневмонии в 18 случаях, а эффективность левофлоксацина удалось оценить только у 15 больных. Во всех этих случаях левофлоксацин оказался клинически эффективным.
Наиболее широкие показания к применению левофлоксацина и препарата IV поколения – моксифлоксацина существуют в США [25], где доля пенициллинустойчивых штаммов пневмококка составляет от 17,9% до 33,8% для различных штатов (2001 г.). Согласно этим рекомендациям (см. табл. 5) левофлоксацин является препаратом второго ряда для больных пневмонией легкого течения, не требующих госпитализации, и госпитализированных пациентов без тяжелых сопутствующих заболеваний. В остальных случаях левофлоксацин назначается в качестве препарата первой линии для эмпирической терапии, при этом прослеживается тенденция к его использованию в комбинации с цефтриаксоном4, что обеспечивает большую эффективность при терапии ВП тяжелого течения (см. табл. 6).
Специалисты из Великобритании, в которой уровень резистентности пневмококка до настоящего времени остается наиболее низким в Западной Европе (всего 6,7%; 2001 г.), отличаются более сдержанным подходом к назначению левофлоксацина [6]. В рекомендациях Британского торакального общества левофлоксацину5 отводится роль препарата второго ряда для лечения ВП в условиях стационара (при лечении ВП тяжелого течения его рекомендуется назначать в комбинации с пенициллином).
Исходя из вышесказанного, применение левофлоксацина в нашей стране оправдано ввиду его высокой эффективности и может эффективно использоваться при:
А) лечении ВП в амбулаторных условиях (прием левофлоксацина внутрь в виде монотерапии) –
- у больных при неэффективности первоначального лечения (пенициллины, макролиды, пероральные цефалоспорины и др.).
- у больных с высоким риском инфекции, вызванной резистентным пневмококком:
– возраст > 65 лет
– лечение b –лактамными антибиотиками в течение последних 3–х мес.
– иммуносупрессивные состояния, включая терапию глюкокортикостероидами
– тяжелые сочетанные заболевания [5].
Б) лечении ВП в стационаре –
При лечении ВП в стационаре левофлоксацин следует назначать в/в, рациональным представляется ступенчатый подход к лечению [8]: переход к пероральному назначению препарата после клинического улучшения состояния больного и микробиологической эрадикации возбудителя [6].
Комбинированное применение левофлоксацина с другими АБП:
- левофлоксацин в/в + цефалоспорины III поколения в/в – при лечении пневмонии, вызванной S.pneumoniae, устойчивым к пенициллину /МИК для пенициллина >2 мкг/мл/ и макролидам.
- левофлоксацин в/в + цефалоспорины III поколения в/в +/– аминогликозиды – у больных с бронхоэктазами и больных с тяжелым течением пневмонии (в условиях ОИТ).
1. Чучалин А.Г., Цой А.Н., Архипов В.В. с соавт. Пневмония с точки зрения доказательной медицины, М., 2000, с. 111.
2. Страчунский Л.С., Богданович Т.М. Состояние антибиотикорезистентности в России. В кн.: Антибактериальная терапия. Практическое руководство. Под редакцией Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова; Москва, 2000, с. 7–11.
3. Козлов С.Н., Рачина С.А., Домникова Н.П. с соавт., Фармакоэпидемиологический анализ лечения внебольничной пневмонии в амбулаторных условиях. Клиническая микробиология и антимикробная химиотерапия, 2000; Том. 2(3): с. 74–81.
4. Bartlett, JG, Breiman, RF, Mandell, LA, File, TM, Jr. Community–acquired pneumonia in adults: Guidelines for management. Guidelines from the Infectious Disease Society of America. Clin Infect Dis 1998; 26:811.
5. Guidelines for the Management of Adults with Community–acquired Pneumonia. Diagnosis, Assessment of Severity, Antimicrobial Therapy, and Prevention, Am J Respir Crit Care Med, 2001; Vol 163: 1730–1754
6. BTS Guidelines for the Management of CAP in adult, Thorax, 2001; 56 (sapi. 4).
1. Hooper D.C. Macrolides, Fluoroquinolones, and Aminoglycosides. Лекция, прочитанная в Massachusetts General Hospital 10 июля 2002.
8. Синопальников А.И., Дуганов В.К. Левофлоксацин: ступенчатая терапия внебольничной пневмонии у взрослых. РМЖ, 2001; том 9(15): с. 650–655.
9. Wise R, Honeybourne D: Pharmacokinetics and pharmacodynamics of fluoroquinolones in the respiratory tract. Eur Resp J, 1999; 14:221–229
10. Schentag J. and Tillotson G.S. Chest, 1997; 112(6 Suppl): 314–319.
11. Preston SL, Drusano GL, Berman AL, et al. Levofloxacin population pharmacokinetics and creation of a demographic model for prediction of individual drug clearance in patients with serious community–acquired infection. Antimicrob Agents Chemother 1998;42:1098–104
12. File TM et al. A multicenter, randomized study comparing the efficacy and safety of intravenous and/or oral levofloxacin versus ceftriaxone with community–acquired pneumonia 1997;41:1965–1972.
13. Norrby RS et al. A comparative study of levofloxacin and ceftriaxone in the treatment of hospitalized patients with pneumonia 1998;30:397–404.
14. Frank E, Liu J, Kinasewitz G, Moran GJ et. al. A multicenter, open–label, randomized comparison of levofloxacin and azithromycin plus ceftriaxone in hospitalized adults with moderate to severe community–acquired pneumonia. Clin Ther 2002 Aug;24(8):1292–308
15. Gotfried MH, Dattani D, Riffer E et. al. A controlled, double–blind, multicenter study comparing clarithromycin extended–release tablets and levofloxacin tablets in the treatment of community–acquired pneumonia. Clin Ther 2002 May;24(5):736–51
16. Sullivan JG et al. J Resp Dis 20(11 suppl):S49 (1999)
17. Bru JP. Update on the role of levofloxacin in the management of acute community–acquired pneumonia. Presse Med 2002 Jun 15;31(21 Pt 2):S19–22
18. Ball P, Mandell L, Niki Y, et al: Comparative tolerability of the newer fluoroquinolone antibacterials. Drug Saf 21:407–421, 1999
19. Breen J, Skuba K, Grasela D: Safety and tolerability of gatifloxacin, an advanced third–generation, 8–methoxy fluoroquinolone. J Respir Dis 20:S70–S76, 1999 (suppl 11).
20. Bartlett, JG, Breiman, RF, Mandell, LA, File, TM, Jr. Community–acquired pneumonia in adults: Guidelines for management. Guidelines from the Infectious Disease Society of America. Clin Infect Dis 1998; 26:811.
21. George, J, Morrissey, I. The bactericidal activity of levofloxacin compared with ofloxacin, D–ofloxacin, ciprofloxacin, sparfloxacin and cefotaxime against Streptococcus pneumoniae. J Antimicrob Chemother 1997; 39:719.
22. Klugman, KP, Gootz, TD. In–vitro and in–vivo activity of trovafloxacin against Streptococcus pneumoniae. J Antimicrob Chemother 1997; 39 Suppl B:51.
23. Hoogkamp–Korstanje, JA. In–vitro activities of ciprofloxacin, levofloxacin, lomefloxacin, ofloxacin, pefloxacin, sparfloxacin and trovafloxacin against gram–positive and gram–negative pathogens from respiratory tract infections. J Antimicrob Chemother 1997; 40:427.
24. From the Food and Drug Administration. First drug for penicillin–resistant community–acquired pneumonia. JAMA 2000; 283:1679.
25. Community–Acquired Pneumonia (CAP) Year 2002. Antibiotic Selection and Management Update. Evaluation, Risk Stratification, and Current Antimicrobial Treatment Guidelines for Hospital–Based Management of CAP: Outcome–Effective Strategies Based on New NCCLS Breakpoints and Recent Clinical Studies – The ASCAP Panel Consensus Report, 2002, CLINICAL UPDATE; MARCH 1, 2002
Читайте также:

