Чем обусловлена вирулентность дизентерийных бактерий
Обновлено: 26.04.2024
Этиология. С 1930 г. бациллы, выделяемые от больных дизентерией, официально были объединены в род Shigella, семейство Enterobacteriaceae. Идентификация шигелл осуществляется по их биохимическим и антигенным свойствам (О — антигенам), в соответствии с чем выделяют четыре группы шигелл (см. таблицу 1).
По своим морфологическим свойствам шигеллы представляют собой неподвижные, грамотрицательные бактерии. Общим и важнейшим свойством всех представителей рода Shigella является инвазивность, т. е. способность бактерий к инвазии в эпителиальные клетки кишечника с последующим размножением и паразитированием в них. Различные виды шигелл сильно отличаются по своим исходным биологическим свойствам, что, собственно, и определяет степень их вирулентности и патогенности для человека. Наиболее высокой вирулентностью обладают Sh. dysenteriae 1, что обусловлено прежде всего их способностью продуцировать один из мощнейших природных токсинов — Шига-токсин. Некоторые другие виды шигелл также способны продуцировать шига-подобные токсины, но с существенно более низкой активностью. Исключительно высокие вирулентные свойства Sh. dysenteriae 1 определяют крайне низкую инфицирующую дозу, которая составляет всего десятки или сотни микробных клеток. Для других видов шигелл инфицирующая доза определяется на один-два порядка выше.
Шигеллы относительно устойчивы к факторам внешней среды и способны длительно сохраняться на предметах домашнего обихода, в воде они сохраняют свою жизнеспособность до двух-трех недель, а в высушенном и замороженном состоянии — до нескольких месяцев. Высокие же температуры, наоборот, способствуют быстрой их гибели: при температуре +60°С — в течение 10 мин, а при кипячении — мгновенно. Достаточно высокую чувствительность шигеллы проявляют к дезинфицирующим средствам, ультрафиолетовым и прямым солнечным лучам.
Несмотря на разнообразие возбудителей шигеллезов, наибольшее эпидемическое значение для большинства стран мира имеют Sh. flexneri и Sh. sonnei. Хотя шигеллы распространены повсеместно (антропонозная инфекция), наиболее высокие показатели заболеваемости регистрируются в странах и регионах с низкой санитарией и высокой плотностью населения, что существенно облегчает возможность передачи возбудителя от человека к человеку. По расчетным данным, ежегодно в мире регистрируется около 140 млн случаев заболеваний шигеллезами. Восприимчивость к шигеллезной инфекции у лиц разных возрастных групп неодинакова. Наиболее восприимчивы к ним дети до двух-трех лет.
Патогенез. Основу патогенеза инфекционных заболеваний составляют особенности и характер взаимодействия микробов не только с клетками макроорганизма, но и с неспецифическими и специфическими защитными системами организма.
Шигеллы обладают достаточно выраженными вирулентными свойствами, вследствие чего заболевание может развиваться и при невысокой инфицирующей дозе (в сравнении с такими энтеропатогенными бактериями, как сальмонеллы и кишечные палочки). Благодаря относительной резистентности к действию желудочного сока и желчных кислот, шигеллы, не теряя своей вирулентности, проходят через желудочный барьер и проксимальные отделы тонкой кишки. В патогенезе заболевания выделяют тонко- и толстокишечные фазы, степень выраженности которых в конечном итоге и определяет вариант течения заболевания. У больных с типичным, колитическим вариантом острой дизентерии, тонкокишечная фаза клинически вообще не манифестируется, и заболевание изначально проявляется поражением дистального отдела толстой кишки. Тонкокишечная фаза обычно бывает непродолжительной и ограничивается двумя-тремя днями. Первичная транслокация шигелл через эпителиальный барьер осуществляется специализированными М-клетками, способными транспортировать как сами бактерии, так и их антигены в лимфатические образования кишечника (фолликулы, Пейеровы бляшки) с последующим их проникновением в эпителиальные клетки и резидентные макрофаги. Высвобождаемые в процессе транслокации шигелл токсические субстанции (экзо- и эндотоксины, энтеротоксины и т. д.) инициируют развитие синдрома интоксикации [3], который при шигеллезах всегда предшествует развитию диарейного синдрома.
Ключевым фактором вирулентности шигелл является их инвазивность, т. е. способность к внутриклеточному проникновению, размножению и паразитированию в клетках слизистой оболочки толстой кишки (преимущественно в дистальном отделе) и резидентных макрофагах собственной пластинки (см. рисунок 1). Посредством макроцитопиноза шигеллы проникают в цитоплазму эпителиальных клеток, где очень быстро лизируют фагосомальную мембрану, что приводит к повреждению клеток и их гибели. Последующее распространение шигелл происходит через базолатеральные мембраны эпителиальных клеток. Повреждение и разрушение эпителиальных клеток сопровождаются развитием воспалительной инфильтрации полиморфно-ядерными лейкоцитами собственной пластинки, формированием язв и эрозий слизистой оболочки толстой кишки, что клинически проявляется развитием диареи экссудативного типа. Способность к инвазии и внутриклеточному размножению шигелл кодируется генетическими механизмами, экспрессия которых происходит только в условиях in vivo. Несмотря на инвазивность, шигеллы не способны к глубокому распространению, в силу чего системной диссеминации возбудителя при шигеллезах, как правило, не происходит (за исключением Sh. dysenteriae 1).
Моторика кишечника является важным защитным механизмом, ограничивающим и препятствующим прикреплению и инвазии шигелл к эпителиальным клеткам, что наглядно демонстрируют затягивание и утяжеление инфекционного процесса у лиц, получающих препараты, подавляющие моторику кишечника.
Наблюдаемые у больных с шигеллезами дисбиотические изменения в составе нормальной микрофлоры толстого кишечника оказывают существенное влияние на скорость репарации слизистой в стадии реконвалесценции и восстановление функциональной активности кишечника.
После перенесенного заболевания у больных формируется непродолжительный (до одного года) типо- и видоспецифический иммунитет, в силу чего возможно реинфицирование.
Клиника. Клиническая картина шигеллезов весьма вариабельна, что нашло свое отражение в применяемой клинической классификации заболевания (см. таблицу 2). Хотя считается, что Sh. sonnei, как менее вирулентные штаммы шигелл, чаще вызывают более легкие формы заболевания, следует помнить, что этиология шигеллеза лишь предопределяет, но не определяет особенностей течения заболевания у конкретных больных (по форме, варианту и тяжести течения).
Хроническая форма дизентерии в настоящее время встречается достаточно редко и, по данным литературы, не превышает в 1-2% случаев, хотя существует мнение, что столь низкий ее удельный вес может быть обусловлен недостаточно разработанными критериями диагностики. Значительно чаще врачи в своей практической деятельности встречаются с острыми формами шигеллезов, которые и представляют наибольший интерес в плане адекватной оценки выявляемой у больного клинической картины заболевания, полноты обследования, правильности и своевременности проводимой терапии.
Инкубационный период при шигеллезах может варьировать от 8—12 ч (при гастроэнтеритическом варианте) до пяти дней (при колитическом варианте заболевания), составляя, в среднем, два–три дня.
Если примесь слизи в стуле является типичным признаком острой дизентерии, то кровь может присутствовать в микроскопических количествах и обнаруживаться только при копроцитоскопическом исследовании. Визуализируемая примесь крови в стуле определяется в виде прожилок. При более тяжелом течении заболевания дефекация может заканчиваться выделением небольшого количества слизи с прожилками крови.
Критериями тяжести течения колитического варианта острой дизентерии являются выраженность интоксикационного синдрома и характер поражения дистального отдела слизистой толстого кишечника (см. таблицу 3). Выраженного обезвоживания у больных при колитическом варианте острой дизентерии не выявляется ввиду отсутствия рвоты и скудного характера стула.
Гастроэнтероколитический вариант дизентерии также характеризуется острым началом заболевания: с озноба, лихорадки, головной боли и одновременным появлением синдрома гастроэнтерита — спастических болей в эпигастральной области, тошноты, рвоты, жидкого водянистого стула. Клинические признаки колита в первые сутки заболевания, как правило, отсутствуют и появляются лишь спустя один—три дня, что соответствует патоморфологическим этапам поражения слизистой желудочно-кишечного тракта. В зависимости от кратности рвоты и интенсивности диарейного синдрома, у больных достаточно рано выявляются признаки обезвоживания организма (сухость слизистых ротоглотки, бледность кожных покровов и цианоз, заостренные черты лица, снижение артериального давления, олигоурия и др.). С момента распространения патологического процесса на слизистую толстого кишечника проявления гастроэнтерита постепенно купируются: рвота прекращается, уменьшается объем испражнений, в стуле появляются патологические примеси (слизь и кровь). В зависимости от характера поражения слизистой дистального отдела толстой кишки, больные могут отмечать появление тенезмов и ложных позывов. При пальпации живота в первые дни заболевания отмечается урчание по ходу толстого кишечника, а в последующие дни появляется и нарастает болезненность и спазм сигмовидной кишки.
Тяжесть течения гастроэнтероколитического варианта дизентерии определяется на основании выраженности интоксикации и обезвоживания организма. В большинстве случаев оно не превышает II-III степени.
Редким вариантом течения острой дизентерии является гастроэнтеритический, характеризующийся большим сходством с пищевыми токсикоинфекциями.
Осложнения. Хотя наиболее высок риск развития осложнений у больных дизентерией, вызванной Sh. dysenteriae 1, на современном этапе прослеживается отчетливая тенденция к увеличению тяжелых форм дизентерии, обусловленных другими видами шигелл (в частности, Sh. flexneri), что, соответственно, отражается и на возможности развития осложнений. К числу наиболее грозных осложнений относятся: инфекционно-токсический шок; перфорация кишечника с развитием перитонита; энцефалический синдром (синдром фатальной энцефалопатии или синдром Ekiri), который преимущественно развивается у детей и иммунокомпрометированных пациентов при дизентерии, обусловленной Sh. sonnei или Sh. flexneri; бактериемия, выявляющаяся при дизентерии Sh. dysenteriae 1 в 8% случаев и крайне редко — при инфицировании другими видами шигелл (у детей до года, ослабленных, истощенных и иммунокомпрометированных пациентов); гемолитико-уремический синдром, развивающийся через неделю от начала заболевания и характеризующийся микроангиопатической гемолитической анемией, тромбоцитопенией и острой почечной недостаточностью. Нередко у больных могут развиваться осложнения, связанные с активизацией вторичной микрофлоры: пневмонии, отиты, инфекции мочевыводящих путей и др. К числу редких, но вероятных осложнений относятся реактивный артрит и синдром Рейтера (около 2% заболевших, экспрессирующих HLA-B27). В последние годы обсуждается возможная роль шигеллезов в формировании синдрома раздраженного кишечника.
Диагностика и дифференциальная диагностика. Специфическая диагностика шигеллезов основана на выделении и идентификации шигелл из испражнений больного и проведения серологических и/или иммунологических исследований, направленных на обнаружение антигенов шигелл или антител к ним. Без лабораторного подтверждения диагноз дизентерии может быть установлен только при типичной клинической картине.
Хотя диагностическая ценность эндоскопического исследования толстой кишки (ректороманоскопия и фиброколоноскопия) у больных с подозрением на шигеллезы ограничена, полученная при ее проведении информация позволяет: а) объективно оценить характер поражения слизистой толстой кишки; б) проводить дифференциальную диагностику и в) контролировать эффективность проводимой терапии.
В зависимости от характера поражения выделяют следующие варианты проктосигмоидита: катаральный, катарально-геморрагический, эрозивный, эрозивно-язвенный и фибринозный, которые, как правило, соответствуют тяжести течения заболевания.
При проведении дифференциальной диагностики в первую очередь необходимо исключить другие острые кишечные инфекционные заболевания, для которых типично развитие экссудативной диареи, а именно энтероинвазивные эшерихиозы, сальмонеллез, иерсиниоз (Y. enterocolitica), кампилобактериоз (Campylobacter jejuni), инфекция Clostridium difficile и амебиаз (протозойное заболевание, обусловленные Entamoeba histolytica). Кроме этого, необходимо помнить, что под маской шигеллезов могут дебютировать такие заболевания, как неспецифический язвенный колит и болезнь Крона.
Лечение. Лечение больных дизентерией может осуществляться не только в условиях специализированного инфекционного отделения, но и амбулаторно, что определяется клиническими и эпидемиологическими показаниями. В первую очередь следует госпитализировать пациентов со среднетяжелыми и тяжелыми формами заболевания, при затяжном и хроническом течении — пациентов с тяжелыми сопутствующими заболеваниями, детей до одного года и пожилых, а также лиц, представляющих эпидемическую опасность (независимо от варианта и тяжести течения заболевания) — работников пищевых предприятий и лиц, к ним приравненных.
Учитывая характер поражения слизистой кишечника, пациенты с дизентерией, особенно в острый период болезни, нуждаются в строгом соблюдении лечебного питания. Из рациона следует исключить любые продукты, оказывающие раздражающее (механическое, химическое и др.) действие. Ввиду формирующейся у больных недостаточности лактозы, из диеты исключается цельное молоко. Расширение диеты осуществляют постепенно, только по мере выздоровления больного. И все же переход на обычное питание следует осуществлять не ранее полного выздоровления, характеризующееся репарацией слизистой (см. таблицу 3).
Поскольку антибактериальная терапия всегда рекомендовалась для лечения больных дизентерией, серьезную проблему на сегодняшний день представляет формирование у шигелл резистентности к антимикробным препаратам, особенно в тех странах, где осуществляется их безрецептурная продажа и самолечение [5]. Недавно проведенные в нашей стране исследования [6] подтвердили высокую частоту резистентности у Sh. flexneri и Sh. sonnei к цефотаксиму (96,6 и 94,2%, соответственно), тетрациклину (97,7 и 92,8%), левомицетину (93,2 и 50,7%), ампициллину (95,5 и 26,1) и ампициллину/сульбактаму (95,5 и 23,2%). Резистентность не была выявлена лишь к ципрофлоксацину, норфлоксацину и налидиксовой кислоте.
Выбор антимикробного препарата и схема его применения у больных дизентерией определяются вариантом и тяжестью течения заболевания. При гастроэнтеритическом варианте антимикробная терапия не показана и больным назначают лишь патогенетическую терапию. При легком течении колитического и гастроэнтероколитического вариантов дизентерии больным целесообразно назначать фуразолидон по 0,1 г четыре раза в день или налидиксовую кислоту (невиграмон) по 0,5-1,0 г четыре раза в день в течение трех—пяти дней. Наиболее эффективными средствами для лечения больных со среднетяжелым и тяжелым течением дизентерии являются препараты фторхинолонового ряда (ципрофлоксацин, норфлоксацин и др.), цефалоспорины III поколения (цефотаксим), которые назначают в общетерапевтических дозах в течение пяти—семи дней. При тяжелом течении может проводиться комбинированная антибактериальная терапия (фторхинолоны и аминогликозиды; цефалоспорины и аминогликозиды).
Кроме антибактериальной терапии важное место в лечении больных дизентерией занимает патогенетическое лечение, включающее проведение дезинтоксикации и регидратации. В острый период заболевания больным целесообразно назначать десмол и смекту, обладающие противовоспалительным и мембраностабилизирующим действием на слизистую кишечника. После купирования интоксикационного синдрома больным показаны препараты, нормализующие процессы пищеварения и всасывания (дигестал, мезим-форте, панзинорм, фестал, холензим, ораза и др.). Коррекцию микробиоценоза кишечника следует проводить только в периоде реконвалесценции, когда купирована островоспалительная реакция. В этот же период больным показаны физиотерапевтические процедуры, ускоряющие процесс репарации слизистой толстого кишечника.
Литература
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук
ММА им. И.М. Сеченова
Причины и возбудитель дизентерии. Механизмы развития дизентерийной инфекции
При разрушении в организме человека все шигеллы образуют эндотоксин: палочка Григорьева-Шига, в отличие от других шигелл, способна выделять экзотоксин (нейротоксин), обладающий выраженной энтеротоксической активностью. Бактерии Григорьева-Шига отличаются самой высокой вирулентностью и вызывают тяжелые эпидемии дизентерии с большой летальностью (до 30-40%). Шигелла Зонне способна размножаться и накапливаться в пищевых продуктах (салаты, мясной фарш, компоты и др.), особенно в молоке при температуре +25°С и выше Все шигеллы хорошо сохраняются на продуктах растительного происхождения (зелень, фрукты, ягоды, овощи и др.) от нескольких дней до 1-2 мес; в воде-до 2 мес; в испражнениях- 10-15 суток; переносят замораживание до 40 дней. Обычные дезинфицирующие средства (например 5% раствор Лизола) убивает их через минуту. Наиболее устойчивы во внешней среде шигеллы Зонне.
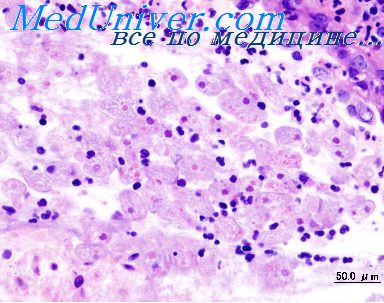
Механизмы развития дизентерийной инфекции
В развитии болезни имеют значение вид шигелл, доза возбудителя, фактор заражения (пища или вода), состояние организма человека до начала заболевания. Механизм развития патологического процесса при дизентерии сложен и, несмотря на многочисленные исследования отечественных и зарубежных ученых, еще полностью не изучен. Из существующих теорий патогенеза (токсикоинфекционная, аллергическая, инвазивная, связанная с внутриклеточным паразитированием возбудителя, иммуногенетическая и др.) ни одна в полной мере не объясняет сложного механизма развития патологического процесса при шигеллезной инфекции Бесспорным является факт, что после попадания шигелл через рот происходят гибель их в желудке и кишках, высвобождение и проникновение эндотоксина (а при шигеллезе Григорьева-Шига и экзотоксина) в кровь.
Это ведет к развитию общей интоксикации и сенсибилизации организма к шигеллезным токсинам, а позднее и к продуктам повреждения стенки кишечника, что облегчает внедрение возбудителя в слизистую оболочку толстой кишки. Бактериемии, как правило, не наблюдается. В эксперименте на людях - добровольцах показано, что размножение возбудителя в слизистой оболочке кишечника и ее повреждение (чаще дистальных отрезков толстой кишки) возможно только после предварительной специфической сенсибилизации организма к шигеллам. Опыты заражения дизентерией человека путем введения живой культуры возбудителя в прямую кишку не приводят к развитию болезни, что свидетельствует о решающей роли в ее патогенезе токсико-аллергического механизма. После инвазии с помощью имеющихся ферментов (гидролазы, муциназы и др.), шигеллы разрушают слизистую оболочку кишечника, преодолевают клеточные мембраны, проникают внутрь энтероцитов и размножаются в них.
Внутриклеточное паразитирование шигелл ведет к дегенеративным изменениям эпителия кишечника, слущиванию, частичному или полному его разрушению. Благодаря инвазивным свойствам шигеллы паразитируют в стенке кишечника. Под влиянием аутоантигенов тканевого происхождения возникают дополнительная аутосенсибилизация и усиление воспалительной реакции в кишке.
При дизентерии патологические изменения дистрофического характера обнаруживаются во всех отделах желудочно-кишечного канала, органах пищеварения, нервном аппарате кишечника и связанных с ним анатомически и функционально нервных сплетениях (мейснеровском и аурбаховском), солнечном сплетении, в шейных симпатических узлах, других отделах симпатической нервной системы, узловатом ганглии блуждающего нерва. В печени, поджелудочной железе, миокарде, почках вследствие интоксикации также происходят дистрофические изменения. В тяжелых случаях, наблюдавшихся в прежние годы, находили циркуляторные расстройства в мозговых оболочках и тканях мозга, кровоизлияния и некрозы в надпочечниках.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Клиника инфекций вызванной энтеробактериями. Диагностика, лечение
Выделяют два вида сальмонелл: Salmonella enterica и Salmonella bongori. Вид Salmonella enterica включает подвиды: enterica, salamae, arizonae, diarizonae, houtenae. Наиболее патогенны для человека и других теплокровных животных серовары подвида enterica.
Сальмонеллёз. Сальмонеллы хорошо приспособлены к обитанию в организме различных животных. У человека инфекция обычно не выходит за пределы кишечника. Заболевание характеризуется саморазрешающейся диареей. В некоторых случаях микроорганизмы могут вызывать инвазивные, угрожающие жизни человека заболевания, сопровождающиеся бактериемией, септицемией и остеомиелитом.
Сальмонелл обнаруживают в организме большинства домашних животных. Важными источниками инфекции считают больных людей и реконвалесцентных носителей. Механизм передачи заболевания — фекально-оральный (при употреблении контаминированных продуктов питания). Самые тяжёлые случаи сальмонеллёза наблюдают у пациентов со сниженным иммунитетом и сниженной секрецией желудочного сока, а также у лиц, перенёсших спленэктомию. В некоторых случаях заболевание осложняется реактивным артритом или развивается хроническое носительство.
Брюшной тиф. Возбудители брюшного тифа — серовары typhi и paratyphi подвида Salmonella enterica. Заболевание характеризуется поражением стенки кишечника, затем регионарных лимфатических узлов, сопровождается первичной бактериемией и инфекцией ретикулоэндотелиальной системы. В последующем бактерии попадают в кишечник из жёлчного пузыря, размножаются в пейеровых бляшках (развивается вторичная бактериемия), вызывают изъязвление стенки кишечника, которое может привести к кровотечению или перфорации. Пациенты предъявляют жалобы на высокую температуру, нарушение функций кишечника (диарею или запор) и сыпь (розеолёзные элементы на передней брюшной стенке). Наблюдают гепатоспленомегалию. Иногда брюшной тиф осложняется остеомиелитом и реже менингитом.
Инфекции мочевыводящих путей и пиелонефрит. Большинство инфекций мочевыводящих путей вызвают определённые серотипы Escherichia coli. Они способны к повышенному образованию К-антигена и гемолизина и прикреплению к эпителию мочевыводящих путей посредством пилей (последнее свойство характерно и для некоторых видов протея). При наличии у возбудителя маннозоустойчивых пилей развивается пиелонефрит. Важный фактор вирулентности бактерий рода Proteus — уреаза, снижающая рН и стимулирующая процесс образования камней.
Менингит и абсцессы мозга. Важной причиной менингита у новорождённых (характеризуется высокой смертностью) является Escherichia coli, штаммы которой в большом количестве продуцируют капсульный Kl-антиген. Кроме того, заболевание может быть следствием нейрохирургических вмешательств, операций по протезированию. Следует отметить, что энтеробактерии очень часто присутствуют в патогенной микрофлоре, сопровождающей абсцессы головного мозга.
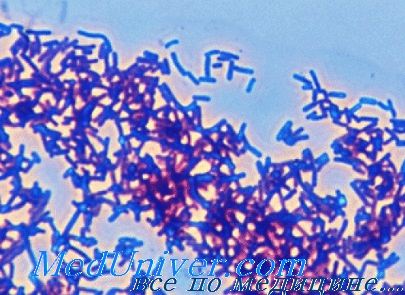
Возбудитель сальмонеллеза - Salmonella enterica
Остеомиелит и септический артрит. Тяжелейшее осложнение у пациентов с серповидно-клеточной анемией и ВИЧ-инфекцией — остеомиелит или септический артрит, вызванные сальмонеллами. Кроме того, сальмонеллы и другие энтеробактерии часто вызывают инфекции костей и суставов у пожилых пациентов. Иногда эти заболевания возникают вследствие проникающего ранения. Для лечения обычно применяют фторхинолоны, так как они обладают способностью проникать в костную ткань (например, ципрофлоксацин).
Инфекции, вызванные представителями рода Klebsiella. Микроорганизмы рода Klebsiella обычно вызывают внутрибольничные инфекции. Кроме того, они могут быть причиной развития пневмонии (особенно у пациентов, находящихся на искусственной вентиляции лёгких), инфекций мочевыводящих путей, раневых инфекций и бактериемии. У высоковосприимчивых пациентов известны случаи заболеваний, сопровождающихся септицемией и заканчивающихся летальным исходом. Первичная пневмония, вызванная подвидом Pneumoniae вида К. pneumoniae, — редкое и крайне тяжёлое внебольничное заболевание, характеризующееся неблагоприятным исходом. Возбудитель прогрессирующей гранулематозной инфекции слизистой оболочки полости носа — Klebsiella rhinoscleromatis. Большинство случаев заболевания регистрируют в тропических регионах мира. Другой вид — Klebsiella ozanae — возбудитель хронической бронхо-эктатической болезни.
Инфекции, вызванные бактериями родов Enterobacter, Serratia и Citrobacter. Представители этих родов обитают в окружающей среде и могут поражать пациентов лечебных учреждений, вызывая раневые инфекции, бактериемию и внутрибольничную пневмонию. Выбор антибактериального препарата осложняется тем, что большинство возбудителей устойчиво к действию антибиотиков.
Диагностика энтеробактерий:
• Бактериологическое исследование крови или костного мозга (особенно в диагностике брюшного тифа).
• Изучение биохимических свойств возбудителя (например, способности расщеплять углеводы).
• Серотипирование (серотипы различают по липополисахаридному (О) и жгутиковому (Н) антигену) и фаготипирование применяют при эпидемиологических исследованиях.
• Колицинотипирование.
• Современные молекулярно-генетические исследования.
Лечение и профилактика инфекции вызванной энтеробактериями
Большинство грамотрицательных энтеробактерии чувствительны к действию аминогликозидов, цефалоспоринов широкого спектра действия, фторхинолонов, бета-лактамов и карбапенемов (например, меропенем). Лечение назначают только после определения чувствительности возбудителя к антимикробным средствам, так как некоторые микроорганизмы способны вырабатывать бета-лактамазу и ферменты, разрушающие аминогликозидные препараты. Возросшая в последнее время устойчивость энтеробактерии к антибиотикам широкого спектра действия обусловлена появлением штаммов, обладающих бета-лактамазами широкого спектра действия.
Препараты выбора при инфекциях мочевыводящих путей — цефалексин, ампициллин, нитрофурантоин или триметоприм.
Для профилактики заболеваний, сопровождающихся диареей, необходимо соблюдать правила личной гигиены, приготовления пищи, а также использовать безопасные источники водоснабжения. Основной метод лечения — пероральная регидратация организма.
Препарат выбора при брюшном тифе — ципрофлоксацин, альтернативные средства — триметоприм или цефалоспорины третьего поколения. В некоторых странах инфекционисты сталкиваются с заболеваниями, вызванными мультирезистентными штаммами возбудителя. Для профилактики заболевания людям, посещающим эти регионы, рекомендуют использовать живую аттенуированную (Ту21А) или бесклеточную (содержит Vi-антиген) вакцины, но вакцинация лишь частично защищает от инфекции.
Видео строение, микробиология возбудителя брюшного тифа (S. typhi)
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инфекции вызванные энтеробактериями. Механизмы развития
Энтеробактерии (кишечные бактерии) — представители большого семейства (более двадцати родов и свыше ста видов) факультативных грамотрицательных палочковидных анаэробов, хорошо растущих на питательных средах, восстанавливающих нитраты и ферментирующих глюкозу. Способны вызывать множество различных заболеваний.
Энтеробактерии распространены повсеместно. Они составляют основу нормальной микрофлоры организма человека и животных; в большом количестве их обнаруживают в почве и воде. Заражение происходит при контакте с животными, другими людьми и контаминированными предметами. Очень часто заболевания вызывают условно-патогенные представители нормальной микрофлоры человека.
Численность энтеробактерии зависит от их локализации в организме, его состояния (здоровый или больной) и проводимой антимикробной терапии.
Патогенез инфекции вызванной энтеробактериями
Капсулы энтеробактреий. Многие микроорганизмы обладают полисахаридной капсулой (например, бактерии рода Klebsiella, Escherichia coli и Salmonella typhi). Основной фактор вирулентности Salmonella typhi — капсульный Vi-антиген, поэтому для профилактики тифа применяют вакцину, содержащую его. Чаше всего менингит и септицемию у новорождённых вызывает Escherichia coli K1.
Существуют определённые биохимические и структурные сходства между Escherichia coli К1, N. meningitidis группы В и антигенами центральной нервной системы человека, что даёт некоторое преимущество вышеперечисленным микроорганизмам.
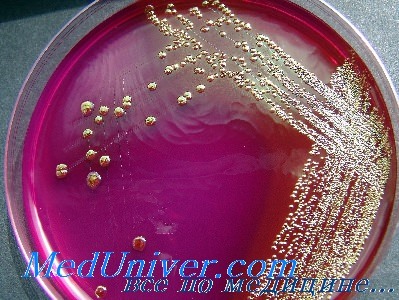
Энтеробактерии - Escherichia coli
Токсины энтеробактерий. Энтеротоксигенные штаммы Escherichia coli (ЕТЕС). Продуцируют термолабильный (LT) и термостабильный (ST) токсины, которые воздействуют на энтероциты, усиливая секрецию жидкости, вызывая диарею. Термолабильный токсин на 70% гомологичен по структуре с холерным экзотоксином. Так же как и последний, он разрушается при высокой температуре и способствует увеличению содержания циклической формы аденозинмонофосфата (цАМФ) в клетках кишечника.
Стабильный при высокой температуре, ST-токсин усиливает синтез циклической формы гуанилмонофосфата. Штаммы Escherichia coli, продуцирующие эти токсины, вызывают диарею путешественников (заболевание, при котором в течение непродолжительного времени возникает диарея).
Энтероагрегативные штаммы Escherichia coli (EAggEC). Некоторые штаммы Escherichia coli при прикреплении к энтероцитам вызывают их агрегацию. Они не поражают сами клетки, но вызывают хроническую диарею. Возбудители покрыты волокнистыми (фибриллярными) компонентами, которые предположительно обеспечивают их способность к адгезии. Некоторые штаммы продуцируют ST-подобный или гемолизинподобный токсины.
Энтерогеморрагические штаммы Escherichia coli (EHEC). Название штаммов связано с воздействием токсина возбудителей на клетки почек обезьян в тестах in vitro. Вызываемая ими геморрагическая диарея обычно сопровождается гемолизом и острой почечной недостаточностью (гемолитико-уремический синдром). Эти штаммы продуцируют вероток-син. Энтерогеморрагические штаммы Escherichia coli — представители нормальной микрофлоры кишечника крупного рогатого скота. Заражение человека происходит при несоблюдении санитарно-гигиенических норм во время работы на скотобойнях и предприятиях пищевой промышленности.
Токсин, подобный веротоксину Шига (Shiga toxin), — основной фактор вирулентности Shigella dysenteriae.
Обмен генетической информацией. Энтеробактерии могут получать генетическую информацию от других микроорганизмов посредством транспозонов, интегронов или плазмид. При этом гены, кодирующие устойчивость к антибиотикам, распространяются от одной бактерии к другой. Кроме того, с помощью обмена генетической информацией энтеробактерии могут приобретать различные факторы патогенности. При получении возбудителем ряда связанных между собой генов возникает так называемый островок патогенности.
Именно благодаря этой способности некоторые штаммы рода Salmonella могут поражать клетки кишечника. В условиях лечебных учреждений обычно выживают антибиотико-резистентные штаммы. В отделениях интенсивной терапии некоторых больниц периодически регистрируют вспышки инфекций, вызванных мультирезистентными штаммами Klebsiella pneumoniae.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое дизентерия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Шигеллёзы, или дизентерия — это группа острых/хронических заболеваний, вызываемых бактериями рода Шигелла, которые поражают желудочно-кишечный тракт (преимущественно дистальный отдел толстой кишки). Манифестные формы (клиническая картина) дизентерии: синдром общей инфекционной интоксикации, синдром поражения желудочно-кишечного тракта (дистальный колит), синдром обезвоживания. При отсутствии адекватного лечения приводит к серьёзным осложнениям и хронизации.
Возбудитель дизентерии
семейство — кишечные бактерии (Enterobacteriaceae)
род — Шигелла (Shigella)
виды — 4 основных:
- Dysenteriae (серовары — шигелла Григорьева-Шига, Штутцера-Шмитца, Ларджа-Сакса);
- Flexneri (Флекснера);
- Boydii (Боудии);
- Sonnei (Зонне).
Являются факультативно-анаэробными (способны существовать как при наличии, так и при отсутствии кислорода), граммотрицательными, неподвижными палочками. Хорошо растут на обычных питательных средах.
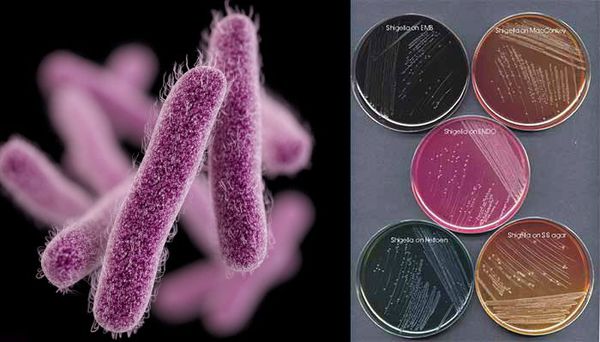
Имеют О-антиген (серологическая специфичность) и К-антиген (оболочечная структура). Клеточная стенка частично состоит из эндотоксина (липополисахарида), высвобождающегося при гибели микроорганизма. Бактерии вида Shigella Dysenteriae серовара Григорьева-Шига продуцируют высокоактивный цитотоксин, который нарушает синтез белка рибосомами клеток кишечного эпителия. Цитотоксин в совокупности с энтеротоксином (усиливающим секрецию жидкости и солей в просвет кишки) и нейротоксином (оказывающим нейротоксическое действие на сплетения Ауэрбаха) образует экзотоксином — токсин, выделяемый в процессе жизнедеятельности шигелл (Цитотоксин + энтеротоксин + нейротоксин = экзотоксин). Также у данной группы микроорганизмов происходит выделение гемолизинов — веществ, разрушающих эндотелий капилляров и вызывающий ишемию в тканях кишечника).
Факторы патогенности шигелл (механизм приспособления бактерий):
- адгезия (прикрепление к слизистой оболочке кишечника);
- инвазия (проникновение в эпителиальные клетки слизистой оболочки толстого кишечника);
- токсинообразование;
- внутриклеточное размножение.
Тинкториальные свойства (особенности микроорганизмов при окрашивании): быстро изменяют чувствительность к антибактериальным препаратам. Характерна высокая выживаемость во внешней среде (в воде, почве и пище при комнатной температуре сохраняются до 14 дней, в канализационных стоках — до 30 дней, при благоприятных условиях могут быть жизнеспособны до 4 месяцев). Способны к размножению в пищевых продуктах. При воздействии УФО (ультрафиолетового облучения) погибают за 10 минут, в 1% феноле — за 30 минут, при кипячении — мгновенно.
Интересная особенность: чем выше ферментативная активность возбудителя дизентерии, тем ниже вирулентность (минимальная доза возбудителя, способная заразить человека) и наоборот. [3] [6]
Эпидемиология
Антропоноз (повсеместное распространение).
Источник инфекции — человек (больной, носитель и лица с субклинической формой заболевания).
Минимальная инфицирующая доза для бактерии Григорьева-Шига — 10 микробных тел в 1 грамме вещества, для Флекснера — 10 2 бактерий, для Зонне — от 10 7 .
Длительное время в РФ превалировали случаи заражения, вызванные шигеллой Флекснера 2а, однако в настоящее время ввиду широкого развития туризма длительного преобладания какой-либо формы нет.
Механизм передачи — фекально-оральный (пищевой, водный, контактно-бытовой), из них преимущественно:
- Григорьева-Шига (контактно-бытовой путь);
- Зонне (с молоком и молочными продуктами);
- Флекснера (водный путь);
- Дизентериа (пищевой путь).
Наибольшую опасность представляют работники питания и водоснабжения. Больные заразны с начала болезни (конца инкубационного периода) и до трёх недель болезни.
Иммунитет непродолжителен и моноспецифичен (вырабатывается только к одному серотипу, который вызвал заболевание). [1] [4] [5]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы дизентерии
Инкубационный период — от 1 до 7 дней.
Начало заболевания острое (развитие основных синдромов наблюдается в первые сутки заболевания), характерна лихорадка постоянного типа.
Читайте также:

