Что такое деревья лихорадки
Обновлено: 05.05.2024
Что такое лихорадка Западного Нила? Каковы проблемы ее диагностики и дифференциальной диагностики?
Что такое лихорадка Западного Нила?
Каковы проблемы ее диагностики и дифференциальной диагностики?
Вирус лихорадки Западного Нила (ЛЗН) впервые выделен в 1937 году в Уганде при массовом обследовании на носительство вируса желтой лихорадки у больной с лихорадочным заболеванием, сопровождавшимся сонливостью. Через три месяца в крови у нее были обнаружены антитела против выделенного вируса.
Вирус ЛЗН (ВЛЗН) относится к роду Flavivirus семейства Flaviviridae (ранее входившему в семейство Togaviridae), содержит однонитевую несегментированную РНК, его репликация происходит в цитоплазме пораженных клеток. ВЛЗН принадлежит к антигенному комплексу японского энцефалита, включающего также возбудителей энцефалита Сент-Луис, желтой лихорадки, денге и др. (более 15 нозоформ).
Заболевания, вызываемые вирусами этого комплекса, характеризуются лихорадкой, геморрагическим синдромом, поражением ЦНС, гепатитом, которые встречаются в различных сочетаниях 7
Вследствие несовершенства механизма передачи наследственной информации ВЛЗН, как и многие другие однонитевые РНК-вирусы, обладает значительной изменчивостью генетической структуры и широким антигенным спектром. Это, по-нашему мнению, может приводить к изменению потенциала вирулентности и характера клинических проявлений болезни. Филогенетические исследования штаммов ВЛЗН, изолированных в 1937-2000 годах в различных регионах мира, показали их широкую вариабельность [16, 17].
Резервуаром вируса являются птицы водно-околоводного комплексов, чем и объясняется широкое распространение вируса в природе. Основными переносчиками ВЛЗН являются орнитофильные комары рода Culex, а также Aedes и др. Вирус адаптируется к местным видам аргасовых и иксодовых клещей, участвующих в сохранении вирусной популяции в межэпизоотический период. В циркуляцию вируса могут включаться дикие и домашние животные, например лошади, у которых болезнь протекает тяжело, с картиной энцефаломиелита [9].
Восприимчивость человека к ВЛЗН высока, хотя, по-видимому, преобладает бессимптомное инфицирование или легкие лихорадочные формы болезни. Так, в Бухаресте в 1996 году число бессимптомных или слабо выраженных случаев было в 140-320 раз больше, чем клинически выраженных [14]. В пользу этого говорит и высокая частота обнаружения антител у населения в высокоэндемичных районах. Однако данных о протективных свойствах антител нет. В этой связи интерес представляет возрастная структура больных. В высокоэндемичных регионах среди больных преобладают дети младшего возраста, в слабоэндемичных регионах болеют, причем тяжело, лица старших возрастных групп. Так, во время наблюдавшейся нами вспышки в Волгограде среди лиц с подтвержденным диагнозом пациенты старше 50 лет составили 51%, дети —16%, 78% умерших были старше 60 лет. Аналогичная ситуация наблюдалась и в Бухаресте в 1996 году, когда заболеваемость среди лиц до 50 лет составила 6 на 100 тыс. населения, а старше 70 лет — 40 на 100 тыс., летальность, соответственно, 0 и 15% [12, 14]. Аналогичный феномен наблюдается и при японском энцефалите и энцефалите Сент-Луис.
Возможно, что в данном случае мы сталкиваемся с феноменом антителозависимого иммунологического усиления, описанным при денге. При первичном заражении вирусом денге развивается доброкачественное заболевание. При повторном заражении другим серотипом вируса возникает тяжелейший синдром шока денге. Суть феномена состоит в фиксации комплекса вирус — антитело на поверхности мембраны клеток, что способствует увеличению числа инфицированных клеток, в частности моноцитов и макрофагов, и развитию генерализованных реакций. При ЛЗН в слабоэндемичных районах возможно повторное инфицирование лиц старших возрастов другим сероваром вируса или модифицированным вирусом. Однако эта гипотеза требует подтверждения.
Другие аспекты патогенеза ЛЗН также изучены мало. Анализ наших собственных наблюдений, патоморфологических и вирусологических данных позволяет предположить, что ВЛЗН распространяется гематогенно, в том числе внутри инфицированных лейкоцитов [1], поражая эндотелий сосудов, ганглиозные клетки коры головного мозга, кардиомиоциты. Ответная реакция проявляется формированием периваскулярных лимфоидных инфильтратов. Поражение нейроцитов сопровождается их дистрофией и некрозом. Повреждение сосудов способствует развитию отека-набухания мозга, возникновению локальных и генерализованных проявлений тромбогеморрагического синдрома.
Наблюдавшаяся в 1999 году в Волгограде вспышка ЛЗН существенно отличалась, так же как и другие регистрировавшиеся в последнее время вспышки, от описанных в предшествующие годы. Она по своим масштабам уступала лишь вспышке заболеваний в ЮАР в 1974 году.
Вспышка возникла в июле — сентябре в Волгограде, городе Волжском и близлежащих областях, когда в стационары поступило 739 больных с однотипной картиной (лихорадка, головная боль, боли в мышцах, суставах, резкая слабость, симптомы поражения ЦНС). Следует подчеркнуть, что в 1997 и 1998 годах в Волгограде в летние месяцы наблюдался беспрецедентный для России рост заболеваемости нейроинфекциями. Так, в 1997 году за июль — август заболело серозными и гнойными менингитами и менингоэнцефалитами 135 человек, преимущественно дети от 3 до 9 лет. Течение нейроинфекций было доброкачественным. В 1988 году только за месяц, с 10 августа по 9 сентября, заболело 149 человек, причем преобладали взрослые, в том числе 42% старше 50 лет, 9 больных (6%) умерли. Таким образом, есть основания полагать, что случаи заболевания ЛЗН имели место уже в 1997 году.
Хотя в целом по характеру интоксикационного синдрома течение болезни соответствовало имеющимся в литературе описаниями ЛЗН, имелись и существенные различия: продолжительность лихорадочного периода в среднем составляла более 8 суток, в отдельных случаях до 4 недель. Явления склерита и конъюнктивита отмечены только у 13% больных, сыпь — в единичных случаях, катаральные явления, полиаденопатия, гепатолиенальный синдром не наблюдались. Жидкий стул отмечен у 5% больных.
У всех пациентов доминировали симптомы поражения ЦНС: интенсивная головная боль диффузного характера, сопровождающаяся тошнотой, а у половины больных рвотой центрального характера. Нередко отмечалось головокружение, заторможенность, адинамия, корешковые боли, гиперстезия кожи; у 25% больных — повышение AД, более чем у половины (50%) — менингеальный синдром.
При исследовании цереброспинальной жидкости у 347 больных патологических изменений не выявлено, менингеальный и общемозговой синдромы были кратковременными, температура тела нормализовалась в течение 2-8 суток, то есть наблюдалась лихорадочная (гриппоподобная) форма болезни.
У 308 больных в течение 2-3 суток симптомы поражения ЦНС нарастали. Помимо менингеального синдрома выявлялась общемозговая симптоматика, мышечный тремор, анизорефлексия, нистагм, пирамидные знаки. ЦСЖ при люмбальной пункции вытекала под повышенным давлением, была прозрачной или опалесцирующей. При микроскопии выявлялся плеоцитоз в пределах от 15 до 2000 в 1 мкл, в среднем 200-300 клеток в 1 мкл. Плеоцитоз был лимфоцитарным, с примесью нейтрофилов. В первые трое суток у части больных плеоцитоз был смешанным или нейтрофильным (до 80% нейтрофилов). Количество белка повышалось в пределах 0,45-1,65 г/л. Содержание глюкозы находилось у верхних границ нормы. Течение болезни было относительно тяжелым, но доброкачественным. Температура нормализовалась в пределах 7-12 суток, ЦСЖ — в течение 2-3 недель, однако длительно сохранялась мышечная слабость, утомляемость. Эта форма болезни трактовалась нами как менингеальная.
У 84 больных была менингоэнцефалитическая форма болезни, которая характеризовалась тяжелым, злокачественным течением. Интоксикация и гипертермия были выражены с первых дней. Симптомы поражения ЦНС нарастали. С третьего-четвертого дня болезни на фоне менингеального синдрома начинала превалировать энцефалитическая симптоматика: спутанность сознания, возбуждение, стопор, а в отдельных случаях кома; часто отмечались судороги, мышечный тремор, парезы нижних конечностей, реже — черепных нервов, нистагм, нарушение стволовых функций. 40 больных умерли при явлениях отека мозга и расстройства дыхания. По сравнению с предыдущей группой наблюдалась меньшая выраженность менингеального синдрома, плеоцитоз ЦСЖ находился в пределах 10-300 клеток в 1 мкл, содержание белка повышалось до 0,6-3,0 г/л.
Летальность составила 5,4% общего числа больных, а в группе больных менингоэнцефалитом — 48%. При лихорадочной и менигеальной формах болезни летальных исходов не было.
Эти данные позволяют заключить, что современную ЛЗН следует отнести к группе тяжелых (опасных) вирусных болезней.
Диагноз ЛЗН может быть подтвержден выделением культуры вируса из крови в культуре клеток МК-2 или путем внутримозгового заражения мышей. Возбудитель может быть обнаружен прямым методом флюоресцирующих антител. Эффективны и широко применяются серологические реакции (РТГА, РСК, РН), в последние годы используется метод ИФА. О наличии ВЛЗН свидетельствует нарастание титра антител в четыре раза (на два разведения) при исследовании парных сывороток, взятых с интервалом 7-10 дней, или обнаружение антител класса IgM, поскольку в эндемичных районах антитела класса IgG могут обнаруживаться у значительной части населения. К недостаткам серологических реакций можно отнести значительный процент отрицательных результатов и затруднения при дифференцировке с другими флавирусными инфекциями комплекса японского энцефалита, так как возбудители имеют общие антигены и возможны перекрестные положительные реакции.
Наиболее эффективным и практически доступным методом ранней диагностики (с первого дня болезни) является полимеразная цепная реакция (ПЦР), позволяющая обнаружить специфические фрагменты генома вируса в крови и цереброспинальной жидкости, а также в трупном материале [12, 14-17]. Амплификация при помощи ПЦР генома ВЛЗН из культуры вируса или непосредственно из клинических образцов тканей больного может быть дополнена его детальным филогенетическим анализом.
Так, проведенное нами изучение генетической структуры ВЛЗН, выделенного в Волгограде, показало наличие в его геноме отличий от классического вируса и близость к вирусу, выделенному в Нью-Йорке [12, 16, 17]. Возможно, что особенности клинической картины болезни, наблюдавшиеся нами во время вспышки в Волгограде, связаны с изменением антигенных свойств вируса и резким возрастанием потенциала его вирулентности.
Изменения вирулентности вируса и, соответственно, распространение болезни в человеческой популяции известны и в отношении других флавирусов. Так, в 1945-1949 годы на территории Омской области и в прилегающих регионах отмечалась интенсивная вспышка флавирусной Омской геморрагической лихорадки. Заболеваемость достигла 4 тыс. на 100 тыс. населения, затем она снизилась до единичных случаев, хотя циркуляция вируса в этом регионе продолжается [1].
Дифференциальный диагноз при ЛЗН проводится в зависимости от клинической формы с широким кругом заболеваний. Важно учитывать эпидемиологические особенности ЛЗН: сезонность, ограниченную периодом активности комара — переносчика инфекции в данной местности, единичные случаи болезни в очаге, отсутствие контагиозности, связь заболевания с употреблением каких-либо пищевых продуктов или пользованием определенным источником водоснабжения. Гриппоподобную форму болезни приходится дифференцировать с лептоспирозом, гриппом, при наличии катаральных явлений — с другими ОРВИ; при диспептических расстройствах — с энтеровирусной инфекцией; в случаях, протекающих с лимфаденопатией и гепатолиенальным синдромом, — с аденовирусной инфекцией и инфекционным мононуклеозом.
Менингеальную форму болезни необходимо дифференцировать прежде всего с энтеровирусными менингитами, лимфоцитарным хориоменингитом и другими серозными вирусными менингитами.
Тяжелые случаи менингоэнцефалитов дифференцируются с герпетическим энцефалитом, туберкулезным менингитом. Преобладание в первые дни болезни в ЦСЖ нейтрофилов, тяжелая картина болезни, по нашим наблюдениям, нередко приводят к ошибочной диагностике бактериальных гнойных менингитов. Следует иметь в виду, что при гнойных менингитах и менингоэнцефалитах менингеальный синдром развивается на 1-2-й дни болезни, общемозговой синдром и очаговая симптоматика — на 2-4-й дни болезни, плеоцитоз ЦСЖ превышает 1000 в 1 мкл, преобладают сегментоядерные нейтрофилы, содержание глюкозы снижено, в крови — воспалительная реакция. При вирусных менингитах и менингоэнцефалитах ЦСЖ прозрачная, плеоцитоз в ранние сроки, когда возможно преобладание нейтрофилов, не превышает 200 клеток, обычно обнаруживаются молодые формы нейтрофилов, содержание глюкозы у верхних границ нормы или повышено. В крови тенденция к лейкопении и лимфоцитозу.
Этиотропная терапия и иммунотерапия при ЛЗН не разработаны. Госпитализация проводится по клиническим показаниям (гипертермия, выраженный нейротоксикоз, менингеальный синдром, общемозговая и очаговая неврологическая симптоматика). В остальных случаях больные лечатся на дому симптоматическими средствами. В связи с сосудистыми расстройствами следует избегать назначения ацетилсалициловой кислоты.
При менингеальной форме болезни больные нуждаются в умеренной дегидратационной терапии с использованием солюретиков, дезинтоксикации путем инфузии полиионных растворов, поляризующей смеси, применении анальгетиков.
Наиболее сложную задачу представляет лечение больных тяжелой менингоэнцефалитической формой болезни. Важное значение наряду с дегидратацией имеет поддержание нормоволемии, так как избыточная дегидратация приводит к снижению ОЦК, уменьшению мозгового кровотока, усилению гипоксии мозга, являющейся ключевым механизмом развития его отека-набухания. Именно об этом, по нашим наблюдениям, чаще всего забывают практические врачи. С самого начала лечения необходимо проведение оксигенотерапии путем ингаляции кислородно-воздушной смеси. При нарастании признаков отека мозга (развитие комы, судорожного синдрома, появление тахипноэ с резким снижением pCO2 и развитием гипоксемии) необходимо переводить больных на ИВЛ, не дожидаясь возникновения глубоких степеней дыхательных расстройств. С целью снижения проницаемости гематоэнцефалического барьера необходимо назначение дексаметазона в дозе 0,25±0,5 мг/кг в сутки. Показано также применение антиоксидантов, антигипоксантов, ноотропов, противосудорожных средств, коррекция нарушений КЩС и электролитного баланса.
Профилактика ЛЗН направлена на борьбу с комарами, в частности обработку мест их выплода (водоемы, подвалы жилых домов), использование средств защиты от комаров (затягивание окон сеткой, обработка жилых помещений и кожи репелентами). Эффективность этих мер была доказана во время вспышки ЛЗН в Нью-Йорке в 1999 году.
Литература
Лихорадка Западного Нила: история и эпидемиология
По данным Д. К. Львова, на территории бывшего СССР вирус циркулирует от Белоруссии до Приморского края, в частности в Закавказье, бассейне Каспийского моря, Средней Азии. Регистрировались и единичные заболевания среди людей [1, 9].
С 1996 года ситуация изменилась. В этом году в Бухаресте и прилегающих районах, то есть за пределами тропического и субтропического пояса, возникла крупная вспышка ЛЗН. Заболело не менее 400 человек, летальность составила около 4-6%, было инфицировано около 4% населения города [13, 14]. Летом 1999 года в Нью-Йорке произошла вспышка ЛЗН. Только менингоэнцефалитом заболело 58 человек, 7 из них умерли [15, 16]. Первоначально диагноз трактовался как энцефалит Сент-Луис, поскольку ранее на Американском континенте ЛЗН не регистрировалась. В этом же году в Волгоградской, Астраханской и Краснодарской областях также возникли крупные вспышки ЛЗН [9-12, 17]. Все эти вспышки, в отличие от описанных ранее, характеризовались высокой частотой поражения ЦНС и высокой летальностью. До настоящего времени в районах, вовлеченных в эти вспышки, наблюдаются случаи заболевания людей и инфицирования птиц ЛЗН (Румыния, 1997-1998 [18]), а также выявляются перезимовывающие комары-вирусоносители (Нью-Йорк, 2000, D. Morse, personal communication), то есть циркуляция вируса продолжается.
Таким образом, за последние годы резко расширился ареал ЛЗН, которая приобрела черты тяжелой нейроинфекции. Учитывая широкую циркуляцию вируса на территории России и стран ближнего зарубежья, следует признать, что для российского здравоохранения ЛЗН представляет новую актуальную проблему.
Что такое поллиноз (сенная лихорадка)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Воронцовой Ольги Анатольевны, аллерголога со стажем в 20 лет.
Над статьей доктора Воронцовой Ольги Анатольевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Поллиноз, или сенная лихорадка (Hay fever) — это сезонное заболевание, которое обусловлено повышенной чувствительностью к пыльце различных растений.
Основные проявления поллиноза — воспаление слизистых оболочек, преимущественно дыхательных путей и глаз, связанное с периодом цветения определённых растений. Теоретически аллергическая реакция может существовать на пыльцу любого растения, но, как правило, её провоцирует пыльца ветроопыляемых растений. На Земле несколько тысяч распространённых видов растений, и только около 50 из них производят аллергенную пыльцу. Растения с яркой окраской и приятным запахом редко вызывают аллергию.
На распространённость поллинозов влияет ряд факторов:
- природно-климатические условия (распространённость поллиноза значительно выше в южных регионах);
- распространённость тех или иных видов растений и степень их аллергенной активности;
- экологические условия (городские жители болеют в 6 раз чаще).
Пыльца — это мужские половые клетки растений, которые представлены множеством пыльцевых зёрен, имеющих особенности, которые опытным глазом можно различить, рассматривая пыльцу под микроскопом (различная конфигурация, размеры, шипы, гребни, валики, поры), специфические для конкретных видов растений. Диаметр пыльцевых зерен аллергенных растений составляет в среднем от 20 до 60 мкм.

Учёт концентрации пыльцы в воздухе называется пыльцевым мониторингом, во многих крупных городах России он проводится, а данные размещаются на сайте в открытом доступе.
Среди наиболее распространённых растений пыльца берёзы обладает наиболее выраженной аллергенной активностью. И для возникновения симптомов совсем не обязательно находиться в лесу или парке. Мелкая пыльца этого дерева разлетается на десятки километров.
Пыльца аллергенных представителей злаковых трав имеет диаметр 20-25 мкм.
Наиболее аллергенные злаки в России:
Сорняки также являются ветроопыляемыми, и их пыльца разносится на большие расстояния. К ним относятся сложноцветные:
- амброзия;
- ромашковые (полынь);
- маревые (марь белая, перекати-поле);
- лебеда.
Наиболее выраженной аллергенной активностью обладает пыльца полыни и амброзии.
Аллерген пыльцы полыни может вызывать перекрёстные реакции (реакции на иные аллергены со сходной структурой) с аллергенами пыльцы амброзии, подсолнечника, одуванчика, мать-и-мачехи, берёзы.
В средней полосе России пыление растений происходит в течение трёх основных периодов:
- весеннего, когда наибольшей аллергенной активностью обладает пыльца берёзы, ольхи, орешника, дуба, ясеня. К слову сказать, примерно в этот период цветет и тополь, но его пыльца малоаллергенна;
- раннего летнего (первая половина календарного лета), когда пылят злаковые травы (ежа, тимофеевка, овсяница и др.);
- позднего летнего (конец лета и ранняя осень) — пыление сорных трав: полыни, лебеды, подорожника, на Юге — амброзии. [4]
Грамотный опрос специалиста аллерголога-иммунолога может ощутимо сузить перечень планируемых лабораторных исследований. В европейских странах с диагностикой несколько сложнее, потому как пыление разных растений происходит практически одновременно.
Расхожее мнение пациентов о существовании аллергии на тополиный пух не совсем верно, так как в период образования этого пуха совпадает с периодом максимальных концентраций пыльцы трав, а пух лишь является переносчиком этих пыльцевых зёрен, как бы наматывая их на себя, и транспортирует их, сам являясь лишь механическим раздражителем.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы поллиноза
Пыльцевая аллергия проявляет себя всеми признаками воспаления — покраснением, отёком, зудом, обильными отделениями слизистого характера [4] , а также:
Более редкие симптомы поллиноза:
- сыпь на коже, зуд;
- боль в горле;
- боли в животе, изжога;
- жидкий стул;
- боль в сердце.
Все перечисленные жалобы, как правило, сочетаются с жалобами общего характера (головной болью, слабостью, быстрой утомляемостью, общим недомоганием, головокружением, сонливостью, снижением памяти, повышением температуры, что в ряде случаев трактуется как проявления острого респираторного заболевания). [5]
Для поллиноза характерно улучшение состояния пациента в дождливые, пасмурные, безветренные дни, чего не происходит при ОРВИ и ОРЗ.
Патогенез поллиноза
В основе патогенеза поллиноза лежит аллергическая реакция немедленного типа. После того, как аллерген попадает на слизистую оболочку какого-либо органа (большая часть оседает на слизистой носа), вырабатываются антитела (иммуноглобулины Е), которые, соединяясь с аллергенами (пыльцой растений) при повторном попадании, вызывают igE-зависимую активацию тканевых базофилов (тучных клеток). В результате происходит выброс ряда биологически активных веществ: гистамина, лейкотриенов, простагландинов, брадикининов, фактора активации тромбоцитов.
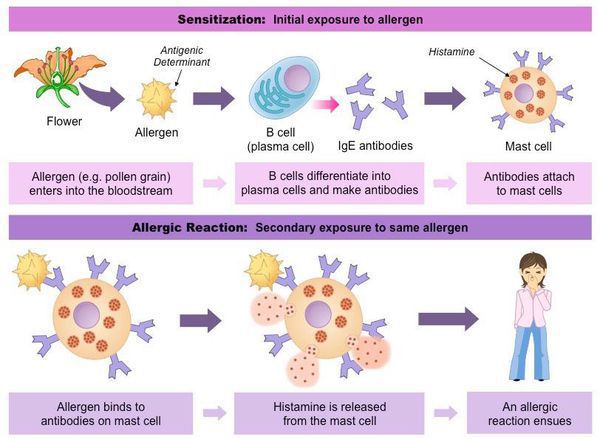
Возникает аллергическая воспалительная реакция: увеличивается образование слизи, снижается функция мерцательного эпителия дыхательных путей. Гистамин расширяет кровеносные сосуды, вследствие чего снижается кровяное давление. Из-за того, что расширяются артериолы мозга, повышается давление спинно-мозговой жидкости и появляется головная боль. При повышении концентрации гистамина в крови на коже может появиться крапивница (сыпь), повыситься температура тела, возможно затруднение дыхания из-за отёка слизистой оболочки дыхательных путей и спазма гладких мышц. Отмечается частое сердцебиение (тахикардия), повышенное слюноотделение и т. п. Этим действием гистамина объясняется значительная часть общих симптомов поллиноза. [6]
Классификация и стадии развития поллиноза
Общепринятой классификации поллиноза сегодня не существует. По выраженности симптомов и их влиянию на качество жизни пациентов различают 3 вида течения поллиноза:
- лёгкое (симптомы слабовыражены, не доставляют беспокойства, потребность в терапии минимальна);
- средней тяжести (ощутимый дискомфорт, снижение работоспособности, нарушение сна, значительное снижение качества жизни пациентов);
- тяжёлое течение поллиноза (приводит к нетрудоспособности и отрицательно сказывается на качестве жизни). [7]
Осложнения поллиноза
Несвоевременная диагностика и лечение риноконъюнктивальной формы поллиноза (когда вовлекаются только структуры носа и глаз) может привести к бронхиальной астме либо ухудшить течение уже имеющейся. Среди осложнений — нарушения слуха, разрастание слизитой носа (формирование полипов), что в дальнейшем может потребовать оперативного вмешательства.
Длительно сохраняющаяся отёчность слизистой носовых ходов и постоянное дыхание через рот у маленького ребёнка может привести к характерному выражению лица с приподнятой верхней губой и формированию неправильного прикуса в дальнейшем. Нарушение носового дыхания ощутимо снижает внимание детей и может повлечь за собой снижение успеваемости у школьников.
Диагностика поллиноза
Сегодня известно очень много методов исследования для диагностики поллиноза. Все они взаимодополняемые, сложно ориентироваться на какой-то один параметр или одно отклонение от нормы при обследовании.
Самым основным и самым важным является сбор анамнеза: детальный расспрос пациента о симптомах, их выраженности, длительности, ранее принимаемых лекарственных препаратах по этому поводу и оценка их эффективности, по мнению больного. Периодичность жалоб, разница в самочувствии при смене места пребывания, региона (например, резкое улучшение самочувствия в командировке, в отпуске). Уточняется, есть ли среди кровных родственников кто-то с аллергическими заболеваниями — это повышает риск возникновения подобных заболеваний. Грамотный расспрос позволяет в дальнейшем минимизировать финансовые затраты на поиск причинного аллергена, обойтись без промежуточных анализов.
К базовым лабораторным показателям относятся общий анализ крови, где косвенным признаком аллергических изменений в организме человека будет повышение уровня эозинофилов, общего иммуноглобулина Е (igE), или более современный показатель — эозинофильный катионный белок.
При наличии клиники со стороны глаз может потребоваться консультация офтальмолога.
Для точного определения действующего аллергена проводят кожное тестирование с набором пыльцевых аллергенов, распространённых в местности проживания пациента. Аллергические кожные пробы выполняют в период, когда контакт с пыльцой полностью отсутствует. [8] Это простой и быстрый тест, но у него имеются ограничения и противопоказания:
- период обострения основного заболевания;
- крапивница или астматические приступы;
- приём антигистаминных препаратов;
- применение в лечении системных гормонов (например, Преднизолон);
- ОРВИ, грипп, тяжёлые заболевания сердечно-сосудистой системы, печени, почек и других органов;
- беременность;
- туберкулёзный процесс любой стадии.
Определение специфических иммуноглобулинов Е (igE)
Можно провести диагностику, не травмируя кожу, по анализу крови. Пациенту для этого нужно лишь сдать кровь из вены. Далее в лаборатории проводится анализ (радиоизотопный, хеминилюминесцентный или иммуноферментный)
Молекулярная аллергология — это самый современный метод диагностики аллергических заболеваний, позволяет повысить точность диагноза и прогноза при аллергии и играет важную роль в 3-х ключевых моментах:
- дифференцирование истинной сенсибилизации и перекрёстной реактивности у полисенсибилизированных пациентов (если аллергические проявления имеются сразу на несколько аллергенов);
- оценка риска развития острых системных реакций вместо слабых и местных при пищевой аллергии, что уменьшает необоснованное беспокойство пациента;
- выявление причинных аллергенов для проведения аллерген-специфической иммунотерапии (АСИТ).
Наиболее распространена технология чипов Immuna Solid phase Allergen Chip (ISAC). Это самая полноценная платформа, которая включает в себя более 100 аллергенных молекул в одном исследовании.
Результаты всех этих тестов (кожных и лабораторных) обязательно должны сопоставляться с клиникой болезни, так как наличие сенсибилизации к аллергенам необязательно сопровождается клиническими проявлениями.
Лечение поллиноза
Поллиноз лечится в амбулаторно-поликлинических условиях.
Основные виды терапии поллинозов:
- предупреждение контакта с аллергеном;
- фармакотерапия;
- аллерген-специфическая иммунотерапия;
- обучение пациента.
Предупреждение контакта с аллергеном
Элиминация аллергенов уменьшает выраженность проявлений поллиноза и потребность в медикаментозном лечении. Общеизвестными мероприятиями являются:
Фармакотерапия
Объём медикаментозной терапии и выбор лекарственных средств зависит от выраженности клинических проявлений и определяется только врачом.
В перечне препаратов по данному заболеванию фигурируют:
Специфическая иммунотерапия (АСИТ, СЛИТ) имеет целью снижение специфической чувствительности конкретного больного к конкретному причинному аллергену. [9] Это достигается введением аллергена, начиная с малых доз, с постепенным их увеличением. Данная терапия может проводиться водно-солевыми аллергенами, адъювантными аллерговакцинами (подкожные инъекции). Также есть препараты для сублингвального (подъязчычного) применения: капли или таблетки, в составе которых есть определённая доза аллергена. АСИТ будущего — это накожные методы, притом сразу с несколькими аллергенами, но пока об этом приходится только мечтать и врачам, и пациентам.
Прогноз. Профилактика
Нельзя недооценивать клинику аллергических состояний, так как с течением времени симптомы могут усугубиться, а объём требуемой медикаментозной терапии — ощутимо увеличиться. Целесообразно провести профилактику прогрессирования заболевания, к примеру, предотвратить формирование бронхиальной астмы. [11] [12]
В целях профилактики лицам с поллинозом можно порекомендовать ряд мероприятий:
Вирусные тропические лихорадки: диагностика, лечение, профилактика
В роли возбудителей энцефалита и геморрагической лихорадки могут выступать свыше сотни различных вирусов. Практически все они избирают человека в качестве хозяина случайно, при вторжении последнего в их жизненный цикл. Передача осуществляется при прямом контакте с заражённой кровью или физиологическими жидкостями, а также при укусах членистоногих (комаров, клещей и мошек). Некоторые инфекции характеризуются достаточно высокой смертностью пациентов.
Желтая лихорадка. Возбудитель жёлтой лихорадки — оболочечный однонитевой плюс-РНК-вирус. Заражение происходит при укусе комара Aedes aegypti. Жёлтая лихорадка — зоонозная инфекция, при этом человек становится случайным хозяином (джунглевая форма). Вспышки возникают периодически также при проникновении возбудителя в городскую среду (городская форма).
Методы диагностики — культивирование вируса, серологическое исследование. Профилактика — введение живой аттенуированной (ослабленной) вакцины и контроль над распространением переносчиков (комаров).
Лихорадка Денге
Переносчики лихорадки Денге — комары рода Aedes. Возбудитель — флавиви-рус, похожий по своим свойствам на вирус жёлтой лихорадки. Установлено 4 серотипа вируса. Инкубационный период 2—15 дней. При возникновении лихорадки наблюдают виремию, продолжающуюся несколько дней. Вирус лихорадки Денге распространён на территории стран тропической зоны и Ближнего Востока. Эпидемии возникают при появлении нового серотипа либо при массовом попадании неиммунных людей в места обитания вируса; в городах распространяются очень быстро, заболевание протекает тяжело.
После внезапного возникновения жара, головной боли и общего недомогания пациенты начинают жаловаться на боли в суставах и костях. Лихорадка может быть двухволновой. В некоторых случаях отмечают небольшую сыпь. Наиболее тяжёлая и опасная форма заболевания сопровождается геморрагическим синдромом, характеризующимся развитием шока и геморрагического диатеза (геморрагическая форма денге). Смертность 5—10%.
Методы диагностики — серологическое исследование, культивирование вируса, молекулярно-генетические методы. Единственный способ профилактики заболевания — количественный контроль переносчиков. Лечение симптоматическое.
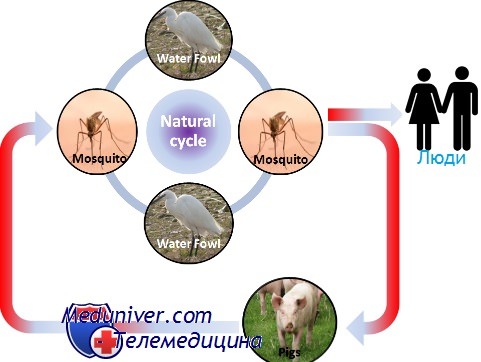
Эпидемиология японского энцефалита
Японский энцефалит В
Возбудитель японского энцефалита В — флавивирус; переносчики — комары. Природным источником вируса являются свиньи. В клинической картине доминируют симптомы тяжёлого энцефалита с высокой летальностью. Болезнь начинается остро с лихорадки, сильной головной боли, тошноты и рвоты.
В некоторых случаях отмечают судороги. При обследовании обнаруживают поражение черепных нервов и пирамидного пути. Для профилактики применяют вакцину.
Вирус лихорадки западного Нила
Заражение вирусом лихорадки западного Нила происходит так же, как при лихорадке Денге и японском энцефалите В. Вирус впервые был обнаружен в Северной Америке в 1999 г. и быстро проник на территорию Канады, Латинской Америки и Карибского бассейна.
Геморрагическая лихорадка Ласса
Ласская лихорадка — тяжёлая геморрагическая лихорадка, вызываемая аренавирусом. Передача инфекции осуществляется посредством контактного механизма от крыс к человеку, а затем и от человека к человеку. Вирус поражает все органы и системы организма. Пациенты жалуются на лихорадку, изъязвления в ротовой полости, мышечную боль и геморрагическую сыпь. Диагноз устанавливают на основании данных клинической картины и анамнеза заражения пациента.
Для его подтверждения применяют молекулярно-генетический метод с использованием обратной транскриптазы или серологические методы. На ранних стадиях заболевания и после контакта с инфицированными людьми назначают рибавирин.
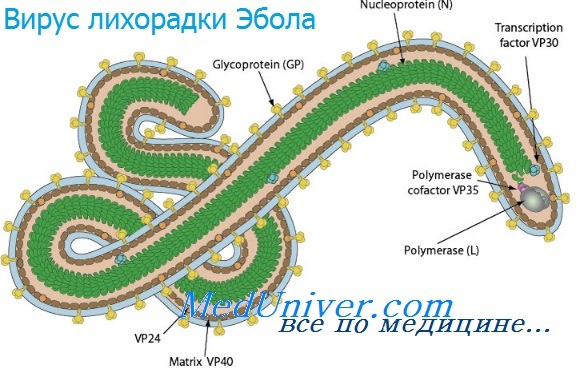
Инфекции вирусов лихорадки Эбола и марбургской болезни
Инфекции вирусов лихорадки Эбола и марбургской болезни - филовирусные инфекции распространены на территории Африки и передаются человеку от приматов и грызунов. Они характеризуются развитием тяжёлой геморрагической лихорадки и высоким уровнем смертности. Инфекция также передаётся при тесном контакте с инфицированными (особенно во внутрибольничной среде). Основной метод лечения — поддерживающая терапия и введение гипериммунной сыворотки.
Профилактику внебольничных инфекций затрудняет отсутствие возможности изоляции источника заболевания. Для предотвращения распространения внутри-больничной инфекции необходимо соблюдать строгие меры предосторожности при контакте с кровью и физиологическими жидкостями больных пациентов. Вакцина на основе вируса везикулярного стоматита, кодирующего антигены вируса лихорадки Марбург, способна защитить приматов даже при введении после заражения.
Хантавирус - хантавирусная лихорадка
Возбудитель передаётся человеку от грызунов, относится к группе буньявирусов. Инфекция, вызванная им, характеризуется геморрагической лихорадкой с почечным синдромом или хантавирусным лёгочным синдромом. Вирус широко распространён во всём мире. Передача от человека к человеку невозможна. По окончании инкубационного периода (2—3 нед) возникают лихорадка, головная боль, боль в спине, поражение конъюнктивы и нёба, а позднее — гипотензия, шок, олигурия, почечная недостаточность. Смертность около 5%.
Методы диагностики — серологическое исследование, молекулярно-генетические с использованием обратной транскриптазы. Предполагают, что рибавирин способен уменьшать вероятность смертельного исхода, но необходимые клинические исследования проведены не были.
Вирус Нипах
Парамиксовирус Нипах — возбудитель тяжёлых инфекций у людей и животных. Впервые выделен в Малайзии; обнаруживают на территории многих азиатских стран. Вызываемое им заболевание сопровождается развитием лихорадки и энцефалита и характеризуется высоким уровнем смертности. Источник инфекции — летучие мыши, питающиеся фруктами. Заражение происходит при контакте с мышами или промежуточными хозяевами (свиньями). Кроме того, возможна передача инфекции от человека к человеку.
Родственный вирусу Нипах вирус Хендра встречают реже. Переносчиками также служат летучие мыши. В клинической картине доминирует гриппоподобный синдром или энцефалит.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Типы лихорадки - характеристика, примеры
Описано 4 типа лихорадки: интермиттирующая, ремиттирующая, постоянная и возвратная. Определение типа лихорадки лишь иногда оказывает помощь в установлении диагноза. Чрезмерное использование жаропонижающих средств маскирует или искажает типы лихорадки.
Типы лихорадки
| Тип | Характеристика | Примеры* |
| Интермиттирующая | Температура нормализуется один или несколько раз в день | Гнойная инфекция, абсцессы, лимфомы, туберкулез, ювенильный ревматоидный артрит |
| Ремиттирующая | Температура колеблется, но не возвращается к норме | Большинство вирусных и многие бактериальные инфекции |
| Постоянная | Температура постоянно увеличена с небольшими колебаниями | Брюшной тиф, сыпной тиф |
| Возвратная | Безлихорадочные периоды длительностью один и более дней между приступами лихорадки | Малярия, болезнь содоку**, инфекция Borrelia, болезнь Ходжкина (лимфогранулематоз) |
** Инфекции, вызванные Spirillum minus или Streptobacillus moniliformis.
1. Интермиттирующая лихорадка характеризуется падением температуры до нормального уровня по крайней мере один раз в сутки. Нередко такая лихорадка следует за нормальными суточными колебаниями температуры, будучи наиболее низкой по утрам и наиболее высокой по вечерам. Если пик лихорадки особенно высок, то речь идет о гектической или септической лихорадке.
Интермиттирующая лихорадка характерна для гнойных бактериальных инфекций, но нередко отмечается и при туберкулезе, и лимфомах.
2. При ремиттирующей лихорадке температура колеблется, но не возвращается к нормальной. Это наиболее распространенный тип лихорадки.
3. Постоянная лихорадка характеризуется стойким повышением температуры тела с небольшими ее колебаниями или без них. Она отмечается при сыпном и брюшном тифе.
4. Возвратный тип лихорадки наблюдается при малярии, лихорадке содоку и инфекции, вызванной Borrelia (возвратная лихорадка). Если период нормальной температуры является относительно длительным (2 нед или более), то такая лихорадка называется лихорадкой Пеля—Эбштейна. Она характерна для лимфогранулематоза.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Поллиноз — классическое аллергическое заболевание, в основе которого лежит аллергическая реакция немедленного типа. Заболевание характеризуется острым аллергическим воспалением слизистых оболочек дыхательных путей, глаз, кожи. Реже в процесс вовлекаются
Поллиноз — классическое аллергическое заболевание, в основе которого лежит аллергическая реакция немедленного типа. Заболевание характеризуется острым аллергическим воспалением слизистых оболочек дыхательных путей, глаз, кожи. Реже в процесс вовлекаются пищеварительная, сердечно-сосудистая, мочеполовая, нервная системы. Заболевание отличается четкой, из года в год повторяющейся сезонностью и совпадает по времени с пылением определенных растений. Ежегодно клинические симптомы поллиноза повторяются в одни и те же месяцы, даже числа, за исключением жаркой или холодной погоды, когда период пыления растений начинается раньше или запаздывает. Характерна четкая связь с пребыванием в определенной местности, где пылят аллергенные растения. Выезд больного из данного региона приводит к исчезновению симптомов поллиноза. Интенсивность клинических проявлений заболевания зависит от концентрации пыльцы в воздухе. Поэтому больные чувствуют себя значительно хуже за городом, в поле, где концентрация пыльцы выше. Дождливая погода благоприятно сказывается на состоянии больных (количество пыльцы уменьшается). Жаркая погода приводит к обильному образованию пыльцы и ведет к нарастанию клинических проявлений.
В разных странах мира поллинозами страдает от 0,2 до 39 % населения. Чаще всего болеют лица от 10 до 40 лет, у детей до 3 лет заболевание поллинозом встречается редко, до 14 лет в 2 раза чаще заболевают мальчики, а возрасте от 15 до 50 лет лица женского пола. Среди горожан заболеваемость выше в 4–6 раз, чем у сельских жителей. Распространенность пыльцевой аллергии зависит от природно-климатических, экологических и этнографических особенностей.
Выделены 3 основные группы аллергенных растений: древесные, злаковые и разнотравье, сорняки.
Первый пик заболеваемости поллинозом — весенний — вызывает пыльца деревьев (с середины апреля до конца мая). Среди деревьев выраженной аллергенной активностью обладает пыльца березы, дуба, орешника, ольхи, клена, ясеня, платана, вяза, тополя.
Второй весенне-летний подъем заболеваемости вызывает цветение злаков с начала июня до конца июля. Наибольшей антигенной активностью обладают дикорастущие (тимофеевка, овсяница луговая, ежа сборная, пырей, мятлик луговой, костер, лисохвост, райграс), культивируемые злаки (рожь, кукуруза).
Третья пыльцевая волна (июль–сентябрь) связана с бурным пылением сорных трав (полынь, лебеда, амброзия, подсолнечник).
Установлено, что в центральной полосе России чаще заболевание связано с сенсибилизацией к пыльце злаковых трав, деревьев, сорных трав. На юге России основные аллергены амброзия, полынь, подсолнечник, кукуруза. В Сибири в спектре сенсибилизации преобладает пыльца деревьев и злаков. В странах центральной Европы ведущая роль в этиологии поллинозов принадлежит злаковым травам и деревьям, в северной Европе — злакам и сорнякам, в южной Европе — деревьям, кустарникам и травам, в США — амброзии.
Известно, что существует сходство между аллергенами различных видов пыльцы. Антигены присутствуют не только в пыльцевых зернах, но и в других частях растений (семена, листья, стебли, плоды). Это является причиной появления у больных поллинозом перекрестной пищевой аллергии и непереносимости препаратов растительного происхождения.
Факторы, способствующие сенсибилизации: наследственность по атопическим заболеваниям; высокий уровень сывороточного IgE; место рождения (зона высокой концентрации пыльцы растений); месяц рождения (дети, рожденные в сезон пыления, имеют большую вероятность заболеть); низкий вес ребенка при рождении; искусственное вскармливание; частые респираторные инфекции; курение; нерациональное питание; загрязнение атмосферного воздуха (промышленные и химические аллергены, ксенобиотики изменяют химический состав пыльцевых зерен, способствуют накоплению токсических компонентов).
Наиболее частыми проявлениями поллиноза являются аллергический ринит (95–98%), аллергический конъюнктивит (91–95%), пыльцевая бронхиальная астма (30 — 40% больных). У ряда пациентов отмечаются кожные проявления поллиноза: крапивница, отек Квинке, дерматит. К редким проявлениям поллиноза относятся поражение урогенитального тракта (вульвовагиниты, уретрит, цистит, нефрит) и желудочно-кишечного тракта (тошнота, рвота, боли в эпигастрии, расстройства стула). Особенностью этих вариантов поражения является сезонность развития симптомов, благоприятное течение, эффект от использования антигистаминных препаратов, присутствие других симптомов поллиноза. Описаны проявления поллиноза в виде пыльцевого аллергического миокардита.
При употреблении в пищу продуктов растительного происхождения или фитопрепаратов, имеющих общие антигенные свойства с пыльцой растений, а также меда могут возникать симптомы аллергического гастроэнтерита, крапивницы, отека Квинке вплоть до анафилактического шока. Такие реакции возможны и вне пыльцевого сезона. Непереносимость пищевых продуктов и лекарственных растений подробно указана в таблице 1.
Для диагностики поллинозов используют данные аллергологического анамнеза, результаты специфического обследования (кожные пробы, провокационные тесты) и лабораторные методы исследования.
Первичная профилактика поллиноза направлена на предупреждение развития пыльцевой аллергии.
- Ограничение общей антигенной нагрузки.
- Рациональное питание.
- Использование методов физического оздоровления и закаливания.
- Рациональное озеленение городов (использование неаллергенных растений).
- Для родителей с атопическими заболеваниями, планирование рождения ребенка вне сезона пыления.
Вторичная — предупреждает ухудшение состояния у тех лиц, которые уже страдают поллинозом.
- Обучение больного и членов его семьи по вопросам лечения и профилактики пыльцевой аллергии.
- Контроль за концентрацией пыльцы в помещении (закрытые окна и двери, кондиционер, увлажнители и очистители воздуха, водные пылесосы).
- Выезд в другие климатические зоны в период цветения.
- Ограничение выхода на улицу в солнечную ветренную погоду.
- Исключение из диеты продуктов с перекрестными аллергенными свойствами.
- Ограничение воздействия неспецифических раздражителей (лаки, краски, химикаты).
- Отказ от фитотерапии.
- Своевременная диагностика, адекватная фармакотерапия и аллергенспецифическая иммунотерапия.
- Не проводить профилактические прививки и плановые оперативные вмешательства в период пыления растений, на пыльцу которых у пациента аллергия.
Основные принципы лечения аллергических заболеваний используются и в лечении поллиноза: элиминация аллергенов, предсезонная аллергенспецифическая иммунотерапия и фармакотерапия в период обострения.
Наиболее эффективным методом специфического лечения является полная элиминация аллергенов.
Больным рекомендуется: не выезжать за город и в зеленую зону, ограничение прогулок; смена одежды после прогулок; ношение темных очков на улице; душ после пребывания на улице; кондиционирование воздуха в помещении; исключение продуктов с перекрестными аллергенными свойствами и фитотерапии.
В настоящее время для лечения больных с тяжелыми проявлениями поллиноза сконструированы безаллергенные палаты, снабженные системой тонкой очистки воздуха, позволяющей задерживать пыльцу.
Много лет с успехом применяется аллергенспецифическая иммунотерапия (АСИТ) или специфическая аллерговакцинация.
В процессе АСИТ: снижается тканевая чувствительность к аллергенам; уменьшается неспецифическая гиперреактивность тканей к различным медиаторам; уменьшаются признаки аллергического воспаления.
Фармакотерапия поллинозов состоит в использовании фармакологических средств, направленных на устранение основных симптомов ринита, конъюнктивита, бронхиальной астмы. Гистамин — главный медиатор, участвующий в развитии симптомов ринита и конъюнктивита. Антигистаминные препараты — основная патогенетическая терапия поллинозов в период обострения. Их действие связано с блокадой Н1-гистаминовых рецепторов. Принято разделять антигистаминные препараты на: седативные, или I поколения (классические), и неседативные, или II поколения (табл. 2).
Фармакологические эффекты антигистаминных лекарственных средств (АГЛС) I поколения: антигистаминное действие (блокада Н1-гистаминных рецепторов и устранение эффектов гистамина); антихолиргическое действие (уменьшение экзокринной секреции, повышение вязкости секретов); центральная холинолитическая активность (седативное, снотворное действие); усиление действия депрессантов ЦНС; потенцирование эффектов катехоламинов (колебание АД); местно-анестезирующее действие.
Антагонисты Н1-рецепторов I поколения имеют следующие недостатки: неполная связь с Н1-рецепторами (необходимы относительно высокие дозы); кратковременный эффект; блокирование М-холинорецепторов, α-адренорецепторов, кокаиноподобное и хинидиноподобное дейсствие; из-за развития тахифилаксии необходимо чередование АГЛС разных групп каждые 2-3 нед.
Широкое применение в лечении поллинозов нашли АГЛС II поколения (акривастин, астемизол, цетиризин, эбастин, лоратадин, фексофенадин, дезлоратадин). Они эффективны для купирования зуда, чихания и ринореи, но не действуют на заложенность носа. При пероральном приеме антигистаминные препараты оказывают выраженное действие также на конъюнктивит и сыпь. За исключением акривастина, все АГЛС II поколения используются 1 раз/сут.
Акривастин, астемизол, лоратадин и терфенадин трансформируются в активные метаболиты с помощью системы цитохрома Р450 в печени. Цетиризин и фексофенадин не метаболизируются в печени и выводятся в неизменном виде с мочой и калом. Дезлоратадин (эриус) представляет собой активный метаболит лоратадина и не связан с Р450. Система цитохрома Р450 отвечает за метаболизм и других лекарственных препаратов, обладающих конкурентным действием. Одновременное назначение терфенадина и астемизола с противогрибковыми препаратами (кетоконазол), макролидными антибиотиками (эритромицин), грейпфрутовым соком приводит к кардиотоксическому эффекту, в связи с чем эти препараты исключены из продажи на территории России. У остальных препаратов II поколения отсутствуют клинические данные, позволяющие связать развитие осложнений с приемом данных препаратов. II поколение антигистаминных препаратов вызывает заметно меньше нежелательных кардиотоксических и холинергических эффектов, чем их предшественники I поколения.
Лоратадин— противоаллергический эффект развивается в течение первого часа после приема внутрь и сохраняется 24 ч. Препарат не проникает через гематоэнцефалический барьер, следовательно, не влияет на ЦНС и не оказывает седативного действия; лишен антихолинергической активности. Прием пищи не влияет на абсорбцию лоратадина. Возраст, нарушение функции печени, почек не влияет на показатели фармакокинетики. Лоратадин характеризуется высоким профилем безопасности, редко встречаются жалобы на утомляемость, головную боль, сухость во рту, тошноту, сердцебиения. Возможно повышение концентрации лоратадина в плазме при сочетании с эритромицином, кетоконазолом, циметидином без изменений на ЭКГ и клинических проявлений.
Цетиризин — метаболит гидроксизина, в терапевтических дозах не вызывает антихолинергического и антисеротонинового эффекта, не усиливает действие алкоголя. В основном, цетиризин выводится в неизмененном виде почками, небольшое количество метаболизируется в печени. У пациентов с нарушением функции почек общий клиренс цетиризина уменьшается, в связи с этим необходимо снижение дозы в 2 раза. При применении цетиризина в терапевтических дозах не выявлено клинических нарушений способности концентрации внимания и быстроты психомоторных реакций, редко встречаются сухость во рту, диспептические расстройства, преходящая сонливость, головная боль, утомляемость. Препарат не усиливает действие алкоголя. Препарат разрешен к применению у детей с 2-летнего возраста. Взаимодействия с другими ЛС не установлены.
Фексофенадин — первый примененный в клинике метаболит антигистаминных препаратов II поколения. Фексофенадин — активный метаболит терфенадина, характеризуется высокой селективностью к H1-гистаминовым рецепторам и отсутствием антихолинергических и антиадренергических свойств. Фексофенадин не проникает через гематоэнцефалический барьер, клинически эффективен в неизмененном виде, без предшествующего метаболизма. Фексофенадин не блокирует медленные калиевые каналы, следовательно, не вызывает изменение интервала Q-T. Препарат быстро всасывается при приеме внутрь, максимальная концентрация в плазме достигается через 1–3 ч, а длительность действия составляет 24 ч. Возможно совместное назначение с противогрибковыми препаратами и макролидами без корректировки дозы. Прием пищи не снижает абсорбции препарата, при длительном использовании нет эффекта кумуляции.
Дезлоратадин — активный метаболит лоратадина. Препарат обладает сходными фармакологическимим свойствами, однако по активности превосходит лоратадин. Дезлоратадин ингибирует многие цитокины, хемокины, молекулы адгезии. Препарат назначается 1 раз/сут, безопасен при нарушении функции печени. Не вызывает сонливости и удлинения интервала Q-T на ЭКГ. Прием пищи не оказывает влияния на всасывание ЛС. Изучается антигистаминное, противоастматическое и противовоспалительное действие препарата.
Топические глюкокортикостероиды-ГКС (беклометазон, будесонид, флунизолид, флютиказон, мометазон, триамцинолон) являются наиболее эффективными препаратами для контроля местных симптомов при поллинозах, особенно при выраженной ринорее и пыльцевой бронхиальной астме. Регулярное профилактическое использование топических ГКС у взрослых и детей эффективно уменьшает заложенность носа, ринорею, чихание и зуд и предотвращает развитие приступов удушья. Топические ГКС уменьшают назальную и бронхиальную гиперреактивность, активно уменьшают воспаление слизистой; эффект проявляется через 6–12 ч и достигает максимума через несколько дней. Кроме того, использование топических глюкокортикостероидов позволяет снизить курсовую стоимость лечения.
Системные ГКС применяются при неэффективности других препаратов и притяжелых проявлениях поллиноза. Как правило, назначают короткие курсы (< 3 нед) до полного купирования симптомов.
Кромоны, используемые для лечения поллинозов, представлены динатриевой солью кромоглициевой кислоты (кромолин, ДСКК) и недокромилом натрия. Предполагают, что кромоны блокируют кальциевые каналы мембран тучных клеток, ингибируют фосфодиэстеразу или ингибируют окислительное фосфорилирование. Эффективность кромонов при пыльцевом рините остается спорной, особенно по сравнению с топическими кортикостероидами и антигистаминными препаратами. Следовательно, кромоны не могут считаться препаратами выбора, хотя они и играют определенную роль при профилактическом лечении конъюнктивитов, а также в начальных стадиях и при легких формах ринита и бронхиальной астмы.
Деконгенстанты (сосудосуживающие препараты) регулируют тонус симпатической иннервации кровеносных сосудов, активируя адренергические рецепторы и вызывая вазоконстрикцию. Включают α1-адреномиметики (например, фенилэфедрин), α2-адреномиметики (например, оксиметазолин, ксилометазолин, нафазолин), вещества, способствующие выделению норадреналина (например, эфедрин, псевдоэфедрин). Топические деконгестанты очень эффективны в лечении заложенности носа. Длительное (> 10 дней) использование препаратов может приводить к тахифилаксии, рикошетному отеку слизистой оболочки носа и развитию медикаментозного ринита, поэтому продолжительность применения должна быть ограничена 10 днями. Не рекомендуется применение у детей младше 1 года и у взрослых старше 60 лет, беременных; при гипертензии и кардиопатии, при гипертиреозе, гипертрофии простаты, глаукоме, психических заболеваниях, при приеме α-блокаторов или ингибиторов моноаминооксидазы.
При пыльцевых ринитах используют и антихолинергические препараты. Ипратропиум бромид эффективен в лечении заболеваний, сопровождающихся ринореей, но он не действует на чихание и заложенность носа. Действие препарата наступает через 15–30 мин. Характерно дозозависимое побочное антихолинергическое действие. Эти препараты могут применяться в комплексе с другими средствами.
Лечение бронхиальной астмы следует проводить в соответствии с рекомендациями GINA 2002 г. Для купирования приступов удушья используют β2-агонисты; для базисной терапии применяют кромоны, топические ГКС.
Безопасность топических ГКС убедительно доказана при пыльцевых рините и астме. В больших дозах они могут давать побочные эффекты. При одновременном применении назальных и ингаляционных ГКС возможно суммирование побочных эффектов.
Объем терапии поллиноза зависит от степени тяжести процесса. У больных с интермиттирующим и легким персистирующим течением используют: топические АГЛС или препараты кромогликата натрия, при неэффективности местной терапии — АГЛС II поколения. При среднетяжелым течении — топические ГКС в сочетании с АГЛС II поколения. В качестве дополнительной терапии возможно применение глазных капель кромогликата натрия, ГКС, деконгестантов. При тяжелом течении поллиноза к данной терапии при крайней необходимости возможно назначение системных ГКС. Для лечения пыльцевой аллергии рассматривается возможность использования антилейкотриеновых ЛС.
Таким образом, основными принципами лечения поллиноза являются элиминация аллергена, АСИТ, фармакотерапия. АСИТ назначает и проводит только врач-аллерголог, в связи с чем все больные с пыльцевой аллергией должны находиться на диспансерном учете в аллергологическом кабинете.
Л. А. Горячкина, профессор, доктор медицинских наук
Е. В. Передкова, доцент, кандидат медицинских наук.
Е. Р. Бжедугова РМАПО, ГКБ №52, г. Москва
Читайте также:

