Что такое посттравматическая инфекция
Обновлено: 05.05.2024
Ключевые слова: COVID-19, посттравматическое стрессовое расстройство, психотерапия, фармакотерапия, фабомотизол, анксиолитик.
“Сoronavirus syndromе”: prevention of phsychotrauma caused by COVID-19
N.V. Solovieva 1 , E.V. Makarova 1,2 , I.V. Kichuk 3
1 Personilized Psychiatry JSC, Moscow
2 National Medical Research Center of Rehabilitation and Resort Medicine, Moscow
3 Pirogov Russian National Research Medical University, Moscow
COVID-19 (COronaVIrus Disease 2019) is a new viral infection characterized by rapid spread, high mortality rate, significant social and economic consequences that destroy the usual way of life. Coronavirus syndrome is a mental disorder presenting itself a response to the COVID-19 pandemic. Presumably, the coronavirus syndrome will affect up to 10% of the population involved in the pandemic, mainly people who have been exposed to a combination of psychosocial and biological factors of stress vulnerability. The article discusses predisposing factors and clinical manifestations of coronavirus syndrome. The risk groups of developing coronavirus syndrome are medical workers who provide care to patients with COVID-19; patients who have suffered a severe disease form, lost relatives and friends, as well as those who have suffered extensive financial losses and lost their jobs. The authors consider treatment methods for coronavirus syndrome: psychotherapy (cognitive behavioural therapy with narrative and exposure methods) and pharmacotherapy, which should be aimed at relieving anxiety, restoring sleep, treating depression and other mental disorders. The a uthors also emphasize that timely psychotherapy and pharmacotherapy of the coronavirus syndrome is very important since it is assumed that this syndrome will reduce the work productivity of the population at a time when it will be extremely necessary for economic recovery.
Keywords: COVID-19, post-traumatic stress disorder, psychotherapy, pharmacotherapy, fabomotizol, anxiolytic.
For citation: Solovieva N.V., Makarova E.V., Kichuk I.V. “Coronavirus syndromе”: prevention of phsychotrauma caused by COVID-19. RMJ. 2020;9:18–22.
Введение
Клинические проявления стрессовых расстройств
Клиническая картина ПТСР развивается в течение периода от 30 дней до 6 мес. после случившегося эпизода и затрагивает до 10% лиц, его переживших [12].
ПТСР проявляется дезадаптацией психики (психобиологической дисфункцией) и сопровождается множеством внутриличностных и межличностных конфликтов, переосмыслением или утратой смысла жизни, крушением устоявшихся идеалов и неверием в успешное будущее, иными словами — той или иной степенью экзистенциального кризиса [13].
Среди клинических признаков ПТСР можно выделить [14–19]: постоянно повторяющиеся воспоминания о стрессовой ситуации; акцентуацию черт характера; снижение социальной активности, недоверие к окружающим; нарушения мышления, формирование патологических идей и установок; формирование обсессий и компульсий; аффективные симптомы, связанные с повышенной эмоциональной возбудимостью, агрессией, раздражительностью либо подавленностью, апатией и депрессией; неприятие реальности; алкоголизм, наркоманию, девиантное поведение; трудности концентрации внимания, когнитивный дефицит; нарушения сна в виде плохого качества сна, затруднения засыпания, кошмарных сновидений либо гиперсомнии. Чем травма тяжелее, тем больше вероятность развития расстройства, однако оно возникает не у всех даже при серьезной психологической травме. Таким образом, существует ряд факторов, которые определяют уязвимость человека и его способность к быстрому восстановлению. Более того, по данным B. Frueh et al. (2005), клинические проявления ПТСР после войны возникали у многих людей, никогда не участвовавших в боях [20].
Исследования, направленные на поиск морфологических и биохимических отклонений при ПТСР, выявили уменьшение объема гиппокампа у пациентов [21, 22] (однако этот феномен является предпосылкой к развитию дезадаптации в ответ на травму) и специфические нейротрансмиттерные изменения: дисфункцию моноаминергических систем [23] и рецепторов γ-аминомасляной кислоты (ГАМК) [24, 25], а также уменьшение концентрации кортизола в плазме крови в связи с индукцией отрицательной обратной связи по гипоталамо-гипофизарно-адреналовой оси [26].
Сама по себе психическая и/или соматическая реакция на стрессовое событие представляется совершенно естественной. Не любое ее проявление стоит рассматривать как патологию. Более того, определенный уровень стресса будет, напротив, расширять адаптационные возможности организма в дальнейшем [27]. По наблюдениям психологов, эмоциональные всплески, переживание и проговаривание своих страхов, гнева, раздражения, с последующей рефлексией негативного опыта способствуют интеграции травмы и более быстрой компенсации психического состояния [28, 29]. Хроническим считается стрессовое расстройство, затянувшееся более 3 мес. [30], однако нормативные параметры в данном вопросе всегда очень индивидуальны, а врач, в свою очередь, должен обращать внимание на проявления дезадаптации, степень снижения работоспособности и качества жизни, наличие у пациента критического отношения к своему состоянию.
К группам повышенного риска можно отнести следующих лиц:
медицинские работники, особенно врачи, оказывающие помощь пациентам с COVID-19 в условиях повышенной нагрузки, дефицита информации о заболевании, отсутствия вакцин и специфических лекарственных средств, нехватки средств индивидуальной защиты;
люди других профессий, вынужденные продолжать работать во время эпидемии, подвергая себя риску заражения;
пациенты, перенесшие COVID-19, особенно в случае госпитализации при тяжелом течении болезни;
люди, утратившие близких и родственников;
люди, потерявшие работу и понесшие финансовые потери;
лица, злоупотребляющие психоактивными веществами.
Второй биологический фактор — наличие в анамнезе негативных факторов, делающих психику человека менее гибкой. К таким факторам относятся гипертоническая болезнь, сахарный диабет, ожирение, атеросклероз сосудов головного мозга, патология щитовидной железы, дисбаланс половых гормонов, наличие в анамнезе черепно-мозговых травм, коматозных состояний, нейроинфекций, отравлений алкоголем, наркотическими веществами, угарным газом и другими токсическими веществами, дефицит нутриентов, витаминов, микро- и макроэлементов различного генеза и пр. [34].
Многие отмечают измененное чувство времени (один день будто бы длится бесконечно) и нарушения сна (трудности засыпания, прерывистый сон, кошмарные сновидения), снижение мотивации и чувство потерянности. У людей с психическими заболеваниями в анамнезе вероятны обострения психических расстройств. В отсутствие строгого регламента жизни возрастает процент употребления психоактивных веществ и алкоголя, случаи конфликтов и драк на этом фоне. Вполне ожидаемы вегетативные и психосоматические проявления [30].
У значительной части людей данный этап ограничится мобилизацией сил, сопровождающейся специфическими биологическими изменениями в организме без клинических проявлений. В первую очередь, рецепторы γ-аминомасляной кислоты (ГАМК) из-за избыточной нагрузки становятся менее чувствительными к аффинному медиатору ГАМК, что приводит к нарушению физиологических процессов торможения в ЦНС и повышению уровня тревоги [24]. Затем изменяется работа всей моноаминергической системы, что в последующем приводит к дисфункции серотонина, дофамина, норадреналина [23, 37, 38], уменьшается концентрация кортизола в плазме крови (в связи с индукцией отрицательной обратной связи по гипоталамо-питуитарно-адреналовой оси) [27].
При длительной стрессовой ситуации в данном периоде может развиваться расстройство адаптации, или стрессорное расстройство, — состояние неадекватной реакции организма на стрессовые ситуации, которое может проявляться повышенной тревожностью и напряженностью, беспокойством, депрессивным настроением, астенией, но при этом не достигать развернутой картины тревожных и депрессивных расстройств.
3-й этап. ПТСР. Разовьется после осознания социумом и отдельными людьми реальности проблемы и ее последствий. Это отсроченная реакция на стресс, которая развивается спустя 1 мес. или полгода после окончания пандемии. Она может возникать и у людей, которые не имели никаких психических расстройств на первых двух этапах.
Можно выделить следующие клинические проявления: личностная и социальная дезориентация, чувство потери смысла жизни; раздражительность, эмоциональная лабильность; заострение личностных особенностей; депрессия, апатия, снижение общего тонуса и работоспособности либо маниакальные проявления при низкой продуктивности деятельности; усиление психоэмоционального напряжения, тревожности и беспокойства, чрезмерная бдительность, особенно ко всему, что кажется угрожающим по отношению к здоровью, личному пространству, финансовому благополучию; обострение чувства самости, вплоть до эгоцентризма.
На этом этапе особенно актуальными станут жалобы на нарушения внимания, трудности запоминания, удерживание в памяти той или иной информации, трудности ее воспроизведения. Это связано не напрямую с нарушениями памяти, а с тем, что внимание человека фиксировано на пережитом, не распространяется на настоящие события жизни, не может переключиться на текущие задачи и проблемы. Из-за этого будут страдать трудоспособность, общение, образ жизни. Повышается степень внушаемости, что увеличивает риск стать жертвой мошенничества. Напряжение будет поддерживаться всем, напоминающим об инфекции или изоляции, о необходимости жесткого соблюдения дисциплины.
Клинические проявления могут быть более серьезными у врачей, работающих с COVID, людей, потерявших родных и близких, место работы или свой бизнес. В этой группе гораздо больше шансов воспринять ситуацию как непосредственную травму и, следовательно, выше риск формирования развернутой картины ПТСР с такими серьезными симптомами, как:
Навязчивые и угнетающие воспоминания о событиях, снова и снова повторяющиеся переживания ярких моментов, связанных с эпидемией, иногда флешбэки — внезапные, яркие, повторные переживания. Флешбэки бывает трудно отличить от действительности, во время них может возникать помрачение сознания, иногда с агрессией.
Переживание неизбежности утраты, собственного бессилия.
Тяжелые сновидения, могут быть нарушения засыпания с наплывами неприятных воспоминаний, ночные пробуждения и ранние пробуждения в состоянии тревоги.
Страх повторения пережитого кошмара, фобии, панические атаки.
Значимое падение работоспособности и апатия либо развитие гиперастении, вплоть до разрушающей нецелесообразности.
Настроение на данном этапе снижено, нет интереса к новому, к ранее значимой активности, взгляд в будущее пессимистичен, сложно увидеть перспективы развития, что вызывает раздражительность, вспышки злобы, идет поиск виновных на стороне или попытка определить степень своей виновности, вплоть до самобичевания. Возможно возникновение или обострение уже имеющихся соматических заболеваний. Высок риск злоупотребления алкоголем, каннабиноидами, начала употребления иных психоактивных веществ.
Биологические изменения с повышением патологической активности головного мозга на этом этапе можно увидеть на электроэнцефалограмме в виде увеличения спектральной мощности и снижения когерентности между височными, височно-теменными и теменно-лобными отделами головного мозга [39], тенденции к общей десинхронизации: увеличение мощности β-ритма, снижение относительной представленности α-диапазона [40–42].
Осложнения связаны с удлинением стрессовой реакции, невротизацией и психопатизацией личности, а также с переходом невротического расстройства в органическое (особенно при употреблении психоактивных веществ). Присутствует риск не только утраты пластичности общения и способности приспосабливаться к происходящему, заострения личностных особенностей (формирования эксплозивных, истерических, демонстративных или шизоидных черт характера), но и появления цинизма, склонности к антисоциальным действиям или бездействию, ограничения коммуникаций, зачастую на фоне алкоголя и/или наркотиков. Также существует риск суицида.
Профилактика и лечение
Всеми специалистами отмечается, что лечение ПТСР — это сложная и длительная задача. Национальный институт здравоохранения и усовершенствования медицинского обслуживания (The National Institute for Health and Care Excellence, NICE) в стандартах помощи пациентам со стрессовыми расстройствами (2018) [15] предлагает руководствоваться следующими принципами:
поддержка (от специалистов здравоохранения, вовлечение пациентов в специальные группы общения, предоставление информации);
создание безопасной среды;
вовлечение родных и близких в проблему;
активное взаимодействие с пациентом в процессе составления плана лечения;
активный мониторинг состояния больного.
В качестве профилактических вмешательств рассматривается:
Психотерапия. Наиболее эффективной считается когнитивно-поведенческая терапия с нарративным и экспозиционным подходами. Терапия должна быть направлена на принятие пандемии COVID-19 и ее последствий как данность, десенсибилизацию и переработку психотравмы, формирование перспектив будущего, новых паттернов поведения.
Фармакотерапия, которая должна быть направлена на купирование тревоги, восстановление сна, лечение депрессии и иных психических отклонений. При отсутствии глубоких психических нарушений, в т. ч. при выявлении расстройства адаптации, желательно стремиться к назначению препаратов, не оказывающих тормозящего действия на работу ЦНС и способствующих адаптации психики к происходящим изменениям. Подобный подход можно назвать профилактической фармакотерапией, направленной на предотвращение усугубления симптоматики и развития глубоких тревожных и депрессивных расстройств. Как правило, в таком случае терапия направлена на восстановление физиологических процессов торможения в ЦНС, реализующихся через ГАМК-бензодиазепиновые рецепторы. К подобным препаратам селективного (т. е. избирательного) действия относится современный анксиолитик Афобазол ® (международное непатентованное наименование: фабомотизол). Препарат воздействует на σ-1-рецепторы в нейронах, что приводит к восстановлению их структур и функций, нарушающихся на фоне хронического стресса. Происходящее восстановление структуры и функции ГАМК-бензодиазепиновых рецепторов приводит к восстановлению их чувствительности к эндогенным медиаторам торможения, что в свою очередь приводит к восстановлению процессов торможения в ЦНС, снижению проявлений чрезмерной тревоги и повышению адаптационных возможностей психики. Отсутствие тормозящего действия на ЦНС приводит к тому, что данный препарат не вызывает дневной сонливости, нарушения памяти и концентрации внимания, а также привыкания и зависимости при длительном применении. Эффективность и благоприятный профиль безопасности фабомотизола были подтверждены в многочисленных исследованиях и программах клинического наблюдения, проведенных у пациентов с генерализованным тревожным расстройством, расстройством адаптации, а также у пациентов с широким спектром тревожных расстройств на фоне имеющейся соматической патологии. Применение препарата Афобазол ® способствует снижению тревоги, напряженности, страхов и опасений, депрессивного настроения, беспокойства, раздражительности, бессонницы. Обычно курс терапии составляет от 1 до 3 мес. [43]. Препарат хорошо переносится и поэтому доступен в аптеках без рецепта.
В случае формирования ПТСР подходы в лечении остаются похожими, однако работа с психотерапевтом может занять более длительный период и потребовать назначения более серьезных препаратов [44]. Цель лечения — помочь психике адаптироваться, восстановить у пациента социальную активность, работоспособность, улучшить психическое и физическое качество жизни. Лечение может занять от 6 до 12 нед. и дольше [14–16].
Заключение
Благодарность
Политравма – это одновременное или практически одновременное возникновение двух и более травматических повреждений, каждое из которых требует специализированного лечения. Для политравмы характерно наличие синдрома взаимного отягощения и развитие травматической болезни, сопровождающееся нарушениями гомеостаза, общих и местных процессов адаптации. При таких повреждениях, как правило, требуется интенсивная терапия, экстренные операции и реанимационные мероприятия. Диагноз выставляется на основании клинических данных, результатов рентгенографии, КТ, МРТ, УЗИ и других исследований. Перечень лечебных процедур определяется видом травмы.
МКБ-10
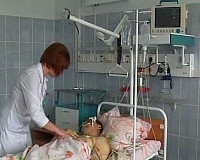
Общие сведения
Политравма – обобщающее понятие, означающее, что у пациента одновременно имеется несколько травматических повреждений. При этом возможно как поражение одной системы (например, костей скелета), так и нескольких систем (например, костей и внутренних органов). Наличие полисистемных и полиорганных поражений негативно влияет на состояние больного, требует проведения интенсивных лечебных мероприятий, повышает вероятность развития травматического шока и летального исхода.
Классики травматологии и ортопедии рассматривали политравму преимущественно, как проблему военного времени. В наши дни в связи с механизацией промышленности и широким распространением автомобильного транспорта резко возросло количество политравм, полученных в мирных условиях вследствие автодорожных происшествий и несчастных случаев на производстве. Лечение политравмы обычно осуществляют врачи-травматологи при участии реаниматологов. Кроме того, в зависимости от вида и локализации повреждений, в диагностике и лечении политравмы могут участвовать торакальные хирурги, абдоминальные хирурги, урологи, нейрохирурги и другие специалисты.

Причины политравмы
Самыми распространенными являются множественные повреждения в результате автодорожных происшествий (более 50%), второе место занимают несчастные случаи на производстве (более 20%), третье – падения с высоты (более 10%). Мужчины страдают примерно вдвое чаще женщин. В 1-5% от общего количества случаев политравмы пострадавшими являются дети, основной причиной является участие в ДТП (дети младшего возраста – как пассажиры, в старших возрастных группах преобладают случаи наездов на детей-пешеходов и велосипедистов). У детей при политравме чаще наблюдаются ранения нижних конечностей и ЧМТ, а травмы брюшной полости, грудной клетки и костей таза выявляются реже, чем у взрослых.
У взрослых при политравме в результате автодорожных происшествий преобладают повреждения конечностей, ЧМТ, травмы грудной клетки, травмы брюшной полости, переломы таза, разрывы мочевого пузыря и повреждения шейного отдела позвоночника. Наибольшее влияние на прогноз для жизни оказывают травмы брюшной полости, грудной клетки и черепно-мозговые травмы. При случайных падениях с большой высоты чаще выявляется тяжелая черепно-мозговая травма, при попытках самоубийства – множественные повреждения нижних конечностей, поскольку пациенты практически всегда прыгают ногами вперед. Падения с высоты нередко сопровождаются разрывом внутриторакальных сосудов, что приводит к быстрому развитию геморрагического шока.
Классификация
Отличительными чертами политравмы являются:
- Синдром взаимного отягощения и травматическая болезнь.
- Атипичные симптомы, затрудняющие диагностику.
- Высокая вероятность развития травматического шока и массивной кровопотери.
- Нестойкость механизмов компенсации, большое количество осложнений и летальных исходов.
Различают 4 степени тяжести политравмы:
- Политравма 1 степени тяжести – имеются легкие повреждения, шок отсутствует, исходом становится полное восстановление функции органов и систем.
- Политравма 2 степени тяжести – имеются повреждения средней степени тяжести, выявляется шок I-II степени. Для нормализации деятельности органов и систем необходима длительная реабилитация.
- Политравма 3 степени тяжести – имеются тяжелые повреждения, выявляется шок II-III степени. В исходе возможна частичная или полная утрата функций некоторых органов и систем.
- Политравма 4 степени тяжести – имеются крайне тяжелые повреждения, выявляется шок III-IV степени. Деятельность органов и систем грубо нарушена, существует высокая вероятность летального исхода как в остром периоде, так и в процессе дальнейшего лечения.
С учетом анатомических особенностей выделяют следующие виды политравмы:
- Множественная травма – два или более травматических повреждения в одной анатомической области: перелом голени и перелом бедра; множественные переломы ребер и т. д.
- Сочетанная травма – два или более травматических повреждения разных анатомических областей: ЧМТ и повреждение грудной клетки; перелом плеча и повреждение почки; перелом ключицы и тупая травма живота и т. д.
- Комбинированная травма – травматические повреждения в результате одновременного воздействия различных травмирующих факторов (термического, механического, радиационного, химического и т. д.): ожог в сочетании с переломом бедра; радиационное поражение в сочетании с переломом позвоночника; отравление токсическими веществами в сочетании с переломом таза и т. д.
Сочетанные и множественные повреждения могут являться частью комбинированной травмы. Комбинированная травма может возникать при одновременном прямом действии поражающих факторов или развиваться вследствие вторичного повреждения (например, при появлении очагов пожара после обрушения производственной конструкции, ставшей причиной перелома конечности).
С учетом опасности последствий политравмы для жизни пациента различают:
- Нежизнеопасную политравму – повреждения, не вызывающие грубых нарушений жизнедеятельности и не представляющие непосредственной опасности для жизни.
- Жизнеопасную политравму – повреждения жизненно важных органов, которые можно скорректировать путем своевременного хирургического вмешательства и/или адекватной интенсивной терапии.
- Смертельную политравму – повреждения жизненно важных органов, деятельность которых невозможно восстановить даже путем оказания своевременной специализированной помощи.
С учетом локализации выделяют политравму с поражением головы, шеи, груди, позвоночника, таза, живота, нижних и верхних конечностей.
Диагностика
Диагностика и лечение при политравме зачастую представляют собой единый процесс и осуществляются одновременно, что обусловлено тяжестью состояния пострадавших и высокой вероятностью развития травматического шока. В первую очередь оценивается общее состояние пациента, исключаются или выявляются повреждения, которые могут представлять опасность для жизни. Объем диагностических мероприятий при политравме зависит от состояния пострадавшего, к примеру, при выявлении травматического шока осуществляют жизненно важные исследования, а диагностику мелких повреждений проводят, по возможности, во вторую очередь и только если это не утяжеляет состояние больного.
Всем пациентам с политравмой выполняют срочные анализы крови и мочи, а также определяют группу крови. При шоке осуществляют катетеризацию мочевого пузыря, контролируют количество выделяемой мочи, регулярно измеряют АД и пульс. В ходе обследования может быть назначена рентгенография грудной клетки, рентгенография костей конечностей, рентгенография таза, рентгенография черепа, эхоэнцефалография, диагностическая лапароскопия и другие исследования. Больных с политравмой осматривают травматолог, нейрохирург, хирург и реаниматолог.
Лечение политравмы
На начальном этапе лечения на первый план выступает противошоковая терапия. При переломах костей осуществляют полноценную иммобилизацию. При размозжениях, отрывах и открытых переломах с массивным кровотечением производят временную остановку кровотечения с использованием жгута или кровоостанавливающего зажима. При гемотораксе и пневмотораксе проводят дренирование грудной полости. При повреждении органов брюшной полости выполняют экстренную лапаротомию. При сдавлении спинного и головного мозга, а также при интракраниальных гематомах производят соответствующие операции.
Если есть повреждения внутренних органов и переломы, являющиеся источником массивного кровотечения, хирургические вмешательства осуществляют одновременно двумя бригадами (хирурги и травматологи, травматологи и нейрохирурги и т. д.). Если массивное кровотечение из переломов отсутствует, открытую репозицию и остеосинтез переломов при необходимости производят после вывода пациентов из шока. Все мероприятия проводят на фоне инфузионной терапии.
Затем пациентов с политравмой госпитализируют в отделение реанимации или палату интенсивной терапии, продолжают инфузии крови и кровезаменителей, назначают препараты для восстановления функций органов и систем, осуществляют различные лечебные мероприятия (перевязки, смену дренажей и т. д.). После улучшения состояния больных с политравмой переводят в травматологическое (реже – нейрохирургическое или хирургическое отделение), продолжают лечебные процедуры, проводят реабилитационные мероприятия.
Прогноз и профилактика
Травматическая болезнь – общий ответ организма на травматическое воздействие. Включает в себя ряд приспособительных и патологических реакций, а также местных и общих изменений, происходящих в организме с момента травмы до выздоровления или смерти больного. Влияет на исход травмы, в значительной степени определяет прогноз в отношении жизни и трудоспособности. Включает в себя изменения в психоэмоциональной сфере, процессах метаболизма и гемостаза, состоянии иммунной системы, работе сердца, легких, органов пищеварения и ЦНС. Имеет стадийное течение.
МКБ-10
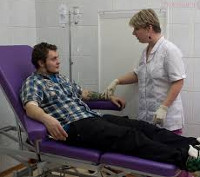
Общие сведения
Травматическая болезнь – относительно новая концепция в травматологии, позволившая пересмотреть отношение к травме. Ранее как в практической медицине, так и в научных работах доминировал взгляд на травму, как на изолированное поражение определенного органа. Формирование концепции травматической болезни дало возможность рассмотреть изменения, происходящие в организме больного, как единую систему взаимосвязанных процессов. В настоящее время данная концепция считается общепризнанной и широко используется практическими врачами: травматологами, реаниматологами, терапевтами, хирургами, психологами, иммунологами, кардиологами, физиотерапевтами и другими специалистами, которые принимают участие в лечении больного на стационарном и поликлиническом этапах.

Первый период травматической болезни
Начинается сразу после травматического воздействия и продолжается 6-12 часов. Может проявляться в виде терминального состояния или травматического шока. При повреждении груди возможно развитие острой сердечной или дыхательной недостаточности, при черепно-мозговых травмах – травматическая кома. В этом периоде пациенты находятся либо на догоспитальном этапе, либо на этапе поступления и обследования. На догоспитальном этапе проводят временную иммобилизацию, инфузионную терапию, искусственное дыхание, обезболивание и т. д.
При поступлении в стационар на фоне продолжающихся реанимационных мероприятий осуществляют неотложные инвазивные манипуляции интенсивной терапии (трахеостомию, катетеризацию подключичной артерии, катетеризацию мочевого пузыря и т. д.). Выполняют диагностические манипуляции (люмбальную пункцию, лапароцентез), а также манипуляции и операции, направленные на устранение состояний, представляющих непосредственную угрозу для жизни пациента (плевральную пункцию, торакоскопию, лапароскопию и т. д.).
При благоприятном развитии событий этап завершается постановкой диагноза, устранением жизнеугрожающих состояний, относительной стабилизацией показателей дыхания и кровообращения и возмещением кровопотери. Из противошоковой палаты или операционной больных переводят в отделение реанимации. Основной причиной смерти пациентов в этом периоде являются несовместимые с жизнью повреждения, тяжелый шок и массивная кровопотеря с развитием ДВС-синдрома.
Второй период травматической болезни
Продолжается 12-48 часов. На этом этапе пульс, артериальное давление и другие показатели сохраняются в пределах нормы или приближаются к своим нормальным значениям, но организм функционирует неустойчиво. Пациенты находятся в отделении реанимации, им проводят интенсивную терапию. При необходимости в этом периоде осуществляют срочные хирургические вмешательства: операции на спинном мозге, позвоночнике, костях, магистральных сосудах конечностей и т. д.
План лечения, объем и способ оперативных вмешательств определяют индивидуально, с учетом характера травм, вероятности развития опасных осложнений, возраста и общего состояния больного, наличия острых и хронических заболеваний. В одних ситуациях оказывается целесообразным отложить операцию на более поздний срок, чтобы не увеличить опасность для жизни пациента. В других, напротив, может быть показано одновременное вмешательство на нескольких областях тела. Основной причиной гибели пострадавших в этом периоде является полиорганная недостаточность.
Третий период травматической болезни
Начинается на третьи сутки, может продолжаться до двух недель. На этом этапе наиболее высока вероятность развития осложнений. Во время предыдущих периодов организм пациента страдал от кровопотери, ДВС-синдрома и эндотоксикоза. Все перечисленное стало причиной формирования множественных очагов микротромбозов во внутренних органах: почках, кишечнике, печени, селезенке, легких и сердце. Теперь микроорганизмы, попадающие в кровь из ран, кишечника и верхних дыхательных путей, начали оседать в пострадавших участках, провоцируя образование очагов воспаления, отрыв тромбов и их миграцию по сосудистому руслу и т. д.
Особенно часто страдают легкие. Из-за воспаления базальная мембрана альвеол теряет способность пропускать кислород, в таких случаях возникает респираторный дистресс-синдром, заканчивающийся смертью в 90% случаев. У больных, перенесших тяжелый шок, на 3-6 сутки может развиться очаговая пневмония или синдром шокового легкого, также завершающийся летальным исходом. Возможна тромбоэмболия, а при тяжелой скелетной травме (например, переломе таза или переломе бедра) – и жировая эмболия.
Осложнения возникают с определенной периодичностью. Так, нарушения со стороны легких при травматической болезни обычно выявляются на 3-4 сутки, перитониты, гнойные трахеобронхиты, менингоэнцефалиты, а также местные инфекционные осложнения (миозиты, анаэробные целлюлиты, флегмоны и абсцессы) – на 6-10 сутки. Тактика лечения определяется индивидуально. Проводится антибиотикотерапия и дезинтоксикационная терапия, в ряде случаев требуются оперативные вмешательства.
Четвертый период травматической болезни
Продолжительность четвертого периода травматической болезни сильно колеблется в зависимости от локализации и тяжести травмы, а также от наличия и характера осложнений. Состояние организма постепенно улучшается, все жизненно важные функции нормализуются. В этом периоде осуществляются плановые операции по восстановлению поврежденных органов и тканей, назначается консервативное лечение, проводятся реабилитационные мероприятия. Степень восстановления органов, пострадавших в результате травмы или осложнений, может сильно варьировать.
Наряду с традиционными медицинскими мероприятиями на этом этапе большое значение приобретает работа по нормализации психологического состояния пациентов. Травма, сопровождающаяся утратой способности к самообслуживанию, изменением условий жизни и социального статуса, является тяжелейшим стрессом не только для тела, но и для психики. А продолжительное лечение еще больше усугубляет эти изменения. Может наблюдаться утрата мотивации, повышенная агрессивность, эмоциональная лабильность, депрессия, наличие эффекта вторичной выгоды и т. д. Поэтому современные ученые и практические врачи, специализирующиеся на лечении травматической болезни, рекомендуют проводить реабилитацию с участием психологов и психотерапевтов.
2. Шокогенная травма и травматическая болезнь (лекция) / Шапот Ю.Б., Селезнев С.А., Куршакова И.В., Карташкин В.Л. // Бюллетень ВСНЦ СО РАМН - 2005 - №3
3. Патологическая физиология и современные принципы лечения тяжелых сочетанных травм / Штейнле А.В. // Сибирский медицинский журнал (Томск) - 2009 - №3
Для цитирования: Зубеев П.С., Верещагин Н.А., Кудыкин М.Н. Посттравматическое воспаление мягких тканей и опорно-двигательного аппарата. РМЖ. 2013;15:819.
В клинической практике врачей любой специальности травма мягких тканей и опорно-двигательного аппарата занимает важное место. Наибольший уровень этого вида травм отмечается у мужчин в возрасте 20–50 лет, а у женщин – 30–59 лет, причем во всех возрастных группах данный показатель значительно выше у мужчин. По характеру повреждений около 50% травм – это вывихи, растяжения капсульно-связочного аппарата, травмы мышц и сухожилий, переломы костей верхних и нижних конечностей. Известно, что на любую травму организм отвечает неспецифической воспалительной реакцией – реактивным воспалением, которая является адаптационной и защитной реакцией и клинически проявляется болью, отеком и нарушением функции поврежденной области.
В лечении пациентов с повреждениями опорно-двигательной системы важной задачей является достижение быстрого и стойкого анальгетического эффекта, особенно в раннем посттравматическом или постоперационном периодах. Для решения этой задачи применяются нестероидные противовоспалительные препараты (НПВП), которые обладают как противовоспалительным, так и анальгетическим действием.
Как известно, действие НПВП основано, прежде всего, на ингибиции циклооксигеназ – ЦОГ-1 и ЦОГ-2. В современной фармакологии принято выделять селективные ингибиторы ЦОГ-1 и неселективные ингибиторы ЦОГ-1 и ЦОГ-2, преимущественно селективные ингибиторы ЦОГ-2 и высокоселективные ингибиторы ЦОГ-2 [1].
Позитивный лечебный эффект НПВП связан с подавлением активности ЦОГ-2 (циклооксигеназа 2-го типа). Этот фермент, участвующий в каскаде распада поврежденных при травме и других поражениях клеточных мембран, отвечает за выделение провоспалительных простагландинов и других медиаторов воспаления не только в суставах, но и в других органах и тканях, в первую очередь в стенках сосудов.
Выбор конкретного препарата определяется двумя основными параметрами: эффективностью и безопасностью [2, 3]. Длительное применение НПВП создает опасность целого ряда нежелательных реакций, основной из которых является их ульцерогенное действие. Чем более селективен препарат в отношении ЦОГ-2, тем менее выражен этот эффект, однако в то же время уменьшается анальгетическое действие препарата. У неселективных ингибиторов ЦОГ-1 и ЦОГ-2, наоборот, повышается риск нежелательных реакций со стороны желудочно-кишечного тракта (ЖКТ), но усиливается противовоспалительное и обезболивающее действие [1]. При необходимости проведения длительного курса лечения предпочтение обычно отдают селективным ингибиторам ЦОГ-2 [4].
Принципиальным моментом, который следует учитывать при выборе НПВП, считается скорость достижения клинического эффекта. Особое значение этот параметр имеет при купировании острых болевых синдромов, например травматического генеза. Известно, что НПВП с хорошей биодоступностью, максимально быстро создающие высокую пиковую концентрацию в крови, являются наиболее эффективными средствами для ургентного обезболивания. Быстрое развитие обезболивающего эффекта определяет необходимость их применения у пациентов с травмой и воспалением мягких тканей и опорно-двигательного аппарата. Однако большинство НПВП являются неселективными, что вызывает большое количество побочных эффектов и значительно снижает возможность использования лекарственных препаратов.
Преимущества селективных ингибиторов ЦОГ-2 в терапии болевых синдромов, в т.ч. при травме и в послеоперационном периоде, хорошо известны [5]:
1. Достоверное уменьшение частоты развития нежелательных явлений со стороны ЖКТ, почек, печени.
2. Отсутствие негативного влияния на синтез основных компонентов матрикса суставного хряща в отличие от неселективных НПВП.
3. Возможность длительного применения при заболеваниях и травмах суставов и пролонгация противовоспалительной терапии при необходимости (упорный синовит и др.).
Препаратом, обладающим указанными выше свойствами, является нимесулид. Ключевое значение имеет его высокая биодоступность – уже через 30 мин. после перорального приема достигается значимая концентрация препарата в крови, составляющая не менее 25% от максимальной. Полный обезболивающий и противовоспалительный эффект нимесулида отмечается через 1–3 ч после приема [6–8].
После перорального применения у здоровых добровольцев нимесулид (таблетка 100 мг) быстро всасывается и распределяется. Максимальная концентрация (Cmax) составляет от 2,86 до 6,50 мг/л, время до достижения максимальной концентрации (tmax) – 1,22–2,75 ч после применения. Средний период полувыведения – от 1,80 до 4,73 ч. Стабильный уровень концентрации достигается в течение 24–48 ч при ежедневном пероральном или ректальном приеме 2 р./сут. [9]. При клиническом использовании НПВП в течение длительного времени у пожилых пациентов, которые обладают повышенной чувствительностью к этим препаратам, довольно часто наблюдаются побочные эффекты [10]. Безопасной альтернативой в таких ситуациях является применение местных НПВП, что приводит к уменьшению системных побочных явлений.
Проведенное группой авторов исследование эффективности местного применения нимесулида показало, что данное лекарственное средство проникает трансдермально и достигает биофазы (синовиальной жидкости) в достаточной для производства его главной фармакологической активности (ингибирование ЦОГ) концентрации и, следовательно, оказывает положительное клиническое воздействие на болевой синдром, тугоподвижность суставов и адекватное функционирование пораженного органа [11]. Следует отметить, что степень проникновения препарата и скорость достижения биофазы зависят от его липофильности и увлажнения рогового слоя эпидермиса, а также от состояния барьерной функции кожи [12]. Клинический эффект данных средств определяется концентрацией действующего вещества, оптимальной терапевтической дозой, обеспечивающей анальгетический и противовоспалительный эффекты. Гели по сравнению с мазями являются более перспективной лекарственной формой, т.к. имеют рН, близкий к рН кожи, не закупоривают ее поры, быстро и равномерно распределяются. При их использовании создается высокая концентрация действующего вещества в периартикулярных тканях, а в кровоток препарат поступает в минимальной концентрации, не вызывающей каких-либо системных нежелательных реакций [13].
Клиническая эффективность топических средств при различных заболеваниях опорно-двигательного аппарата, включая травмы мягких тканей, суставов и связочного аппарата, была изучена в ряде исследований. Согласно полученным данным, в случае острой фазы артрита (первые 18 ч), как и в случае хронической фазы артрита (14 дней), гель нимесулид оказался эффективнее, чем гели диклофенак и пироксикам [14]. Применение нимесулида показало быстрое наступление лечебного эффекта. Авторами был сделан вывод, что хороший анальгетический эффект геля, содержащего нимесулид, позволяет применять препарат локально, что может быть более безопасным и эффективным методом лечения, чем назначение внутрь или ректально [15].
Основанием для проведения открытого сравнительного исследования геля диклофенак и геля нимесулид при РА послужил дискутируемый в литературе вопрос о выраженности анальгетического эффекта неселективных и селективных по отношению к ЦОГ-2 НПВП [16]. В результате оказалось, что анальгезирующий эффект обоих препаратов сопоставим. Выраженность боли в исследуемом коленном суставе достоверно уменьшалась как при ходьбе по ровной местности, так и при подъеме/спуске по лестнице в обеих группах. Скорость наступления эффекта была различной, в среднем составляла 30 мин., длительность аналгезии сохранялась от 4 до 6 ч, что свидетельствует о необходимости трехразового нанесения геля на пораженный сустав в течение суток. Эффект локальной терапии оценили как хороший 37,9% больных, применявших гель нимесулид, и 33,3% лечившихся гелем диклофенак, как удовлетворительный – 48,3 и 50% соответственно. Не отметили эффекта трое больных, получавших нимесулид, и пятеро – диклофенак. Переносимость гелевых форм была хорошей, побочных реакций (местных и системных) авторами не отмечено.
Согласно результатам метаанализа 86 рандомизированных клинических испытаний, в которых НПВП для местного применения сравнивались с плацебо, другими НПВП для местного использования или НПВП для перорального приема, локальные НПВП значимо превосходят плацебо по эффективности [13]. В этот обзор были включены исследования, в которых боль являлась клиническим исходом при острых (травма мягких тканей, растяжения и вывихи) или хронических заболеваниях (остеоартрит и ревматизм). Было показано, что при острых болях местное лечение эффективнее плацебо уже на 1-й нед., при хронических – через 2 нед. терапии. Нежелательные явления – как местные (3,6%), так и системные (0,5%) – встречались редко и были сопоставимы с плацебо. Согласно полученным данным, местное применение НПВП достоверно эффективнее плацебо, а число локальных (6%) и системных (3%) нежелательных явлений и количество больных, прервавших лечение из-за побочных реакций, было сопоставимым с числом больных, получавших наружно НПВП, и на фоне лечения плацебо [17].
В результате проведения оценки качества лечения больных остеоартрозом методом анкетирования исследователи выявили, что больные выполняют рекомендации врача главным образом в части проведения симптоматической терапии и широко используют местное лечение НПВП [18].
В некоторых ситуациях использование местных топических средств либо невозможно, либо не дает достаточного анальгезирующего эффекта, например при травме позвоночника и значительно выраженном болевом синдроме. В таких случаях необходимо и вполне оправданно использование пероральных анальгетиков, содержащих нимесулид. Так, исследование итальянских авторов показало высокую эффективность нимесулида у больных с переломом позвоночника на фоне остеопороза [19].
Применение пероральных форм нимесулида показало высокую клиническую эффективность и при острой патологии плечевого сустава [20]. Так, авторами в ходе двойного слепого плацебо-контролируемого исследования при сравнительной оценке эффективности обезболивания во время острого воспаления плечевого сустава установлено, что анальгезирующая способность нимесулида в дозе 100 мг значительно превосходит таковую диклофенака в дозе 75 мг при сравнимой безопасности применения. Аналогичные результаты были получены и в другом исследовании [21], в ходе которого проведена сравнительная оценка эффективности диклофенака и нимесулида при острой патологии плечевого пояса.
Хорошую эффективность и переносимость нимесулида у больных травматологического профиля зафиксировало исследование, проведенное группой итальянских исследователей среди детей с острой травмой в возрасте от 7 до 14 лет. В результате исследования обезболивающего потенциала нимесулида у этой категории больных установлено, что данный препарат обладает высокой анальгезирующей активностью, сравнимой с эффективностью наркотических анальгетиков, но при этом его использование не приводит к росту числа побочных эффектов от проводимой терапии [22].
Одной из самых частых причин обращения за медицинской помощью является спортивная травма, которая не сопровождается нарушением целостности костных структур, не требует оперативного лечения и длительной иммобилизации, но при этом ее наличие ухудшает качество жизни человека и требует обезболивания и эффективного купирования симптомов, таких как боль, отек и ограничение движений в конечности. При проведении мультицентрового исследования эффективности и безопасности лечения так называемых малых спортивных повреждений установлены эффективность и преимущества применения нимесулида у данных больных. Так, применение пероральной формы нимесулида в дозе 300 мг/сут. позволило полностью купировать симптомы повреждения и вернуться к привычной спортивной активности всем больным, получавшим лечение, при этом не зафиксировано побочных эффектов исследуемого препарата [23].
Заключение
Обзор современной литературы показал, что проведение лечебных мероприятий с включением в состав комплексной терапии НПВП, содержащих нимесулид, оказывается эффективным для различной патологии, в т.ч. и при травме мягких тканей и опорно-двигательного аппарата. В совокупности представленные данные свидетельствуют о хорошей переносимости и отсутствии системных нежелательных реакций, свойственных НПВП, при сравнительно высокой эффективности лечения.
Литература
1. Клиническая фармакология нестероидных противовоспалительных средств / под ред. Ю.Д. Игнатова, В.Г. Кукеса, В.И. Мазурова. М.: ГЭОТАР-Медиа, 2010. 576 с.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты (Перспективы применения в медицине). М.: Анко, 2000.
3. Steinmeyer J. Pharmacological basis for the therapy of pain and inflammation with nonsteroidal anti-inflammatory drugs // Arthritis Res. 2000. Vol. 2 (5). Р. 379–385.
4. Moore R., Barden A., Barden J. Systematic review of dexketoprofen in acute and chronic pain BMC // Clin Pharmacol. 2008.
5. Боль (практическое руководство для врачей) / под ред. Н.Н. Яхно, М.Л. Кукушкина. М., 2012. 512 с.
6. Насонов Е.Л. Эффективность и переносимость нестероидного противовоспалительного препарата. Нимесулид: новые данные // РМЖ. 2001. № 15. С. 6–8.
7. Rainsford K. Current status of the therapeutic uses and actions of the preferential cyclo-oxygenase-2 NSAID, nimesulide // Inflammopharmacology. 2006. Vol. 14 (3–4). Р. 120–137.
8. Bennett A. Nimesulide a well established cyclooxygenase-2 inhibitor with many other pharmacological properties relevant to inflammatory diseases. In: Therapeutic Roles of Selective COX-2 Inhibitors. Editors Vein J.R., Botting R.M. William Harvey Press, 2001. Р. 524–540.
9. Bernareggi A. Clinical pharmacokinetics of nimesulide // Clin Pharamacokinetic. 1998. Vol. 35. Р. 247–274.
10. Ruoff G.E. Challenges of managing chronic pain in the elderly // Semin Arthritis Rheum. 2001. Vol. 32 (Suppl 1). Р. 43–50.
11. Erdogan F., Ergun H., Gokay N.S. et al. The diffusion of nimesulide gel into synovial fluid: a comparison between administration routes // International Journal of Clinical Pharmacology and Therapeutics. 2006. Vol. 44. № 6. Р. 270–275.
12. Хитров Н.А., Цурко В.В., Семочкина Е.Н. Локальная терапия остеоартроза // Лечащий врач. 2002. Vol. 3. Р. 48–55.
13. Moore R.A., Tramer M.R., Carall D. et al. Quantative systemic review of topically applied NSAID–s // Brit. Med. J. 1998. Vol. 316. Р. 333–338.
14. Gupta S.K., Prakash J., Awor L. et al. Anti-inflammatory activity of topical nimesulide gel in various experimental models // Inflamm Res. 1996. Vol. 45 (12). Р. 590–592.
15. Sengupta S., Velpandian T., Kabir S.R. et al. Analgesic efficacy and pharmacokinetics of topical nimesulide gel in healthy human volunteers: double-blind comparison with piroxicam, diclofenac and placebo // Eur J Clin Pharmacol. 1998. Vol. 54 (7). Р. 541–547.
16. Балабанова Р.М., Федина Т.П., Запрягаева М.Е. и соавт. Эффективность геля Найз (нимесулид) в качестве аддитивной терапии у больных ревматоидным артритом // РМЖ. 2008. № 16 (10). С. 684–687.
17. Mason L., Moore R.A., Derry S., Edwards J.E., McQuay H.J. Systematic review of topical for the treatment of chronic pain // BMJ. 2004. Vol. 328. Р. 991–994.
18. Замятина Е.А., Багирова Г.Г. Как лечатся больные остеоартрозом? Тезисы II Всероссийского конгресса ревматологов России. 2011. 27. № 98.
19. Rossini M., Bertoldo F., Lovato R., Bortolotti R., Gatti D., Adami S. Use of nonsteroidal anti-inflammatory drugs in patients with vertebral osteoporotic fractures // Reumatismo. 2002 Oct-Dec. Vol. 54 (4). Р. 340–343.
20. Wober W. Comparative efficacy and safety of nimesulide and diclofenac in patients with acute shoulder, and a meta-analysis of controlled studies with nimesulide // Rheumatology (Oxford). 1999 May. Vol. 38 (Suppl 1). Р. 33–38.
21. Wober W., Rahlfs V.W., Buchl N., Grassle A., Macciocchi A. Comparative efficacy and safety of the non-steroidal anti-inflammatory drugs nimesulide and diclofenac in patients with acute subdeltoid bursitis and bicipital tendinitis // Int J Clin Pract. 1998 Apr-May. Vol. 52 (3). Р. 169–175.
22. Facchini R., Selva G., Peretti G. Tolerability of nimesulide and ketoprofen in paediatric patients with traumatic or surgical fractures // Drugs. 1993. Vol. 46 (Suppl 1). Р. 238–241.
23. Calligaris A., Scaricabarozzi I., Vecchiet L. A multicentre double-blind investigation comparing nimesulide and naproxen in the treatment of minor sport injuries // Drugs. 1993. Vol. 46 (Suppl 1). Р. 187–190.
Читайте также:

