Цитомегаловирусная инфекция что это у ребенка мононуклеоз
Обновлено: 25.04.2024
Инфекционный мононуклеоз. Болезнь Филатова у детей
Инфекционный мононуклеоз — острое инфекционное заболевание, вызываемое вирусом, обладающим тропизмом к лимфоретикулярным тканям.
В качестве возбудителя инфекционного мононуклеоза описывались дифтерийная палочка, кокки, спирохеты, листереллы, риккетсии. Гипотеза о вирусной природе возбудителя впервые была высказана в 1939 г. P. Wising. Наиболее убедительной является работа G. Schneider и соавт. (1964), которые выделили цитопатогснный агент от больных инфекционным мононуклеозом в культуре тканей. В последние годы высказано предположение, что этиологическим агентом инфекционного мононуклеоза является герпесоподобный вирус Эпштейна — Барра, так как у больных вырабатываются антитела против этого вируса. Хотя этот вопрос до конца не ясен, вирусная природа заболевания не вызывает сомнений.
Заболевают инфекционным мононуклеозом преимущественно дети и люди молодого возраста. Максимальное число заболеваний приходится на возраст от 2 до 10 лет.
Источником инфекции может быть больной инфекционным мононуклеозом и здоровый человек — вирусоноситель. Высказывается предположение о возможности заражения от больных латентной формой. Передача инфекции в основном воздушно-капельным путем, но может происходить также контактным и алиментарным путем. Заболевания возникают преимущественно в виде спорадических случаев, но описаны и эпидемические вспышки, главным образом среди детей.
В литературе имеются указания на возможность трансплацентарной передачи инфекционного мононуклеоза, обусловливающего желтуху новорожденного. Описан случай тяжелого врожденного порока сердца у ребенка, мать которого болела инфекционным мононуклеозом в ранний период беременности.
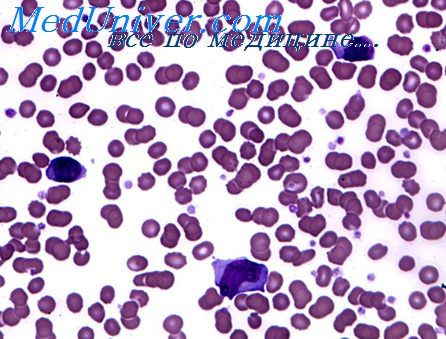
Летальные исходы при инфекционном мононуклеозе довольно редки, и поэтому патологоанатомичсские изменения изучены главным образом на данных гистологического исследования биоптатов лимфатических узлов, печени, селезенки, костного мозга, а также оперативно удаленных миндалин. Наиболее полные сведения о морфологии этого заболевания приводят Е. Н. Тер-Григорова (1960), Г. Маринеску (1964), R. Custer и Е. Smith (1948).
По данным Е. Н. Тер-Григоровой, макроскопическая картина на секции характеризуется генерализованным увеличением лимфатических узлов (особенно шейных), селезенки, печени, наличием ангины, набуханием и отеком глоточного кольца, иногда явлениями геморрагического диатеза. Консистенция лимфатических узлов мягкая, эластичная, поверхность разреза сочная, ткань желтоватого, серовато-красного цвета с белесовато-желтоватыми участками некроза. Селезенка увеличена, капсула напряжена, ткань на разрезе темно-красного цвета, со значительным соскобом пульпы и крови. Печень увеличена, полнокровна, иногда желтушна, строение долек нередко подчеркнуто. Миндалины увеличены, отечны, полнокровны, иногда покрыты фибринозным налетом или некротизированы и изъязвлены. Отмечается полнокровие мягких мозговых оболочек и ткани мозга.
На ранних стадиях заболевания в фолликулах и мозговых тяжах лимфатических узлов отмечается пролиферация ретикулярных и лимфоидных клеток с образованием крупных мо-нонуклеарных форм, часть из которых с базофильной цитоплазмой. В период разгара заболевания структура лимфатического узла полностью стерта. Обнаруживаются многочисленные фигуры митоза. Иногда встречаются многоядерные гигантские клетки с пиронинофильной цитоплазмой. В. Tindll и соавт. (1972) считают их результатом пролиферации иммунобластов. Капсула лимфатического узла и окружающая клетчатка также инфильтрированы мононуклеарами. В ряде случаев наблюдались очаговые и распространенные некрозы. G. Marinescu и соавт. (1964) обнаружили в лимфатических узлах месячного ребенка гиперплазию центров размножения фолликулов.
При повторной биопсии лимфатических узлов в период реконвалесценции выявляется полное восстановление структуры органа.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
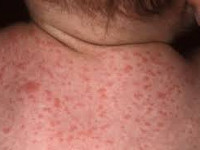
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Инфекционный мононуклеоз (иначе называемый доброкачественным лимфобластозом, болезнью Филатова) представляет собой острую вирусную инфекцию, характеризующуюся преимущественным поражением ротоглотки и лимфоузлов, селезенки и печени. Специфическим признаком заболевания является появление в крови характерных клеток – атипичных мононуклеаров. Возбудителем инфекционного мононуклеоза является вирус Эпштейна-Барр, относящийся к семейству герпесвирусов. Его передача от больного осуществляется аэрозольным путем. Типичными симптомами инфекционного мононуклеоза выступают общеинфекционные явления, ангина, полиаденопатия, гепатоспленомегалия; возможны пятнисто-папулезные высыпания на различных участках кожи.
МКБ-10
Общие сведения
Инфекционный мононуклеоз (иначе называемый доброкачественным лимфобластозом, болезнью Филатова) представляет собой острую вирусную инфекцию, характеризующуюся преимущественным поражением ротоглотки и лимфоузлов, селезенки и печени. Специфическим признаком заболевания является появление в крови характерных клеток – атипичных мононуклеаров. Распространение инфекции – повсеместное, сезонность не выявлена, отмечается повышенная заболеваемость в пубертатный период (девушки 14-16 лет и юноши 16-18 лет). Заболеваемость после 40 лет крайне редка, исключение составляют ВИЧ-инфицированные лица, у которых может развиться манифестация латентно существующей инфекции в любом возрасте. В случае заражения вирусом в раннем детском возрасте заболевание протекает по типу острой респираторной инфекции, в более старшем возрасте – без выраженной симптоматики. У взрослых клиническое течение заболевания практически не отмечается, поскольку у большинства к 30-35 годам сформирован специфический иммунитет.
Причины
Инфекционный мононуклеоз вызывается вирусом Эпштейна-Барр (ДНК-содержащий вирус рода Lymphocryptovirus). Вирус относится к семейству герпесвирусов, но в отличие от них не вызывает гибели клетки-хозяина (вирус преимущественно размножается в В-лимфоцитах), а стимулирует ее рост. Помимо инфекционного мононуклеоза вирус Эпштейна-Барр вызывает лимфому Беркитта и карциному носоглотки.
Резервуаром и источником инфекции является больной человек или носитель инфекции. Выделение вируса больными людьми происходит, начиная с последних дней инкубационного периода, и продолжается 6-18 месяцев. Вирус выделяется со слюной. У 15-25 % здоровых людей с положительным тестом на специфические антитела возбудитель обнаруживается в смывах из ротоглотки.
Механизм передачи вируса Эпштейна-Барр – аэрозольный, преимущественный путь передачи – воздушно-капельный, возможна реализация контактным путем (поцелуи, половые контакты, грязные руки, посуда, предметы быта). Кроме того, вирус может быть передан при переливании крови и интранатально от матери к ребенку. Люди обладают высокой естественной восприимчивостью к инфекции, но при заражении преимущественно развиваются легкие и стертые клинические формы. Незначительная заболеваемость среди детей до года говорит об имеющем место врожденном пассивном иммунитете. Тяжелому течению и генерализации инфекции способствует иммунодефицит.
Патогенез
Вирус Эпштейна-Барр вдыхается человеком и поражает клетки эпителия верхних дыхательных путей, ротоглотки (способствуя развитию умеренного воспаления в слизистой оболочке), оттуда возбудитель с током лимфы попадает в регионарные лимфоузлы, вызывая лимфаденит. При попадании в кровь вирус внедряется в В-лимфоциты, где начинает активную репликацию. Поражение В-лимфоцитов приводит к формированию специфических иммунных реакций, патологической деформации клеток. С током крови возбудитель распространяется по организму. В связи с тем, что внедрение вируса происходит в иммунные клетки и значимую роль в патогенезе играют иммунные процессы, заболевание относят в СПИД-ассоциированным. Вирус Эпштейна-Барр сохраняется в организме человека на всю жизнь, периодически активируясь на фоне общего снижения иммунитета.
Симптомы инфекционного мононуклеоза
Инкубационный период колеблется в широких пределах: от 5 дней до полутора месяцев. Иногда могут отмечаться неспецифические продромальные явления (слабость, недомогание, катаральные симптомы). В таких случаях идет постепенное нарастание симптоматики, недомогание усиливается, температура поднимается до субфебрильных значений, отмечается заложенность носа, першение в горле. При осмотре выявляется гиперемия слизистой ротоглотки, миндалины могут быть увеличены.
В случае острого начала заболевания развивается лихорадка, озноб, повышение потоотделения, отмечается симптоматика интоксикации (ломота в мышцах, головная боль), больные жалуются на боль в горле при глотании. Лихорадка может сохраняться от нескольких дней до месяца, течение (тип лихорадки) может приобретать различное.
Спустя неделю заболевание обычно переходит в фазу разгара: проявляется вся основная клиническая симптоматика (общая интоксикация, ангина, лимфоаденопатия, гепатоспленомегалия). Состояние больного обычно ухудшается (усугубляются симптомы общей интоксикации), в горле характерная картина катаральной, язвенно-некротической, пленчатой или фолликулярной ангины: интенсивная гиперемия слизистой оболочки миндалин, желтоватые, рыхлые налеты (иногда по типу дифтерийных). Гиперемия и зернистость задней стенки глотки, фолликулярная гиперплазия, возможны кровоизлияния слизистой.
В первые же дни заболевания возникает полиаденопатия. Увеличение лимфоузлов возможно обнаружить практически в любой доступной для пальпаторного исследования группе, чаще всего поражаются затылочные, заднешейные и подчелюстные узлы. На ощупь лимфоузлы плотные, подвижные, безболезненные (либо болезненность выражена слабо). Иногда может отмечаться умеренный отек окружающей клетчатки.
В разгар заболевания у большинства больных развивается гепатолиенальный синдром – печень и селезенка увеличены, может проявляться желтушность склер, кожных покровов, диспепсия, потемнение мочи. В некоторых случаях отмечаются пятнисто-папулезные высыпания разнообразной локализации. Сыпь кратковременная, не сопровождается субъективными ощущениями (зуд, жжение) и не оставляет после себя каких-либо остаточных явлений.
Разгар заболевания занимает обычно около 2-3 недель, после чего происходит постепенное стихание клинической симптоматики и наступает период реконвалесценции. Температура тела нормализуется, признаки ангины исчезают, печень и селезенка возвращаются к своему нормальному размеру. В некоторых случаях в течение нескольких недель могут сохраняться признаки аденопатии и субфебрилитет.
Инфекционный мононуклеоз может приобретать хроническое рецидивирующее течение, в результате чего продолжительность заболевания увеличивается до полутора и более лет. Течение мононуклеоза у взрослых обычно постепенное, с продромальным периодом и меньшей выраженностью клинической симптоматики. Лихорадка редко продолжается более 2 недель, лимфоаденопатия и гиперплазия миндалин выражена слабо, однако чаще отмечаются симптомы, связанные с функциональным расстройством работы печени (желтуха, диспепсия).
Осложнения
Осложнения инфекционного мононуклеоза преимущественно связаны с развитием присоединившейся вторичной инфекции (стафилококковые и стрептококковые поражения). Может возникнуть менингоэнцефалит, обструкция верхних дыхательных путей гипертрофированными миндалинами. У детей может отмечаться тяжелый гепатит, иногда (редко) формируется интерстициальная двусторонняя инфильтрация легких. Также к редким осложнениям относят тромбоцитопению, перерастяжка лиенальной капсулы может спровоцировать разрыв селезенки.
Диагностика
Неспецифическая лабораторная диагностика включает тщательное исследование клеточного состава крови. Общий анализ крови показывает умеренный лейкоцитоз с преобладанием лимфоцитов и моноцитов и относительной нейтропенией, сдвиг лейкоцитарной формулы влево. В крови появляются крупные клетки разнообразной формы с широкой базофильной цитоплазмой – атипичные мононуклеары. Для диагностики мононуклеоза значимо увеличение содержания этих клеток в крови до 10-12%, нередко их количество превышает 80% всех элементов белой крови. При исследовании крови в первые дни мононуклеары могут отсутствовать, что, однако, не исключает диагноз. Иногда формирование этих клеток может занимать 2-3 недели. Картина крови обычно постепенно приходит в норму в периоде реконвалесценции, при этом атипичные мононуклеары нередко сохраняются.
Специфическая вирусологическая диагностика не применяется в силу трудоемкости и нерациональности, хотя возможно выделить вирус в смыве из ротоглотки и идентифицировать его ДНК с помощью ПЦР. Существуют серологические методы диагностики: выявляются антитела к VCA- антигенам вируса Эпштейна-Барр. Сывороточные иммуноглобулины типа М нередко определяются еще в период инкубации, а в разгар заболевания отмечаются у всех больных и исчезают не ранее 2-3 дней после выздоровления. Выявление этих антител служит достаточным диагностическим критерием инфекционного мононуклеоза. После перенесения инфекции в крови присутствуют специфические иммуноглобулины G, сохраняющиеся пожизненно.
Больные инфекционным мононуклеозом (или лица с подозрением на эту инфекцию) подвергаются трехкратному (в первый раз - в период острой инфекции, и с интервалом в три месяца – еще дважды) серологическому исследованию на предмет выявления ВИЧ-инфекции, поскольку при ней также может отмечаться наличие мононуклеаров в крови. Для дифференциальной диагностики ангины при инфекционном мононуклеозе от ангин другой этиологии необходима консультация отоларинголога и проведение фарингоскопии.
Лечение инфекционного мононуклеоза
Инфекционный мононуклеоз легкого и среднетяжелого течения лечится амбулаторно, постельный режим рекомендован в случае выраженной интоксикации, тяжелой лихорадки. При имеющих место признаках нарушения функции печени, назначается диета №5 по Певзнеру.
Этиотропное лечение в настоящее время отсутствует, комплекс показанных мероприятий включает дезинтоксикационную, десенсибилизационную, общеукрепляющую терапию и симптоматические средства в зависимости от имеющейся клиники. Тяжелое гипертоксическое течение, угроза асфиксии при пережатии гортани гиперплазированными миндалинами являются показанием к кратковременному назначению преднизолона.
Антибиотикотерапия назначается при некротизирующих процессах в зеве с целью подавления местной бактериальной флоры и профилактики вторичных бактериальных инфекций, а также в случае имеющихся осложнений (вторичные пневмонии и др.). В качестве препаратов выбора назначают пенициллины, ампициллин и оксациллин, антибиотики тетрациклинового ряда. Сульфаниламидные препараты и хлорамфеникол противопоказаны ввиду побочного угнетающего действия на кроветворную систему. Разрыв селезенки является показанием к экстренной спленэктомии.
Прогноз и профилактика
Неосложненный инфекционный мононуклеоз имеет благоприятный прогноз, опасные осложнения, способные его значительно усугубить, при этом заболевании возникают достаточно редко. Имеющие место остаточные явления в крови являются поводом к диспансерному наблюдению в течение 6-12 месяцев.
Профилактические мероприятия, направленные на снижение заболеваемости инфекционным мононуклеозом, сходны с таковыми при острых респираторных инфекционных заболеваниях, индивидуальные меры неспецифической профилактики заключаются в повышении иммунитета, как с помощью общих оздоровительных мероприятий, так и с применением мягких иммунорегуляторов и адаптогенов при отсутствии противопоказаний. Специфическая профилактика (вакцинация) для мононуклеоза не разработана. Меры экстренной профилактики применяются по отношению к детям, общавшимся с больным, заключаются в назначении специфического иммуноглобулина. В очаге заболевания производится тщательная влажная уборка, личные вещи подвергаются дезинфекции.
ЦМВИ у детей. Что делать если у ребенка обнаружили цитомегаловирусную инфекцию?
Цитомегаловирусная инфекция (ЦМВИ) во многом остается "темной лошадкой" для современных инфекционистов. Обладателям вируса-возбудителя в теории может быть кто угодно, но далеко не каждый об этом догадывается. Дело обстоит таким образом, во-первых, потому что довольно часто носительство бывает бессимптомным, во-вторых, в связи с тем что возможности передачи вируса весьма широкие. Возбудитель ЦМВИ попадает в организм через плаценту, вертикально (когда плод проходит через родовые пути), при грудном вскармливании с молоком, при переливании крови и в процессе полового контакта. В отношении детей большую роль играют первые три способа передачи вируса.
Цитомегаловирус в организме может вести себя по-разному, собственно, именно это во многом затрудняет его диагностику. Как уже говорилось выше, он может вообще никак себя не проявлять, но лишь при одном условии - прочной и хорошо функционирующей иммунной системе, которая активное размножение вируса в клетках организма может подавить. Однако в условиях иммунодефицита этот вирус становится по-настоящему опасен. Поэтому от него страдают помимо больных СПИДом и людей пожилого возраста еще и дети.
ЦМВИ выявляется особенно часто у детей до двух лет - это период становления иммунитета ребенка. Его иммунная система не в столько в дефиците, сколько супрессирована, то есть в некоторой степени подавлена, особенно на первых месяцах жизни. Таким образом природа защищает новорожденного от чрезмерно сильных реакций иммунитета на огромное множество чужеродных агентов. После года та защита, которую малыш получал с молоком матери, начинает исчезать, а свои противовирусные частицы вырабатываться в должной мере пока не могут. В связи с этим дети нередко страдают от ЦМВИ.

Проявления ЦМВИ достаточно широко варьируют, так как вирус способен проникать практически во все клетки организма и вызывать цитопатический эффект. Проще говоря, клетки меняются и утрачивают способность нормально функционировать. Что говорит о врожденной ЦМВИ, которую ребенок получил либо через плаценту еще в утробе, либо в процессе родов?
1. У таких детей имеется желтушность кожных покров и склер глаз. Печень значительно увеличена, так как цитомегаловирус имеет склонность поселяться сразу в клетки этого органа.
2. Из-за нарушения работы печени страдает и свертываемость крови, на основании этого дети с ЦМВИ страдают от повышенной кровоточивости (на коже появляются синячки, сыпь, плохо заживает пупочная ранка, кровь может появиться в стуле).
3. Также значительно увеличивается селезенка.
4. Помимо этого есть ряд других признаков: страдают легкие (вплоть до развития пневмонии), нарушена центральная нервная система (менингит, энцефалит, гидроцефалия характеризуются судорогами, повышенной возбудимостью). Изменено состояние органов ЖКТ, что характеризуется колитами, энтеритами, недостаточностью поджелудочной железы. Вирус не обходит стороной и почки, приводя к развитию нефрита.
К сожалению, выхаживать таких новорожденных чрезвычайно трудно, ведь на фоне такого "букета" к ослабленному организму присоединяются другие инфекционные заболевания. Поэтому тяжело текущие ЦМВИ часто заканчиваются гибелью новорожденного еще в первые недели его жизни, либо вовсе приводят к выкидышу, если женщина заразилась на ранних сроках беременности.
К счастью, такое тяжелое течение заболевания бывает далеко не у всех новорожденных (всего у 10 %), так что причина тяжести ЦМВИ в этом случае во многом остается загадкой. Те же дети, которые относительно легко переживают инфекцию, нередко впервые сталкиваются с ней через месяц-два после рождения. И в этом случае симптомы могут быть самыми разными. Обычно снижается слух или зрение, нарушается работа нервной системы, страдает физическое развитие. Вот с такими проблемами родители приходят к педиатру, и установить истинную причину - ЦМВИ удается не всегда.
Стоит помнить о и передаче вируса ребенку с материнским молоком. Когда инфицирование происходит таким путем, у ребенка часто возникает пневмония, которая лечению антибактериальными препаратами не поддается.

Дети старшего возраста и подростки с ЦМВИ сталкиваются еще реже в силу прочности их иммунной системы. Но если вирус все же активизировался, то проявляет он себя обычно снижением работоспособности, болью в суставах, лихорадкой и головными болями. Вывод таков, что по одним признакам установить наличие ЦМВ невозможно, всегда требуется лабораторное подтверждение. Оно заключается в поиске специфических антител, которые наш организм вырабатывает в ответ на наличие конкретных вирусных частиц. Есть специфические антитела - есть и вирус. Что же делать, если у ребенка обнаружили ЦМВИ?
1. Обнаружение ЦМВИ возможно еще в процессе беременности, посредством УЗИ, ведь вирус может приводить к формированию множественных видимых пороков у плода. Поскольку такие дети в будущем практически не жизнеспособны, беременность предлагается прервать.
2. В том случае, когда ЦМВИ выявляется у ребенка через некоторое время после рождения (не в первые дни), тактика врача будет зависеть от течения инфекционного процесса. Есть конкретные лекарственные средства, которые назначают для подавления ЦМВ - Ганцикловир, Фоскарнет. Однако принимать решение об их применении самостоятельно нельзя, так как эти лекарственные средства обладают рядом очень серьезных побочных эффектов. Они негативно сказываются на состоянии крови и токсичны для почек. В связи с этим их применяют только при острой необходимости, когда цитомегаловирус выходит из-под контроля. Новый препарат Цитотект, тоже подходит для лечения ЦМВИ, но вводится он также исключительно по назначению специалиста.
3. Нужно добиваться, чтобы признаки ЦМВИ не появлялись у ребенка. А для этого очень важно укреплять его иммунитет, который самостоятельно способен подавлять вирус и не давать ему негативно влиять на здоровье малыша. Есть множество природных иммуностимуляторов, которые разрешено давать детям (настойка эхинацеи, элеутерококка), Иммунал, Иммудон и другие средства, которые можно использовать курсами после консультации у педиатра с целью улучшения работы иммунной системы. Не последнюю роль играет питание. Не забывайте, что оно должно привносить в организм нужное количество белков, углеводов и жиров, микроэлементов, витаминов. Следите за тем, чтобы ребенок соблюдал режим, не переутомлялся, регулярно бывал на свежем воздухе и физически был активен.
- Вернуться в оглавление раздела "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

