Цитопатическое действие вич это
Обновлено: 25.04.2024
ВИЧ-инфекция вызывает в организме человека возникновение хронически, реже остро протекающего заболевания с преимущественным поражением клеток крови и органов иммуногенеза, заключительным этапом которого является тотальное угнетение иммунной системы и развитие синдрома приобретенного иммунодефицита (СПИДа).
Этиология, эпидемиология, патогенез
Этиология. Возбудителем является Т-лимфоцитарный (лимфотропный) вирус иммунодефицита человека - ВИЧ (НТLV-III или НIV). Несмотря на то, что у некоторых животных, в частности у отдельных видов обезьян, выявлено аналогичное заболевание, считается, что эти вирусы не вызывают заболевание у людей.
ВИЧ впервые выделили в 1983 г. независимо друг от друга Л.Монтанье (Франция) и Р.Галло (США). Вирус принадлежит к семейству Т-лимфотропных ретровирусов и назван в 1986 г. вирусом иммунодефицита человека или ВИЧ. В последнее время этот вирус стали обозначать ВИЧ-1, так как был выявлен другой вирус - ВИЧ-2 (вирус "африканского СПИДа"), который чаще обнаруживается у аборигенов Западной Африки. Кроме того, имеется ВИЧ -3, выявляемый в Японии. Обнаружено много различных штаммов вируса, благодаря его феноменальной склонности к мутациям. Диаметр вирусных частиц 100-150 мкм. Нуклеоид содержит две молекулы РНК (геном вируса) и обратную транскриптазу. Капсид содержит два гликопротеида - 41 и 120, причем последний обеспечивает специфическое связывание вируса с клетками, несущими на своей поверхности антиген СD4. Такими клетками являются:
- Т-CD4+-лимфоциты (хелперы) циркулирующие в крови и входящие в состав лимфоидных фолликулов;
- В-лимфоциты (те, которые имеют рецептор СD4+);
- моноциты и макрофаги;
- дендритические клетки;
- микроглия;
- эндотелиоциты.
ВИЧ нестоек во внешней среде и гибнет при температуре 56њС в течение 30 мин, при 70-80њ - в течение 10 мин, быстро инактивируется этиловым спиртом, ацетоном, эфиром, 1% раствором глютаральдегида и др., но относительно устойчив к действию ионизирующей радиации и ультрафиолетовому облучению.
Источником заражения является больной человек и вирусоноситель. Наибольшая концентрация вируса обнаруживается в крови, сперме, спинномозговой жидкости, в меньших количествах вирус выявляется в слезах, в слюне, цервикальном и вагинальном секретах больных. В настоящее время доказаны 3 пути инфицирования:
- половой (при гомо- и гетеросексуальных контактах);
- посредством парентерального введения вируса с препаратами крови или при использовании инфицированных инструментов;
- от матери ребенку - транспланцентарный или с молоком.
Риск заражения при гомосексуальных связях составляет 1:10, при гетеросексуальных - 1:100, 1:1000. Высокая вероятность инфицирования при гомосексуальных контактах объясняется большой травматизацией слизистой при анальном и орогенитальном сексе, а также доказанным фактом проникновения ВИЧ через неповрежденную слизистую прямой кишки, эпителиальные клетки которой имеют на своей поверхности немногочисленные CD4-рецепторы. Вероятность передачи при однократном половом контакте невелика от 1:100 (1%) до 1:1000 (0,01%). Вместе с тем, известны случаи, когда единственного полового акта было достаточно для заражения. Однако, описано много случаев, когда постоянный партнер (муж или жена) больного оставались без признаков инфекции, несмотря на длительные половые контакты с вирусоносителем.
Передача ВИЧ от матери ребенку (плоду) может происходить трансплацентарно, в родах и в постнатальном периоде. Вероятность заражения плода (новорожденного) от инфицированной матери составляет от 10 до 70% (в среднем 20-40%).
Искусственный механизм заражения осуществляется через зараженную кровь и ее компоненты, донорские органы, ткани, сперму. Инфицирование при этом может произойти:
- при переливании крови и ее компонентов, препаратов, изготовленных из крови инфицированного или больного,
- при использовании недостаточно обеззараженных игл или шприцев при парентеральном, чаще внутривенном, введении медикаментов (особенно при введении наркотиков),
- при случайном уколе иглой во время или после медицинских манипуляций или попадания крови инфицированного на микротравмы у медицинских работников,
- при использовании нестерильного медицинского инструментария. Вероятность заражения реципиента после однократного переливания инфицированной крови составляет более 90%. При однократном контакте через общие инструменты для инъекции, содержащих кровь инфицированного (шприцы, иглы) вероятность передачи ВИЧ выше, чем при однократном половом акте и составляет 1:100 (1%) до 1:200 (0,5%). Наиболее низкая вероятность инфицирования при случайных уколах иглой - около 0,3%, т.е. менее чем 1:300.
Патогенез. У взрослых индивидуумов ВИЧ попадает в кровь либо парентерально при инъекциях, либо при половом контакте через поврежденные слизистые оболочки половых путей. Обладая тропизмом к СD4+ рецепторам, вирус прикрепляется к эпитопам клеточной мембраны, чаще всего Т-лимфоцитов - хелперов. Затем он проникает внутрь, где встраивается в генетический аппарат клетки. С помощью обратной транскриптазы, используя хромосомную ДНК клетки-мишени, вирус кодирует продукцию себе подобных частиц до тех пор, пока клетка не погибнет. После гибели клетки, вирус заселяет новые клетки, имеющие СD4+ рецепторы. В СD4+ лимфоцитах-хелперах ВИЧ может находится в латентном состоянии неопределенно долго. Поведение ВИЧ в организме хозяина зависит от типа инфицированной клетки, уровня ее метаболизма, состояния иммунной системы.
Заболевание при ВИЧ инфицировании развивается длительное время. Среди периодов ВИЧ-инфекции различают:
- инкубационный (асимптомное носительство);
- лимфаденопатического синдрома (ЛАС) или персистирующей генерализованной лимфоаденопатии;
- синдрома, ассоциированного со СПИДом (пре-СПИД), или СПИД-ассоциированного комплекса (САС);
- синдрома приобретенного иммунодефицита (СПИД).
- лихорадка - 92%;
- миалгия - 83%;
- полиаденопатия - 75%;
- спленомегалия - 75%;
- уртикарии - 50%;
- пальмо-плантарное шелушение - 15%;
- синдром мононуклеоза и плазмоцитоза в формуле крови - 70%;
- печеночный цитолиз - 20%.
Период персистирующей генерализованной лимфоаденопатии характеризуется стойким, в течение нескольких месяцев, увеличением различных групп лимфатических узлов. В основе лимфоаденопатии лежит неспецифическая гиперреактивность В-клеток, проявляющаяся фолликулярной гиперплазией лимфатических узлов (увеличение лимфоидных фолликулов и их светлых центров). Длительность стадии - 3-5 лет.
СПИД-ассоциированный комплекс, или преСПИД развивается на фоне умеренного иммунодефицита и характеризуется снижением массы тела до 20%, развитием лихорадки, диарреи, прогрессирующей полилимфоаденопатии, повторных острых вирусных респираторных инфекций, например, опоясывающего лишая. Этот период длится несколько лет.
Период синдрома приобретенного иммунодефицита (СПИД) сопровождается резкой потерей массы тела, вплоть до кахексии, развитием деменции. В финале развивается резкое угнетение клеточного и гуморального звеньев иммунитета, что проявляется в клинике развитием оппортунистических инфекций (вирусных, бактериальных, грибковых) и злокачественных опухолей (злокачественных В-клеточных лимфом и саркомы Капоши).
Повреждения, наблюдаемые при инфицировании вирусом иммунодефицита человека (ВИЧ), очень полиморфны, имеют разнообразную локализацию и природу. Тем не менее, они могут быть классифицированы следующим образом:
- поражения лимфоузлов;
- повреждения, обусловленные оппортунистическими инфекциями;
- развитие злокачественных опухолей.
Изменения в лимфоузлах выражаются множественными, часто симметричными аденопатиями, наиболее часто локализующимися в шейной, подмышечной и подчелюстной областях. Особенно типичной является персистирующая генерализованная лимфаденопатия, причем существующая более трех месяцев. Среди структурных проявлений самого заболевания (ВИЧ-инфекции) наиболее характерны изменения, сходные с выявляемыми при других генерализованных РНК-вирусных инфекциях, однако с преимущественным поражением лимфоидной системы.
Гистологические изменения лимфоузлов схематично развиваются в три стадии:
- вначале возникает преимущественно фолликулярная гиперплазия в кортикальных и медуллярных зонах лимфатических узлов с многочисленными крупными фолликулами, которые содержат объемные светлые центры, состоящие, в основном, из крупных клеток с высокой пролиферативной активностью, с фигурами митоза, и макрофагов. Периферический лимфоцитарный венчик очень узкий или вообще отсутствует в большей части фолликулов, либо сохранен лишь в части ободка. Это сопровождается инфильтрацией герминативных центров малыми лимфоцитами и внутрифолликулярными геморрагиями. Характерно усиление фагоцитоза эритроцитов. Паракортикальные зоны у взрослых людей могут быть гиперплазированы, у детей чаще содержат обычное число клеток с преобладанием среди них малых лимфоцитов. Среди клеток выявляются диффузно расположенные иммунобласты со значительной митотической активностью. Медуллярные тяжи определяются с трудом. Краевые и промежуточные синусы увеличиваются в размерах, в них выявляются отдельные нейтрофильные полиморфноядерные лейкоциты и закономерно появляются крупные одноядерные клетки - макрофаги и слущенные клетки эндотелия. Эти клетки имеют округлое или изредка дольчатое ядро и широкую светлую цитоплазму. Появляются также многоядерные клетки, напоминающие аналогичные клетки при кори. Паракортикальные зоны представлены Т-лимфоцитами. В этих областях также часто обнаруживаются Т-иммунобласты и происходит гиперплазия ретикулярных клеток. При иммуноцитохимическом исследовании выявляется выраженная гиперплазия и гипертрофия ретикулярных клеток фолликулов и выраженная активация В-клеток. В периферической зоне, кроме них, присутствуют Т-лимфоциты. В дальнейшем наблюдается фрагментация фолликулов. Периферические зоны неровны и местами отсутствуют, из-за чего часть герминативных центров имеет зубчатые границы. Они содержат значительное число малых лимфоцитов, а также иммунобластов и макрофагов. Чаще всего фолликулярная гиперплазия сочетается с более или менее значительной гиперплазией межфолликулярных зон, с наличием в них многочисленных посткапиллярных венул. Типична пролиферация клеток эндотелия, особенно венул, в которых выявляются фигуры митоза. Кроме того, имеются расширенные синусы и многочисленные плазмоциты на границе медуллярной и периферической зон.
- диффузная гиперплазия типа ангиоиммунобластной лимфаденопатии является вторым этапом эволюции предыдущей формы. Для этой стадии типично стирание обычной структуры лимфоузла. Лимфоузел, который содержит либо очень мало фолликулов, либо лишен их вовсе, и представлен множеством сосудов, а его клеточный состав полиморфен за счет наличия малых круглых или неправильной формы лимфоцитов, плазмоцитов, иммунобластов, интердигитирующих клеток, эозинофилов и тканевых базофилов. Фолликулы мелкие, атрофичные. Нередко отмечается гиалиноз центров фолликулов. Пролиферативная активность клеток в сохранившихся герминативных центрах низкая, периферические зоны утрачены, типична деструкция дендритных клеток.
- стадия лимфоидного истощения развивается на поздних этапах развития. На последней стадии лимфоузел состоит из одной стромы; отмечается резкое расширение синусов, переполненных крупными одноядерными клетками, нередко с фагоцитированными эритроцитами. Лимфоузлы становятся маленькими, склерозированы, со значительным уменьшением числа лимфоидных элементов и сохранением лишь некоторых плазмоцитов и иммунобластов. Подобные лимфоузлы содержат большое количество макрофагов с явлениями фагоцитоза. По мере развития заболевания сходные изменения выявляются в селезенке и тимусе, а также в лимфоидном аппарате кишки, в том числе червеобразного отростка. Происходит постепенная атрофия лимфоидной ткани этих органов, отчетливо определяемая уже макроскопически.
Помимо описанных повреждений, в лимфоузлах могут выявляться изменения, соответствующие оппортунистическим инфекционным заболеваниям или опухолям, особенно типа саркомы Капоши или лимфомы.
Повреждения, связанные с оппортунистическими инфекциями, имеют самую различную локализацию и природу: бактериальную, грибковую, паразитарную или вирусную. Оппортунистическими называют инфекции, вызываемые условнопатогенными (маловирулентными) возбудителями, заражение которыми у здорового человека не сопровождается патологическими изменениями. Такими возбудителями инфекции являются:
- простейшие (пневмоцисты, токсоплазмы, криптоспоридии);
- грибы (рода Candida, криптококки);
- вирусы (цитомегаловирусы, герпетические вирусы, некоторые вирусы медленных инфекций);
- бактерии (Мусоbacterium avium intracellulare, легионелла, сальмонелла).
Для оппортунистических инфекций при СПИДе характерно тяжелое рецидивирующее течение, часто с генерализацией процесса и устойчивостью к проводимой терапии.
Легкие при ВИЧ ассоциированном СПИДе поражаются чаще всего (до 80% больных). В легких может быть обнаружена гиперплазия альвеолоцитов с последующим их слущиванием, что напоминает умеренно выраженную десквамативную пневмонию при других РНК-вирусных инфекциях. Легочные поражения, часто встречающиеся при СПИДе, могут быть его начальными клиническими проявлениями. При этом речь может идти о диффузных поражениях по типу интерстициальной пневмопатии, множественных или единичных легочных очагах. Наиболее часто пневмонии, вызванные Pneumocystis carinii, сопровождаются поражением обоих легких по типу интерстициальной пневмонии с наличием внутриальвеолярных паразитов, хорошо выявляемых импрегнацией серебром по Гроккоту. Диагноз in vivo основан на выявлении паразитов в содержимом альвеолярного лаважа. Легочная патология, обусловленная инфицировании цитомегаловирусом, часто сочетающаяся с инфицированием пневмоцистами, также проявляется в виде интерстициальной пневмопатии. Диагноз подтверждает выявление внутриклеточных цитомегаловирусных включений в содержимом альвеолярного лаважа. Другие легочные поражения наблюдаются реже, к ним относятся гистоплазмоз, криптококкоз, кандидоз, паразитарные поражения (токсоплазмоз), банальные бактериальные или микобактериальные инфекции.
Центральная нервная система при ВИЧ-инфекции стоит на втором месте по частоте поражения, которое выражается в виде самых разнообразных неврологических проявлений. Речь может идти об энцефалопатиях, причиной которых часто является цитомегаловирус, реже - вирус герпеса или микобактерии. Развивается ВИЧ-ассоциированный подострый энцефаломиелит. Изменения развиваются преимущественно в белом веществе и в подкорковых структурах, включая базальные ганглии и семиовальные центры. При микроскопическом исследовании находят микроглиальные узелки, многоядерные симпласты, в которых удается обнаружить частицы ВИЧ. Такие микроглиальные узелки могут быть найдены также в мозговом стволе, мозжечке, спинном мозге и реже в коре головного мозга. Считается патогномоничным образование многоядерных клеток типа симпластов, которые могут располагаться изолированно или в комбинации с микроглиальными узелками. Кроме того, может иметь место прогрессирующий мультифокальный лейкоэнцефалит, фокальные мозговые поражения, в особенности связанные с токсоплазмозом и проявляющиеся в виде множественных или единичных абсцессов. Часто также наблюдается повреждение мозговых оболочек в виде вялотекущего негнойного лептоменингита, возбудителем которого чаще всего является Cryptococcus neoformans. Диагноз подтверждается выявлением паразитов в спинномозговой жидкости. Характерна вакуолизация белого вещества (спонгиоз). Особенно часта, но неспецифична, вакуолярная миелопатия с поражением боковых и задних столбов спинного мозга. Белое вещество выглядит в этом случае дырчатым. Изменения ЦНС могут быть первым симптомом быстро прогрессирующей и закончившейся летально ВИЧ-инфекции.
Повреждения пищеварительного тракта представляют третью локализацию оппортунистических инфекций. Чаще всего встречается кандидозный эзофагит. На уровне тонкой и толстой кишок могут наблюдаться другие оппортунистические инфекции, проявляющиеся обычно диарреей. Здесь речь может идти о криптоспоридиозе или о вирусных поражениях типа герпеса и ЦМВ или сальмонеллезах. Диагноз криптоспоридиоза и вирусных поражений обычно основан на. выявлении паразитов при биопсиях. Значительно реже оппортунистические инфекции наблюдаются в печени и желчных путях.
Наконец, можно наблюдать поражения кожи и слизистых, обусловленные оппортунистическими инфекциями. Некоторые из них, особенно кожные, связаны с генерализованной септицемией, например, гистоплазмозом и криптококкозом. Другие встречаются реже, например, кандидоз, банальный гингивостоматит, или неизвестное раньше повреждение, именуемое языка, локализующееся по его краям и имеющее вид беловатых линейных образований. Гистологически значительный поверхностный паракератоз со светлыми клетками, содержащими многочисленные вирусные частицы типа Эпштейна-Барра, хорошо выявляемые при электронной микроскопии.
Возможно поражение яичек с частичным или полным прекращением дифференцировки сперматозоидов, тяжелой атрофией семенных канальцев, лимфоидной инфильтрацией и фиброзом, выраженными в различной степени.
В почках выявляется отложение иммунных комплексов в клубочках, дистрофические изменения нефротелия и гиперплазия отдельных его клеток, микрокистозная тубулоэктазия и расширение капсул почечных телец. Наряду с этим отмечается очаговый гломерулосклероз.
В надпочечниках возможны очаговые некрозы и обширные кровоизлияния.
Опухоли при СПИДе в основном двух типов:
- ангиосаркома Капоши, которая раньше наблюдалась редко и в основном у людей пожилого возраста. При СПИДе она является начальным проявлением, особенно у гомосексуалистов. Речь идет о ярко-красных кожных узелках различной локализации. Саркома Капоши сочетается с повреждением слизистой неба, лимфоузлов, в некоторых случаях - множественными висцеральными поражениями, развивается медленно. Микроскопически опухоль состоит из множества новообразованных, хаотично расположенных тонкостенных сосудов с хорошо определяемым эндотелием и пучков веретенообразных клеток. В рыхлой строме часто видны кровоизлияния и скопления гемосидерина. У больных СПИДом саркома Капоши имеет злокачественный характер и отличается от классического варианта генерализацией процесса с поражением лимфатических узлов, желудочно-кишечного тракта, легких и других внутренних органов.
- злокачественные неходжкинские лимфомы, наблюдаемые при СПИДе, - лимфомы типа В, часто располагающиеся вне лимфоузлов, поражающие центральную нервную систему, пищеварительный тракт, верхние дыхательные пути, костный мозг. Речь идет о высокозлокачественных лимфомах иммунобластического типа или типа Беркитта.
СПИД всегда заканчивается летально.
Автор: Шлопов В. Г.
опубликовано 11/12/2009 15:51
обновлено 13/05/2011
— Инфекционные болезни
6.3. ПАТОГЕНЕЗ ВИЧ-ИНФЕКЦИИ
В связи с тем что вирусы являются патогенами внутриклеточными, ка-ждый представитель мира вирусов имеет тропность к определенному типу клеток. Тропизм вируса определяется наличием на клетке-мишени рецептора для данного вируса, а также возможностью генома вируса встроиться в геном клетки. Рецепторы для определенного вируса могут быть на клетках различ-ных типов. Рецепторную функцию выполняют различные структуры (лиган-ды): белки, липиды, углеводные компоненты белков и липидов. Эти лиганды локализованы на плазматической мембране и выполняют важнейшие функ-ции жизнеобеспечения клетки – проникновение в нее гормонов, питательных веществ, факторов роста и регуляции и т.п.
Рецепторы, независимо от их биохимического строения, имеют общую структурную характеристику, а именно, состоят из участка, расположенного вне клетки, участка, локализованного внутримембранно, и участка, погру-женного в цитоплазму.
Рецепторами для ВИЧ являются дифференцировочный антиген CD4, а также неспецифические, не зависящие от наличия CD4 компоненты. CD4 -гликопротеид с молекулярной массой 55 000, по своему строению имеющий гомологии с определенными участками иммуноглобулинов. Аналогичные гомологии имеет и белок вируса gp120, что и определяет тропность ВИЧ. Фиксация вируса через gp120 ВИЧ-1 (или gp105 в случае инфицирования ВИЧ-2) с мембранным рецептором CD4 клетки хозяина блокирует основную функцию этих иммунокомпетентных клеток - восприятие сигналов от анти-генпрезентирующих клеток. Последующая за рецепцией репликация вируса ведет к гибели клеток, выпадению функции, ими выполняемой, развитию иммунодефицита.
В организме человека имеется целый ряд иммунокомпетентных, сома-тических и ряд других клеток, имеющих рецепторы для ВИЧ (CD4+ лимфо-циты, CD8+ лимфоциты, дендритные клетки, моноциты, эозинофилы, мега-кариоциты, нейроны, микроглия, сперматозоиды), и наблюдается цитопати-ческий эффект во многих из них в случае проникновения вируса.
В 1996 году Бергер открыл корецептор для ВИЧ. Этот рецептор вместе с CD4 опосредует инфицирование СО-вариантами ВИЧ-1, адаптированных к росту в Т-хелперах, но не в макрофагах. На сегодня известно около 10 хемо-киновых рецепторов.
Таким образом, выделены белки - хемокины, блокирующие проникно-вение ВИЧ в макрофаги с антигеном CD4, и белки - корецепторы, способст-вующие инфицированию. При этом корецепторы – это рецепторы для хемо-кинов, но их использует ВИЧ в качестве рецептора, с помощью которого проникает внутрь клетки.
Проникнув в СD4+ клетки, ВИЧ сразу же начинает репликацию, при этом, чем активнее CD4+ клетки, тем выше процесс репродукции вируса. Все регуляторы, активирующие СD4+клетки, обеспечивают увеличение реплика-ции вируса. К подобным регуляторам относятся фактор некроза опухолей (ФНО), фактор, стимулирующий колонии гранулоцитов/макрофагов, интер-лейкин-6 (ИЛ-6). К негативным регуляторам, тормозящим репликацию виру-са, относятся интерферон (ИФ) и трансформирующий фактор роста.
Морфофункциональные изменения в моноцитах/макрофагах оказыва-ют разнонаправленное действие не только на Т-лимфоциты, но и естествен-ные киллеры - главные клетки противоопухолевой защиты. Активность по-следних по мере прогрессирования заболевания неуклонно снижается. Дефи-цит ИЛ-2 и γ-интерферона даже при нормальном количестве NK-клеток ве-дет к снижению функциональной активности их у больных ВИЧ-инфекцией (Ковальчук Л.В., Чередеев А.Н.,1991).
Выделено два типа CD4+клеток: Т-хелперы-1 (Th1) и Т-хелперы-2 (Th2). Тh1 продуцируют цитокины, стимулирующие клеточный иммунитет, а Тh2 – цитокины, усиливающие антителогенез. Соотношение Тh1 и Тh2 взве-шенно и конкурентно; суперэкспрессия цитокинов одного типа клеток ведет к супрессии другого. У больных ВИЧ-инфекцией идет угнетение Тh1, чем обеспечиваются и вирусная патология, и онкогенез.
Жизненный цикл ВИЧ после проникновения в организм имеет после-довательный характер: связывание вириона с поверхностью клетки, слияние мембран вириона и клетки, проникновение вируса внутрь клетки, высвобож-дение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая транскрипция белков вируса, наработка всех компонентов вируса с формированием новых вирионов и их высвобождени-ем из клетки, влекущим за собой гибель клетки-мишени (рис.6.4.).
Рис. 6.4. Стадии проникновения ВИЧ в клетку (Ледванов М.Ю., 1997).
Судьба ДНК-транскрипта генома ВИЧ, интегрированных в хромосому пораженной клетки, может быть различна. Она определяется активностью положительных и отрицательных регуляторных генов. Если активны все по-ложительные регуляторные гены, то происходит репродукция вируса со все-ми вытекающими отсюда последствиями – идет активация инфекции.
Если активны все отрицательные регуляторные гены, синтеза компо-нентов вириона не происходит, и инфекция не развивается.
Если активны положительные регуляторные гены белков суперкапсид-ной оболочки, происходит образование этих белков, и они экспрессируются на поверхности инфицированных клеток. Такие клетки способны взаимодей-ствовать с CD4 - рецепторами клеток организма и нарушать их функции. Та-ким образом, хотя репродукции вирусов не происходит, имеют место опре-деленные проявления инфекции.
Равным образом события развиваются при активности положительных регуляторных белков капсидной оболочки. Их повреждающее действие на клетки существенно ниже, но они индуцируют образование соответствую-щих антител.
Если же активны положительные регуляторные гены только геномных белков, то в пораженных клетках образуется обратная транскриптаза, которая довольно быстро разрушается.
Сродство вирусного мембранного гликопротеида gp120 (gp105 в случае ВИЧ-2) к клеточному рецептору CD4 определяет высокую степень избира-тельного поражения клеточных структур, поэтому в патологический процесс вовлекаются, в первую очередь, и в большей степени CD4+ лимфоциты, мо-ноциты крови, макрофаги тканей, дендритные клетки крови, лимфатических узлов, селезенки, кожи, альвеолярных и интерстициальных макрофагов лег-ких, микроглия и другие клетки нервной системы, имеющие CD4 - рецепто-ры. Так же поражаются В- и О-лимфоциты, ретикулярные клетки, эпители-альные клетки кишечника, клетки Лангерганса, причем последние инфици-руются даже легче, чем CD4+ лимфоциты. Именно клеткам Лангерганса придается большое значение в распространении ВИЧ по организму, ибо в них вирус сохраняется длительное время, иногда годы.
Наличие CD4 рецептора на многих и не только иммунокомпетентных клетках, возможность поражать и клетки, не имеющие этого рецептора, оп-ределяют политропность ВИЧ и полиморфизм клинической картины. Сте-пень поражения тех или иных, содержащих СD4 рецепторы, клеток зависит от плотности этих рецепторов на мембране клеток. Наиболее высока плот-ность на Т-хелперной субпопуляции лимфоцитов, что и определяет во мно-гом патогенез болезни. Но степень поражения клеток-мишеней вирусом за-висит также и от возможности репликации вируса в том или ином виде кле-ток. Очевидно, осуществляется репликация в основном в лимфоцитах с CD4+ фенотипом и моноцитах/макрофагах.
Если на CD4+ лимфоциты вирус оказывает цитопатическое действие с лизисом клетки или слиянием в синцитий, то в моноцитах/макрофагах ВИЧ реплицируется с умеренной интенсивностью; вирионы оформляются в ок-руглые частицы еще в цитоплазме клетки и по выходе из нее не оказывают цитонекротического действия. Изучение динамики сывороточных монокинов подтверждает активное участие в патогенезе ВИЧ-инфекции моноци-тов/макрофагов, основных продуцентов фактора некроза опухолей и интер-лейкина-1b (выполняющих роль передатчика Т-лимфоцитам антигенспеци-фических сигналов, необходимых для их активации в иммунном ответе). С гиперпродукцией ФНО-a , ИЛ-1b и ИЛ-6 связывают развитие при ВИЧ-инфекции лихорадки, анемии, диареи, кахексии, патологических изменений на коже и слизистых при саркоме Капоши, церебральных симптомов. ФНО-a при этом оказывает прямое цитопатическое действие на инфицированные ВИЧ Т-хелперы. В то же время было установлено, что ВИЧ ингибирует про-дукцию ИЛ-2 и γ-ИФ, синтезируемым Т-хелперами первого типа, и не инги-бирует функцию Т-хелперов второго типа. Следовательно, играя важную роль в регуляции синтеза цитокинов, ВИЧ за счет переключения иммунного ответа с Т-хелперов первого типа на Т-хелперы второго типа, стимулирует гуморальное звено иммунитета.
После инфицирования клетки вирусом происходит соединение вирус-ной оболочки с помощью белка gp41 с мембраной клетки. Помимо того, ви-русный белок gp41 обеспечивает слияние мембран соседних клеток между собой с образованием одной многоядерной клетки - синцития. При этом слияние может быть как зараженных клеток между собой, так и зараженных с незараженными. Но синцитий в основном индуцируют вирусы, выделенные от больных с клиническими проявлениям ВИЧ-инфек-ции, и не образуют выделенные от инфицированных людей, не имеющих клинических проявле-ний.
С момента интеграции генома вируса в геном клетки начинается стадия латентной инфекции. В этот период вирус находится в клетке в виде интег-рированного в геном ДНК – провируса. Раньше полагали, что в этот период отсутствуют процессы транскрипции и трансляции с вирусных генов, а по-этому и экспрессии вирусных белков, нет иммунного ответа на вирус как в виде специфических иммуноглобулинов, так и сенсибилизированных лим-фоцитов. Но последние исследования показали, что сразу после проникнове-ния вируса в клетку начинаются и трансляция, и транскрипция.
Состояние латентной инфекции без клинических признаков болезни может длиться от 2 до 11 лет. Активация длинных концевых повторов и экс-прессия генов ВИЧ, кодирующих белки вируса, знаменуют собой манифе-стацию болезни.
В расшифровке патогенеза ВИЧ-инфекции многие вопросы решены, установлены основные этапы развития процесса в клетке после инфицирова-ния ее вирусом. Выявлен ряд факторов, активирующих экспрессию генов ВИЧ. К ним относятся факторы, активирующие Т-лимфоциты: специфиче-ские антигены (например, вирусы группы Herpes), неспецифические антиге-ны (например, митогены типа фитогемаглютинина), цитокины (например, фактор некроза опухолей, некоторые интерлейкины, гамма-интерферон), бактериальные иммуномодуляторы (например, монофосфат липида из саль-монелл). К активаторам экспрессии ВИЧ относятся глюкокортикостероидные гормоны, в частности, дексаметазон и гидрокортизон, ультрафиолетовое об-лучение, перекись водорода, свободные кислородные радикалы. Активирует инфекционный процесс беременность; более прогрессирующее течение ВИЧ-инфекции имеют психически неуравновешенные лица, дезадаптированные, по сравнению с людьми, имеющими уравновешенную психику.
Довольно сложен и до конца не выяснен механизм репликации вируса в инфицированной клетке. Известно, что в цитоплазме информация с вирус-ной РНК посредством обратной транскриптазы (ревертазы) переписывается на ДНК, первоначально образуется однонитевая структура; затем та же об-ратная транскриптаза обеспечивает образование второй нити, и линейная промежуточная форма ДНК-транскриптаза вируса - транспортируется в ядро, где с помощью фермента интегразы интегрирует в хромосому клетки, пре-вращаясь в провирус.
Исключительно важный этап патогенеза болезни – сборка вирусных частиц и выход нового потомства вируса из инфицированной клетки. Сборка происходит на плазматической мембране лимфоцита, куда поступают все компоненты вирусной частицы, в том числе и белки-предшественники. За-вершается процесс почкованием вирусных частиц с клеточной поверхности. Отличительной чертой ВИЧ является взрывной характер процессов актива-ции транскрипции, синтеза белков-пред-шественников, сборки вирионов и их почкования: за 5 мин одна лимфоцитарная клетка может образовать до 5000 вирусных частиц.
Ключевой вопрос патогенеза ВИЧ-инфекции – механизм иммунного повреждения. Как установлено, в составе белков gp120, главного комплекса гистосовместимости (HLA) класса II и CD4-рецепторов имеются сходные участки, что определяет перекрестное реагирование образующихся к ВИЧ антител с этими структурами. Например, происходит блокада кооперации CD4+ лимфоцитов и HLA II. Антитела к gp120 ВИЧ реагируют с CD4, обу-словливая неадекватную стимуляцию CD4+ клеток. На всех ядросодержащих клетках имеются антигены HLA I; вирус же нарушает синтез этих антигенов, участвующих в распознавании CD8+ лимфоцитами зараженных вирусом клеток, что тормозит процесс лизиса инфицированных клеток.
Взаимосвязь жизненного цикла вируса и иммунных сдвигов в началь-ной фазе ВИЧ-инфекции изучена в эксперименте при заражении SIV обезьян; полученные данные экстраполированы на человека. Как показали исследова-ния, вирус первоначально локализуется в лимфоидной системе, вирусная экспрессия определяет клинику ранней фазы болезни. Пик экспрессии вируса в клетках лимфоидной ткани предшествует накоплению его в плазме. Появ-ление вирусспецифических цитотоксических Т-лимфоцитов (CTL) совпадает со временем окончания экспрессии вируса в лимфатических узлах. Продук-ция комплементсвязывающих антител облегчает переход вируса в сеть денд-ритных клеток герминальных центров лимфатических узлов. Повреждающее действие CTL и продукция комплементсвязывающих антител оказывают ос-новное патогенное действие в результате виремии. Образование нейтрали-зующих антител обеспечивает переход острой фазы болезни в хроническую.
Иммунопатогенетически ВИЧ-инфекция проявляется дефицитом Т- и В-звеньев иммунной системы, дефицитом комплемента, фагоцитов, сниже-нием функции неспецифических факторов защиты. В результате идет фор-мирование анергии с проявлениями аллергического, аутоаллергического и иммунокомплексного патологического процесса. Уже во II стадии ВИЧ-инфекция характеризуется снижением абсолютного числа лейкоцитов за счет CD3+, CD4+, p24+ и gp120+ лимфоцитов, повышением уровня естественных киллеров (NК-клетки), нарастанием реакции торможения миграции лимфо-цитов с конкавалином А и фитогемагглютинином. Изменения гуморального звена иммунитета проявляются нарастанием IgG+ В-лимфоцитов и 4-5-кратным ростом уровня сывороточных IgE.
Для изменений В-звена иммунитета характерна активация В-лимфоцитов. Изменение их метаболизма сопровождается уменьшением вре-мени полуобмена иммуноглобулиновых рецепторов с повышением в крови концентрации клеточных рецепторов (Р-белки). Суммарная концентрация сывороточных иммуноглобулинов растет, но выявляется диспропорция уровней подклассов иммуноглобулинов. Так, содержание IgG1 и IgG3 у больных увеличивается, а концентрация IgG2 и IgG4 существенно уменьша-ется. Очевидно, повышение уровня IgG2 связано с высокой восприимчиво-стью больных к стафилококкам, пневмококкам, палочке инфлюэнцы. Не-смотря на гипергаммаглобулинемию, увеличение количества циркулирую-щих в крови В-лимфоцитов, их функциональная активность на митогены ос-таются относительно сниженными, что позволяет В-систему иммунитета у ВИЧ-больных расценивать как супрессированную. К тому же, количество В-клеток в периферической крови больных в стадии СПИДа может быть сни-жено в три и более раз.
Многочисленными исследованиями показано, что взаимодействие gp120 ВИЧ-1 с мембраной CD4+ лимфоцитов определяет не только отрица-тельные реакции инфицированных клеток, но и приводит к программирован-ной клеточной гибели - апоптозу зрелых CD4+ лимфоцитов или CD34+ ге-мопоэтических клеток-предшественников даже при отсутствии их инфици-рования вирусом.
Специфический иммунный ответ при ВИЧ-инфекции имеет ряд осо-бенностей. Локализуясь в иммуноците, вирус проникает в органы и ткани, пребывая вне доступности для иммунной системы, чем определяется перси-стенция в клетках как вируса, так и его компонентов – белков, нуклеокапси-дов, нуклеиновой кислоты. Активация инфекционного процесса ведет к гу-моральному иммунному ответу с образованием антител. Но в связи с наличи-ем в составе вирусного белка gp120, HLA класса II и CD4-рецептора лимфо-цита сходных участков образующиеся антитела перекрестно реагируют с ни-ми, чем обусловливают нарушение кооперативных взаимодействий в функ-ционировании иммунной системы. Все это определяет формирование ауто-аллергических реакций. Именно поэтому в ходе развития инфекционного процесса формируется гиперчувствительность замедленного и немедленного типов, преимущественно к антигенам ВИЧ, в частности, gр41 и gp120. Так, Л.Монтанье (1996) считает, что в патогенезе СПИДа основное место принад-лежит аутоиммунному процессу. В пользу этого говорят исследования харак-тера иммунных реакций у больных: наличие аутоантител и аллоантител к лимфоцитам, формирование аллергических реакций цитотоксического типа, накопление циркулирующих иммунных комплексов, наличие комплементо-посредованной цитотоксичности, активация антителозависимой клеточной цитотоксичности. Кроме того, при сильном антительном ответе возможность развития аутоиммунных процессов обусловлена мимикрией структуры gp120 под структуру иммуноглобулинов (Atlan H. et al.,1993). В пользу наличия ау-тоиммунных процессов в патогенезе ВИЧ-инфекции говорят и клинические проявления болезни, в частности, часто сопутствующие болезни такие ти-пичные аутоаллергические варианты патологии, как спондилоартропатии, системные ревматоидные синдромы: волчаночноподобный синдром Шегре-на, полимиозит, некротизирующий васкулит.
У половины больных развиваются манифестные формы аллергии, пре-имущественно в виде ринита, лекарственной аллергии, крапивницы, атопиче-ского дерматита, ангионевротического отека с повышением у них уровня специфических IgE к бытовым, эпидермальным, пыльцевым и пищевым ал-лергенам с положительной коррелятивной связью между общим уровнем IgE и содержанием СD8+ лимфоцитов (Ю.А.Митин, 1997).
Наряду с поражением иммунной системы в патологический процесс вовлекается и кроветворная ткань. Для заболевания характерны лейкопения, анемия, тромбоцитопения. Угнетается функциональная активность грануло-цитов. У больных ВИЧ-инфекцией в костном мозге резко снижено содержа-ние колониеобразующих единиц гранулоцитов, макрофагов, мегакариоцитов. Однако дисфункция стволовых клеток не связана с их прямым инфицирова-нием, ибо не обнаружено присутствия ВИЧ в кроветворных клетках при изу-чении методом гибридизации in situ и иммуногистохимическим исследова-нием гемопоэтических колоний, а также с помощью полимеразной цепной реакции. Пока нет однозначного мнения о причинах ингибиции пролифера-тивной активности стволовых клеток, хотя и установлено, что различные изоляты ВИЧ, воздействуя на CD34+ клетки, угнетают их функциональную активность. Также установлено, что подавление кроветворения в результате действия ВИЧ связано с усилением продукции костномозговыми моноцита-ми/макрофагами фактора некроза опухолей.
Таким образом, поражение иммунной системы при ВИЧ-инфекции но-сит системный характер, проявляясь глубокой супрессией Т- и В-звеньев клеточного иммунитета. В ходе развития ВИЧ-инфекции происходят законо-мерные изменения гиперчувствительности немедленного и замедленного ти-па, гуморального иммунитета и факторов неспецифической защиты, функ-циональной активности лимфоцитов и моноцитов/макрофагов. Нарастает уровень сывороточных иммуноглобулинов, циркулирующих иммунных ком-плексов. Наряду с дефицитом CD4+ лимфоцитов в динамике болезни нарас-тает функциональная недостаточность СD8+ лимфоцитов, NK-клеток, ней-трофилов. Нарушение иммунного статуса клинически проявляется инфекци-онным, аллергическим, аутоиммунным и лимфопролиферативным синдро-мами иммунологической недостаточности, синдромом, свойственным болез-ни иммунных комплексов. Все это определяет в целом клинику ВИЧ-инфекции.
ВИЧ-инфекция - это заболевание, вызываемое вирусом иммунодефицита человека, длительное время персистирующим в лимфоцитах, макрофагах, клетках нервной ткани, в результате чего развивается медленно прогрессирующее поражение иммунной и нервной системы, проявляющееся вторичными инфекциями, опухолями, подострым энцефалитом и другими патологическими изменениями, приводящими к гибели больного.
ВИЧ-инфекция - это смена стадий, последнюю из них обозначают термином СПИД - синдром приобретенного иммунодефицита человека, являющуюся заключительной, терминальной стадией процесса.
Возбудитель и эпидемиология ВИЧ-инфекции
Возбудитель ВИЧ-инфекции - вирус иммунодефицита человека, принадлежит к подсемейству лентивирусов, семейства ретровирусов. Выделяют два типа вируса -ВИЧ-1 и ВИЧ-2. Вирусная частица представляет собой форму, близкую к сферической, со средним диаметром 100-120 нм, состоящую из ядра, окруженное оболочкой. Ядро содержит РНК и ферменты - обратную транскриптазу (ревертазу), интегразу, протеазу. Наличие обратной транскриптазы обеспечивает обратную направленность потока генетической информации: не от ДНК к РНК, а наоборот, от РНК к ДНК.
В составе вириона имеется оболочка и нуклеоид. Наружная оболочка пронизана вирусными белками: трансмембранным и внешним глико-протеидами. Белки выполняют функцию детерминанты и участвуют в прикреплении к мембране клетки-хозяина, С внутренней стороны оболочки расположен каркас, образованный белком р 17, окружающий внутреннюю структуру вириона - нуклеоид (сердцевина). Собственно оболочка сердцевины образована белком р 24. Внутри нуклеоида располагается геном вируса, состоящих из 2 цепочек РНК, окруженных белками р 7 и р 9 .
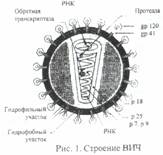
Жизненный цикл ВИЧ включает в себя процессы специфической сорбции вируса на CD 4(+) - лимфоцитах за счет процессов диффузии мембран, синтез ДНК копии генома и дальнейшей ее интеграции в хромосому клетки-хозяина.
При попадании ВИЧ в клетку под действием фермента обратной транскриптазы происходит образование ДНК ВИЧ, встраивающейся в ДНК клетки-хозяина, которая в дальнейшем продуцирует вирусные частицы.
ВИЧ не стоек в окружающей среде. Полностью инактивируется нагреванием при температуре 56°С в течение 30 мин, быстро погибает при кипячении (1-3 мин), а также под воздействием дезинфицирующих средств н концентрациях, обычно используемых в практике. ВИЧ в то же время устойчив к ультрафиолетовым лучам и ионизирующей радиации.
Источником заражения является человек, инфицированный ВИЧ как в стадии бессимптомного носителъства, так и развернутых клинических проявлений болезни. Вирус обнаруживается в крови, сперме, спинномозговой жидкости, грудном молоке, менструальной крови, влагалищном секрете, которые являются факторами передачи ВИЧ-инфекции. В слюне, слезной жидкости, моче ВИЧ находится в небольшом количестве, недостаточном для заражения.
Пути передачи ВИЧ-инфекции - половой (гетеро- и гомосексуальный), парентеральный и вертикальный.
Вертикальный путь передачи может быть от инфицированной матери ребенку во время беременности и родов, а также во время грудного вскармливания, возможно также заражение матери от ВИЧ-инфецированного ребенка при его вскармливании.
Патогенез ВИЧ-инфекции.
При попадании ВИЧ в клетку, РНК под воздействием ревертазы превращается в ДНК, которая встраивается в ДНК клетки-хозяина, продуцируя новые вирусные частицы - копии РНК вируса, оставаясь в клетке пожизненно. Ядро окружено оболочкой, в составе которой имеется белок g р 120, обуславливающий прикрепление вируса к клеткам организма человека, имеющим рецептор - белок CD 4 .
ВИЧ адсорбируется на клетках, в состав мембраны которых входит белок CD 4. Это Т-лимфоциты с фенотипом CD 4(+) , макрофаги, В-лимфоциты, клетки нейроглии (вследствие этого происходит поражение центральной нервной системы), клеток слизистой оболочки кишечника, дендритных клеток. Прежде всего поражаются С D 4(+)-лимфоциты, являющиеся центральной фигурой иммунного ответа. Причиной снижения Т-хелперов является не только прямое цитопатическое действие вируса, но и слияние неинфицированных клеток с инфицированными и образование синтиция.
Одновременно происходит нарушение функции В-лимфоцитов. повышается количество иммуноглобулинов, циркулирующих иммунных комплексов, что ведет к большему снижению С D 4(+) - лимфоцитов. Все перечисленные механизмы и формируют различные клинические проявления заболевания. В результате поражения центральных звеньев иммунной системы человек, инфицированный ВИЧ, становится беззащитным перед возбудителями различных инфекций, в первую очередь, условно-патогенными (оппортунистическими) микроорганизмами, которые не представляют угрозы для практически здорового человека.
В связи с прогрессированием вторичного иммунодефицитного состояния формируются опухолевые и аутоиммунные процессы, в патологический процесс всегда вовлекается ЦНС, куда проникает вирус вместе с инфицированными моноцитами. Поражение клеток нейроглии приводит к трофическим повреждениям нейронов, ткани мозга, нарушению мозговой деятельности, и в конечном итоге развитию СПИД-деменции (слабоумию).
Российская классификация ВИЧ-инфекции, 2006 год (В.В. Покровский)
Продолжительность клинических проявлений во второй стадии может варьировать от нескольких дней до нескольких месяцев, однако обычно они регистрируется в течение двух-трех недель.
В целом продолжительность стадии первичных проявлений ВИЧ-инфекции составляет один год с момента появления симптомов острой инфекции или сероконверсии.
Длительность субклинической стадии составляет от двух-трех до 20-ти и более лет, но в среднем она продолжается 6-7 лет. Скорость снижения уровня С04-лимфоцитов в этот период в среднем составляет 50-70x106/л в год.
В зависимости от тяжести вторичных заболеваний выделяют стадии 4А, 4Б, 4В.
4А обычно развивается через 6-10 лет от момента заражения. Для нее характерны бактериальные, грибковые и вирусные поражения слизистых и кожных покровов, воспалительные заболевания верхних дыхательных путей. Обычно стадия 4А развивается у пациентов с уровнем С04-лимфоцитов 500-350x106/л (у здоровых лиц число С04-лимфоцитов колеблется в пределах 600-1900x106/л).
4Б чаще возникает через 7-10 лет от момента заражения. Кожные поражения в этот период носят более глубокий характер и склонны к затяжному течению. Начинают развиваться поражения внутренних органов. Могут отмечаться потеря веса, лихорадка, локализованная саркома Капоши, поражение периферической нервной системы. Обычно стадия 4Б развивается у пациентов с уровнем С04-лимфоцитов 350-200x106/л.
4В преимущественно выявляется через 10-12 лет от момента заражения. Она характеризуется развитием тяжелых, угрожающих жизни вторичных заболеваний, их генерализованным характером, поражением ЦНС. Обычно стадия 4В имеет место при уровне С04- лимфоцитов менее 200x106/л.
Несмотря на то, что переход ВИЧ-инфекции в стадию вторичных заболеваний является проявлением истощения защитных резервов организма зараженного человека, этот процесс имеет обратимый характер (по крайней мере, на какое-то время). Спонтанно или вследствие проводимой терапии клинические проявления вторичных заболеваний могут исчезать. Поэтому в стадии вторичных заболеваний выделяют фазы прогрессирования (при отсутствии противоретровирусной терапии или на фоне противоретровирусной терапии) и ремиссии (спонтанной, после ранее проводимой противоретровирусной терапии или на фоне противоретровирусной терапии).
ВИЧ – заболевание, вызываемое вирусом иммунодефицита человека. Сегодня в мире отмечается пандемия ВИЧ-инфекции, заболеваемость населения планеты неуклонно растёт.
ВИЧ-инфекция
ВИЧ-инфекция представляет собой заболевание, вызываемое вирусом иммунодефицита человека, характеризующееся синдромом приобретённого иммунодефицита, способствующего возникновению вторичных инфекций и злокачественных образований в связи с глубоким угнетением защитных свойств организма. Сегодня в мире отмечается пандемия ВИЧ-инфекции, заболеваемость населения планеты, в особенности стран Восточной Европы неуклонно растёт.
Характеристика возбудителя
Вирус иммунодефицита человека ДНК-содержащий, относится к роду Lentivirus семейства Retroviridae. Различают два типа: ВИЧ-1 является основным возбудителем ВИЧ-инфекции, причиной пандемии, развития СПИД. ВИЧ-2 – малораспространённый тип, встречается в основном в Западной Африке. ВИЧ – нестойкий вирус, быстро погибает вне организма носителя, чувствителен к воздействию температуры (снижает инфекционные свойства при температуре 56°С, погибает через 10 минут при нагревании до 70-80°С). Хорошо сохраняется в крови и её препаратах, подготовленных для переливания. Антигенная структура вируса весьма изменчива.
Резервуаром и источником ВИЧ-инфекции является человек: страдающий СПИД и носитель. Природных резервуаров ВИЧ-1 не выявлено, есть мнение, что естественным хозяином в природе являются дикие шимпанзе. ВИЧ-2 переносится африканскими обезьянами. Восприимчивость к ВИЧ у других видов животных не отмечена. Вирус содержится в высоких концентрациях в крови, сперме, секрете вагинальных желез и менструальных выделениях. Может выделяться из женского молока, слюны, слёзного секрета и ликвора, но эти биологические жидкости представляют меньшую эпидемиологическую опасность.
Вероятность передачи ВИЧ-инфекции повышается при наличии повреждений кожных покровов и слизистых оболочек (травмы, ссадины, эрозия шейки матки, стоматит, пародонтоз и др.). ВИЧ передаётся с помощью гемоконтактного и биоконтактного механизма естественным путём (при половых контактах и вертикально: от матери к ребёнку) и искусственным (преимущественно реализуется при гемоперкутанном механизме передачи: при трансфузиях, парентеральных введениях веществ, травматических медицинских процедурах).
Риск поражения ВИЧ при единичном контакте с носителем невысок, регулярные половые контакты с инфицированным его значительно повышают. Вертикальная передача инфекции от больной матери ребенку возможна как во внутриутробном периоде (через дефекты плацентарного барьера), так и при родах, при контакте ребенка с кровью матери. В редких случаях фиксируется постнатальная передача с грудным молоком. Заболеваемость среди детей у заражённых матерей достигает 25-30%.
Парентеральное заражение происходит при инъекциях с помощью игл, загрязнённых кровью ВИЧ-инфицированных лиц, при гемотрансфузиях заражённой крови, нестерильных медицинских манипуляциях (пирсинг, татуировки, медицинские и стоматологические процедуры, производящиеся инструментарием без должной обработки). Контактно-бытовым путем ВИЧ не передаётся. Восприимчивость человека к ВИЧ-инфекции – высокая. Развитие СПИД у лиц старше 35-ти лет, как правило, происходит в более короткие сроки с момента заражения. В некоторых случаях отмечается невосприимчивость к ВИЧ, что связывают со специфическими иммуноглобулинами А, присутствующими на слизистых половых органов.
Патогенез ВИЧ-инфекции
Вирус иммунодефицита человека при попадании в кровь внедряется в макрофаги, микроглию и лимфоциты, имеющие важное значение в формировании иммунных реакций организма. Вирус уничтожает способность иммунных телец к распознаванию своих антигенов как чужеродных, заселяет клетку и приступает к репродукции. После выхода размножившегося вируса в кровь, клетка-хозяин погибает, а вирусы внедряются в здоровые макрофаги. Синдром развивается медленно (годами) и волнообразно.
Первое время организм компенсирует массовую гибель иммунных клеток, вырабатывая новые, со временем компенсация становится недостаточной, количество лимфоцитов и макрофагов в крови значительно снижается, иммунная система разрушается, организм становится беззащитен как по отношению к экзогенной инфекции, так и к бактериям, населяющим органы и ткани в норме (что ведёт к развитию оппортунистических инфекций). Кроме того, нарушается механизм защиты от размножения дефектных бластоцитов – злокачественных клеток.
Заселение вирусом иммунных клеток часто провоцирует различные аутоиммунные состояния, в частности характерны неврологические расстройства в результате аутоиммунного поражения нейроцитов, которые могут развиться даже раньше, чем проявится клиника иммунодефицита.
Классификация ВИЧ
В клиническом течении ВИЧ-инфекции различают 5 стадий:
- инкубации;
- первичных проявлений;
- латентная;
- стадия вторичных заболеваний;
- терминальная.
Стадия первичных проявлений может протекать бессимптомно, в виде первичной ВИЧ-инфекции, а также сочетаться с вторичными заболеваниями. Четвертая стадия в зависимости от тяжести подразделяется на периоды: 4А, 4Б, 4В. Периоды проходят фазы прогрессирования и ремиссии, различающиеся в зависимости от имеющей место противоретровирусной терапии или её отсутствия.
Симптомы ВИЧ-инфекции
1. Стадия инкубации – может составлять от 3-х недель до 3-х месяцев, в редких случаях удлиняется до года. В это время идёт активное размножение вируса, но иммунный ответ на него пока отсутствует. Инкубационный период ВИЧ заканчивается либо клиникой острой ВИЧ-инфекции, либо появлением в крови ВИЧ-антител. На этой стадии основанием для диагностики ВИЧ-инфекции является обнаружение вируса (антигенов или частиц ДНК) в сыворотке крови.
2. Стадия первичных проявлений характеризуется проявлением реакции организма на активную репликацию вируса в виде клиники острой инфекции и иммунной реакции (выработка специфических антител). Вторая стадия может протекать бессимптомно, единственным признаком развивающейся ВИЧ-инфекции будет положительная серологическая диагностика на антитела к вирусу. Клинические проявления второй стадии протекают по типу острой ВИЧ-инфекции. Начало острое, отмечается у 50-90% пациентов спустя три месяца после момента заражения, зачастую предшествуя формированию ВИЧ-антител. Острая инфекция без вторичных патологий имеет довольно разнообразное течение: могут отмечаться лихорадка, разнообразные полиморфные высыпания на кожных покровах и видимых слизистых оболочках, полилимфаденит, фарингит, лиенальный синдром, диарея. У 10-15% больных острая ВИЧ-инфекция протекает с присоединением вторичных заболеваний, что связано со снижением иммунитета. Это могут быть ангины, пневмонии различного генеза, грибковые инфекции, герпес и др. Острая ВИЧ-инфекция обычно длится от нескольких дней до нескольких месяцев, в среднем 2-3 недели, после чего в подавляющем большинстве случаев переходит в латентную стадию.
3. Латентная стадия характеризуется постепенным нарастанием иммунодефицита. Гибель иммунных клеток на этой стадии компенсируется их повышенным производством. В это время диагностировать ВИЧ можно с помощью серологических реакций (в крови присутствуют антитела к ВИЧ). Клиническим признаком может быть увеличение нескольких лимфатических узлов из разных, не связанных между собой групп, исключая паховые лимфоузлы. При этом других патологических изменений со стороны увеличенных лимфоузлов (болезненность, изменения окружающих тканей) не отмечается. Латентная стадия может продолжаться от 2-3-х лет, до 20-ти и более. В среднем она длится 6-7 лет.
4. Стадия вторичных заболеваний характеризуется возникновением сопутствующих (оппортунистических) инфекций вирусного, бактериального, грибкового, протозойного генеза, злокачественных образований на фоне выраженного иммунодефицита. В зависимости от выраженности вторичных заболеваний различают 3 периода течения:
4А. Потеря массы тела не превышает 10%, отмечаются инфекционные (бактериальные, вирусные и грибковые) поражения покровных тканей (кожи и слизистых оболочек). Работоспособность снижена.
4Б. Потеря в весе более 10% общей массы тела, продолжительная температурная реакция, возможна длительная диарея, не имеющая органической причины, может присоединяться туберкулёз легких, инфекционные заболевания рецидивируют и прогрессируют, выявляется локализованная саркома Капоши, волосистая лейкоплакия.
4В. Отмечается общая кахексия, вторичные инфекции приобретают генерализованные формы, отмечается кандидоз пищевода, дыхательных путей, пневмоцистная пневмония, туберкулёз внелегочных форм, диссеминированная саркома Капоши, неврологические расстройства.
Подстадии вторичных заболеваний проходят фазы прогрессирования и ремиссии, различающиеся в зависимости от имеющей место противоретровирусной терапии или её отсутствия. В терминальной стадии ВИЧ-инфекции вторичные заболевания, развившиеся у больного, приобретают необратимый характер, меры лечения теряют свою эффективность, летальный исход наступает спустя несколько месяцев.
Течение ВИЧ-инфекции довольно многообразно, не всегда имеют место все стадии, те или иные клинические признаки могут отсутствовать. В зависимости от индивидуального клинического течения продолжительность заболевания может составить как несколько месяцев, так и 15-20 лет.
Особенности клиники ВИЧ-инфекции у детей
ВИЧ в раннем детском возрасте способствует задержке физического и психомоторного развития. Рецидивирование бактериальных инфекций у детей отмечают чаще, чем у взрослых, нередки лимфоидные пневмониты, увеличение лёгочных лимфоузлов, различные энцефалопатии, анемия. Частой причиной детской смертности при ВИЧ-инфекциях является геморрагический синдром, являющийся следствием выраженной тромбоцитопении. Наиболее частым клиническим проявлением ВИЧ-инфекции у детей является задержка темпов психомоторного и физического развития. ВИЧ-инфекция, полученная детьми от матерей анте- и перинатально протекает заметно тяжелее и быстрее прогрессирует, в отличие от таковой у детей, заражённых после года.
Диагностика ВИЧ-инфекции
В настоящее время основным диагностическим методом при ВИЧ-инфекции является выявление антител к вирусу, производящееся преимущественно с применением методики ИФА. В случае положительного результата исследуют сыворотку крови с помощью методики иммунного блоттинга. Это позволяет идентифицировать антитела к специфическим антигенам ВИЧ, что является достаточным критерием для окончательного диагностирования. Невыявление с помощью блоттинга антител характерной молекулярной массы, однако, не исключает ВИЧ. В инкубационный период иммунный ответ на внедрение вируса ещё не сформирован, а в терминальной стадии в результате выраженного иммунодефицита антитела перестают вырабатываться.
При подозрении на ВИЧ и отсутствии положительных результатов иммунного блоттинга эффективным методом выявления частиц РНК вируса является ПЦР. Диагностированная серологическими и вирусологическими методами ВИЧ-инфекция является показанием к динамическому наблюдению состояния иммунного статуса.
Лечение ВИЧ-инфекции
Терапия ВИЧ-инфицированных лиц подразумевает постоянный контроль иммунного статуса организма, профилактику и лечение возникающих вторичных инфекций, контроль над развитием новообразований. Зачастую ВИЧ-инфицируемым лицам требуется психологическая помощь и социальная адаптация. В настоящее время в связи со значительным распространением и высокой социальной значимостью заболевания в государственных и мировых масштабах осуществляется поддержка и реабилитация больных, расширяется доступ к социальным программам, предоставляющим больным медицинскую помощь, облегчающую течение и улучшающую качество жизни пациентов.
На сегодняшний день преимущественным этиотропным лечением является назначение препаратов, снижающих репродуктивные способности вируса. К антиретровирусным препаратам относятся:
- нуклеозидные ингибиторы транскриптазы (НИОТ) различных групп: зидовудин, ставудин, залцитабин, диданозин, абакавир, комбинированные препараты;
- нуклеотидные ингибиторы обратной транскриптазы (НтИОТ): невирапин, эфавиренз;
- ингибиторы протеазы: ритонавир, саквинавир, дарунавир, нелфинавир и другие;
- ингибиторы слияния.
При принятии решения о начале противовирусной терапии пациентам следует помнить, что применение препаратов осуществляется многие годы, практически пожизненно. Успех терапии напрямую зависит от строгого соблюдения рекомендаций: своевременного регулярного приёма лекарственных средств в необходимых дозировках, соблюдение предписанной диеты и строгое следование режиму.
Возникающие оппортунистические инфекции лечат в соответствии с правилами эффективной против вызвавшего их возбудителя терапии (антибактериальные, противогрибковые, противовирусные средства). Иммуностимулирующая терапия при ВИЧ-инфекции не применяется, поскольку способствует её прогрессированию, цитостатики, назначаемые при злокачественных образованиях, угнетают иммунитет.
Лечение ВИЧ-инфицированных включает общеукрепляющие и поддерживающие организм средства (витамины и биологически активные вещества) и методики физиотерапевтической профилактики вторичных заболеваний. Больным, страдающим наркоманией, рекомендуется лечение в соответствующих диспансерах. В связи со значительным психологическим дискомфортом, многие пациенты проходят длительную психологическую адаптацию.
Прогноз при ВИЧ-инфекции
ВИЧ-инфекция полностью неизлечима, во многих случаях противовирусная терапия даёт незначительный результат. На сегодняшний день в среднем ВИЧ-инфицированные живут 11-12 лет, однако тщательная терапия и современные лечебные препараты позволяют заметно удлинить срок жизни пациентов. Основную роль в сдерживании развивающегося СПИД играет психологическое состояние больного и его усилия, направленные на соблюдение прописанного режима.
Профилактика ВИЧ-инфекции
В настоящее время Всемирная организация здравоохранения проводит общие профилактические мероприятия по снижению заболеваемости ВИЧ-инфекцией по четырем основным направлениям:
- просвещение в вопросах безопасности половых отношений, распространение презервативов, лечение заболеваний, передающихся половым путём, пропаганда культуры половых взаимоотношений;
- контроль над изготовлением препаратов из донорской крови;
- ведение беременности ВИЧ-инфицированных женщин, обеспечение их медицинской помощью и предоставление им средств химиопрофилактики (в последнем триместре беременности и в родах женщины получают антиретровирусные препараты, которые также на первые три месяца жизни назначаются новорождённым детям);
- организация психологической и социальной помощи и поддержки ВИЧ-инфицированных граждан, консультирование.
В настоящее время в мировой практике особое внимание уделяют таким эпидемиологически важным в отношении заболеваемости ВИЧ-инфекцией факторам, как наркомания, беспорядочная половая жизнь. В качестве профилактической меры во многих странах производится бесплатная раздача одноразовых шприцев, метадоновая заместительная терапия. В качестве меры, способствующей снижению половой неграмотности, в учебные программы вводятся обучающие половой гигиене курсы

Пн–Пт:
• отдел диспанс. наблюд. и амбул. лечения: с 08:00 до 17:30
• отдел организац. эпид. обслед. населения: с 08:00 до 15:42
Сб: с 09:00 до 15:00 – дежурный врач и медсестра
Вс: выходной
Читайте также:

