Дети с иммунитетом к вич
Обновлено: 05.05.2024
На этой неделе китайский учёный сообщил о рождении генетически отредактированных близнецов. В их геном были внесены изменения, позволяющие почти полностью исключить риск развития хронической ВИЧ инфекции. 1% европейцев обладают такой устойчивостью с рождения. Рассказываем о появлении и механизме резистентности к ВИЧ.
Более 40 миллионов человек по всему миру заражены вирусом иммунодефицита человека (ВИЧ). Если сразу после заражения иммунная система не успевает уничтожить все вирусные частицы, они могут проникнуть внутрь клеток и встроиться в их геном. В результате этого человек становится носителем инфекции. Хроническая ВИЧ инфекция на сегодняшний день неизлечима, однако поддается контролю и в случае своевременной терапии не оказывает сильного влияния на самочувствие человека.
Для проникновения в клетку ВИЧ должен связаться с двумя рецепторами на ее поверхности. Один из рецепторов – CD4, присутствует на поверхности T-лимфоцитов и отвечает за распознавание чужеродных агентов. Второй рецептор, необходимый для слияния оболочки вируса и клетки, - CCR5. Его роль в иммунной реакции до конца не изучена, предполагается, что он участвует в развитии воспалительной реакции.

У некоторых людей с рождения есть защита от ВИЧ, обусловленная наличием в их геноме мутаций. Это снижает риск развития хронической инфекции даже в случае заражения. Одной из них является мутация в гене рецептора CCR5, представляющая собой потерю части гена (32 нуклеотида) - ССR5Δ32. В результате вирус не может связаться с рецептором и проникнуть в клетку.
При этом риск развития хронической инфекции низкий только у гомозиготных носителей мутации - у тех, кому мутантный ген достался от обоих родителей. Существуют противоречивые данные о влиянии мутации только в одной копии гена CCR5 на риск развития ВИЧ: от наличия защиты до отсутствия какого-либо влияния на течение заболевания.

Предполагается, что мутация ССR5Δ32 возникла около 1000 лет назад в Северной Европе среди викингов. Распространение мутации в Европе обычно связывают с набегами викингов на соседние народы. Длительное время было непонятно, что способствовало распространению и закреплению мутации среди народов Европы, ведь ВИЧ — сравнительно молодая инфекция, и носители этой мутации не получали какого-либо преимущества. Однако впоследствие было обнаружено, что кроме ВИЧ эта мутация также снижает вероятность заразиться черной оспой, многочисленные эпидемии которой в свое время привели к массовой гибели людей по всему миру.
В настоящее время частота встречаемости этой мутации в странах Европы составляет около 10%. Частота мутации среди клиентов Genotek оказалась равной 9,7%. При этом только 1,1% людей оказались носителями мутации в двух копиях гена CCR5, они имеет низкий риск развития хронической инфекции даже в случае заражения.
Гомозиготное носительство делеции в гене CCR5 не является абсолютной защитой от заражения ВИЧ и поводом не использовать до- и пост-контактную профилактику при угрозе заражения. Известны единичные случаи, когда у людей с таким генотипом развивалось хроническое носительство ВИЧ после заражения. Возможно, это связано с тем, что кроме CCR5, вирус может использовать другие рецепторы для проникновения в клетки (например, рецептор СXCR4).

Один известный случай излечения человека от хронической ВИЧ инфекции связан с этой мутацией. Тимоти Браун, или Берлинский пациент, был заражен ВИЧ и болен лейкемией. Ему требовалась пересадка костного мозга. Врач смог подобрать донора, гомозиготного по мутации в CCR5. Через 20 месяцев после операции, несмотря на отсутствие терапии, ВИЧ перестал обнаруживаться в крови, костном мозге и слизистой оболочке кишечника пациента.
А совсем недавно российским ученым удалось получить человеческие эмбрионы с измененным геном CCR5, используя 16 оплодотворенных яйцеклеток не пригодных для программ ЭКО. Из 16 модифицированных яйцеклеток, только 8 продолжили развитие, причем в 5 из них модификация прошла успешно и обе копии гена были изменены.
А в ноябре 2018 года было распространено заявление ученого из Китая, которому якобы удалось провести аналогичный эксперимент, в результате которого родились девочки-близнецы, у одной из которых мутация в CCR5 присутствует в двух генах, а другой - только в одном. Родители близнецов приняли решение не раскрывать своих имен и места жительства, никаких других доказательств, кроме заявления врача, также нет.
Известно, что эксперимент провел профессор Хэ Цзянькуй из Южного университета науки и технологий в Шэньчжэ. Его суть состояла в том, что он имплантировал в матку зародыш, подвергнутый геномному редактированию методом CRISPR/cas9, который был создан в 2015 году. Как сообщил ученый, девочки совершенно здоровы, но за их состояниями будут следить в ближайший год.

Профессор Хэ Цзянькуй. Фото © Marilynn Marchione | AP
Ученый смог удалить участок ДНК, содержащий ген CCR5, который кодирует белок, позволяющий ВИЧ проникать в иммунную клетку и инфицировать ее. Ранее было доказано, что мутации в этом гене обеспечивают устойчивость человека к этому заболеванию.
Сам профессор пока отказался представить общественности новорожденных детей и их родителей, сославшись на то, что они не желают общаться с журналистами. Кроме этого, эксперимент не был описан ни в одном научном журнале. А в клинике, где, по словам ученого, якобы проводился эксперимент, отказались подтвердить эту информацию.
Известно, что в США и других развитых странах технологии редактирования генома эмбриона, который использовал ученый, запрещены из-за их непредсказуемости и по соображениями этики - их приравнивают к опытам над людьми. Но в Китае они не преследуются законом, хотя и противоречат рекомендациям Минздрава.
Несмотря на всю грандиозность и важность возможного открытия, многие ученые-генетики подвергли критике китайского профессора, поскольку любые изменения в геноме человека могут нести самые непредсказуемые последствия и будут унаследованы всеми потомками родившихся детей.
Также встает вопрос об этичности эксперимента и соотношения риска и польза, так как объектом вмешательства, вероятно, стали совершенно здоровые эмбрионы. Известно, что ВИЧ-инфекция не является смертельным заболеванием и существуют достаточно надежные способы профилактики передачи ВИЧ от матери ребенку. По общему мнению экспертов, не было ни малейшей необходимости прибегать к дорогостоящему и опасному методу редактирования генов с помощью технологии CRISPR8/cas9, чтобы предотвратить инфицирование детей ВИЧ.
Это не первый случай, когда китайские ученые сообщили о вмешательстве в геном человеческого эмбриона с целью возможности создания врожденной устойчивости к ВИЧ-инфекции. Но тогда эксперименты проводились над эмбрионами непригодными для процедуры экстракорпорального оплодотворения.
Кроме этого в сентября 2018 год ученые из Исследовательского центра акушерства, гинекологии и перинатологии имени Кулакова, МГУ и медицинского университета имени Пирогова сообщили, что смогли создать эмбрионы, обладающие устойчивостью к инфицированию ВИЧ.
Благодаря современной антиретровирусной терапии, принятым организационным мерам по своевременному обследованию беременных и назначению им АРВ-препаратов в России, как и во многих других странах, уровень вертикальной передачи ВИЧ от матери ребенку снизился в последние годы до минимальных значений — более 98% детей не получают ВИЧ. Специалисты и молодые родители с гордостью считали, что проблема сохранения здоровья ребенка, мать которого ВИЧ-положительна, решена. Однако, как выяснилось, это совсем не так: российские ученые установили, что у детей, рожденных ВИЧ-положительными матерями, существенно выше риск перинатальных потерь, мертворождения, ранней и поздней младенческой смертности. И дело тут совсем не в вирусе.

Василий Шахгильдян, врач-инфекционист
В чем проблема?
За весь период наблюдения, на 31 декабря 2020 года, от ВИЧ-положительных женщин родились 218 956 детей. Вирус выявили у 11 724 из них. При этом, по данным за 2020 год, на свет появились 13 186 малышей, из них инфицированы ВИЧ — всего 165 (по данным в настоящее время).
В 2019 году у женщин с ВИЧ родились 13 675 детей, из них 13 559 — живыми. Показатель мертворожденности (число мертворожденных на 1000 родившихся живыми и мертвыми) составил в случае ВИЧ-инфекции у матери 8,5‰ — то есть на 55% выше, чем в общей популяции (5,5‰).
- показатель перинатальной смертности (количество мертворожденных и умерших в первые 168 часов на 1000 родившихся живыми и мертвыми) в случае ВИЧ-инфекции у матери был 11,0‰, что на 60% выше показателя в общей популяции (6,8‰);
- показатель ранней неонатальной смертности (число мертворожденных и умерших в первые 168 часов на 1000 родившихся) среди детей от матерей с ВИЧ оказался на 82% выше, чем в общей популяции (2,5‰ и 1,4‰, соответственно);
- показатель младенческой смертности (количество умерших на 1000 родившихся живыми) детей ВИЧ-инфицированных матерей был на 33% выше (6,5‰), показателя в общей популяции (4,9‰).
С чем это может быть связано?
Одной из наиболее вероятных причин специалисты считают более высокую частоту внутриутробных инфекций, в том числе врожденной цитомегаловирусной инфекции. По словам Шахгильдяна, частота ее у детей, рожденных ВИЧ-положительными матерями, существенно выше.
Возможно, иммуносупрессия и другие более тонкие иммунологические нарушения в случае наличия ВИЧ-инфекции у матери увеличивают вероятность передачи ЦМВ через плаценту и создают условия для заражения плода и развития болезни.

Коллаж: Анна Сбитнева
Наиболее типичными клиническими проявлениями врожденной ЦМВ-инфекции являются тромбоцитопеническая пурпура, тромбоцитоз, длительная выраженная желтуха, низкий вес младенца, недоношенность, увеличение печени и селезенки, микроцефалия и гидроцефалия, гепатит, судорожный синдром, синдром мышечных и двигательных нарушений, поражение органов зрения, снижение слуха. При отсутствии лечения значительное число детей погибает в первые месяцы жизни или в 40–90% случаев у малышей развиваются тяжелые отдаленные неврологические нарушения.
Кроме того, даже при бессимптомном течении врожденной ЦМВ-инфекции есть риски отдаленных последствий. В 3–15% случаях формируются поздние неврологические осложнения, включая сенсоневральную глухоту (четверть всех случаев), нарушение восприятия речи при сохранении слуха, детский церебральный паралич, эпилепсию, задержку в развитии речи, снижение способности к обучению, чтению, гиперактивность, поведенческие проблемы.

Коллаж: Анна Сбитнева
По словам Шахгильдяна, расчетные данные показывают, что только в 2019 году не менее 400 младенцев ВИЧ-инфицированных матерей были внутриутробно заражены ЦМВ, из них 110–140 детей — страдают от ЦМВ-заболевания и/или могут иметь отдаленные психомоторные и когнитивные расстройства.
Что делать женщинам и врачам?
По словам врачей, при ведении ВИЧ-положительных беременных и их новорожденных детей очень важно заботиться не только о том, чтобы ребенок не был заражен ВИЧ, но и защитить его от иных внутриутробных инфекций. Это вполне возможно, учитывая существование современных методов лабораторной диагностики и лечения.
«Например, есть возможность использования молекулярных методов диагностики (ПЦР), позволяющих определять у беременной наличие ДНК ЦМВ в крови и моче и тем самым своевременно выявлять вторичную активной ЦМВ-инфекцию, которая также, как и острая (первичная) ЦМВ-инфекция может служить причиной заражения плода вирусом. Или, благодаря выявлению ДНК вируса простого герпеса (ВПГ) в соскобе из цервикального канала у женщины в третьем триместре беременности, устанавливать факт бессимптомного выделения вируса из урогенитального тракта, что может быть причиной заражения вирусом простого герпеса во время рождения ребенка и развития тяжелого неонатального герпеса. Естественно, выявление неблагоприятного факта является основанием для начала соответствующего лечения.

Коллаж: Анна Сбитнева
Кроме того, своевременная вакцинация молодой женщины позволит защитить ее, а значит, в дальнейшем при беременности — и ее будущего ребенка от ряда тяжелых инфекций.
«До наступления беременности женщины с ВИЧ должны вакцинироваться от гепатита В, краснухи, кори, ветряной оспы, коклюша, чтобы не подхватить эти инфекции во время беременности. Должна быть создана комплексная программа вакцинации молодых ВИЧ-положительных женщин. Когда женщина только начинает диспансерное наблюдение в центре по профилактике и борьбе со СПИДом, необходимо сосредотачиваться не только на антиретровирусной терапии и отслеживать показатели вирусной нагрузки и иммунного статуса, но и предлагать соответствующие обследования для создания персональной программы вакцинации от ряда инфекций.
Что произошло
В ноябре 2018 года китайский ученый Хэ Цзянькуя (He Jiankui) рассказал на отраслевой конференции , что внес изменения в эмбрионы семи пар, когда они проходили репродуктивное лечение. В итоге с измененным ДНК родились девочки-двойняшки Лулу и Нана.

Некоторое время сам факт операции вызывал сомнения. Потому что, кроме слов Хэ на конференции и его же интервью Associated Press, никакого подтверждения не было. Однако три месяца спустя власти КНР официально подтвердили заявления Хэ Цзянькуя, обязали остановить исследования и обвинили ученого в нарушении нескольких государственных законов.
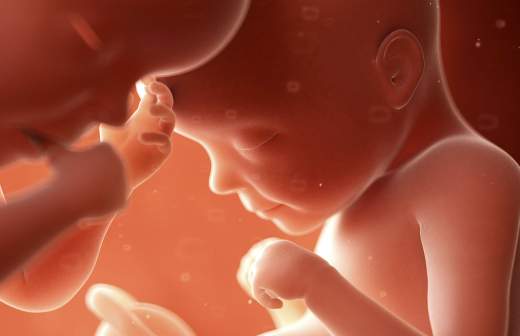
Пять месяцев назад ученые и медики критиковали редактирование генома эмбрионов — теперь призывают делиться опытом
Перед этим ученый говорил, что выбрал Китай для эксперимента именно потому, что в стране не действовал запрет на редактирование генома эмбрионов. Видимо, он проверил не все законы. 30 декабря 2019 года Суд города Шэньчжэнь на юге Китая приговорил ученого Хэ Цзянькуя (He Jiankui) к трем годам тюрьмы и штрафу в 3 млн юаней (около $430 тыс.). Он осужден за модификацию генома эмбрионов человека.
Что сделал ученый

Хэ Цзянькуй в своей лаборатории в Шэнчжене
Как менялось отношение научного сообщества
Когда Хэ рассказал об исследованиях на Втором международном саммите по генетическому редактированию человека в Гонконге, большинство коллег отнеслось к ним негативно. Нобелевский лауреат Дэвид Балтимор (David Baltimore) напомнил, что отключение гена CCR5 повышает опасность заражения лихорадкой Западного Нила и другими вирусными заболеваниями, а также увеличивает вероятность смерти от гриппа. Неприемлемым назвала эксперимент и Дженнифер Дудна (Jennifer Doudna), одна из создательниц технологии редактирования генома CRISPR/Cas9, которую использовал Хе.

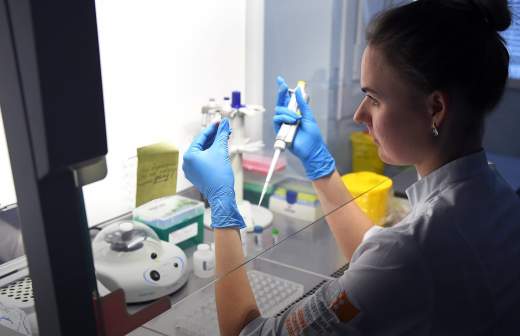
Введение белка Cas9 в пипетку
В феврале 2019 года в американском рецензируемом журнале Cell вышла статья о позитивном побочном эффекте редактирования генома. Тесты показали, что удаление у мышей того самого гена CCR5 улучшает их когнитивные (познавательные) функции. Также ученые выяснили, что люди, у которых CCR5 отсутствует из-за естественной мутации, быстрее восстанавливаются после инсульта.

Ввод белка Cas9 в эмбрион

Главный генетик России Сергей Куцев — о росте числа наследственных патологий в регионах и новых способах их лечения
Что пошло не так
Хэ мог бы получить Нобелевскую премию, если эксперимент прошел так, как он планировал. А планировал он воссоздать существующую в природе мутацию в гене CCR5, которая должна защищать своего носителя от ВИЧ. Однако поздний анализ генома девочек показал, что система редактирования внесла не ту мутацию. Причина неудачи в особенности работы CRISPR/Cas9. Ломает ген он легко, а вот нужные изменения вносит хоть и точнее других технологий, но далеко не идеально.
Хэ Цзянькуй, взяв на себя риск, не справился с задачей. Он понял, что редактирование генов может принести ему хорошую прибыль, и в погоне за личной славой и выгодой еще в 2016 году на собственные средства привлек сообщников и использовал технику, уровень безопасности и эффективности которой до сих пор не ясны. И, намеренно избегая какого-либо надзора и контроля, осуществил официально запрещенный в стране эксперимент по модификации ДНК. Больше того, он подделал материалы о соответствии эксперимента морально-этическим нормам и ввел в заблуждение испытуемых, создав впечатление, что эксперимент проводится законно. По крайней мере, так утверждает Государственный комитет КНР по делам здравоохранения и планового деторождения.

Эмбриологи команды Хэ Цзянькуя рассматривают изображения эмбриона на компьютере
Правда, Грили полагает, что произойдет это не скоро. Пока технология CRISPR слишком сложна. И крупные игроки не будут заниматься незаконными исследованиями, чтобы спрогнозировать возможную выгоду.
Эксперименты продолжатся
А пока ученые по всему миру продолжают изучать возможность воздействия на геном человека. Просто делают это не с эмбрионами. В США еще в январе 2018 года начали вводить добровольцам модифицированные лимфоциты в качестве иммунотерапии рака. В Великобритании, где в 2016 году было разрешено в исследовательских целях редактировать геном эмбрионов человека, запрет после истории с китайскими двойняшками так и не был введен. И там в том же 2016 году на свет появился ребенок, родителями которого можно считать трех человек.

Эмбрион с модифицированными генами
В России этой технологией интересуется не только Денис Ребриков. В феврале этого года Минобрнауки вместе с РАН разработали проект программы развития генетических технологий на 2019–2027 годы. Сделать это распорядился в ноябре 2018 года президент Владимир Путин. Тогда отмечалось, что программа нужна для ускорения развития генетических технологий и предупреждения чрезвычайных ситуаций биологического характера.
ВИЧ-инфекция у детей – это патологическое состояние, вызванное вирусом иммунодефицита человека (ВИЧ) и характеризующееся прогрессирующим снижением иммунитета ребенка. Специфических клинических симптомов нет, основные проявления – лихорадка, диарея неясной этиологии, лимфаденопатия, частые инфекционные и бактериальные заболевания, СПИД-ассоциированные и оппортунистические патологии. Основные методы лабораторной диагностики ВИЧ-инфекции у детей – ИФА, иммуноблоттинг, ПЦР. Специфическое лечение включает в себя схемы антиретровирусных препаратов (ингибиторов обратной транскриптазы и протеазы).

Общие сведения
ВИЧ-инфекция у детей – это заболевание, которое развивается в результате длительной персистенции вируса иммунодефицита человека в лимфоцитах и клетках нервной системы и характеризуется медленно прогрессирующей дисфункцией иммунной системы. Впервые данный вирус был описан французским вирусологом профессором Люком Монтанье в 1983 году. ВИЧ – это РНК-содержащий ретровирус, имеющий сложное строение и высокую изменчивость, что обеспечивает его выраженную способность к репликации и стойкости в организме человека. Распространенность ВИЧ-инфекции у детей за последние 15 лет уменьшилась более чем на 50%. Ежегодно в мире фиксируется порядка 250 тысяч случаев, из них в России около 6,5-7,5 тысяч. Правильное проведение профилактики вертикальной трансмиссии вируса позволило снизить частоту инфицирования с 30% до 1-3% беременностей ВИЧ-позитивных матерей.

Причины ВИЧ-инфекции у детей
ВИЧ-инфекция у детей имеет несколько механизмов передачи. Вирус может быть получен ребенком гематогенным путем от матери во время беременности. Также инфицирование может произойти во время использования необработанного медицинского инструментария, гемотрансфузий, трансплантации органов, у старших детей – при незащищенном половом акте. Все эти пути реализуются за счет содержания вируса в биологических жидкостях (кровь, спинномозговая жидкость, сперма, влагалищные выделения), тканях и органах инфицированного человека.
Основная причина (примерно 80%) ВИЧ-инфекции у детей – вертикальная передача вируса от матери к ребенку. Выделяют 3 периода, в которых потенциально возможно заражение – перинатальный (через систему плацентарного кровообращения), интранатальный (при контакте кожных покровов ребенка с кровью и секретом влагалища матери) и постнатальный (через грудное молоко). Риск инфицирования указанными путями составляет 20%, 60% и 20% соответственно. К факторам, повышающим риск передачи, относятся отсутствие профилактического лечения матери во время вынашивания ребенка, многоплодная беременность, преждевременные роды и роды через естественные половые пути, маточные кровотечения и аспирация крови ребенком, прием наркотических веществ и алкоголя во время беременности, вскармливание грудным молоком, экстрагенитальная патология и коинфекция.
Патогенез ВИЧ-инфекции у детей основан на связывании вируса с CD4+ Т-лимфоцитами, в которых он модифицирует ДНК клетки. В результате этого начинается синтез новых вирусных частичек, а затем – вирионов. После полной репродукции вируса происходит гибель Т-лимфоцитов, однако инфицированные клетки остаются в системном кровотоке, служа резервуаром. Как результат отсутствия функционально полноценных иммунокомпетентных клеток развивается иммунодефицит. Характерной особенностью ВИЧ-инфекции у детей является сопутствующий дефицит В-лимфоцитов и тропность вируса к тканям ЦНС. Проходя сквозь гематоэнцефалический барьер, вирус вызывает аномалию расположения глиальных клеток, задержку развития головного мозга, дистрофию и атрофию нервной ткани и определенных нервов (чаще всего – зрительного). В педиатрии поражение ЦНС является одним из первых маркеров наличия ВИЧ.
Симптомы ВИЧ-инфекции у детей
Клиническая картина ВИЧ-инфекции у детей может существенно отличаться в зависимости от периода и способа передачи вируса. При инфицировании парентеральным или половым путем присутствует острый ретровирусный синдром, после чего заболевание протекает в 4 стадии: два латентных этапа и два периода развернутых клинических симптомов. При вертикальном пути заражения острый ретровирусный синдром и бессимптомная стадия не выявляются. Острый ретровирусный синдром наблюдается у 30-35% детей после окончания инкубационного периода (от 2 недель до 3 месяцев с момента инфицирования). Клинически ВИЧ-инфекция у детей на этом этапе может проявляться фарингитом, лимфоаденопатией, гепатоспленомегалией, субфебрилитетом, уртикарной или папулезной сыпью, редко – менингеальными симптомами. Ее длительность колеблется от 2 суток до 2 месяцев, в среднем составляет 21 день.
Следующая стадия – бессимптомного носительства и персистирующей лимфаденопатии. Возможное проявление ВИЧ-инфекции у детей на этой стадии – увеличение двух групп лимфоузлов. Ее длительность – от 2 до 10 лет. Вторая стадия характеризуется потерей массы тела (порядка 10%), поражением кожных покровов и слизистых оболочек (дерматиты, микозы придатков кожи, рецидивные заболевания слизистых ротовой полости и губ), рецидивирующим опоясывающим герпесом. Общее состояние, как правило, не нарушается. Третья стадия включает в себя выраженные проявления иммунодефицита: общее недомогание, диарею невыясненной этиологии, анорексию, лихорадку, головную боль, потливость по ночам, спленомегалию. ВИЧ-инфекция у детей на данном этапе сопровождается неврологическими нарушениями, отмечаются периферическая невропатия, ухудшение памяти. Также она характеризуется рецидивирующим кандидозом полости рта, простым и опоясывающим герпесом, ЦМВ-паротитом. При четвертой стадии (стадия СПИДа) на первый план выходят клинические проявления тяжелых оппортунистических заболеваний и опухолей.
У младенцев и детей в возрасте до 3 лет типичной особенностью является высокая частота тяжелых бактериальных инфекций. Практически в 50% случаев ВИЧ-инфекции у детей возникают гнойные отиты, менингиты, поражения кожи, бактериальные пневмонии со склонностью к абсцедированию и появлению плеврального выпота, бактериальный сепсис, поражения суставов и костей. Как правило, в роли возбудителей выступают S. pneumoniae, S. aureus, H. influenzae, E. coli и некоторые виды сальмонелл.
Диагностика ВИЧ-инфекции у детей
Диагностика ВИЧ-инфекции у детей основывается на данных анамнеза и лабораторных тестах. Объективный осмотр и инструментальные методы исследования информативны только в случае развития бактериальных инфекций или СПИД-ассоциированных заболеваний. Подозрение на ВИЧ-инфекцию у детей возникает при выявлении педиатром хотя бы четырех из следующих симптомов: отягощенный эпидемиологический анамнез, генерализованная гиперплазия лимфоузлов, потеря массы тела (свыше 10% от исходной), необоснованная диарея (более 1 месяца), стойкая или перемежающаяся гипертермия (более 1 месяца), частые бактериальные, вирусные, грибковые или паразитарные заболевания, СПИД-ассоциированные и оппортунистические патологии и т. д.
Ведущее место в диагностике ВИЧ-инфекции у детей занимают лабораторные тесты. Среди неспецифических изменений в общем и биохимическом анализах крови могут присутствовать анемия, лейкопения, тромбоцитоз или тромбоцитопения, повышение уровня АлТ и/или АсТ. При иммунологических исследованиях у таких детей можно выявить повышение уровня иммуноглобулинов, падение уровня CD4 и соотношения CD4/CD8, уменьшение продукции цитокинов, повышение уровня циркулирующих иммунокомплексов, у новорожденных возможна гипо-γ-глобулинемия. Специфическая диагностика ВИЧ-инфекции у детей подразумевает проведение ИФА с определением антител к вирусу. При его позитивном результате осуществляется иммуноблоттинг с идентификацией иммуноглобулинов к некоторым белкам вируса (gp 41, gp 120, gp 160). В последнее время широко используются тесты для определения вирусной нагрузки (количества копий вирусной РНК).
Лечение ВИЧ-инфекции у детей
Лечение ВИЧ-инфекции у детей заключается в проведении специфической антиретровирусной терапии, профилактике или лечении оппортунистических заболеваний и устранении симптомов патологии. В современной медицинской практике используются противовирусные препараты, ингибирующие обратную транскриптазу (нуклеозидные и ненуклеозидные аналоги) и протеазу. Наиболее эффективной считается схема, состоящая их трех препаратов – два нуклеозидных аналога и один ингибитор протеазы. Выбор конкретных медикаментов, схема их употребления подбираются индивидуально для каждого ребенка. В зависимости от имеющихся оппортунистических заболеваний используются специфические этиотропные (антибиотики, противотуберкулезные, противовирусные, противогрибковые препараты и пр.) и симптоматические (жаропонижающие, антигистаминные, пробиотики, витаминные комплексы, дезинтоксикационная терапия) средства.
Прогноз и профилактика ВИЧ-инфекции у детей
Прогноз при ВИЧ-инфекции у детей серьезный. Как правило, правильно подобранная антиретровирусная терапия позволяет добиться замедления репликации вируса на долгие годы, однако на данный момент ВИЧ остается неизлечимым заболеванием. На фоне проводимого лечения удается достичь высокого качества и удовлетворительной продолжительности жизни и полной адаптации ребенка в социуме.
Профилактика ВИЧ-инфекции у детей включает в себя исключение всех возможных путей передачи вируса: контроль переливаемой крови и трансплантируемых органов, медицинского инструментария, избежание незащищенных половых актов. Отдельное место занимает профилактика вертикальной трансмиссии. Согласно рекомендациям UNICEF, она включает в себя помещение беременной ВИЧ-позитивной женщины на учет у гинеколога, прием противовирусных средств с 24-28 недели, рациональный выбор способа родоразрешения, исключение грудного вскармливания, назначение противовирусных средств ребенку с момента рождения. Данные меры позволяют снизить риск развития ВИЧ-инфекции у детей до 1-3%.
Читайте также:

