Доклад на тему кожный лейшманиоз
Обновлено: 25.04.2024
Кожно-слизистый лейшманиоз (эспундия, espundia, mucocutaneous leishmaniasis, кожно-слизистый бразильский лейшманиоз) - разновидность кожного лейшманиоза Нового света заболевание кожи и слизистых оболочек, вызываемое простейшим паразитом Leishmania braziliensis.
Что провоцирует / Причины Кожно-слизистого лейшманиоза (эспундии):
Возбудитель кожно-слизистого лейшманиоза - Leishmania braziliensis. Распространён в лесах Южной Америки к востоку от Анд, протекает с обширным поражением кожи, в последующем слизистых оболочек, обычно верхних дыхательных путей, иногда с глубоким разрушением мягких тканей и хрящей.
Патогенез (что происходит?) во время Кожно-слизистого лейшманиоза (эспундии):
Заболевание переносится москитами родам Phlebotomus. В Южной Америке переносчиками возбудителей кожного лейшманиоза являются москиты из рода Lutzomyia. Причем в организме москитов паразит находится в жгутиковой форме, а в организме человека - в лейшманиальной (внутриклеточной).
Резервуар инфекции - крупные лесные грызуны. Обычно регистрируют у рабочих, занятых на лесных и дорожных работах, среди населения лесных посёлков.
Лейшманиозы относятся к зоонозным инфекциям и поражают грызунов и псовых на всех населенных континентах, за исключением Австралии. Распространенность лейшманиозов варьирует: на побережье Средиземного моря ими поражены 4 - 10% собак, а в южных районах нашей страны - 80-95% песчанок; у многих из них инвазия протекает субклинически. Распространение болезни происходит тогда, когда самка москита рода Lutzomyia заглатывает амастогиты при кровососании на инфицированных млекопитающих. В желудке насекомого амастиготы превращаются в промастиготы, мигрируют в хоботок и при очередном кровососании попадают в кожу нового хозяина. Выплод москитов происходит в теплом влажном микроклимате - в норах грызунов, термитниках, в скоплениях гниющей растительности. Человек заражается лейшманиозом, попадая в такой природный очаг. Наличие инфекции у домашних собак служит важным резервуаром лейшманиоза в городах. Передача лейшманиозов от человека человеку, за исключением случаев индийского кала-азара, происходит весьма редко. Еще реже передача инфекции может произойти при переливаниях крови, инъекциях и половых контактах. По оценочным данным, в мире насчитывается свыше 12 млн человек, пораженных лейшманиозом.
Промастиготы попадают в кожу в небольшое скопление крови, образовавшееся при кровососании москита. Лейшманий фиксируют комплемент на своей поверхности посредством альтернативного пути и быстро проникают в макрофаг благодаря рецептору комплемента 3-го типа (РКЗ) и рецептору маннозила/флюкозила. Промастиготы превращаются в амастиготы внутри фаголизосом и размножаются бинарным делением. В конечном итоге они разрывают клетку и проникают в соседние макрофаги.
Дальнейшее развитие заболевания определяется уровнем клеточного иммунитета хозяина, равно как и видовой формой возбудителя. При кожно-слизистом лейшманиозе спустя некоторое время после полного или частичного заживления первичного элемента могут появиться метастатические поражения кожных и слизистых покровов. Разрушительный характер метастатических поражений связывают с развитием повышенной чувствительности к антигенам простейшего. Исключением из типичного характера развития кожного лейшманиоза является диффузный кожный лейшманиоз, при котором не отмечается инфильтрации лимфоцитами и плазматическими клетками или снижения числа возбудителей; лейшманиновая реакция остается отрицательной, а поражение кожи становится хроническим, прогрессирующим и распространенным. При этом у больных, по-видимому, имеется избирательная анергия к антигенам лейшманий, которая опосредуется, по крайней мере, частично, прилегающими клетками-супрессорами. Способность лейшманий вызывать прогрессирующее заболевание может быть связана с формированием в организме хозяина Т-лимфоцитов-супрессоров. После выздоровления остается иммунитет к данному штамму возбудителя.
Симптомы Кожно-слизистого лейшманиоза (эспундии):
Симптомы кожно-слизистого лейшманиоза появляются через 1-4 нед после укуса переносчика. Клиническая картина: характерны безболезненные, деформирующие поражения рта и носа, метастазирующие на соседние участки с появлением грибовидных и эрозивных язв на языке, слизистой щёк и носа; возможны рецидивы через несколько лет после спонтанного исчезновения первичных очагов.
Слизистые поражения возникают при наличии открытых язв, но чаще поражение носоглотки возникают после рубцевания кожных язв. Сопровождается разрушением носовой перегородки, мягкого неба, хрящей глотки и гортани.
Заболевание сопровождают лихорадка, снижение веса и вторичные бактериальные инфекции.
Осложнения кожно-слизистого лейшманиоза:
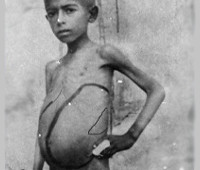
- На поздних стадиях заболевания возможны отёки, кахексия, гиперпигментация.
- Бактериальные суперинфекции и кровотечения из ЖКТ могут стать причиной смерти нелеченых больных с висцеральным лейшманиозом.
- У 3-10% леченых пациентов развиваются изменения кожных покровов в виде депигментированных пятен и бородавкообразных узелков на лице и разгибательной поверхности конечностей.
- У пациентов со слизисто-кожным лейшманиозом возможны метастатические деструктивные поражения слизистой носоглотки.
Диагностика Кожно-слизистого лейшманиоза (эспундии):
Для диагностики заболевания проводятся анализ материала из лимфатических узлов, язв, а также анализ крови. При висцеральном лейшманиозе результаты анализа крови показывают повышение СОЭ, уменьшение содержания альбуминов, повышение уровня глобулинов, анемию, тромбоцитопению. Дополнительным указанием на возможность заболевания является пребывание больного в эндемичных по лейшманиозу районах в последние год-два.
Лечение Кожно-слизистого лейшманиоза (эспундии):
Лечение кожно-слизистого лейшманиоза проводится специфическими препаратами только по назначению врача. Дополнительно к основному лечению для предотвращения развития побочных бактериальных инфекций назначают антибиотики. Также прописывают витамины, антианемические средства, проводят инфузии эритроцитарной массы и плазмы.
Препараты выбора: Антимонил глюконат натрий - по 20 мг/кгв/в или в/м 1 р/сут в течение 20-30 дней. Меглумин антимониат (глюкантим) - по 20-60 мг/кг глубоко в/м 1 р/сут в течение 20-30 дней. При рецидиве заболевания или недостаточной эффективности лечения следует провести повторный курс инъекций в течение 40-60 дней. Эффективно дополнительное назначение аллопуринола 20-30 мг/кг/сут в 3 приёма внутрь.
Альтернативные препараты при рецидивах заболевания и резистентности возбудителя к препаратам выбора: Амфотерицин В - 0,5-1,0 мг/кг в/в через день, или Пентамидин - в/м 3-4 мг/кг 3 р/нед в течение 5-25 нед. При отсутствии эффекта химиотерапии дополнительно человеческий рекомбинантный у-интерферон.
Течение и прогноз. При ранней диагностике и своевременном лечении выздоравливают более 90% больных. Даже на фоне химиотерапии смертность достигает 15-25%. При отсутствии лечения 95% взрослых и 85% детей погибают в течение 3-20 мес.
Профилактика Кожно-слизистого лейшманиоза (эспундии):
Проводят уничтожение насекомых-переносчиков, грызунов и бродячих собак в районах, прилегающих к населённым пунктам. Лицам, посещающим эндемичные очаги, рекомендовано пользоваться индивидуальными средствами защиты (репелленты, противомоскитные сетки и т.д.). Своевременное лечение больных лейшманиозом.
К каким докторам следует обращаться если у Вас Кожно-слизистый лейшманиоз (эспундия):
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Кожно-слизистого лейшманиоза (эспундии), ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Лейшманиоз представляет собой протозойную инфекцию с трансмиссивным механизмом распространения, характеризующуюся поражением кожных покровов или внутренних органов внутриклеточными паразитами – лейшманиями. Лейшманиозы подразделяют на висциральные, протекающие с поражением легких, печени, селезенки, сердца, и кожные, проявляющиеся трансформирующимися в очаги изъязвления папулами. Диагностика лейшманиоза осуществляется путем выявления лейшманий в крови пациента (при висцеральной форме) или в отделяемом кожных элементов (при кожной форме).
Общие сведения
Лейшманиоз представляет собой протозойную инфекцию с трансмиссивным механизмом распространения, характеризующуюся поражением кожных покровов или внутренних органов внутриклеточными паразитами – лейшманиями.
Характеристика возбудителя
Лейшманиоз вызываются семнадцатью из более чем двадцати видов простейших паразитов рода Leishmania. Лейшмании развиваются внутри клеток хозяина (преимущественно в макрофагах и элементах ретикулоэндотелиальной системы). В течение своего жизненного цикла им необходимо сменить двух хозяев. В организме позвоночных животных лейшмании находятся в безжгутиковой форме, развиваясь в жгутиковую форму в теле членистоногого. Лейшмании отличаются резистентностью к антибиотикам, и чувствительны к препаратам пятивалентной сурьмы.
Подавляющее большинство лейшманиозов – зоонозы (резервуаром и источником инфекции являются животные), только два вида – антропонозы. Виды животных, участвующих в распространении лейшманиоза, довольно ограничены, поэтому инфекция является природно-очаговой, распространяется в пределах обитания соответствующей фауны: грызунов песчаниковых видов, псовых (лисы, собаки, шакалы), а также переносчиков – москитов. Преимущественно очаги лейшманиоза располагаются в странах Африки и Южной Америки. Большинство из них - развивающиеся, среди 69 стран, где распространен лейшманиоз, 13 являются беднейшими странами мира.
Человек является источником инфекции в случае поражения кожной формой лейшмании, при этом москиты получают возбудителя с отделяемым кожных язв. Висцеральная лейшмания в подавляющем большинстве случаев является зоонозной, москиты заражаются от больных животных. Заразность москитов отсчитывается с пятого дня попадания лейшманий в желудок насекомого и сохраняется пожизненно. Человек и животные контагиозны в течение всего срока пребывания возбудителя в организме.
Лейшманиоз передается исключительно с помощью трансмиссивного механизма, переносчики – москиты, получают инфекцию, питаясь кровью больных животных, и переносят здоровым особям и людям. Человек обладает высокой восприимчивостью к инфекции, после перенесения кожного лейшманиоза сохраняется продолжительный стойкий иммунитет, висцеральная форма такового не формирует.
Патогенез
Возбудитель проникает в толщу кожи человека при укусе москита, формируя в области входных ворот лейшманиозную гранулему. Впоследствии, при висцеральной форме инфекции гранулема рассасывается, а при кожной - прогрессирует в язву. Лейшмании разносятся по организму с током лимфы, поражая регионарные лимфатические узлы. Вдоль лимфатического сосуда паразиты могут формировать лейшманиомы – ряд последовательно располагающихся специфических язв.
В Южной Америке отмечаются формы лейшмании, протекающие с поражением слизистых оболочек ротовой полости, носоглотки и верхних дыхательных путей с грубой деформацией глубоких тканей и развитием полипозных образований. Висцеральная форма лейшманиоза развивается в результате рассеивания возбудителя по организму и попадания в печень, селезенку, костный мозг. Реже – в кишечную стенку, легкие, почки и надпочечники.
Возникающий иммунный ответ подавляет инфекцию, при этом заболевание протекает латентно, либо с маловыраженной симптоматикой. При иммунодефиците, сниженных защитных свойствах лейшманиоз прогрессирует, протекает с выраженной клиникой интоксикационного синдрома, лихорадкой. Размножение паразитов в печени способствуют замещению гепатоцитов фиброзной тканью, в селезенке отмечают атрофию пульпы с участками инфарктов и некротизации. Вследствие поражения костного мозга развивается анемия. В целом висцеральный лейшманиоз, прогрессируя, вызывает общую кахексию.
Классификация
Лейшманиозы подразделяются на висцеральные и кожные формы, каждая форма, в свою очередь, разделяется на антропонозы и зоонозы (в зависимости от резервуара инфекции). Висцеральные зоонозные лейшманиозы: детский кала-азар (средиземноморско-среднеазиатский), лихорадка дум-дум (распространена в восточной Африке), носоглоточный лейшманиоз (кожно-слизистый, лейшманиоз Нового Света).
Индийский кала-азар является висцеральным антропонозом. Кожные формы лейшманиоза представлены болезнью Боровского (городской антропонозный тип и сельский зооноз), пендинской, ашхабадской язвами, багдадским фурункулом, эфиопским кожным лейшманиозом.
Симптомы лейшманиоза
Висцеральный средиземноморско-азиатский лейшманиоз
Инкубационный период этой формы лейшманиоза составляет от 20 дней до нескольких (3-5) месяцев. Иногда (довольно редко) затягивается до года. У детей раннего возраста в этот период может отмечаться первичная папула в месте внедрения возбудителя (у взрослых встречается в редких случаях). Инфекция протекает в острой, подострой и хронической формах. Острая форма обычно отмечается у детей, характеризуется бурным течением и без должной медицинской помощи заканчивается летально.
Чаще всего встречается подострая форма заболевания. В начальном периоде отмечается постепенное нарастание общей слабости, разбитости, повышенной утомляемости. Отмечается снижение аппетита, побледнение кожи. В этом периоде при пальпации можно выявить некоторое увеличение размеров селезенки. Температура тела может подниматься до субфебрильных цифр.
Подъем температуры до высоких значений говорит о вступлении заболевания в период разгара. Лихорадка имеет неправильный или волнообразный характер, продолжается в течение нескольких дней. Приступы лихорадки могут сменяться периодами нормализации температуры или снижения до субфебрильных значений. Такое течение обычно продолжается 2-3 месяца. Лимфатические узлы увеличены, отмечается гепато- и, в особенности, спленомегалия. Печень и селезенка при пальпации умеренно болезненны. При развитии бронхоаденита отмечается кашель. При такой форме нередко присоединяется вторичная инфекция дыхательной системы и развивается пневмония.
С прогрессированием заболевания отмечается усугубление тяжести состояния больного, развивается кахексия, анемия, геморрагический синдром. На слизистых оболочках ротовой полости возникают некротизированные участки. Ввиду значительного увеличения селезенки происходит смещение сердца вправо, тоны его глухие, ритм сокращений ускорен. Отмечается склонность к падению периферического артериального давления. С прогрессированием инфекции формируется сердечная недостаточность. В терминальном периоде больные кахексичны, кожные покровы бледные и истонченные, отмечаются отеки, выражена анемия.
Хронический лейшманиоз протекает латентно, либо с незначительной симптоматикой. Антропонозный висцеральный лейшманиоз может сопровождаться (в 10% случаев) появлением на коже лейшманоидов – мелких папиллом, узелков или пятен (иногда просто участки со сниженной пигментацией), содержащих возбудителя. Лейшманоиды могут существовать годами и десятилетиями.
Кожный зоонозный лейшманиоз (болезнь Боровского)
Распространен в тропическом и субтропическом климате. Инкубационный период его составляет 10-20 дней, может сокращаться до недели и удлиняться до полутора месяцев. В области внедрения возбудителя при этой форме инфекции обычно формируется первичная лейшманиома, первоначально имеющая вид розовой гладкой папулы около 2-3 см в диаметре, в дальнейшем прогрессирующей в безболезненный или малоболезненный при надавливании фурункул. Спустя 1-2 недели в лейшманиоме формируется некротический очаг, и вскоре образуется безболезненное изъязвление с подрытыми краями, окруженное валиком инфильтрированной кожи с обильным отделяемым серозно-гнойного или геморрагического характера.
Диффузно-инфильтрирующий лейшманиоз
Отличается значительной распространенной инфильтрацией кожи. Со временем инфильтрат регрессирует, не оставляя последствий. В исключительных случаях отмечаются мелкие язвы, заживающие без заметных рубцов. Такая форма лейшманиоза достаточно редка, обычно отмечается у пожилых лиц.
Туберкулоидный кожный лейшманиоз
Наблюдается в основном у детей и молодых людей. При этой форме вокруг послеязвенных рубцов или на них появляются мелкие бугорки, могущие увеличиваться в размерах и сливаться друг с другом. Изъязвляются такие бугорки редко. Язвы при этой форме инфекции оставляют значительные рубцы.
Антропонозная форма кожного лейшманиоза
Характеризуется продолжительным инкубационным периодом, который может достигать нескольких месяцев и лет, а также медленным развитием и умеренной интенсивностью кожных поражений.
Осложнения лейшманиоза
Длительно протекающий лейшманиоз прогрессирует с развитием пневмонии, нефритов, агранулоцитоза, геморрагического диатеза, а также может осложняться гнойно-некротическими воспалениями.
Диагностика лейшманиоза
Общий анализ крови при лейшманиозе показывает признаки гипохромной анемии, нейтропении и анэозинофилии при относительном лимфоцитозе, а также пониженную концентрацию тромбоцитов. СОЭ повышена. Биохимический анализ крови может показать гипергаммаглобулинемию. Выделение возбудителя кожного лейшманиоза возможно из бугорков и язв, при висцеральном - лейшмании обнаруживаются в посеве крови на стерильность. При необходимости для выделения возбудителя производят биопсию лимфоузлов, селезенки, печени.
В качестве специфической диагностики осуществляют микроскопическое исследование, бакпосев на питательной среде NNN, биопробы на лабораторных животных. Серологическая диагностика лейшманиоза проводится с применением РСК, ИФА, РНИФ, РЛА. В периоде реконвалесценции отмечается позитивная реакция Монтенегро (кожная проба с лейшманином). Производится при эпидемиологических исследованиях.
Лечение лейшманиоза
Этиологическое лечение лейшманиоза заключается в применении препаратов пятивалентной сурьмы. При висцеральной форме их назначают внутривенно с нарастанием дозировки на 7-10 дней. В случае недостаточной эффективности терапию дополняют амфотерицином В, вводимым с 5% раствором глюкозы внутривенно медленно. На ранних стадиях кожного лейшманиоза бугорки обкалывают мономицином, сульфатом берберина или уротропином, а также назначают эти препараты в виде мазей и примочек.
Сформировавшиеся язвы являются показанием к назначению мирамистина внутримышечно. Для ускорения заживления язв эффективна лазерная терапия. Препаратами резерва при лейшманиозе являются амфотерицин В и пентамидин, их назначают в случаях рецидивирования инфекции и при резистентности лейшманий к традиционным средствам. Для повышения эффективности терапии можно добавить человеческий рекомбинантный гаммаинтерферон. В некоторых случаях бывает необходимо хирургическое удаление селезенки.
Прогноз и профилактика лейшманиоза
При легко протекающем лейшманиозе возможно самостоятельное выздоровление. Благоприятен прогноз при своевременном выявлении и должных медицинских мерах. Тяжелые формы, инфицирование лиц с ослабленными защитными свойствами, отсутствие лечения значительно ухудшают прогноз. Кожные проявления лейшманиоза оставляют косметические дефекты.
Профилактика лейшманиоза включает меры по благоустройству населенных пунктов, ликвидацию мест расселения москитов (свалок и пустырей, затопленных подвальных помещений), дезинсекцию жилых помещений. Индивидуальная профилактика заключается в использовании репеллентов, других средств защиты от укусов москитов. При обнаружении больного производят химиопрофилактику пириметамином в коллективе. Специфическая иммунная профилактика (вакцинация) производится лицам, планирующим посещение эпидемически опасных районов, а также неимунному населению очагов инфекции.
Висцеральный лейшманиоз – это хроническое инфекционное протозойное заболевание с поражением печени и селезенки, развитием анемии и кахексии. Другими симптомами являются лихорадка, увеличение лимфоузлов, кожные проявления. Диагностика включает выявление возбудителя из крови и биоптатов внутренних органов, реже путем биопроб на грызунах, поиск антител к возбудителю. Лечение состоит из курса этиотропных препаратов (преимущественно пятивалентной сурьмы) и коррекции органных дисфункций в качестве симптоматической терапии. В некоторых случаях показаны гемотрансфузии.
МКБ-10
Общие сведения
Висцеральный лейшманиоз (лихорадка дум-дум, кала-азар, черная лихорадка) принадлежит к трансмиссивным инфекциям, вызываемым простейшими. В 1903 году английский патолог Лейшман совместно с итальянским ученым Донованом описал морфологию органных поражений и выделил возбудителя. В честь исследователей инфекционный агент получил своё название Leishmania donovani. Болезнь наиболее распространена в тропических и субтропических странах, сезонный рост заболеваемости зависит от особенностей жизненного цикла переносчика и приходится на период с мая по ноябрь.

Причины
Возбудитель инфекции – простейший паразитический микроорганизм лейшмания. Источниками и резервуарами инфекции служат теплокровные дикие и домашние животные (грызуны, ленивцы, лисы, собаки), люди. Путь инфицирования преимущественно трансмиссивный, переносчики – самки москитов рода Phlebotomus. Имеются данные о единичных случаях заражения при переливаниях крови, передачи лейшманий от матери плоду, при использовании нестерильного медицинского инструментария и игл во время внутривенного введения наркотических средств.
В своем развитии лейшманиям необходимо пройти две стадии: безжгутиковую и жгутиковую в организме человека либо животного и переносчика соответственно. Амастиготы обитают внутри клеток, лишены способности к перемещению, промастиготы имеют жгутики для активных движений в пространстве. Находясь внутри самки москита, лейшмании активно размножаются в пищеварительном канале насекомого, после чего перемещаются к хоботку. Наиболее подвержены заражению дети до 5 лет, молодые мужчины, сельскохозяйственные работники, туристы, пациенты с ВИЧ-инфекцией, онкопатологиями.
Патогенез
В месте укуса переносчика формируется первичный аффект в виде гранулемы, которая состоит из макрофагов с размножающимися внутри лейшманиями, ретикулоцитов, эпителиоцитов и гигантских клеток. Через некоторое время гранулема подвергается обратному развитию, реже рубцеванию, а находящиеся в макрофагах возбудители с током лимфы и крови попадают во внутренние органы. При нормальном состоянии иммунной системы происходит разрушение пораженных клеток. В случае иммунодефицита лейшмании размножаются с увеличенной скоростью, поражают паренхиматозные органы.
Это приводит к возникновению воспалительных изменений, активному фиброзированию и увеличению размеров органов. В печеночной ткани при патогистологическом исследовании обнаруживаются участки интерлобулярного фиброза и дистрофия гепатоцитов, в лимфатических узлах – дистрофические изменения зародышевого центра и аплазия костного мозга, в селезенке – атрофия пульпы, зоны инфарктов, некроза и геморрагических инфильтратов. При длительном течении висцерального лейшманиоза возникает амилоидоз внутренних органов.
Классификация
Разделение висцерального лейшманиоза на сельский и городской виды подразумевает разные источники инфекции (домашние и дикие животные), а также тяжесть течения патологии – считается, что при городском типе болезнь протекает доброкачественнее. Выделяют острый, подострый и хронический варианты органного лейшманиоза. Наиболее благоприятным течением отличается хроническая форма, острый тип данной протозойной инфекции чаще всего встречается у детей, характеризуется бурным развитием симптомов и нередкими летальными исходами. Для подострого варианта типично наличие осложнений.
Симптомы висцерального лейшманиоза
Инкубационный период составляет от 20 дней до 1 года, чаще 3-5 месяцев. Для манифестации болезни характерно постепенное начало, появление кожной папулы бледно-розового цвета на месте внедрения возбудителя, сменяющейся участком депигментации (лейшманоид). Отмечается слабость, беспричинная усталость, снижение аппетита, похудание. В дальнейшем присоединяется лихорадка до 39-40° C, которая протекает с чередованием высокой и нормальной температуры тела на продолжении нескольких месяцев.
Наблюдается безболезненное увеличение всех групп лимфатических узлов, изменение их консистенции до плотно-эластической. Пациенты с висцеральным лейшманиозом почти всегда отмечают тяжесть и дискомфорт в подреберьях. При прогрессировании болезни наблюдается гепатоспленомегалия с появлением отеков и увеличением живота. Снижается количество выделяемой мочи. В связи с развитием гиперспленизма и поражения костного мозга возникают кровотечения. Обнаруживается одышка, язвенно-некротические поражения ротовой полости, бледность кожи, нарушения дефекации.
Осложнения
Наиболее частые осложнения (тромбогеморрагический синдром, гранулоцитопения, агранулоцитоз) связаны с поражением кроветворной системы, следствием чего является некроз миндалин, слизистой рта и десен (нома). Отечно-асцитический синдром при висцеральном лейшманиозе возникает из-за вовлечения печени, сопровождается хронической сердечной недостаточностью, нарушениями в работе ЖКТ (энтероколитом), нефритом, снижением либидо, олиго- и аменореей. Характерны случаи бактериальной пневмонии ввиду высокого стояния диафрагмы и снижения дыхательной емкости легких. К редким осложнениям относят разрывы селезенки, геморрагический шок, ДВС-синдром.
Диагностика
Определение висцеральной формы лейшманиоза требует осмотра инфекциониста, по показаниям назначаются консультации других специалистов. Важно уточнить у пациента факт пребывания в эндемичных зонах земного шара в течение предшествующих пяти лет, наличие вакцинации от лейшманиоза, род профессиональных занятий. Лабораторные и инструментальные методы верификации болезни включают в себя:
- Физикальное исследование. Во время объективного осмотра обращает на себя внимание бледность, сухость, истончение кожи, наличие язв в полости рта. Лимфоузлы плотные, увеличенные, безболезненные. При аускультации тоны сердца приглушены, выслушивается тахикардия, шумы, в легких могут определяться участки ослабленного дыхания. Пальпация живота безболезненна, размеры селезенки и печени резко увеличены. Часто обнаруживаются периферические отеки, асцит.
- Лабораторные исследования. Признаками лейшманиоза в общем анализе крови служат анемия, пойкилоцитоз, анизоцитоз, лейкопения, нейтропения, анэозинофилия, тромбоцитопения, резкое ускорение СОЭ. Биохимические параметры изменены в сторону повышения АЛТ, АСТ, СРБ, креатинина и мочевины, гипоальбуминемии. Наблюдается увеличение времени свертывания крови. В общеклиническом анализе мочи отмечается повышение плотности мочевого осадка, протеинурия, гематурия.
- Выявление инфекционных агентов. Для обнаружения лейшманий проводится микроскопия, посев биологических препаратов и крови, реже биопробы на хомячках. Серологическая диагностика (ИФА) направлена на выявление противолейшманиозных антител. Использование внутрикожной пробы Монтенегро является косвенным методом подтверждения диагноза в период реконвалесценции, применяется при эпидемиологических исследованиях в популяции.
- Инструментальные методики. Рентгенография ОГК выполняется для исключения пневмонии, туберкулезного поражения. Сонография брюшной полости визуализирует увеличение размеров печени, селезенки, признаки портальной гипертензии, наличие асцита. УЗИ и биопсию лимфатических узлов, стернальную пункцию, трепанобиопсию костного мозга, диагностическую торакоскопию и лапароскопию осуществляют по показаниям.
Туберкулез проявляется длительным субфебрилитетом, редко сухим кашлем и симптомами дисфункции вовлеченных в патологический процесс органов; часто диагноз верифицируется только лабораторно-инструментальными методиками. Схожесть клинических симптомов заболевания наблюдается с такими патологиями, как лейкоз и лимфогранулематоз, при данных патологиях диагностическими критериями становятся данные анализов крови и биопсии костного мозга. Сепсис клинически протекает схоже, но обычно имеет первичный очаг поражения (рана, гнойное образование и др.).
Лечение висцерального лейшманиоза
Пациенты с данным заболеванием госпитализируются в стационар. В обязательном порядке необходимо ограничить возможность контакта с москитами, поэтому над кроватями и в оконных проемах устанавливают противомоскитные сетки. Постельный режим показан до устойчивых нормальных цифр температуры тела в течение 3-5 дней, из-за риска разрыва селезенки при её значительном увеличении не рекомендуются резкие наклоны, повороты, поднятие тяжестей более 10 кг. Режим питания предусматривает высококалорийную, богатую белками пищу, водная нагрузка подбирается индивидуально.
Этиотропная терапия висцерального лейшманиоза должна включать препараты сурьмы (натрия стибоглюконат) либо пентамидин, милтефозин, липосомальный амфотерицин В. Некоторые исследования показали эффективность терапевтического приема производных пятивалентной сурьмы в сочетании с сульфатом паромомицина, при этом сокращается длительность курса лечения. Пациентам с осложнениями, ВИЧ-инфекцией, тяжелыми сопутствующими болезнями рекомендовано курсовое введение амфотерицина В как первой линии лечения висцерального лейшманиоза.
Выраженная анемия является показанием для эритроцитарных гемотрансфузий, реже требуется введение тромбомассы и донорских лейкоцитов. Коррекция анемии заключается в длительном приеме препаратов железа, по показаниям – колониестимулирующих факторов. Симптоматическое лечение предполагает дезинтоксикацию, прием жаропонижающих средств (аспирин – с осторожностью), антибиотиков в случае присоединения вторичных инфекций. Важной составляющей лечения является борьба с отеками, в числе прочего в план терапии включаются мочегонные средства и растворы альбумина.
Прогноз и профилактика
Прогноз при ранней диагностике благоприятный за исключением случаев болезни у ВИЧ-инфицированных пациентов – у данной категории больных даже слабопатогенные штаммы лейшманий вызывают органные поражения. Продолжительность лечения составляет 14-30 дней, наблюдение за реконвалесцентами занимает 4-6 месяцев из-за возможных рецидивов лейшманиоза. У 17% пролеченных пациентов в течение 5 лет после выздоровления могут обнаруживаться симптомы посткала-азарного дермального лейшманиоза, протоколы диагностики и лечения для которого окончательно не разработаны.
Специфическая профилактика заключается в плановом введении живой вакцины, рекомендована лицам, проживающим или планирующим длительное либо кратковременное пребывание на эндемичных территориях, туристам. Введение препарата необходимо осуществлять зимой или осенью минимум за три месяца до поездки. Неспецифические меры предотвращения висцерального лейшманиоза включают своевременное выявление, изоляцию и лечение больных, использование противомоскитных сеток, вакцинацию собак, устранение свалок, меры дезинсекции и дератизации. Борьба с москитами заключается, в том числе, в осушении болот, подвалов и овощехранилищ.
4. A Treatment outcomes of visceral leishmaniasis in Ethiopia from 2001 to 2017: a systematic review and meta-analysis / Eyob Alemayehu Gebreyohannes, Akshaya Srikanth Bhagvathula, Tadesse Melaku Abegaz// Infect Dis Poverty – 2018 - №7.
Лейшманиоз — протозойная инфекция, передаваемая при укусе москитов, вызывающая клинический спектр проявлений, начиная от бессимптомной формы и заканчивая язвенными поражениями кожи, слизистой оболочки и поражением внутренних органов.
По данным ВОЗ, лейшманиоз является эндемическим заболеванием для 97 стран, в том числе для некоторых регионов Африки, Ближнего Востока, Южной Азии, Южной Европы, северной части Южной и Центральной Америки [1]. Эндемичность в РФ не установлена, тем не менее ежегодно поступают сведения о новых случаях заболевания [2].
Кожный лейшманиоз — наиболее распространенная форма лейшманиоза, которая вызывает повреждения кожи на открытых участках тела.
Для российского туриста риск заражения лейшманиозом существует при посещении не только стран дальнего, но и ближнего зарубежья: Азербайджана, Армении, Грузии, Кыргызстана, Таджикистана, Узбекистана в пик активности переносчиков возбудителя с мая по сентябрь [4].
Классификация лейшманиоза
Существует 3 основных типа лейшманиоза: кожный, висцеральный, слизисто-кожный. Клиническая эпидемиология выделяет две отдельные группы — болезни Старого и Нового Света — в зависимости от географии передачи.
Лейшманиоз Старого Света эндемичен в странах Азии, Африки, Ближнего Востока и Средиземноморья, вызывается главным образом Leishmania tropica, Leishmania major и Leishmania infantum. Переносчиком являются кровососущие москиты р. Phlebotomus. Среди кожного лейшманиоза Старого Света выделяют зоонозный (рано изъязвляющийся лейшманиоз) с инкубационным периодом 2–4 нед, причиной которого является L. Major, и антропонозный (поздно изъязвляющийся) с инкубационным периодом 2–8 мес, причиной которого является L. tropica. Источником возбудителей зоонозного лейшманиоза являются мелкие млекопитающие (песчанки), собаки, волки, лисы. Источником антропонозного кожного лейшманиоза служит больной человек.
Лейшманиоз Нового Света распространен в странах Южной Америки и некоторых регионах США. Возбудителями кожного лейшманиоза Нового Света являются Leishmania braziliensis, Leishmania guyanensis, Leishmania panamensis, Leishmania peruviana, Leishmania mexicana и Leishmania amazonensis. Переносчик — муха Lutzomyia.
Клинически и патогенетически лейшманиоз Старого и Нового Света почти не различаются, только при лейшманиозе Нового Света чаще поражаются еще и слизистые оболочки [2, 5].
Кожный лейшманиоз может проявляться локализованной, хронической рецидивирующей, диффузной и острой формами. Локализованная форма кожного лейшманиоза проявляется папулами или узлами, которые возникают на месте укусов, чаще всего это лицо и открытые участки тела. Со временем папулы/узлы превращаются в хорошо очерченные безболезненные язвы с фиолетовым венчиком. Цвет венчика объясняется разрушением эпидермиса и просвечиванием сосудов дермы. Заживают язвы с формированием втянутых рубцов. Возможны лимфаденопатия и наличие сателлитов. Острая форма лейшманиоза Старого Света клинически напоминает фурункул.
Поражения лейшманиоза Старого Света и L. Mexicana имеют тенденцию к самопроизвольному заживлению в течение нескольких месяцев, но для заживления лейшманиоза, вызванного L. Braziliensis, могут потребоваться годы. После заживления остается рубец, обычно округлой формы.
Некоторыми авторами описаны атипичные формы кожного лейшманиоза: эритематозная вулканическая язва, волчанка, экзематозная, рожистое воспаление, сухая, зостерообразная, паронихиальная, споротрихоидная, шанкриформная и кольцевидная [5]. В определенных случаях клиническая картина может имитировать такие заболевания, как подкожный и глубокий микоз, кожные лимфомы, псевдолимфомы, базально-плоскоклеточный рак. Сообщалось о поражениях в области лица, щек, ушей, носа, век, конечностей, туловища, ягодиц, а также в области ладоней и гениталий. Причина клинического плеоморфизма кожного лейшманиозного неясна, но иммуносупрессия, по-видимому, играет важную роль в некоторых случаях (в том числе недоедание и ВИЧ-инфекция) [6]. Не существует установленных руководящих принципов для лечения атипичного кожного лейшманиоза. Тем не менее препараты пятивалентной сурьмы остаются первой линией лечения всех форм лейшманиоза, даже у ВИЧ-инфицированных пациентов и при атипичных формах.
Кроме того, есть данные о туберкулоидной форме, которая описана И.И. Гительзоном в 1932 г. и первоначально названа им металейшманиозом. Туберкулоидная форма развивается через несколько месяцев, а иногда и через несколько лет вокруг рубца от бывших лейшманиом. Этот процесс имеет длительное течение (многие годы), при этом характерен медленный периферический рост. Описаны лепроматоидная и промежуточная формы лейшманиоза. Диффузно-инфильтрирующая лейшманиома практически не встречается. Ассоциация микробной флоры осложняет течение лейшманиоза и задерживает выздоровление.
Возбудитель передается самками москитов, в организме которого паразиты находятся в жгутиковой форме (промастиготы). Промастиготная форма лейшманий представляет собой подвижную форму с передним жгутиком. Форма промастиготы развивается в метациклическую инфекционную форму в течение приблизительно 10 дней. Паразит попадает в организм человека с укусом москита и проникает в макрофаги. Лейшмании способны выжить в кислой среде лизосомы и стать амастиготными формами. Эти формы являются облигатными, внутриклеточными, неподвижными диаметром около 2,5–7 мкм. Именно эта форма амастиготы вызывает заболевание у людей и влияет на клеточный иммунитет. В конце концов другой москит при укусе больного человека инфицируется этой формой и лейшмания трансформируется в форму промастиготы у насекомого [7].
Известно, что выраженный ответ Th1 с выработкой IL-2 и IFN-γ приводит к быстрому разрешению инфекции. При слабом Th1-ответе или реакции Th2 с выработкой IL-4 и IL-10 инфекция продолжает развиваться, что наблюдается при диффузном кожном лейшманиозе. После перенесенного заболевания развивается стойкий иммунитет именно к этому виду лейшмании.
Без лечения лейшманиоз Старого Света редуцирует через 2–4 мес, если вызван L. major, или через 6–15 мес, если вызван L. tropica. Кожный лейшманиоз Нового Света, вызванный L. mexicana, редуцирует через 3 мес более чем в 75% случаев, вызванный L. braziliensis и L. Panamensis, — менее чем в 10% случаев [2].
Диагностика лейшманиоза
Диагноз основывается на одном из следующих методов:
— обнаружение амастиготов лейшмании при цитологическом исследовании из участка поражения с окраской по Романовскому—Гимзе (при зоонозном лейшманиозе в язвах обнаруживают мало лейшманий, что требует более настойчивого поиска в биоптатах и соскобах материала);
— гистологическое исследование биопсии кожи, в том числе с использованием специфических методов иммуногистохимии;
— посев на двухфазные среды, такие как Novy-MacNeal-Nicolle с последующим микроскопическим исследованием для выявления промастиготов возбудителя через 1–4 нед после посева [7];
— молекулярная диагностика методом ПЦР для выявления ДНК кинопласта (kinoplast DNA) лейшмании, позволяет определить род Leishmania.
Тактика лечения пациентов
Тактика лечения зависит от формы и стадии заболевания, общего состояния пациента, вида возбудителя. В настоящее время не существует идеальной или универсально применимой терапии для кожного лейшманиоза. Некоторые схемы лечения кажутся высокоэффективными только в отношении определенных видов/штаммов Leishmania в определенных регионах мира. Следует учитывать как виды паразитов, так и факторы хозяина (например, сопутствующие заболевания и иммунный статус). Из-за выраженных побочных эффектов препаратов системное лечение кожного лейшманиоза показано в следующих случаях:
— локализация поражений имеет важное эстетическое или функциональное значение или размер поражения 4 см и более;
— поражения располагаются в участках, которые затруднительны для местного лечения, например вокруг глаз;
— количество высыпаний (3 активных поражения и более);
— поражения кожи приводят к функциональным расстройствам;
— наружное лечение неэффективно;
— иммуносупрессия у пациента;
— поражения присутствуют более 6 мес [8].
Лекарственными средствами первой линии терапии для кожного лейшманиоза являются препараты пятивалентной сурьмы: стибоглюконат натрия 20 мг/кг/день внутривенно или внутримышечно, антимонат меглюмина 20 мг/кг/день 20 дней и милтефозин 2,5 мг/кг/день перорально (не более 150 мг) в течение 28 дней. Вторая линия терапии включает топический паромомицин 2 раза в день 10–20 дней, пентамидин 2–3 мг внутривенно или внутримышечно ежедневно или через день, 4–7 доз, флуконазол 200 мг/день или 6–8 мг/кг/день внутрь в течение 6 нед или другие азолы: кетоконазол 600 мг/день или 10 мг/кг/день 4 нед (в некоторых странах кетоконазол из-за побочных действий не применяют), итраконазол 7 мг/кг/день 3 нед, липосомальный амфотерицин В 3 мг/кг 1–5 дней, 14 дней и 21 день, дезоксихолат амфотерицина В 10 мг/кг однократно или 1 мг/кг через день 15 внутривенных вливаний, аллопуринол 300 мг/сут 3 мес (L. tropica), или 300 мг 3 раза в день 6 нед (L. mexicana), или 100 мг 4 раза в сутки (L. panamensis), или 1,5–2,5 мг/кг/день 28 дней (L. donovani). В 2014 г. FDA одобрило лечение кожного лейшманиоза противоопухолевым препаратом: милтефозин в дозе 2,5 мг/кг/день (до 150 мг/день) в течение 28 дней per os [9]. Местное лечение включает применение комбинированной мази с содержанием 15% паромомицина и 12% хлорида метилбензэтония (кожный лейшманиоз Нового Света), паромомицин/гентамицин (кожный лейшманиоз Старого Света), имиквимод. Внутриочаговое введение стибоглюконата натрия 0,2–0,4 мл внутрикожно 3 раза в неделю 2 мес эффективно при лечении лейшманиоза Старого Света. Физиотерапия включает применение криотерапии, кюретажа, радиочастотной терапии, CO2-лазера. Однако доступность и официальные рекомендации для применения этих методов терапии различны в каждой стране. Лечение с помощью сурьмы быстрее излечит поражения и предотвратит рецидив, местное распространение, заболевание слизистой оболочки (обычно) и передачу. Считается, что пятивалентная сурьма работает путем ингибирования синтеза аденозинтрифосфата [10, 11].
Опыт лечения кожного лейшманиоза в России описывает применение: доксициклин 100 мг 2 раза в сутки, хлорохин по 200 мг 2 раза в сутки 10-дневными курсами с 5-дневным перерывом. Рифампицин 600 мг/сут в течение 6 мес, иногда до 1 года. Возможен более короткий прием рифампицина по 600 мг/сут — от 3 нед до 3 мес (иногда дольше) в сочетании с дапсоном в дозе 2 мг/сут на 1 кг массы тела в течение 3 нед. Кетоконазол в дозе 400 мг/сут в течение 3 мес или 600 мг/сут на протяжении 28 дней. В последнее время используют итраконазол в дозе 200 мг/сут (4 мг/сут на 1 кг массы тела) в течение 1–3 мес. Описано также применение аллопуринола, метронидазола, гризеофульвина, однако опубликованный клинический опыт лечения этими препаратами ограничен [12].
Наружная терапия — мази с антибиотиками (0,1% гентамициновая, 3% тетрациклиновая), эпителизирующие средства (метилурациловая мазь, мазь, содержащая хлорамфеникол и метилурацил, пируанский бальзам); коагуляция элементов эрбиевым лазером [13, 14].
Варианты лечения детей ограничены и могут потребовать приема плохо переносимых лекарств. Несмотря на различия в ответах на эти препараты, схемы лечения детей основаны на экстраполяции данных об эффективности их применения у взрослых. Дети — особая популяция для лечения лейшманиоза. Наблюдательные исследования и клинические испытания показали более высокую долю неудачного лечения препаратами первого ряда кожного лейшманиоза у детей, особенно в младших возрастных группах (
Клинический случай

Рис. 1. Очаг кожного лейшманиоза на левом предплечье.

Рис. 2. Пациентка Д., 8 лет, очаг кожного лейшманиоза на тыле кисти II, IV пальцев.

Рис. 3. Пациентка Д., 8 лет, очаг кожного лейшманиоза на щеке.
Данные клинико-лабораторного обследования: ОАК в пределах референсных значений. Бактериологическое исследование биоматериала на условно-патогенную микрофлору: рост микрофлоры отсутствует. ИФА на определение АТ к Borrelia burgdorferi: IgG и IgM отрицательные. Исследование методом микроскопии: акантолитические клетки не обнаружены. Для подсчета эозинофилов нет материала. Исследование патогенных грибов методом микроскопии (с кожи лица): грибковые элементы не обнаружены. ИФА к антигенам гельминтов: IgG к описторхис, трихинелла, токсокара, эхинококк, аскариды отрицательный.
Во время биопсии взят материал для цитологического исследовании с окраской по Романовскому—Гимзе для обнаружения амастигот лейшмании: результат отрицательный. Диагностическая биопсия кожи левого предплечья: в дерме гистиоцитарная инфильтрация из эпителиоидных клеток со слабоэозинофильной цитоплазмой с формированием некротизирующихся гранулем, окруженных лимфоцитами, плазматическими клетками и единичными нейтрофилами. В цитоплазме субэпидермально расположенных гистиоцитов определяются немногочисленные мелкие базофильные структуры с округ-лыми очертаниями. Заключение: гистологические изменения более всего соответствуют лейшманиозу кожи. Менее вероятна болезнь Розаи — Дорфмана. Для уточнения диагноза рекомендуется обследование пациента в специализированном учреждении (рис. 4, 5).

Рис. 4. Гистология биоптата из очага.
Окраска гематоксилином и эозином, ×50.

Рис. 5. Гистология биоптата из очага.
Окраска гематоксилином и эозином, ×1000 (иммерсия).
После получения данных диагностической биопсии пациентка направлена в Институт паразитологии и тропической медицины, где на основании проведенных клинико-лабораторных, цитологического исследований, данных биопсии подтвержден диагноз кожного лейшманиоза.
Лечение пациенты получили в Азербайджане (Баку) антимониатом меглумина (глюкантим) с положительным эффектом. Патологические очаги стали менее инфильтрированными, уменьшились в размерах, побледнели. Лейшманиомы у обоих детей располагались на открытых участках тела (в том числе на лице), что при длительном характере течения заболевания и тенденцией к рубцеванию при отсутствии лечения в дальнейшем могло бы привести к стигматизации и психоэмоциональной дезадаптации.
Заключение
Читайте также:

