Экспериментальная группа по вич
Обновлено: 25.04.2024
Клинические испытания новых подходов к генной терапии могут проложить путь к функциональному излечению или долговременной ремиссии ВИЧ. American Gene Technologies тестирует генетически модифицированные ВИЧ-специфические CD4 Т-клетки, устойчивые к проникновению вирусов, а Excision BioTherapeutics разрабатывает метод удаления ДНК ВИЧ из хромосом инфицированных клеток. Обзор исследований опубликован в журнале POZ.
Американские генные технологии: AGT103-T
Экспериментальная терапия, получившая название AGT103-T, включает генетически модифицированные CD4 Т-клетки, способные противостоять ВИЧ. Сначала у пациента берут образец клеток периферической крови и отбирают клетки CD4, распознающие белок Gag ВИЧ. Затем в клетку вставляется ген, отключающий рецепторы CCR5, которые ВИЧ использует для проникновения в клетки. В конечном итоге модифицированные CD4 возвращаются в организм.
Согласно данным, первое клиническое испытание AGT103-T проходит успешно. После оценки промежуточных результатов первых 3 участников независимый совет по безопасности не обнаружил серьезных побочных эффектов. Ожидается, что в этом месяце лечение получат еще 2 пациента.
Настоящая проверка функционального излечения — это прекращение приема антиретровирусных препаратов, чтобы увидеть, восстановится ли вирусная нагрузка. Первые участники начнут тщательно контролируемое прерывание лечения в начале 2022 года, сообщают исследователи.
Эксцизионная биотерапия: EBT-101
Excision BioTherapeutics применяет другой подход, используя генную терапию для деактивации генетических кодов ВИЧ в зараженных клетках, тем самым останавливая производство нового вируса.
EBT-101 вводится в виде однократной внутривенной инфузии. Через три месяца после введения участники исследования начнут контролируемый перерыв в лечении антиретровирусными препаратами, чтобы увидеть, как генная терапия влияет на развитие вируса.
В сентябре Управление по санитарному надзору за качеством пищевых продуктов и медикаментов дало компании добро на начало первой фазы испытаний EBT-101.
— Геннадий, Андреас, расскажите, пожалуйста, какие еще исследователи принимают участие в проекте?
Геннадий Бочаров: Помимо меня и моего коллеги Андреаса Мэйерханса, на котором лежит экспериментальная часть исследования, над проектом работает Виталий Вольперт, профессор математики из института Камиля Жордана при Университете Лион-1, он специализируется на математических решениях и моделировании. Мы также сотрудничаем с Пермским краевым центром по профилактике и борьбе со СПИДом и инфекционными заболеваниями — там проводятся клинические исследования уровня вирусной нагрузки, а также гормональных и иммунных показателей у детей, рожденных от ВИЧ-инфицированных матерей.
Их возглавляет четвертый основной исполнитель проекта — Борис Бахметьев, кандидат медицинских наук, заведующий лабораторией экологической иммунологии Института экологии и генетики микроорганизмов УрО РАН.
— Как вам удалось собрать такой коллектив из ученых, представляющих разные страны?
— Расскажите, пожалуйста, что уже было сделано в рамках конкретно этого исследования?
Геннадий Бочаров: Сейчас мы сфокусировались на трех фундаментальных аспектах и многофункциональном математическом моделировании. Мы хотим понять фундаментальный механизм, который отвечает за развитие хронических инфекций, и изучить мультимодальные (то есть действующие на различные системы организма) средства контроля, которые можно было бы применять для корректировки нежелательных сдвигов в динамике инфекционных заболеваний.
Существует три различающихся по своей природе способа повлиять на динамику взаимодействия ВИЧ с организмом инфицированного человека.
Первый, достаточно широко доступный, — антиретровирусная терапия. Существует примерно 26 препаратов, которые позволяют воздействовать на различные этапы внутриклеточной репликации и созревания вируса. В целом это хороший способ, но есть некоторое количество побочных эффектов, он дорогой, и не все пациенты придерживаются схем лечения, которые им предлагают, поскольку это существенно нарушает качество их жизни.
— А какие могут быть побочные эффекты?
Андреас Мэйерханс: Например, нарушения в работе сердечно-сосудистой системы, центральной нервной системы, системы регуляции метаболизма.
Лекарства, которые сейчас существуют на рынке, употребляют в различных комбинациях, при этом они воздействуют на разные этапы репликации вируса.
Поэтому одна из наших задач — скомбинировать эти лекарственные средства в одно, спроектировать максимально эффективное терапевтическое средство путем поиска на основе анализа чувствительности моделей синергийных эффектов в их совместном действии. Необходимо сделать так, чтобы результат приема лекарств сохранялся, чтобы симптомы не вернулись в течение одной-двух недель. Это возможно путем изменения баланса ВИЧ и иммунной системы таким образом, чтобы противовирусные иммунные реакции могли ослаблять вирусные процессы до непатогенного уровня.
Геннадий Бочаров: В России вирусом иммунодефицита заражено более миллиона человек, и не все получают дорогостоящее лечение. Вторая проблема состоит в том, что антиретровирусная терапия не обеспечивает реальную полноценную защиту.
Иммунная система не восстанавливается, даже если снижается вирусная нагрузка.
Это происходит потому, что нарушается баланс между различными субпопуляциями клеток иммунной системы, например регуляторными Т-клетками и Т-лимфоцитами хелперами CD4+. Уровень активности иммунных процессов определяется балансом активирующих и супрессирующих сигналов. При ВИЧ-инфекции усиливается экспрессия рецепторов, которые отвечают за передачу сигналов на снижение функциональной активности или даже гибель клеток.
— То есть частичное восстановление иммунной системы становится возможным?
Геннадий Бочаров: Да, при данном подходе частичное восстановление, безусловно, происходит. Но полного восстановления нет, и более того, антиретровирусная терапия не обеспечивает восстановление численности CD4+ Т-хелперов. Это наглядно демонстрируют исследования, проводимые нашими коллегами, с которыми мы активно сотрудничаем, — академиком Валерием Черешневым и д.м.н. Константином Шмагелем (г. Пермь) по лечению пациентов, больных ВИЧ и гепатитом C.
— А почему функции иммунной системы не восстанавливаются, если снижена вирусная нагрузка?
Геннадий Бочаров: Тут все дело в глубине поражений и изменений в организме человека при попадании и развитии ВИЧ-инфекции. Вирус иммунодефицита поражает клетки иммунной системы человека, которые находятся в лимфоидных органах, в частности в лимфоидной ткани кишечника, селезенке и лимфоузлах, коих в организме насчитывается более 500.
— И что происходит в этих органах?
Геннадий Бочаров: Лимфоидные органы состоят из стромы, которая формируют каркас, в конкретном случае — из фибробластных ретикулярных клеток (ФРК). Когда Т-лимфоцит CD4+ или CD8+ попадает в лимфатический узел, ему нужно вступить в контакт с клетками стромы. Если лимфоцит получает сигнал от ФРК, то он выживает, а если сигнала нет, то клетка гибнет.
В ходе инфицирования ВИЧ разрушается эпителий стенок кишечника, бактериальные продукты проникают в кровь и вызывают системное хроническое воспаление.
В иммунной системе есть механизмы, которые блокируют хроническую активацию, — это регуляторные Т-клетки, упомянутые ранее. В числе других процессов они стимулируют синтез коллагена фибробластными ретикулярными клетками. Коллагеновые нити частично блокируют свободную миграцию клеток, транспорт цитокинов, и иммунная активность в целом снижается. И фиброз, который имеет место при ВИЧ-инфекции, рассматривается как одна из ключевых причин, по которой полное восстановление иммунитета невозможно. Это ставит задачу анализа с помощью моделей и антифиброзной терапии как компонента мультимодальных воздействий. Для исследования структуры и функции лимфатических узлов при экспериментальных вирусных инфекциях мы также сотрудничаем с Институтом иммунобиологии кантонального госпиталя города Санкт-Галлен (Швейцария), руководимым профессором Б. Людвигом.
Наконец, ключевая проблема лечения ВИЧ-инфекции состоит в том, что вирус полностью интегрируется в человеческую хромосому, становится невидимым, пока клетка не активируется.
А еще он способен видоизменяться со временем путем процессов мутирования и рекомбинации геномов, что делает вирус движущейся мишенью для иммунной системы в пространстве антигенных признаков. Соответственно, и течение болезни протекает у всех по-разному.
— Как вы предлагаете решить эту проблему?
Геннадий Бочаров: Это подводит к необходимости теоретически исследовать третий способ повлиять на динамику взаимодействия ВИЧ с организмом. С помощью создания многофункциональной математической модели мы можем изучить, насколько иммунная система чувствительна к внешним воздействиям, а в будущем — спроектировать эффективный комбинированный препарат с минимальной концентрацией лекарственных компонентов, которые действуют на различные звенья инфекции и иммунофизиологических процессов и обладают синергийным эффектом.
Андреас Мэйерханс: Это очень важно, потому что уменьшение уровня вирусной нагрузки антиретровирусными лекарствами связано с зависимостью состояния организма от препарата, и прекращение приема вызовет рецидив заболевания. К тому же лекарства могут иметь побочные эффекты, как отмечалось выше.
— А как проходила экспериментальная часть исследования?
Андреас Мэйерханс: Мы рассматривали инфекцию вируса милимфоцитарного хориоменингита (ВЛХМ) мышей, имеющую много общих закономерностей в динамике с ВИЧ-инфекцией.
— Поэтому для клинической части исследования был выбран именно ВЛХМ, а не, например, вирус иммунодефицита обезьян?
Андреас Мэйерханс: Лабораторные исследования мы начали проводить около трех лет назад.
У нас собраны данные транскриптомного анализа по динамике активности около 11 тыс. генов при остром и хроническом вариантах течения инфекции.
Программисты-биоинформатики проанализировали имеющиеся данные, и по итогам работы построены математические модели динамики экспрессии генов. В Барселоне, кстати, мы контактируем с двумя госпиталями, а одна из моих бывших аспиранток принимает непосредственное участие в мониторинге испытаний вакцин. Это дает нам дополнительную информацию, которую мы используем при создании математических моделей.
— То есть в проекте участвуют молодые ученые?
Геннадий Бочаров: Да, в исследовании задействованы шесть молодых специалистов из России — один из ИВМ РАН (к.ф.-м.н. А.А. Данилов), трое аспирантов из МГУ имени М.В. Ломоносова (В.В. Желткова, А.А. Кислицын, Р.С. Савинков), два магистра из МФТИ (Д.С. Гребенников) и МГУ имени М.В. Ломоносова (Р.М. Третьякова), а также аспирант из Лиона (Анасс Бучнита). Мы надеемся, что в течение трех следующих лет они станут по-настоящему опытными исследователями в области математической иммунологии и внесут свой вклад в развитие научной школы, созданной академиком Г.И. Марчуком.
Следует также дополнить, что мы активно сотрудничаем с коллегами из научных институтов Новосибирска (д.б.н. С.И. Бажан, д.б.н. В.А. Лихошвай, д.б.н. Т.М. Хлебодарова, к.ф.-м.н. И.А. Гайнова) в области моделирования внутриклеточного онтогенеза ВИЧ, Екатеринбурга (д.ф.-м.н. А.В. Ким) — в задачах оптимального управления динамикой ВИЧ-инфекции и Москвы (д.б.н. Э.В. Карамов) — по анализу генетических особенностей ВИЧ-инфекции в РФ.
— Расскажите, пожалуйста, о ваших дальнейших научных планах.
Геннадий Бочаров: К концу года мы планируем разработать многомасштабную модель ВИЧ-инфекции и исследовать на ее основе факторы, лежащие в основе фенотипически различных вариантов течения ВИЧ-инфекции и несостоятельности иммунного ответа.
Планируем сдать в печать книгу о математическом моделировании в иммунологии.
Вообще математическое моделирование сложных систем является востребованным методом не только в иммунологии или в биологии, поэтому обучение студентов их содержательному моделированию — актуальная задача.
CRISPR! CAS!
В этом году группе исследователей из США удалось уничтожить генетический материал аналогичного ВИЧ вируса (это вирус иммунодефицита обезьян (ВИО)) во всех клетках и тканях двух подопытных животных.
Почему это важно? Если ранее главным потенциальным способом излечения ВИЧ считалась пересадка генетически устойчивого к вирусу донорского материала (в первую очередь костного мозга), то теперь ему появляется важная альтернатива.
Интересно, что вторая сенсация года связана, собственно, и с той, и с другой технологией. Дело в том, что устойчивый к ВИЧ ген распределен по человеческой популяции весьма неравномерно. Большинство его носителей происходят из стран Северной Европы, а стало быть, их материал вряд ли удастся пересадить ввиду определенных особенностей трансплантации костного мозга представителям азиатских народов, в том числе китайцам, равно как и представителям этнических групп, почти не вступающих в смешанные браки.
Компенсировать несправедливость природы взялся китайский профессор Хэ Цзянькуй из Южного университета науки и технологий в Шэньчжэ.

Профессор Хэ Цзянькуй из Южного университета науки и технологий в Шэньчжэ
Почти год назад, в январе, китайские власти подтвердили, что в этой стране действительно имел место успешный эксперимент, в ходе которого ученый имплантировал в матку зародыш, подвергнутый геномному редактированию методом CRISPR/CAS9.
Ученый смог удалить участок ДНК, содержащий ген CCR5, который кодирует белок, позволяющий ВИЧ проникать в иммунную клетку и инфицировать ее.
Ученый еще до начала исследования сфабриковал заключение комиссии по этике, а также данные о ВИЧ-статусе некоторых участников, так как экстракорпоральное оплодотворение для ВИЧ-позитивных людей в Китае запрещено. Мировое научное сообщество резко осудило изыскания китайского профессора как аморальные и опасные.
Чуть позже оказалось, что в курсе эксперимента, еще до того как информация просочилась в СМИ, были лауреат Нобелевской премии биолог Крейг Мелло и профессор физики и биоинженерии из университета Райса в Хьюстоне Майкл Дим. Оба они также понесли репутационные потери. Но больше всего досталось самому изобретателю.
Уже зимой появилась информация о том, что китайскому генетику может грозить смертная казнь, так как власти страны обвинили его в коррупции и взяточничестве. А в декабре уходящего года суд все-таки приговорил ученого за преднамеренное нарушение государственных нормативов в области научных исследований к трем годам тюремного заключения.
Интересно, что эксперимент, очень похожий на опыт с обезьянами, но уже на человеческом материале в октябре этого года завершился в Китае частичным провалом. От ВИЧ-инфекции пересадка модифицированного (а не природно-устойчивого) донорского материала 27-летнего пациента не спасла, зато доказала, что сама процедура безвредна, а стало быть, технология CRISPR/CAS9 на данный момент остается самым вероятным претендентом на то, чтобы стать доказанным методом излечения от ВИЧ-инфекции взрослых пациентов. Отдельным пунктом стоит подчеркнуть: вполне вероятно, впервые эта технология окажется применена и запущена в массовое использование не на Западе, а, собственно, в странах Юго-Восточной Азии.

Новые препараты, пациенты и антитела
Западные ученые тем временем отчитываются в успехах технологии пересадки родного, не модифицированного, материала с целью элиминации вируса.
В Сиэтле весной 2019 года на крупнейшей Конференции по ретровирусам и оппортунистическим инфекциям (CROI 2019) безусловной сенсацией стало известие о фактическом излечении, а вернее элиминации, вируса иммунодефицита в организме сразу двух пациентов — из Германии (дюссельдорфский пациент) и Англии (лондонский пациент).
Обоим мужчинам в ходе терапии рака был пересажен костный мозг от донора, имеющего врожденную резистентность (устойчивость) к ВИЧ.
Всего на данный момент это третий случай подобного исцеления. Первый имел место также в Германии (берлинский пациент) — осенью прошлого года мы публиковали интервью с врачом, который работал с ним. Однако до последнего времени считалось, что повторить берлинской эксперимент невозможно. В этом году стало окончательно ясно, что несмотря на все издержки (весьма токсичная химиотерапия перед пересадкой) эта технология может быть распространена и на других пациентов, живущих с вирусом.
Главной альтернативой пересадке костного мозга и генной модификации по-прежнему остаются так называемые широко нейтрализующие антитела, способны распознавать штаммы ВИЧ и блокировать их проникновение в здоровые клетки.
Как считается, введение их пациенту может стать более безопасным методом терапии, способным заменить актуальную антиретровирусную терапию препаратами, препятствующими репликации вируса в организме за счет ингибирования работы того или иного фермента вируса в клетке.

Как стало известно в этом году, дальнейшими их разработками займется такой фармгигант, как ViiV Healthcare GSK. Антитела, исследуемые ее подразделениями, носят название N6LS и действуют целенаправленно против вирусов, которые прикрепляются к белку gp120 на поверхности CD4+ T-лимфоцита. На фазе исследований IIа, к которым приступает компания, будут оценены эффективность и безопасность использования антител у людей.
Кроме того, в октябре этого года исследователи из Глэдстоуна в сотрудничестве с компанией Xyphos Biosciences предложили новую технологию для борьбы с резервуарами ВИЧ-инфекции.
Наличие этих резервуаров остается главной причиной, по которой традиционная АРВТ пока не в силах полностью уничтожить вирус в организме. Ученые из Глэдстоуна считают, что можно сократить количество инфицированных клеток при помощи новой технологии, разработанной на основе CAR-T и получившей название convertible CAR. Она создает иммунные клетки — цитоксичные Т-лимфоциты, на поверхность которых выводятся антитела, позволяющие Т-лимфоциту прикрепиться к необходимой клетке, а затем атаковать и уничтожить ее.
Преимущество convertible CAR в том, что с ее помощью к лимфоцитам можно прикрепить любое количество антител, тогда как CAR-T предполагает борьбу только с одним типом заболевания. Это делает новую технологию пригодной для лечения ВИЧ, у которого огромное количество генотипов.
На этом следует сделать паузу в перечислении сложных терминов. Год ознаменовался и другими свершениями, хоть, на первый взгляд, и меньшими по масштабу.
Так, первого апреля 2019 года хирурги из госпиталя Джонса Хопкинса пересадили ВИЧ-положительному пациенту почку, полученную от ВИЧ-положительного донора. Это была первая в истории трансплантация органа от живого донора с ВИЧ — раньше органы пересаживали только от умерших людей, живших с вирусом иммунодефицита.
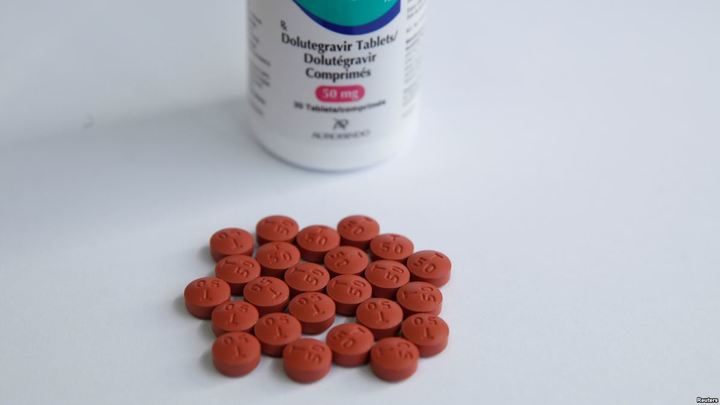
На международной конференции IAS 2019 в Мехико было представлено исследование, согласно которому риск возникновения дефекта нервной трубки у плода от приема долутегравира крайне низок — он составляет лишь 0,3 %. Именно опасность такого побочного эффекта терапии делала этот препарат недоступным для значительного числа ВИЧ-положительных пациентов а Африке — за счет процентного перевеса там среди людей, живущих с вирусом, женщин детородного возраста.
Кроме того, ученым удалось доказать эффективность двойного режима терапии на основе долутегравира и ламивудина. Этот режим может прийти на смену традиционной АРВТ из трех компонентов.
Там же были представлены исследования экспериментальной вакцины от ВИЧ. В ближайшее время стартует третья — последняя — фаза ее испытаний. В первую очередь она будет апробирована среди мужчин-геев и транссексуалов.
Что касается PrEP, компания Merck представила имплантаты со своим новым препаратом — ислатравиром — в этом качестве. Имплантат будет способен предоставлять защиту от ВИЧ на срок более года. Не требуя ежедневного приема таблеток.
Новые клинические рекомендации
В 2019 году Европейское клиническое общества по борьбе со СПИДом (EACS) опубликовало новые рекомендации, традиционно являющиеся основой для национальных рекомендаций по лечению ВИЧ-инфекции во многих странах.
Тут впервые появились отдельные разделы для трансгендерных и пожилых людей, а в список рекомендованных схем впервые была включена двухкомпонентная терапия долутегравир + ламивудин, о которой мы писали в предыдущем разделе.
Преимущество в обновленных рекомендациях получили небустированные ингибиторы интегразы с высоким генетическим барьером (долутегравир или биктегравир). А нуклеозидная основа тенофовир + ламивудин была признана эквивалентной схеме тенофовир + эмтрицитабин.
Для нашей страны важно, что в самый канун нового года Россия выпустила собственные обновленные рекомендации. Отражающие некоторые принципы, упомянутые в европейском документе.
Проект рекомендаций уже опубликован на сайте Национальной ассоциации специалистов по профилактике, диагностике и лечению ВИЧ-инфекции. В документе впервые регламентирован тот факт, что антиретровирусная терапия должна назначаться всем ВИЧ-позитивным пациентам вне зависимости от количества CD4-клеток и уровня вирусной нагрузки. А это огромный шаг для российской медицины, пусть все западные страны сделали его еще много лет назад. Именно за него бились многие российские инфекционисты все последние годы.
Отдельно раннее начало лечения оказалось прописано для беременных женщин: АРВТ должна назначаться в минимально короткий срок после постановки диагноза. И это тоже очень важно. Вторым новшеством стало утверждение долутегравира в качестве предпочтительного препарата первой линии.
Теперь он должен будет заменить использовавшийся ранее эфавиренз (600 мг). То есть предпочтительная схема первой линии для взрослых в России теперь будет выглядеть как: долутегравир + ламивудин (или эмтрицитабин) + тенофовир.
Перебои и госзакупки
Несмотря на такой новогодний подарок и включение в рекомендации современных препаратов, главной российской новостью 2019 года все-таки стали бесконечные и катастрофические перебои с поставкой лекарств от ВИЧ в российские регионы. В частности ламивудина — самого распространенного препарата класса НИОТ.
В конце августа стало известно о проблемах с этим препаратом в Краснодарском крае, до этого — в Туле, где лекарства не было около двух месяцев, список же всех субъектов федерации, столкнувшихся с этой нехваткой, покрывает почти всю географию страны.
Причиной перебоев стала череда сорванных Министерством здравоохранения аукционов. Началась история с провала зимних, состоявшихся с конца февраля по март, и последовавших за ними весенних торгов. Более того, частично сорваны оказались даже летние.
Дело в том, что каждый раз цена, заявленная министерством, оказывалась заниженной, вынуждая фармкомпании не выдвигаться по тем или иным позициям. По словам представителей самого Минздрава, виной этому стала неадекватность референтных цен, указанных в каталоге лекарственных препаратов, обязательном к использованию по новым правилам, вступившим в силу с января 2019 года. По результатам года министерство обещало пересмотреть правила закупок и скорректировать инструкции по определению минимальной цены на аукционе, правила приобретения у единственного поставщика и некоторые другие пункты своих регламентов. Проект приказа можно прочитать по этой ссылке.
Инъекционная терапия, FDA и страсти по тенофовиру
Инъекционная схема АРВ-терапии — отдельный сюжет этого года. Как ранее уже писал СПИД.ЦЕНТР, она подразумевает введение двух препаратов — каботегравира (ингибитор интегразы) и рилпивирина (ненуклеозидный ингибитор обратной транскриптазы (ННИОТ)) — пациентам раз в месяц или даже реже, что может стать современной альтернативной ежедневному приему препаратов в виде таблеток, особенно для тех, кто демонстрирует низкую приверженность.
Ранее опубликованные на конференции CROI результаты испытаний подтвердили эффективность схемы в подавлении вируса при весьма невысокой вероятности побочных эффектов.
Ее разработчики, Janssen и ViiV, подали долгожданное (это действительно так!) новшество на одобрение в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в апреле этого года. Именно с этого, как правило, стартует распространение по миру большинства передовых западных препаратов, однако американское надзорное ведомство не одобрило инъекционную схему, сославшись на необходимость уточнения ряда производственных вопросов и отложив свое решение на 2020 год.
Стоит напомнить, что испытания этих двух лекарств в России параллельно с мировым исследованием стартовали еще осенью 2018 года. Тогда СПИД.ЦЕНТР связался с участником этого этапа испытаний, чтобы расспросить о плюсах и минусах такого лечения.
Из новостей фармбизнеса стоит также отметить появление препарата Quadramine (лопинавир, ритонавир, абакавир и ламивудин) как схемы, специально разработанной для новорожденных пациентов с ВИЧ. И презентацию новых препаратов для лиц с полирезистентным ВИЧ — ибализумаба (торговое наименование Trogarzo) и фостемсавира (Fostemsavir).
Это особенно важно, так как за последние годы в России число ВИЧ-положительных пациентов с резистентностью выросло вдвое. На данный момент резистентность имеется уже у 7 % пациентов, хотя 3-4 года назад этот показатель составлял всего 3-4 %.
В октябре FDA одобрило Дескови в качестве второго после Трувады средства для PrEP. Этот препарат компании Gilead содержит новую версию тенофовира (TAF), менее токсичную, как утверждают ее разработчики. Впрочем, большое число исследований, опубликованных в этом году (к примеру это, это и это), ставят под сомнение преимущества TAF перед старой версией тенофовира (TDF), чей эксклюзивный патент компания Gilead недавно потеряла.
Как потенциально более дешевый препарат старый тенофовир будет доступен большему числу пациентов, убеждены эксперты. А учитывая патентный скандал вокруг выпуска Трувады, может быть, и более предпочтителен в качестве PrEP, поскольку компания не славится взвешенностью своей ценовой политики и ответственностью при выборе методов максимизации коммерческой прибыли.
Для России ключевыми событиями стали также следующие.
Конференция PROHIV, состоявшаяся в третий раз при поддержке фонда СПИД.ЦЕНТР и совпавшая с мировым подведением итогов программы UNAIDS 90-90-90. И пусть пока наша страна не в силах похвастаться масштабными успехами по достижению заветных параметров, с которыми мировое сообщество ассоциирует контроль над эпидемией, на конференции все же прозвучал ряд важных докладов, касающихся ситуации с эпидемией в нашей стране.
Кроме того, привлекали внимание продолжающиеся попытки ФАС запустить в стране механизм принудительного лицензирования препаратов, чреватый уходом с рынка крупных западных производителей.
Дальнейшее развитие политики импортозамещения и подготовка связанных с нею каталогов взаимозаменяемости препаратов могут в будущем стать актуальны и для сферы терапии ВИЧ-инфекции. На примере замены препаратов от муковисцидоза российскими дженериками эта политика уже успела зарекомендовать себя не с лучшей стороны.
Вслед за передачей Минздравом права на закупки АРВТ для тюрем Федеральной системе исполнения наказаний (ФСИН) последовали перебои в организации таких поставок и весьма негативные экспертные доклады относительно тюремной медицины в России. Это обернулось попытками передать всю медицинскую службу ФСИН (в том числе и обеспечение АРВТ) обратно Минздраву.
Что принесет новый 2020 год по каждому из этих сюжетов — пока сказать сложно. Но сайт СПИД.ЦЕНТР продолжит наблюдать, а стало быть, и оповещать своих читателей. До встречи в Новом году
Наши главные цели и задачи:
- снижение числа новых случаев инфицирования ВИЧ и удержание роста эпидемии среди населения;
- улучшение качества жизни людей, живущих с ВИЧ (ЛЖВ);
- повышение правовой грамотности населения в сфере ВИЧ и развитие навыков отстаивания собственных прав при неправомерных ограничениях доступа к лечению и медицинским услугам;
- противодействие распространению идей ВИЧ-диссидентства;
- снижение внутренней и внешней стигматизации и дискриминации со стороны общества в отношении представителей уязвимых групп населения, в том числе к ЛЖВ;
- развитие гражданского общества.
Наши приоритетные направления деятельности:
- разработка и реализация профилактических программ социально значимых заболеваний, таких как: ВИЧ-инфекция, гепатиты В/С, сифилис и другие ИППП;
- расширение доступа к прохождению экспресс-тестирования на ВИЧ;
- комплексное медико-социальное сопровождение, социальная реабилитация и адаптация людей, живущих с ВИЧ и затронутых ВИЧ-инфекцией;
- юридическое консультирование и социально-правовое сопровождение по фактам ограничений прав и свобод в связи с наличием ВИЧ-инфекции, противоречащих законодательству Российской Федерации;
- психологическая помощь и поддержка.
Наши основные целевые группы:
- люди, живущие с ВИЧ и затронутые ВИЧ-инфекцией;
- мужчины, практикующие секс с мужчинами (МСМ).
Услуги МОО "Позитивный Диалог":
Структура МОО "Позитивный диалог"
Общее собрание членов Организации.
- Ступишин Михаил Юрьевич
- Лоза Александр Михаилович
- Панченко Николай Дмитриевич
Президент Организации - Ступишин Михаил Юрьевич
HIV TV
Что если у тебя СПИД?
Насколько важен прием АРВТ?
Читайте также:

