Энцефалит изменение глазного дна
Обновлено: 13.05.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Определение
Энцефалит – это группа заболеваний, для которых характерно воспаление вещества головного мозга. В настоящее время энцефалитом называют не только инфекционное, но и инфекционно-аллергическое, аллергическое и токсическое поражения мозга.
Причины возникновения энцефалитов
Первичные энцефалиты, к которым относятся клещевой энцефалит, герпетический энцефалит, энцефалит, вызванный вирусом Коксаки (А9, В3, В6), ЕСНО (2, 11, 24) и некоторые другие, возникают в результате проникновения вируса через гематоэнцефалический барьер, по причине чего повреждаются нейроны головного мозга и развивается воспалительный процесс.
Вторичные энцефалиты рассматриваются как осложнение перенесенных инфекционных заболеваний: гриппа, краснухи, кори, ветряной оспы, лептоспироза и др., а также поствакцинальные энцефалиты.
Гриппозный энцефалит вызывают вирусы гриппа А1, А2, А3, В. Патогенетическими механизмами при гриппозной инфекции становятся токсическое поражение головного мозга и недостаточность мозгового кровообращения.
Возбудителем энцефалита при краснухе становится РНК-содержащий вирус семейства Togaviridae.
Коревой энцефалит вызывается вирусом кори – это форма поражения головного (иногда и спинного) мозга (энцефаломиелит). Энцефалит считается самым распространенным неврологическим осложнением кори (более 95% всех случаев неврологических осложнений). Он наблюдается с частотой 1:1000 случаев кори, чаще у детей старше 2 лет - как у мальчиков, так и у девочек.
Поствакцинальные энцефалиты могут развиваться после вакцинации, особенно после введения некоторых антирабических прививок. В основе поствакцинальных энцефалитов лежит перекрестная аутоиммунная реакция на антигены вакцины и антигены мозга, морфологически выражающаяся в воспалительном поражении мозговых сосудов и окружающего вещества мозга.
Лептоспирозные энцефалиты вызывается Leptospira interrogans. Источником заражения являются домашние инфицированные животные. Наиболее распространен лептоспироз в южных регионах. В развитии заболевания большое значение имеют аутоиммунные реакции.
В группу подострых склерозирующих лейкоэнцефалитов входят формы хронических и подострых энцефалитов с прогрессирующим тяжелым течением (энцефалит с включениями Даусона, подострый склерозирующий лейкоэнцефалит Ван-Богарта, узелковый панэнцефалит Петте Деринга).
В развитии болезни большую роль играют персистирующие вирусные инфекции: коревая, энтеровирусная, вирус клещевого энцефалита. У больных подострым склерозирующим панэнцефалитом обнаруживают в крови и ликворе очень высокие титры коревых антител (не отмечаемые даже у больных с острой коревой инфекцией). Кроме того, значимое место занимают аутоиммунные механизмы, а также приобретенный или врожденный дефект иммунной системы.
Классификация заболевания
Классификация энцефалитов отражает факторы, приводящие к развитию заболевания, и связанные с ними клинические проявления и особенности течения.
По срокам возникновения различают:
- первичные энцефалиты - самостоятельные заболевания, вызываемые преимущественно нейротропными вирусами:
- вирусные: полисезонные (герпетический, энтеровирусный, гриппозный, цитомегаловирусный, вирус бешенства и др.); арбовирусные, или трансмиссивные (клещевой, комариный (японский), австралийский долины Муррея, американский Сент-Луис); вызванные неизвестным вирусом (эпидемический);
- микробные и риккетсиозные (при сифилисе, болезни Лайма, сыпном тифе и др.);
- коревые, краснушные, ветряночные;
- поствакцинальные;
- бактериальные и паразитарные (стафилококковый, стрептококковый, туберкулезный, токсоплазменный, хламидийный, малярийный и др.)
Заболевание может протекать в острой, подострой, хронической и рецидивирующей форме и поражать различные отделы головного мозга.
Различают среднее, тяжелое и крайне тяжелое течение энцефалита.
Симптомы энцефалита
Первичные полисезонные энцефалиты
Инкубационный период может варьировать от 2-3 дней до нескольких недель. Наблюдаются продромальные явления в виде сниженного аппетита, вялости, субфебрилитета. Начало заболевания происходит на фоне резкого подъема температуры. Выраженность клинических проявлений и их течение могут быть разными - от легких стертых форм до тяжелых молниеносных, при которых летальный исход наступает на 1-2-е сутки заболевания. Продолжительность острого периода составляет от 3-5 дней до нескольких недель. Тяжелое течение с выраженным и быстро прогрессирующим отеком головного мозга отмечается в основном при энцефалитах герпетической этиологии.На первый план выходит общемозговая симптоматика: рвота, судорожные пароксизмы, вялость, расстройства сознания, возможны дыхательные и сердечно-сосудистые нарушения. Преобладание общемозговых проявлений, нарушения сознания и выраженные менингеальные симптомы (т. е. вовлечение в воспалительный процесс церебральных оболочек) более характерны для детей младшего возраста.
Очаговая симптоматика зависит от локализации патологических изменений в головном мозге - выделяют стволовую, мозжечковую, полушарную формы.
Мозжечковый синдром характеризуется острым расстройством координации, тремором, мышечной гипотонией. Имеет наиболее благоприятное течение с полным регрессом указанной симптоматики и без последующей задержки психомоторного развития даже у маленьких детей.
Стволовой синдром проявляется поражением проходящих в стволе черепных нервов и пирамидных путей. Возникает специфическое нарушение походки и координации движений, вызванное патологической работой вестибулярного аппарата, присутствуют глазодвигательные нарушения (косоглазие, парез взора, двоение в глазах), резкая мышечная гипотония, сменяющаяся затем спастическим парезом рук и ног. Реже развиваются расстройство глотания, сосания, фонации. Возможны нейроэндокринные нарушения, а в тяжелых случаях - сердечные и дыхательные расстройства центрального генеза, которые могут стать причиной летального исхода.
Полушарный синдром чаще сопровождается расстройствами сознания, нарушениями ориентации в пространстве и во времени, вялостью. Возможны эпизоды психомоторного возбуждения, галлюцинаторный синдром. В первые дни возникают эпиприступы, которым, как правило, предшествуют парезы, развивающиеся остро и инсультоподобно.
Типичные симптомы начала герпетического энцефалита - лихорадка, головная боль, нарушение психических функций, эпилептические припадки, мышечная слабость, снижение памяти. Далее присоединяется нарушение поведения, речи и расстройство координации движений.
Вторичные энцефалиты при общих инфекциях
Клиническая картина гриппозного энцефалита развивается чаще в конце заболевания и даже через 1-2 недели после выздоровления: самочувствие больного снова ухудшается, повышается температура тела, возникают общемозговые симптомы (головная боль, рвота, головокружение). Возможно поражение периферической нервной системы в виде невралгии тройничного и большого затылочного нервов, пояснично-крестцового и шейного радикулита, поражения симпатических узлов. В крови определяют лейкоцитоз или лейкопению. Течение благоприятное. Заболевание продолжается от нескольких дней до месяца и заканчивается полным выздоровлением.
Коревой энцефалит развивается остро, чаще на 3-5-й день после появления сыпи. К этому моменту температура тела может уже нормализоваться, но нередко снова поднимается до высоких значений. Выявляют менингеальные симптомы, проявляющиеся головной болью, головокружением, тошнотой, рвотой, нарушением сознания (возбуждением, бредом, галлюцинациями); наблюдают поражение черепно-мозговых нервов; нарушение двигательной функции конечностей и функции тазовых органов. При тяжелом течении летальность достигает 25%, причем тяжесть энцефалита не зависит от течения кори.
![Коревой энцефалит.jpg]()
Энцефалит при ветряной оспе - тяжелое инфекционно-аллергическое заболевание. Его клиническая картина развивается на 3-7-й день после появления высыпаний (редко в более поздние сроки или до периода высыпаний) и проявляется гипертермией, коматозным состоянием, судорогами, менингеальными симптомами (головной болью, головокружением, тошнотой, рвотой, нарушением сознания), нарушением двигательных функций. Рано появляются признаки отека мозга. Течение обычно благоприятное и лишь в единичных случаях - очень тяжелое с риском летального исхода. После выздоровления могут длительно сохраняться парезы, гиперкинезы, судорожные припадки.
Энцефалит при краснухе может развиться через 1-10 (чаще 2-5 дней) после появления сыпи. Известны случаи манифестации острого энцефалита за несколько дней до появления сыпи, а также без высыпаний, что осложняет постановку диагноза. Чаще всего энцефалит развивается у детей в возрасте 3-15 лет, у взрослых случаи энцефалита описываются в качестве казуистики. Редко неврологическая симптоматика сопровождается вторичными высыпаниями.
Лептоспирозные энцефалиты характеризуются острым началом и протекают как респираторно вирусная инфекция. Наблюдается волнообразная лихорадка с болями в мышцах. В последующем в клинической картине могут преобладать симптомы поражения печени и почек, а со 2–3-й недели - поражения нервной системы в виде энцефалита или энцефаломиелита с вовлечением черепных нервов. Течение заболевания, как правило, благоприятное, иногда возможно спонтанное выздоровление.
Подострым склерозирующим лейкоэнцефалитам подвержены в основном дети и подростки до 15 лет, однако иногда болезнь регистрируется и у взрослых. Начало заболевания подострое: появляются симптомы, расцениваемые как неврастенические - рассеянность, раздражительность, утомляемость, плаксивость.
Различают 4 стадии склерозирующего лейкоэнцефалита:
- 1-я стадия продолжается до 6 месяцев: возможны изменения личности, перепады настроения или депрессия, могут присутствовать лихорадка и головная боль;
- 2-я стадия может включать судороги, мышечные спазмы, потерю зрения и слабоумие;
- 3-я стадия характеризуется быстрым прогрессированием деменции, усилением тонуса мышц при ослаблении судорожного синдрома. На этой стадии осложнения могут привести к летальному исходу;
- 4-я стадия характеризуется нарушениями дыхания, частоты сердечных сокращений и кровяного давления, что приводит к коме и смерти.
В 80% случаев заболевание длится 1–3 года, 10% больных живут дольше (до 10 лет), у 10% описано молниеносное течение, когда смерть наступает менее чем через 3 месяца. Специфического лечения нет.
Диагностика энцефалитов
Цель диагностики первичных полисезонных энцефалитов - установление вида возбудителя. Для этого проводится серия серологических исследований. Диагностическое значение имеет многократное нарастание титра антител к определенному вирусу при сравнении результатов исследования сыворотки пациента, взятой в начале заболевания и спустя 2 недели.
Энцефалит, вызванный вирусом простого герпеса, выявляют с помощью определения повышения уровня специфических антител IgM и Ig G в крови.
Синонимы: Анализ крови на антитела к герпесу 1, 2; IgM антитела к вирусу простого герпеса первого и второго типа; Антитела класса M к ВПГ-1, ВПГ-2. Нerpes simplex virus type 1 (HSV-1), Нerpes simplex virus type 2 (HSV-2), IgM; Anti-HSV-1, 2 IgM antibodies; IgM to HSV-1 and HSV-24 HSV-1, 2-speci.
Энцефалит (др.-греч. ἐνκεφαλίτις, воспаление мозга) - группа заболеваний, характеризующихся воспалением. В настоящее время энцефалитом называют не только инфекционное, но и инфекционно-аллергическое, аллергическое и токсическое поражение головного мозга.
Что провоцирует / Причины Энцефалита:
Для энцефалитов, вызванных нейротропными вирусами, свойственны эпидемичность, контагиозность, сезонность и климатогеографические особенности распространения. По излюбленной локализации патологического процесса выделяют энцефалиты с преимущественным поражением белого вещества – лейкоэнцефалиты (группа подострых прогрессирующих лейкоэнцефалитов), энцефалиты с преобладанием поражения серого вещества - полиоэнцефалиты (эпидемический летаргический энцефалит); энцефалиты с диффузным поражением нервных клеток и проводящих путей головного мозга - панэнцефалиты (клещевой энцефалит, комариный, австралийский, американский). В зависимости от преимущественной локализации энцефалиты делят на стволовые, мозжечковые, мезэнцефальные, диэнцефальные. Часто наряду с веществом головного мозга поражаются и некоторые отделы спинного мозга - в таких случаях говорят об энцефаломиелите. Энцефалиты могут быть диффузными и очаговыми, по характеру экссудата гнойными и негнойными.
Патогенез (что происходит?) во время Энцефалита:
Пути проникновения вируса в организм различны. Чаще наблюдается гематогенный путь распространения. При комарином и клещевом энцефалитах вирус, попадая при укусе в кровеносные сосуды, поступает с током крови в различные органы, в том числе и мозг. В головном мозге наиболее ранимыми оказываются структуры на дне III желудочка, подкорковые узлы, кора большого мозга, клеточные образования мозгового ствола и спинного мозга. Возможны также контактный, алиментарный, воздушно-капельный пути передачи инфекции от человека к человеку или от животного.
Тропизм вирусов к нервной ткани обеспечивается специфическими рецепторами структуры вируса. Взаимодействие вирус - клетка хозяина является сложным процессом, включающим многие патофизиологические механизмы. Клиническая картина заболевания, его тяжесть и особенности течения зависят от способности организма отвечать на воздействие инфекционного агента, а также от биологической природы вируса. Иммунный ответ зависит от многих факторов, в том числе от антигенных свойств вируса, генетически детерминированной силы иммунного ответа макроорганизма, его реактивности в данный момент. В последние годы открыт новый класс имунных клеток, не относящихся ни к Т-, ни к В-лимфоцитам. Эти клетки называются естественными киллерами, они играют существенную роль в противовирусном иммунитете, обеспечивая цитотоксическую функцию. Большое значение имеет интерферон природного происхождения, продуцируемый иммунными клетками. Интерферон является иммунорегулятором, а также одним из эффективных факторов неспецифической противовирусной защиты, блокирующих репликацию вируса. Патогенез энцефалитов определяется, кроме непосредственного разрушения нейронов вирусом, токсическим действием, а также неспецифическими изменениями: поражением сосудистой стенки с повышением ее проницаемости, развитием отека, ликвородинамических и сосудистых нарушений.Патоморфология
Гистологические изменения при энцефалитах не имеют специфического характера и могут встречаться при различных заболеваниях нервной системы. Они развиваются как универсальная реакция мозга на повреждающий агент вне зависимости от его природы. Тем не менее ответ мозга, вызываемый патологическим агентом, может варьировать с преобладанием той или иной реакции, что зависит от особенностей повреждающего фактора и состояния иммунологической реактивности организма. Тканевые реакции при энцефалитах в острый период заболевания заключаются в явлениях резкого отека, геморрагии, пролиферации микроглии, иногда в виде узелков, дегенерации нейронов (тигролиз, атрофия, нейронофагия) и нервных волокон (демиелинизация, дегенерация, распад осевых цилиндров). Отмечается диффузная инфильтрация нервной ткани, особенно периваскулярных пространств, мононуклеарами, плазматическими клетками, полинуклеарами. Определяются изменения сосудистой стенки в виде пролиферативного эндартериита. В хронической стадии преобладают изменения дегенеративного характера, продуктивная глиальная реакция с образованием узелков или рубцов.Симптомы Энцефалита:
Симптомы энцефалита различны в зависимости от возбудителя, локализации патологического процесса, течения заболевания. Однако имеются общие характерные для энцефалита клинические симптомы.
Продромальный период свойственен всем инфекционным заболеваниям. Он продолжается от нескольких часов до нескольких дней и проявляется повышением температуры (лихорадкой), симптомами раздражения верхних дыхательных путей или желудочно-кишечного тракта.
Характерны общемозговые симптомы: головная боль, обычно в области лба и орбит, рвота, светобоязнь, эпилептические припадки. Нарушения сознания от легких степеней (вялость, сонливость) до комы. Возможны психомоторное возбуждение и психосенсорные расстройства.
Развиваются очаговые симптомы поражения ЦНС. Они зависят от локализации патологического процесса и формы энцефалита, могут проявляться симптомами выпадения (парезы конечностей, афазия) и раздражения (эпилептические припадки).
Кроме типичной клинической картины энцефалита, часто встречаются бессимптомные, абортивные формы, реже - молниеносные. При асимптомных вариантах отсутствуют менингеальные симптомы, однако отмечаются умеренная головная боль и лихорадка неясного происхождения, нерезко выраженные преходящие эпизоды диплопии, головокружения, парестезии и т.п. Изменения цереброспинальной жидкости уточняют природу заболевания.При абортивной форме неврологические признаки отсутствуют, заболевание проявляется симптомами острой респираторной или гастроинтестинальной инфекции. На фоне умеренной головной боли, небольшой температуры может появиться ригидность шейных мышц, что говорит о необходимости люмбальной пункции.
Молниеносная форма протекает от нескольких часов до нескольких дней и заканчивается летально. Заболевание начинается высокой температурой, интенсивной диффузной головной болью. Быстро наступает нарушение сознания, больные впадают в коматозное состояние. Выражена ригидность шейных мышц. Смерть наступает от бульварных нарушений или вследствие острой сердечной недостаточности.Диагностика Энцефалита:
Наиболее важным и диагностически ценным является исследование цереброспинальной жидкости, в которой обнаруживают лимфоцитарный плеоцитоз (от 20 до 100 клеток в 1 мкл), умеренное увеличение белка. Ликвор вытекает под повышенным давлением. В крови отмечаются лейкоцитоз, увеличение СОЭ. На ЭЭГ выявляются диффузные неспецифические изменения, доминирует медленная активность (тета- и дельта-волны). При наличии эпилептических припадков регистрируется эпилептическая активность. Магнитно-резонансная томография выявляет локальные гиподенсные изменения головного мозга. Иногда наблюдается картина объемного процесса при геморрагических энцефалитах, особенно височной доли. На глазном дне нередко выявляются застойные диски зрительных нервов.
Этиологический диагноз основывается, кроме типичных клинических проявлений, на результатах бактериологических (вирусологических) и серологических исследований. Идентификация вируса может быть трудной, а иногда и невозможной. Вирус можно выделить из испражнений и других сред, однако наибольшее значение имеет выявление специфических антител с помощью серологических реакций: реакции нейтрализации (РН), реакции связывания комплемента (РСК), реакции торможения гемагглютинации (РТГА), полимеразной цепной реакции (ПЦР).
Лечение Энцефалита:
Патогенетическая терапия
Производится пероральное и парентеральное введение жидкости с учетом водно-электролитного баланса и кислотно-основного состояния.При тяжёлом течении болезни применяют глюкокортикоиды. Если у больного нет бульбарных нарушений и расстройств сознания, то преднизолон применяется в таблетках из расчета 1,5-2 мг/кг в сутки. Назначается препарат равными дозами в 4-6 приемов в течение 5-6 дней, затем дозировка постепенно снижается (общий курс лечения 10-14 дней). При бульбарных нарушениях и расстройствах сознания преднизолон вводится парентерально из расчета 6-8 мг/кг. Люмбальная пункция при этом противопоказана. Для борьбы с гипоксией через носовые катеторы вводится увлажненный кислород (по 20-30 минут каждый час), проведится гипербарическая оксигенация (10 сеансов под давлением р 02-0,25 МПа), также внутривенно введится оксибутират натрия по 50 мг/кг в сутки или седуксен по 20-30 мг в сутки.
Показания. Аллергические реакции, гемотрансфузионный шок, анафилактический шок, анафилактоидные реакции, отек мозга, бронхиальная астма, астматический статус, острый гепатит, печеночная кома.
Противопоказания. Гиперчувствительность, предшествующая артропластика, патологическая кровоточивость, чрессуставной перелом кости, асептический некроз формирующих сустав эпифизов костей. С осторожностью. Паразитарные и инфекционные заболевания вирусной, грибковой или бактериальной природы: простой герпес, ветряная оспа, корь; амебиаз, стронгилоидоз (установленный или подозреваемый); системный микоз; активный и латентный туберкулез, язвенная болезнь желудка и 12-перстной кишки, эзофагит, гастрит, острая или латентная пептическая язва, дивертикулит, артериальная гипертензия, гиперлипидемия, сахарный диабет, тяжелая хроническая почечная и/или печеночная недостаточность, нефроуролитиаз.
Побочные действия. Тошнота, рвота, повышение или снижение аппетита, брадикардия, бессонница, головокружение.
Также, при лечении энцефалита, для дегидратации и борьбы с отеком и набуханием мозга используют диуретики (10-20 % раствор маннитола по 1-1,5 г/кг внутривенно; фуросемид 20-40 мг внутривенно или внутримышечно, 30 % глицерол 1-1,5 г/кг внутрь, диакарб, бринальдикс).
Показания. Отёк мозга, гипертензия, острая почечная недостаточность, эпилепсия, болезнь Меньера, глаукома, подагра.
Противопоказания. Гиперчувствительность, острая почечная недостаточность, печеночная недостаточность, гипокалиемия, ацидоз, гипокортицизм, болезнь Аддисона, уремия, сахарный диабет, беременность (I триместр), нефрит, гипохлоремия, геморрагичесий инсульт.
Побочные действия. Гипокалиемия, миастения, судороги, обезвоживание, тахикардия, тошнота, рвота.
Рядом российских фармакологов и клиницистов утверждается существование высокоэффективного противовирусного препарата йодантипирина. Заявляется, что он обладает этиотропным эффектом в отношении флавивирусной инфекции, однако следует отметить, что в нигде в мире с противовирусной целью данный препарат не применяется, и отсутствуют какие-либо достоверные данные доказательной медицины, подтверждающие его клиническую эффективность.
Показания: Клещевой энцефалит (лечение и профилактика у взрослых).
Противопоказания: Гиперчувствительность, гиперфункция щитовидной железы.
Побочные действия: Аллергические реакции, отеки, тошнота.Этиотропная терапия
Этиотропная терапия заключается в назначении гомологичного гамма-глобулина, титрованного против вируса клещевого энцефалита. Препарат оказывает четкий терапевтический эффект, особенно при среднетяжелом и тяжелом течении болезни. Гамма-глобулин рекомендуется вводить по 6 мл внутримышечно, ежедневно в течение 3 суток. Лечебный эффект наступает через 12-24 ч после его введения: температура тела снижается, состояние больного улучшается, головные боли и менингеальные явления уменьшаются. Чем раньше вводится гамма-глобулин, тем быстрее наступает лечебный эффект. В последние годы для лечения клещевого энцефалита применяются сывороточный иммуноглобулин и гомологичный полиглобулин, которые получают из плазмы крови доноров, проживающих в природных очагах клещевого энцефалита. В первые сутки лечения сывороточный иммуноглобулин рекомендуется вводить 2 раза с интервалами 10-12 ч по 3 мл при легком течении, по 6 мл - при среднетяжелом и по 12 мл - при тяжелом. В последующие 2 дня препарат назначают по 3 мл однократно внутримышечно. Гомологичный полиглобулин вводится внутривенно по 60-100 мл. Считается, что антитела нейтрализуют вирус, защищают клетку от вируса, связываясь с ее поверхностными мембранными рецепторами, обезвреживают вирус внутри клетки, проникая в нее путём связывания с цитоплазматическими рецепторами.Также применяют противовирусные препараты - нуклеазы, задерживающие размножение вируса. Используют РНК-азу внутримышечно на изотоническом растворе по 30 мг 5-6 раз в день. На курс - 800-1000 мг препарата. Антивирусное действие оказывает препарат цитозинарабиноза, который вводят внутривенно в течение 4-5 дней из расчета 2-3 мг на 1 кг массы тела в сутки.
Инфузионная терапия
При выраженных явлениях интоксации проводится инфузионная терапия. При отеке головного мозга, бульбарных нарушениях наиболее быстрый эффект оказывает внутривенное введение преднизолона (2-5 мг/кг) или дексазона, гидрокортизона. При психомоторном возбуждении, эпилептических припадках внутривенно или внутримышечно вводится седуксен - 0,3-0,4 мг/кг, натрия оксибутират - 50-100 мг/кг, дроперидол - от 0,5 до 6-8 мл, гексенал - 10 % раствор 0,5 мл/кг (с предварительным введением атропина); в клизмах - хлоралгидрата 2 % раствор 50-100 мл.В комплекс терапии следует включать антигистаминные препараты - раствор кальция хлористого, димедрол, дипразин, пипольфен или супрастин, витамины группы В, особенно В6 и В12, АТФ. При развитии вялых парезов показано применение дибазола, галантамина, прозерин, оксазила.
Симптоматическая терапия
- Жаропонижающие препараты
- Противовоспалительные (глюкокортикоиды)
- Противосудорожная терапия (бензонал, дифенин, финлепсин)
- Дезинтоксикационная терапия (солевые растворы, белковые препараты, плазмозаменители)
- Реанимационные мероприятия (ИВЛ, кардиотропные препараты)
- Предупреждение вторичных бактериальных осложнений (антибиотики широкого спектра действия)Восстановительное лечение
После выписки из стационара при наличии неврологических нарушений проводится курсовое восстановительное лечение. Больным могут назначаться витамины группы В, экстракт алоэ, церебролизин (противопоказан при наличии судорог), аминалон, пирацетам, пиридитол, пантогам.Лечение паркинсонизма. Эффективным методом лечения паркинсонизма является прием L-ДОФА (предшественник дофамина). Препарат проникает через гематоэнцефалический барьер и компенсирует недостаток дофамина в базальных ганглиях.
Наиболее эффективно комбинированное лечение, которое позволяет выравнивать баланс путем усиления дофаминергической системы (применение L-ДОФА или L-ДОФА-содержащих препаратов и медитана) и подавления холинергической системы (с помощью циклодола).
Лечение L-ДОФА проводится по определенной схеме, предусматривающей постепенное увеличение дозировки и количества препарата в течение нескольких недель. Для уменьшения раздражения стенок желудочно-кишечного тракта препарат назначают после еды. Начальная доза 0,125 г в сутки, с постепенны мповышением на 0,125-0,25 г в сутки. Лечебный эффект наблюдается на разных дозировках обычно от 2 г до 5-6 г в сутки. При длительном применении препарата в течение многих лет его эффективность снижается.
Противопоказанием к проведению такого лечения являются кровоточащие язвы желудка, тяжелые заболевания печени и почек, декомпенсированное состояние сердечно-сосудистой системы, глоукома, психические заболевания.
Положительные результаты применения L-ДОФА или её производных отмечаются примерно у 70 % больных. Некоторые из них возвращаются к труду.Лечение гиперкинезов. Назначают метаболические препараты, α-адреноблокаторы, нейролептики (галоперидол, аминазин) и транквилизаторы.
Лечение Кожевниковской эпилепсии. Также назначают метаболические препараты, антиконвульсанты (депакин, тегретол, смесь Серейского), транквилизаторы (элениум, мепробамат, триоксазин, гиндарин, мебикар) и нейролептики (аминазин).
Профилактика Энцефалита:
Для защиты человека и животных от этих заболеваний разработаны эффективные вакцины. Профилактика включает также борьбу с переносчиками. Специфической терапии не существует. Изредка встречаются также неинфекционные, т.н. вторичные энцефалиты, возникающие как осложнение или последствие отравления свинцом, эпидемического паротита (свинки), кори, ветряной оспы, гриппа и других заболеваний.
К каким докторам следует обращаться если у Вас Энцефалит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Энцефалита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
МКБ-10
![Энцефалит Расмуссена]()
Общие сведения
Энцефалит Расмуссена — прогрессирующий очаговый энцефалит с хроническим течением, характеризующийся наличием кожевниковской эпилепсии, очагового сенсомоторного неврологического дефицита и когнитивных расстройств. Подробная информация о нем впервые была предоставлена медицинскому сообществу в 1958 году американским врачом Т. Расмуссеном. Как отдельная нозологическая единица энцефалит Расмуссена выделен относительно недавно. Заболевание является крайне редким. Сам Расмуссен в течение 35 лет наблюдал лишь 51 случай подобного энцефалита.
Заболеванию подвержены только дети. Около 85% случаев приходится на возраст до 10 лет. Пик заболеваемости попадает на возрастной период от 5 до 8 лет. Единичные варианты, когда энцефалит Расмуссена дебютирует до 1 года или после 14-летнего возраста, считаются атипичными. Характерно начало энцефалита после перенесенного инфекционного заболевания (чаще ОРВИ). В литературе по неврологии указаны случаи, когда энцефалит Расмуссена сочетался с прогрессирующей гемиатрофией лица.
![Энцефалит Расмуссена]()
Причины
В настоящее время этиопатогенез не установлен. В качестве гипотез рассматриваются 2 варианта: вирусная этиология и аутоиммунный генез заболевания.
- Приверженцы вирусной гипотезы считают энцефалит Расмуссена медленно текущей вирусной нейроинфекцией и соответственно относят его к вирусным энцефалитам. В пользу вирусной теории говорят изменения, обнаруживаемые при гистологическом исследовании пораженных церебральных тканей (периваскулярные инфильтраты, мелкоочаговый глиоз, пролиферация микроглии). Однако все попытки выделить возбудитель пока остаются безрезультатными.
- В пользу аутоиммунной теории свидетельствуют исследования 2002 года, выявившие антитела к глутаматному рецептору, в результате воздействия которых происходит раскрытие ионных каналов и возбуждение нейронов. При этом эксайтотоксичность (повреждение нервных клеток под действием возбуждающих нейротрансмиттеров) обуславливает гибель астроцитов и нейронов. Кроме того, у пациентов, имеющих энцефалит Расмуссена, отмечается высокая встречаемость антигенов НLА. Вероятно, подверженность нейронов указанным выше патологическим изменениям обусловлена иммуногенетическими факторами.
Патоморфология
Морфологически энцефалит Расмуссена отличается очаговым характером возникающих изменений. Патологические процессы распространяются на одну долю или одну гемисферу мозга. В отдельных случаях при раннем дебюте заболевания имеет место двусторонний характер морфологических изменений, однако всегда выявляется первичный очаг поражения. Варианты с распространением патологического процесса на вторую гемисферу мозга являются прогностически неблагоприятными и зачастую приводят к гибели пациентов.
Симптомы энцефалита Расмуссена
Базовым симптомокомплексом выступает кожевниковская эпилепсия — сочетание парциальных судорожных эпиприступов с миоклониями. Наиболее часто наблюдаются простые (без утраты сознания) моторные фокальные приступы, локализующиеся в лице или одной из конечностей. Они могут носить клонический или тонический характер. Возможна вторичная генерализация пароксизмов с переходом в клонико-тонический генерализованный эпиприступ. Миоклонии — фокальные мышечные подергивания — носят практически постоянный характер. В начале заболевания они могут отсутствовать, появляются через несколько месяцев или возникают вместе с очаговым неврологическим дефицитом спустя 1,5-2,5 года после дебюта эпиприступов.
Очаговая симптоматика представлена в основном центральным гемипарезом, контралатеральным пораженной гемисфере. Наблюдаются сенсорные нарушения по проводниковому типу, гемианопсия, афазия (при нарушениях в доминантном полушарии). Когнитивные расстройства, сопровождающие энцефалит Расмуссена, сводятся к прогрессирующим нарушениям памяти, внимания, праксиса и приводят к развитию олигофрении. Сочетаются с психическими отклонениями.
Стадии энцефалита Расмуссена
- Продромальный период может продолжаться несколько лет. У 70% пациентов характеризуется возникновением простых фокальных судорожных пароксизмов двигательного типа. В 20% случаев энцефалит Расмуссена манифестирует эпилептическим статусом. Возможно развитие вторично-генерализованных эпиприступов. В начальном периоде частота пароксизмов, как правило, небольшая; в дальнейшем наблюдается ее существенный рост. Уже в дебюте энцефалита возможно появление паралича Тодда — транзиторного пареза, возникающего в конечностях вслед за происходящими в них в ходе эпиприступа судорожными сокращениями.
- Активный период знаменуется присоединением очаговых неврологических симптомов (гемипареза, гемианопсии, гемигипестезии, нарушений речи), мнестических нарушений и практически постоянными миоклониями. В этой стадии у 80% пациентов наблюдаются простые фокальные моторные пароксизмы, у 28% - сложные фокальные приступы, у 40% - вторично-генерализованные, у 23% - соматосенсорные. Эпилептические гемиприступы по типу джексоновской эпилепсии, затрагивающие мышцы одной половины туловища, согласно некоторым авторам, встречаются лишь в 10% случаев. Период длительности двигательного дефицита при параличе Тодда постепенно увеличивается, затем отмечается перманентный гемипарез, со временем принимающий стойкий характер.
- Период стабилизации у большей части пациентов (около 80 %) наступает спустя не более 3-х лет от времени манифестации энцефалита. Отмечается стабилизация и даже некоторое понижение частоты судорожных приступов. Однако на этом фоне продолжают прогрессировать сенсомоторные, зрительные и когнитивные нарушения. У четверти пациентов диагностируют нейроэндокринные расстройства: преждевременное половое созревание, ожирение.
Диагностика
В продромальном периоде в связи с отсутствием очаговой симптоматики постановка точного диагноза весьма затруднительна. В активной стадии невролог при обследовании выявляет наличие центрального гемипареза с усилением рефлексов и пирамидными знаками, постоянные миоклонические сокращения, нарушения речи, повышенную психическую истощаемость, снижение памяти и внимания и пр. нарушения.
- Электроэнцефалография. В активном периоде выявляет нарушения у всех пациентов. Отмечается замедление основного ритма, возможно полное отсутствие альфа-ритма. В пораженном полушарии наблюдается пик-волновая активность.
- Офтальмологическая диагностика.Определение полей зрения выявляет гемианопсию, при офтальмоскопии изменения глазного дна зачастую отсутствуют.
- Лабораторная диагностика. Исследование цереброспинальной жидкости проводятся с целью исключения другой клинически сходной патологии ЦНС.
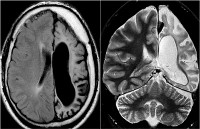
- Томография. Первостепенное значение в постановке диагноза имеет проведение КТ или МРТ головного мозга в динамике. Патогномоничным томографическим признаком, характеризующим энцефалит Расмуссена, выступает прогрессирующая церебральная гемиатрофия. Как правило, вначале регистрируется увеличивающееся с течением времени расширение сильвиевой щели, затем отмечаются атрофические изменения конвекситальных отделов церебральной коры. При наблюдении в динамике типично увеличение зоны корковой атрофии наподобие растекания масляного пятна по пергаменту.
Дифференциальная диагностика проводится с:
- внутримозговыми опухолями;
- церебральными кистами;
- энцефалитами другой этиологии;
- иными видами эпилепсии у детей (синдромом Леннокса-Гасто, синдромом Ландау-Клеффнера, фокальной корковой дисплазией);
- лейкодистрофиями;
- лейкоэнцефалитом Шильдера и др.
Лечение энцефалита Расмуссена
Консервативная терапия включает противоэпилептическое лечение и попытки патогенетической терапии, направленной на замедление прогрессирования атрофических изменений в мозге. Сопровождающие энцефалит Расмуссена эпилептические приступы относятся к резистентным формам эпилепсии.
Консервативная терапия
Антиконвульсантную терапию обычно начинают с назначения вальпроатов. Препаратами выбора также являются топирамат, леветирацетам и фенобарбитал. Резистентность пароксизмов заставляет врачей переходить на комбинированную терапию. Рекомендованы сочетания вальпроатов с топираматом или леветирацетамом, топирамата с леветирацетамом. У некоторых пациентов эффективно сочетание вальпроатов с карбамазепином, хотя последний противопоказан в качестве монотерапии по причине усугубления миоклонических проявлений. Отдельные авторы указывают на временный антиконвульсивный эффект внутривенных инфузий больших доз ноотропила.
Относительно методов патогенетической терапии пока не существует единого мнения. Применяется иммуносупрессивное и иммуномодулирующее лечение, назначение противовирусных фармпрепаратов и глюкокортикостероидов. Последнее время в качестве стартового лечения все чаще используют терапию иммуноглобулинами. По мере прогрессирования симптоматики к ним добавляют кортикостероиды (дексаметазон, метилпреднизолон). При отсутствии положительного результата такой терапии переходят к иммуносупрессии с использованием азатиоприна или циклофосфана. Однозначных данных о результативности противовирусного лечения с применением зидовудина, ацикловира, интерферона пока нет. Возможно проведение плазмафереза, иммуносорбции.
Хирургическая тактика
Прогноз
В большинстве случаев энцефалит Расмуссена имеет неутешительный прогноз. За исключением единичных случаев спонтанной стабилизации заболевания, у пациентов отмечается тяжелейший двигательный и когнитивный дефицит. Летальный исход может наступить в период от 3 до 15 лет со времени дебюта энцефалита.
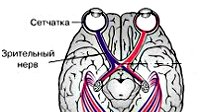
Атрофия зрительного нерва (оптическая нейропатия) – частичная или полная деструкция нервных волокон, передающих зрительные раздражения от сетчатки в головной мозг. Атрофия зрительного нерва приводит к снижению или полной утрате зрения, сужению полей зрения, нарушению цветового зрения, побледнению ДЗН. Диагноз атрофии зрительного нерва ставится при выявлении характерных признаков заболевания с помощью офтальмоскопии, периметрии, цветового тестирования, определения остроты зрения, краниографии, КТ и МРТ головного мозга, В-сканирующего УЗИ глаза, ангиографии сосудов сетчатки, исследования зрительных ВП и др. При атрофии зрительного нерва лечение направлено на устранение патологии, повлекшей за собой данное осложнение.
МКБ-10
![Атрофия зрительного нерва]()
Общие сведения
Различные заболевания зрительного нерва в офтальмологии встречаются в 1-1,5% случаев; из них от 19 до 26% приводят к полной атрофии зрительного нерва и неизлечимой слепоте. Патоморфологические изменения при атрофии зрительного нерва характеризуются деструкцией аксонов ганглиозных клеток сетчатки с их глиально-соединительнотканной трансформацией, облитерацией капиллярной сети зрительного нерва и его истончением. Атрофия зрительного нерва может являться следствием большого количества заболеваний, протекающих с воспалением, сдавлением, отеком, повреждением нервных волокон или повреждением сосудов глаза.
![Атрофия зрительного нерва]()
Причины атрофии зрительного нерва
Факторами, приводящими к атрофии зрительного нерва, могут выступать заболевания глаза, поражения ЦНС, механические повреждения, интоксикации, общие, инфекционные, аутоиммунные заболевания и др.
Причинами поражения и последующей атрофии зрительного нерва нередко выступает различная офтальмопатология: глаукома, пигментная дистрофия сетчатки, окклюзия центральной артерии сетчатки, миопия, увеит, ретинит, неврит зрительного нерва и пр. Опасность повреждения зрительного нерва может быть связана с опухолями и заболеваниями орбиты: менингиомой и глиомой зрительного нерва, невриномой, нейрофибромой, первичным раком орбиты, остеосаркомой, локальными орбитальными васкулитами, саркоидозом и др.
Среди заболеваний ЦНС ведущую роль играют опухоли гипофиза и задней черепной ямки, сдавление области перекреста зрительных нервов (хиазмы), гнойно-воспалительные заболевания (абсцесс головного мозга, энцефалит, менингит), рассеянный склероз, черепно-мозговые травмы и повреждения лицевого скелета, сопровождающиеся ранением зрительного нерва.
Нередко атрофии зрительного нерва предшествует течение гипертонической болезни, атеросклероза, голодание, авитаминоз, интоксикации (отравления суррогатами алкоголя, никотином, хлорофосом, лекарственными веществами), большая одномоментная кровопотеря (чаще при маточных и желудочно-кишечных кровотечениях), сахарный диабет, анемии. Дегенеративные процессы в зрительном нерве могут развиваться при антифосфолипидном синдроме, системной красной волчанке, гранулематозе Вегенера, болезни Бехчета, болезни Хортона.
В ряде случаев атрофия зрительного нерва развивается как осложнение тяжелых бактериальных (сифилиса, туберкулеза), вирусных (кори, коревой краснухи, ОРВИ, опоясывающего герпеса) или паразитарных (токсоплазмоза, токсокароза) инфекций.
Врожденные атрофии зрительного нерва встречаются при акроцефалии (башнеобразном черепе), микро- и макроцефалии, черепно-лицевом дизостозе (болезни Крузона), наследственных синдромах. В 20% наблюдений этиология атрофии зрительного нерва остается невыясненной.
Классификация
Атрофия зрительного нерва может носить наследственный и ненаследственный (приобретенный) характер. К наследственным формам атрофии зрительного нерва относят аутосомно-диминантную, аутосомно-рецессивную и митохондриальную. Аутосомно-доминантная форма может иметь тяжелое и легкое течение, иногда сочетается с врожденной глухотой. Аутосомно-рецессивная форма атрофии зрительного нерва встречается у больных с синдромами Вера, Вольфрама, Бурневилли, Йенсена, Розенберга-Чатториана, Кенни-Коффи. Митохондриальная форма наблюдается при мутации митохондриальной ДНК и сопровождает болезнь Лебера.
Приобретенные атрофии зрительного нерва, в зависимости от этиологических факторов, могут носить первичный, вторичный и глаукоматозный характер. Механизм развития первичной атрофии связан со сдавлением периферических нейронов зрительного пути; ДЗН при этом не изменен, его границы остаются четкими. В патогенезе вторичной атрофии имеет место отек ДЗН, обусловленный патологическим процессом в сетчатке или самом зрительном нерве. Замещение нервных волокон нейроглией носит более выраженный характер; ДЗН увеличивается в диаметре и теряет четкость границ. Развитие глаукоматозной атрофии зрительного нерва вызвано коллапсом решетчатой пластинки склеры на фоне повышенного внутриглазного давления.
По степени изменения окраски диска зрительного нерва различают начальную, частичную (неполную) и полную атрофию. Начальная степень атрофии характеризуется легким побледнением ДЗН при сохранении нормальной окраски зрительного нерва. При частичной атрофии отмечается побледнение диска в одном из сегментов. Полная атрофия проявляется равномерным побледнением и истончением всего диска зрительного нерва, сужением сосудов глазного дна.
По локализации выделяют восходящую (при повреждении клеток сетчатки) и нисходящую (при повреждении волокон зрительного нерва) атрофию; по локализации - одностороннюю и двустороннюю; по степени прогрессирования - стационарную и прогрессирующую (определяется в ходе динамического наблюдения офтальмолога).
Симптомы атрофии зрительного нерва
Основным признаком атрофии зрительного нерва служит не поддающееся коррекции с помощью очков и линз снижение остроты зрения. При прогрессирующей атрофии снижение зрительной функции развивается в сроки от нескольких дней до нескольких месяцев и может закончиться полной слепотой. В случае неполной атрофии зрительного нерва патологические изменения достигают определенной точки и далее не развиваются, в связи с чем зрение утрачивается частично.
Объективные признаки атрофии зрительного нерва выявляются в процессе офтальмологического обследования.
Диагностика
При обследовании пациентов с атрофией зрительного нерва необходимо выяснить наличие сопутствующих заболеваний, факт приема медикаментов и контакта с химическими веществами, наличие вредных привычек, а также жалоб, свидетельствующих о возможных интракраниальных поражениях.
При физикальном обследовании офтальмолог определяет отсутствие или наличие экзофтальма, исследует подвижность глазных яблок, проверяет реакцию зрачков на свет, роговичный рефлекс. Обязательно проводится проверка остроты зрения, периметрия, исследование цветоощущения.
Основную информацию о наличии и степени атрофии зрительного нерва получают с помощью офтальмоскопии. В зависимости от причин и формы оптической нейропатии офтальмоскопическая картина будет отличаться, однако есть типичные характеристики, встречающиеся при различных видах атрофии зрительного нерва. К ним относятся: побледнение ДЗН различной степени и распространенности, изменение его контуров и цвета (от сероватого до воскового оттенка), экскавация поверхности диска, уменьшение на диске числа мелких сосудов (симптом Кестенбаума), сужение калибра артерий сетчатки, изменения вен и др. Состояние ДЗН уточняется с помощью томографии (оптической когерентной, лазерной сканирующей).
Электрофизиологическое исследование (ЗВП) выявляет снижение лабильности и повышение пороговой чувствительности зрительного нерва. При глаукоматозной форме атрофии зрительного нерва с помощью тонометрии определяется повышение внутриглазного давления. Патология глазницы выявляется с помощью обзорной рентгенографии орбиты. Обследование сосудов сетчатки проводится с помощью флуоресцентной ангиографии. Исследование кровотока в глазничной и надблоковой артериях, интракраниальном участке внутренней сонной артерии производится с помощью ультразвуковой допплерографии.
При необходимости офтальмологическое обследование дополняется исследованием неврологического статуса, включающим консультацию невролога, проведение рентгенографии черепа и турецкого седла, КТ или МРТ головного мозга. При выявлении у пациента объемного образования мозга или внутричерепной гипертензии необходима консультация нейрохирурга. В случае патогенетической связи атрофии зрительного нерва с системными васкулитами, показана консультация ревматолога. Наличие опухолей орбиты диктует необходимость осмотра больного офтальмоонкологом. Лечебная тактика при окклюзирующих поражениях артерий (глазничной, внутренней сонной) определяется хирургом-офтальмологом или сосудистым хирургом.
При атрофии зрительного нерва, обусловленной инфекционной патологией, информативны лабораторные тесты: ИФА и ПЦР-диагностика, при атрофии наследственного генеза - генодиагностика.
Дифференциальный диагноз атрофии зрительного нерва следует проводить с периферической катарактой и амблиопией.
Лечение атрофии зрительного нерва
Поскольку атрофия зрительного нерва в большинстве случаев не является самостоятельным заболеванием, а служит следствием других патологических процессов, ее лечение необходимо начинать с устранения причины. Пациентам с интракраниальными опухолями, внутричерепной гипертензией, аневризмой сосудов головного мозга и др. показана нейрохирургическая операция.
Неспецифическое консервативное лечение атрофии зрительного нерва направлено на максимально возможное сохранение зрительной функции. С целью уменьшения воспалительной инфильтрации и отека зрительного нерва проводятся пара-, ретробульбарные инъекции р-ра дексаметазона, внутривенные вливания р-ра глюкозы и кальция хлорида, внутримышечное введение мочегонных препаратов (фуросемида).
Для улучшения кровообращения и трофики зрительного нерва показаны инъекции пентоксифиллина, ксантинола никотината, атропина (парабульбарно и ретробульбарно); внутривенное введение никотиновой кислоты, эуфиллина; витаминотерапия (В2, В6,В12), инъекции экстракта алоэ или стекловидного тела; прием циннаризина, пирацетама, рибоксина, АТФ и др. В целях поддержания низкого уровня внутриглазного давления проводятся инстилляции пилокарпина, назначаются мочегонные средства.
В случае отсутствия противопоказаний при атрофии зрительного нерва назначается иглорефлексотерапия, физиотерапия (электрофорез, ультразвук, лазеро- или электростимуляция зрительного нерва, магнитотерапия, эндоназальный электрофорез и др.). При снижении остроты зрения ниже 0,01 любое проводимое лечение не эффективно.
Прогноз и профилактика
В случае, если атрофию зрительного нерва удалось диагностировать и начать лечить на ранней стадии, возможно сохранение и даже некоторое повышение зрения, однако полного восстановления зрительной функции не происходит. При прогрессирующей атрофии зрительного нерва и отсутствии лечения может развиться полная слепота.
Для предотвращения атрофии зрительного нерва необходимо своевременное лечение глазных, неврологических, ревматологических, эндокринных, инфекционных заболеваний; предупреждение интоксикаций, своевременное переливание крови при профузных кровотечениях. При первых признаках нарушения зрения необходима консультация окулиста.
Читайте также: