Энцефалиты на фоне эпилепсии
Обновлено: 02.05.2024

Долгое время взаимосвязи между эпилепсией, судорогами и эмоциями была предметом дебатов, как среди клиницистов , так и нейробиологов. В своем знаменитом наблюдении Гиппократ отмечал, что «меланхолики обычно становятся эпилептиками, а эпилептики - меланхоликами: важно направление, которое принимает болезнь; если она затрагивает тело , то появляется склонность к эпилепсии, если интеллект, то - к меланхолии.
Аффективные расстройства и расстройства тревожного спектра являются наиболее частыми психическими расстройствами , сочетающимися с эпилепсией, с распространенностью от 20% до 22%; однако в отдельных популяциях распространенность подобной коморбидности может достигать 50%. Причины такой ассоциации являются биологическими и психосоциальными. Эпилепсия - это хроническое заболевание, которое приводит к ряду социальных ограничений и дискриминации больных, что способствует деморализации и низкой самооценке. Более того, эпилепсия и расстройства настроения, по-видимому, имеют общую нейробиологическую основу с вовлечением лимбических структур и возможностью модуляции основных путей нейротрансмиттеров противосудорожными препаратами.
По сравнению с расстройствами настроения психозы, по-видимому, относительно редки у пациентов с эпилепсией, но представляют собой серьезные осложнения, которые влияют на заболеваемость и смертность. Эпидемиологические данные указывают на то, что частота "неорганических", "неаффективных психозов", включая шизофреноподобные состояния и связанные с ними расстройства, как правило, заметно представлена у пациентов с эпилепсией по сравнению с общей популяцией или с другими хроническими заболеваниями. Более высокая распространенность психозов наблюдалась у госпитализированных пациентов с эпилепсией. Связь между эпилепсией и психозами имеет сильные нейробиологические основы, связанные с вовлечением конкретных областей мозга.
Аффективные расстройства (нарушения настроения) при эпилепсии часто игнорируются и не фиксируются из-за недостатка времени врача - эпилептолога, отсутствия у последнего достаточной квалификации и нежелания клиницистов направлять пациентов к психиатру из-за психических расстройств. Кроме того, до 50% пациентов с эпилепсией и депрессией представляют психические симптомы, которые не учитываются стандартизованными классификационными системами. Это особенно заметно в случае интерикатльного ( между судорожными приступами ) дисфорического расстройства (IDD).
Конкретные психопатологические симптомы при эпилепсии представляют собой своеобразный кластер симптомов, характеризующийся периодическими изменениями настроения и вспышками раздражительности и агрессивного поведения. Эти эпизоды возникают без внешних триггеров и без помрачения сознания; они начинаются и заканчиваются быстро и повторяются довольно регулярно (каждые несколько дней до нескольких месяцев и от нескольких часов до двух дней). Кластер симптомов, описанный у пациентов с дисфорией ( IDD) и эпилепсией, весьма специфичен и редко встречается в практике врача - психиатра даже у пациентов с быстрым циклическим биполярным расстройством или циклотимией. Интересно отметить, что примерно у 50% пациентов дисфорические симптомы проявляют четкую связь с эпилептическими судорогами и возникающими либо перед припадком, либо после его окончания.
Эпилептические припадки характеризуются не только иктальной фазой, но и рядом нарушений поведения , которые могут предшествовать приступу или следовать за ним. Перииктальные симптомы могут не соответствовать временным критериям классификацияй, когда они слишком кратковременны.
Иктальные психозы обычно представляют собой "неконвульсивный эпилептический статус" с частой причиной происхождения - поражение височной доли. Постиктальные психозы, вероятно, наиболее актуальны в эпидемиологических оценках и составляют примерно 25% всех психозов при эпилепсии. Они обычно следуют после серии вторичных генерализованных тонико-клонических приступов, за которыми идет период нормального психического состояния от 24 до 48 часов. Почти у всех пациентов этот отчетливый интервал, и неспособность его распознавать может привести к неправильным диагнозам. Патогенез постиктальных психозов неизвестен, но его клиническая картина представляет собой достаточно стереотипное явление, которое происходит главным образом у пациентов с легкой умственной неполноценностью и эпилепсией ( очагом ) в височной доле. Результаты исследований показывают корреляцию между постиктальными психозами и де - жавю аурой или иктальным страхом ( фобией). Феноменология постиктальных психозов является полиморфной, но большинство пациентов испытывают патологическое настроение и параноидный бред с мистическим и религиозным содержанием. Сознание может быть изменено (например, от дезориентировки до полностью сумеречного состояния сознания). Высокий уровень тревоги со страхом перед надвигающейся смертью представляет собой еще один типичный симптом, который может проявиться в эпизодах насилия, или самоубийств, особенно , если у пациента присутствуют командные галлюцинации.
Психозы после судорожного приступа ( постиктальные) характеризуются спонтанной ремиссией в течение нескольких дней или недель; лечение антипсихотическим препаратом требуется только для снижения смертности и заболеваемости. Наконец, следует иметь в виду, что в незначительных случаях постиктальные психозы могут перейти в хронический интериктальный психоз.
В настоящее время интериктальные психозы представляют собой редкое осложнение, и общее впечатление врачей заключается в том, что они, вероятно, связаны с эффективным лечением эпилептических синдромов. Неврологические исследования пациентов с интериктальными психозами выявляют церебральные пороки развития, такие как гематомы и ганглиоглиомы, и грубые аномалии, такие как увеличенные желудочки и перивентрикулярный глиоз.Связь между психозами и мезо-мембранными структурами определенных локусов хорошо известна и подтверждена клиническими данными и результатами нейровизуализации. Однако, время поражений и функциональные изменения в мозге пациентов с интериктальными психозами в значительной степени отличаются от тех, которые описаны при шизофрении, что предполагает факт интеграции интериктальных психозов с эпилепсией.
Феноменология интериктальных психозов, по-видимому, несколько отличается от феноменологии шизофрении. Исследователи подчеркивают сохранение аффекта в контексте симптомов первого ранга Шнайдера с религиозным мистическим содержанием. Была также отмечена маловероятность появления негативных симптомов и отсутствие формальных расстройств мышления и кататонических состояний. Долгосрочный прогноз межприступных психозов, по-видимому, лучше при эпилепсии , чем при шизофрении, с менее выраженным ухудшением познавательной способности и институционализацией. Вероятно, это связано с относительной сохранностью личности и тенденцией к ослаблению психотических симптомов с течением времени.
В клинической картине эпилепсии могут присутствовать другие психопатологические синдромы , такие как маниакальные и депрессивные эпизоды и диссоциативные состояния.

С эпилептологической точки зрения, лимбический энцефалит (LE) является наиболее важным иммунным синдромом, связанным с недавно обнаруженными антинейрональными аутоантителами ( ANAB) . Основными признакамиэтого синдрома являются подострое начало дефицита рабочей памяти, изменение психического статуса, спутанность сознания, делирий или другие психопатологические симптомы . Кроме того, может наблюдаться прогрессирующее нарушение сознания вплоть до комы. Для идентификации LE необходимо наличие хотя бы одного из следующих критерий наблюдения : приступы de novo или даже эпилептический статус, новый очаговый неврологический дефицит, плеоцитоз спинномозговой жидкости или признаки МРТ, указывающие на энцефалит. Быстрое распознавание лимбического энцефалита является ключевым моментом, поскольку существуют эффективные методы лечения, и данные исследований все чаще свидетельствуют о том, что раннее начало лечения связано с лучшими результатами и исходами. Другим важным антителом, связанным с эпилепсией, является антитело, направленное против цитозольного фермента глутаматдекарбоксилазы (GAD). GAD катализирует превращение глутамата в γ-аминомасляную кислоту (GABA), а наличие антител против GAD связано с эпилепсией, синдромом "скованного человека" (ригидности ) - SPS и лимбического энцефалита (LE).
Большинство обнаруженных ранее ANAB (обнаруженных до 2007 г.) распознают внутриклеточные эпитопы и были связаны с опухолями, вызывающими паранеопластические синдромы, тогда как те ANAB, идентифицированные позже, реже являются паранеопластическими и направлены в основном на антигены на клеточной мембране. Энцефалит с антителами против GAD является исключением, потому что антитела против внутриклеточных антигенов индуцируются в отсутствие опухоли.
Энцефалит против NMDAR
Психопатологические симптомы важны на раннем этапе болезни, так как 75% взрослых пациентов сначала попадают на прием к психиатру. Эти симптомы были первоначальным проявлением у 59% национальной французской когорты (n = 111), из которых 40% испытывали галлюцинации и 23% испытывали депрессию. Меньшая часть этих пациентов была устойчивой к психотропнмы препаратам к нейролептикам или антидепрессантам. Направление в неврологическое (реанимационное) отделение было связано с множеством других причин, таких как развивающиеся судороги и эпилептический статус, и, в частности, с развитием злокачественного нейролептического синдрома у 21 пациента. 40% пациентов впервые были госпитализированы в психиатрические учреждения, однако более половины из этих пациентов также имели по крайней мере один неврологический признак, а у 38% неврологические симптомы развились в течение нескольких дней. У маленьких детей судороги и дискинезии являются начальными симптомами у половины пациентов.
Энцефалит против LGI1
Энцефалит Anti-Caspr2
Анти-AMPAR энцефалит
Анти- GABA B R энцефалит
Эта форма энцефалита получает все большее признание и является одной из самых распространенных после энцефалита NMDAR и LGI1. Более половины случаев являются паранеопластическими, в основном связанными с мелкоклеточным раком легкого. Интересно, что антитела к рецептору GABA B отсутствуют у больших групп пациентов с мелкоклеточным раком легкого, что указывает на то, что присутствие антител может оказывать свое патогенное действие в отсутствие опухоли. Преобладают пациенты мужского пола старше 40 лет, у которых возникают приступы (частичные комплексные, вторично генерализованные приступы или часто рефрактерный эпилептический статус [SE]). Кроме того, у пациентов наблюдается потеря памяти, спутанность сознания и тяжелая бессонница. Редкие симптомы включают атаксию и синдром опсоклонуса / миоклонуса.
Энцефалит против mGluR5
Энцефалит, связанный с антидипептидил-пептидазоподобным протеином-6 (DPPX)
Энцефалит, связанный с антидипептидил-пептидазоподобным протеином-6 (DPPX) потенциалзависимого калиевого канала Kv4.2 вызывают классические симптомы лимбического энцефалита со спутанностью сознания, потерей памяти, психозом или депрессией, а также симптомами поражения ствола мозга (нарушения движений глаз, атаксия, дизартрия и т. дисфагия и дыхательная недостаточность), нарушения сна и миоклонус. Как уникальный клинический признак, обильная и трудно поддающаяся лечению неинфекционная диарея в двух третях случаев предшествует LE от нескольких недель до месяцев.. Это может быть результатом экспрессии эпитопа как в клетках кишечника, так и в нейронах. Судороги наблюдаются редко (около 15%). Антитела также были обнаружены при прогрессирующем энцефаломиелите с ригидностью и миоклонусом (PERM).
Анти- GABA A (β3 / γ2) R-энцефалит
LE, связанный с антителами против субъединиц β3 и γ2 рецепторов GABA A, встречается редко и в двух третях случаев поражает мужчин в возрасте от 3 до 74 лет. Причина такого гендерного неравенства неизвестна, но интересна, поскольку преобладание мужчин при аутоиммунных заболеваниях встречается редко. Можно предположить, что женские половые гормоны, такие как аллопрегнанолон, или оральные контрацептивы могут консолидировать γ2-субъединицы и защищать от судорог и SE. Рецепторы GABA А , особенно внесинаптические, могут модулироваться нейростероидами с подобной половым гормонам структурой. Около 20% пациентов болеют раком. Основные симптомы типичны для LE, но у 50–70% пациентов бывают тяжелые судороги, вплоть до почти неразрешимого эпилептического статуса ( SE). Кроме того, у некоторых пациентов также имеется SPS или синдром опсоклонуса / миоклонуса. Ответ судорог и SE на иммуносупрессию замечательный, тогда как классические противосудорожные препараты неэффективны против эпилептической активности.
Лечение аутоиммунного энцефалита
Плазмаферез хорошо зарекомендовал себя как вариант лечения, но недавно было опубликовано исследование иммуноабсорбции (IА). 86% процентов пациентов с ANAB улучшили cвое состояние , тогда как пациенты с внутриклеточно-направленными антителами к антигенам не улучшили свой статус. Клиренс антител также был интересен: титры снижались на 97% (сыворотка) и 64% (CSF) через 4 дня после IA и далее падали до 98% (сыворотка) и 88% (CSF) через 4 недели, что свидетельствует о продолжительном лечебном эффекте. Считается, что В-клетки имеют решающее значение для продолжающегося иммунного ответа у пациентов с ANAB. IL-6 - это цитокин, который, как считается, играет ключевую роль в созревании B-клеток и терминальной дифференцировке в плазматические клетки, которые секретируют большое количество антител. Исследование оптического нейромиелита (NMO) с участием пациентов с положительными антителами к аквапорину-4 определило, что IL-6 является ключевым цитокином для созревания B-клеток и выработки специфичных для заболевания антител. Предварительные данные об использовании тоцилизумаба, моноклонального антитела против IL-6, при NMO и аутоиммунном энцефалите обнадеживают, и необходимо провести дополнительную работу для оценки эффективности этого препарата в качестве автономной терапии второй линии.

Неврологические расстройства при COVID-19 можно обсудить в трех разделах: (1) неврологические особенности вирусной инфекции, (2) постинфекционные неврологические осложнения, (3) инфекции у пациентов с неврологическими сопутствующими заболеваниями. Другой вопрос, который заслуживает упоминания, - это меры предосторожности в плане заражения и лечения коронавирусной инфекции , которые следует предпринимать для особой группы неврологических больных пациентов, которым требуются иммунодепрессанты. Последняя группа в основном состоит из рассеянного склероза, миастении и аутоиммунного энцефалита.
Головная боль
Нарушение мозгового кровообращения
Проблема усложняется, если рассматривать лечение пациента с ишемическим инсультом на фоне коронавирусной инфекции. Применение антиагрегантов и антикоагулянтов здесь требует осторожности, потому что известно, что вирус вызывает выраженное поражение дыхательных путей, а, по мнению некоторых авторов, поражение нервной системы может частично отвечать за нарушение дыхания.
Помрачение сознания
Атаксия
В исследовании в Ухане атаксия была обнаружена только у одного пациента, хотя подробное описание или анатомическая основа этого конкретного симптома не была доступна в этой статье. В одном из центров лечения ковида недавно столкнулись с 72-летним мужчиной с острым началом мозжечковой атаксии с последующей энцефалопатией, у которого наконец была диагностирована пневмония, вызванная SARS-CoV-2. Примечательно, что у этого пациента неврологические расстройства на несколько дней опережали респираторные нарушения.
Судорожный припадок
Судороги предположительно усложняют клиническую ситуацию из-за повреждения скелетных мышц, которое уже является хорошо известным проявлением болезни. Тот факт, что неврологические осложнения чаще встречаются у тяжелобольных пациентов, а также факторы риска сердечно-сосудистых заболеваний являются прогностическими факторами тяжести, потенциал лекарственного взаимодействия некоторых противоэпилептических препаратов заслуживает внимания в таких клинических ситуациях. Таким образом, с точки зрения невролога, судорожный приступ у пациента с COVID-19 будет иметь важные последствия как с диагностической, так и с терапевтической точки зрения.
Поражение мышц, печени и почек
Уже были отмечены симптомы повреждения скелетных мышц, часто связанные с поражением печени и почек. В литературе сообщалась , что частота при ковиде здесь составляет 10,7%, и, как и другие неврологические особенности, эта клиническая картина также связана с тяжелой формой болезни. Можно предположить, что пациенты с ранее существовавшей почечной или печеночной недостаточностью будут очень уязвимы в плане развития признаков полиорганной недостаточности на фоне повреждения скелетных мышц. Мышечные ферменты, включая креатинкиназу и лактатдегидрогеназу, значительно повышены у пациентов с симптомами ковида - наблюдение, которое подтверждает повреждение мышечной мембраны. Однако точный механизм повреждения мышц не установлен. Возможные варианты включают вирусную инвазию в мышцы через тропизм рецептора ACE-2 и иммуноопосредованное повреждение мышечных волокон. Потребуются дальнейшие исследования, чтобы выяснить механизмы, лежащие в основе повреждения скелетных мышц при COVID-19.
Потеря обоняния и вкуса
В литературе сообщалось, что гипогевзия, как и гипосмия, являются довольно постоянными симптомами инфекции SARS-CoV-2. Все они классифицируются как проявления поражения периферических нервов, в то время как другим отмеченным признаком является невралгия. Однако стоит отметить, что обонятельный нерв считается частью ЦНС, и гипосмия может быть скорее отражением поражения обонятельной луковицы, чем периферической невропатии. Точно так же гипоплазия, если она вызвана оптической невропатией, может отражать проявление ЦНС, потому что зрительный нерв, согласно классическому учению, является продолжением мозга.
Постинфекционные осложнения
Неврологические расстройства до ковида и после
Можно ожидать, что пациенты с ограниченной подвижностью и пациенты, получающие иммуносупрессивную терапию, будут более восприимчивы к коронавирусной инфекции. В прессе уже обсуждались проблемы, с которыми столкнутся пациенты с деменцией в этот период социального дистанцирования и домашней изоляции. Очевидно, проблема будет острее для тех больных, которые зависят от других в повседневной жизни. Ситуация будет аналогичной для пациентов с выраженными двигательными проблемами. Предполагается, что из-за их ограниченной мобильности социальное дистанцирование скажется на них хуже. Снижение подвижности и деменция также могут предрасполагать пациента к вирусной инфекции, причем , ассоциация здесь становится двусторонней.
В современной неврологии широко используются иммунодепрессанты для борьбы с некоторыми заболеваниями ЦНС и ПНС. Прототипом среди этих заболеваний является рассеянный склероз, требующий длительной иммуносупрессии. Данные по COVID-19 показывают, что пожилые люди, а также люди с нарушенной иммунной регуляцией с большей вероятностью не только заразятся инфекцией, но и значительно ухудшат свое состояние , как в плане уже имеющегося неврологического расстройства , так общего состояния. Поэтому, как и в онкологическом отделении, пациенты неврологического отделения, которые принимали циклические иммунодепрессанты, нуждаются во внимании. При работе с такими случаями следует проявлять соответствующую осторожность как со стороны невролога, так и со стороны родственников пациента. В недавней статье на эту тему говорится , что преимущества продолжения иммунотерапии у пациентов с рассеянным склерозом и связанными с ним расстройствами могут перевешивать риски отмены лекарств при опасениях заражения COVID-19. В частности, это связано с тем, что большинство инфекций, как и среди населения в целом, считаются умеренными и самоограничивающимися.
Реабилитация больных, перенесших ковид
С ростом числа выздоравливающих от инфекции SARS-CoV-2 проблема реабилитации должна стать важной задачей . Общение с неврологами, работающими в этой области , показывает, что есть первые доказательства необходимости реабилитации, включая неврологические аспекты, у клинически выздоровевших пациентов. Можно предположить, что психосоциальные последствия длительного социального дистанцирования и домашней изоляции потребуют адекватных мер психологической реабилитации, поскольку пандемия не ослабевает в своей выраженности. Мои собственные наблдения говорят о том, что после ковида болезнь Альцгеймера начинает проявлять себя в более молодом возрасте , а следовательно ее профилактика также становится важной аздачей нейропсихиатра.
Острый респираторный синдром
С момента начала вспышки SARS-CoV-2, если есть одно легочное проявление, получившее максимальное внимание, то это острый респираторный исндром . Имеющиеся данные свидетельствуют о том, что значительный процент людей, переживших это состояние , может страдать от долговременных когнитивных нарушений ( памяти, внимани яи мышления). Было замечено, что несколько факторов, включая механическую вентиляцию легких, вызывают снижение высших функций мозга. Было замечено, что несколько факторов, включая механическую вентиляцию легких, вызывают снижение высших функций мозга. после острого респираторного синдрома. Острое повреждение гематоэнцефалического барьера считается здесь основным механизмом когнитивных нарушений. Эффект от такой травмы может быть усилен, если имеется ранее существовавшее когнитивное нарушение, которое соответствует хроническому повреждению гематоэнцефалического барьера. С другой стороны, у пациентов с черепно-мозговой травмой развивается нейрогенный отек легких. Таким образом, предполагается, что так называемая ось мозг-легкие работает в обоих направлениях.
Приведенные выше наблюдения особенно актуальны в настоящих обстоятельствах, учитывая необходимость искусственной вентиляции легких у большинства серьезно пострадавших пациентов с COVID-19. Поскольку пандемия продолжает разворачиваться, число людей, прекращающих искусственную вентиляцию легких, возрастет, и будут учитываться долгосрочные когнитивные нарушения. Можно ожидать, что мы не только станем свидетелями снижения когнитивных способностей, продолжающегося в течение нескольких месяцев в этой группе пациентов, но также некоторые из них могут прогрессировать до преждевременного начала деменции.
МКБ-10
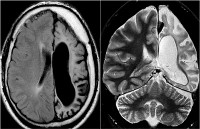
Общие сведения
Энцефалит Расмуссена — прогрессирующий очаговый энцефалит с хроническим течением, характеризующийся наличием кожевниковской эпилепсии, очагового сенсомоторного неврологического дефицита и когнитивных расстройств. Подробная информация о нем впервые была предоставлена медицинскому сообществу в 1958 году американским врачом Т. Расмуссеном. Как отдельная нозологическая единица энцефалит Расмуссена выделен относительно недавно. Заболевание является крайне редким. Сам Расмуссен в течение 35 лет наблюдал лишь 51 случай подобного энцефалита.
Заболеванию подвержены только дети. Около 85% случаев приходится на возраст до 10 лет. Пик заболеваемости попадает на возрастной период от 5 до 8 лет. Единичные варианты, когда энцефалит Расмуссена дебютирует до 1 года или после 14-летнего возраста, считаются атипичными. Характерно начало энцефалита после перенесенного инфекционного заболевания (чаще ОРВИ). В литературе по неврологии указаны случаи, когда энцефалит Расмуссена сочетался с прогрессирующей гемиатрофией лица.

Причины
В настоящее время этиопатогенез не установлен. В качестве гипотез рассматриваются 2 варианта: вирусная этиология и аутоиммунный генез заболевания.
- Приверженцы вирусной гипотезы считают энцефалит Расмуссена медленно текущей вирусной нейроинфекцией и соответственно относят его к вирусным энцефалитам. В пользу вирусной теории говорят изменения, обнаруживаемые при гистологическом исследовании пораженных церебральных тканей (периваскулярные инфильтраты, мелкоочаговый глиоз, пролиферация микроглии). Однако все попытки выделить возбудитель пока остаются безрезультатными.
- В пользу аутоиммунной теории свидетельствуют исследования 2002 года, выявившие антитела к глутаматному рецептору, в результате воздействия которых происходит раскрытие ионных каналов и возбуждение нейронов. При этом эксайтотоксичность (повреждение нервных клеток под действием возбуждающих нейротрансмиттеров) обуславливает гибель астроцитов и нейронов. Кроме того, у пациентов, имеющих энцефалит Расмуссена, отмечается высокая встречаемость антигенов НLА. Вероятно, подверженность нейронов указанным выше патологическим изменениям обусловлена иммуногенетическими факторами.
Патоморфология
Морфологически энцефалит Расмуссена отличается очаговым характером возникающих изменений. Патологические процессы распространяются на одну долю или одну гемисферу мозга. В отдельных случаях при раннем дебюте заболевания имеет место двусторонний характер морфологических изменений, однако всегда выявляется первичный очаг поражения. Варианты с распространением патологического процесса на вторую гемисферу мозга являются прогностически неблагоприятными и зачастую приводят к гибели пациентов.
Симптомы энцефалита Расмуссена
Базовым симптомокомплексом выступает кожевниковская эпилепсия — сочетание парциальных судорожных эпиприступов с миоклониями. Наиболее часто наблюдаются простые (без утраты сознания) моторные фокальные приступы, локализующиеся в лице или одной из конечностей. Они могут носить клонический или тонический характер. Возможна вторичная генерализация пароксизмов с переходом в клонико-тонический генерализованный эпиприступ. Миоклонии — фокальные мышечные подергивания — носят практически постоянный характер. В начале заболевания они могут отсутствовать, появляются через несколько месяцев или возникают вместе с очаговым неврологическим дефицитом спустя 1,5-2,5 года после дебюта эпиприступов.
Очаговая симптоматика представлена в основном центральным гемипарезом, контралатеральным пораженной гемисфере. Наблюдаются сенсорные нарушения по проводниковому типу, гемианопсия, афазия (при нарушениях в доминантном полушарии). Когнитивные расстройства, сопровождающие энцефалит Расмуссена, сводятся к прогрессирующим нарушениям памяти, внимания, праксиса и приводят к развитию олигофрении. Сочетаются с психическими отклонениями.
Стадии энцефалита Расмуссена
- Продромальный период может продолжаться несколько лет. У 70% пациентов характеризуется возникновением простых фокальных судорожных пароксизмов двигательного типа. В 20% случаев энцефалит Расмуссена манифестирует эпилептическим статусом. Возможно развитие вторично-генерализованных эпиприступов. В начальном периоде частота пароксизмов, как правило, небольшая; в дальнейшем наблюдается ее существенный рост. Уже в дебюте энцефалита возможно появление паралича Тодда — транзиторного пареза, возникающего в конечностях вслед за происходящими в них в ходе эпиприступа судорожными сокращениями.
- Активный период знаменуется присоединением очаговых неврологических симптомов (гемипареза, гемианопсии, гемигипестезии, нарушений речи), мнестических нарушений и практически постоянными миоклониями. В этой стадии у 80% пациентов наблюдаются простые фокальные моторные пароксизмы, у 28% - сложные фокальные приступы, у 40% - вторично-генерализованные, у 23% - соматосенсорные. Эпилептические гемиприступы по типу джексоновской эпилепсии, затрагивающие мышцы одной половины туловища, согласно некоторым авторам, встречаются лишь в 10% случаев. Период длительности двигательного дефицита при параличе Тодда постепенно увеличивается, затем отмечается перманентный гемипарез, со временем принимающий стойкий характер.
- Период стабилизации у большей части пациентов (около 80 %) наступает спустя не более 3-х лет от времени манифестации энцефалита. Отмечается стабилизация и даже некоторое понижение частоты судорожных приступов. Однако на этом фоне продолжают прогрессировать сенсомоторные, зрительные и когнитивные нарушения. У четверти пациентов диагностируют нейроэндокринные расстройства: преждевременное половое созревание, ожирение.
Диагностика
В продромальном периоде в связи с отсутствием очаговой симптоматики постановка точного диагноза весьма затруднительна. В активной стадии невролог при обследовании выявляет наличие центрального гемипареза с усилением рефлексов и пирамидными знаками, постоянные миоклонические сокращения, нарушения речи, повышенную психическую истощаемость, снижение памяти и внимания и пр. нарушения.
- Электроэнцефалография. В активном периоде выявляет нарушения у всех пациентов. Отмечается замедление основного ритма, возможно полное отсутствие альфа-ритма. В пораженном полушарии наблюдается пик-волновая активность.
- Офтальмологическая диагностика.Определение полей зрения выявляет гемианопсию, при офтальмоскопии изменения глазного дна зачастую отсутствуют.
- Лабораторная диагностика. Исследование цереброспинальной жидкости проводятся с целью исключения другой клинически сходной патологии ЦНС.
- Томография. Первостепенное значение в постановке диагноза имеет проведение КТ или МРТ головного мозга в динамике. Патогномоничным томографическим признаком, характеризующим энцефалит Расмуссена, выступает прогрессирующая церебральная гемиатрофия. Как правило, вначале регистрируется увеличивающееся с течением времени расширение сильвиевой щели, затем отмечаются атрофические изменения конвекситальных отделов церебральной коры. При наблюдении в динамике типично увеличение зоны корковой атрофии наподобие растекания масляного пятна по пергаменту.
Дифференциальная диагностика проводится с:
- внутримозговыми опухолями;
- церебральными кистами;
- энцефалитами другой этиологии;
- иными видами эпилепсии у детей (синдромом Леннокса-Гасто, синдромом Ландау-Клеффнера, фокальной корковой дисплазией);
- лейкодистрофиями;
- лейкоэнцефалитом Шильдера и др.
Лечение энцефалита Расмуссена
Консервативная терапия включает противоэпилептическое лечение и попытки патогенетической терапии, направленной на замедление прогрессирования атрофических изменений в мозге. Сопровождающие энцефалит Расмуссена эпилептические приступы относятся к резистентным формам эпилепсии.
Консервативная терапия
Антиконвульсантную терапию обычно начинают с назначения вальпроатов. Препаратами выбора также являются топирамат, леветирацетам и фенобарбитал. Резистентность пароксизмов заставляет врачей переходить на комбинированную терапию. Рекомендованы сочетания вальпроатов с топираматом или леветирацетамом, топирамата с леветирацетамом. У некоторых пациентов эффективно сочетание вальпроатов с карбамазепином, хотя последний противопоказан в качестве монотерапии по причине усугубления миоклонических проявлений. Отдельные авторы указывают на временный антиконвульсивный эффект внутривенных инфузий больших доз ноотропила.
Относительно методов патогенетической терапии пока не существует единого мнения. Применяется иммуносупрессивное и иммуномодулирующее лечение, назначение противовирусных фармпрепаратов и глюкокортикостероидов. Последнее время в качестве стартового лечения все чаще используют терапию иммуноглобулинами. По мере прогрессирования симптоматики к ним добавляют кортикостероиды (дексаметазон, метилпреднизолон). При отсутствии положительного результата такой терапии переходят к иммуносупрессии с использованием азатиоприна или циклофосфана. Однозначных данных о результативности противовирусного лечения с применением зидовудина, ацикловира, интерферона пока нет. Возможно проведение плазмафереза, иммуносорбции.
Хирургическая тактика
Прогноз
В большинстве случаев энцефалит Расмуссена имеет неутешительный прогноз. За исключением единичных случаев спонтанной стабилизации заболевания, у пациентов отмечается тяжелейший двигательный и когнитивный дефицит. Летальный исход может наступить в период от 3 до 15 лет со времени дебюта энцефалита.
Кожевниковская эпилепсия — отдельная клиническая форма эпилепсии, характеризующаяся возникновением простых парциальных эпиприступов на фоне постоянных локальных клонических судорог (миоклоний). Наиболее часто встречается при клещевом энцефалите. В клинической картине, кроме судорожного синдрома, наблюдается гемипарез и эмоционально-психические нарушения. Диагностический поиск осуществляется по данным клинической симптоматики, анамнеза, ЭЭГ, ПЭТ, КТ или МРТ головного мозга. Лечение направлено на устранение причинной патологии и борьбу с эпилепсией.
МКБ-10
G40.1 Локализованная (фокальная) (парциальная) симптоматическая эпилепсия и эпилептические синдромы с простыми парциальными припадками
Общие сведения

Причины кожевниковской эпилепсии
Морфологическим субстратом эпилепсии Кожевникова выступают изменения 3-5 слоев церебральной коры прецентральной извилины, ответственной за генерацию двигательных импульсов, затем поступающих к мотонейронам спинного мозга и от них по периферическим нервным стволам - к мышцам. Клинические проявления связаны с повышением возбудимости нейронов определенного участка коры прецентральной извилины и формированием очага постоянной эпилептогенной активности. Предполагают наличие структурно-функциональных изменений не только в коре, но также в соответствующих подкорковых структурах и спинальных мотонейронах, с образованием регионарной эпилептогенной системы.
Факторами, вызывающими указанные изменения, могут выступать различные патологические процессы. Наиболее часто кожевниковская эпилепсия встречается при клещевом энцефалите и энцефалите Расмуссена. Она может наблюдаться при других инфекционных поражениях мозга (например, при церебральном цистицеркозе, нейросифилисе, туберкулезном менингоэнцефалите), фокальной корковой дисплазии, опухолях головного мозга, артериовенозных мальформациях, инсульте, дисметаболических нарушениях (например, при сахарном диабете) и пр. В ряде случаев кожевниковская эпилепсия является следствием перенесенной черепно-мозговой травмы.
Симптомы кожевниковской эпилепсии
У некоторых пациентов кожевниковская эпилепсия наблюдается в остром периоде клещевого энцефалита, но чаще она развивается спустя 1-6 месяцев от времени его дебюта. При энцефалите Расмуссена миоклонический компонент редко проявляется в продромальной стадии, чаще развернутая картина эпилепсии Кожевникова наблюдается в активном периоде (спустя 1-2,5 года от манифестации энцефалита).
Простые фокальные двигательные эпиприступы, как правило, протекают в виде клонических сокращений мышц одной половины лица или одной руки (чаще только кисти). Может наблюдаться одновременное вовлечение руки и лица. Реже встречаются пароксизмы с клоническими судорогами в ноге, еще реже — с вовлечением всей половины тела (гемиконвульсивные приступы). Судороги возникают в противоположной эпилептогенному очагу половине тела, т. е. контрлатерально. Зачастую перед их появлением пациенты ощущают жжение, онемение или покалывание в подверженной судорогам области.
Начавшийся локально эпиприступ может иметь вторичную генерализацию, когда судороги распространяются на все мышечные группы и сопровождаются утратой сознания. Однако в большинстве случаев такие вторично-генерализованные пароксизмы наблюдаются достаточно редко. В отдельных случаях наряду с указанными типами эпиприступов имеют место психосенсорные или психомоторные пароксизмы, протекающие на фоне нарушенного сознания.
Перманентные клонические сокращения, которыми сопровождается кожевниковская эпилепсия, зарубежными авторами относятся к миоклоническим феноменам. Однако они отличаются от сокращений при миоклонус-эпилепсии большей амплитудой, приводящей к возникновению насильственных двигательных актов клонического типа. Несмотря на свой асинхронный характер, по причине постоянной локализации в одних и тех же группах мышц, такие миоклонические/клонические сокращения обуславливают стереотипность возникающего гиперкинеза. Они могут быть локального или многоочагового типа, т. е. затрагивать мышцы одной анатомической области (лица, кисти, стопы) или сразу нескольких (одновременно и лица, и руки). Клонические мышечные сокращения постоянно присутствуют у пациента, не проходят даже в период сна.
Помимо эпилептических пароксизмов и постоянных клонических феноменов, кожевниковская эпилепсия сопровождается очаговым неврологическим дефицитом в виде пареза мышц конечностей, противоположных очагу церебрального поражения. Парез носит центральный характер и сопровождается сухожильной гиперрефлексией. Зачастую после эпилептического пароксизма выраженность пареза временно усиливается. Часто наблюдаются интеллектуальное снижение и нарушения психоэмоциональной сферы (депрессия, фобические расстройства, агрессивность), может отмечаться психопатическая симптоматика.
Диагностика кожевниковской эпилепсии
Диагноз базируется на типичном клиническом симптомокомплексе, включающем простые парциальные двигательные пароксизмы, перманентные фокальные миоклонии и гемипарез. Важное значение имеет сбор анамнеза с целью выявления причины заболевания, особенно данных о перенесенном в последние полгода клещевом энцефалите. Электроэнцефалография регистрирует эпилептиформные разряды, локализующиеся в контрлатеральной судорогам области центральной борозды мозга.
Дополнительные обследования пациента направлены на диагностику причинного заболевания и могут включать биохимический анализ крови, определение сахара крови, исследование цереброспинальной жидкости, RPR-тест и др. С целью исключения интракраниального объемного образования обязательно проведение КТ, МСКТ или МРТ головного мозга. Последняя предпочтительнее у детей, поскольку не несет лучевой нагрузки. Локализация зоны поражения возможна также при помощи позитронно-эмиссионной томографии.
Лечение и прогноз кожевниковской эпилепсии
Терапия состоит из лечения основного заболевания и купирования судорожного синдрома. Она осуществляется неврологом в тесном взаимодействии с эпилептологом и по необходимости - с психиатром. При выявлении клещевого энцефалита, туберкулезного процесса, сифилиса и т. п. проводится соответствующая этиотропная терапия. Диагностирование опухоли является поводом для консультации нейрохирурга с целью решения вопроса о ее хирургическом удалении. При энцефалите Расмуссена осуществляется терапия иммуноглобулинами и глюкокортикостероидами.
Отличительной особенностью эпилепсии Кожевникова является ее резистентность к противосудорожному лечению. В связи с этим после стартовой монотерапии вальпроатами, леветирацетамом, топираматом или клоназепамом, как правило, назначают политерапию с индивидуальным подбором различных сочетаний указанных препаратов. Возможно также назначение карбамазепина в комбинации с вальпроатами. В тяжелых случаях показано оперативное лечение эпилепсии: фокальная резекция зоны эпилептогенной импульсации, таламотомия.
Наиболее часто наблюдается стабильное течение эпилепсии. Возможно прогрессирующее течение с нарастанием частоты эпиприступов, увеличением распространенности миоклоний, усугублением неврологического и когнитивного дефицита; ремиттирующее течение с наличием различных по длительности периодов относительной ремиссии. Обратное развитие симптоматики маловероятно. Некоторое улучшение на фоне проводимой терапии отмечается не более чем у четверти пациентов.
Читайте также:

