Энтеровирусная неполио инфекция у детей методические рекомендации
Обновлено: 13.05.2024
Введение
Серозные менингиты (СМ) являются распространенными формами поражения центральной нервной системы, частота которых в структуре нейроинфекций достигает 25–30% [1–4]. Среди заболевших СМ дети и подростки составляют 65–78%. В последние годы наблюдается рост заболеваемости СМ, в этиологии которых имеют значение как вирусы (энтеровирусы, герпес-вирусы, вирус лихорадки Западного Нила, ВИЧ и др.), так и бактерии (туберкулезные палочки, лептоспиры, грибы рода кандида, иерсинии, боррелии и эрлихии) [3]. Тенденции распространения заболевания по-прежнему указывают на возникновение спорадических случаев и вспышек [4]. Основу клинической картины СМ составляют общемозговые и менингеальные симптомы, выраженность которых отражает степень воспалительных и гемо-ликвородинамических нарушений. Несмотря на сравнительно благоприятное течение серозных менингитов, у реконвалесцентов в 40–60% случаев диагностируются неврологические нарушения, чаще всего в виде церебрастенического (32,2%) и невротического (12,3%) синдромов [4]. В патогенезе серозных менингитов имеет значение как синдром системного воспалительного ответа, воспаление мягких мозговых оболочек, нарушение гемо- и ликвородинамики, так и нейрометаболические изменения, степень выраженности которых зависит от тяжести менингита. В этой связи общепринятой терапевтической тактикой СМ является применение не только этиотропных препаратов, но и патогенетических средств, включающих дегидратационные, сосудистые и обязательно ноотропные препараты. В настоящее время появляются новые ноотропные препараты с комплексным механизмом действия, влияющие на различные патогенетические звенья патологического процесса. Одним из таких препаратов является нооклерин, обладающий церебропротективными свойствами с отчетливым ноотропным, психостимулирующим и психогармонизирующим действием при астенических состояниях, нарушениях памяти различного генеза [5–6].
Цель исследования – оценить терапевтическую эффективность препарата нооклерин при серозных менингитах у детей.
Материалы и методы
Проведено клинико-лабораторное обследование 50 больных с СМ в возрасте от 10 до 18 лет, проходивших лечение в Научно-исследовательском институте детских инфекций в 2012–2013 гг. Все дети поступали с подозрением на менингит на 1–2-й день заболевания. Достоверных гендерных различий выявлено не было – с одинаковой частотой болели как мальчики (52%), так и девочки (48%). У 32 (64%) пациентов была установлена энтеровирусная этиология заболевания, а 18 детей (36%) переносили серозный менингит неустановленной этиологии.
Диагноз серозного менингита выставлялся на основании данных анамнеза заболевания, клинической картины и лабораторных показателей (клинический анализ ЦСЖ и общий анализ крови). Все больные были разделены на 2 группы:
1 группа (основная группа – 35 детей) вместе с базовой терапией серозного менингита получала препарат нооклерин с 5-го дня госпитализации, доза препарата зависела от возраста пациента. Так, детям с 10 до 12 лет нооклерин назначался по 2,5 мл (0,5 г) 2 раза в день, старше 12 лет — 5,0 мл (1 г) 2 раза в день, длительность приема препарата составила 2 месяца.
2 группа (группа сравнения – 15 детей) получала только базовую терапию.
Базовая терапия серозного менингита включала противовирусные (амиксин), дегидратационные (диакарб), дезинтоксикационные препараты.
Обе группы были сопоставимы по возрасту, полу, тяжести заболевания и этиологии менингита.
Всем детям проводился мониторинг клинико-неврологических показателей в течение всего периода стационарного лечения и через 2 месяца после выписки из стационара. Оценивалась длительность основных симптомов заболевания – температуры, симптомов интоксикации, головной боли, рвоты, сохранения менингеальных симптомов, сроки санации ЦСЖ. Также проводилось этиологическое обследование для определения возбудителя, вызвавшего серозный менингит (энтеровирусы, герпес-вирусы, боррелии, вирус клещевого энцефалита) в крови и ЦСЖ методом полимеразно-цепной реакции (ПЦР), одновременно с этим в крови методом иммуноферментного анализа (ИФА) определялись иммуноглобулины (Ig) IgM и IgG к тем же возбудителям.
Качество жизни оценивали при помощи опросника PedsQL4.0. Опросник состоит из 23 вопросов и включает 4 шкалы: физическое функционирование (8 вопросов), эмоциональное функционирование (5 вопросов), социальное функционирование (5 вопросов) и жизнь в учебном заведении (5 вопросов). Общее количество баллов после процедуры перекодирования каждого из пяти вариантов ответа рассчитывается в итоге по 100-балльной шкале (от 0 до 100 баллов): чем выше итоговая величина, тем лучше качество жизни ребенка [7]. Оценка степени астении, когнитивных функций и качества жизни проводилась дважды: в день госпитализации и через 2 месяца после выписки при диспансерном осмотре. В эти же сроки проводилось ЭЭГ-обследование.
Результаты и обсуждение
Анализ течения острого периода серозного менингита в обеих группах не выявил достоверных отличий по длительности основных симптомов заболевания (рис. 1).
Рис. 1. Длительность основных клинических симптомов у больных с серозными менингитами, получавших нооклерин (группа 1), и в группе сравнения (группа 2) (р>0,05)
Однако при осмотре детей, перенесших серозный менингит, в периоде реконвалесценции через 2 месяца после выписки из стационара больные из контрольной группы достоверно более часто жаловались на эмоциональную лабильность, неустойчивость настроения, повышенную утомляемость в вечерние часы и к концу учебной недели, головные боли, возникающие после эмоциональной или умственной нагрузки, уменьшение работоспособности, чем дети, получавшие нооклерин (табл. 1).
Таблица 1
Частота предъявляемых жалоб больных из группы, получавшей нооклерин (группа 1) и группы сравнения (группа 2) через 2 месяца после выписки из стационара
| Жалобы | 1 группа (n=35) | 2 группа (n=15) | ||
| n | % | n | % | |
| Эмоциональная лабильность | 2 | 5.7±3,92* | 5 | 33,3±12,6* |
| Неустойчивость настроения | 2 | 5,7±3,92** | 7 | 46,7±13,3** |
| Нарушение сна | 1 | 2,9±2,84 | 2 | 13.3±9,08 |
| Утомляемость | 2 | 5,7±3,92* | 5 | 33,3±12,6* |
| Головная боль | – | – | 4 | 26± 11,72* |
| Уменьшение работоспособности | – | – | 6 | 40±13,09** |
| Снижение памяти | 1 | 2,9±2,84 | 3 | 20±10,69 |
Таким образом, проявления церебрастенического синдрома в группе сравнения выявлялись значительно чаще, чем у детей, получавших нооклерин.
В группе сравнения также отмечалось снижение средней балльной оценки уровня астении к моменту выписки из стационара (18,2±0,91), но она оставалась достоверно выше, чем в группе детей, получавших нооклерин, и соответствовала умеренной степени астении. В дальнейшем, при третьем обследовании через 2 месяца после выписки из стационара, она практически не изменилась и составила 17,4±2,4, что было достоверно выше, чем в основной группе.
Таким образом, проведенное тестирование больных серозными менингитами по двум шкалам для определения уровня астении в остром периоде заболевания и в катамнезе через 2 месяца после выписки в различных группах выявило достоверно более низкий уровень развития астенических проявлений у детей, получавших нооклерин, к моменту выписки из стационара, а также значительное уменьшение проявлений астении через 2 месяца приема препарата, по сравнению с группой сравнения. Полученные данные подтверждают тот факт, что нооклерин оказывает не только психостимулирующее, но и церебропротективное действие.
Наряду с оценкой уровня астении у детей, переносящих серозный менингит, нами проводилась оценка изменения качества жизни у этих пациентов (табл. 2).
Таблица 2
Оценка показателей качества жизни больных серозными менингитами, получавших нооклерин (группа 1), и в группе сравнения (группа 2) до и после лечения
| Показатели | До заболевания | Через 2 месяца после выписки | ||
| 1 группа (n=35) | 2 группа (n=15) | 1 группа (n=35) | 2 группа (n=15) | |
| ФФ | 84,29±2,15 | 86,67±4,13 | 83,71±1,5 | 81,67±5,9 |
| ЭФ | 90,21±1,85 | 87,64±2,64* | 82,96±4,2 | 66,47±3,3* |
| СФ | 92,62±0,92 | 85,85±0,69 | 90,42±1,79 | 82,92±1,16 |
| КФ | 78,08±2,44 | 79,54±1,47* | 75,25±5,54 | 53,16±3,29* |
| ПСЗ | 86,79±1,36 | 85,11±1,68* | 81,43±3,15 | 69,82±2,41* |
| ОБ | 86,3±3,7 | 85,25±3,17* | 82,75±3,17 | 71,91±1.27* |
При проведении тестирования по опроснику для родителей PedsQL версия 4.0 в день поступления в стационар оценивался исходный уровень качества жизни ребенка до заболевания серозным менингитом. При анализе полученных данных достоверных отличий по всем шкалам качества жизни у обеих групп получено не было. Было отмечено, что в обеих группах имелось некоторое снижение качества жизни по шкале когнитивного функционирования до 78,08±2,44 баллов (группа 1) и 75,25±5,54 балла (группа 2).
Таким образом, проведенное исследование выявило снижение уровня качества жизни через 2 месяца после перенесенного серозного менингита у детей, получавших только базовую терапию в остром периоде заболевания (группа 2), в то время как у детей, получавших вместе с базовой терапией серозного менингита в течение 2 месяцев нооклерин, качество жизни оставалось на первоначальном уровне.
Также нами проведен сравнительный анализ показателей ЭЭГ-обследования в группе детей, получавших нооклерин с 5-го дня лечения серозного менингита (группа 1) и в группе сравнения (группа 2). ЭЭГ-обследование проводилось дважды: в первые 2 суток поступления ребенка на лечение в стационар и через 2 месяца после выписки.
При ЭЭГ-исследовании в остром периоде серозного менингита достоверных отличий у больных основной группы и группы сравнения получено не было. В обеих группах наблюдалось общее понижение амплитуды альфа-ритма, в некоторых случаях альфа-ритм был представлен отдельными элементами на фоне полиморфной кривой; в обеих группах регистрировалась диффузная медленноволновая активность без четкого преобладания по отведениям. Спектр ЭЭГ в обеих группах был смещен в сторону тета-диапазона.
При повторном исследовании через 2 месяца после выписки из стационара в группе детей, получавших нооклерин (группа 1), в 37,2% случаев (n=13) наблюдалась картина ЭЭГ, соответствующая возрастной норме, в 40% (n=14) отмечались легкие признаки дезорганизации основной активности: умеренное понижение амплитуды альфа-ритма, периодическое проведение альфа-ритма в лобные отведения, отдельные медленные волны без четкого преобладания по отведениям. В 22,8% случаев (n=8) регистрировались признаки средней степени выраженности дезорганизации основной активности (постоянное проведение альфа-ритма в лобные отведения, средней степени выраженности понижение его амплитуды, медленноволновая активность с формированием редких (1–2 за все время записи) билатерально-синхронных вспышек).
Рис. 4. Частота (%) изменения ЭЭГ-показателей у больных серозными менингитами, получавших нооклерин (группа 1), и в группе сравнения (группа 2) при обследовании через 2 месяца после выписки из стационара
Таким образом, данные, полученные при ЭЭГ-обследовании в остром периоде заболевания и в катамнезе через 2 месяца после выписки из стационара полностью коррелируют с клиническими наблюдениями и данными, полученными при анкетировании больных. Не исключено, что нооклерин как препарат, по своей химической структуре близкий к естественным веществам, оптимизирующим деятельность мозга (гамма-аминомасляная и глутаминовая кислоты), при применении у детей, больных серозными менингитами, облегчая процесс передачи нервного импульса, улучшая фиксацию, консолидацию и воспроизведение памятных следов, стимулируя процессы тканевого обмена, способствует оптимизации нейрометаболических процессов, что предупреждает формирование органического дефицита. Применение нооклерина в комплексной терапии серозных менингитов сглаживает межполушарные различия в функционировании головного мозга, что также способствует протекции развития симптоматической эпилепсии в периоде поздней реконвалесценции.
Заключение
Полученные данные клинического наблюдения за больными с серозным менингитом, проведенное тестирование для определения уровня астении и качества жизни, ЭЭГ-обследование в остром периоде заболевания и в катамнезе в течение 2 месяцев у больных, получавших нооклерин и в группе сравнения, показали терапевтическую эффективность нооклерина, а также подтвердили его психостимулирующие, нейрометаболическое и церебропротективное действие. Переносимость препарата у детей хорошая. Побочных эффектов выявлено не было. В связи с этим препарат нооклерин может быть включен в стандарт оказания помощи детям, переносящим серозный менингит для профилактики и лечения постинфекционной астении для улучшения исходов заболевания.
Литература
- Лобзин, Ю.В. Энтеровирусные инфекции / Ю.В. Лобзин, Н.В. Скрипченко, Е.А. Мурина. – СПб., 2012. – 432 с.
- Михайлова, Е.В. Менингиты энтеровирусной этиологии у детей: современные подходы к диагностике и особенности клинического течения / Е.В. Михайлова, А.В. Штейнберг, И.Г. Еремеева // Инфекционные болезни. – 2008. – № 6 (1). – С. 31–34.
- Скрипченко, Н.В. Вирусные энцефалиты и менингиты у детей / Н.В. Скрипченко, М.Н. Сорокина. – М.: Медицина, 2004. – 415 с.
- Скрипченко, Н.В. Энтеровирусная (неполио) инфекция у детей : методические рекомендации / Н.В. Скрипченко [и др.]. – СПб.: – 2013. – 18 с.
- Аведисова, А.С. Новый отечественный препарат нооклерин в терапии астении и других заболеваний / А.С. Аведисова // Фармотека. – 2005. – № 6. – С. 51–54.
- Александровский, Ю.А. Применение препарата нооклерин в качестве антиастенического средства у больных с функциональной астенией / Ю.А. Александровский, А.С. Аведисова, Д.В. Ястребов // Психиатрия и психофармакотерапия. – 2003. – № 6. – С. 51–54.
- Лукьянова, Е.М. Оценка качества жизни в педиатрии /Е.М. Лукьянова // Качественная клиническая практика. – 2002. – № 4. – С. 34–42 References
References
- Lobzin Yu.V., Skripchenko, N.V., Murina E.A. Enteroviral infection, S-Pb., 2012/ – 432 p.
- Mixailova E.V., Shteinberg A.V., Eremeeva I.G. Infechionnie bolezni – 2008. – 6 (1). – P. 31–34.
- Skripchenko, N.V., Sorokina M.N. Viral encephalitis and meningitis inchildren. Moscow: Medicine, 2004. –415p.
- Shteinberg A.V., Ivanova G.P. et al Methodological guidelines – S-Pb.: – 2013. – 18 p.
- Avedisova A.S. Pharmoteka. – 2005. – №6. – P. 51-54
- Aleksandrovski Yu.A., Avedisova A.S., Yastrebov D.V. Psixiatriya i psixofarmakoterapiya. – 2003. – №6. –P . 51–54
- Lukianova E.M. Kachestvennaia klinicheskaia praktika. – 2002. – №4. – P. 34-42.
Авторский коллектив:
Иванова Марина Витальевна – старший научный сотрудник отдела нейроинфекций и органической патологии нервной системы Научно-исследовательского института детских инфекций ФМБА России, к.м.н.
Скрипченко Наталья Викторовна – заместитель директора по научной работе Научно-исследовательского института детских инфекций ФМБА России, д.м.н., профессор
Матюнина Наталья Викторовна – младший научный сотрудник отдела нейроинфекций и органической патологии нервной системы Научно-исследовательского института детских инфекций ФМБА России
Вильниц Алла Ароновна – старший научный сотрудник отдела нейроинфекций и органической патологии нервной системы Научно-исследовательского института детских инфекций ФМБА России, к.м.н.
Войтенков Владислав Борисович – заведующий отделением функциональных методов диагностики, исполняющий обязанности руководителя отдела функциональной и лучевой диагностики Научно-исследовательского института детских инфекций ФМБА России
Категории МКБ: Другие уточненные инфекции, характеризующиеся поражением кожи и слизистых оболочек (B08.8), Энтеровирусная инфекция неуточненная (B34.1), Энтеровирусная экзантематозная лихорадка [бостонская экзантема] (A88.0), Энтеровирусный везикулярный стоматит с экзантемой (B08.4), Энтеровирусный везикулярный фарингит (B08.5)
Общая информация
Краткое описание
Энтеровирусные инфекции (Enterovirosis) – группа антропонозных острых инфекционных заболеваний, вызываемых энтеровирусами, характеризующихся лихорадкой и полиморфизмом клинической картины (с преимущественным поражением ЦНС, сердечно-сосудистой системы, желудочно-кишечного тракта, мышечной системы, слизистых оболочек и кожи).
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| А85.0 | Энтеровирусный энцефалит, энтеровирусный энцефаломиелит |
| А87.0 | Энтеровирусный менингит; менингит, вызванный вирусом Коксаки/менингит, вызванный ЕСНО-вирусом |
| А88.0 | Энтеровирусная экзантематозная лихорадка (бостонская экзантема) |
| В08.4 | Энтеровирусный везикулярный стоматит с экзантемой, вирусная пузырчатка полости рта и конечностей |
| В08.5 | Энтеровирусный везикулярный фарингит, герпетическая ангина |
| В08.8 | Другие уточнённые инфекции, характеризующиеся поражением кожи и слизистых оболочек; энтеровирусный лимфонодулярный фарингит |
| В34.1 | Энтеровирусная инфекция неуточнённая; инфекция, вызванная вирусом Коксаки, БДУ; инфекция, вызванная ЕСНО-вирусом, БДУ |
Дата разработки протокола: 2017 год.
Сокращения, используемые в протоколе:
| АД | артериальное давление |
| ДВС | диссеминированное внутрисосудистое свертывание |
| ИВЛ | искусственная вентиляция легких |
| ИТШ | инфекционно-токсический шок |
| ИФА | иммуноферментный анализ |
| КТ | компьютерная томография |
| МРТ | магнитно-резонансная томография |
| МКБ | международная классификация болезней |
| ОАК | общий анализ крови |
| ОАМ | общий анализ мочи |
| ОПП | острое повреждение почек |
| ОРИТ | отделение реанимации и интенсивной терапии |
| ПЦР | полимеразная цепная реакция |
| РНК | рибонуклеиновая кислота |
| РН | реакция нейтрализации |
| РНГА | реакция непрямой гемагглютинации |
| РСК | реакция связывания комплемента |
| СЗП | свежезамороженная плазма |
| СМЖ | спинномозговая жидкость |
| СОЭ | скорость оседания эритроцитов |
| УЗИ | ультразвуковое исследование |
| ЦНС | центральная нервная система |
| ЭВИ | энтеровирусная инфекция |
| ЭКГ | электрокардиография |
| ЭхоКГ | эхокардиография |
| ЭЭГ | электроэнцефалография |
Пользователи протокола: врачи скорой неотложной помощи, фельдшеры, врачи общей практики, инфекционисты, терапевты, невропатологи, офтальмологи, дерматовенерологи, оториноларингологи, хирурги, анестезиологи-реаниматологи, организаторы здравоохранения.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
Классификация
Классификация [1,2]
В зависимости от выраженности клиническ
их проявлений:
· бессимптомная (доклиническая);
· манифестная (клиническая);
В зависимости от тяжести течения:
· легкая;
· среднетяжелая;
· тяжелая.
Критерии тяжести:
- выраженность синдрома интоксикации;
- выраженность местных изменений;
В зависимости от течения:
· острое гладкое;
· с осложнениями;
· рецидивирующее.
В зависимости от наличия осложнений:
· неосложненная форма;
· осложненная форма (с указанием осложнения):
− пневмония;
− острый респираторный дистресс-синдром;
− отек-набухание головного мозга;
− судорожный синдром;
− гиповолемический шок;
− острое почечное повреждение;
− другие.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ 6
Диагностические критерии 5
Жалобы на момент осмотра и\или в анамнезе:
Бессимптомная (доклиническая) стадия: активно жалоб не предъявляет.
Клиническая стадия (неосложненная): жалобы и клинические проявления зависят от формы заболевания. Нередко наблюдаются сочетанные признаки различных клинических форм.
Наиболее частые клинические проявления ЭВИ:
· Острое начало;
· Лихорадка (до 38 - 40ͦ С);
· Головная боль;
· Слабость, недомогание;
· Головокружение;
· Тошнота, рвота;
· Гиперемия зева;
· Зернистость задней стенки глотки;
· Гиперемия лица, шеи, верхней половины туловища;
· Сыпь на лице, туловище, конечностях (в том числе, ладонях и стопах);
· Энантема на слизистой полости рта;
· Инъекция сосудов склер.
Энтеровирусная инфекция и беременность 15:
Новорожденный может инфицироваться внутриутробно, но чаще — во время родов или сразу после них. Результат зависит от вирулентности конкретного циркулирующего серотипа, способа передачи инфекции и наличия или отсутствия пассивно передаваемых материнских антител.
Перенесенная инфекция Коксаки во время беременности может вызывать врожденные пороки развития сердечно-сосудистой (тетрада Фалло, атрезия аорты, атрезия трикуспидального клапана), мочеполовой и пищеварительной систем у новорожденного. Энтеровирус может быть причиной развития тяжелой инфекции центральной нервной системы у новорожденных.
Лабораторные исследования [1,2,6,13,14,17]:
Основные:
· ОАК: лейкопения, лейкоцитоз, относительный лимфоцитоз, моноцитоз, умеренное повышение СОЭ.
· ОАМ: протеинурия, цилиндрурия, микрогематурия (при токсическом поражении почек).
· ИФА или РПГА – используются парные сыворотки, полученные с интервалом в 10–12 дней (первая на 4–5-й день болезни, вторая – после 14-го дня болезни). Диагностический критерий – нарастание титра антител в 4 раза и более.
· ПЦР фекалий (носоглоточной слизи) на Enterovirus: детекция РНК Enterovirus.
· исследование СМЖ (при менингите):
- цвет – ликвор прозрачный, или слегка опалесцирующий;
- давление – жидкость вытекает струей или частыми каплями;
- лимфоцитарный плеоцитоз;
- повышение белка до 1-4,5 г/л (наиболее высокое - при развитии менингоэнцефалита);
- сахар в норме;
- снижение хлоридов.
Дополнительные:
· иммунохроматографический тест фекалий на энтеровирус;
· тест Xpert EV на энтеровирус в образцах СМЖ у пациентов с симптомами менингита (на основе ПЦР-анализа).
Инструментальные методы диагностики – проводятся по показаниям (при развитии осложнений):
· ЭКГ: признаки миокардита;
· рентгенография органов грудной клетки: признаки пневмонии;
· КТ и МРТ головного мозга: отек головного мозга, признаки менингоэнцефалита, дисциркуляторная энцефалопатия;
· УЗИ: оценка размеров печени и селезенки;
· ЭхоКГ: признаки миокардита, эндокардита, сердечной недостаточности;
· ЭЭГ: признаки судорожной активности, гибели мозга при энцефалите.
Показания для консультации специалистов:
Показания к консультации других специалистов определяет форма инфекции:
· консультация хирурга – при эпидемической миалгии;
· консультация офтальмолога – при эпидемическом геморрагическом конъюнктивите;
· консультация кардиолога – при перикардитах и миокардитах;
· консультация невропатолога – при менингите и менингоэнцефалитической форме энтеровирусной инфекции;
· консультация пульмонолога – при развитии пневмонии и бронхитов;
· консультация дерматолога – при поражении кожных покровов;
· консультация реаниматолога – для определения показаний перевода в ОРИТ.

Диагностический алгоритм: (схема)
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований [1,2,5-12,17]
| Заболевание | Сходные симптомы | Отличительные симптомы | Лабораторные тесты |
| Инфекционный мононуклеоз | Лимфоаденопатия, ангина, гепатолиенальный синдром, лихорадка | Длительность не более 1 мес., преобладает системное увеличение лимфоузлов. | Положительный тест Пауля-Буннеля. В крови атипичные мононуклеары более 10%. |
| Краснуха | Увеличение затылочных лимфоузлов, экзантема | Эпиданамнез, кратковременность симптомов, поражаются только затылочные лимфоузлы. | Антитела к вирусу краснухи в нарастающем титре. |
| Токсоплазмоз | Энцефалит, лимфоаденопатия, гепатомегалия, желтуха, экзантема. | Эпиданамнез, хориоретинит, кальцификаты в головном мозге, висцеральные поражения. | Бактериология, серология, РСК, РНИФ, кожная проба |
| Острый менингоэнцефалит (вирусной, бактериальной этиологии). | Менингеальный, энцефалический синдром, полиомиелитоподобный синдром | Эпиданамнез, более четко очерчена клиническая картина, при бактериальных неменингококковых менингитах — наличие очагов инфекции. | Микробиология, серология, вирусология, иммунофлюоресцентный метод диагностики |
| Аденовирусная инфекция | Лихорадка, назофарингит, лимфаденит | Эпиданамнез, острое течение, лимфаденит преимущественно регионарных лимфоузлов | Вирусология, серология с нарастанием титра АТ, иммунофлюоресцентное исследование, гемограмма. |
| Энтеровирусная инфекция | Лихорадка, экзантема, полиадения, гепатолиенальный синдром, энцефалит. | Герпангина, диарея, лимфаденит менее выражен. | Серология в нарастающем титре. |
| Сепсис | Лихорадка, интоксикация, полиорганность проявлений, экзантема, менингит, отит, синусит, пневмонии. | Наличие первичного очага (кожа, легкие, кишечник и др.) | Выделение возбудителя из крови и др. материала, отрицательный тест на ВИЧ-АТ, гипогаммаглобулинемия, нормальное количество СД-4. |
| Хронический вирусный гепатит | Снижение аппетита, увеличение печени, селезенки, полиадения, желтуха. | Связь с перенесенным вирусным гепатитом, симптоматика выражена умеренно, полиорганность не характерна. | Маркеры ВГ (А, В, С, Д) в сыворотке крови, снижение СД-8, уровень СД-4 нормальный. |
| Кишечная инфекция, сальмонеллез (генерализованная форма). | Диарея, потеря массы, лихорадка, интоксикация, наличие очагов в других органах (менингит, пневмония) | Генерализованные формы развиваются только у детей первых месяцев жизни Преморбидный фон отягощен, чаще внутрибольничная инфекция | Посевы кала, крови, серология (РПГА) |
| Глистные инвазии. | Снижение аппетита, вялость, снижение массы тела, диарея, полиадения. | Эпидемиология, синдром мальабсорбции не характерен. | Обнаружение личинок гельминтов в кале, дуоденальном содержимом, мокроте, моче. |
| Туберкулез | Полиадения, интоксикация, поражение легких, ЦНС, лихорадка, потеря массы тела, слабость, гепатолиенальный синдром. | Эпиданамнез, наличие первичного комплекса в легких | Бактериология — выделение БК из мокроты, Rg- исследование легких (очаги, каверны). Туберкулиновые пробы. |
| Эпидемический паротит и паротиты другой этиологии. | Увеличение околоушных слюнных желез. | При эпидпаротите: возникает остро, проходит в течении 10 дней, могут вовлекаться другие слюнные железы, орхиты, панкреатиты. При опухоли, слюннокаменной болезни — процесс односторонний. | Серологические исследования с нарастанием титра антител (РНГА). Rg - логические методы исследования. |
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Серозный менингит и менингоэнцефалитическая форма энтеровирусной инфекции | Паротитная инфекция Туберкулезный менингит Менингококковая инфекция Пневмококковый менингит Hib менингит | Паротит, панкреатит, орхит Бак.исследование крови, ликвора, мокроты на TBC, Бак.исследование мазка из зева, ликвора, крови на менингококк, пневмококк, гемофильную палочку | -ИФА (IgM) -ПЦР фекалий |
| Эпидемическая миалгия | Острая хирургическая патология Плеврит Стенокардия | Консультация хирурга Рентгенография легких ЭКГ | -РН, РСК, РТГА и реакция преципитации в геле с энтеровирусным антигеном -ПЦР крови, ликвора -вирусологическое исследование носоглоточной слизи, СМЖ, фекалий, крови |
| Полиомиелитоподобная форма энтеровирусной инфекции | Полиомиелит | Вирусологическое исследование крови, кала | -РН, РСК, РТГА и реакция преципитации в геле с энтеровирусным антигеном -ПЦР крови, ликвора -вирусологическое исследование носоглоточной слизи, СМЖ, фекалий, крови |
| Энтеровирусная экзантема | Скарлатина Корь Краснуха Аллергия | Этапность высыпаний, характер и локализация экзантемы | -РН, РСК, РТГА и реакция преципитации в геле с энтеровирусным антигеном -ПЦР крови, ликвора -вирусологическое исследование носоглоточной слизи, СМЖ, фекалий, крови |
| Герпангина | Афтозный стоматит | -РН, РСК, РТГА и реакция преципитации в геле с энтеровирусным антигеном -ПЦР крови, ликвора -вирусологическое исследование носоглоточной слизи, СМЖ, фекалий, крови | |
| Энтеровирусная диарея | Острые диарейные инфекции | Бак.исследованиекала на патогенную флору | -РН, РСК, РТГА и реакция преципитации в геле с энтеровирусным антигеном -ПЦР крови, ликвора -вирусологическое исследование носоглоточной слизи, СМЖ, фекалий, крови |
Алгоритм дифференциального диагноза серозных менингитов:
Ключевые слова: энтеровирусная инфекция, энтеровирусы, вирусоносительство, бессимптомные формы, полиомиелитоподобные формы, серозный менингит, энерготропная терапия, L-карнитин, Элькар ®
Keywords: enterovirus infection, enteroviruses, carriage of viruses, asymptomatic forms, poliomyelitis-like forms, serous meningitis, energotropic therapy, L-carnitine, Elkar ®
Введение
Актуальность энтеровирусной инфекции (ЭВИ) связана с ее клиническим полиморфизмом, повсеместной распространенностью, широтой и массовостью поражения энтеровирусами (ЭВ) населения, склонностью к вспышечному характеру заболевания.
Особенностью ЭВИ является поражение центральной нервной системы (ЦНС) с развитием полиомиелитоподобных форм. Установлено, что от 18 до 31% случаев поражения ЦНС у детей раннего возраста связано с внутриутробным инфицированием ЭВ [1]. Способность ЭВ к персистенции с формированием аутоиммунного процесса может приводить к гибели плода, самопроизвольным выкидышам и заболеваниям новорожденных.
Для ЭВИ характерна высокая генетическая изменчивость с образованием новых высокопатогенных штаммов и отсутствием стойкого иммунитета. Не менее важным фактором считается способность ЭВ запускать аутоиммунные механизмы с поражением паренхиматозных органов, что зачастую приводит к хронизации процесса [2, 3].
Отсутствие этиотропной терапии ЭВИ и вакцинопрофилактики этой инфекции побуждает к поискам методов патогенетической терапии и ее обоснованию.
Эпидемиология
Энтеровирусы являются одними из самых распространенных патогенов человека. Во всем мире они ежегодно вызывают почти миллиард инфекций у людей [1]. В то же время продолжают появляться все новые серотипы ЭВ, некоторые из которых, как полагают ученые, получены людьми от других приматов [4]. Вследствие высокой генетической изменчивости ЭВ в последние годы обнаружены их новые высокопатогенные штаммы (А71 и D68) [4, 5], вызываемая ими инфекция протекает с респираторными и неврологическими симптомами и характеризуется тенденцией к вспышкам и высокой летальности [1, 4, 6].
По данным литературы, заболеваемость ЭВ типа A71 связана со вспышками hand, foot and mouth disease и редкими поражениями ЦНС в виде энцефалита с поражением ствола мозга. Данные вспышки регистрировались главным образом в Азиатско-Тихоокеанском регионе. В странах Азии также наблюдалась значительная распространенность ЭВ, а именно Коксаки А16 [7]. Выявление ЭВ серотипа D68 связано с развитием респираторных проявлений и дебютом острых вялых параличей в Северной Америке, Европе и Азии в последние 5 лет [8, 9]. В последние годы тяжелые формы заболеваний, вызванных ЭВ типов A71 и D68, регистрировались и в ряде европейских стран [10].
На рисунке представлены данные о заболеваемости детей ЭВИ в целом и заболеваемости серозным менингитом как одной из форм ЭВИ у детей в РФ. Согласно этим данным рост заболеваемости детей ЭВИ не имеет тенденции к снижению. Наоборот, за последние годы, а именно с 2015 по 2019 г., заболеваемость ЭВИ увеличилась почти в 2 раза. Заболеваемость серозным менингитом энтеровирусной этиологии также остается на стабильно высоком уровне.
По эпидемиологическим данным, ЭВИ имеет летне-осеннюю сезонность, хотя спорадические случаи в отдельных регионах России встречаются круглогодично, а максимальная заболеваемость данной инфекцией чаще регистрируется в августе-сентябре [2].
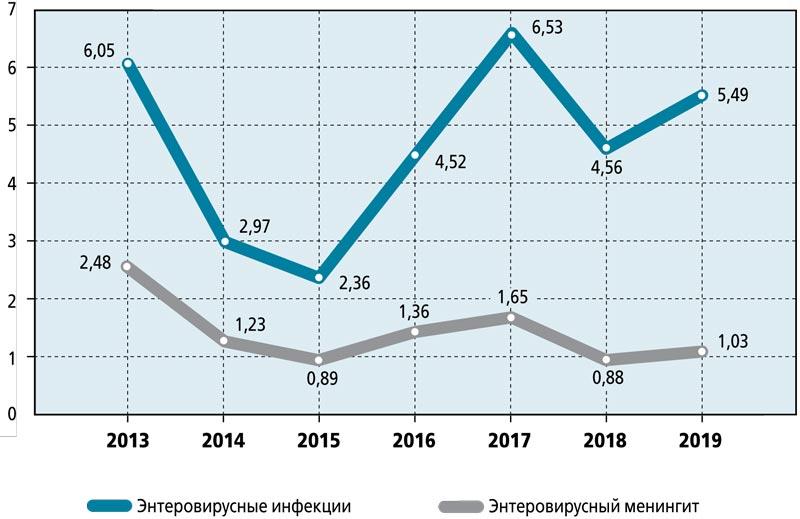
Показатели заболеваемости энтеровирусной (неполио) инфекцией за 2013-2019 гг. по РФ (на 100 тыс. населения)
Этиологическая характеристика энтеровирусов
ЭВ представляют собой род вирусов из семейства пикорнавирусов (Picornaviridae), порядок Picornavirales.
Согласно современной таксономии, основанной на геномных и биологических свойствах вирусов, ЭВ делятся на 15 видов, из которых ЭВ видов А-D и риновирусы видов A-C заражают человека [3, 5]. Это одна из самых многочисленных групп вирусов, включающая полиовирус, неполиомиелитные энтеровирусы, вирус гепатита А и риновирусы A, B, C.
Семейство характеризуется икосаэдрической симметрией капсида и одноцепочечной + РНК как носителя наследственной информации [1, 5]. Название ЭВ связано с их репродукцией в желудочно-кишечном тракте, однако энтерит они вызывают редко.
Клиническая картина
В классификации ЭВИ выделяют типичные и атипичные формы. Клиническая классификация представлена в таблице.
Клиническая классификация форм энтеровирусной инфекции
Клиническая картина ЭВИ характеризуется полиморфизмом симптомов – от 3- и 5-дневной лихорадки, респираторных поражений дыхательной системы, экзантемных форм до более грозных проявлений, паралитических полиомиелитоподобных форм. Инкубационный период длится от 2 до 35 дней, в среднем 7-10 дней.
ЭВИ может протекать в виде поражения дыхательной системы – герпангины, ринита, фарингита, бронхита, бронхиолита, пневмонии, вплоть до отека легких. Эти клинические формы составляют до 30% всех случаев ЭВИ у детей [4]. Экзантемные формы, варианты с формированием серозного менингита и паралитические полиомиелитоподобные формы ЭВИ встречаются значительно реже.
Тем не менее дети младше 5 лет подвержены тяжелым формам с развитием неврологических осложнений, таких как асептический мозжечковый менингит, мозжечковый энцефалит, острый вялый паралич. Развитие данных неврологических и респираторных форм чаще вызвано ЭВ типа A71 и D68.
Одна из форм ЭВИ – серозно-вирусный менингит. В большинстве случаев асептический серозный менингит протекает классически и характеризуется острым началом, выраженной головной болью, рвотой и симптомами интоксикации. Менингеальный синдром носит непостоянный характер и отличается диссоциацией менингеальных симптомов.
У новорожденных и детей грудного возраста асептический серозный менингит развивается как составляющая тяжелого системного поражения, включающего некроз печени, миокардит, некротизирующий энтероколит, внутрисосудистую коагуляцию. Менингеальные симптомы могут быть стертыми. Летальный исход у детей этого возраста является не следствием поражения ЦНС, а результатом острой печеночной недостаточности (вирусы ЕСНО) или миокардита (вирусы Коксаки).
После воспалительных форм ЦНС формируются резидуальные явления. Данные изменения наблюдаются в подростковом периоде и характеризуются проявлением таких форм, как цереброастенический синдром, неврозоподобные расстройства, гипертензионный синдром.
В отечественной литературе практически отсутствуют сведения о редких проявлениях ЭВИ, поражении ЭВ сердечно-сосудистой системы, желчного пузыря и почек.
В 50% случаев выявлена взаимосвязь с тропностью ЭВ к кардиомиоцитам и развитием дилатационной кардиомиопатии у детей [8]. Данная инфекция способствуют развитию кардиомиопатии двумя различными способами. При первом типе поражения ЭВ могут непосредственно инфицировать и индуцировать гибель клеток кардиомиоцитов. Во втором же случае ЭВ вызывают аутоиммунный ответ, при котором собственная иммунная система хозяина разрушает кардиомиоциты (стадия апоптоза) и приводит к формированию кардиомиопатии.
Изучая данные литературы, мы также обнаружили связь ЭВ Коксаки B4 с развитием сахарного диабета I типа. Вирус Коксаки В4 выступает триггером в развитии патологического процесса в поджелудочной железе [4, 8], вызывая апоптоз ^-клеток и гипогликемию в экспериментальных исследованиях. Таким образом, подтверждается тот факт, что ЭВ могут вызывать поражение поджелудочной железы с последующим развитием гипо- или гипергликемии.
Вопросы диагностики и терапии
Лабораторная диагностика ЭВИ осложняется большим количеством серотипов возбудителей, поэтому наряду с классическими вирусологическими методами в диагностике используют молекулярно-биологические методы, позволяющие секвенировать геном возбудителя и определить филогенетические связи между различными штаммами ЭВ [2]. Тип ЭВ может быть определен с использованием молекулярного типирования (генотипирования), которое основано на определении нуклеотидной последовательности области генома, кодирующей капсидный белок VP1. Полипептид VP1 содержит аминокислотные последовательности, определяющие серотип вируса, и является главным рецепторным локусом вириона. Определение типа ЭВ проводят путем секвенирования фрагментов области генома, кодирующей белки капсида VP3 и VP1. Молекулярное типирование ЭВ с использованием амплификации и секвенирования нуклеотидных последовательностей региона VP1 является прямым методом идентификации, обладает высокими показателями специфичности [11].
Диагноз ЭВИ и ее форм базируется в основном на клинической симптоматике и эпидемиологических данных.
Патогенетическая и симптоматическая терапия ЭВИ проводится с учетом клинической формы и основана на восстановлении метаболизма и энергетического потенциала поврежденных клеток. На этом фоне при развитии неврологической симптоматики в периоде реконвалесценции, особенно после серозно-вирусного менингита, может быть рекомендована метаболическая терапия [12], коррекция вегетативных расстройств, ассоциированных с синдромом вегетативной дистонии.
В основе патогенеза синдрома вегетативной дистонии лежит дезинтеграция высших вегетативных центров, нарушение равновесия между симпатическим и парасимпатическими отделами, расстройство взаимодействия различных органов и систем организма, метаболических процессов, что отражается на развитии адаптационно-компенсаторных реакций, формировании энергетического обмена [13].
В многочисленных исследованиях было показано, что нарушения энергетического обмена выявлены у детей с перинатальной патологией, урологическими и нефрологическими заболеваниями, острыми респираторными инфекциями [12, 14-17]. При всех отмеченных патологических состояниях целесообразно применение энерготропных препаратов.
В современной литературе имеются данные об использовании препаратов L-карнитина у детей и подростков при вегетативных расстройствах [13] и при всех указанных выше патологических состояниях и заболеваниях.
Карнитин улучшает белковый и жировой обмен, повышает секрецию и ферментативную активность желудочного и кишечного соков, способствует усвоению пищи, снижает избыточную массу тела. Участвует в транспорте ксенобиотиков и органических кислот из клетки, усиливает процесс детоксикации, позволяя устранить последствия интоксикации организма.
Элькар ® улучшает обмен веществ, непосредственно влияет на обеспечение клеток организма энергией, тем самым способствуя нормализации клеточного энергообмена, коррекции метаболических нарушений.
Важным направлением реабилитации детей после перенесенных вирусных инфекций является назначение препаратов на основе L-карнитина в связи с уникальностью его воздействия на клеточный метаболизм [18, 19]. Необходимость включения Элькара в патогенетическую терапию при инфекционных заболеваниях у детей отмечена в исследовании Т.А. Руженцовой [17]: вирусные агенты, в том числе и ЭВ [8], способны не только длительно персистировать в организме, находясь в латентном состоянии, и активизироваться на фоне ослабления иммунитета при присоединении интеркуррентной инфекции, но и вызывать поражение миокарда, что зачастую бывает сложно связать с первоначальным этиологическим фактором [17].
В работах О.В. Гончаровой показано, что включение в реабилитацию детей с острыми респираторными инфекциями препарата Элькар ® в возрастных дозах курсами длительностью 1-1,5 мес предупреждает развитие повторных эпизодов острых респираторных инфекций у детей и сокращает длительность их течения, восстанавливая активность иммунных клеток [14]. Кроме того, в литературе представлены данные об эффективности применения Элькара в дозе 30-50 мг/кг/сут в 2-3 приема курсами 1-1,5 мес при гипоксических состояниях у детей с перинатальной патологией [12]. Такая коррекция патологических процессов возможна и в периоде реконвалесценции серозных менингитов. Курсы необходимо повторять 2 раза в год в течение 3 лет.
Элькар ® незаменим для восстановления детей после болезни. Он улучшает энергообеспечение органов и тканей, повышает аппетит и усвоение белков, помогает организму работать на полную мощность, являясь естественным эндогенным метаболитом живого организма, принимая участие во всех видах обмена веществ, в регуляции энергетических и пластических процессов.
Элькар ® эффективно восполняет потребность организма в L-карнитине, когда организму необходима энергетическая поддержка.
Заключение
Значительный полиморфизм клинических проявлений ЭВИ с отсутствием четкой зависимости от серологического типа возбудителя, большая частота бессимптомных форм, длительное вирусоносительство, отсутствие специфических методов профилактики делают ЭВИ неуправляемой болезнью. Глубокое знание клинической симптоматики, своевременность постановки диагноза, а также принятые меры профилактики способствуют снижению частоты осложненных и тяжелых форм ЭВИ.
Энтеровирусы ассоциируются со многими заболеваниями, этиология которых ранее не связывалась с инфекционными факторами, – это кардиомиопатии, нефриты, сахарный диабет, васкулиты, бесплодие.
Таким образом, хотя большинство энтеровирусных инфекций и являются бессимптомными (90% случаев), эти энтеровирусы ответственны за различные инфекционные синдромы. Прогноз их развития зависит от инфекционной дозы, органа-мишени, возраста, пола, иммунного статуса пациента, проводимой патогенетической терапии и реабилитации.
Энтеровирусные (неполио) инфекции (ЭВИ) - группа острых инфекционных заболеваний вирусной этиологии, вызываемых различными представителями энтеровирусов.
Основными возбудителями ЭВИ являются вирусы Коксаки A (24 серотипа), Коксаки B (6 серотипов), ECHO (34 серотипа) и неклассифицированные энтеровирусы человека 68 - 71 типов.
Энтеровирусы отличаются высокой устойчивостью во внешней среде, способны сохранять жизнеспособность в воде поверхностных водоемов и влажной почве до 2-х месяцев.
Источником инфекции является человек (больной или носитель).
Инкубационный период составляет в среднем от 1 до 10 дней. Среди заболевших ЭВИ преобладают дети.

ЭВИ свойственна высокая контагиозность для неиммунных лиц.
Передача ЭВИ осуществляется при реализации фекально-орального (водным, пищевым и контактно-бытовым путями) и аэрозольного (воздушно-капельным и пылевым путями) механизмов
ЭВИ распространена повсеместно. Заболевание встречается в виде спорадических случаев, локальных вспышек (чаще в детских коллективах), эпидемий.
Причиной формирования локальных очагов с групповой заболеваемостью может являться занос инфекции в учреждение, на территорию и возможность ее распространения в условиях несоблюдения требований санитарного законодательства как по условиям размещения, так и по состоянию систем водопользования и организации питания.
Эпидемиологическую значимость представляет вода открытых водоемов, загрязненная сточными водами, как в качестве источников питьевого водоснабжения, так и используемая в качестве рекреационных зон для купания населения.
Наблюдается преимущественно, летне-осенняя сезонность заболеваемости ЭВИ. Локальные вспышки ЭВИ могут регистрироваться в течение всего года, часто - вне зависимости от сезонного эпидемического подъема заболеваемости.
Медицинскому наблюдению подлежат:
- контактные с больными ЭВИ в организованных коллективах детей (детские образовательные организации, летние оздоровительные учреждения, санатории и другие), на предприятиях пищевой промышленности и приравненных к ним объектах водоснабжения;
- контактные из домашних очагов: дети дошкольного возраста и взрослые из категории лиц, работающих в учреждениях, организациях, характер деятельности которых связан с производством, транспортированием и реализацией пищевых продуктов и питьевой воды, с воспитанием и обучением детей, обслуживанием больных, с коммунальным и бытовым обслуживанием населения.
Медицинское наблюдение за контактными осуществляется ежедневно с внесением результатов осмотра в соответствующие медицинские документы (листы наблюдений).
Длительность медицинского наблюдения за контактными в очаге с момента изоляции последнего заболевшего ЭВИ составляет:
- 10 дней - при регистрации легких форм ЭВИ (при отсутствии явных признаков поражения нервной системы): энтеровирусная лихорадка, эпидемическая миалгия, герпетическая ангина и другие;
- 20 дней - при регистрации форм ЭВИ с поражением нервной системы.
После изоляции больного ЭВИ (или лица с подозрением на это заболевание) в детском организованном коллективе проводятся ограничительные мероприятия:
- в течение 10 дней - при регистрации легких форм ЭВИ (без признаков поражения нервной системы);
- в течение 20 дней - при регистрации форм ЭВИ с поражением нервной системы.
Ограничительные мероприятия это:
- запрещение участия карантинной группы в общих культурно-массовых мероприятиях детской организации;
- организация прогулок карантинной группы с соблюдением принципа групповой изоляции на участке и при возвращении в группу;
- соблюдение принципа изоляции детей карантинной группы при организации питания.
Организация дезинфекции в очагах ЭВИ
Текущая дезинфекция в домашнем очаге проводится членами семьи, в организованных коллективах - сотрудниками учреждения после проведенного медицинскими работниками инструктажа.
Заключительная дезинфекция проводится организациями, осуществляющими дезинфекционную деятельность в установленном порядке.
Текущая и заключительная дезинфекции проводятся с использованием дезинфекционных средств, разрешенных к применению в установленном порядке и обладающих вирулицидными свойствами, - в соответствии с инструкцией/методическими указаниями по их применению.

Постановление Главного государственного санитарного врача РФ от 27.07.2011 N 106 "Об утверждении СП 3.1.2950-11 "Профилактика энтеровирусной (неполио) инфекции"
Энтеровирусная инфекция – что это?
Энтеровирусные (неполио) инфекции - группа острых инфекционных заболеваний, вызываемых различными представителями энтеровирусов.

Основные возбудители:
- Коксаки A (24 серотипа),
- Коксаки B (6 серотипов),
- ECHO (34 серотипа)
- неклассифицированные энтеровирусы человека 68 - 71 типов.
Энтеровирус – это опасно?

Большинство энтеровирусных инфекций протекают легко. Но некоторые штаммы могут вызывать более тяжелые заболевания, особенно у маленьких детей.
Как происходит заражение?

Источник инфекции – человек (больной или носитель).
Заражение происходит воздушно-капельным путем, через пыль, а также водным, пищевым и контактно-бытовым путями.
Вода открытых водоемов, загрязненная сточными водами, как в качестве источников питьевого водоснабжения, так и используемая в качестве зон для купания населения - наиболее опасна в плане передачи инфекции.
Инкубационный период 1-10 дней.
Кто может заразиться?

Энтеровирусами может заразиться любой Чаще всего заражаются и заболевают дети, младенцы и подростки, т.к они еще не обладают иммунитетом (защитой) от предыдущих воздействий этих вирусов.
Имеет ли заболевание сезонность?
Вспышки энтеровирусной инфекции преимущественно возникают в летне-осенний период, но отдельные случаи встречаются в течение всего года.
Как протекает инфекция?

Энтеровирусная инфекция характеризуется разнообразием клинических проявлений и множественными поражениями органов и систем: серозный менингит, геморрагический конъюнктивит, синдром острого вялого паралича, заболевания с респираторным синдромом и другие.
Один и тот же серотип энтеровируса способен вызывать развитие нескольких клинических синдромов и, наоборот, различные серотипы энтеровирусов могут вызвать сходные клинические проявления болезни. Наибольшую опасность представляют тяжелые формы инфекции с поражением нервной системы.
Как защититься?

Соблюдение правил личной гигиены имеет жизненно важное значение для предотвращения распространения энтеровирусных инфекций.
- мытье рук с мылом
- тщательное мытье овощей и фруктов перед употреблением
- приобретение продуктов питания только в санкционированных местах
- термическая обработка продуктов
- купание только в разрешенных местах
- соблюдение гигиены во время купания (не заглатывать воду)
- недопущение контактов с инфицированными людьми, особенно с сыпью
- пить только бутилированную воду
При подозрении на инфекционное заболевание – немедленно обратитесь к врачу.
Читайте также:

