Эпидемиология инфекций мочевыводящих путей
Обновлено: 26.04.2024
Категории МКБ: Интерстициальный цистит (хронический) (N30.1), Инфекция мочевыводящих путей без установленной локализации (N39.0), Острый тубулоинтерстициальный нефрит (N10), Острый цистит (N30.0), Пионефроз (N13.6), Хронический тубулоинтерстициальный нефрит (N11)
Общая информация
Краткое описание
Союз педиатров России
Клинические рекомендации: Инфекция мочевыводящих путей у детей
N10/ N11/ N13.6/ N30.0/ N30.1/ N39.0
Бактериурия – присутствие бактерий в моче (более 105 колоний-образующих единиц (КОЕ) в 1 мл мочи), выделенной из мочевого пузыря.
Асимптоматической бактериурией называют бактериурию, обнаруженную при диспансерном или целенаправленном обследовании у ребенка без каких- либо жалоб и клинических симптомов заболевания мочевой системы.
Острый пиелонефрит – воспалительное заболевание почечной паренхимы и лоханки, возникшее вследствие бактериальной инфекции.
Хронический пиелонефрит – повреждение почек, проявляющееся фиброзом и деформацией чашечно-лоханочной системы, в результате повторных атак инфекции МВП. Как правило, возникает на фоне анатомических аномалий мочевыводящего тракта или обструкции.
Рефлюкс-нефропатия - фокальный или диффузный склероз почечной паренхимы, первопричиной которого является пузырно-мочеточниковый рефлюкс, приводящий к внутрипочечному рефлюксу, повторным атакам пиелонефрита и склерозированию почечной ткани.
Уросепсис - генерализованное неспецифическое инфекционное заболевание, развивающееся в результате проникновения из органов мочевой системы в кровеносное русло различных микроорганизмов и их токсинов.
Классификация
Этиология и патогенез
Среди возбудителей инфекций мочевыводящих путей у детей преобладает грам-отрицательная флора, при этом около 90% приходится на инфицирование бактериями Escherichia coli. Грамположительные микроорганизмы представлены, в основном, энтерококками и стафилококками (5-7%). Кроме того, выделяют внутрибольничные инфекции штаммами Klebsiella, Serratia и Pseudomonas spp. У новорождённых детей относительно частой причиной инфекций мочевыводящих путей являются стрептококки групп А и В. В последнее время отмечен рост выявления Staphylococcus saprophyticus, хотя его роль остается спорной.
В настоящее время более половины штаммов E. coli при ИМВП у детей приобрели устойчивость к амоксициллину, однако сохраняют умеренную чувствительность к амоксициллину/клавуланату.
Среди многочисленных факторов, обуславливающих развитие инфекции МВП, приоритетное значение имеют биологические свойства микроорганизмов, колонизирующих почечную ткань, и нарушения уродинамики (пузырно-мочеточниковый рефлюкс, обструктивная уропатия, нейрогенная дисфункция мочевого пузыря).
Наиболее частым путем распространения инфекции считается восходящий. Резервуаром уропатогенных бактерий являются прямая кишка, промежность, нижние отделы мочевыводящих путей.
Анатомические особенности женских мочевыводящих путей (короткая широкая уретра, близость аноректальной области) обуславливают большую частоту встречаемости и рецидивирования ИМВП у девочек и девушек.
При восходящем пути распространения инфекции МВП после преодоления бактериями везикоуретерального барьера происходит их быстрое размножение с выделением эндотоксинов. В ответ происходит активация местного иммунитета макроорганизма: активация макрофагов, лимфоцитов, клеток эндотелия, приводящая к выработке воспалительных цитокинов (ИЛ 1, ИЛ 2, ИЛ 6, фактора некроза опухоли), лизосомальных ферментов, медиаторов воспаления; происходит активация перекисного окисления липидов, что приводит к повреждению почечной ткани, в первую очередь, канальцев.
Гематогенный путь развития инфекции мочевых путей встречается редко, характерен преимущественно для периода новорожденности при развитии септицемии и у детей грудного возраста, особенно при наличии иммунных дефектов. Этот путь также встречается при инфицировании Actinomyces species, Brucella spp., Mycobacterium tuberculosis.
Эпидемиология
Распространенность ИМВП в детском возрасте составляет около 18 случаев на 1000 детского населения. Частота развития ИМВП зависит от возраста и пола, при этом чаще страдают дети первого года жизни. У детей грудного и раннего возраста ИМВП – самая частая тяжелая бактериальная инфекция, она наблюдаются у 10-15% госпитализируемых лихорадящих больных этого возраста. До 3-х месячного возраста ИМВП чаще встречается у мальчиков, в более старшем возрасте – у девочек. В младшем школьном возрасте: 7.8% у девочек и 1.6% у мальчиков. С возрастом после первого перенесенного эпизода ИМВП возрастает относительный риск развития рецидива.
Категории МКБ: Интерстициальный цистит (хронический) (N30.1), Инфекция мочевыводящих путей без установленной локализации (N39.0), Острый тубулоинтерстициальный нефрит (N10), Острый цистит (N30.0), Пионефроз (N13.6), Хронический тубулоинтерстициальный нефрит (N11)
Общая информация
Краткое описание
Союз педиатров России
Клинические рекомендации: Инфекция мочевыводящих путей у детей
N10/ N11/ N13.6/ N30.0/ N30.1/ N39.0
Бактериурия – присутствие бактерий в моче (более 105 колоний-образующих единиц (КОЕ) в 1 мл мочи), выделенной из мочевого пузыря.
Асимптоматической бактериурией называют бактериурию, обнаруженную при диспансерном или целенаправленном обследовании у ребенка без каких- либо жалоб и клинических симптомов заболевания мочевой системы.
Острый пиелонефрит – воспалительное заболевание почечной паренхимы и лоханки, возникшее вследствие бактериальной инфекции.
Хронический пиелонефрит – повреждение почек, проявляющееся фиброзом и деформацией чашечно-лоханочной системы, в результате повторных атак инфекции МВП. Как правило, возникает на фоне анатомических аномалий мочевыводящего тракта или обструкции.
Рефлюкс-нефропатия - фокальный или диффузный склероз почечной паренхимы, первопричиной которого является пузырно-мочеточниковый рефлюкс, приводящий к внутрипочечному рефлюксу, повторным атакам пиелонефрита и склерозированию почечной ткани.
Уросепсис - генерализованное неспецифическое инфекционное заболевание, развивающееся в результате проникновения из органов мочевой системы в кровеносное русло различных микроорганизмов и их токсинов.
Классификация
Этиология и патогенез
Среди возбудителей инфекций мочевыводящих путей у детей преобладает грам-отрицательная флора, при этом около 90% приходится на инфицирование бактериями Escherichia coli. Грамположительные микроорганизмы представлены, в основном, энтерококками и стафилококками (5-7%). Кроме того, выделяют внутрибольничные инфекции штаммами Klebsiella, Serratia и Pseudomonas spp. У новорождённых детей относительно частой причиной инфекций мочевыводящих путей являются стрептококки групп А и В. В последнее время отмечен рост выявления Staphylococcus saprophyticus, хотя его роль остается спорной.
В настоящее время более половины штаммов E. coli при ИМВП у детей приобрели устойчивость к амоксициллину, однако сохраняют умеренную чувствительность к амоксициллину/клавуланату.
Среди многочисленных факторов, обуславливающих развитие инфекции МВП, приоритетное значение имеют биологические свойства микроорганизмов, колонизирующих почечную ткань, и нарушения уродинамики (пузырно-мочеточниковый рефлюкс, обструктивная уропатия, нейрогенная дисфункция мочевого пузыря).
Наиболее частым путем распространения инфекции считается восходящий. Резервуаром уропатогенных бактерий являются прямая кишка, промежность, нижние отделы мочевыводящих путей.
Анатомические особенности женских мочевыводящих путей (короткая широкая уретра, близость аноректальной области) обуславливают большую частоту встречаемости и рецидивирования ИМВП у девочек и девушек.
При восходящем пути распространения инфекции МВП после преодоления бактериями везикоуретерального барьера происходит их быстрое размножение с выделением эндотоксинов. В ответ происходит активация местного иммунитета макроорганизма: активация макрофагов, лимфоцитов, клеток эндотелия, приводящая к выработке воспалительных цитокинов (ИЛ 1, ИЛ 2, ИЛ 6, фактора некроза опухоли), лизосомальных ферментов, медиаторов воспаления; происходит активация перекисного окисления липидов, что приводит к повреждению почечной ткани, в первую очередь, канальцев.
Гематогенный путь развития инфекции мочевых путей встречается редко, характерен преимущественно для периода новорожденности при развитии септицемии и у детей грудного возраста, особенно при наличии иммунных дефектов. Этот путь также встречается при инфицировании Actinomyces species, Brucella spp., Mycobacterium tuberculosis.
Эпидемиология
Распространенность ИМВП в детском возрасте составляет около 18 случаев на 1000 детского населения. Частота развития ИМВП зависит от возраста и пола, при этом чаще страдают дети первого года жизни. У детей грудного и раннего возраста ИМВП – самая частая тяжелая бактериальная инфекция, она наблюдаются у 10-15% госпитализируемых лихорадящих больных этого возраста. До 3-х месячного возраста ИМВП чаще встречается у мальчиков, в более старшем возрасте – у девочек. В младшем школьном возрасте: 7.8% у девочек и 1.6% у мальчиков. С возрастом после первого перенесенного эпизода ИМВП возрастает относительный риск развития рецидива.
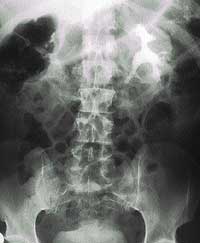
Инфекции мочевыводящих путей (ИМП) в большинстве стран мира — одна из наиболее актуальных проблем. Так, в США ИМП становятся причиной обращения к врачу 7 миллионов пациентов в год, а для миллиона пациентов являются причиной госпитализации [9]. Особую категорию ИМП составляют осложненные инфекции. Согласно современной классификации, к осложненным инфекциям мочевыводящих путей (ОИМП) относятся заболевания, объединенные наличием функциональных или анатомических аномалий верхних или нижних мочевых путей или протекающие на фоне заболеваний, снижающих общий иммунный статус.
Необходимо отметить, что группа ОИМП представлена крайне разнородными заболеваниями: от тяжелого пиелонефрита с явлениями обструкции и угрозой развития уросепсиса до катетер-ассоциированных инфекций МВП, которые могут исчезнуть самостоятельно после извлечения катетера.
Причины возникновения осложненных ИМП
Наиболее часто встречающиеся причины возникновения ОИМП приведены в табл. 1 [5].
Нарушения уродинамики вследствие обструкции МВП
На основании данных можно сделать вывод, что в большинстве случаев причиной осложненного течения ИМП становятся нарушения уродинамики по обструктивному типу при камнях различной локализации, стриктурах мочеточника и лоханочно-мочеточникового сегмента, инфравезикальной обструкции. Восстановление нормальной уродинамики является краеугольным камнем лечения любой мочевой инфекции. В тех случаях, когда причина возникновения обструкции не может быть ликвидирована немедленно, следует прибегать к дренированию верхних мочевых путей нефростомическим дренажем, а в случае инфравезикальной обструкции — к дренированию мочевого пузыря цистостомическим дренажем. Обе операции предпочтительно выполнять чрезкожно под ультразвуковым контролем.
Инородные тела МВП
Часто причиной осложнений при ИМП становятся инородные тела в мочевыводящих путях: конкременты почек и мочевого пузыря, различные дренажи. Лечение подобных инфекций длительное и подчас малоэффективное. Причина кроется в образовании на поверхности инородных тел микробной пленки, которая состоит из связанных между собой и с какой-либо поверхностью микроорганизмов, находящихся в различных фазах роста, их внеклеточных продуктов, соматических клеток, органического и неорганического материала [1].
Биопленка может быть ассоциирована не только с поверхностью дренажных трубок и конкрементов, но и с рубцово-измененными и некротизированными тканями, присутствующими в просвете мочевыводящих путей после предшествующих оперативных вмешательств. Так или иначе, но большинство осложняющих факторов благоприятствуют образованию биопленок. Бактерии, формирующие биопленку, значительно отличаются от планктонных свободно плавающих микробных клеток, не говоря уже о культуре микроорганизмов, использующейся для лабораторных тестов. Доза антибиотика, бактерицидная в отношении возбудителя в лабораторных условиях, зачастую не оказывает на биопленку никакого воздействия; кроме того, бактерии в биопленке более устойчивы к факторам окружающей среды. Вышесказанное свидетельствует о том, что именно биопленка в итоге является основной причиной возникновения трудностей, которые часто сопровождают лечение осложненной хронической персистирующей инфекции мочевыводящих путей.
Нейрогенные нарушения мочеиспускания
К заболеваниям, нарушающим нормальную уродинамику и осложняющим течение ИМП, относятся и нейрогенные нарушения мочеиспускания. Рассчитывать на успех лечения ИМП можно только после коррекции нейрогенных нарушений и восстановления нормальной уродинамики.
Сопутствующие заболевания
Особую группу составляют осложняющие факторы, связанные с наличием сопутствующих тяжелых заболеваний. Список этих заболеваний является предметом обсуждения, однако некоторые нозологии могут быть внесены в него без колебаний. Это заболевания, обусловливающие общее снижение иммунологической реактивности организма: сахарный диабет, иммунодефицитные состояния. К фоновым заболеваниям, значительно осложняющим течение ИМП, относятся также серповидно-клеточная анемия, почечная и печеночно-почечная недостаточность.
Катетер-ассоциированные ИМП
Факторы риска развития ОИМП
Помимо причин, обусловливающих возникновение ОИМП, существует ряд факторов риска развития этого состояния (табл. 3) [5].
Серьезную проблему для выбора эффективной терапии представляет сочетание ОИМП с хроническим простатитом. Хронический простатит — одно из самых трудных для диагностики и лечения заболеваний в урологии. Любое повышение внутриуретрального давления приводит к рефлюксу мочи и содержащихся в ней микроорганизмов в протоки периферической зоны в обход протоков центральной зоны предстательной железы, соустье которых с уретрой по своей природе почти клапанное. При несостоятельности внутреннего сфинктера нейрогенного происхождения или резекции шейки мочевого пузыря ткань простаты подвергается постоянному риску инфицирования и реинфицирования. Хронический бактериальный простатит характеризуется персистированием преимущественно грамотрицательных бактерий в секрете простаты и рецидивирующими ИМП [1, 3].
Этиология ОИМП
В табл. 2 приведены возбудители, наиболее часто являющиеся причиной возникновения ИМП [7]. Обращает на себя внимание, что на втором и третьем местах после наиболее распространенного возбудителя ИМП — кишечной палочки — при осложненных ИМП находятся Enterococcus spp. и Pseudomonas spp., а при катетер-ассоциированных инфекциях — дрожжевые грибки, отсутствующие при неосложненных ИМП.
Микробиологические особенности осложненных ИМП учитываются при выборе препарата для их лечения.
Лечение ОИМП
Лечение инфекции мочевых путей подразумевает проведение эффективной антибактериальной терапии при условии восстановления нормальной уродинамики и направлено на профилактику уросепсиса и возникновения рецидивов. Исключения составляют катетер-ассоциированные инфекции, в большинстве случаев исчезающие после удаления катетера. Открытым остается вопрос о необходимости антибактериальной терапии у пациентов с асимптоматической бактериурией. Большинство урологов считают, что лечение в подобных ситуациях не показано.
Дополнительной проблемой, значительно усложняющей лечение ОИМП, является высокая устойчивость микроорганизмов к большинству антибактериальных препаратов, длительно применяющихся в урологической практике. Госпитализация, неадекватные по длительности курсы лечения и некорректное назначение лекарственных препаратов приводят зачастую к возникновению антибиотико-устойчивых штаммов.
В нашей клинике в случае тяжелых инфекций мочевыводящих путей, а также в послеоперационном периоде после масштабных оперативных вмешательств мы в последнее время применяем новый антимикробный препарат группы фторхинолонов — L-изомер офлоксацина — левофлоксацин (таваник). Подобный выбор при назначении антибактериальной терапии объясняется доказанной способностью препаратов этой группы лучше проникать в биопленку [2, 9].
Поскольку на левофлоксацин приходится практически вся противомикробная активность в рацемической смеси изомеров, его активность in vitro в два раза превышает активность офлоксацина. Биодоступность препарата равняется 99 %, а особенности его фармакокинетики таковы, что 87 % препарата экскретируется с мочой в неизмененном виде [4]. Несмотря на наличие перекрестной устойчивости между левофлоксацином и другими фторхинолонами, некоторые микроорганизмы, устойчивые к хинолонам, могут проявлять чувствительность к левофлоксацину.
В исследованиях in vitro левофлоксацин доказал свою эффективность в отношении E.coli, Enterobacter, Klebsiella, Proteus Mirabilis, Pseudomonas aurugenosa, являющихся наиболее частыми возбудителями осложненной и неосложеннной форм урогенитальной инфекции (табл. 2).
Курс лечения таваником в дозе 250 мг однократно в течение суток на протяжении 10 дней проведен нами у 20 больных. Согласно полученным данным, эффективность и безопасность лечения были признаны хорошими и очень хорошими у 95% пациентов. Сходные результаты приводят в своих работах G. Richard, C. DeAbate et al., применявшие препарат по аналогичной схеме и добившиеся клинического эффекта у 98,1% пациентов [8]. Столь высокие показатели объясняются непродолжительностью применения левофлоксацина в урологической практике, чем и обусловлено отсутствие устойчивых к его действию штаммов микроорганизмов. Надо отметить, что устойчивость к препаратам этой фармакологической группы, связанная со спонтанными мутациями in vitro, встречается крайне редко [9].
Наряду с фторхинолонами в лечении ИМП широко применяются цефалоспорины II поколения (цефуроксим) и особенно III поколения (цефотаксим, цефтазидим и др.), а также карбапенемные антибиотики (имипенем/циластатин, меропенем).
При осложненных инфекциях МВП иногда назначают полусинтетические пенициллины (ампициллин, пиперациллин) и их комбинации с ингибиторами b-лактамаз (ампициллин/сульбактам, пиперациллин/тазобактам), ко-тримоксазол, аминогликозиды (обычно в комбинации с b-лактамами). Однако эффективность этих препаратов при ОИМП прогнозировать достаточно сложно из-за существенных различий в чувствительности возбудителей в зависимости от региона, стационара и источника развития инфекции (внебольничные или госпитальные). Таким образом, при назначении указанных препаратов в ходе терапии ОИМП следует опираться на данные бактериологического исследования мочи и учитывать чувствительность выделенных микроорганизмов.
Препараты нитрофуранового ряда — нефторированные хинолоны (налидиксовая кислота), оксихинолины (5-НОК) — не должны применяться для терапии ОИМП, так как они являются уроантисептиками, то есть создают терапевтическую концентрацию в моче, но не в паренхиме почек.
Длительность курса антибактериальной терапии ОИМП должна составлять не менее 14 дней. Более короткие курсы (7-10 дней) допустимы при назначении фторхинолоновых антибиотиков, выделении высокочувствительного возбудителя и устранении факторов, осложняющих течение ИМП [5].
В заключение хочется подчеркнуть, что лечение инфекций мочевыводящих путей — процесс сложный, длительный и зачастую малоэффективный, поскольку из всего многообразия существующих на сегодня антибактериальных препаратов ни один не обладает достаточно высокой эффективностью в отношении биопленок. Поэтому усилия врачей должны быть направлены преимущественно на профилактику возникновения подобных инфекций.
Введение. Инфекции мочевыводящих путей (ИМП) являются одной из самых распространенных бактериальных инфекций, представляющих практический интерес для специалистов разных направлений. Самой распространенной нозологической формой ИМП является острый неосложненный цистит (ОНЦ). На сегодняшний день существует ограниченное число исследований, посвященной изучению данной проблемы в Российской Федерации.
Цель исследования. Целью настоящего исследования явилась оценка распространённости и клинических особенностей внебольничных ИМП в Российской Федерации.
Результаты. На первом этапе исследования было опрошено 660 женщин, средний возраст - 20,9 ± 1,6 (медиана - 18,0) лет. О перенесенном эпизоде дизурии в течение жизни сообщили 19,0% ± 1,5% опрошенных, при этом у 22,9% респонденток отмечен рецидивирующий цистит. В ходе второго этапа исследования было опрошено 525 респонденток, средний возраст составил 21,1 ± 1,8 года. О перенесенном эпизоде дизурии в течение жизни сообщили 21,1% ± 1,7 опрошенных, при этом 28,5% ± 2,0 респонденток, сообщают о развитии 3 или более эпизодов дизурии в течение последних 12 месяцев.
Медиана продолжительности симптомов цистита составила 2 дня как в ходе первого, так и второго этапов исследования. Чаще всего симптомы дизурии сохранялись 1-3 дня (64,1%), 4-5 дней (23,0%) или 5-7 дней (9,5%). В наибольшей степени с развитием цистита коррелировали отягощенных семейный анамнез (ОР - 2,26-2,42), сексуальная активность и использование спермицидов – (ОР - 1,69 и 2,43). Установлено от 40% до 50,9% респонденток в случае развития дизурии не обращаются за медицинской помощью. При обращении за медицинской помощью, чаще всего консультировались у врача уролога (15,8% - 22,3%), гинеколога (16,7% - 17,7%), реже у терапевта (8,8 – 11,4) или врачей других специальностей (1,3% - 14,8%). Не фармакологические методы лечения использовали 20,1% - 23,1% опрошенных, фитотерапию – 24,0% - 23,9%. Наиболее часто использовали антибиотики, спазмолитики и НПВС. За последние 12 лет отмечается существенные изменения в структуре используемых при цистите антибиотиков – резко снизилась частота использования ампицилина, амоксициллина, ко-тримоксазола, гентамицина. Напротив, повысилась частота использования фосфомицина, норфлоксацина, левофлоксацина.
Выводы. О возникновении симптомов ОЦ по данным опроса молодых женщин, сообщают 19,1% - 21,1% опрошенных. 22,9% - 28,5% женщин сообщают о развитии 3 и более рецидивов дизурии в течение года. При развитии дизурии, клинические симптомы сохраняются в течение 2 дней (медиана), у основной части пациентов (64,1% - 70,9%) длительность дизурии находится в диапазоне 1-3 дней. Риск развития симптомов ОЦ положительно коррелирует с активностью половой жизни, отягощенным семейным анамнезом, использованием спермицидов – ОР - 1,69, 2,42, 2,43 соответственно. При развитии симптомов ОЦ 40,3-50,9% респондентов не обращались за медицинской помощью, основным методом лечения цистита в амбулаторных условиях является использование антибиотиков.
Раскрытие информации: Исследование не имело спонсорской поддержки. Авторы заявляют об отсутствии конфликта интересов.
Ключевые слова
Для цитирования:
For citation:
Введение
Инфекции мочевыводящих путей (ИМП) представляют собой одну из наиболее актуальных проблем современной медицины. Это связано как с широкой распространенностью ИМП, так и с наличием сложностей с выбором рациональной антимикробной терапии. Данные многочисленных исследований свидетельствуют о широкой распространенности ИПМ, как среди амбулаторных, так и госпитализированных пациентов [1]. Установлено, что наиболее распространенной нозологической формой ИМП является острый неосложненный цистит (ОНЦ). Так, было показано, что эпизод неосложненной ИМП в течение жизни переносит каждая вторая женщина, при этом у 30% из них заболевание имеет рецидивирующее течение [2]. По данным североамериканских ученых, ОНЦ - ежегодная причина около 2 млн визитов к врачу. В России распространенность ОНЦ колеблется в пределах от 26 млн до 36 млн случаев в год [3][4]. Как правило, ОНЦ развивается у женщин репродуктивного возраста, симптомы данного заболевания могут сохраняться на протяжении 6-7 дней, при этом в течение 2-3 дней наблюдается снижение общей активности пациенток, а невозможность посещать учебные заведения и работу отмечается на протяжении 1-2 дней [4].
На диагностику и лечение инфекций мочевыводящих путей (ИМП) регулярно затрачиваются значительные ресурсы системы здравоохранения разных стран. Так, в США именно ИМП ежегодно являются причиной 8 млн обращений к врачу и 100 тыс. госпитализаций, при этом на их лечение приходится до 15% всех назначений антибиотиков в амбулаторной практике, что сопровождается затратами в 1,6 млрд долларов США [5][6].
Целью настоящего исследования явилась оценка распространённости и клинических особенностей внебольничных ИМП в РФ.
Материалы и методы
Исследование проводили в два этапа, первый этап выполнен в 2005-2006 годах, второй этап - в 2017 г. Как во время первого, так и второго этапов использовали метод анкетирования.
В ходе первого этапа проводили анкетирование молодых женщин в организованных коллективах (ВУЗы и колледжи) с помощью бумажной традиционной анкеты, состоящей из 19 вопросов, касающихся частоты развития симптомов типичных для острого цистита (дизурии), данных о рецидивировании, сопутствующих заболеваниях, наследственном анамнезе, активности половой жизни, обращении к врачу, самолечении. Анкету было предложено заполнить студенткам немедицинских учебных заведений. Анкетирование проводили в 20 городах Российской Федерации, Республики Беларусь и Казахстана.
Результаты
На первом этапе исследования было опрошено 660 женщин в возрасте от 16 до 51 года. Средний возраст участниц - 19,2 ± 1,5 года, средний возраст респонденток, сообщивших по крайней мере об одном эпизоде дизурии - 20,9 ± 1,6 (медиана - 18,0) лет (табл. 1).
Читайте также:

