Этиология пневмонии наиболее характерная для вич инфекции
Обновлено: 11.05.2024
Болезнь вызывается вирусом иммунодефицита человека, относящимся к семейству ретровирусов, роду лентивирусов. Устойчивость его во внешней среде колеблется: при температуре 56*С погибает через 30 мин., при кипячении через 1-3 мин. Однако вирус устойчив к ионизирующей радиации и к ультрафиолетовым лучам. Вирусу присуща большая генетическая изменчивость и склонность к антигенному дрейфу - он в 5 раз менее стабилен, чем вирус гриппа и в 100 раз лабильнее вирусов гепатита.
Как и все ретровирусы, геном ВИЧ представлен рибонуклеиновой кислотой и подвергается обратной транскрипции. ВИЧ поражает клетки крови человека, имеющие на своей поверхности CD4-рецепторы (CD4+ Т-лимфоциты, макрофаги и дендритные клетки).
После того, как число CD4+ T-лимфоцитов становится ниже 200 в одном микролитре крови, система клеточного иммунитета перестает защищать организм. Острая инфекция со временем переходит в латентную форму, и ранним симптомом ВИЧ-инфекции и далее СПИД является число CD4+ T-лимфоцитов в крови.
Скорость развития инфекции зависит от многих факторов, например, от статуса иммунной системы инфицированного. Пожилые люди имеют более слабую иммунную систему и поэтому имеют повышенный риск быстрого развития заболевания, в сравнении с молодыми людьми. Недостаточный уровень медицинского ухода и наличие сопутствующих инфекционных заболеваний, например, туберкулёза, вызывает предрасположенность к скоротечному развитию заболевания.
Оболочка вируса состоит из двуслойной липидной мембраны, в которую встроен ряд белков:
gp41 — трансмембранный гликопротеин,
gp120 — поверхностный гликопротеин .
С помощью поверхностного гликопротеина вирус присоединяется к CD4-рецептору и одному из двух корецепторов, находящихся на поверхностной мембране клеток. Для Т-лимфоцитов корецептором является CXCR-4, а для макрофагов — CCR-5.
Цитоплазматическая мембрана клетки и мембрана вируса сливаются, вирус проникает внутрь клетки, где из капсида высвобождается вирусная РНК, и происходит катализируемая обратной транскриптазой обратная транскрипция — синтез двуцепочечной ДНК на матрице одноцепочечной вирусной РНК.
Синтезированная ДНК транспортируется внутрь ядра клетки хозяина и интегрируется в хромосому хозяина (процесс, катализируемый интегразой). Клеточная РНК-полимераза катализирует синтез вирусной геномной РНК и вирусных мРНК. Синтезированные РНК транспортируются из ядра клетки в цитоплазму, где на матрице мРНК на рибосомах синтезируются вирусные ферменты, структурные и регуляторные белки. Геномная РНК вируса, а также вирусные белки (структурные и некоторые другие, входящие в состав вириона), транспортируются к местам сборки вирионов. Новые вирусные частицы отпочковываются от поверхности клетки, захватывая часть её мембраны, и выходят в кровяное русло, а CD4+ лимфоцит хозяина погибает.
В лимфоидной ткани ВИЧ размножается в течение всей ВИЧ-инфекции, поражая макрофаги, активированные и покоящиеся CD4+ лимфоциты, фолликулярные дендритные клетки. Количество клеток, содержащих провирусную ДНК, в лимфоидной ткани в 5—10 раз выше, чем среди клеток крови, а репликация ВИЧ в лимфоидной ткани на 1—2 порядка выше, чем в крови. Таким образом, основным резервуаром ВИЧ служат лимфатические узлы.
Для активации CD8+ лимфоцитов и образования антиген специфических цитотоксических T-лимфоцитов необходима презентация пептидного антигена в комплексе с человеческим лейкоцитарным антигеном. Дендритные клетки, необходимыe для начала первичных антиген специфичных реакций, захватывают антигены, перерабатывают и переносят их на свою поверхность, где эти антигены, в комплексе с дополнительными стимулирующими молекулами, активируют T-лимфоциты. Зараженные клетки часто не выделяют дополнительных стимулирующих молекул и поэтому не способны вызвать образование достаточного числа клеток иммунного ответа (B- и T-лимфоцитов), функция которых зависит от дендритных клеток.
После завершения обратной транскрипции в CD4+ лимфоците вирусный геном представлен провирусной невстроенной ДНК. Для встраивания провирусной ДНК в геном клетки-хозяина и для образования новых вирусов необходима активация T-лимфоцитов. Контакт CD4+ лимфоцитов и антиген представляющих клеток в лимфоидной ткани, наличие вирусов на поверхности фолликулярных дендритных клеток и присутствие провоспалительных цитокинов (ИЛ-1, ИЛ-6 и ФНОα) способствуют размножению ВИЧ в инфицированных клетках. Поэтому лимфоидная ткань служит самой благоприятной средой для репликации ВИЧ.
Известно несколько разновидностей этого вируса:
ВИЧ – I - обусловил современную пандемию СПИДа,
LAV - 2 (или ВИЧ – 2) - патоген для человека, но вызываемое им заболевание протекает легче и у меньшего числа инфицированньх развивается клиника, характерная для СПИДа, обусловленного ВИЧ - I.
НТLV- IV (или ВИЧ–3) - способен инфицировать Т-лимфоциты, но не разрушает их и не вызывает зяболевания, поэтому считается непатогенным для человека .
ВОЗ рекомендует различать четыре стадии ВИЧ-инфекции:
I/ Начальная (острая) ВИЧ - инфекция;
2/ Персистирующая генерализованная лимфадэнопатия;
З/ СПИД - ассопировонный комплекс (пре-СПИД);
4/ Развернутый СПИД.
( 5/ СПИД – деменция( в связи с очень частым поражением центральной нервной системы и глубокими нарушениями ее функций).)
В России и странах СНГ получила распространение классификация, предложенная В. И. Покровским в 1989 году.
I — стадия инкубации
II — стадия первичных проявлений
А — острая лихорадочная фаза
Б — бессимптомная фаза
В — персистирующая генерализованная лимфаденопатия
III — персистирующая генерализованная лимфаденопатия
А — потеря массы тела менее 10 %, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий герпес, повторные фарингиты, синуситы
Б — прогрессирующая потеря массы тела более 10 %, необъяснимая диарея или лихорадка более 1 месяца, повторные и/или стойкие бактериальные и протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек: повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши
В — генерализованные бактериальные, грибковые, вирусные, протозойные и паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелёгочный туберкулёз, кахексия, диссеминированная саркома Капоши, поражения ЦНС различной этиологии
IV — терминальная стадия
Согласно ней пациенту диагностируют либо СПИД, либо ВИЧ-инфекцию. Согласно CDC-классификации лица, которые подпадают под критерии категорий А3, В3, С1, С2 и С3 подлежат учёту, как больные СПИДом.
Начальная стадия. Начальная стадия, развивающаяся приблизительно у половины инфицированные протекает остро. Эта стадия наступает спустя 2-4 нед после заражения, продолжается от 3 до 14 сут с последующим спонтанным регрессом, сопровождается образованием антител к ВИЧ. Клинические проявления: головная боль, недомогание, общая слабость, повышенная потливость, артралгия, миалгия, лихорадка, ангина, фарингит, генерализованная лимфаденопатия, гепатолиенальный синдром, диарея. Возможны эпилептиформные припадки. Поражение кожи представлено многочисленными, рассеянными по всей поверхности бледно-розовыми пятнами округлых и овальных очертаний размерами от окружности булавочной головки до чечевицы и более. Характерна лимфопения.
Бессимптомная стадия. Бессимптомная стадия, или стадия вирусоносительства, не сопровождается какими-либо клиническими проявлениями. Ее распознавание возможно лишь лабораторным путем: выделением вируса, определением антигена и антител к нему и изучением иммунных показателей.Обычно прибегают к определению антител (сероконверсии), что достигается методом серологических реакций. Для выявления вирусоносителей, а следовательно, и наиболее "коварных" источников инфекции ВИЧ обследуют в первую очередь доноров крови, плазмы, спермы и органов, представителей групп риска и половых партнеров больных этой инфекцией. Распознавание бессимптомной стадии сопряжено с большими трудностями. При вирусоносительстве не всегда имеются антитела и его продолжительность точно не установлена.В клинической практике сероконверсия наступает приблизительно в сроки от 2 до 7 нед. Допускается скрытая персистентная вирусемия при отсутствии антител.
Стадия генерализованной лимфаденопатии .Стадия генерализованной лимфаденопатии относится к числу закономерных состояний при инфекции ВИЧ. Она встречается у 90 % больных. Из периферических лимфатических узлов в процесс вовлекаются преимущественно расположенные выше пояса: кубитальные, под- и надключичные, подбородочные, подчелюстные, около- и заушные, затылочные и особенно часто подкрыльцовые и шейтные. Однако могут оказаться увеличенными паховые, бедренные и подколенные лимфатические узлы. Лимфаденопатия может рассматриваться как клинический тест инфекции ВИЧ, если она поражает не менее двух групп лимфатических узлов (лежащих выше пояса) и сохраняется более 3 мес. При этом необходимо исключить лимфаденопатию иной природы (опухолевую, паразитарную, микотическую, бактериальную, трепонемную и др.). Число увеличенных узлов и их сочетание очень разнообразны: от единичных лимфаденитов до тотальной лимфаденопатии. Однако обычно увеличено небольшое число узлов 2- 3 групп. Диаметр узлов колеблется от 0,5 до 2 см, достигая порой 4-5 см, когда узлы легко определяются визуально. Лимфатические узлы обычно изменены по реактивному типу: они имеют плотноэластическую или мягкую консистенцию, остаются изолированными, подвижными и безболезненными. Иногда узлы образуют целые плеяды, приобретают склонность к слиянию, становятся болезненными, особенно при пальпации. Кожа над пораженными узлами не изменена. СПИД-зависимый комплекс обычно формируется на фоне генерализованной лимфаденопатии спустя 1,5-3 года от ее начала в результате присоединения в разной последовательности и сочетании многочисленных и разнообразных общих нарушений и поражения различных органов тканей и систем.
В зависимости от преимущественной локализации очагов поражения, условно выделяют 4 клинические формы СПИДа: легочную, жедудочно-кишечную, церебральную и диссеминироврнную.
Легочная форма характеризуется возникновением пневмонии, преимущественно пневмоцистной природы, которая отмечается, примерно, у 60% больных.
Желудочно - кишечная форма проявляется тяжелой хронической диареей, ведущей к потере маасы тела, опухолевыми процессами в прямой кишке и на языке. Ведущая роль в возникновении поносов в 60% случаев принадлежит простейшим, преимущественно криптоспори дням.
Поражения центральной нервной системы отмечаются более чем у 30% больных СПИДом и проявляются самым разнообразными неврологическими симптомами и синдромами, присущими менингоэнцефалиту, энцефалиту, гемипарезу, атаксии, первичным и вторичным опухолям мозга, очаговым мозговым явлением. Возникают расстройства памяти, психики, развивается деменция вследствие атрофии головного мозга.
Пневмония у ВИЧ-инфицированных характеризуется особенностью возбудителей инфекции, течения заболевания и лечения. Нередко клиническая картина ничем не отличается от других видов воспаления лёгких, однако в виду отсутствия у врачей настороженности в отношении ВИЧ-инфекции, диагностика иммунодефицитных пневмоний затруднительна.
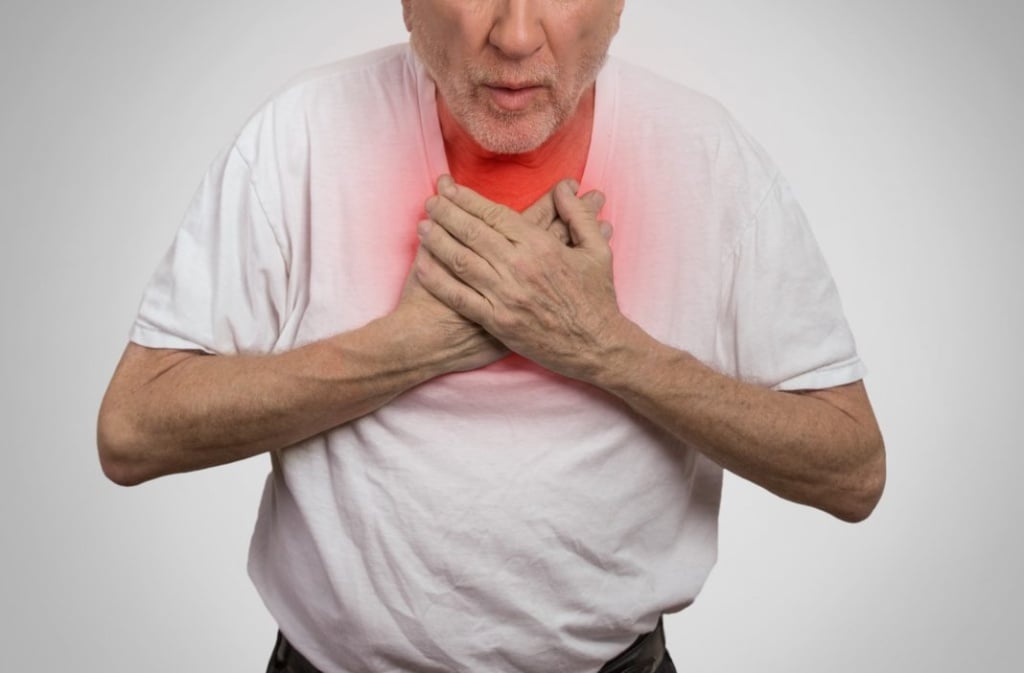
В Юсуповской больнице пульмонологи применяют современную аппаратуру и инновационные методы обследования, позволяющие быстро установить точный диагноз. Для лечения пациентов пульмонологи используют современные препараты, эффективно действующие в условиях иммунодефицита. В клинике терапии работают врачи, имеющие огромный опыт лечения иммунодефицитных пневмоний. Все сложные случаи воспаления лёгких обсуждаются на заседании экспертного Совета.
Причины пневмонии при ВИЧ-инфекции
Пневмонию у ВИЧ-инфицированных вызывают грамотрицательные палочки. Часто при наличии иммунодефицита в виде пневмонии протекает туберкулёз. Одними из наиболее известных и значимых возбудителей оппортунистических пневмоний у ВИЧ-инфицированных пациентов в эру ретровирусной терапии остаются пневмоцисты.
Развитие пневмоцистной пневмонии определяет не только степень выраженности иммунодефицита, но и его характер. Средняя частота пневмоцистной пневмонии при ВИЧ-инфекции в настоящее время составляет 50 %, а при других иммунодефицитных состояниях не превышает 1 %. Развитию воспаления лёгких способствует нарушение клеточного и гуморального иммунитета.
Клинико-диагностические критерии пневмонии
Диагностика пневмонии у ВИЧ-инфицированных является сложной из-за отсутствия патогномоничных клинических признаков, частого сочетанного течения нескольких оппортунистических заболеваний одновременно на фоне глубокого поражения иммунной системы. Отсутствуют и точные лабораторные критерии, которые позволяли бы подтвердить диагноз.
Пневмония у ВИЧ-инфицированных начинается подостро. На протяжении нескольких недель нарастают следующие симптомы:
- лихорадка;
- одышка;
- сухой кашель;
- чувство тяжести в грудной клетке;
- утомляемость;
- похудание.
Во время физикального исследования врачи обнаруживают лихорадку и учащённое дыхание, перкуссия и аускультация грудной клетки изменений не выявляют. В Юсуповской больнице пациентам с подозрением на иммунодефицитную пневмонию делают крупнокадровую флюорографию или рентгенографию в двух проекциях. На рентгенограммах можно увидеть двусторонние изменения – ограниченные затемнения легочных полей или сетчатую перестройку легочного рисунка. Иногда пульмонологи видят множественные очаговые тени или круглые полости. У некоторых ВИЧ-инфицированных больных изменений, характерных для воспаления лёгких, может совсем не быть. В этом случае в Юсуповской больнице пациентам делают компьютерную томографию.
Изменения лабораторных показателей неспецифичны. В большинстве случаев пневмоний у ВИЧ-инфицированных увеличивается активность лактатдегидрогеназы, однако это бывает и при других респираторных заболеваниях на фоне СПИДа. При измерении газового состава крови врачи иногда обнаруживают гипоксемию, увеличение парциального давления кислорода и респираторный алкалоз (смещение рН в кислую сторону). Характерным признаком инфекции является снижение парциального давления кислорода при физической нагрузке.
Поскольку пневмоцистную пневмонию легко спутать с другими свойственными ВИЧ-инфицированным заболеваниями, а курс лечения долгий и сопряжён с тяжелыми побочными эффектами, врачи Юсуповской больницы для подтверждения диагноза используют лабораторные методы. Сначала прибегают к иммунофлюоресцентному окрашиванию мокроты с использованием моноклональных антител. Если возбудитель не найден, выполняют диагностическую бронхоскопию и трансбронхиальную биопсию лёгкого. Если бронхоскопия оказалась неинформативной или состояние пациента ухудшается, врачи клиник-партнёров проводят открытую биопсию лёгкого.
Золотым стандартом диагностики пневмонии у ВИЧ-инфицированных является микроскопическая визуализация возбудителя. В настоящее время часто используют иммунофлюоресцентную диагностику с использованием моноклональных антител. Серологические методы могут быть малоинформативными из-за выраженного иммунодефицита. В клиниках-партнёрах проводят молекулярную диагностику иммунодефицитных пневмоний.
При исследовании периферической крови специфических изменений при пневмоцистной пневмонии не наблюдается. Диагностировать пневмоцистную пневмонию помогает высокий уровень скорости оседания эритроцитов. Часто имеют место изменения в крови, характерные для поздних стадий СПИДа.
Лечение пневмонии у ВИЧ-инфицированных
Резервной схемой лечения пневмоцистной пневмонии умеренной степени тяжести является комбинация клиндамицина с примахином. Схема лечения пневмонии у ВИЧ-инфицированных обязательно включает комбинированную антиретровирусную терапию, если пациент не получал её ранее. Кортикостероидные гормоны назначают на фоне начала антибактериальной терапии с целью предупреждения усиления дыхательной недостаточности.
Запишитесь на приём к пульмонологу по телефону клиники. Контакт-центр Юсуповской больницы работает круглосуточно. Пациентов с симптомами пневмонии в зависимости от тяжести течения заболевания госпитализируют в клинику терапии или отделение реанимации и интенсивной терапии. Пульмонологи лечат пациентов с воспалением лёгких согласно европейских рекомендаций, используют индивидуальные схемы терапии.
Одной из ведущих патологий среди заболеваний органов дыхания является внебольничная пневмония. В связи с массовым применением антибактериальных препаратов значительно изменились поведение и пейзаж возбудителей. С появлением антиретровирусной терапии снизились показатели регистрации оппортунистических инфекции, связанных со СПИДом, но заболеваемость бактериальными пневмониями не уменьшается. Частыми возбудителями внебольничных пневмоний являются бактерии, среди которых Streptococcus pneumonia занимает лидирующее место. Другими микроорганизмами, вызывающими инфекции респираторной системы у ВИЧ-инфицированных больных, являются S. aureus, H. influenzae, K. pneumoniae, P. aeruginosa, представители семейства Enterobacter, а также атипичные возбудители, такие как Legionella pneumophila, Mycoplasma pneumonia и Chlamydophila pneumoniae, которые встречаются у пациентов с ВИЧ-инфекцией значительно реже, чем у ВИЧ-отрицательных. Очень часто у ВИЧ-инфицированных пациентов выявляют одновременно несколько возбудителей пневмоний, например, бактерии в сочетании с вирусами, микобактериями или грибковой микрофлорой, что изменяет клиническое течение, рентгенологические показатели и прогноз заболевания.
Проблема пневмоний всегда представляла большой научный и практический интерес. В последнее время она привлекает к себе еще большее внимание в связи с широким распространением ОРВИ, гриппа и приобретенных иммунодефицитых состояний, которые способствуют росту удельного веса пневмоний в структуре общей заболеваемости населения.
Широкое использование в диагностике пневмоний рентгенологических методов исследования ставит вопрос о необходимости улучшения лучевой диагностики как в организационном (обеспечение доступности КТВР и МСКТ), так и в научном плане (разработка алгоритмов рентгенологической дифференциальной диагностики пневмоний, различных в этиологическом и в патогенетическом отношении).
В настоящее время особую важность приобретают также вопросы бактериологической диагностики пневмоний. Можно согласиться с мнением ряда исследователей о том, что разделение этиологического и патогенетического фактора при пневмониях не всегда просто и подчас условно. Однако этиологическая роль эндогенных микробов не должна оспариваться. Точное установление возбудителя приводит к рациональному выбору лекарственного препарата (антибактериального, антимикотического, противовирусного и др.) и выздоровлению пациента.
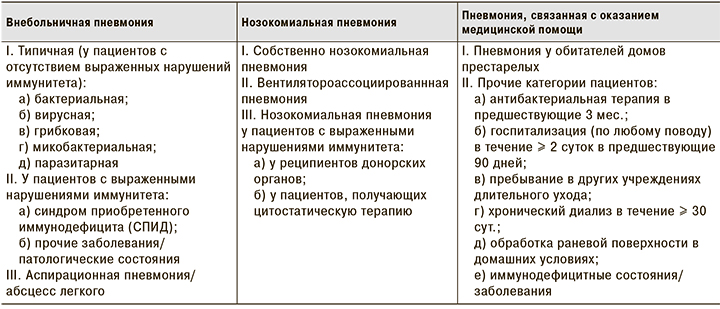
Согласно классификации академика А.Г. Чучалина, (см. таблицу) пневмонии подразделяются на внебольничные, нозокомиальные (госпитальные, приобретенные в лечебном учреждение при длительном нахождение в нем) и связанные с оказанием медицинской помощи [1].
Этиологическим агентом пневмоний могут быть вирусы, грибы, бактерии, простейшие, гельминты. Некоторых возбудителей можно отнести к облигатным пнеймотропам (пневмококки, Klebsiella pneumoniae или палочка Фридлендера, микобактерии туберкулеза и т. д.). Другие микроорганизмы, находящиеся в полости рта и верхних дыхательных путях, являются условно патогенными (стафилококки, стрептококки, вирусы гриппа и т. д.) и вызывают заболевание при определённых условиях, приводящих к снижению резистентности организма [1].
Одной из ведущих патологий в группе заболеваний органов дыхания является внебольничная пневмония. Согласно предложенной классификации, выделяют внебольничную пневмонию типичную и аспирационную и пневмонию у пациентов с нарушениями иммунной системы [1].
Показатель заболеваемости внебольничной пневмонией на территории Российской Федерации в 2011 г. составлял 316,0 на 100 тыс. населения, а в 2017 г. – уже 413,15, темп прироста составил 30,7%. Известно, что данные официальной статистики не отражают истинной картины заболеваемости пневмонией, и по мнению ученых [2, 3], ежегодно число заболевших превышает 1,5 млн человек.
В связи с массовым применением антибактериальных препаратов возникла серьезная проблема значительного изменения поведения и пейзажа возбудителей. Поэтому при изучении этиологической структуры пневмоний в настоящее время следует непременно учитывать следующие факторы:
- высокую эффективность антибактериальных препаратов, приводящих к купированию большинства пневмококковых пневмоний;
- подавление en masse пневмококковой флоры, уменьшение активности и снижение выработки токсинов;
- изменчивость возбудителей, что сказывается на возникновении резистентности штаммов пневмококков и стрептококков;
- значительное увеличение в связи с лекарственным дисбактериозом удельного веса патогенных стафилококков и отчасти стрептококков в этиологии пневмоний, особенно детского возраста;
- широкое необоснованное применение антибиотиков широкого спектра действия, приводящее к развитию микотических пневмоний;
- увеличение регистрации атипичных и вирусных пневмоний в ослабленных организмах.
Бактериальная пневмония является основной причиной заболеваемости и смертности среди ВИЧ-инфицированных лиц, при этом вероятность ее развития в 25 раз выше, чем среди обычного населения [5–8]. Известно, что бактериальная пневмония, исключая пневмонию, вызванную Pneumocystis jirovecil, была главной причиной летального исхода среди зараженного ВИЧ контингента в Соединенных Штатах в течение 1990–1999 [9].
С появлением антиретровирусной терапии (АРТ), отмечено снижение регистрации оппортунистических инфекции, связанные со СПИДом [10, 11]. Тем не менее в настоящее время при широком применении АРТ, заболеваемость бактериальными пневмониями не уменьшается. По мнению ряда авторов [12, 13], в Италии показатель заболеваемости бактериальной пневмонией в период высокого охвата АРТ (около 65,0%) составил 7700 и 9100 случаев на 100 тыс. ВИЧ-инфицированных пациентов [12, 13]. В Европе у пациентов в стадии СПИДа развитие рецидивирующей бактериальной пневмон.
19517 04 Сентября
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
ВИЧ: причины появления, симптомы, диагностика и способы лечения.
Определение
ВИЧ (вирус иммунодефицита человека) – инфекционное хроническое заболевание, передающееся контактным путем, медленно прогрессирующее и характеризующееся поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИДа). СПИД – это финальная стадия ВИЧ-инфекции, когда из-за ослабленной иммунной системы человек становится беззащитным перед любыми инфекциями и некоторыми видами рака. Опасность представляют так называемые оппортунистические инфекции – заболевания, вызываемые условно-патогенной или непатогенной флорой: вирусами, бактериями, грибами, которые у здоровых людей не приводят к серьезным последствиям или протекают легко и излечиваются самостоятельно. При СПИДе они наслаиваются друг на друга, имеют затяжное течение, плохо поддаются терапии и могут стать причиной летального исхода.
Причины появления ВИЧ
Источником инфекции является человек, инфицированный ВИЧ, на любых стадиях заболевания. Вирус передается через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь (незащищенный секс с инфицированным партнером) – доминирующий фактор распространения ВИЧ-инфекции.
Передача ВИЧ от матери ребенку может произойти на любом сроке беременности (через плаценту), во время родов (при прохождении через родовые пути) и грудного вскармливания (при наличии язвочек, трещин на сосках матери и во рту ребенка).
Высокий риск инфицирования существует при внутривенном введении наркотических веществ нестерильными шприцами, при переливании ВИЧ-инфицированной крови и ее препаратов, использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, опасность могут представлять органы и ткани доноров, используемые для трансплантации.

Попадая в кровоток, вирус проникает в Т-лимфоциты хелперы, или CD-4 клетки (рановидность лейкоцитов), которые помогают организму бороться с инфекциями. Т-хелперы имеют на поверхности так называемые CD4-рецепторы. ВИЧ связывается с этими рецепторами, проникает в клетку, размножается в ней и в конечном счете уничтожает ее. Со временем вирусная нагрузка увеличивается, а количество Т-хелперов снижается.
При отсутствии лечения через несколько лет из-за значительного снижения числа Т-хелперов появляются связанные со СПИДом состояния и симптомы.
Классификация заболевания
- Стадия инкубации - от момента заражения до появления реакции организма в виде клинических проявлений острой инфекции и/или выработки антител (специфических белков, продуцируемых в ответ на проникновение антигена, в данном случае – вируса).
- Стадия первичных проявлений клинических симптомов:
В дальнейшем продолжается активное размножение вируса и разрушение Т-лимфоцитов, развивается стадия вторичных изменений, для которой характерно прогрессирующее снижение веса, общая слабость, стойкое повышение температуры, озноб, выраженная потливость. Клинические проявления оппортунистических заболеваний обусловливают клиническую картину этой стадии: пациентов беспокоят кашель и одышка, тошнота, рвота, боли в животе, тяжелая диарея, кожные высыпания, сильные головные боли, снижение памяти и внимания и др.
Диагностика ВИЧ
Лабораторные методы исследования:
Скрининг (обследование здоровых людей) на ВИЧ должен быть проведен любому человеку, который считает, что может быть заражен, а также перед любой госпитализацией и операцией, всем беременным женщинам и их половым партнерам.
Обследование целесообразно проходить людям с высоким риском заражения ВИЧ, например, при наличии заболеваний, имеющих одинаковый с ВИЧ-инфекцией механизм передачи (вирусные гепатиты В и С, заболевания, передающиеся половым путем), лицам, имеющим регулярные незащищенные половые контакты, инъекционным наркоманам, детям, рожденным от матерей с ВИЧ-инфекцией, медицинским работникам, напрямую контактирующим с кровью на работе и др.
Существуют экспресс-тесты для скрининга ВИЧ, которые можно делать в домашних условиях. Для определения специфических антител/антигенов к ВИЧ (ВИЧ-1, 2, антиген p24) используют кровь, слюну или мочу. Точность любого экспресс-теста ниже, чем теста, проводимого в лаборатории.
Для стандартного скринингового обследования определяют антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) в крови с помощью иммуноферментного анализа (ИФА).
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 10 рабочих дней. Синонимы: Анализ крови на антитела к ВИЧ1 и 2 и антиген ВИЧ1 и 2; ВИЧ-1 p24; ВИЧ-1-антиген, p24-антиген; ВИЧ 1 и 2 антитела и антиген p24/25, ВИЧ тест-системы 4-г.
Пневмоцистная пневмония — редкая форма патологии легких, вызываемая внеклеточным грибом Pneumocistis jiroveci, поражающая лиц с тяжелыми дефектами иммунитета, больных, принимающих иммуносупрессивную терапию, онкологических больных, недоношенных и ослабленных детей, ВИЧинфицированных пациентов в стадии СПИДа. По таксономическому положению пневмоцисты относят к высшим грибам — аскомицетам или базидиомицетам, для них также характерны некоторые свойства протозоев [8]. Распространенность пневмоцист в природе широкая, выявляют пневмоцисты не только у людей, но и у животных. Для человека патогенна P. jiroveci, названная в честь чешского ученого-паразитолога Отто Йировеца, впервые описавшего этот микроорганизм как причину заболевания у человека.
Заражение происходит воздушно-капельным путем. Пневмоцисты обладают тропизмом к легочной паренхиме и не вызывают поражения верхних и средних дыхательных путей. Сезонность заболевания не характерна. Развитие пневмоцистоза определяется биологическими свойствами возбудителя и состоянием иммунной системы человека и связано с поражением как гуморального, так и клеточного иммунитета, в том числе с лимфоцитозависимым дефектом макрофагов, не распознающих размножающихся пневмоцист [3]. Клетками-мишенями для пневмоцист являются альвеолоциты 1-го типа, поражение которых проявляется деструкцией клеток, нарушением целостности альвеолярной мембраны и развитием экссудативных явлений. Для построения собственной клеточной оболочки P. jiroveci используют фосфолипиды сурфактанта человека. Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта [1]. Активность альвеолярных макрофагов при этом направлена на защиту альвеол от избыточной продукции сурфактанта, а не на поглощение возбудителя. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Белки экссудата разрушают и инактивируют сурфактант, активируют фиброзирование межальвеолярных перегородок, что приводит к гипоксемии. Происходит снижение секреторной функции альвеолоцитов 2-го типа и возрастание их пролиферативной активности [7].
Частота пневмоцистной пневмонии у больных ВИЧ-инфекцией в странах Европы и США достигает 60%. Летальность от пневмоцистной пневмонии в среднем составляет 13%. В России частота пневмоцистной пневмонией у ВИЧ-инфицированных колеблется от 5,6 до 8,5%. Летальные исходы от пневмоцистной пневмонии у больных с поздними стадиями ВИЧ-инфекции составляют 7,1% и занимают 4 место после туберкулеза, бактериальной пневмонии, инфекционного эндокардита [4]. Заболевание, как правило, ограничивается легкими, но при глубокой иммуносупрессии возможны генерализованные формы. Пневмоцистная пневмония — наиболее частая СПИД-индикаторная патология у детей; ее частота у больных СПИДом детей, по данным центра по контролю заболеваний (CDC) США 1995 г., составляла 34% от всех случаев СПИДа у детей. Чаще эта инфекция развивается у детей первого года жизни (57—72% случаев), пик заболеваемости приходится на возраст 3—6 мес, поэтому детям первого года жизни особенно показана медикаментозная профилактика. Риск пневмоцистной пневмонии на первом году жизни у ВИЧинфицированных детей, не получающих профилактику, составляет 7—20%. Пневмоцистная пневмония может сочетаться с другими инфекционными поражениями легких на фоне ВИЧ-ассоциированной иммуносупрессии, что значительно усложняет диагностику. У детей, получающих профилактику бисептолом, пневмоцистная пневмония практически не регистрируется. Пневмоцистная пневмония — самая частая причина смерти младенцев, инфицированных ВИЧ, от нее умирают 50—60% младенцев на стадии СПИДа [6]. Диагностика пневмоцистной пневмонии сложна из-за отсутствия патогномоничных клинических признаков, частого сочетания с несколькими инфекционными заболеваниями на фоне глубокой депрессии иммунной системы, а также трудностей лабораторного подтверждения. Самым важным для диагностики пневмоцистной пневмонии является клиническая настороженность в отношении к этой инфекции у ВИЧ-инфицированных. В клинической картине пневмоцистной пневмонии у больных ВИЧ-инфекцией отмечается подострое начало заболевания, субфебрильная или небольшая фебрильная лихорадка, непродуктивный, навязчивый, приступообразный кашель, длящийся несколько недель или месяцев или постоянный, мучительный кашель, экспираторная или смешанная одышка, возникающая вначале при физической нагрузке, а затем и в покое, прогрессирующая дыхательная недостаточность. Может выделяться пенистая мокрота. Над легкими может определяться укорочение перкуторного звука, аускультативно жесткое дыхание, рассеянные сухие хрипы, крепитация, больше в задних отделах легких [2].
Н.И. Петрук , Д.Ю. Овсянников , А.М. Болибок , А.В. Шолтояну , С.А. Носов , И.И. Крюков , Л.А. Захарова , А.А. Крушельницкий , Е.А. Дегтярева , О.И. Жданова
Читайте также:

