Флегмона у детей сепсис
Обновлено: 25.04.2024
Флегмоной подкожной клетчатки называется разлитое гнойное воспаление ее с переходом в некроз или абсцедирование; она имеет стремление к распространению по рыхлым клетчаточным пространствам во всех направлениях.
Тяжесть заболевания зависит от возраста ребенка, возбудителя заболевания и его вирулентности.
В зависимости от локализации процесса различают - подкожные, субфасциальные, внутримышечные, забрюшинные, медиастинальные флегмоны.
Клиническая картина характеризуется быстрым появлением процесса и его распространением: отек, боль, гиперемия, нарушение функции пораженной части тела, локальная гипертермия. На ранних стадиях - плотный инфильтрат, в запущенных случаях - определяется флюктуация. При прогрессирующей флегмоне прогноз неблагоприятный.
Код протокола: H-S-031 "Флегмона подкожной клетчатки у детей"
Классификация
Факторы и группы риска
Наличие повреждений кожного покрова с признаками инфицирования, другие гнойно-воспалительные процессы.
Диагностика
В некоторых случаях наступает некроз кожи, ее отторжение с образованием обширных раневых дефектов. Дно раны серого цвета с остатками омертвевшей клетчатки, края подрытые, неровные, грануляции отсутствуют. Такой вид раны заставляет думать о неблагоприятном прогнозе. При благоприятном течении после отторжения омертвевшей кожи образуются раны небольших размеров (3-6 см в диаметре), которые постепенно выполняются грануляциями, постепенно эпителизирующимися по краям. В дальнейшем на месте раневого дефекта часто образуются грубые рубцы, вызывающие деформацию грудной клетки, поясничный лордоз и кифоз, прогрессирующие с ростом ребенка.
Лечение
Цели лечения: оперативное лечение и санация гнойных очагов, восстановление исходного состояние кожных покровов, предотвращение рецидивов.
Лечение
Под общим обезболиванием производят множественные разрезы кожи в шахматном порядке над очагом поражения и по границе со здоровой кожей. Длина разреза 1-1,5 см, в глубину они должны проникать до подкожной жировой клетчатки.
Затем накладывают повязку с гипертоническим раствором хлорида натрия или антисептиком (фурацилин, диоксидин, хлоргексидинтиоглюконат, перманганат калия) на 2-3 часа. При последующих перевязках следят за распространением процесса, в случае необходимости производят дополнительные разрезы. При некрозе кожи и появлении демаркационной линии производят некрэктомию. После очищения раны от некротических масс и гноя используют мазевые повязки. На протяжении всего лечения применяют физиотерапевтические процедуры (УФО, УВЧ и др.), а также стимулируют рост и эпителизацию грануляций путем применения консервированной плаценты, фибринной пленки, обработки раны ультразвуком, лучами лазера.
Параллельно местной проводят интенсивную терапию, в комплекс которой должны входить дезинтоксикационные, антибактериальные и иммуностимулирующие мероприятия. Для лечения и профилактики возникновения микоза при длительной массивной антибиотикотерапии - итраконазол оральный раствор из расчета 5 мг\кг\день, в течение 10 дней.
Прогноз при флегмоне новорожденных всегда серьезен. Чем раньше поставлен диагноз и начаты лечебные мероприятия, тем больше вероятность благоприятного исхода заболевания. Летальность по разным данным - 15-30%.
4. *Тикарциллин + клавулановая кислота, лиофилизированный порошок 3000 мг/200 мг для приготовления раствора для внутривенных инфузий
5. *Амоксициллин+клавулановая кислота таблетки, покрытые оболочкой 500 мг/125 мг, 875 мг/125 мг, порошок для приготовления раствора для внутривенного введения во флаконах 500 мг/100 мг, 1000 мг/200 мг
27. *Препараты, получаемые из крови, плазмозамещающие средства и средства для парентерального питания
Индикаторы эффективности лечения: восстановление исходного состояние кожных покровов, предотвращение рецидивов.
* – препараты, входящие в список основных (жизненно важных) лекарственных средств.
Сепсис новорожденных – генерализованная гнойно-септическая инфекция, характеризующаяся наличием первичного очага и циркуляцией инфекции в крови. Сепсис новорожденных проявляется признаками инфекционного токсикоза (температурной реакцией, вялостью, диспепсией, землистой окраской кожных покровов) и образованием гнойных метастатических очагов в различных органах (мозговых оболочках, легких, костях, печени и пр.). Диагноз сепсиса у новорожденных устанавливается на основании клинических критериев и выделения возбудителя при бактериологическом посеве крови. Лечение сепсиса новорожденных включает системную антибиотикотерапию, санацию первичного и метастатических гнойных очагов, посиндромную терапию.
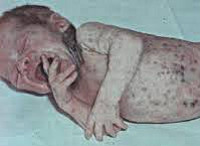
Общие сведения
Сепсис новорожденных – общий инфекционный процесс, обусловленный попаданием условно-патогенной и гноеродной микрофлоры из локальных очагов в кровяное русло и сопровождающийся тяжелыми системными проявлениями. По данным зарубежной педиатрии, частота сепсиса новорожденных составляет 0,1-0,8%; среди недоношенных и детей с перинатальной патологией, находящихся в ОРИТ, - 14%. Неонатальная смертность, обусловленная сепсисом новорожденных, высока и стабильна – около 30-40%. Развитию сепсиса способствуют недостаточная сформированность барьерных механизмов и иммунитета у новорожденных, пограничные состояния периода новорожденности, патологическое протекание перинатального периода, сложность ранней диагностики септических состояний.

Причины
В настоящее время доминирующее место (около 50%) среди возбудителей сепсиса новорожденных принадлежит грамположительной флоре (главным образом, стафилококкам, гемолитическому стрептококку группы А). Чуть реже (до 40% случаев) выявляется грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, клебсиелла и др.); в 10% этиологическими агентами выступает смешанная флора (часто ассоциация стафилококка с грибами Candida).
Со стороны матери факторами, способствующими бактериальной контаминации новорожденного, выступают бактериальный вагиноз, кольпиты, эндометрит. Большое значение имеет степень и характер иммуносупрессии у новорожденного, которые могут быть связаны с неполноценным питанием или приемом лекарств беременной, наследственным иммунодефицитом или ВИЧ-инфекцией. В отдельных случаях причиной вспышек сепсиса новорожденных становится несоблюдение санитарного режима в родильных или детских отделениях.
Классификация
По времени развития выделяют внутриутробный и постнатальный (ранний неонатальный и поздний неонатальный) сепсис новорожденных. Внутриутробный сепсис предполагает антенатальное или интранатальное инфицирование плода; при этом первичный гнойно-септический очаг располагается вне организма ребенка (чаще всего в его роли выступает плацентит, хорионит, хориоамнионит и т. д.). В случае постнатального сепсиса первичный гнойно-воспалительный очаг всегда располагается в организме самого новорожденного.
Ранний неонатальный сепсис новорожденных развивается в первые 4-ро суток жизни ребенка. Клинические течение заболевания обычно молниеносное, с быстрым развитием полиорганнной недостаточности, летальным исходом в 5-20% случаев. Поздний неонатальный сепсис новорожденных манифестирует на 5-й день и позднее. Характеризуется медленно прогрессирующим течением, возникновением вторичных септических очагов, 5-10%-ной летальностью.
Течение сепсиса новорожденных может быть молниеносным (3-7 дней), острым (до 4-8 недель), подострым (до 1,5-3 месяцев), затяжным (более 3 месяцев). С учетом локализации первичного септического очага и входных ворот различают: пупочный, кожный, легочный, ринофарингеальный, отогенный, риноконъюнктивальный, кишечный, урогенный, катетеризационный и др. виды сепсиса новорожденных. Сепсис новорожденных может протекать в форме септицемии или септикопиемии.
Симптомы сепсиса новорожденных
Септицемия или сепсис новорожденных без метастазов обычно развивается на фоне предшествующего мокнущего пупка, конъюнктивита, гнойничковой сыпи, опрелостей, стоматита. Предвестниками сепсиса новорожденных могут выступать вялость или беспокойство, снижение аппетита, обильные частые срыгивания, плохая прибавка в весе. В период разгара развивается температурная реакция (гипер- или гипотермия), отечный синдром или эксикоз, гипотрофия. Характерным признаком сепсиса новорожденных является грязновато-серый (землистый) оттенок кожных покровов, желтушность, мраморность кожи, сыпь.
Вследствие токсического поражения различных органов возникают гепатоспленомегалия, пневмопатия (тахипноэ, цианоз), кардиопатия (тахикардия или брадикардия, артериальная гипотензия), диспепсия, мочевой синдром (олигурия, анурия, ОПН), геморрагический синдром, надпочечниковая недостаточность. Чаще всего септицемия осложняется присоединением пневмонии, которая выступает как самостоятельное интеркуррентное заболевание.
Септикопиемия или сепсис новорожденных с гнойными метастазами характеризуется возникновением на фоне интоксикации вторичных очагов отсева в мозговых оболочках, легких, костях, печени, других органах. Чаще всего септикопиемия протекает с развитием гнойного менингита, абсцедирующей пневмонии, остеомиелита; реже – с формированием абсцесса печени, гнойного артрита, панофтальмита, медиастинита, флегмоны желудка или кишечника. В восстановительном периоде происходит санация пиемических очагов, стихание токсикоза, постепенное восстановление нарушенных функций.
Молниеносная форма сепсиса новорожденных протекает с развитием септического шока: стремительным ухудшением состояния ребенка, снижением температуры тела, брадикардией, кровоточивостью, отеком легких, острой почечной недостаточностью. Летальный исход при молниеносном течении сепсиса новорожденных наступает в течение 3-5 суток.
Диагностика сепсиса новорожденных
Диагноз сепсиса новорожденного может быть заподозрен неонатологом или педиатром на основании лихорадки свыше 3 дней или прогрессирующей гипотермии; гиперлейкоцитоза, сменяющегося лейкопенией; повышением содержания в крови маркеров инфекционного процесса (СРБ, интерлейкина-8, прокальцитонина).
Факт бактериемии при сепсисе новорожденных подтверждается путем посева крови на стерильность. Важное значение имеет выявление первичного гнойного очага и метастатических очагов, микробиологического исследование отделяемого из них (бактериологическое исследование мазка с конъюнктивы, мочи на микрофлору, соскоба/отделяемого с кожи на микрофлору, мазка из глотки, кала на дисбактериоз и т. п.).
Дифференциальная диагностика сепсиса новорожденных осуществляется с локализованными гнойно-воспалительными заболеваниями (пневмонией, медиастинитом, перитонитом, менингитом, энтероколитом), генерализованными вирусными инфекциями (цитомегалией, герпесом, энтеровирусной инфекцией) и микозами (кандидозом, аспергиллезом) и др. Для этого используются дополнительные лабораторные методы – ПЦР, ИФА, микроскопия.
Лечение сепсиса новорожденных
Терапия при сепсисе новорожденных проводится одновременно в нескольких направлениях и включает санацию септического и пиемических очагов, подавление циркуляции возбудителя в крови, коррекцию нарушенных функций.
Основу этиологического лечения сепсиса новорожденных составляет антибиотикотерапия: эмпирическая комбинированная до уточнения характера микрофлоры) и целенаправленная после получения антибиотикограммы. Противомикробные препараты вводятся внутривенно, в максимальных возрастных дозировках в течение 10-15 суток с последующей сменой. Чаще всего в клинической практике для лечения сепсиса новорожденных в различных сочетаниях используются цефалоспорины, аминогликозиды, аминопенициллины, карбапенемы и др.
С целью местного лечения гнойных очагов производится вскрытие фурункулов и абсцессов, перевязки с антибактериальными и ферментными препаратами; назначается УВЧ, СВЧ, электрофорез.
Патогенетическая терапия сепсиса новорожденных включает иммунокоррекцию (плазмаферез, гемосорбцию, введение иммуноглобулинов), проведение дезинтоксикационной терапии (внутривенной инфузии глюкозо-солевых растворов и свежезамороженной плазмы), адекватную кислородотерапию и т. д. При сепсисе новорожденных обязательно проводится мониторинг состояния жизненно-важных функций: АД, ЧСС, ЭКГ, КОС и газового состава крови, биохимических показателей (сахара крови, креатинина, электролитов), гематокрита.
В остром периоде сепсиса целесообразно пребывание новорожденных в кувезе, кормление материнским молоком, тщательный уход. В восстановительном периоде к лечению подключается гимнастика, массаж, лечебные ванны.
Прогноз и профилактика сепсиса новорожденных
Прогноз сепсиса новорожденных серьезный: летальность составляет от 30-40% до 60% среди глубоко недоношенных детей. У выздоровевших детей в отделенном периоде могут отмечаться частые ОРВИ, пиелонефрит, анемия, перинатальная энцефалопатия.
Профилактика сепсиса новорожденных включает выявление и санацию инфекций мочеполовой сферы у беременной, соблюдение противоэпидемических мероприятий медперсоналом родильных домов и отделений новорожденных, тщательный гигиенических уход за новорожденным, естественное вскармливание. Вопрос о сроках вакцинации новорожденных с сепсисом против туберкулеза и против гепатита В , проводимой в первые дни жизни, решается в индивидуальном порядке.
Это острое гнойное воспаление мягких тканей и/или внутренних органов (средостенье, брюшная полость, забрюшинное пространство, малый таз и т.д.).
Название происходит от греческого слова, означающего воспаление или отек.
Флегмона может поражать внутренние органы, такие как аппендикс, почки, печень, селезёнка, сосуды кишечника, предстательной железы, поджелудочной железы, или находиться где угодно под кожей.
Имеет свойство быстро распространяться и в ряде случаев может быть опасной для жизни.
Что вызывает флегмону, причины
Причиной развития флегмоны является проникновение, активное развитие и распространение инфекции. В результате чего формируется гнойное расплавление тканей (жировой, мышечной, и т.д.) с повреждением близлежащих органов (стенки сосуда, кишки, почки и т.д.).
Флегмона обычно вызывается бактериями: чаще аэробными, такими как стрептококки, золотистый стафилококк и т.д, реже анаэробами (образующими споры).
Другие факторы, которые влияют на развитие флегмоны:
- наличие хронической интоксикации за счет хронического воспаления, отравления, приема химиопрепаратов, лучевой болезни,
- обширные тяжелые травмы,
- состояние иммунитета пациента,
- вирулентность бактерий (способность вызвать заболевание).
Бактерии могут проникнуть через царапину, укус насекомого или травму с образованием флегмоны прямо под кожей. Также могут перемещаться с током крови из воспаленного органа (абсцесс почки, легкого, печени, аппендикулярный абсцесс, параректальный абсцесс и т.д.).
Бактерии могут также прикрепляться к стенке внутреннего органа, такого как стенка желудка или аппендикс, и образовывать флегмону.
Люди с ослабленной иммунной системой могут быть особенно уязвимы для формирования флегмоны.
Симптомы и проявления флегмоны
Различаются в зависимости от места и тяжести инфекции.
Основными симптомами являются покраснение кожи и отек в месте воспаления.

Флегмона мягких тканей на фоне прогрессирующего абсцесса
Пораженная часть тела чувствительна к прикосновениям и болит. К этому симптому позже добавляется лихорадка. Могут возникать опухшие связанные лимфатические узлы.
Проявления флегмоны кожи
- покраснение кожи
- воспаление
- блезненный отек тканей
- опухшие лимфатические узлы
- повышенная локальная температура
- усталость
- лихорадка
- головная боль
Внутренние органы
Флегмона может поражать любой внутренний орган. Симптомы могут варьироваться в зависимости от органа и конкретных бактерий.
- нарушение функции органа
- боль в животе
- лихорадка
- озноб
- тошнота
- рвота
- понос
- кишечная непроходимость
- повышенная температура тела
- потеря аппетита
- увеличение жажды
- потоотделение
- увеличение лейкоцитов (лейкоцитоз)
Диагностика флегмоны
- симптомы, жалобы, когда они начались и как долго продолжаются,
- физическое обследование пациента,
- предыдущая история болезни пациента, принимаемые препараты,
- пальпация при физикальном осмотре.
Кожная флегмона всегда видна, в то время как внутренние флегмоны диагностировать сложнее.

Анаэробная флегмона спины
Обследования могут включать:
- анализ крови
- анализ мочи
- УЗИ
- рентген
- МРТ (магнитно-резонансная томография)
- КТ (компьютерная томография)
Как лечится флегмона?
Лечение только оперативное. Объем операции напрямую зависит от локализации, глубины и площади поражения.
Основной целью лечения является:
- купирование гнойного расплавления тканей,
- дренирование гнойного отделяемого, что исключает всасывание продуктов распада и отравление организма продуктами распада,
- ликвидация очага развития флегмоны, что обеспечивает устранение причины флегмонозного процесса, чтобы можно было добиться полного выздоровления и предотвратить рецидив.
Консервативное лечение возможно только в двух случаях:
- когда флегмона в самом начале своего развития и нет чёткого очага нагноения (встречается крайне редко),
- как второй этап лечения после полноценного вскрытия.
В тяжелых случаях требуется хирургическое вмешательство для дренирования флегмоны, удаления мертвых тканей и предотвращения дальнейшего распространения инфекции.

Дренирование флегмоны мягких тканей спины
Операция проводится под общим наркозом, где полость, в которой находится флегмонозный процесс, очищается антибиотиками и антисептическими растворами, а мертвая ткань удаляется. Внутривенные антибиотики назначаются пациенту в послеоперационном периоде.
Осложнения флегмоны

Гнойно-некротическая флегмона голени в процессе очищения раневой поверхности и формирования грануляций
- гангрена,
- сепсис,
- тромбоз артерий и вен нижних конечностей, мезентериальных сосудов,
- абсцессы печени, почек, селезёнки, органов дыхания, лёгких, головного мозга,
- тромбэмболия мелких и крупных ветвей легочной артерии,
- полиорганная недостаточность.
При прогрессирующем заболевании гной накапливается в более глубоких слоях кожи, вызывая развитие воспаления окружающих тканей, затрагивая кровеносные и лимфатические сосуды и нервы.

Флегмона задней поверхности бедра
Разница между флегмоной и абсцессом
При абсцессе гнойный очаг чётко отграничен от окружающих тканей без тенденции к распространению.

Постинъекционный абсцесс

Абсцесс голени, развившийся после укуса кошки

Флегмона задней поверхности голени
Но иногда бывают случаи, когда не просто отличить абсцесс от флегмоны, особенно в начальной стадии её формирования, в тот самый период, когда содержимое гнойной полости (сукровица, гной, фибрин) выходит из-под контроля и только начинает распространяться по окружающим тканям.

Абсцесс, осложнившийся флегмоной мягких тканей
Прогноз и перспективы
Зависят от тяжести инфекции и области, которая заражена.
При своевременно начатом комплексном лечении (полноценная операция и адекватная консервативная терапия) перспективы и прогноз благоприятные. В запущенных случаях и при неадекватном лечении перспективы и прогноз значительно хуже, вплоть до негативных из-за крайне быстро развивающихся тяжёлых осложнений (сепсис, почечно-печёночная и сердечно-лёгочная полиорганная недостаточность).
Профилактика развития флегмоны
Заключается в своевременном и полноценном лечении любых ран и любых нагноений кожи, которое не допустит проникновения инфекции в мягкие ткани. При развитии любого нагноения (инфицированная рана, фурункул, гидраденит, абсцесс, парапроктит и т.д.) необходимо полноценное и своевременное вскрытие гнойника + адекватная санация и дренирование гнойной полости.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Сепсис новорожденных - генерализованная форма гнойно-воспалительной инфекции, вызванной условно-патогенной бактериальной микрофлорой, патогенез которой связан с дисфункцией иммунной системы (преимущественно фагоцитарной) с развитием неадекватной системной воспалительной реакции (СВР) в ответ на первичный септический очаг.
Системная воспалительная реакция - общебиологическая неспецифическая иммуноцитологическая реакция организма в ответ на действие повреждающего эндогенного или экзогенного фактора. В случае развития инфекции СВР возникает в ответ на первичный гнойно-воспалительный очаг. Для СВР характерно бурное нарастание продукции провоспалительных (в большей степени) и противовоспалительных (в меньшей степени) цитокинов, неадекватное действию повреждающего фактора, что индуцирует апоптоз и некроз, обусловливая повреждающее действие СВР на организм.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Код по МКБ-10
Эпидемиология сепсиса новорожденных
В отечественной литературе нет достоверных данных о частоте инфекции среди новорождённых, что в значительной степени связано с отсутствием общепринятых диагностических критериев диагноза. По зарубежным данным, частота септических состояний среди новорождённых составляет 0,1-0,8%. Особый контингент больных - дети, находящиеся в отделениях реанимации и интенсивной терапии (ОРИТ), а также недоношенные новорождённые, среди них частота развития данного заболевания в среднем составляет 14%.
В структуре неонатальной смертности септические состояния составляет в среднем 4-5 на 1000 живорождённых. Показатели летальности от инфекции крови также довольно стабильны и составляют 30-40%.

[11], [12], [13], [14], [15]
Чем вызывается сепсис новорожденных?
Септическое состояние обусловлен исключительно условно-патогенной микрофлорой. В ряде случаев, например при иммунодефиците новорождённого, инфекция крови может быть составной частью генерализованной смешанной инфекции - вирусно-бактериальной, бактериальногрибковой и т.д.
Причиной данного заболевания у детей могут стать свыше 40 условно-патогенных микроорганизмов, но чаще всего инфекция крови обусловлен стрептококками, стафилококками, кишечной палочкой, клебсиеллой и другими грамотрицательными бактериями и анаэробами.
Этиологическая структура сепсиса новорождённых зависит от времени инфицирования плода и новорождённого.
Ранний (врождённый) неонатальное септическое состояние чаще всего обусловлен грамположительными кокками S. agalacticae относящимися к стрептококкам группы В. Данный возбудитель может быть причиной антенатального и интранального инфицирования плода;
Наиболее вероятная этиология раннего сепсиса новорождённых в зависимости от времени инфицирования плода и новорождённого
S. agalacticae
E. coli (редко)
S. agalacticae
E. coli
S. aureus
S. aureus et epidermidis
E. coli
Klebsiella spp.
S. pyogenes
E. coli и другие представители семейства кишечных грамотрицательных бацилл вызывают инфицирование плода значительно реже.
Поздний неонатальный сепсис новорожденных обычно возникает вследствие постнатального инфицирования. Основные возбудители - E. coli, S. aureus и Klebsiella pneumoniae; стрептококки группы В встречаются редко. Возрастает значение стрептококков группы А, псевдомонад и энтерококков.
В структуре грамотрицательных возбудителей данного заболевания, составляющих около 40%, в течение последних 10 лет произошли некоторые изменения. Возросла роль Pseudomonas spp. Klebsiella spp. и Enterobacter spp. Как правило, эти возбудители вызывают инфекцию крови у пациентов ОРИТ, находящихся на искусственной вентиляции лёгких (ИВЛ) и парентеральном питании, хирургических больных.
На этиологическую структуру постнатальной заболеваемости существенное влияние оказывает локализация первичного септического очага. Например, в этиологии пупочного вида инфекции ведущую роль играют стафилококки и E. coli, а в этиологии кожного и риноконъюнктивального септического состояния - стафилококки и ß-гемолитические стрептококки группы А. Также спектр возбудителей госпитальной инфекции зависит от входных ворот инфекции. Например, при катетеризационном септическом состоянии преобладающую роль играют стафилококки или смешанная генерализованная инфекция, обусловленная ассоциацией стафилококков с грибами рода Candida. При абдоминальном госпитальной инфекции часто выделяют энтеробактерии, анаэробы.
Наиболее вероятные возбудители сепсиса новорождённых в зависимости от локализации первичного очага инфекции
Локализация первичного очага
Наиболее вероятные возбудители
S. aureus et epidermidis
E. coli
K. pneumoniae
S. aureus et epidermidis Ps. aeruginosa (при ИВЛ)
Acinetobacter spp. (при ИВЛ)
Enterobacteriaceae spp.
Enterobacter spp.
Брюшная полость (после хирургических вмешательств)
Enterobacteriaceae spp.
Enterococcus spp.
Ps. aeruginosa
Анаэробы
Кожа, риноконъюнктивальная область
S. epidermidis et aureus
S. pyogenes et viridans
Ротоглотка и носоглотка, среднее ухо
S. epidermidis et aureus
S. pyogenes et viridans E. coli
E. coli и другие виды семейства Enterobacteriaceae Enterococcus spp.
Венозное русло (после применения внутривенного катетера)
S. aureus et epidermidis
Этиология генерализованных инфекций у иммунокопрометированных пациентов (в том числе у глубоко незрелых новорождённых) также имеет ряд особенностей и зависит от характера иммуносупрессии (приобретённые дисфункции иммунной системы, вторичная иммунная недостаточность, медикаментозная иммуносупрессия, врождённая, наследственная или приобретённая нейтропения, первичные иммунодефициты и ВИЧ-инфекция). Далеко не всегда инфекцией, развивающейся на таком фоне, бывает именно сепсис новорождённых.
Патогенез сепсиса новорожденных
Пусковой момент заболевания - наличие первичного гнойного очага на фоне изначальной несостоятельности противоинфекционной защиты. В этой ситуации массивное микробное обсеменение, превосходящее возможности противомикробной защиты, приводит к прорыву инфекционного начала в системный кровоток больного (бактериемия).
Наиболее вероятные возбудители генерализованных инфекций при иммунодефицитах у младенцев
Наиболее вероятные возбудители
Вторичные иммунные дисфункции, включая дисфункции при гестационной незрелости
Enterobacteriaceae spp.
Staphylococcus spp.
S. pyogenes
Грибы рода Candida
Цитомегаловирус
Enterobacteriaceae spp.
S. Aureus
Грибы рода Aspergillus et Candida
S. aureus E. coli
Грибы рода Candida
Оппортунистическая микрофлора (грибы, микобактерии, цитомегаловирус и т.д.)
Enterobacterioceae spp.
S. aureus et epidermidis Гемолитические стрептококки группы А
Помимо описанного выше, нейтрофилы играют роль фагоцитов. Значимость фагоцитоза, осуществляемого нейтрофилами и макрофагами, существенно различается - истинный фагоцитоз осуществляют именно макрофаги. Нейтрофильный фагоцитоз, хотя и протекает более интенсивно, чем у мононуклеаров, обусловлен другими биохимическими процессами, потому что задача у них иная. Основная функция нейтрофилов - инициация воспалительной реакции. Биологически активные вещества, секретируемые нейтрофильными гранулоцитами, имеют провоспалительную направленность; среди них различают цитокины, работающие в очагах острого воспаления (ИЛ-8, ИЛ-1, фактор некроза опухоли, гранулоцитарно-макрофагальный колониестимулирующий фактор и гранулоцитарный колониестимулирующий фактор) и участвующие в регуляции хронического воспаления (ИЛ-6, у-интерферон, трансформирующий фактор роста). Нейтрофилы синтезируют широкий спектр поверхностных адгезивных молекул, с помощью которых они взаимодействуют с клетками эндотелия сосудов, иммунной системы, тканей и органов. В результате адгезии изменяется чувствительность самих нейтрофилов к цитокинам и другим медиаторам, что позволяет им адекватно реагировать на изменения в тканях и органах. Цитотоксичность нейтрофилов значительно выше, чем у киллерных лимфоидных клеток (Т-лимфоцитов) и натуральных киллеров (NК-клеток). Факторы цитотоксичности нейтрофилов нацелены на ядерные структуры клеток-мишеней, структурные элементы генетического аппарата поглощённого объекта, разрушение генома с использованием факторов, индуцирующих апоптоз (ФИА). Клетки, подвергающиеся апоптозу, становятся объектами фагоцитоза и быстро разрушаются.
Нейтрофилы активно фагоцитируют микроорганизмы, не заботясь об истинном их переваривании, выбрасывают в межклеточное пространство значительные количества ФИА, чтобы как можно быстрее вызвать повреждения генетического аппарата патогенных микроорганизмов. Влияние высвобождения содержимого нейтрофильных гранул на процессы воспаления огромно. Содержимое нейтрофильных гранул индуцирует агрегацию тромбоцитов, выход гистамина, серотонина, протеаз, производных арахидоновой кислоты, активаторов свёртывания крови, системы комплемента, кинин-каллекреиновой системы и др. ФИА нейтрофилов губительны для любых клеток, так как вызывают разрушение нуклеопротеиновых комплексов генома.
Таким образом, в условиях инфекционного процесса нейтрофилы инициируют СВР, участвуют в презентации антигена возбудителя для активации специфического иммунного ответа организма. При чрезмерной активации нейтрофилов их цитотоксическое действие не ограничивается чужеродными клетками, реализуясь в отношении собственных клеток и тканей организма.
Чрезмерная СВР лежит в основе гиперактивации гипоталамо-гипофизарно-надпочечниковой системы, в норме обеспечивающей адекватную реакцию организма на стресс. Активация этой системы приводит к выбросу АКТГ и повышению содержания кортизола в крови. Чрезмерная активация гипоталамо-гипофизарно-надпочечниковой системы при септическом шоке, молниеносном течении данного заболевания приводит к неадекватной реакции на выброс АКТГ. Наряду с этим значительно снижается функциональная активность щитовидной железы, с чем связано замедление окислительного метаболизма, ограничивающее адаптивные возможности организма новорождённого. При тяжёлом септическом состоянии (молниеносное течение, септический шок) у ряда больных падает содержание соматотропного гормона (СТГ). Низкое содержание СТГ в условиях базальной гиперкортизолемии способствует бурному развитию некротических процессов (СТГ тормозит воспалительный процесс).
Другое проявление неадекватной СВР - неуправляемая активация свёртывающей системы крови, в условиях нарастающей депрессии фибринолиза неизбежно приводящая к тромбоцитопатии и коагулопатии потребления.
Таким образом, СВР, индуцированная чрезмерной активацией нейтрофилов периферической крови, активацией гипоталамо-гипофизарно-надпочечниковой системы и системы гемостаза, лежит в основе формирования полиорганной недостаточности, приводящей к глубоким расстройствам гомеостаза, иногда несовместимым с жизнью.
Для мононуклеаров нейтрофилы - клетки-помощники. Основная роль моноцитов и макрофагов - истинный фагоцитоз с дальнейшим тщательным перевариванием полуразрушенных нейтрофилами частиц клеток-мишеней, самих нейтрофилов и воспалительного клеточного дендрита. Фагоцитоз, осуществляемый макрофагами, способствует стиханию процессов воспаления и заживлению повреждённых тканей.
Формирование медиаторного ответа на бактериальную инфекцию, лежащего в основе синдрома СВР, - генетически контролируемый процесс, в котором участвуют рецепторы клеток, распознающие различные структуры микробного происхождения и индуцирующие экспрессию факторов неспецифической резистентности.
Синдром СВР лежит в основе прогрессирующей органной дисфункции, в ряде случаев достигающей степени органной недостаточности. Для патогенеза септического состояния характерно стремительное развитие полиорганной недостаточности и глубокие расстройства гомеостаза. Один из признаков нарушения гомеостаза при инфекции крови - выраженная пролиферация условно-патогенной микрофлоры, создающая предпосылки для возникновения новых инфекционных очагов и дополнительной транслокации инфекционного начала в системный кровоток. В настоящее время популярна концепция, согласно которой нарушения гомеостаза связаны с попаданием в кровь эндотоксина или липополисахаридного комплекса эндотоксина грамотрицательных бактерий, бурно колонизирующих верхние отделы тонкого кишечника в условиях тканевой гипоксии. Эндотоксин значительно усиливает СВР, провоцирует нарушения гомеостаза, рефрактерную к лечению гипотензию. Поступление в кровоток антигенов приводит к дезорганизации СВР - медиаторному хаосу. Антигенная перегрузка - причина выраженной иммуносупрессии в условиях бактериемии и нарушения микроциркуляции, способствующая формированию метастатических гнойных очагов, поддерживающих СВР, токсинемию и антигенемию. Дезорганизация СВР - основа развития септического шока.
Симптомы сепсиса новорождённых
Симптомы сепсиса новорожденных, независимо от формы (септицемия или септикопиемия), характеризуются тяжесть общего состояния новорождённого. Выражены нарушения терморегуляции (у доношенных морфофункционально зрелых новорождённых - лихорадка, у недоношенных, маловесных детей, на отягощённом преморбидном фоне - прогрессирующая гипотермия), нарушено функциональное состояние ЦНС (прогрессирующее угнетение). Характерен грязновато-бледный или сероватый оттенок кожных покровов с желтушностью и геморрагиями, участками склеремы. Выражена мраморность кожи, возможен акроцианоз. Рано возникает и быстро нарастает желтуха. Нередко развивается общий отёчный синдром. Характерна склонность к спонтанной кровоточивости. Черты лица нередко заострены.
Дыхательная недостаточность развивается без воспалительных изменений на рентгенограмме, часто происходит повреждение сердца по типу токсической кардиопатии, сопровождающееся развитием острой сердечной недостаточности. Характерно увеличение размеров селезёнки и печени, вздутие живота, выражена венозная сеть на передней брюшной стенке, часто наблюдаются срыгивания, рвота и анорексия, дисфункция желудочно-кишечного тракта вплоть до пареза кишечника. Типично отсутствие прибавки массы тела, формирование гипотрофии.
Для недоношенных детей типично подострое течение данного заболевания в виде синдрома дыхательных расстройств (одышка с периодами брадипноэ или апноэ), брадикардии, нарушения сосательного рефлекса, тенденции к гипотермии. Перечисленные симптомы сепсиса новорожденных отражают различные степени развития полиорганной недостаточности. Наиболее типичные синдромы полиорганной недостаточности при инфекции крови, а также характерные для них изменения, обнаруживаемые при лабораторных и инструментальных методах обследования, отражены в таблице.
Первичный септический очаг
Как было отмечено выше, изучая клиническую картину заболевания при позднем сепсисе новорождённых, в большинстве случаев можно обнаружить первичный септический очаг.
После внедрения первичной хирургической обработки пуповинного остатка произошло снижение частоты возникновения омфалита; в настоящее время эти заболевания встречаются не более чем в трети случаев. На этом фоне значительно возросла частота развития лёгочного (до 20-25%) и кишечного септического состояния (не менее 20%). Другие локализации первичного очага встречаются значительно реже и не превышают 2-6%. В отдельных случаях входные ворота инфекции установить не удаётся. Это особенно характерно для детей с малым гестационным возрастом, у которых слабо выражены процессы альтерации.
Клинические и лабораторные критерии органной недостаточности при септическом состоянии (Балк Р. и др., 2001, в модификации)
Читайте также:

