Гемибиотрофный паразит что это
Обновлено: 06.05.2024
Кости и мышцы при паразитарной инфекции - лучевая диагностика
а) Визуализация:
• Характеризуется вторичной кальцификацией мягких тканей вследствие кальцификации погибших гельминтов
• Цистицеркоз (свиной цепень):
о Множественные мелкие линейные/овоидные очаги кальцификации расположенные вдоль длинной оси брюшка мышцы
о Проглоченные гельминты проникают в тонкий кишечник и перемещаются в подкожную жировую клетчатку и мышцы
о Характерные очаги инфекции: легкие, головной мозг, глаза, печень
о ↑ заболеваемости на западе Америки, особенно среди латиноамериканцев
• Дракункулез (ришта):
о Кальцифицированные женские особи гельминтов: линейные, могут быть закрученные или фрагментированные; чаще в нижних конечностях
о Употребление зараженной воды
о Другие проявления: стерильные абсцессы, асептический артрит
(Слева) Фронтальная КТ: множественные овальные внутримышечные кальцификаты, характерные для цистицеркоза. Следует отметить, что на сегодняшний день эта паразитарная инфекция чаще встречается на западе США, особенно у латиноамериканцев.
(Справа) Рентгенография в ПЗ проекции: множественные овоидные, имеющие форму риса, кальцификаты, ориентированные вдоль длинной оси мышечных волокон бедра. Классическая картина цистицеркоза. (Слева) Рентгенография в ПЗ проекции: процесс остеолизиса, поражающий проксимальную часть бедренной кости, неровный наружный край кортикального вещества кости. Визуализируется образование мягких тканей с периферической минерализацией.
(Справа) Аксиальный КТ-срез с КУ, этот же пациент: визуализируется мягкая ткань внутри костного мозга с внутрикостной деструкцией. Образование мягких тканей - многодольчатая кистозная структура. Отмечается минерализация стенки кисты. Находки типичны для эхинококкоза костей и мягких тканей.
• Эхинококкоз (гидатидная болезнь):
о Кальцификация по типу яичной скорлупы по периферии кисты
о Паразит попадает с пищей; человек-промежуточный хозяин
о Наиболее часто поражаются: легкие, печень
о Костно-мышечные очаги: позвоночник, кости таза, конечности
о Классическое проявление: множественные кисты (комплексы по типу виноградной грозди) с дочерними кистами
о Очаги могут быть мягкотканными или костными с распадом ± увеличение кости
о МРТ Т1 ВИ: жидкость имеет различную интенсивность сигнала от низкой до высокой; зависит от содержания белка
о MPT С+: усиление кисты по периферии и в перегородках
б) Дифференциальная диагностика:
• Линейная кальцификация мягких тканей: сосудистая, дерматомиозит
• Очаговая кальцификация мягких тканей: флеболиты, гранулемы

Тип питания (степень паразитизма) – способность микроорганизма извлекать питательные вещества для собственного роста и размножения из живого, ослабленного или погибшего организма-хозяина, для фитопатогена – растения-хозяина [2] .
Тип питания микроорганизма может быть сапрофитным или паразитическим. Паразиты, в свою очередь, делятся на некротрофов, биотрофов и гемибиотрофов.
Трофность
Сапротрофы – извлекают питательные вещества из имеющихся (готовых) мертвых тканей и являются сапрофитами [2] .
Некротрофы – паразиты, убивающие своими выделениями какой-либо участок растения, прежде, чем оккупировать его, то есть как и сапротрофы питаются содержимым мертвых клеток [2] .
Биотрофы – паразиты, извлекающие питательные вещества непосредственно из живых клеток растения-хозяина [2] .
Различия между сапротрофами, некротрофами и биотрофами заключаются в соотношении скоростей гибели зараженных тканей (некроза) иразвития паразита в растении.
На практике тип питания определяется достаточно просто. Если распространение некроза опережает распространение паразита, то тип питания – некротрофный. Если распространение паразита опережает некроз – питание биотрофное [2] .
При некротрофном паразитизме воздействие на клетки хозяина более грубое, чем при биотрофном. Некротрофный тип питания менее специализирован и скорее всего, является первичным. Эволюцию типов питания от сапротрофии к биотрофии прослеживают у почвообитающих грибов. В их числе обнаруживаются различные переходные виды [2] .
Гемибиотрофы – переходная форма между некротрофами и биотрофами. Это паразиты, имеющие смешанное питание. Первоначально они питаются биотрофно, а после гибели зараженной ткани, продолжают развиваться в ней, питаясь некротрофно [2] .
Примером гемибиотрофного микроорганизма является возбудитель парши яблони – гриб Venturia inaegualis. Первоначально данный патоген образует внутритканевый (эндофитный) мицелий между мезофиллом и эпидермисом, не повреждая клеток, то есть питается биотрофно. После гибели клеток Venturia inaegualis распространяется в них некротрофно, а после отмирания и опадения листьев продолжает питаться сапротрофно [1] [2] .

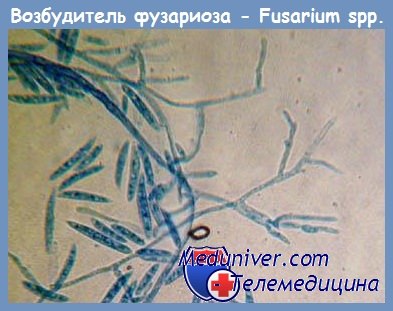
Конидии и конидиеносцы гемибиотрофного гриба

Четыре группы степени паразитизма
Автотрофы – организмы, способные создавать в процессе фотосинтеза органическое вещество. Паразитические микроорганизмы, как известно, к таким не относятся [3] .
Гетеротрофы – организмы не способные самостоятельно вырабатывать органическое вещество и питающиеся только за счет органики, создаваемой автотрофами и, находящиеся в определенной зависимости от них как от источника энергии. К таким организмам относятся грибы, все бактерии, фитоплазмы, вирусы [3] .
По способу использования органического вещества (типу питания) все гетеротрофы делят на четыре группы:
- сапрофиты облигатные (сапротрофы) – организмы, питающиеся мертвыми растительными остатками или почвенным гумусом, на растениях развиваться не способны;
- паразиты факультативные (условные) – организмы, в основном питающиеся сапротрофно, но обладающие способностью поражать ослабленные растения или их части;
- сапрофиты факультативные – паразиты, обладающие способностью продолжать вегетативный рост и размножение на растительных остатках после гибели растения-хозяина;
- паразиты облигатные – организмы, обладающие способностью извлекать питательные вещества только из клеток живого растения, после гибели растения переходят в покоящиеся формы или погибают [2][3] .
Такая классификация вытекает из соотношения сапротрофной и паразитической фаз в жизненном цикле микроорганизма.
На живом растении встречаются паразиты облигатные, сапротрофы факультативные и очень редко паразиты факультативные. На мертвом растении – сапротрофы облигатные и паразиты факультативные, редко – сапротрофы факультативные [2] .
Фузариоз - диагностика, лечение
Эпидемиология фузариоза. Грибы рода Fusarium spp. широко распространены в природе: в почве, растительном мусоре. Инфицирование макроорганизма происходит при попадании спор грибов через верхние дыхательные пути или при непосредственном (контактном) поражении кожи, особенно когда нарушена ее целостность.
Fusarium spp. вызывают повреждение ногтевых пластинок (онихомикозы), которые впоследствии могут стать входными воротами диссеминированной инфекции у иммунокомпрометированных больных.
Инвазивный фузариоз чаще возникает у больных с нейтропенией, при трансплантации костного мозга.
Клиническая картина фузариоза. У 60—70 % больных фузариозом имеются множественные очаги на коже на фоне упорной лихорадки. Фузариоз кожи проявляется в виде гранулем, язв, пустул, некроза, очаговых инфильтратов; инвазия грибами может быть подобна ecthyma gangrenosum. Во всех случаях показаны биопсия этих образований, микологическое и гистологическое исследование.
Изолированное поражение легочной ткани Fusarium spp. наблюдается значительно реже, чем при аспергиллезе. В отличие от аспергиллеза и других плесневых микозов для грибов Fusarium spp. характерна высокая частота выделения их из крови (фунгемия), достигающая 50—60 %. Полиорганная диссеминация возникает часто, возможно поражение любого органа. Летальность при инвазивном фузариозе высокая, составляет более 70 %. Своевременно установить диагноз удается крайне редко, излечение возможно только при повышении (восстановлении) содержания лейкоцитов.
Диагностика фузариоза. Диагноз устанавливают на основании выделения и идентификации грибов в культуре из очага поражения или крови. Fusarium spp. — единственные оппортунистические плесневые грибы, которые могут быть легко выделены из крови. При гистологическом исследовании биоптатов Fusarium spp. нельзя дифференцировать от иных мицелиальных грибов, таких как Aspergillus или Scedosporium spp. Серологических тестов не существует.
Лечение фузариоза. Препаратом выбора является вориконазол (вифенд). Активность препарата доказана в исследованиях in vitro и in vivo. Положительные результаты при терапии вориконазолом, включая диссеминированные формы фузариоза, отмечаются у 40— 50 % больных.
Вориконазол вводят внутривенно по 6 мг/кг каждые 12 ч в 1-й день, в последующие дни — по 4 мг/кг каждые 12 ч; пероральное применение при массе тела больного более 40 кг — 400 мг каждые 12 ч в 1-е сутки, далее по 200 мг каждые 12 ч. При массе тела менее 40 кг дозу пероральной формы уменьшают в 2 раза.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Паразитарные воспалительные миопатии. Миопатия при цистицеркозе.
Течение заболевания, прогноз и лечение паразитарных миопатий
1. Токсоплазмоз — это протозойная инфекция, вызванная Toxoplasma gondii. Заражение происходит при употреблении в цищу зараженного паразитами мяса или при контакте с фекалиями больных кошек. Также возможен трансплацентарный или трансфузионный путь передачи возбудителя. Наиболее часто токсоплазмоз встречается у больных СПИДом. Миопатия — это только один из симптомов системной инфекции. Течение заболевания подострое, прогрессирующее и клинически неотличимое от других видов воспалительных миопатии. Иногда наблюдаются лихорадка, миалгии, лимфаденопатия и боли в шее.
Уровень креатинкиназы в крови может быть повышен. На ЭМГ обнаруживаются изменения, характерные для полиомиозита. Диагноз токсоплазмоза подтверждается методами серологической диагностики. Тахизоиды в мышечной ткани могут быть выявлены при биопсии.

Точная диагностика токсоплазменного миозита важна, т. к. лечение значительно отличается от лечения других видов миозита. Препаратами выбора являются пириметамин и сульфадиазин или трисульфапиридины. Пириметамин — антагонист фолиевой кислоты, поэтому ее назначают дополнительно для уменьшения риска подавления функции костного мозга.
2. Цистицеркоз. Заражение цистицеркозом происходит при употреблении в пищу свинины, подвергшейся недостаточной термической обработке, или при использовании загрязненной фекалиями воды и пищи. Заболевание вызывается личиночной формой ленточного червя Taenia solium. Заболевание может развиться спустя много лет после первичного инфицирования. Возбудитель внедряется в мягкие ткани, чаще всего в скелетные мышцы, ЦНС и глаза. Пораженная мышца увеличена в размерах, в ней прощупываются болезненные узелки.
Часто отмечается эозинофилия. Для подтверждения диагноза проводится исследование кала на яйца и взрослые формы паразита, серологическое исследование цереброспинальной жидкости (ЦСЖ) и сыворотки крови для выявления специфического антигена. Однако для подтверждения инфекционной этиологии миопатии необходима биопсия мышцы с макро- и микроскопическим выявлением инкапсулированной личиночной формы, а также специфического антигена. Псевдогипертрофия мышц обусловлена множественными паразитарными включениями. Часто наблюдается кальцификация цист в мышцах.
Для борьбы со взрослыми формами паразита применяется никлозамид и антибиотик парамомицин. Празиквантел (билтрицид), используемый для лечения цистицеркоза ЦНС, неэффективен. Преднизолон назначается наряду с основными препаратами для подавления воспалительной реакции. Иногда цисты удаляют хирургическим путем. 3. Трихинеллез вызван нематодой Trichinella spiralis. Личиночные формы паразита инфильтрируют многие ткани, но наиболее часто — мышечную. Инкубационный период составляет 2—12 дней после употребления в пищу свинины, не прошедшей адекватную термическую обработку и зараженной инкапсулированными личинками.
Продромальный период часто характеризуется болью в животе, диареей, за чем следуют лихорадка, миалгии и слабость проксимальных мышечных групп. Слабость может распространяться на экстраокулярные мышцы, межреберные мышцы и диафрагму. Может также наблюдаться периорбитальный отек и птоз. Миалгии достигают пика своей выраженности на третьей неделе болезни. Иногда отмечается поражение сердечной мышцы. На ЭМГ обнаруживаются признаки, характерные для острой миопатии. У 60% больных в крови отмечается выраженная эозинофилия. Антитела к Trichinella spiralis определяются примерно через 3 недели после инфицирования. Диагноз подтверждается обнаружением личинки при биопсии мышц.
Препаратом выбора для лечения взрослой и личиночных форм паразита является альбендазол. Его назначают по 400 мг 3 раза в сутки в течение двух недель. Препарат противопоказан детям и беременным женщинам. Больным с выраженной слабостью рекомендован преднизолон в дозе 1,0—1,5 мг/кг/сут. Прогноз плохой у больных с выраженным миозитом сердечной мышцы, с энцефалитом и иммунодефицитом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.
В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
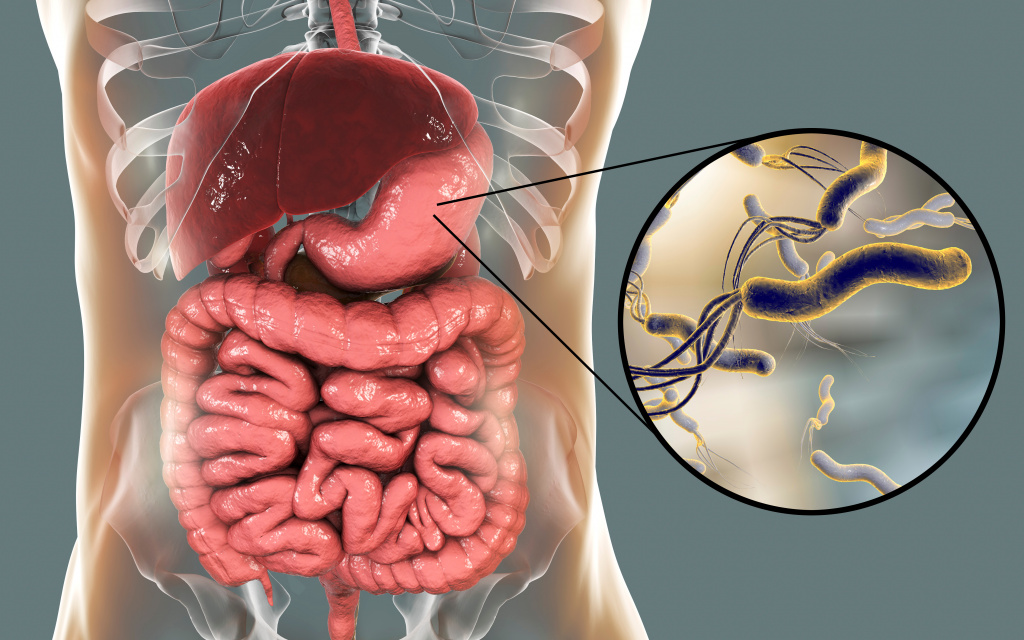
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.

Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.
Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге - 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
Заболевания, связанные с H. pylori:
- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.
Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Синонимы: Дыхательный тест с 13С-меченной мочевиной. 13 UBT; 13C-UBT. Краткая характеристика 13С-уреазного дыхательного теста Дыхательный тест в текущей модификации предназначен для лиц старше 12 лет. 13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования.
Читайте также:

