Гинекология стрептококк зеленящий стрептококк
Обновлено: 10.05.2024
В этой статье мы поговорим о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Почему за исключением S. pyogenes? Да потому что данного возбудителя мы рассмотрели в отдельной статье. Кроме того, мы уже говорим практически на одном языке, а потому можем себе позволить поговорить о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Микробиологические аспекты
Для начала разберемся с классификациями, чтобы понимать принципы разнесения стрептококков по группам. Так сложилось, что для классификации стрептококков используются их фенотипические характеристики, а именно характеристики по гемолитическим свойствам:
- β-гемолитические стрептококки вызывают полный гемолиз эритроцитов питательной среды с формированием прозрачной зоны вокруг колоний на кровяном агаре
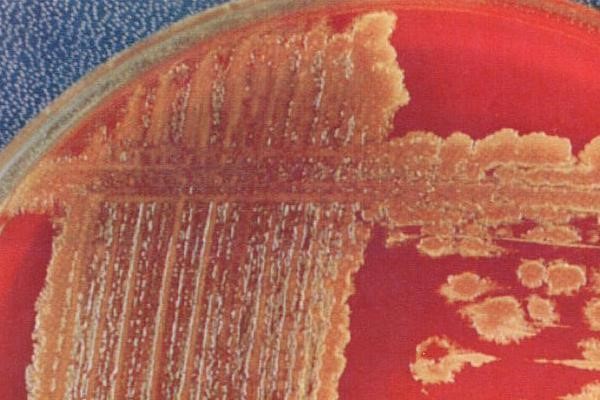
- α-гемолитические (зеленящие) образуют зеленоватый ореол вокруг колоний в результате неполного разложения гемоглобина
- γ-гемолитические по-другому именуются негемолитическими, то есть ничего никуда из крови не разлагают.
Собственно, почему кровь? Дело в том, что стрептококки крайне требовательны к питательным средам и к условиям, в которых их растят. И чтобы они выросли, в питательные среды (в основном, жидкие) необходимо или добавлять мясной экстракт, или использовать коммерческие питательные среды с добавлением крови барана, или 5%-й кровяной агар – и все это с большим количеством дополнительных компонентов. Для определения характера гемолиза традиционно используется среда с 5%-й дефибринированной кровью барана.
Подобное разделение по группам и типам гемолиза является решающим для деления стрептококков, имеющих медицинское значение, позволяя разделить патогенные и условно-патогенные микроорганизмы. Про патогенные мы уже поговорили ранее, теперь будем вести разговор о более обширной группе условно-патогенных представителей и начнем со стрептококков групп A, C, D и F, оставив для отдельного разговора группу В и единственного ее представителя – S. agalactiae.
Основными характеристиками представителей этих групп является то, что все они:
- Обладают β-гемолитической активностью
- Относятся к нормальной микрофлоре человека и животных
- Могут вызывать оппортунистические инфекции в различных локализациях
- Fc-антиген, способный взаимодействовать с Fc-фрагментом IgG, тем самым угнетая систему комплемента и подавляя активность фагоцитов. Кроме того, он же активирует выработку аутоиммунных антител, которые в дальнейшем участвуют в развитии иммунного воспаления;
- Р-антиген, обладающий иммуносупрессивной активностью и являющийся общим для всех стрептококков. Он подавляет выработку антител и усиливает реакции гиперчувствительности замедленного типа.
Кроме того, стрептококки имеют такой фактор патогенности, как М-протеин, который нарушает фагоцитарную активность путем маскировки рецепторов для комплемента, что очень затрудняет борьбу с этими возбудителями.
Клинические аспекты
1. Streptococcus dysgalactiae – объединяет двух представителей Streptococcus dysgalactiae subsp. dysgalactiae и Streptococcus dysgalactiae subsp. equisimilis. Первый живет на животных (и вызывает маститы у коров, на человеке в качестве возбудителя пока не ловили), второй на человеке – в верхних дыхательных путях и влагалище – и может быть причиной менингита, септических артритов и инфекций кожи (при условии наличия соответствующей симптоматики и в отсутствии других вероятных возбудителей).
2. Стрептококки группы Anginosus (S. anginosus, S. constellatus, S. intermedius) относятся к представителям нормальной флоры человека. Обрести зубы и стать возбудителями инфекции их могут заставить травмы, оперативные вмешательства, сахарный диабет, онкологические заболевания и иммунодефициты различной этиологии. Сами по себе на человека не бросаются и обнаружение оных вне клинической картины истребления не требует.
- S.anginosus – в норме обитает в полости рта, верхних дыхательных путях и влагалище. При патологии может быть высеян из урогенитальной и желудочно-кишечной локализаций.
- S. constellatus – в норме живет в верхних дыхательных путях и ЖКТ. При патологических процессах могут быть обнаружены где угодно.
- S. intermedius – в норме обитает в полости рта и верхних дыхательных путях. При патологических процессах в основном высевается из мозга, из крови при эндокардитах и из печеночных абсцессов (проще говоря оттуда, где в норме все должно быть стерильно).
3. S. equi клинического значения не имеет, так как является зоонозом и вызывает ветеринарные проблемы у коров, лошадей, морских свинок, овец и коз. Иногда – при употреблении зараженных молочных продуктов – может быть обнаружен у людей, больных нефритом.
4. S. canis, как понятно из названия, выделяют от собак. У людей могут вызывать инфекции мягких тканей, пневмонии, сепсис, остеомиелит.
5. S. iniae – обнаруживается у дельфинов и рыб. А также у людей, занятых на обработке замороженной рыбы. Крайне редко вызывает заболевание (описаны всего несколько случаев), хорошо лечится бета-лактамами и макролидами.
6. И несколько чисто зоонозных представителей, не имеющих медицинского значения, но иногда сеющихся с людей, которые за этими животными ухаживают или лечат:
- S. porcinus – вызывает абсцессы глотки свиней, пневмонию и аборты;
- S. didelphis – вызывает инфекции кожи, печени, легких и селезенки у опоссумов;
- S. phocae – выделяется у морских котиков при пневмонии у оных.
Как мы увидели, в большинстве своем перечисленные возбудители относятся к нормальной микрофлоре верхних дыхательных путей, кожи, ЖКТ и урогенитального тракта, а чтобы они вызвали заболевание, во внутреннюю среду организма должно проникнуть очень большое количество оных, при этом иммунная система должна быть подавлена тем или иным образом. Чаще всего такую роль играют медицинские вмешательства (инъекции, операции, катетеризация сосудов, гемодиализ и т. п.) на фоне тяжелых основных или сопутствующих заболеваний. Тогда стрептококки способны вызвать инфекции кожи и мягких тканей, верхних дыхательных путей, эндокардиты и сепсис, инфекции урогенитального тракта, при этом строгой локализации процесса соответствующим возбудителем уже не будет, а будет инфекция, связанная с медицинским вмешательством.
Что делать?
Как можно раньше провести бактериологическую диагностику и главным в ней будет правильная техника взятия биологического материала, чтобы точно исключить его контаминацию ни в чем не повинными мирными соседями, просмотрев истинного возбудителя. Техника взятия материала и правила транспортировки в лабораторию подробно расписаны здесь.
Чем лечить?
Этот вопрос мы можем задать только тогда, когда точно понимаем, что именно вышеуказанные зверушки являются возбудителями и никто за ними не прячется. Хорошая новость в том, что стрептококки до сих пор сохранили высокую чувствительность к бета-лактамам вообще и к пенициллинам в частности, то есть лечить их дешево. Плохая новость в том, что фактически утеряна чувствительность к макролидам, и поэтому они не могут быть препаратами выбора – это обязательно надо учитывать при назначении стартовой терапии.
Кроме того, стрептококки продолжают демонстрировать высокую чувствительность к ванкомицину, но в виду неоднозначности самого препарата в плане безопасности его применения, им тоже не следует злоупотреблять и включать его в схему лечения только в случае наличия аллергии к пенициллиновому ряду.
Итак, мы закончили краткое рассмотрение представителей стрептококков групп A, C, D, F и G, и нам осталось рассмотреть только одного представителя из группы В, а именно S.agalactiae, чем мы и займемся в следующей статье.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Стрептококковая инфекция - группа инфекционных болезней, вызываемых стрептококками различных серологических групп, с воздушно-капельным и алиментарным путём передачи возбудителя, протекающих с лихорадкой, интоксикацией, местными нагноительными процессами и развитием постстрептококковых аутоиммунных (ревматизм, гломерулонефрит) осложнений.
Коды по МКБ-10
- А38. Скарлатина.
- А40. Стрептококковая септицемия.
- А40.0. Септицемия, вызванная стрептококком группы А.
- А40.1. Септицемия, вызванная стрептококком группы В.
- А40.2. Септицемия, вызванная стрептококком группы D.
- А40.3. Септицемия, вызванная Streptococcus pneumoniae.
- А40.8. Другие стрептококковые септицемии.
- А40.9. Стрептококковая септицемия неуточнённая.
- В95.0. Стрептококки группы А как причина болезней, классифицированных в других рубриках.
- В95.1. Стрептококки группы В как причина болезней, классифицированных в других рубриках.
- В95.2. Стрептококки группы D как причина болезней, классифицированных в других рубриках.
- В95.3. Streptococcus pneumoniae как причина болезней, классифицированных в других рубриках.
- В95.4. Другие стрептококки как причина болезней, классифицированных в других рубриках.
- В95.5. Неуточнённые стрептококки как причина болезней, классифицированных в других рубриках.
Чем вызывается стрептококковая инфекция?
Стрептококковая инфекция вызывается стрептококками. Наиболее значимы стрептококковый патоген - S. Pyogenes, он является бета-гемолитическим, а в классификации Lancefield отнесен к группе А. Таким образом мы получаем: бета-гемолитический стрептококк группы А (ГАБГС).
Какие симптомы имеет стрептококковая инфекция?
Два наиболее частых острых заболевания, вызываемых бета-гемолитическим стрептококком группы А, - фарингит и кожные инфекции. В дополнение к этому, отсроченные негнойные осложнения, такие как острая ревматическая лихорадка и острый гломерулонефрит, иногда появляются через 2 и более недель после перенесенной стрептококковой инфекции, вызванной бета-гемолитическим стрептококком группы А. Болезни, вызываемые другими видами стрептококков, обычно менее распространены и включают инфекции мягких тканей или эндокардит. Некоторые не-ГАБГС инфекции преимущественно возникают в определенных популяциях (например, стрептококки группы В - у новорожденных и у родильниц, энтерококки - у больничных пациентов).
Инфекции могут распространяться по протяжению пораженных тканей и по лимфатическим путям в региональные лимфатические узлы. Также могут возникать местные гнойные осложнения, такие как перитонзиллярный абсцесс, средний отит, синусит. Также может возникать бактериемия. Возникнет ли нагноение, зависит от остроты заболевания и восприимчивости пораженной ткани.
Стрептококковый фарингит обычно вызывается бета-гемолитическим стрептококком группы А. Приблизительно у 20 % пациентов при этом заболевании возникают такие симптомы стрептококковой инфекции, как боль в горле, лихорадка, покраснение стенок глотки и гнойный налет на миндалинах. У остальных 80 % симптомы стрептококковой инфекции менее выраженны, и исследование выявляет те же признаки, что и при вирусном фарингите. Шейные и подмаксиллярные лимфатические узлы могут увеличиться в размерах и стать болезненными. Стрептококковый фарингит может привести к перитонзиллярному абсцессу. Кашель, ларингит и заложенный нос не характерны для стрептококковой фарингеальной инфекции. Наличие данных симптомов обычно указывает на заболевание другой этиологии, чаще всего вирусной или аллергической. 20 % людей являются бессимптомными носителями бета-гемолитического стрептококка группы А. Кожные инфекции включают импетиго и целлюлит. Целлюлит может очень быстро распространяться. Это связано с бесчисленными литическими ферментами, которые продуцируют в основном стрептококки группы А. Эризипелоид является частным случаем целлюлита.
Некротизирующий фасциит, вызываемый гноеродным стрептококком, - это острая кожная или редко мышечная инфекция, которая распространяется по фасциальным перемычкам. Стрептококки при некротизирующем фасците происходят из кожи или внутренностей, а повреждение может быть хирургическим, тривиальным, удаленным от места заболевания или слепым, как при дивертикуле толстой кишки и аппендикулярном абсцессе. Это заболевание чаще возникает у внутривенных наркоманов. Ранее известный как стрептококковая гангрена и популярно называемый мясопожирающей бактерией, синдром также может быть полимикробным, когда в воспалении принимает участие также аэробная и анаэробная сапрофитная флора, включающая и Clostridium Perfringens. Когда данный синдром захватывает брюшину, он называется гангреной Fournier. Часты сопутствующие заболевания, такие как нарушенный иммунитет, диабет и алкоголизм. Симптомы стрептококковой инфекции начинаются с лихорадки и интенсивной местной боли. Тромбоз микроциркуляторного русла вызывает ишемический некроз, что ведет к быстрому распространению инфекции и непропорционально нарастающей интоксикации. В 20-40 % случаев в процесс вовлекаются смежные мышцы. Часто возникают шок и почечная дисфункция. Даже при проведении адекватного лечения смертность все равно остается высокой. Септицемия, гнойный сепсис, эндокардит и пневмонии стрептококковой этиологии остаются серьезными осложнениями, особенно если этиологический микроорганизм представляет собой мультирезистентный энтерококк.
Стрептококковый инфекционно-токсический шок схож с таковым же, вызываемым золотистым стафилококком. Он может быть вызван токсинпродуциующими штаммами бета-гемолитического стрептококка группы А. Пациенты - обычно дети и взрослые с кожными инфекциями или инфекциями мягких тканей, не имеющие другой патологии.
Поздние осложнения стрептококковой инфекции
Механизм возникновения поздних осложнений во многом не изучен, но известно, что возникают реакции перекрестного иммунитета, при которых образовавшиеся антитела к антигенам стрептококка реагируют с тканями хозяина.
Острая ревматическая лихорадка (ОРЛ) - воспалительное расстройство. Она возникает менее чем у 3 % пациентов в течение нескольких недель после перенесенной нелеченной инфекции верхних дыхательных путей, вызванной бета-гемолитическим стрептококком группы А. Сегодня острая ревматическая лихорадка встречается значительно реже, нежели в доантибиотическую эру. Диагноз основывается на комбинации кардита, артрита, хореи, специфических кожных проявлений и лабораторных тестов. Самым важным моментом в лечении стрептококковых фарингитов является профилактика острой ревматической лихорадки.
Постстрептококковый острый гломерулонефрит является острым нефритическим синдромом, который сопровождает фарингит или кожную инфекцию, вызванную определенными нефритогенными штаммами бета-гемолитического стрептококка группы А. Данное последствие может быть вызвано лишь определенным числом стрептококковых серотипов группы А. Общая частота атак после перенесенного фарингита или кожной инфекции составляет приблизительно 10-15 %. Наиболее часто она возникает у детей спустя 1-3 недели после перенесенного заболевания. Почти все дети выздоравливают и не имеют постоянных почечных нарушений, однако это возможно и у некоторых взрослых. Лечение стрептококковой инфекции антибиотиками не оказывает существенного влияния на формирование постсрептококкового гломерулонефрита.
Как диагностируется стрептококковая инфекция?
Стрептококки почти не идентифицируются при культуральном исследовании на кровяном агаре овцы. Тесты быстрого определения антигенов сегодня доступны, что позволяет определить бета-гемолитический стрептококк группы А прямо при изучении мазков из горла. Многие такие тесты основаны на методологии иммунологических анализов. В последнее время более доступными стали оптические иммунологические тесты. Они имеют высокую чувствительность (более 95 %), но различаются между собой по специфичности (50-80 % и 80-90 % для самых последних оптических иммунологических тестов). Отрицательные результаты должны быть подтверждены культуральным исследованием (в частности, когда существует вопрос об использовании макролидов ввиду потенциальной резистентности). К моменту выздоровления доказательства инфекции могутбыть получены непрямым путем по измерению титров антистрептококковых антител в сыворотке крови. Обнаружение антител очень важно для диагностики послестрептококковых заболеваний, таких как острая ревматическая лихорадка и гломерулонефрит. Подтверждение требует последовательного повышения титров антител в образцах, так как однократное повышение титров антител может быть следствием ранее перенесенной длительной инфекции. Образцы сыворотки не следует брать чаще, чем через 2 недели, также их можно брать через 2 месяца. Титр антистрептолизина - о (асл-о) повышается только в 75-80 % случаев инфекции. Для полной диагностики в затруднительных случаях могут использоваться следующие тесты на определение: антигиалуронидазы, антидезоксирибонуклеазы В, антиникотинамидаденинди-нуклеотидазы или антистрептокиназы. Пенициллин, назначенный в первые пять дней от начала заболевания для симптоматического лечения стрептококкового фарингита, может вызвать более позднее появление и снижение по уровню асл-о ответа. Пациенты со стрептококковой пиодермией обычно не дают значительного асл-о ответа, но могут генерировать ответ к другим антигенам (в частности анти-ДНК-аза или антигиалуронидаза).
![Fact-checked]()
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Клинические симптомы стрептококковой инфекции разнообразны и зависят от вида возбудителя, локализации патологического процесса и состояния инфицированного организма. Болезни, вызываемые стрептококками группы А, можно разделить на первичные, вторичные и редко встречающиеся формы. К первичным формам относят стрептококковые поражения ЛОР-органов (ангина, фарингит, ОРЗ, отит и др.), кожи (импетиго, эктима), скарлатину, рожу. Среди вторичных форм выделяют заболевания с аутоиммунным механизмом развития (негнойные) и токсико-септические заболевания. К вторичным формам заболевания с аутоиммунным механизмом развития относят ревматизм, гломерулонефрит, васкулиты, а к токсико-септическим заболеваниям - метатонзиллярный и перитонзиллярный абсцессы, некротические поражения мягких тканей, септические осложнения. К редким формам причисляют некротический фасцит и миозит; энтерит; очаговые поражения внутренних органов, СТШ, сепсис и др.
Клинико-лабораторные симптомы стрептококковой инфекции с признаками инвазии:
- Падение систолического артериального давления до уровня 90 мм рт.ст. и ниже.
- Мультиорганные поражения с вовлечением двух органов и более:
- поражение почек: содержание креатинина у взрослых равно или превышает 2 мг/дл, а у детей в два раза больше возрастной нормы;
- коагулопатия: количество тромбоцитов менее 100х10 6 /л; усиление внутрисосудистого свёртывания крови; незначительное содержание фибриногена и присутствие продуктов его распада;
- поражение печени: возрастная норма содержания трансаминаз и общего билирубина превышена в два раза и более:
- острый РДС: острое начало диффузной лёгочной инфильтрации и гипоксемии (при этом отсутствуют признаки поражения сердца); повышение проницаемости капилляров; распространённый отёк (наличие жидкости в плевральной или перитонеальной области); снижение содержания альбумина в крови;
- распространённая эритематозная пятнистая сыпь с десквамацией эпителия;
- некроз мягких тканей (некротический фасцит или миозит).
Случаи стрептококковой инфекции разделяют на:
- вероятные - наличие клинических признаков болезни при отсутствии лабораторного подтверждения или при выделении другого возбудителя; выделение стрептококка группы А из нестерильных сред организма;
- подтверждённые - наличие перечисленных признаков болезни с выделением стрептококка группы А из обычно стерильных сред организма (кровь, спинно-мозговая жидкость, плевральная или перикардиальная жидкость).
Различают четыре стадии развития инвазивной формы стрептококковой инфекции:
- I стадия - наличие локализованного очага и бактериемии (при тяжёлых формах тонзиллофарингитов и стрептодермий рекомендованы посевы крови);
- II стадия - циркуляция бактериальных токсинов в крови;
- III стадия - выраженный цитокиновый ответ макроорганизма:
- IV стадия - поражение внутренних органов и токсический шок или коматозное состояние.
Чаще заболевают молодые люди. Инвазивной форме стрептококковой инфекции свойственны стремительное нарастание гипотензии, мультиорганных поражений, РДС, коагулопатии, шока и высокая летальность. Предрасполагающие факторы: сахарный диабет, иммунодефицитные состояния, заболевания сосудистой системы, применение глюкокортикоидов, алкоголизм, ветряная оспа (у детей). Провоцирующим моментом может послужить незначительная поверхностная травма, кровоизлияние в мягкие ткани и др.
Некротический фасцит (стрептококковая гангрена)
- Подтверждённый (установленный) случай:
- некроз мягких тканей с вовлечением фасции;
- системное заболевание, включающее один или несколько признаков: шок (падение артериального давления ниже 90 мм рт.ст.), диссеминированное внутрисосудистое свёртывание крови, поражение внутренних органов (лёгкие, печень, почки);
- выделение стрептококка группы А из обычно стерильных сред организма.
- наличие первого и второго признаков, а также серологическое подтверждение стрептококковой (группы А) инфекции (4-кратное нарастание антител к стрептолизину О и ДНКазе В);
- наличие первого и второго признаков, а также гистологическое подтверждение некроза мягких тканей, вызванного грамположительными возбудителями.
Некротический фасцит может быть спровоцирован незначительными повреждениями кожных покровов. Внешние признаки: припухлость; эритема красного, а затем - синюшного цвета; образование быстро вскрывающихся везикул с желтоватой жидкостью. Процесс охватывает не только фасции, но и кожу и мышцы. На 4-5-й день возникают признаки гангрены; на 7-10-й день - резкая очерченность зоны поражения и отслоение тканей. Симптомы стрептококковой инфекции стремительно нарастают, развиваются ранние мультиорганные (почки, печень, лёгкие) и системные поражения, острый РДС, коагулопатия, бактериемия, шок (особенно у пожилых и лиц с сопутствующим сахарным диабетом, тромбофлебитом, иммунодефицитным состоянием). Подобное течение процесса возможно и у практически здоровых людей.
Стрептококковая гангрена отличается от фасцитов другой этиологии. Для неё характерен прозрачный серозный экссудат, диффузно пропитывающий дряблую белесоватую фасцию без признаков гнойного расплавления. От клостридиальной инфекции некротический фасцит отличает отсутствие крепитации и выделения газа.
Стрептококковый миозит - редкая форма инвазивной стрептококковой инфекции. Основные симптомы стрептококковой инфекции - сильная боль, не соответствующая выраженности внешних признаков заболевания (припухлость, эритема, повышение температуры, ощущение растяжения мышц). Характерно стремительное нарастание признаков локального некроза мышечной ткани, мультиорганные поражения, острый дистресс-синдром, коагулопатия, бактериемия, шок. Летальность - 80-100%.
Сильная боль, в зависимости от её локализации, может быть связана с перитонитом, инфарктом миокарда, перикардитом, воспалением тазовых органов. Боли предшествует возникновение гриппоподобного синдрома: лихорадка, озноб, мышечные боли, диарея (20% случаев). Лихорадку обнаруживают примерно у 90% больных; инфекцию мягких тканей, приводящую к развитию некротического фасцита - у 80% больных. У 20% госпитализированных возможно развитие эндофтальмита, миозита, перигепатита, перитонита, миокардита и сепсиса. В 10% случаев вероятна гипотермия, в 80% - тахикардия, гипотензия. У всех больных обнаруживают прогрессирующую почечную дисфункцию, у половины больных - острый респираторный дистресс-синдром. Как правило, он возникает уже на фоне гипотензии и характеризуется тяжёлой одышкой, выраженной гипоксемиеи с развитием диффузных лёгочных инфильтратов и отёка лёгких. В 90% случаев необходимы интубация трахеи и ИВЛ. Более чем у 50% больных наблюдают дезориентацию во времени и пространстве; в некоторых случаях возможно развитие комы. У половины пациентов, имевших на момент госпитализации нормальное артериальное давление, в течение последующих 4 ч обнаруживают прогрессирующую гипотензию. Нередко возникает ДВС-синдром.
Обширные некротические изменения мягких тканей требуют хирургической санации, фасциотомии и, в отдельных случаях, ампутации конечностей. Клиническую картину шока стрептококкового генеза отличают определённая торпидность и склонность к персистированию, устойчивая к проводимым лечебным мероприятиям (антибиотикотерапия, введение альбумина, допамина, солевых растворов и др.).
Поражение почек предшествует развитию гипотензии, что свойственно только стрептококковому или стафилококковому токсическому шоку. Характерны гемоглобинурия, повышение уровня креатинина в 2,5-3 раза, снижение концентрации альбумина и уровня кальция в сыворотке крови, лейкоцитоз со сдвигом влево, увеличение СОЭ, снижение гематокрита почти в два раза.
Поражения, вызванные стрептококками группы В, встречают во всех возрастных категориях, но среди них доминирует патология новорождённых. У 30% детей обнаруживают бактериемию (без конкретного очага первичного инфицирования), у 32-35% - пневмонию, а у остальных - менингит, часто возникающий в течение первых 24 ч жизни. Заболевания новорождённых протекают тяжело, летальность достигает 37%. Часто у детей наблюдают менингиты и бактериемию, при этом 10-20% детей погибают, а у 50% выживших отмечают остаточные нарушения. У родильниц стрептококки группы В вызывают послеродовые инфекции: эндометрит, поражения мочевыводящих путей и осложнения хирургических ран при кесаревом сечении. Кроме того, стрептококки группы В способны вызывать поражения кожного покрова и мягких тканей, пневмонию, эндокардит и менингит у взрослых. Бактериемию наблюдают у лиц пожилого возраста, страдающих сахарным диабетом, заболеваниями периферических сосудов и злокачественными новообразованиями. Особо следует отметить стрептококковые пневмонии, возникающие на фоне ОРВИ.
Стрептококки серологических групп С и G известны как возбудители зоонозов, хотя в ряде случаев могут приводить к локальным и системным воспалительным процессам и у человека. Зеленящие стрептококки способны вызвать бактериальный эндокардит. Меньшие по значимости, но несравненно более частые симптомы стрептококковой инфекции - кариозное поражение зубов, вызываемое стрептококками биогруппы mutans (S. mutans, S. mitior, S. salivarius и др.).
![trusted-source]()
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
- Streptococcussanguis – воистину могуч и вездесущ. Обнаруживается в зубных отложениях с самого прорезывания зубов и до конца жизни, где и есть основное место его обитания. Иногда может быть обнаружен на слизистой глотки и в фекалиях, куда попадают транзитом. При этом надо помнить, что этот микроб вносит существенный вклад в процессы, связанные с кариесом, занимая в последующем ведущее место в ассоциациях микроорганизмов, выделяемых из гнойного экссудата при воспалительных процессах в челюстно-лицевой области, включая одонтогенные абсцессы мозга и других органов. Кроме того, они же могут быть выделены их крови и сердечных клапанов больных инфекционным эндокардитом.
- Streptococcussalivarius – также является одним из основных компонентов нормальной микрофлоры полости рта, а также, но в меньшем количестве, может быть выделен со слизистых дыхательного, желудочно-кишечного и урогенитального тракта. Особенно часто выделяются при анализе микрофлоры языка, слюны и фекалий. И крайне редко из крови при менингитах, септицимии и эндокардитах.
- Streptococcusmutans – выделяется с поверхности зубов и фекалий. Этот микроб является кариесогенным, а значит, может в дальнейшем вызывать бактериемию и бактериальный эндокардит у пациентов, не занимающихся регулярной санацией кариозных очагов в полости рта.
- Streptococcusmitis – в норме выделяется из слюны, мокроты фекалий, при этом может выделяться из верхних дыхательных путей и крови при нозокомиальном инфицировании.
- Совсем неверно упоминать в этом блоке стрептококки группы Anginosus -Streptococcusintermedius/S.anginosus/S.constellatus, но так как мы обсуждаем в основном орофарингеальную флору, способную вызвать инфекционные эндокардиты (и чтобы не писать еще один, совсем малюсенький блок), мы упомянем их здесь. В норме они являются представителями пародонтогенной группы. Но стоит представителю группы S.intermedius оттуда выбраться, как он может вызывать абсцессы печени, мозга и эндокардиты, так как проявляет высокую тропность к их тканям.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
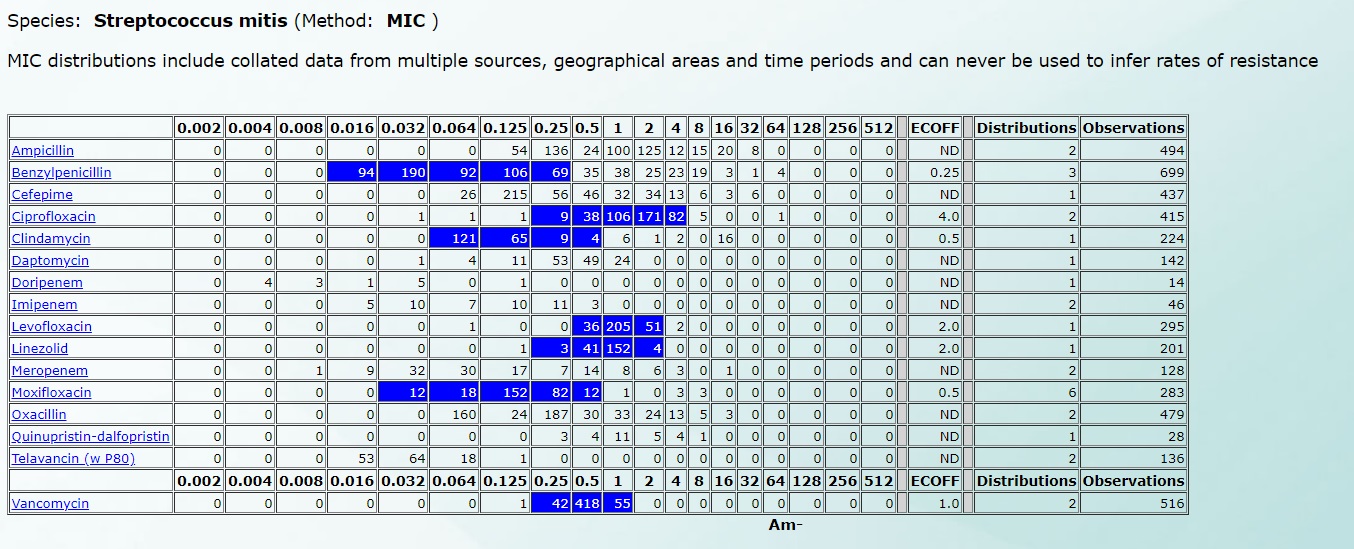
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
![Чувствительность Streptococcus mitis]()
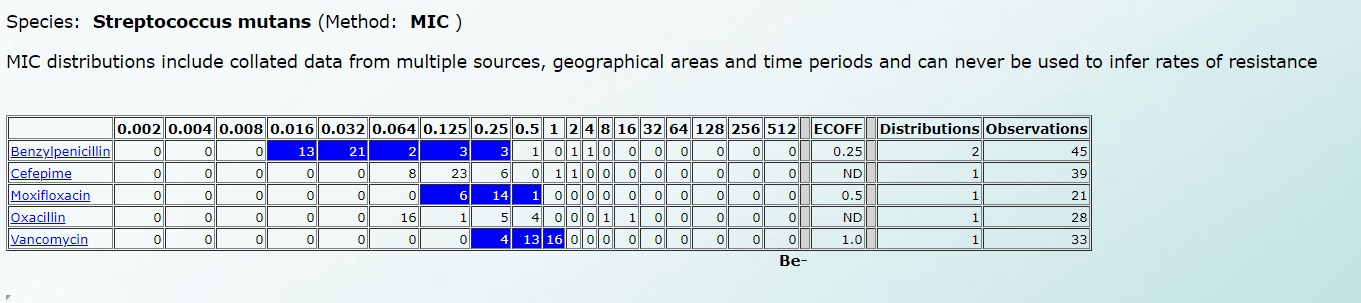
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
![Чувствительность к Streptococcus mutans]()
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
- Пенициллин в высоких дозировках (до 24 млн ЕД в сутки), возможно, в сочетании с аминогликозидами
- Цефтриаксон
- Ванкомицин
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
Тема эта очень узконаправленная, и вопрос в том, насколько она может быть интересна широкому кругу читателей. Однако ради одних только отдаленных последствий заболеваний, вызванных S. agalactiae, ее стоит рассмотреть.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Для начала капелька истории.
Микробиологические аспекты
Согласно современной классификации S. agalactiae относится к стрептококкам группы В и является единственным представителем в указанной группе. Общим с остальными стрептококками является то, что и этот зверь плохо растет в лабораторных условиях на обычных питательных средах, и ему тоже необходимы специальные среды с 5% бараньей кровью (вопрос капризности стрептококков мы обсуждали в первой статье этого года).
Несмотря на капризы вне естественной среды обитания (коей является кишечник), внутри организма человека S. agalactiae проявляет одно из своих главных свойств – устойчивость к фагоцитозу нейтрофилами и моноцитами, что позволяет ему спокойно выживать и колонизировать доступные слизистые оболочки.
Клинические аспекты
S. agalactiae способен вызывать следующие состояния:
- неонатальный сепсис
- менингиты у новорожденных
- хориоамниониты
- аборты в поздние сроки беременности
- спонтанные аборты
- инфекции мочевыводящих путей
- эндокардиты
- сепсис (у матерей)
- инфекции кожи и мягких тканей, как осложнение после кесарева сечения
- маститы и эндометриты у родильниц
- септический артрит
Наиболее чувствительны к S. agalactiae:
- беременные женщины
- новорожденные
- больные с сахарным диабетом
- дети с низкой массой тела и дистрофией
- пожилые пациенты
- иммунокопрометированные пациенты (вне зависимости от причины этих состояний)
Давайте рассмотрим наиболее уязвимые (и актуальные) категории, а именно беременных женщин и новорожденных.
Как мы знаем, основным местом жительства S. agalactiae в организме человека является ЖКТ, еще точнее – кишечник. Считается, что именно оттуда и происходит колонизация влагалища. Правда, тут же у автора возникает логичный вопрос – как? Стрептококки ног не отрастили, данный представитель также не является исключением. Проблемы с гигиеной? В таких масштабах и в странах с нормальным доступом к воде? Ответ нашелся достаточно быстро – колонизации S. agalactiae наиболее подвержены женщины, ведущее бурную сексуальную жизнь в течение года до развития заболевания/беременности, причем ведущие ее с многочисленными непостоянными партнерами. А судя по наличию кишечной флоры в непредназначенной для ее жизни локации, практики этой самой жизни тоже весьма разнообразны. Поэтому при сборе анамнеза, если, конечно, удастся, стоит выяснять регулярность анальных практик (автор с уверенностью может утверждать, что это сложно), и если удалось выяснить этот аспект, в голове должен прозвучать звоночек о том, что пациентка оказывается в группе риска, особенно если она уже беременна. Хотя следует отметь, что роль именно полового пути до сих пор вызывает определенные споры (даже несмотря на многочисленные исследования связи с ЗППП и с носительством S. agalactiae в уретре мужчин). Но автор согласен оставить этот вопрос дискутабельным.
Когда лучше всего определять факт носительства S. agalactiae для принятия адекватных мер по профилактике вышеперечисленных состояний? На 35-37 неделе беременности. Но следует учитывать, что носительство может быть непостоянным (транзиторным или перемежающимся), что затрудняет его обнаружение в скрининговых исследованиях, то есть если при исследованиях его нет, это не значит, что его там действительно нет, особенно если дама вела активную добеременную жизнь.
Какие факторы могут влиять на наличие носительства S. agalactiae?
- Женщины старшего возраста с репродуктивными проблемами ранее
- Расовые различия – у белых женщин частота колонизации в разы меньше (автор уже не может угадать, откуда его читают, поэтому решил указать и этот фактор)
- Количество предыдущих беременностей
Можно ли проводить скрининг до беременности? Можно, но смысла в нем не будет, ибо даже фаза менструального цикла влияет на выявляемость S. agalactiae.
Какие именно осложнения вызывает носительство S. agalactiae у беременных:
- преждевременные роды
- длительный безводный период
- малый вес новорожденных
- мертворождение
А к числу факторов риска развития этих состояний относят:
- кесарево сечение
- сахарный диабет
- общее снижение иммунитета
- массивную колонизацию S. agalactiae
Учитывая вышеперечисленное, массивная колонизация родовых путей матери создает серьезные угрозы инфекции у новорожденных – почти половина новорожденных от таких матерей будет иметь массированную колонизацию кожи и слизистых оболочек S. agalactiae. Заболеет ли каждый из них? Конечно, нет. Статистика говорит, что из таких детей-носителей заболеет не более 2%, которые будут иметь следующий набор факторов риска:
- Факторы, которые непосредственно связаны с матерью:
- Самый главный – наличие S. agalactiae на слизистой шейки матки у беременных
- Инфекции, связанные с S. agalactiae у ранее рожденных детей
- Длительный безводный период
- Преждевременные роды
- Подъем температуры во время родов
- Бактериурия
- Хориоамнионит
- Факторы, связанные непосредственно с новорожденным:
- Недоношенность и малый вес при рождении
- Кесарево сечение
- Длительное инструментальное обследование внутриутробно
У детей S. agalactiae может стать причиной:
- Менингитов
- Пневмоний
- Остеомиелитов
- Сепсиса
- Заболеваний глаз
- Артритов
- Ангин
- Нейтропений
У новорожденных заболевания могут развиваться в разные сроки. Чаще всего инфекции развиваются в течение первых 12 часов (сепсис, менингит, пневмония и нейтропения). Заражение происходит во время родов или внутриутробно перед родами через разорванный плодный пузырь. Летальность при раннем развитии колоссальная – более 50% и развивается в первые сутки. Как вы помните, в таких сроках антибиотики фактически бессильны (вспоминаем правило 48 часов для бактерицидных препаратов). У половины выживших детей затем могут развиваться осложнения со стороны ЦНС (например, ДЦП).
Значительно реже инфекция раскручивается в поздние сроки (от недели до трех месяцев), и чаще всего это будет менингит. Течет более благоприятно, летальность значительно ниже, но она есть. Также могут встречаться инфекции кожи и мягких тканей, септические артриты. После выздоровления в дальнейшем половина детей наблюдаются у неврологов в связи с серьезными неврологическими осложнениями.
Отдельного упоминания требует внутрибольничное распространение S. agalactiae в случае, когда мать не является его носителем и речь идет об инфекциях, связанных с медицинскими вмешательствами. Со всеми вытекающими, которые мы обсуждали в соответствующей статье.
Что со всем этим делать?
- Скрининг – мазок из влагалища и прямой кишки. То есть активное выявление беременных женщин – носителей S. agalactiae для последующей профилактики в родах, если наличие микроорганизма подтвердится. Руководства и рекомендации говорят о проведении скрининга в сроках 35-37 недель. Положительным считается наличие S. agalactiae в любом локусе.
- Далее должна быть проведена оценка факторов риска – если они есть, то рекомендуется назначение препаратов пенициллинового ряда во время родов (по аналогии с периоперационной антибиотикопрофилактикой, с одной существенной разницей – там препараты назначаются за 30-40 минут до оперативного вмешательства, а здесь непосредственно во время родов, и в идеале внутривенно капельно для создания максимальной времязависимой концентрации в тканях и крови, которые сдержат размножение патогенна).
- Если скрининг не проводился и женщина поступила в роддом как есть, то в случае длительного безводного периода и/или подъема температуры в родах выше 38°С также назначается пенициллин в родах.
- Если на скрининге S. agalactiae не выявлен, а также нет факторов риска (лихорадка и безводный период в родах), то профилактика не проводится.
Если имеется аллергия на пенициллиновый ряд, используем клиндамицин, так как эритромицин нам не помощник в виду высочайшего уровня резистентности у почти всех стерептококков.
К сожалению, профилактика не всесильна. Конечно, она предупреждает раннее развитие инфекции, но ничего не может сделать с мертворождением, преждевременными родами или инфекциями, развивающимися в более поздние сроки. Так что вопрос инфекций, связанных с S. agalactiae, будет еще достаточно длительное время очень актуальным, и в нем, к сожалению, нет простых решений.
Читайте также: