Инфекция enterobacter cloacae симптомы лечение
Обновлено: 25.04.2024
Энтеробактер (лат. Enterobacter) — род грамотрицательных палочкообразных перитрихиальных споронеобразующих бактерий, факультативных анаэробов. Энтеробактеры входят в состав нормальной микрофлоры кишечника человека.
Энтеробактер также обитает в кишечнике некоторых видов животных, встречается в почве, воде, пищевых продуктах.
Энтеробактер относится к так называемым колиформным бактериям.
Энтеробактер — возбудитель заболеваний человека
Энтеробактер встречается в толстом кишечнике многих здоровых людей, но он относится к условно-патогенным бактериям и при попадании энтеробактера в другие органы возможно развитие инфекционных заболеваний. Ряд видов энтеробактера (Enterobacter agglomerans, Enterobacter cloacae и др.) вызывают инфекционные заболевания почек и мочевыводящих путей (острый пиелонефрит, обострение хронического простатита), половых органов, респираторной системы.
Энтеробактер является одной из самых частых причин внутрибольничных ангиогенных инфекций и инфекций дыхательных и мочевыводящих путей.
Энтеробактер в анализе мочи
Бактериурия — наличие бактерий в моче может является признаком воспаления в мочевыводящих путях, мочевом пузыре, почках. При отсутствии каких-либо симптомов, истинная бактериурия (инфекция мочевых путей) диагностируется при наличии не менее 10 5 микробных тел энтеробактеров (или других энтеробактерий) в 1 мл свежевыпущенной мочи, иначе предполагается, что загрязнение мочи происходит при ее заборе. Если бактериурия не сопровождается какими-либо симптомами, тогда она называется бессимптомной бактериурией. Бессимптомная бактериурия не всегда требует немедленного лечения.
При наличии симптомов или при заборе мочи катетером диагностический порог может быть значительно уменьшен. В частности, при наличии соответствующей клинической симптоматики (лихорадка, озноб, тошнота, рвота, боли в поясничной области, дизурия) и выделении не менее 10 лейкоцитов в 1 мкл мочи, критерием для диагностики острого пиелонефрита является наличие не менее 10 4 энтеробактеров (или других уропатогенных энтеробактерий) в 1 мл мочи.
Энтеробактер в результатах анализа кала на дисбактериоз

При микробиологическом анализе кала энтеробактер рассматривается в комплексе с другими условно-патогенными бактериями, относящимися к семейству энтеробактерии и входящими в состав нормальной микрофлоры кишечника человека (кроме энтеробактера это клебсиелла, протей, гафния, серратия, морганелла, провиденция, цитробактер и др). В норме общее количество этих бактерий (колониеобразующих единиц, КОЕ) в 1 г кала должно быть меньше 10 4 . Большее количество перечисленных микроорганизмов является признаком дисбактериоза.
При избыточном росте энтеробактера, как следствии дисбактериоза, при медикаментозной терапии применяются различные пробиотки (Бифидумбактерин, Бифиформ, Лактобактерин, Ацилакт, Аципол и др.) и/или адекватные конкретному штамму энтеробактера и причине дисбактериоза антибиотики.
Антибиотики, активные в отношении энтеробактера
Антибактериальные средства (из имеющих описание в данном справочнике), активные в отношении энтеробактера: рифаксимин, ципрофлоксацин, норфлоксацин, офлаксацин, нифурател. В отношении Enterobacter cloacae активны: левофлоксацин, моксифлоксацин.
Энтеробактер в систематике бактерий
Род энтеробактер (Enterobacter) входит в семейство энтеробактерии (Enterobacteriaceae), порядок энтеробактерии (Enterobacteriales), класс гамма-протеобактерии (γ proteobacteria), тип протеобактерии (Proteobacteria), царство бактерии.

Enterobacter cloacae (энтеробактер клоаки) — вид грамотрицательных палочкообразных споронеобразующих бактерий, факультативных анаэробов. Размер клетки: диаметр от 0,6 до 1,0 мкм, длинна — от 1,2 до 3,0 мкм. Имеет большое число жгутиков, обеспечивающих её подвижность. Представитель нормальной микрофлоры кишечника человека.
Уреазо-продуцирующий. Поэтому присутствие его в желудке может увеличивать число ложноположительных результатов при уреазных тестах на Helicobacter pylori (Старостин Б.Д.). Является оксидаза-отрицательной и каталаза-положительной бактерией.
Enterobacter cloacae — причина заболеваний человека
Будучи условно-патогенным микробом, Enterobacter cloacae может вызывать инфекционные заболевания мочеполовой и респираторных систем человека, включая аспирационную пневмонию. Enterobacter cloacae нередко бывает причиной внутрибольничных инфекций.
Enterobacter cloacae в систематике бактерий
Вид Enterobacter cloacae входит в Enterobacter cloacae complex, который относится к роду энтеробактер (Enterobacter), семейству энтеробактерии (Enterobacteriaceae), порядку энтеробактерии (Enterobacteriales), классу гамма-протеобактерии (γ proteobacteria), типу протеобактерии (Proteobacteria), царству Бактерии.
Антибиотики, активные и неактивные в отношении Enterobacter cloacae
Антибактериальные средства (из имеющих описание в данном справочнике), активные в отношении Enterobacter cloacae: левофлоксацин, рифаксимин, норфлоксацин, офлаксацин, ципрофлоксацин, моксифлоксацин. Enterobacter cloacae слабо чувствителен к нифуроксазиду.
Enterobacter cloacae имеет высокую природную чувствительность к меропенему.
Enterobacter cloacae резистентны к цефалоспоринам III поколения и умеренно чувствительны к цефалоспоринам IV поколения (цефепим, цефпиром).

Энтеробактерии (лат. Enterobacteriaceae) — семейство грамотрицательных палочкообразных споронеобразующих бактерий, факультативные анаэробы.
Семейство энтеробактерий включает большое число представителей нормальной микрофлоры человеческого организма и, в то же время, значительное количество патогенных микробов.
Систематика энтеробактерий
Энтеробактерии (Enterobacteriaceae) входят в порядок энтеробактерии (лат. Enterobacteriales), класс гамма-протеобактерии (лат. γ proteobacteria), тип протеобактерии (лат. Proteobacteria), царство бактерии.
По современным представлениям в состав Enterobacteriaceae входят следующие роды бактерий: Atlantibacter, Biostraticola, Buttiauxella, Cedecea, Citrobacter (цитробактер), Cronobacter, Enterobacillus, Enterobacter (энтеробактер), Escherichia (эшерихии), Franconibacter, Gibbsiella, Izhakiella, Klebsiella (клебсиеллы), Kluyvera, Kosakonia, Leclercia, Lelliottia, Mangrovibacter, Pluralibacter, Pseudocitrobacter, Raoultella, Rosenbergiella, Salmonella (сальмонеллы), Shigella (шигеллы), Shimwellia, Siccibacter, Trabulsiella, Yokenella.
В качестве кандидатов рассматриваются роды: Aschnera, Curculioniphilus, Cuticobacterium, Gillettellia, Ishikawaella, Macropleicola, Moranella, Phlomobacter, Profftia, Riesia, Rohrkolberia, Schneideria, Stammerula.
До недавнего времени состав родов семейства энтеробактерий был следующий: Alishewanella, Alterococcus, Aquamonas, Aranicola, Arsenophonus, Averyella, Azotivirga, Brenneria, Buchnera, Budvicia, Buttiauxella, Cedecea, Citrobacter, Dickeya, Edwardsiella, Enterobacter, Erwinia, Escherichia, Ewingella, Grimontella, Hafnia, Klebsiella, Kluyvera, Leclercia, Leminorella, Moellerella, Morganella, Obesumbacterium, Pantoea, Pectobacterium, Photorhabdus, Plesiomonas, Pragia, Proteus (протей), Providencia, Rahnella, Raoultella, Salmonella, Samsonia, Serratia, Shewanella, Shigella, Sodalis, Tatumella, Thorsellia, Tiedjeia, Trabulsiella, Wigglesworthia, Xanthomonas, Xenorhabdus, Xylella, Yersinia (иерсинии), Yokenella. Роды Blochmannia и Phlomobacter рассматривались как кандидаты в семейство Enterobacteriaceae.
Примечания. 1. Исходя из соображений определённости и удобства пользования мы ориентируемся на систематику Национального центра биотехнологической информации США (National Center for Biotechnology Information), не утверждая, что она чем-то лучше или хуже других.
2. Неклассифицированные в отдельные виды штаммы, имеющие в своих названиях цифро-буквенные коды и т.п. штаммы и виды в данной статье не приведены.
Энтеробактерии — возбудители заболеваний

-
— ряд патогенных серотипов могут быть причиной различных инфекционных заболеваний, протекающих с интоксикацией, лихорадкой, обычно с поражением желудочно-кишечного тракта (различные диареи, в том числе диарею путешественников, геморрагический колит, гемолитико-уремического синдром и другие), реже — мочевыводящих, желчевыводящих путей, других органов или с развитием сепсиса
- Менингиты, как следствие черепно-мозговых травм, нейрохирургических вмешательств и при наличии антомических дефектов центральной нервной системы
- Перитониты любой этиологии
- Пельвиоперитониты (в составе микст-флоры)
- У пациентов с диабетической стопой
- У пациентов с инфекциями мочевыводящих путей, особенно в случаях их катетеризации
- Уросепсис
- У внутривенных наркозависимых – наравне с зеленящими стрептококками – энтерококки являются одними из наиболее частых возбудителей, а потому эмпирическая антибактериальная терапия должна перекрывать оба эти возбудителя
- Холангиты и инфекции билиарного тракта
- Катетер-ассоциированные инфекции (наряду с эпидермальными стафилококками)
- Катетер-ассоциированные инфекции: помимо удаления катетера и обязательного исследования оного в микробиологической лаборатории, установки нового катетера в новом месте, также используется ампициллин в комбинации с гентамицином (в тех же дозировках, что описаны выше) либо ванкомицин (15 мг/кг/сут), если пациент демонстрирует аллергическую реакцию на оные, либо линезолид 600 мг каждые 12 часов, либо даптомицин 6 мг/кг/сут (если сможете его добыть).
- Инфекции мочевыводящих путей– здесь предпочтение стоит отдать пероральному амоксициллину в комбинации с клавулановой кислотой дважды в день. Вызвана сия рекомендации тем, что это чаще всего эта инфекция, присущая амбулаторному этапу, будет вызвана дикой и непуганой флорой, и заодно прикроетесь от вероятной кишечной палочки как второго возбудителя. Если ситуация развилась в стационаре – смотрим пункт первый и лечим по той же схеме.
- Отдельного упоминания требует лечение ванкомицин-резистентных энтерококков, так как видят их уже практически все доктора хирургического и реанимационного профиля. Арсенал наш в этом случае крайне беден – это, по сути, только линезолид да даптомицин. Линезодид является бактериостатиком, дающим высокие риски миелосупресии и тромбоцитопении через 2 недели от начала применения, которое должно составлять не менее 8 недель, но это, по сути, единственный шанс для пациента с энтероккоковым менингитом, устойчивым к ванкомицину, так как даптомицин, который надо найти, и как-то убедить его купить (стоит он просто безбожных денег), в мозговые оболочки не проникает в виду размера самой молекулы. Можно также упомянуть о тигециклине (100 мг нагрузочная и далее по 50 мг каждые 12 часов), но он тоже стоит как самолет. Поэтому самым лучшим вариантом лечения ванкомицин-устойчивых энтерококковых инфекций является их недопущение в принципе, то есть СанПин, СанПин и еще раз СанПин. А уж если такой пациент все-таки приключился, то необходима немедленная изоляция оного в отдельную палату, а еще лучше в изолятор, чтобы от него не переинфицировать всех вокруг, если вдруг кто-то про обработку рук забудет.
- Инфекций мочевыводящих путей: катетер – или инструментально-ассоциированных (как результат эндоскопических манипуляций контаминированным инструментарием).
- Внутрибольничных пневмоний, в том числе вентилятор-ассоциированных.
- Инфекций кожи и мягких тканей, таких как раневые инфекции, инфицирование пролежней, ожоговые инфекции и послеоперационные инфекции. Кроме того в случае полимикробного характера инфицирования пролежней возможно развитие сепсиса как исхода раневой инфекции.
- Инфекций кровотока – катетер – и инструмент-ассоциированные.
- Инфекций центральной нервной системы — менингиты, чаще всего внутрибольничные, как следствие нейрохирургических вмешательств.
- Неонатальных инфекций, таких как некротический энтероколит, сепсис и менингит.
- Катетер-ассоциированные инфекции и как их исход – сепсис.
- Инфекции мочевыводящих путей как следствие медицинских манипуляций необработанным инструментом.
- Раневые инфекции в послеоперационном периоде.
- Нозокомиальные пневмонии как следствие интубации.
- Септические артриты.
- Конъюнктивиты и кератиты.
- И редко вызывали остеомиелиты и эндокардиты
- Крайне редко – сепсис, как исход инфекции мочевыводящих путей.
- Раневую хирургическую инфекцию.
- Септический артрит.
- Неонатальный сепсис и хореоамнионит.
- Менингит.
- Перикардит.
-
была причиной кишечной инфекции 2011 года со смертельными исходами в Германии и других странах Европы
Энтеробактерии — представители родов Citrobacier, Enterobacter, Echerichia, Klebsiella, Salmonella могут вызывать инфекции мочеполовой сферы (в том числе циститы, пиелонефриты, острые и хронические простатиты, эпидидимиты и орхиты и т.п.). Бактериурия — наличие бактерий в моче человека может быть только в том случае, если почки, мочевой пузырь или мочеточники инфицированы патогенными бактериями. До 80% бактерий, обнаруживаемых в моче, — энтеробактерии.
Энтеробактерии могут быть причиной вагинитов (воспаления влагалища), цервицитах (воспаления канала шейки матки), других воспалительных гинекологических заболеваниях. Энтеробактерии во влагалище обычно выявляются у пациенток, не соблюдающих правила личной гигиены.
Энтеробактерии могут быть инфекционным агентом при перитоните.
Энтеробактерии — нормальная флора кишечника человека
Энтеробактерии присутствуют в различных отделах желудочно-кишечного тракта здорового человека. Их количество увеличивается от проксимальных отделов (в тощей кишке обнаруживается от 0 до 10 3 КОЕ/мл энтеробактерий, в подвздошной — от 10 2 до 10 6 КОЕ/мл) к дистальным.
Публикации для профессионалов здравоохранения затрагивающие проблематику, связанную с энтеробактериями
Антимикробные препараты, активные в отношении энтеробактерий
Темой сегодняшнего разговора будут одни из наиболее распространенных микроорганизмов из семейства Enterobacteriaceae – энтерококки, которые являются грамположительными кокками и факультативными анаэробами.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будут одни из наиболее распространенных микроорганизмов из семейства Enterobacteriaceae – энтерококки, которые являются грамположительными кокками и факультативными анаэробами.
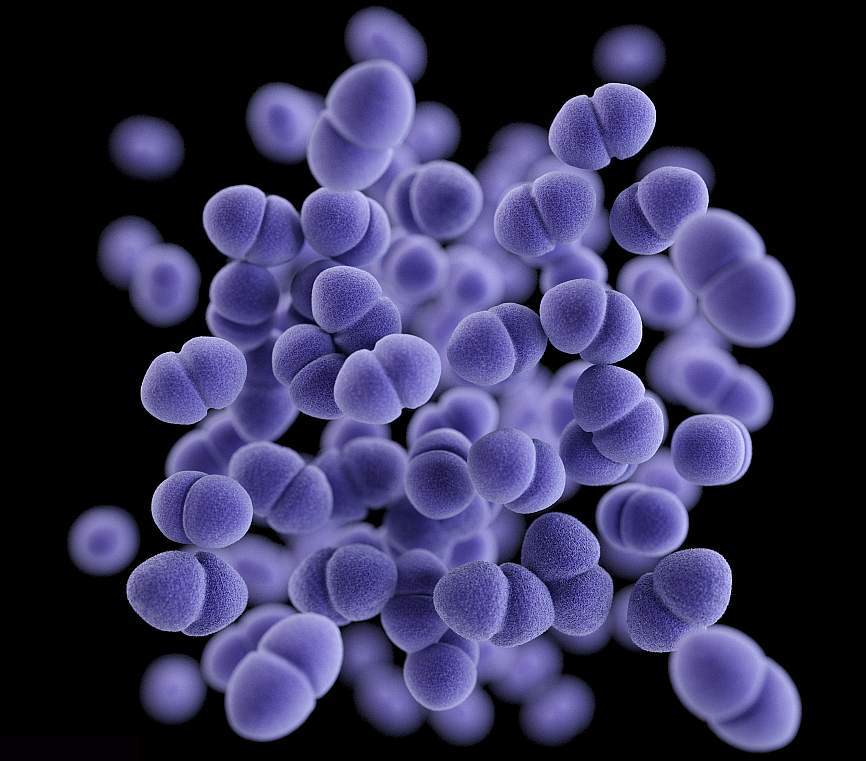
Микробиологические аспекты
Энтерококки входят в состав нормальной микрофлоры кишечника, обитают в основном в тонкой кишке и при этом, обнаруживаясь за пределами своей естественной среды обитания, являются возбудителями множества социально-значимых заболеваний. Наибольшее клиническое значение имеют E.faecalis и E.faecium.
Отличительным свойством энтерококков является их способность к образованию биопленок. О биопленках достаточно подробно мы рассуждали в статье, посвященной синегнойной палочке. И специфика течения многих заболеваний, вызванных энтерококками, объясняется именно пленкообразованием.
Клинические аспекты
Наиболее частым возбудителем внебольничных инфекций является E.faecalis – сюда относятся инфекции мочевыводящих путей и инфекционные эндокардиты у внутривенных наркозависимых пациентов.
E.faecium наиболее часто выявляется при нозокомиальных инфекциях – здесь преобладают так же инфекции мочевыводящих путей, но связанные с проведением инструментальных методов исследования, а также всевозможные виды бактеремий, связанных с медицинскими вмешательствами.
Когда мы можем думать о состояниях, вызванных энтерококками?
Существуют следующие факторы риска инфицирования энтерококками:
Как мы можем заметить, основную роль в развитии заболеваний, вызванных энтерококками, играет человеческий, точнее ятрогенный фактор. Энтерококки, как и вся остальная кишечная микрофлора, по воздуху летать не умеют, да и ножками не ходят, а потому главное в их нераспространении – чистота наших рук и соблюдение санитарно-противоэпидемических правил, написанных, как и большинство подобных документов (например, как ПДД), кровью, причем кровью пациентов.
Аспекты лечения
Их можно разделить на лекарственные и нелекарственные.
Аспекты медикаментозного лечения
Здесь автор отступит от правила и не отправит изучать вопрос по книжкам и таблицам, а попытается расписать антибактериальную терапию более подробно. Это связано и со спецификой самого возбудителя, и со спецификой контингента, имеющего заболевания, им вызванные.
Как уже упоминалось ранее, наряду с зеленящим стрептококком, а вообще намного чаще, энтерококк является основным возбудителем инфекционного эндокардита у лиц с внутривенной наркотической зависимостью. Проще говоря, если перед вами наркозависимый, и у него эндокардит трикуспидального клапана, то первое, о чем вы должны подумать, – это энтерококк, и эмпирическую терапию назначать с учетом этого знания. Конечно, могут быть варианты в виде того же зеленящего стрептококка или даже золотистого стафилококка, но эти возбудители более присущи пациентам с несанированной ротовой полостью и на митральном клапане (зеленящий) или после кардиохирургического вмешательства (золотистый стафилококк). Также на стафилококковый, а не энтерококковый характер поражения будет намекать снимок органов грудной клетки в прямой проекции, подозрительно напоминающий решето (один раз увидев стафилококковую метастатическую пневмонию ее уже ни с чем не перепутаешь).
Чем будем лечить?
Как ни странно это прозвучит в современных условиях, но препаратами выбора будут представители аминопенициллинового ряда – ампициллин (дешевле) или амоксициллин (в разы дороже) в обязательной комбинации с аминогликозидом –гентамицином (этот дешевле) или амикацином. Поэтому если вы работаете в стационаре скорой помощи и у вас попадаются пациенты данной категории – ампициллин для инъекций крайне рекомендуется иметь на полках аптеки в достаточных количествах. Это до сих пор дешево, сердито и очень эффективно в случаях терапии энтерококковых инфекций почти любой этиологии, и главное правильно рассчитать дозу, так как аминопенициллины относятся к так называемым время-зависимым препаратам (читаем первую и вторую часть здесь).
Повторимся еще раз – аминопенициллины в данном случае должны использоваться только в комбинации с аминогликозидами ввиду их синергетического действия в отношении энтерококков и ввиду вероятности микст-инфекции у подобной категории пациентов.
Вопрос по эмпирическому использованию ванкомицина остается дискуссионным – если в случае E.faecalis его можно назначать на уровне эмпирической терапии, когда у пациента имеется документированная аллергия на пенициллины (если конечно вам покрасили мазок по Граму или ваш стационар настолько крут, что имеет свой масс-спектрометр), то в случае E.faecium даже начинать не стоит — сразу зовите специально обученного человека, пусть он думает, что дальше делать.
Как уже было выше упомянуто, цефалоспорины назначать не стоит — энтерококки к ним природно устойчивы. А для того чтобы рука потянулась к карбопенемам, вам надо иметь доказанную мульти-резистентность возбудителя.
В случае развития резистентности к ампициллину используется его защищенная форма в виде ампициллина/сульбактама в комбинации с гентамицином. Дозировки рассчитываются по ампициллину.
Если совсем не повезло и лаборатория дала мультирезистентного фекального энтерококка, то используется комбинация ванкомицин (15 мг/кг/сут) в комбинации с гентамицином (8 мг/кг/сут) под жесточайшим контролем функции почек. Кроме того, в случае мультирезистентного возбудителя может быть использована комбинация имипенема с ампициллином, если, конечно, сможете обосновать ее для страховой компании – автор обосновывала, необходимый эффект получала, пациент не только выживал, но и выздоравливал. Только призывать к такого рода схемам, описанным, в основном, в американской литературе, автор ни в коем случае не будет, особенно в нынешние неспокойные времена. Сейчас наши основные документы по назначению любого вида терапии располагаются здесь.
В случае обнаружения резистентного E.faecium препаратом выбора становится линезолид и, не побоюсь этого слова, молитва, так как срок лечения не менее 8 недель, а кто нам столько препарата выдаст, да и прогноз при применении бактериостатика как-то не очень.
На этом краткий обзор энтерококковых инфекций закончим, и из кишечной микрофлоры у нас останется только королева внтурибольничных инфекций – ее величество Klebsiella, о которой мы поговорим в одной из следующих публикаций.

Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач – клинический фармаколог Трубачева Е.С.
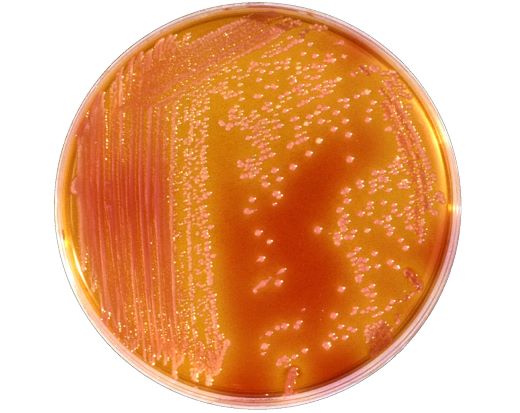
Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Героями сегодняшнего разговора станут энтеробактеры, серрации, морганеллы. Конечно, есть и другие представители и, возможно, в постковид они начнут встречаться намного чаще, но пока нам в рамках Азбуки достаточно вышеперечисленных плюс кишечные палки и клебсиеллы, о которых мы говорили ранее.
Enterobacter spp.
Микробиологические аспекты
Род энтеробактера включает несколько видов, но наиболее клинически значимыми из них являются:
Очень важно помнить, что энтеробактеры проявляют природную устойчивость к большому спектру антибиотиков, таким как бета-лактамы, к которым они продуцируют хромосомные AmpC бета-лактамазы, плазмидные бета-лактамазы расширенного спектра, а также карбапенемазы. Так как клинически значимые представители Enterobacter spp. обитают в желудочно-кишечном тракте человека, то основным источником инфицирования для пациента становится медицинский персонал, который просто по факту своей ежедневной работы в больнице с антибиотиками является резервуаром всевозможных антибиотикорезистентностей.
Клинически значимые аспекты
Enterobacter spp. является причиной:
Чем лечить?
Ответ будет традиционным – лучше вообще не инфицировать, тогда не придется ломать голову, чем все это лечить. В основе терапии лежит обязательное микробиологическое исследование с определением антибиотикочувствительности.
В случае выявления представителей Enterobacter spp. при лечении тяжелых инфекций предпочтение следует отдавать комбинированной терапии, и самыми подходящими будут пиперациллин-тазобактам в комбинации с аминогликозидами или фторхинолонами. А для преодоления резистентности, вызванной бета-лактамазами расширенного спектра, можно использовать карбопенемы.
Для лечения инфекций мочевыводящих путей самым первым и наиважнейшим является удаление мочевого катетера до момента прекращения пиурии. Далее лечим либо исходя из профиля антибиотикограммы, либо ципрофлоксацином в правильно подобранной дозе, либо, как было указано выше, рассматриваем назначение нитрофуранов и фосфомицина.
Serratia spp.
Клинические аспекты
Что вызывает?
Терапевтические аспекты
В первую очередь про серрацию надо узнать, а значит, необходимо микробиологическое исследование. Во-вторую, вспомнить о природной устойчивости. В-третью, держать в уме то, что очень часто цефалоспорины третьего и четвертого поколения тоже не будут работать, так как посредством плазмид получают устойчивость от родственников по семейству Enterobacteriaceae, например, от родной сестры – клебсиеллы. Точно таким же образом серрация может оказаться устойчивой и к карбопенемам. К фторхинолонам резистентность так же уже давно описана.
Так чем лечить?
Лучше вообще не заражать – потому что если бак. лаборатория дает серрацию, то ниоткуда кроме как с наших рук она появиться не может, так как ни ходить, ни летать сия зверюшка до сих пор не научилась.
В случае развития тяжелых инфекций – сепсиса, вентилятор-ассоциированной пневмонии и т. п., и только при документированной чувствительности, препаратами выбора могут быть цефепим или меропенем, или ципрофлоксацин в вену в стандартных дозировках. Если чувствительность утеряна, то зовем клинического фармаколога, а если такового нет, то смотрим в сторону амикацина, пиперациллина-тазобактама и азтреонама, только помним об их побочных эффектах. Курс лечения соблюдать жизненно необходимо, чтобы зверюшка еще куда-нибудь не мутировала и новыми механизмами защиты не обзавелась. Обычно речь идет о 10-14 днях (но так как польза превышает вред, то нефротоксичность аминогликозидов со временем отступит, а ототоксичность – тут уж как повезет).
Инфекции мочеполового тракта лечим так же с учетом чувствительности, и если таковая располагает, то препаратом выбора становятся фторхинолоны, либо комбинация двух антибиотиков, например фторхинолон с карбапенемом или бета-лактам с аминогликозидом.
Эндокардиты с остеомиелитами бывают хоть и редко, но крайне метко, а потому снова сначала исследуем чувствительность, потом индивидуально в каждом случае подбираем антибиотики (а лучше зовем клинического фармаколога, пусть он мучается). И снова крайне важно соблюдение сроков лечения, для эндокардита это порядка четырех, а то и шести недель внутривенной антибактериальной терапии, а для остеомиелита не менее двух недель. Почему нельзя меньше? Потому что последует мутация и новый рецидив, а антибиотиков просто может не хватить, ибо, как и сестра-клебсиелла, серрация тоже умеет в панрезистентность.
В заключении хочется повторить, что и в этом случае проще помыть руки, чем разгребать последствия инфицирования серрацией. Мытье рук и проще, и дешевле, и, что самое главное, спокойнее.
Morganella spp.
Морганеллы будут последними представителями семейства Enterobacteriaceae, которых мы обсуждаем в рамках нашей Азбуки. Если кому-то станет интересно покопаться дальше, то к их услугам всегда будет четырехтомник по медицинской микробиологии под редакцией Лабинской, конкретно второй и третий том, в которых все очень подробно расписано, правда, чтение это для неподготовленного человека будет довольно сложным. Но вернемся к нашей морганелле.
Микробиологические аспекты
Морганелла существует только одна – M.morganii, но имеет два подвида – M.morganii и M.sibonii, которые отличаются только по ферментации треалозы, и никакого клинического значения данное отличие не имеет.
Конечно, и морганелла умеет в природную устойчивость к антибиотикам, а именно к пенициллинам, цефалоспоринам первого и второго поколения, макролидам и ко-тримоксазолу. При этом сохраняет высочайшую чувствительность к аминогликозидам, пиперациллину, цефалоспоринам третьего и четвертого поколения, фторхинолонам и карбопенемам. То есть данную зверюшку есть чем победить.
Клинические аспекты
Морганелла является представителем нормальной микрофлоры человека и самостоятельно крайне редко что-то вызывает. Этим крайне редким являются инфекции мочевыводящих путей, чему способствуют крайне пожилой возраст, длительная госпитализация, мочевой катетер и иммунодефицит любой этиологии.
В плане приобретенной антибиотикорезистентности морганелла обзавелась факторами устойчивости к фторхинолонам, что и понятно, учитывая какие именно заболевания она вызывает и чем их чаще всего лечат.
Что еще может вызывать?
Но стоит иметь в виду, что данные ситуации крайне редки, и стоит изначально подумать не об этом возбудителе, а о том, какой за ним может прятаться в виду контаминации материала, и лучше бы все еще раз пересеять и перепроверить.
Терапевтические аспекты
Если результат микробиологического исследования сомнений не вызывает и вы убеждены, что имеете дело с морганеллами, то препаратами выбора становятся карбопенемы, и только в случае их недоступности и документированной бактериологом чувствительности, можно посмотреть в сторону цефалоспоринов, например, цефтазидима (для которого нужна отдельная цефалоспориназа, чтобы он был инактивирован), а лучше цефтазидим-авибактама. Хотя если недоступны карбопенемы, то и Завицефте, скорее всего, взяться будет неоткуда.
Какие препараты могут быть использованы в качестве резервных? Решать этот вопрос также необходимо только после получения результата микробиологии и чувствительности в идеале по МПК, и только после этого рассматривать назначение цефепима или ципрофлоксацина, или аминогликозидов (они, к слову, в случае морганеллы могут обоснованно выступать в качестве монотерапии инфекций мочевыводящих путей).
Читайте также:

