Инфекция в ротике у грудничка
Обновлено: 07.05.2024
Врожденные инфекции у плода и новорожденного ребенка: виды, возбудители, клиника, диагностика
Передача врождённых и перинатальных инфекций плоду происходит через плаценту (внутриутробные инфекции), во время родов или при контакте с физиологическими жидкостями матери. Длительное разрушение плодных оболочек также способствует развитию внутриутробных заболеваний. Кроме того, заражение может произойти и после рождения (при контакте с матерью и другими людьми).
Врожденная краснуха
Первый признак врождённой краснухи — желтуха, как следствие развития гепатита. Часто возникает гемолиз и тромбоцитопеническая пурпура, а также слабовыраженные клинические проявления менингоэнцефалита. У некоторых новорождённых обнаруживают признаки метафизарной дисплазии. Инфицированные дети при рождении обычно имеют сниженную массу тела и отстают в физическом развитии.
В тяжёлых случаях болезнь обычно заканчивается летальным исходом. Наиболее грозные осложнения — незаращение артериального протока, катаракта, глухота, ретинопатия.
Тест на антитела к краснухе (IgM), которые можно обнаружить в крови детей до 3-го мес жизни, даёт положительный результат. При заболевании матери в I триместре вероятность развития патологии у ребёнка составляет 60%, поэтому некоторые женщины предпочитают прерывать беременность. В дальнейшем риск заметно снижается (2% после 20-й нед), в связи с чем выбор между рождением ребенка с вероятными нарушениями в развитии и прерыванием беременности необходимо делать крайне осторожно.
Цитомегаловирус у плода и новорожденного
Инфекция проявляется примерно в 1% случаев, при этом тяжёлая форма заболевания развивается только у 1% инфицированных. Наиболее высокий риск заражения плода отмечают на сроке гестации, соответствующем I триместру беременности. Симптомы заболевания у новорождённых — сниженная масса тела, гепатомегалия, спленомегалия, тромбоцитопения, продолжительная желтуха, повышенная возбудимость, судорожный синдром, аномальный мышечный тонус и двигательные расстройства.
Наиболее частые осложнения — микроцефалия, нейросенсорная глухота. Нередко обнаруживают кальцификацию головного мозга, гемиплегию (паралич мышц одной стороны тела), замедление психомоторных реакций, хориоретинит и миопатию. Диагностика основана на обнаружении антител к цитомегаловирусу (IgM) или определении экскреции вируса в течение первых двадцати дней жизни.
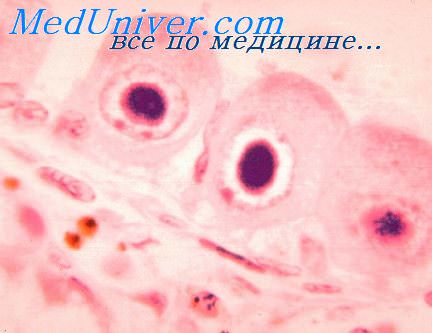
Возбудитель ЦМВ инфекции
Врожденная инфекция вируса простого герпеса
Первичная инфекция, вызванная вирусом простого герпеса, сопровождается виремией. При этом может произойти трансплацентарное заражение плода. При врождённом инфицировании дети рождаются с тяжёлыми отклонениями (пневмония, менингоэнцефалит, гепатоспленомегалия, цитопения), но лишь у некоторых из них присутствуют герпетические очаги на коже и слизистых оболочках. Лечение ацикловиром позволяет снизить смертность с 80—90% до 10—15%.
Терапию следует начинать до получения результатов лабораторного анализа. Первичная инфекция также возникает при заражении от матери, страдающей генитальным герпесом. При этом в первые дни жизни ребёнка возникают очаги на коже, конъюнктиве, слизистой оболочке рта и половых органов, а в 50% случаев наблюдают генерализованное течение инфекции. Лечение: внутривенное введение ацикловира.
Ветряная оспа плода
Инфицирование плода ветряной оспой возникает при заражении беременной в I—II триместре беременности, при этом вероятность передачи инфекции плоду составляет 3%. Заболевание характеризуется развитием рубцовой контрактуры в области лимбических структур головного мозга, микроцефалии или офтальмомикрии. Непривитые беременные в течение десяти дней после возможного заражения (контакта) должны пройти профилактический курс введения иммуноглобулина (содержащим антитела к вирусу ветряной оспы).
Ветряная оспа новорождённых возникает при заболевании матери в течение одной недели до родов. Смертность составляет 40%, поэтому в первые 48 ч жизни ребёнку необходимо ввести специфический иммуноглобулин. При ухудшении состояния следует незамедлительно начать лечение ацикловиром. Применение нормального иммуноглобулина человека не защищает новорождённого от заражения. В некоторых странах применяется вакцина.
Врожденный листериоз
Трансплацентарная передача Listeria monocytogenes происходит при заражении матери инфекцией, протекающей бессимптомно. Заболевание матери на ранних стадиях беременности обычно приводит к смерти плода, а на более поздних — к преждевременным родам. Инфекцию новорождённых обычно осложняет бактериемия, гепатоспленомегалия, менингоэнцефалит, тромбоцитопения и пневмония. При интранатальном заражении инфекция развивается в течение первых двух недель жизни ребенка и сопровождается менингитом и бактериемией.
Для выделения возбудителя на анализ отбирают кровь, спинномозговую жидкость, плацентарную ткань и послеродовую жидкость из матки. Инфицированную мать и ребёнка помещают в отдельную палату, так как они могут стать причиной вспышки заболевания в родильном отделении. Препарат выбора — ампициллин (иногда в комплексе с гентамицином); длительность лечения 2—6 нед.
Врожденный сифилис
Благодаря эффективным пренатальным исследованиям случаи врождённого сифилиса в настоящее время достаточно редки. У заражённых детей обнаруживают лихорадку, а также симптомы, свойственные вторичному сифилису, сыпь, кондиломы и трещины на слизистых оболочках. При развитии остеохондритов возникает выраженный болевой синдром. Очень часто отмечают постоянный насморк (сопение, гнусавость).
Для подтверждения диагноза применяют темнопольную микроскопию образцов поражённой кожи и слизистых оболочек. Специфические IgM или другие антитела персистируют в организме свыше 6 мес после перенесённой инфекции. Поздние симптомы (глухота, атрофия зрительного нерва, паретический нейросифилис) наблюдают в возрасте 12—20 лет. Нередко возникают бугристые образования на лобных костях, хронический большеберцовый периостит, перфорация передних зубов, деформация первых постоянных коренных зубов и высокий изгиб нёба. Препарат выбора — пенициллин.
Врожденный токсоплазмоз
Вероятность врождённого токсоплазмоза варьирует в разных регионах. Например, в Великобритании его регистрируют достаточно редко, а во Франции — часто. При заражении беременной трансплацентарную передачу инфекции плоду наблюдают в каждом третьем случае. Наиболее высок риск развития патологии плода (мертворождение, смерть после рождения, кальцификация головного мозга, церебральный паралич и эпилепсия) при заражении женщины в I и II триместре беременности.
Хориоретинит может возникать только спустя некоторое время после рождения и быть единственным симптомом болезни. Токсоплазмоз у матери подтверждают при обнаружении специфических антител (IgM) или сероконверсии. IgM также обнаруживают у инфицированных новорождённых. Применение спирамицина позволяет снизить риск трансплацентарного заражения, но не влияет на исход заболевания у новорождённых.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Высокая температура при стоматите у детей. Признаки вирусного стоматита и его лечение
По статистике около 80 % всех болезней, возникающих в полости рта у детей,представлены разными степенями тяжести герпетического стоматита. Что собой представляет это заболевание? Почему возникает? Как проявляется и что нужно делать, если ребенок заболел?
Стоматит представляет собой воспаление слизистой оболочки полости рта. Герпетический стоматит вызывают вирусы герпеса. Чаще всего это заболевание появляется у детей от 1 года до 3 лет. Причина такой эпидемиологии заключается в несостоятельности детского иммунитета, который на данном этапе не может вырабатывать специфические антитела против вируса герпеса. Однако дети первого года жизни эти компоненты иммунной системы получают от матери, вместе с молоком. К концу первого года жизни грудное вскармливание прекращается в 90 % случаев, а антитела, полученные ребенком от мамы, разрушаются. Таким образом, детский организм перед вирусной инфекцией становится беззащитен.
Почему чаще всего встречается именно герпетический стоматит? Вирус герпеса чрезвычайно распространен и живуч. Поселившись однажды в слизистой оболочке, он не оставит ее уже никогда. Практически все взрослые люди являются носителями вируса герпеса, а малышам его передают через поцелуи либо воздушно-капельным путем.
Дети после 3 лет сталкиваются с этим заболеванием реже, ведь их иммунитет функционирует несколько лучше, да и с герпетической инфекцией в разных проявлениях иммунная система уже знакома и формирует ответ более эффективно.
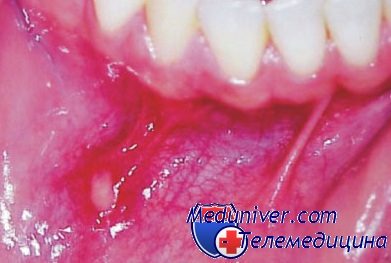
Родителям очень важно знать, как выглядит герпетический стоматит, какими изменениями в организме малыша он сопровождается. Ведь бывали случаи, когда родители лечили ребенка антибиотиками в течение нескольких недель, якобы от ОРЗ, бронхита или ангины. В итоге, конечно, результат антибактериальной терапии при герпетическом стоматите совершенно не оправдывает ожиданий, болезнь только развивается и прогрессирует. Итак, как распознать эту коварную вирусную инфекцию? Есть ряд специфических признаков, которые укажут вам именно на герпетический стоматит.
1. Заболевание начинается остро и внезапно. Сразу поднимается температура до 37 - 37,5 градусов или выше. Хотя общее состояние ребенка удовлетворительное, тут же возникает слабость, вялость, общее недомогание, головокружение, снижение аппетита. Все это - признаки интоксикации, и их выраженность напрямую зависит от тяжести течения герпетического стоматита.
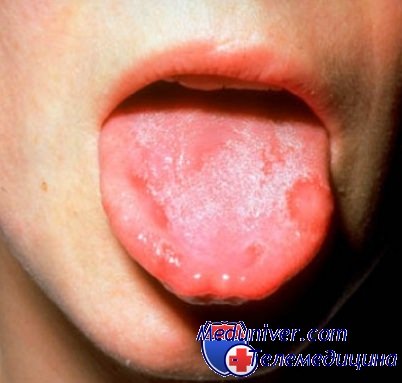
2. Загляните в рот ребенку. На слизистых оболочках внутренней стороны губ, щек, на деснах, небе или языке вы увидите белесые высыпания, похожие на пятнышки или даже пузырьки. Они могут быть одиночными или скученными - это одно из типичных проявлений герпетического стоматита. Если прикоснуться к ним стерильной ватной палочкой, возникнут болезненные ощущения. Обычно через 1 -2 суток эти высыпания начинают исчезать. Они становятся мраморной окраски, края теряют четкость, болезненность при касании также проходит.
Одновременно отмечается покраснение слизистых оболочек, так как сосуды в результате воспаления расширяются и становятся полнокровными.
3. Возможно появление признаков ангины или других ОРЗ. Вместе с тем нередко увеличиваются и становятся болезненными лимфатические узлы - подчелюстные, подбородочный.
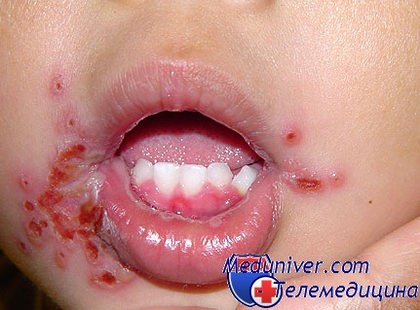
4. Температура тела в период разгара может повышаться до 40 градусов, кожные покровы становятся бледными, увеличивается количество высыпаний, теперь они имеются не только на слизистых оболочках полости рта, но и на лице - губах, вокруг рта. Одновременно изменяется консистенция слюны, она становится густой и тягучей.
Воспаление десен на этом этапе ярко выражено, они могут кровоточить. Все это сопровождается ухудшением общего состояния малыша. Он плохо спит, капризничает, мало ест, чувствует слабость и тошноту.
5. После исчезновения герпетических высыпаний в следующие 2 - 3 дня может сохраняться воспаление десен, особенно около передних зубов. Десны при этом выглядят красными и несколько набухшими, отекшими, увеличение лимфатических узлов также сохраняется некоторое время после постепенного исчезновения признаков болезни.
Чем опасен герпетический стоматит и почему его так важно своевременно выявлять и правильно лечить? Рисков развития осложнений здесь не мало. Во-первых, герпетический стоматит - заболевание более тяжелое, чем обычная "простуда" на губах. У детей он сопровождается выбросом в кровь большого количества токсинов, образующихся в результате деятельности вируса герпеса и воспалительных процессов во рту. Эти токсичные вещества плохо сказываются на работе всех органов и систем детского организма. Страдают дыхание, сердечнососудистая, пищеварительная, нервная системы. В конечном итоге это может привести к очень неприятным осложнениям, вплоть до шока, если течение болезни тяжелое.
Герпетический стоматит сопровождается довольно длительной лихорадкой, причем цифры на градуснике могут вводить родителей в ступор - температура повышается до 40 градусов, в отдельных случаях и более. Такая длительная лихорадка истощает резервы организма, отрицательно сказывается на работе защитных белков. В итоге общая сопротивляемость детского организма снижается, что открывает дорогу для присоединения вторичной, бактериальной инфекции.
Сбивать температуру менее 39.5 градусов все же не рекомендуется, так как процесс может перейти в вяло текущее и рецидивирующее воспаление. Устраните вирусную причину и снимите воспаление, тогда пройдет и лихорадка.
При отсутствии должного лечения герпетические высыпания на слизистых оболочках не всегда самостоятельно исчезают. Они могут рецидивировать, увеличиваться в количестве. Вирус герпеса нарушает нормальную структуру слизистой оболочки, поэтому она некротизируется, изъязвляется, возникает уже язвенный гингивит. Такие поражения являются хорошим местом для развития и бактериального воспаления.
Диагноз герпетический стоматит врач ставит на основе клинической картины, ведь она очень типична. Специфические анализы достаточно трудоемки в проведении, а общий анализ крови покажет только повышение лейкоцитов и СОЭ, что не является специфическими признаками именно герпетического стоматита.
Строго говоря, выделяют 3 формы течения этой болезни: легкую, среднюю и тяжелую. К счастью последняя встречается гораздо реже, но в конечном итоге тяжесть течения болезни во многом зависит от лечения, общего состояния ребенка на момент заболевания, работы его иммунной системы.
Во время лечения следует давать ребенку преимущественно жидкую пищу, чтобы не раздражать и без того воспаленную слизистую оболочку полости рта и не травмировать ее лишний раз. Дети, больные герпетическим стоматитом, должны получать достаточное количество жидкости, она помогает выводить из организма токсины.
Также для обеспечения процесса выздоровления диета должна быть богата витаминами и микроэлементами. В рацион необходимо включать фрукты и ягоды, соки и овощи. Перед кормлением ротовая полость обезболивается 2 % раствором анестезиновой эмульсии.
Боль во рту, сопровождающая герпетический стоматит, непроизвольно приводит к снижению выработки пищеварительных соков. Чтобы процесс переваривания пищи не тормозился, врач иногда назначает принимать пищеварительные ферменты.
В качестве медикаментозного лечения местно применяются противовирусные мази (Виферон, Зовиракс), а также обезболивающие, жаропонижающие и антисептические мази, способствующие заживлению (Холисал Гель, метилурациловая). Их необходимо наносить на области поражения и на здоровые участки во избежание появления на них высыпаний. Также проводится общее лечение ректальными свечами Виферон.
Местно применяются средства, препятствующие высыханию и грубому рубцеванию повреждений слизистой оболочки полости рта. К ним относятся масляные растворы витаминов А и Е, масло шиповника, масло облепихи. Как можно чаще нужно полоскать рот антисептическим раствором хлоргексидина, настоями шалфея или ромашки.
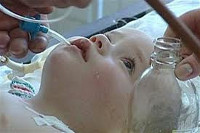
Кишечная инфекция у детей – группа инфекционных заболеваний различной этиологии, протекающих с преимущественным поражением пищеварительного тракта, токсической реакцией и обезвоживанием организма. У детей кишечная инфекция проявляется повышением температуры тела, вялостью, отсутствием аппетита, болями в животе, рвотой, диареей. Диагностика кишечной инфекции у детей основана на клинико-лабораторных данных (анамнезе, симптоматике, выделении возбудителя в испражнениях, обнаружении специфических антител в крови). При кишечной инфекции у детей назначаются антимикробные препараты, бактериофаги, энтеросорбенты; в период лечения важно соблюдение диеты и проведение регидратации.
Общие сведения
Кишечная инфекция у детей – острые бактериальные и вирусные инфекционные заболевания, сопровождающиеся кишечным синдромом, интоксикацией и дегидратацией. В структуре инфекционной заболеваемости в педиатрии кишечные инфекции у детей занимают второе место после ОРВИ. Восприимчивость к кишечной инфекции у детей в 2,5-3 раза выше, чем у взрослых. Около половины случаев кишечной инфекции у детей приходится на ранний возраст (до 3 лет). Кишечная инфекция у ребенка раннего возраста протекает тяжелее, может сопровождаться гипотрофией, развитием дисбактериоза и ферментативной недостаточности, снижением иммунитета. Частое повторение эпизодов инфекции вызывает нарушение физического и нервно-психического развития детей.

Причины
Спектр возбудителей кишечных инфекций у детей крайне широк. Наиболее часто патогенами выступают грамотрицательные энтеробактерии (шигеллы, сальмонеллы, кампилобактеры, эшерихии, иерсинии) и условно-патогенная флора (клебсиеллы, клостридии, протей, стафилококки и др.). Кроме этого, встречаются кишечные инфекции, вызываемые вирусными возбудителями (ротавирусами, энтеровирусами, аденовирусами), простейшими (лямблиями, амебами, кокцидиями), грибами. Общими свойствами всех возбудителей, обусловливающих развитие клинических проявлений, являются энтеропатогенность, способность к синтезу эндо- и экзотоксинов.
Заражение детей кишечными инфекциями происходит посредством фекально-орального механизма алиментарным (через пищу), водным, контактно-бытовым путями (через посуду, грязные руки, игрушки, предметы обихода и т. д.). У ослабленных детей с низкой иммунологической реактивностью возможно эндогенное инфицирование условно-патогенными бактериями. Источником ОКИ может выступать носитель, больной со стертой или манифестной формой заболевания, домашние животные. В развитии кишечной инфекции у детей большую роль играет нарушение правил приготовления и хранения пищи, допуск на детские кухни лиц-носителей инфекции, больных тонзиллитом, фурункулезом, стрептодермией и пр.
Наиболее часто регистрируются спорадические случаи кишечной инфекции у детей, хотя при пищевом или водном пути инфицирования возможны групповые и даже эпидемические вспышки. Подъем заболеваемости некоторыми кишечными инфекциями у детей имеет сезонную зависимость: так, дизентерия чаще возникает летом и осенью, ротавирусная инфекция - зимой.
Распространенность кишечных инфекций среди детей обусловлена эпидемиологическими особенностями (высокой распространенностью и контагиозностью возбудителей, их высокой устойчивостью к факторам внешней среды), анатомо-физиологическими особенностями пищеварительной системы ребенка (низкой кислотностью желудочного сока), несовершенством защитных механизмов (низкой концентрацией IgA). Заболеваемости детей острой кишечной инфекцией способствует нарушение нормальной микробиоты кишечника, несоблюдение правил личной гигиены, плохие санитарно-гигиенические условия жизни.
Классификация
По клинико-этиологическому принципу среди кишечных инфекций, наиболее часто регистрируемых в детской популяции, выделяют шигеллез (дизентерию), сальмонеллез, коли-инфекцию (эшерихиозы), иерсиниоз, кампилобактериоз, криптоспоридиоз, ротавирусную инфекцию, стафилококковую кишечную инфекцию и др.
По тяжести и особенностям симптоматики течение кишечной инфекции у детей может быть типичным (легким, средней тяжести, тяжелым) и атипичным (стертым, гипертоксическим). Выраженность клиники оценивается по степени поражения ЖКТ, обезвоживания и интоксикации.
Характер местных проявлений при кишечной инфекции у детей зависит от поражения того или иного отдела ЖКТ, в связи с чем выделяют гастриты, энтериты, колиты, гастроэнтериты, гастроэнтероколиты, энтероколиты. Кроме локализованных форм, у грудных и ослабленных детей могут развиваться генерализованные формы инфекции с распространением возбудителя за пределы пищеварительного тракта.
В течении кишечной инфекции у детей выделяют острую (до 1,5 месяцев), затяжную (свыше 1,5 месяцев) и хроническую (свыше 5-6 месяцев) фазы.
Симптомы у детей
Дизентерия у детей
После непродолжительного инкубационного периода (1-7 суток) остро повышается температура (до 39-40° C), нарастает слабость и разбитость, снижается аппетит, возможна рвота. На фоне лихорадки отмечается головная боль, ознобы, иногда – бред, судороги, потеря сознания. Кишечная инфекция у детей сопровождается схваткообразными болями в животе с локализацией в левой подвздошной области, явлениями дистального колита (болезненностью и спазмом сигмовидной кишки, тенезмами с выпадением прямой кишки), симптомами сфинктерита. Частота дефекации может варьировать от 4-6 до 15-20 раз за сутки. При дизентерии стул жидкий, содержащий примеси мутной слизи и крови. При тяжелых формах дизентерии возможно развитие геморрагического синдрома, вплоть до кишечного кровотечения.
У детей раннего возраста при кишечной инфекции общая интоксикация преобладает над колитическим синдромом, чаще возникают нарушения гемодинамики, электролитного и белкового обмена. Наиболее легко у детей протекает кишечная инфекция, вызванная шигеллами Зоне; тяжелее - шигеллами Флекснера и Григорьеза-Шига.
Сальмонеллез у детей
Гриппоподобная (респираторная) форма кишечной инфекции встречается у 4-5% детей. При данной форме сальмонеллы обнаруживаются в посеве материала из зева. Ее течение характеризуется фебрильной температурой, головной болью, артралгией и миалгией, явлениями ринита, фарингита, конъюнктивита. Со стороны сердечно-сосудистой системы отмечаются тахикардия и артериальная гипотония.
На тифоподобную форму сальмонеллеза у детей приходится 2% клинических случаев. Она протекает с длительным периодом лихорадки (до 3-4-х недель), выраженной интоксикацией, нарушением функции сердечно-сосудистой системы (тахикардией, брадикардией).
Септическая форма кишечной инфекции обычно развивается у детей первых месяцев жизни, имеющих неблагоприятный преморбидный фон. На ее долю приходится около 2-3% случаев сальмонеллеза у детей. Заболевание протекает крайне тяжело, сопровождается септицемией или септикопиемией, нарушением всех видов обмена, развитием тяжелых осложнений (пневмонии, паренхиматозного гепатита, отоантрита, менингита, остеомиелита).
Эшерихиозы у детей
Данная группа кишечных инфекций у детей крайне обширна и включает коли-инфекци, вызываемые энтеропатогенными, энтеротоксигенными, энтероинвазивными, энтерогеморрагическими эшерихиями.
Кишечная инфекция у детей, вызванная эшерихиями, протекает с субфебрильной или фебрильной температурой, слабостью, вялостью, снижением аппетита, упорной рвотой или срыгиваниями, метеоризмом. Характерна водянистая диарея (обильный, брызжущий стул желтого цвета с примесью слизи), быстро приводящая к дегидратации и развитию эксикоза. При эшерихиозе, вызываемом энтерогеморрагическими эшерихиями, диарея носит кровавый характер.
Вследствие обезвоживания у ребенка возникает сухость кожи и слизистых оболочек, снижается тургор и эластичность тканей, западает большой родничок и глазные яблоки, снижается диурез по типу олигурии или анурии.
Ротавирусная инфекция у детей
Обычно протекает по типу острого гастроэнтерита или энтерита. Инкубационный период в среднем длится 1-3 дня. Все симптомы кишечной инфекции у детей разворачиваются в течение одних суток, при этом поражение ЖКТ сочетается с катаральными явлениями.
Респираторный синдром характеризуется гиперемией зева, ринитом, першением в горле, покашливанием. Одновременно с поражением носоглотки развиваются признаки гастроэнтерита: жидкий (водянистый, пенистый) стул с частотой дефекаций от 4-5 до 15 раз в сутки, рвотой, температурной реакцией, общей интоксикацией. Длительность течения кишечной инфекции у детей – 4-7 дней.
Стафилококковая кишечная инфекция у детей
Различают первичную стафилококковую кишечную инфекцию у детей, связанную с употреблением пищи, обсемененной стафилококком, и вторичную, обусловленную распространением возбудителя из других очагов.
Течение кишечной инфекции у детей характеризуется тяжелым эксикозом и токсикозом, рвотой, учащением стула до 10-15 раз в день. Стул жидкий, водянистый, зеленоватого цвета, с небольшой примесью слизи. При вторичной стафилококковой инфекции у детей кишечные симптомы развиваются на фоне ведущего заболевания: гнойного отита, пневмонии, стафилодермии, ангины и пр. В этом случае заболевание может принимать длительное волнообразное течение.
Диагностика
На основании осмотра, эпидемиологических и клинических данных педиатр (детский инфекционист) может лишь предположить вероятность кишечной инфекции у детей, однако этиологическая расшифровка возможна только на основании лабораторных данных.
Главную роль в подтверждении диагноза кишечной инфекции у детей играет бактериологическое исследование испражнений, которое следует проводить как можно ранее, до начала этиотропной терапии. При генерализованной форме кишечной инфекции у детей проводится посев крови на стерильность, бактериологическое исследование мочи, ликвора.
Определенную диагностическую ценность представляют серологические методы (РПГА, ИФА, РСК), позволяющие выявлять наличие Ат к возбудителю в крови больного с 5-х суток от начала болезни. Исследование копрограммы позволяет уточнить локализацию процесса в ЖКТ.
При кишечной инфекции у детей требуется исключить острый аппендицит, панкреатит, лактазную недостаточность, дискинезию желчевыводящих путей и др. патологию. С этой целью проводятся консультации детского хирурга и детского гастроэнтеролога.
Лечение кишечной инфекции у детей
Комплексное лечение кишечных инфекций у детей предполагает организацию лечебного питания; проведение оральной регидратации, этиотропной, патогенетической и симптоматической терапии.
Диета детей с кишечной инфекцией требует уменьшения объема питания, увеличения кратности кормлений, использования смесей, обогащенных защитными факторами, употребление протертой легкоусвояемой пищи. Важной составляющей терапии кишечных инфекций у детей является оральная регидратация глюкозо-солевыми растворами, обильное питье. Она проводится до прекращения потерь жидкости. При невозможности перорального питания и употребления жидкости назначается инфузионая терапия: внутривенно вводятся растворы глюкозы, Рингера, альбумина и др.
Этиотропная терапия кишечных инфекций у детей проводится антибиотиками и кишечными антисептиками (канамицин, гентамицин, полимиксин, фуразолидон, налидиксовая кислота), энтеросорбентами. Показан прием специфических бактериофагов и лактоглобулинов (сальмонеллезного, дизентерийного, колипротейного, клебсиеллезного и др.), а также иммуноглобулинов (антиротавирусного и др.). Патогенетическая терапия предполагает назначение ферментов, антигистаминных препаратов; симптоматическое лечение включает прием жаропонижающих, спазмолитиков. В период реконвалесценции необходима коррекция дисбактериоза, прием витаминов и адаптогенов.
Прогноз и профилактика
Раннее выявление и адекватная терапия обеспечивают полное выздоровление детей после кишечной инфекции. Иммунитет после ОКИ нестойкий. При тяжелых формах кишечной инфекции у детей возможно развитие гиповолемического шока, ДВС-синдрома, отека легких, острой почечной недостаточности, острой сердечной недостаточности, инфекционно-токсического шока.
В основе профилактики кишечных инфекций у детей – соблюдение санитарно-гигиенических норм: правильное хранение и термическая обработка продуктов, защита воды от загрязнения, изоляция больных, проведение дезинфекции игрушек и посуды в детских учреждениях, привитие детям навыков личной гигиены. При уходе за грудным ребенком мама не должна пренебрегать обработкой молочных желез перед кормлением, обработкой сосок и бутылочек, мытьем рук после пеленания и подмывания ребенка.
Дети, контактировавшие с больным кишечной инфекцией, подлежат бактериологическому обследованию и наблюдению в течение 7 дней.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Читайте также:

