Интенсивная антибиотикотерапия при сепсисе
Обновлено: 05.05.2024
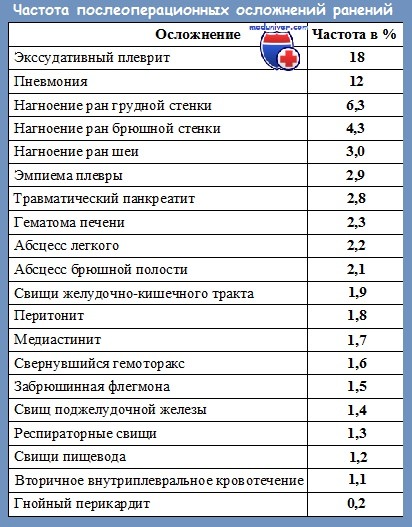
Лечение гнойных и септических осложнений ранений: устранение очага инфекции, антибиотикотерапия
Лечение любого гнойно-септического осложнения является комплексным и включает в себя следующие мероприятия:
1) Устранение первичного очага инфекции хирургическим путем. Хирургическое вмешательство прекращает дальнейшее поступление микроорганизмов. Это может быть ушивание дефекта стенки полого органа, его резекция или удаление. После этого следует санация очага гнойной инфекции, которая заключается в механическом удалении гнойного экссудата, пропитанных гноем некротических тканей из серозных полостей, средостения и забрюшинного пространства. Заключительным этапом хирургического метода лечения является полноценное дренирование гнойного очага.
Наиболее эффективным мы считаем метод активного дренирования с аспирацией и промыванием, принципы и детали которого изложены ниже, в разделах, посвященных специфическим осложнениям ранений.
2) Устранение расстройств внешнего дыхания достигается:
— обогащением кислородом вдыхаемой смеси;
— ИВЛ с положительным давлением в конце выдоха;
— постоянной санацией трахеобронхиального дерева.
Для предупреждения пневмонии применяют аэрозольные ингаляции с антибиотиками, парокислородные ингаляции, муколитики, вибромассаж груди (при отсутствии противопоказаний).
3) Коррекция расстройств системного кровообращения достигается:
— устранением дефицита объема внеклеточной жидкости (кристаллоиды, коллоиды, альбумин, кровь, по показаниям — вазопрессоры);
— снижением вязкости циркулирующей крови.
При проведении инфузионно-трансфузиониой терапии нельзя допускать возникновения легочной артериальной гипертензии.
4) Антибактериальная терапия. На протяжении нескольких десятилетий при лечении гнойных осложнений применялась эскалационная (восходящая) методика антибактериальной терапии, когда при неэффективности препаратов первого ряда назначались более мощные антибиотики.
Так, в прошлом достаточно эффективным было применение амоксициллина или ампициллина с сульбактамом, цефалоспоринов второго поколения (цефуроксима, цефокситина), третьего (цефтриаксона, цефоперазона) или четвертого (цефенима) поколений, фторхинолонов (ципрофлоксацина, левофлоксацина).
Эти препараты обычно применяли в комбинации с аминогликозидами, ванкомицином и антиаэробными средствами (метронидазол, линкомицин, клиндамицин).
Такой подход был клинически и экономически оправдан в условиях низкого уровня резистентности микроорганизмов. Однако во второй половине 80-х и в 90-х годах XX в. отмечен повсеместный рост резистентности, обусловленный как неблагоприятными изменениями внешней среды обитания (экология, социальные условия, алкоголизм, наркомания), так и бесконтрольным употреблением антибиотиков.
В настоящее время устойчивость микроорганизмов объявлена угрозой для человечества в целом. В таких условиях для лечения гнойно-септических осложнений приходится применять деэскалационную методику, которая заключается в максимально раннем назначении массивных доз антибиотика, спектр действия которого максимально охватывает всех возможных возбудителей с последующим (при получении результатов микробиологического исследования) переходом па препараты более узкого спектра.
В этом плане наиболее эффективными в настоящее время являются антибиотики из группы карбоненемов. Несмотря на более чем 20-летнее использование, уровень устойчивости к ним клинически значимых возбудителей остается низким, возможно из-за их устойчивости к бета-лактамазам, выделяемым микроорганизмами для разрушения антибиотиков.
5) Интенсивное парентеральное и энтералъное питание. В первую очередь необходимо обеспечить введение аминокислот, вследствие их усиленного потребления для сохранения барьерной функции кишечника и клеток иммунной системы. Наиболее эффективными в этом смысле являются смеси для энтерального введения, содержащие омега-3 жирные кислоты, глютамин, аргинин, а также пектин.
6) Активные методы детоксикации. Среди методов экстракорпоральной детоксикации у пострадавших с множественными и сочетанными ранениями шеи, груди и живота, осложненными сепсисом, самым распространеным и хорошо изученным является плаз-маферез.
Положительный эффект плазмафереза основан на удалении высокомолекулярных белков острой фазы воспаления, а также нормализации реологических свойств крови. Метод позволяет быстро удалять из циркулирующей крови токсины (как водорастворимые, так и связанные с белками), свободный миоглобин, активированные компоненты свертывающей системы крови, С-реактивный белок, цитокины, комплемент, лизосомальные ферменты, аутоантитела, иммунные комплексы и просто обломки разрушенных клеток и клеток в состоянии апоптоза.
Метод существует в двух модификациях: прерывистый и непрерывный. Не останавливаясь на деталях этих модификаций, необходимо подчеркнуть, что у пострадавших в критическом состоянии используют непрерывную технологию, которая меньше оказывает отрицательное влияние на гемодинамику.
7) Торможение образования медиаторов воспалительной реакции. В настоящее время большие надежды возлагаются на восполнение дефицита селена — микроэлемента, входящего в состав фермента (глютатионпероксидазы), отвечающего за антиоксидантную систему защиты клеток. В частности, достаточное количество этого фермента обеспечивает преобразование свободных радикалов в спирты и таким образом сохраняет целость клеточной мембраны.
Препараты селена при лечении гнойно-септических осложнений применяются в виде пентагидрата селенита натрия. К сожалению, в настоящее время пока нет возможности четко определить закономерности в реакциях и взаимодействиях сотен различных медиаторов, а следовательно, и избирательную нейтрализацию активности циркулирующих в крови медиаторов, как воспалительных, так и противовоспалительных.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Ингибиторы циклооксигеназы при сепсисе. Антибактериальная терапия при сепсисе.
Арахидоновая кислота, входящая в состав липидов, при своем распаде образует эйкосаыоиды: тромбоксан (Тх А2), простагландины (PGE2), простациклин (PGI2), токсичные кислородные радикалы (ОН-, 2-). Совокупность действия эйкосаноидов выражается в повышении проницаемости клеточных мембран, образовании микротромбов, развитии воспалительной реакции, высвобождении эндогенного вазоконстриктора эндотелина, способствующего спазму легочных сосудов. К препаратам, способным ингибировать действие циклооксигеназы, относятся нестероидные противовоспалительные средства кеторолак (90 мг в сутки), диклофенак (150 мг в сутки).
Антагонисты опиоидных рецепторов
Установление роли опиоидных пептидов в патогенезе септического шока (возбуждение ц- и 5-рецепторов) послужило основанием для применения антагонистов опиатов. Применение налоксона способствуем увеличению артериального давления и снижению уровня лактата крови. В комплексе интенсивной терапии септического шока налоксон вводится в дозе 0,4-1,2 мг.
Антибактериальная терапия
Применение рациональной антибактериальной терапии является важным, но не первоочередным направлением в интенсивной терапии септического шока, т. к. направлено только на тех возбудителей, которые поступают в кровоток и существенно не влияют на первичный септический очаг.
Трудности подбора антибиотика в первые часы развития септического шока диктует необходимость применения эмпирической антибактериальной терапии с использованием препаратов с максимально широким спектром действия. Примечательно, что в случае высокой чувствительности возбудителя к антибактериальному препарату, выживаемость больных с септическим шоком возрастает в три раза.
Препаратами выбора при септическом шоке являются карбапенемы (имипинем, меронем), что связано с их ультрашироким спектром действия, низким уровнем приобретенной резистентности и возможностью использования у больных с синдромом мультиорганной дисфункции.
Многочисленными исследованиями установлено, что клиническая эффективность имипинема и меронема в равных суточных дозах одинакова, а монотерапия этими препаратами не уступает режиму комбинированной антибактериальной терапии (цефатоспорины III поколения + аминогликозиды 3 поколения + метронидазол, фторхинолоны + метронидазол).
Применение имипинема, в отличие от меронема, ограничено (особенно у больных с патологией ЦНС) возможностью развития судорожного синдрома, поэтому при инфекционном поражении ЦНС использование имипенема противопоказано.

Меронем назначается внутривенно болюсно с интервалом 8 часов, имипенем только в виде инфузии в течение 60 минут с интервалом 6-8 часов. Суточная доза меронема составляет 3,0 г, имипенема - 4,0 г.
Сочетание цефалоспоринов III поколения (цефтриаксон, цефоперазон) с аминогликозидами 3 поколения (амикацин, нетилмицин) показано при развитии на фоне септического шока ОПН, особенно в случае перитонеальной локализации септическго очага, т. к. цефтриаксон и цефоперазон выводятся из организма преимущественно с желчью, а введение аминогликозидов однократно в максимальной суточной дозе значительно снижает put нефротоксичности.
Цефтриаксон вводится внутривенно в дозе 30 мг/кг с последующими инъекциями по 1-2 г через 12 часов, цефоперазон - по 3 г каждые 6-8 часов. Максимальная суточная доза для амикацина составляет 15 мг/кг, для нетилмицина - 6 мг/кг.
При септическом шоке, развившемся на фоне панкреонекроза, показана комбинация ампициллина, гентамицина и метронидазола.
В случае анаэробного компонента инфекции (абдоминальный, акушерский урологический септический шок) целесообразна комбинация цефалоспоринов IV поколения (цефепим) с метронидазолом или клиндамицином (1 г 2-3 раза в сутки). Указанная комбинация обладает высокой антибактериальной активностью, широким спектром действия, минимальным количеством резистентных к ней P. aeruginosae, высокой устойчивостью к бета-лактамазам и по эффективности сопоставима с монотерапией карбапенемами.
Цефепим вводится внутривенно в дозе 2 г с последующими инъекциями по 1-2 г через 12 часов, метронидазол по 100 мл каждые 8 часов, клиндамицин - по 1 г через 6 часов.
Антибактериальная терапия септического шока, вызванного пневмонией тяжелого течения, проводится в зависимости от характера пневмонии.
При внебольничной пневмонии препаратом выбора являются цефалоспорины III поколения с макролидами. Указанная комбинация практически полностью перекрывает весь спектр возбудителей внегоспитальной пневмонии тяжелого течения.
Особенностью нозокомиальной пневмонии в ОРИТ является то, что она, как правило, развивается на фоне профилактического применения антибиотиков широкого спектра действия, а также у больных, находящихся на ИВЛ.
Развитие септического шока у больных с пневмонией, не получавших ранее антибактериальной терапии или находящихся на ИВЛ менее 5 суток, требует назначения цефалоспоринов III поколения без антипсевдомонадной активности (цефотаксим, цефтриаксон) или фторхинолонов (ципрофлоксацин, офлоксацин) в сочетании с аминогликозидами, а в случае их неэффективности - карбапенемов.
При развитии септического шока у больных на фоне предшествующей терапии антибиотиками или у больных, находящихся на ИВЛ более 5 суток, показано назначение антипсевдомонадных цефалоспоринов (цефаперазон, цефпирамид, цефтазидим) с аминогликозидами 3 поколения.
Септический шок, развившийся на фоне пневмонии с нейтропенией (количество нейтрофилов менее 500 в мкл), требует включения в комплекс интенсивной терапии сочетания цефалоспоринов III IV поколении с аминогликозидами 3 поколения, а в качестве резерва возможно использование тикарциллина или штерациллина с аминогликозидами.
При развитии урологического септического шока целесообразно использовать сочетание цефтриаксона (а при высоком риске синегнойноп инфекции - цефоперазона) с амикащшом.
Антибактериальная терапия менингококкового септического шока должна начинаться параллельно с мероприятиями по стабилизации показателей гемодинамики и нормализации газообмена. Средством выбора антибактериального лечения менингококкового септического шока является бензилпенициллин, т. к. Neisseria meningidis обладает высокой чувствительностью к этому препарату. Бензилпенициллин вводится внутривенно в дозе 200-500 тыс. Ед/кг в сутки.
При использовании больших доз бензилпенициллина или других антибактериальных препаратов, обладающих бактериоцидным эффектом, явления эндогенной интоксикации нередко стремительно нарастают, что получило название синдрома Яриша-Герцгеймера (увеличение концентрации эндотоксина в крови за счет выхода липополисахаридов из разрушенной микробной стенки).
С целью избежания подобной ситуации целесообразно использовать антибактериальные препараты, обладающие не бактерицидным, а бактериостатическим эффектом. В частности, левомицитина сукцинат, который при менингококков ом септическом шоке вводится в дозе 3,0-4,5 г в сутки.
В случае посттравматического или послеоперационного менингита, осложненного септическим шоком, препаратами выбора являются цефалоспорины III поколения в комбинации с ванкомицином, а в качестве альтернативы - комбинация меронема с ванкомицином.
Следует помнить, что некоторые препараты (гипертонические раствора глюкозы, ГКС) уменьшают проникновение антибиотиков через гематоэнцефалический барьер, а другие (кофеин, эуфиллин), наоборот, увеличивают.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

