Какао масло применение при туберкулезе
Обновлено: 25.04.2024
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению? Какова роль фторхинолонов в лечении туберкулеза легких?
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению?
Какова роль фторхинолонов в лечении туберкулеза легких?
Таблица. Стандартные концентрации ПТП, используемые для выявления лекарственной устойчивости МБТ
Первый этап характеризуется проведением интенсивной насыщенной химиотерапии четырьмя-пятью ПТП в течение 2-3 месяцев, что ведет к подавлению размножающейся микобактериальной популяции, уменьшению ее количества и предотвращению развития лекарственной резистентности. На первом этапе используется комбинация препаратов, состоящая из изониазида, рифампицина, пиразинамида, стрептомицина и/или этамбутола.
Второй этап — менее интенсивной химиотерапии — проводится, как правило, двумя-тремя ПТП. Цель второго этапа — воздействие на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм микобактерий. Здесь главной задачей является предупреждение размножения оставшихся микобактерий, а также стимуляция репаративных процессов в легких с помощью различных патогенетических средств и методов лечения.
Такой методический подход к лечению ЛЧТЛ позволяет к концу первого этапа комбинированной химиотерапии под непосредственным медицинским наблюдением абациллировать 100%, а к завершению всего курса лечения — закрыть каверны в легких у более чем 80% больных с впервые выявленным и рецидивным туберкулезом легких [5].
Намного сложнее вопрос о проведении этиотропного лечения второго варианта, к которому мы относим ЛУТЛ, вызванный лекарственно резистентными (ЛР) МБТ к одному и более ПТП и/или их сочетанию. Особенно тяжело протекает ЛУТЛ у больных с множественной ЛР МБТ к изониазиду и рифампицину, то есть к основным и самым эффективным ПТП. Поэтому поиск новых концептуальных путей повышения эффективности лечения ЛУТЛ и разработка современной методологии специфического воздействия на ЛР МБТ является одним из важнейших и приоритетных направлений современной фтизиатрии.
Развитие ЛР у МБТ к ПТП — одна из главных причин недостаточно эффективной этиотропной химиотерапии. Больные туберкулезом, выделяющие ЛР-штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих ЛР-возбудителем. Чем больше число больных, выделяющих ЛР МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной резистентностью не только к основным, но и к резервным ПТП.
Феномен ЛР МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является ЛР. В активно размножающейся бактериальной популяции всегда имеется небольшое количество ЛР-мутантов, которые практического значения не имеют, но по мере уменьшения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством ЛР и устойчивых МБТ [5]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. Следовательно, в клинической практике необходимо исследовать ЛР МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [5].
По определению экспертов ВОЗ [3], ЛУТЛ — это случай туберкулеза легких с выделением МБТ, резистентных к одному и более ПТП. По данным Центрального НИИ туберкулеза РАМН, у каждого второго впервые выявленного и ранее не леченного противотуберкулезными препаратами больного в мокроте выявлялись ЛР к ПТП МБТ, при этом у 27,7% из них наблюдалась устойчивость к двум основным противотуберкулезным препаратам — изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота вторичной ЛР МБТ возрастает до 95,5%.
По нашему мнению, и это составляет основу нашей концепции, для повышения эффективности лечения туберкулеза, вызванного ЛР МБТ, необходимо в первую очередь использовать ускоренные методы выявления ЛР МБТ, что позволяет своевременно изменять режим химиотерапии.
Исследование лекарственной устойчивости МБТ в настоящее время возможно по прямому и непрямому методам.
Непрямой метод определения лекарственной чувствительности МБТ требует от 30 до 60, а иногда до 90 суток, ввиду того что вначале производится посев мокроты на твердые питательные среды и только после получения культуры МБТ производят ее пересев уже на среды с добавлением ПТП. При этом коррекция химиотерапии носит отсроченный характер, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
В последнее время для ускоренного определения лекарственной устойчивости нами применялся радиометрический метод с использованием автоматической системы ВАСТЕС-460 ТВ (Becton Dickinson Diagnostic Systems, Sparks, MD), которая позволяет выявлять лекарственную резистентность МБТ на жидкой среде Middlebrook 7H10 через 6-8 дней.
Не менее важно правильное лечение впервые выявленных больных туберкулезом легких и применение современных режимов химиотерапии с использованием в начале лечения комбинации из четырех-пяти основных противотуберкулезных препаратов до получения результатов лекарственной устойчивости МБТ [2]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной ЛР МБТ бактериостатическое действие окажут два или три химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных и рецидивных больных и назначение ими только трех ПТП является грубой врачебной ошибкой, что в конечном счете ведет к формированию наиболее трудно поддающейся лечению вторичной ЛР МБТ.
Наличие у больного туберкулезом легких ЛР МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и летальных исходов. Особенно тяжело протекают специфические поражения легких у больных с полирезистентными МБТ, которые обладают множественной ЛР, как минимум к изониазиду и рифампицину, т. е. к основным и самым активным противотуберкулезным препаратам. ЛР МБТ имеет не только чисто клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных резервными ПТП обходится намного дороже, чем больных с чувствительными МБТ к основным химиопрепаратам.
В этих условиях расширение списка резервных ПТП, воздействующих на ЛР МБТ, является актуальным и крайне важным для повышения эффективности лечения больных с ЛУТЛ. Кроме того, присоединение к ЛУТЛ неспецифической бронхолегочной инфекции существенным образом утяжеляет течение специфического процесса в легких, требуя назначения дополнительных антибиотиков широкого спектра. В этом плане применение антибиотиков, воздействующих как на МБТ, так и на неспецифическую патогенную бронхолегочную микрофлору, является научнообоснованным и целесообразным.
В этом плане хорошо себя зарекомендовал в России такой препарат из группы фторхинолонов, как офлоксацин (таривид) [3]. Мы же свой выбор остановили на ломефлоксацине, как препарате, который еще не столь широко применяется при лечении туберкулеза и у которого, судя по имеющимся данным, практически не выявляются побочные эффекты и крайне редко формируется ЛР возбудителей инфекционных заболеваний [2].
Ломефлоксацин (максаквин) — антибактериальный препарат из группы фторхинолонов. Как и все представители производных оксихинолонкарбоновой кислоты, максаквин обладает высокой активностью против грамположительных (включая метициллин-устойчивые штаммы Staphylococcus aureus и Staphylococcus epidermidis) и грамотрицательных (включая Pseudomonas) микроорганизмов, в том числе по отношению к различным типам Micobacterium tuberculosis).
Механизм действия максаквина заключается в ингибировании хромосомной и плазмидной ДНК-гиразы, фермента, ответственного за стабильность пространственной структуры микробной ДНК. Вызывая деспирилизацию ДНК микробной клетки, максаквин ведет к гибели последней.
Максаквин обладает иным механизмом действия, нежели другие антибактериальные средства, поэтому к нему не существует перекрестной устойчивости с другими антибиотиками и химиотерапевтическими препаратами [2].
Основной целью настоящего исследования явилось изучение клинической и микробиологической эффективности максаквина при комплексном лечении больных деструктивным ЛУТЛ, выделяющих ЛР МБТ к изониазиду, рифампицину и другим ПТП, а также при сочетании туберкулеза с неспецифической бронхолегочной инфекцией.
Под наблюдением находилось 50 больных деструктивным ЛУТЛ, выделяющих с мокротой ЛР МБТ к изониазиду, рифампицину и ряду других ПТП. Эти люди в возрасте от 20 до 60 лет составили основную группу.
В контрольную группу вошли также 50 больных деструктивным ЛУТЛ легких в той же возрастной группе, выделяющие ЛР МБТ к изониазиду, рифампицину и другим ПТП. Эти пациенты лечились только протионамидом, амикацином, пиразинамидом и этамбутолом.
У 47 больных основной группы и 49 контрольной в мокроте микробиологическими методами были выявлены различные возбудители неспецифической бронхолегочной инфекции.
Среди больных основной группы диссеминированный туберкулез был установлен у 5 человек, инфильтративный — у 12, казеозная пневмония — у 7, кавернозный — у 7 и фиброзно-кавернозный туберкулез — у 17 человек. Большинство больных (45 пациентов) имели распространенный туберкулез легких с поражением более двух долей, у 34 больных был двусторонний процесс. У всех больных основной группы в мокроте были обнаружены МБТ, как методом микроскопии по Цилю — Нильсену, так и методом посева на питательные среды. При этом у них МБТ были устойчивы как минимум к изониазиду и рифампицину. Необходимо отметить, что все пациенты уже ранее неоднократно и неэффективно лечились основными ПТП, и специфический процесс у них приобрел рецидивирующий и хронический характер.
В клинической картине преобладали симптомы интоксикации с высокой температурой тела, потливостью, адинамией, изменениями в крови воспалительного характера, лимфопенией, увеличенной СОЭ до 40-50 мм в час. Следует отметить наличие грудных проявлений болезни — кашель с выделением мокроты, подчас значительного количества, слизисто-гнойной, а у половины больных — гнойной, с неприятным запахом. В легких выслушивались обильные катаральные явления по типу мелко-, средне-, а подчас и крупнопузырчатых влажных хрипов.
У большинства больных преобладали клинические проявления, которые скорее укладывались в картину неспецифического бронхолегочного поражения (бронхита, острой пневмонии, абсцедирования) с частыми и практически не стихающими обострениями.
Основным возбудителем неспецифической инфекции был Streptococcus hemoliticus — у 15,3% и Staphilococcus aureus — у 15% больных. Среди грамотрицательной микрофлоры преобладал Enterobacter cloacae в 7,6% случаев. Следует отметить высокую частоту ассоциации возбудителей неспецифической бронхолегочной инфекции.
МБТ были обнаружены у всех 50 больных. У 42 человек определялось обильное бактериовыделение. У всех пациентов выделенные штаммы МБТ были устойчивы к изониазиду и рифампицину. При этом у 31 больного лекарственная устойчивость МБТ к изониазиду и рифампицину сочеталась с другими ПТП.
Определение минимальной ингибирующей концентрации (МИК) максаквина проводили на лабораторных штаммах H37Rv и Academia, а также клинических штаммах (изолятах), выделенных от 30 больных, из которых 12 изолятов были чувствительны ко всем основным химиопрепаратам и 8 обладали резистентностью к изониазиду, рифампицину и стрептомицину. В опытах in vitro подавление роста лабораторных штаммов МБТ наблюдалось в зоне 57,6±0,04 до 61,8±0,02 мкн/мл, что почти в семь раз больше, чем показатели, характерные для остальных ПТП .
Таким образом, в ходе микробиологических исследований было установлено выраженное бактериологическое действие максаквина на МБТ, при этом более выраженный эффект наблюдался при его воздействии на лекарственно чувствительные штаммы и изоляты. Однако при повышенных концентрациях максаквина эффект также заметен при воздействии на полирезистентные МБТ, устойчивые к основным ППТ.
Лечение максаквином проводилось у всех 50 больных основной группы в разработанной нами комбинации с другими резервными препаратами: протионамидом, амикацином, пиразинамидом и этамбутолом.
Максаквин назначали в дозе 800 мг в сутки перорально однократно в утренние часы сразу вместе с другими противотуберкулезными препаратами для создания максимальной суммарной бактериостатической концентрации в крови и очагах поражения. Доза максаквина выбрана с учетом микробиологических исследований и соответствовала МИК, при которой отмечалось существенное подавление роста МБТ. Терапевтический эффект определяли через месяц — для оценки воздействия его на неспецифическую патогенную бронхолегочную микрофлору и через два месяца — для оценки воздействия на полирезистентные МБТ. Длительность курса лечения резервными химиопрепаратами в сочетании с максаквином составляла два месяца.
Через месяц комплексного лечения было отмечено значительное улучшение состояния больных основной группы, что проявлялось в уменьшении количества мокроты, кашля и катаральных явлений в легких, снижении температуры тела, при этом более чем у двух третей больных — до нормальных цифр.
У всех больных к этому сроку в мокроте перестал определяться рост вторичной патогенной бронхолегочной микрофлоры. К тому же у 34 больных значительно уменьшилась массивность выделения микобактерий туберкулеза. Практически у всех больных нормализовались анализы крови.
Следует отметить, что у 28 пациентов рентгенологически через месяц лечения максаквином в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом отмечалось частичное рассасывание специфических инфильтративных изменений в легких, а также существенное уменьшение перикавитарной воспалительной реакции. Это позволило применить на данном этапе искусственный пневмоторакс, который является обязательным методом в лечении ЛУТЛ и составляет вторую и не менее важную часть нашей концепции повышения эффективности лечения больных деструктивным туберкулезом легких, выделяющих полилекарственнорезистентные МБТ.
При анализе эффективности специфического действия комбинации резервных противотуберкулезных препаратов в сочетании с максаквином на полирезистентные МБТ при лечении 50 больных основной группы мы делали основной акцент на показатель прекращения бактериовыделения, как по микроскопии мокроты по Цилю — Нильсену, так и по посеву на питательные среды через два месяца после химиотерапии.
Анализ частоты прекращения бактериовыделения у больных основной и контрольной группы через два месяца лечения показал, что у пациентов, получавших максаквин в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом, прекращение бактериовыделения было достигнуто в 56% случаях. В контрольной группе больных, не получавших максаквина, — только в 30% случаев.
Следует отметить, что у остальных больных основной группы за этот период времени существенно уменьшилась массивность выделения МБТ.
Инволюция локальных изменений в легких у 50 больных контрольной группы также шла более замедленными темпами, и только у 25 больных к концу второго месяца удалось достичь частичного рассасывания перикавитарной инфильтрации и применить к ним искусственный пневмоторакс. К 39 из 50 пациентов основной группы был применен искусственный пневмоторакс в течение 1,5-2 месяцев, и 17 из них удалось достигнуть закрытия каверн в легких. 11 оставшихся больных, имеющих противопоказания к проведению искусственного пневмоторакса, в этот период были подготовлены к плановому оперативному вмешательству.
При определении лекарственной устойчивости МБТ к максаквину через два месяца лечения у больных основной группы только в 4% случаев была получена вторичная лекарственная устойчивость, сформировавшаяся в процессе двухмесячной химиотерапии, что в конечном итоге потребовало его отмены и замены на другой химиопрепарат, к которому МБТ сохранили свою чувствительность.
К концу второго месяца у 4% больных отмечались явления непереносимости максаквина — в виде диспепсических явлений и диареи, связанной с дисбактериозом, аллергических кожных проявлений и эозинофилии до 32%, что привело к полной отмене препарата. Во всех остальных случаях при двухмесячном ежедневном применении максаквина в суточной дозе 800 мг побочных явлений не отмечалось.
Проведенная после окончания курса лечения максаквином комбинированная химиотерапия резервными препаратами и динамическое наблюдение за этими же больными показали, что достигнутый ко второму месяцу положительный результат в абациллировании мокроты оказал положительное влияние и на конечный результат излечения больных с ЛУТЛ.
Таким образом, применение максаквина в дозе 800 мг в сутки в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом у больных деструктивным ЛУТЛ с сопутствующей неспецифической бронхолегочной инфекцией показало его достаточную эффективность как антибиотика широкого спектра, воздействующего на грамотрицательную и грамположительную микрофлору, и препарата, действующего на туберкулезное воспаление.
Максаквин с полной уверенностью может быть отнесен к группе резервных ПТП. Он эффективно действует не только на МБТ, чувствительные ко всем ПТП, но и на ЛУ МБТ к изониазиду и рифампицину, что и обусловливает целесообразность его назначения таким больным. Тем не менее максаквин не следует рассматривать как основной препарат в схемах лечения больных с впервые выявленным туберкулезом легких, он должен оставаться в резерве и применяться только при ЛУТЛ и сопутствующей неспецифической бронхолегочной инфекции.
Для изониазида это составляет 1 мкг/мл, для рифампицина — 40 мкг/мл, стрептомицина — 10 мкг/мл, этамбутола — 2 мкг/мл, канамицина — 30 мкг/мл, амикацина — 8 мкг/мл, протионамида (этионамида) — 30 мкг/мл, офлоксацина (таривида) — 5 мкг/мл, циклосерина — 30 мкг/мл и для пиразинамида — 100 мкг/мл.
Литература
1. Лечение туберкулеза. Рекомендации для национальных программ. ВОЗ. 1998. 77 с.
2. Мишин. В. Ю., Степанян И. Э. Фторхинолоны в лечении туберкулеза органов дыхания // Русский медицинский журнал. 1999. № 5. С. 234-236.
3. Рекомендации по лечению резистентных форм туберкулеза. ВОЗ. 1998. 47 с.
4. Хоменко А. Г., Мишин В. Ю., Чуканов В. И. и др. Эффективность применения офлоксацина в комплексном лечении больных туберкулезом легких, осложненным неспецифической бронхолегочной инфекцией // Новые лекарственные препараты. 1995. Вып. 11. С. 13-20.
5. Хоменко А. Г. Современная химиотерапия туберкулеза // Клиническая фармакология и терапия. 1998. № 4. С. 16-20.

Текст предназначен исключительно для ознакомления. Мы настоятельно призываем не применять диеты, не прибегать к каким-либо лечебным меню и голоданию без присмотра врачей. Рекомендуем к прочтению: "Почему нельзя самостоятельно садиться на диету".
Питание при туберкулёзе – важная составляющая успешного лечения данной инфекционной патологии.
Главные задачи диетотерапии – снабжение организма питательными веществами, повышение активности клеток иммунной системы, нормализация обмена веществ, ускорение регенерации повреждённых тканей, снижение токсической нагрузки на печень (эндогенной и экзогенной).
Клиническая картина
При сильном иммунитете и правильном лечении повреждённые ткани постепенно рубцуются. Однако, даже надлежащая терапия не может дать стопроцентную гарантию выздоровления, поскольку некоторые бациллы остаются в организме в дремлющем состоянии. Как только создаются благоприятные условия для активации палочки Коха (снижение иммунитета, развитие гиповитаминоза, возрастание токсической нагрузки на печень) на месте очага инфицирования происходит расплавление защитной капсулы. В этот момент микобактерии покидают гранулематозный очаг, а на месте рубцевания ткани образуется полость – каверна (вторичный туберкулёз).
По мере прогрессирования инфекции происходит локальное разрушение верхних и нижних дыхательных путей. При наличии большого количества каверн возникает кровохарканье или лёгочное кровотечение.

Первые симптомы туберкулёза:
- слабость;
- повышенная утомляемость;
- бледность кожных покровов;
- субфебрильная температура (37,2 градусов);
- потливость (особенно по ночам);
- снижение веса;
- увеличение лимфатических узлов;
- бессонница;
- сухой кашель.
Помните, первичный туберкулез лёгких может продолжительное время протекать бессимптомно. Каждый гражданин должен проходить обследование не реже 1 раза в год. Естественно, при появлении жалоб на кашель, одышку, слабость пациент должен быть обследован незамедлительно. Тем, кто находится в контакте с человеком, больным открытой формой туберкулеза, флюорографию нужно делать 1 раз в полгода.
Группа повышенного риска заболевания туберкулезом – больные с хроническими заболеваниями органов дыхания, язвенной болезнью желудка, хроническим гастритом, сахарным диабетом, больные хроническим алкоголизмом, злостные курильщики должны проходить флюорографию не реже 2-х раз в год.
Питание при туберкулёзе
Калорийность дневного рациона больных должна на 10 % превышать энергетическую ценность суточного меню здоровых людей (3000-3500 килокалорий).

Особенности компонентов питания при туберкулезе:
-
. В составе диетического рациона должно присутствовать много протеина, поскольку под влиянием бактериальной интоксикации расход данного вещества возрастает в 2 раза.
Для инфицированных больных дневная норма рассчитывается исходя из соотношения 2 грамма белка на килограмм веса (это 120-130 грамм в сутки для взрослого человека с массой тела 60-70 килограмм). В тяжелых случаях дневную порцию нутриента повышают до 140-150 грамм. Данные компоненты необходимы организму для рубцевания очага воспаления, восстановления тканевых белков, ускорения выработки противотуберкулёзного иммунитета.
Лучшие источники легкоусвояемого белка: кисломолочные продукты (сыворотка, творог, кефир, сметана, сыр), домашняя птица (индейка, курятина), крольчатина, яйца (куриные, перепелиные), морепродукты (мидии, рыба, устрицы, креветки), крупы (перловая, гречневая, овсяная), бобовые (чечевица, горох, соя).
Усвояемость протеинов животного происхождения составляет 94 %, растительного – 70%.
-
. Токсины, выделяемые микобактериями, вызывают глубокие изменения в структуре клеточных мембран, которые приводят к активации перекисного окисления липидов, и, как следствие, нарушению жирового обмена. На фоне данных процессов человек теряет аппетит и стремительно худеет. Кроме того, в 50% случаев возникают дисфункции внутренних органов, в которых сосредоточено много липопротеинов (печени, надпочечников, головного мозга).
Для восполнения дефицита массы тела, дневное меню туберкулёзных больных обогащают жирами исходя из расчета: на килограмм веса должно приходиться 1,2 грамм триглицеридов (это 100-110 грамм). Однако превышение дневной порции липидов даёт обратный эффект: возникают расстройства пищеварения, снижается аппетит, ухудшается детоксикационные функции печени. Кроме того, при обострениях патологии важно потреблять не более 70 – 80 грамм элемента в сутки.
Пополнение липидных запасов осуществляют за счёт потребления ненасыщенных жирных кислот, которые входят в состав растительных масел (льняного, рыжикового, кедрового), морепродуктов, рыбьего жира.
-
. При активных формах туберкулёза (сопровождающихся лихорадочным состоянием), происходит угнетение функции инсулярного аппарата поджелудочной железы, что приводит к снижению синтеза гликогена в печени. Для предупреждения метаболических расстройств в организм больного должно поступать не менее 500 грамм углеводов в сутки. При тяжёлых формах патологии (экссудативном плеврите, фиброзно-кавернозном туберкулезе, казеозной пневмонии, менингите) дневную порцию сахаридов снижают до 350 грамм.
Для восполнения запасов глюкозы используют свежий хлеб, неочищенные крупы, мёд, тростниковый сахар. При этом от употребления кондитерских изделий, сладких напитков и рафинированной выпечки (из белой муки) лучше отказаться.
- Минеральные соли. При активном туберкулёзе потребность в микро- и макроэлементах возрастает вдвое (из-за распада тканей, высокой температуры, потоотделения). Отклонения в минеральном обмене возникают в результате нарушений синтетической и метаболической функций печени.
Ключевую роль в диетотерапии туберкулёза играют макроэлементы: фосфор и кальций. Данные нутриенты участвуют практически во всех энергетических и обменных реакциях в организме. Кроме того, они ускоряют рубцевание ткани в инфекционных очагах, нормализуют процесс свёртывания крови, снижают проявления аллергических реакций, уменьшают проницаемость лимфатических и кровеносных сосудов.
При туберкулёзе суточная потребность в кальции возрастает до 2-3 грамм, в фосфоре – до 3-6 грамм. Данные вещества содержатся в твороге, сыре, сметане, кефире, петрушке, цветной капусте.
- Витамины. Больные туберкулёзом (особенно кавернозной формой), в 90% случаев, страдают от дефицита витаминов группы B, C и А. Введение в рацион больного 2-3 грамм L-аскорбиновой кислоты повышает защитные функции крови (в том числе, синтез T-киллеров, уничтожающих инфекцию), нейтрализует продукты распада микобактерий, стимулирует естественный противоинфекционный иммунитет. Природные источники нутриента: квашеная капуста, петрушка, клюква, шиповник. Кроме того, в питании туберкулёзных пациентов должно присутствовать повышенное количество витамина A (4-5 миллиграмм в сутки).
Ретинол (провитамин А) содержится в молочных продуктах (сливочном масле, сметане), рыбьем жире, яичных желтках, красно-оранжевых овощах и фруктах (моркови, абрикосах, тыкве, хурме, апельсинах). Данное вещество ускоряет регенерацию повреждённых тканей (в том числе эпителия слизистых), снижает концентрацию холестерина в клетках (которым питаются микобактерии), повышает иммунный статус больного, участвует в образовании зрительного пурпура. Наряду с этим в диету при туберкулёзе включают витамины группы B, поскольку они ускоряют заживление тканевых ран, улучшают белково-углеводный обмен, стабилизируют психоэмоциональный фон. Компенсировать недостаток данных нутриентов поможет цельнозерновой хлеб, крупы, бобовые, растительные масла, орехи, семечки, яйца, кисломолочные продукты.
Помните, только грамотно составленный рацион питания (с правильным соотношением пищевых компонентов) помогает ускорить реабилитацию больного после интенсивной антибиотикотерапии.
Продукты пчеловодства на страже здоровья
- Личинки восковой моли. Несмотря на то, что огнёвка является главным паразитом пчелиных сот, на основе её яиц изготавливают противотуберкулёзные настойки. Российский иммунолог И. И. Мечников опытным путём установил, что пищеварительные ферменты личинок восковой моли способны растворять плёнки, которыми покрыты микобактерии. Вследствие этого инфекция становится уязвимой для воздействия основных противотуберкулёзных препаратов.
- Прополис. Благодаря наличию ароматических смол, флавоноидов, бензойной и коричной кислот, продукт обладает ярко выраженными антисептическими, бактерицидными свойствами (особенно против туберкулёзных бактерий). Наряду с этим, прополис повышает естественный противоинфекционный иммунитет, ускоряет выведение вредоносного холестерина, улучшает аппетит и снижает частоту кашлевых приступов. Кроме того, вещество противодействует образованию тромбов, стимулирует процесс кроветворения, устраняет сосудистый спазм.
Интересно, что прополис усиливает в 10-100 раз действие антибиотиков (полимиксина, тетрациклина, неомицина, стрептомицина). При остром течении болезни применяют масляные и водные экстракты продукта пчеловодства, в период ремиссии допустимо использовать спиртовые растворы.
- Маточное молочко. По питательной ценности данный продукт превосходит цельное коровье молоко: в 4-5 раз по содержанию белков, в 3-4 раза – по концентрации углеводов, в 2-3 раза – по жировой составляющей. Кроме того, оно оказывает на организм мощное дезинтоксикационное и анаболическое действие (за счёт содержания флавоноидов, иммуноглобулинов, фитонцидов, аминокислот, фитогормонов, антиоксидантов, ферментов).
При туберкулёзе лёгких маточное молочко целесообразно применять в составе фитокомпозиций с липовым мёдом, прополисом (для усиления биологических свойств).
- Пыльца (пчелиная обножка). Природный концентрат аминокислот, повышающий иммунный статус больного. Помимо этого продукт ускоряет восстановление тканевых белков, улучшает обменные процессы в печени, стимулирует выработку эритроцитов, снижает количество рецидивов, стабилизирует мембраны клеток, обезвреживает токсины и шлаки.
- Мёд. Общеукрепляющий продукт, повышающий жизненный тонус больного. Мёд улучшает ферментативную функцию пищеварительного тракта, стимулирует синтез эритроцитов, повышает фагоцитарную активность лейкоцитов, увеличивает запасы гликогена в печени, ускоряет обезвреживание продуктов распада микобактерий.
Помните, продукты пчеловодства целесообразно использовать как для лечения, так и для профилактики туберкулёза, особенно в тубочагах, где наблюдаются пациенты с виражом туберкулиновых проб.
Особенности питания
Базовые характеристики стола:
Учитывая, что у больных туберкулёзом снижен аппетит, приготовленная еда должна быть максимально вкусной и ароматной.
Перечень рекомендованных продуктов
Для повышения барьерных функций организма рекомендуется употреблять семечки, орехи, нерафинированные масла, зелень, травяные отвары.
Меню на неделю
Понедельник

Завтрак: 200 грамм пшеничной каши, 150 грамм винегрета, 30 грамм слабосолёной сельди (предварительно вымоченной в воде), 10 грамм рыжикового масла.
Ланч: 50 грамм орехового ассорти (миндаль, кешью, грецкие).
Обед: 300 грамм борща, 100 грамм куриного бифштекса, 30 грамм сметаны.
Полдник: 200 миллилитров ягодно-йогуртового коктейля.
Ужин: 200 грамм картофельного пюре, 150 грамм салата из свежих овощей (помидор, огурец, лук, листовая зелень), 1 яйцо (всмятку).
За час до сна: 200 миллилитров кефира.
Вторник
Завтрак: 200 грамм овсяной каши, 100 грамм сухофруктов (клюквы, кураги, изюма), 20 грамм ржаного хлеба.
Ланч: 200 грамм сезонных фруктов (яблок, груш, апельсинов, персиков, слив, бананов).
Обед: 300 грамм овощного супа-пюре, 150 грамм рыбных котлет, 50 грамм листовой зелени.
Полдник: 200 миллилитров ромашкового чая, 150 грамм яблочной шарлотки (домашней).
Ужин: 150 грамм творога, 100 грамм сезонных ягод (малины, клубники, клюквы, ежевики), 30 миллилитров сметаны.
За час до сна: 200 миллилитров сыворотки.
Среда
Завтрак: 100 грамм омлета (из 2-х яиц), 50 грамм голландского сыра, 30 грамм цельнозерновых тостов.
Ланч: 250 миллилитров зелёного коктейля (100 миллилитров йогурта, 100 грамм фруктов или ягод, 50 грамм зелени).
Обед: 300 грамм горохового супа, 150 грамм тушёных овощей (свёклы, моркови, капусты), 15 миллилитров сметаны.
Полдник: 200 миллилитров компота, 150 грамм творожно-клюквенного пудинга.
Ужин: 250 грамм зелёной гречки, 150 грамм заливной рыбы с овощами, 15 миллилитров льняного масла.
За час до сна: 200 миллилитров кефира.
Четверг
Завтрак: 200 г пшеничной каши, 150 г овощной подливы (кабачок, морковь, баклажан, помидор), 20 миллилитров льняного масла.
Ланч: 200 г фруктового микса (авокадо, яблоки, персики, банан, груши).
Обед: 300 г рисового рассольника, 150 г свекольно-морковного салата, 100 г мясного гуляша.
Полдник: 150 г свежевыжатого сока (апельсинового, яблочного, виноградного, клубничного), 100 г тыквенно-овсяного печенья.
Ужин: 250 г блинов с творогом, 150 миллилитров травяного чая (жасмин, роза, липа).
За час до сна: 150 миллилитров самодельного йогурта, 7 миллилитров мёда.
Пятница

Завтрак: 150 грамм макарон (коричневых), 50 грамм куриного гуляша,
Ланч: 200 миллилитров фруктово-ягодного киселя (брусника, чёрная смородина, киви, банан, шиповник, яблоко), 50 грамм орехов (лесных, грецких, миндальных).
Обед: 300 грамм голубцов с мясом, 150 грамм свежей овощной нарезки, 30 грамм термостатной сметаны.
Полдник: 200 миллилитров морковного сока, 70 грамм цельнозерновых хлебцов.
Ужин: 200 грамм овощного рагу, 100 грамм отварной рыбы, 15 миллилитров облепихового масла.
За час до сна: 250 миллилитров сыворотки.
Суббота
Завтрак: 200 г гречки, 100 г куриных котлет (паровых), 50 миллилитров овощной подливы (тушёной).
Ланч: 100 г натуральных сухофруктов (кураги, инжира, чернослива, клюквы, изюма), 50 г сырых орехов (кешью, миндаля, грецких, фундука).
Обед: 300 г чечевичного супа, 100 г мясных вареников, 50 г листовой зелени (кинзы, укропа, базилика, петрушки), 30 миллилитров домашней сметаны.
Полдник: 200 г сезонных ягод (клубники, малины, черники, ежевики), 30 миллилитров сливок.
Ужин: 150 г творога, 50 г бананов, 30 г изюма, 30 г фиников, 20 миллилитров сметаны.
За час до сна: 25 миллилитров ряженки.
Воскресенье
Завтрак: 150 г яблочно-рисового пудинга, 50 г голландского сыра, 30 г ржаных тостов, 10 г сливочного масла.
Ланч: 200 миллилитров ягодного компота, 100 г галет, 15 миллилитров майского мёда.
Обед: 200 г фасолевого супа-пюре, 150 г свекольно-капустного салата, 30 г листовой зелени.
Полдник: 200 г бананово-молочного коктейля.
Ужин: 200 г рыбы с овощами (запечённой), 20 миллилитров облепихового масла.
За час до сна: 250 миллилитров простокваши.
Вывод
Питание при туберкулёзе – важнейшая составляющая лечебной терапии, направленная на подавление бактериальной инфекции, вызванной палочкой Коха. При заражении, в кровь выбрасывается большое количество токсичных ядов (продуктов жизнедеятельности микроорганизмов). Вследствие этого замедляются окислительные процессы в тканях, нарушается обмен эссенциальных структур, снижается ферментативная секреция поджелудочной железы, ухудшается кровообращение. Для минимизации данных проблем пищевой рацион туберкулёзных больных обогащают компонентами питания, обладающими детоксикационной активностью.
Полезные продукты для больных туберкулезом: цельнозерновые и кисломолочные изделия, нешлифованные крупы, орехи, семечки, растительные масла, овощи, фрукты, ягоды. Данные ингредиенты, помимо улучшения функции печени, насыщают организм питательными веществами (аминокислотами, витаминами, минералами), повышают естественный противоинфекционный иммунитет.
Специальность: инфекционист, гастроэнтеролог, пульмонолог .
Общий стаж: 35 лет .
Образование: 1975-1982, 1ММИ, сан-гиг, высшая квалификация, врач-инфекционист .

Туберкулез - это преимущественно хроническое инфекционное заболевание, при котором чаще всего поражены легкие. Реже встречается туберкулез почек, кишечника, гортани, костей и суставов, кожи. Для туберкулеза характерны изменения пораженных органов, включая распад их тканей, и интоксикация организма. При туберкулезе имеют место нарушения обмена веществ и функций различных органов и систем, в частности угнетение функции органов пищеварения.
Важнейшей составной частью режима больных туберкулезом является лечебное питание. Комбинируя определенные продукты, назначая специальные диеты, можно нормализовать нарушенный обмен веществ при развитии туберкулезного воспаления, повысить реактивность организма, создать благоприятные условия для развития репаративных процессов.
Лечебное питание при туберкулезе
Больному туберкулезом необходима диета, в которой должны быть представлены основные продукты, содержащие в своем составе не только оптимальное количество белков жиров и углеводов, но и достаточное количество витаминов и минеральных солей. Важное значение имеет не столько количество пищи и высокий калораж, сколько ее качественный состав.
Главным в лечении впервые выявленного туберкулеза легких или его обострения (рецидива) являются интенсивные режимы приема в течение нескольких месяцев одновременно 4-5 противотуберкулезных препаратов. Естественно, что при такой химиотерапии можно ожидать возникновения побочных эффектов от лекарств. Окончательное устранение инфекции, рассасывание либо отграничение очагов туберкулезного поражения легких остаются задачей самого организма.
Отсюда вытекает необходимость укрепления защитных сил организма, преодоления побочного действия противотуберкулезных препаратов, в том числе за счет целенаправленного питания.
Общие принципы диетотерапии при туберкулезе:
- обеспечить организм полноценным питанием в условиях распада белков, ухудшения обмена жиров и углеводов, повышенного расхода витаминов и минеральных веществ на фоне нередкого резкого снижения аппетита;
- повысить защитные силы организма, направленные против инфекции, и уменьшить явления интоксикации;
- способствовать нормализации нарушенного обмена веществ и устранить вторичные расстройства питания организма, обусловленные туберкулезным процессом;
- содействовать восстановлению тканей, пораженных туберкулезной инфекцией.
Энергоценность диеты зависит от особенностей течения туберкулеза, сопутствующих заболеваний, массы тела больного, а также характера труда при сохраненной трудоспособности. При остром течении или резком обострении болезни и постельном режиме достаточно 2200-2400 ккал в день, при полупостельном режиме больше - 2500-2700 ккал, при затухании острого процесса или обострения 2800-3100 ккал, или 40-45 ккал на 1 кг массы тела.
Для больных легочным туберкулезом с хроническим течением, особенно молодого возраста, а также при истощении необходима диета, энергоценность которой на 15-20% выше физиологических норм. Более высокая энергоценность рациона не является полезной. Быстрая и большая прибавка массы тела может ухудшить состояние больного. Заблуждением является мнение о необходимости сверхусиленного питания больных туберкулезом, что ведет к их перекармливанию и перегрузке органов пищеварения.
В диете должно быть повышено содержание белка в среднем 90-100 г (1,3-1,4 г на 1 кг нормальной массы тела), а при истощении, вялом течении болезни, распаде тканей, затухании обострения 1,5-1,7 г белка на 1 кг нормальной массы тела, в среднем 110-120 г, из них не менее 55-60% - за счет животных продуктов. Высокое содержание белка необходимо для восполнения его повышенного расхода, восстановления тканей в очаге инфекции, усиления защитных сил организма. При тяжелом течении болезни с высокой температурой, сильной интоксикацией количество белков в диете ограничивают до 70-80 г, из них 65% за счет белка животных продуктов.
С учетом вкусов больного источниками белка могут быть различные виды мяса, птицы и рыбы, исключая очень жирные. Целесообразно использование блюд из печени. При хроническом течении туберкулеза легких допустима любая кулинарная обработка указанных продуктов. При отсутствии противопоказаний (например, при плеврите с выпотом) в рацион включают мясные и рыбные продукты - колбасные изделия, ветчину, сельдь, балыки, икру, консервы (шпроты, сардины, лососевые в собственном соку и др.). В питании должны быть яйца и различные блюда из них.
В полном ассортименте используются молочные продукты с обязательным включением творога и сыра, а также кисломолочных напитков, в том числе обогащенных пробиотиками и пребиотиками (кефиры, йогурты и др.). Прием пробиотиков не только нормализует кишечную микрофлору, но и улучшает течение туберкулеза. С другой стороны, курсы кумысотерапии на фоне курортной климатотерапии неплохо зарекомендовали себя при лечении туберкулеза легких.
Содержание жиров в диете не должно превышать 100-110 г, а при обострении болезни 70-80 г. Основные источники пищевых жиров - сливочное и растительные масла в натуральном виде, а также мягкие (наливные) маргарины. Не следует перегружать диету жирами, так как при этом ухудшается сниженный при туберкулезе аппетит, расстраивается пищеварение, в крови накапливаются продукты неполного окисления жиров. Использование сала барсуков, сурков или медведей относится к давним народным средствам лечения туберкулеза, но особое лечебное действие этих жиров не получило научного подтверждения.
Углеводы восполняют нужную для конкретного больного энергоценность, в среднем же их потребление должно быть в пределах физиологических норм: 350-400 г в день, из них 80-100 г - за счет сахара, меда, варенья и других сахаристых продуктов. Вне острого периода болезни в питание включают различные мучные изделия (пироги и пирожки печеные с мясом или рыбой, бисквиты, сдобу и др.), любые блюда из разных круп (особенно гречневой и овсяной), в частности, в сочетании с творогом, макаронные изделия, хорошо разваренные бобовые. Необходимая углеводная часть рациона - овощи, фрукты и ягоды в любой кулинарной обработке, но с обязательным включением сырых. Хронический туберкулез легких не в фазе обострения включен в число заболеваний, при которых применяют ампелометрию - лечение виноградом.
Особого внимания при туберкулезе требует обеспечение организма витаминами, прежде всего В1 (тиамином), В6 (пиридоксином) и С (аскорбиновой кислотой). Это объясняется тем, что на фоне химиотерапии происходит угнетение местного образования ряда витаминов микрофлорой толстого кишечника и всасывания витаминов в кишечнике, а также прямым антагонизмом между противотуберкулезными препаратами и витамином В6, между антибиотиками и витамином В1. Хотя клиническая картина витаминной недостаточности проявляется редко, скрытый дефицит витаминов способствует токсическому влиянию химиопрепаратов на нервную систему, печень, сердце, кожу и слизистые оболочки.
Стандарт лечения больных туберкулезом легких предусматривает назначение дополнения диеты препаратами витаминно-минеральных комплексов.
При неосложненном туберкулезе кулинарная обработка пищи обычная, прием пищи 5-6 раз в день. Необходимо максимально разнообразить питание, исключить частую повторяемость блюд в меню. Указанным требованиям в основном отвечают рассмотренные подходы к питанию, которые применимы при туберкулезе легких в период нерезкого обострения или его затухания, при костно-суставном туберкулезе, при туберкулезе лимфатических узлов.
В условиях стационара при туберкулезе используется высокобелковая диета 11(т).
Химический состав лечебной диеты при туберкулезе
- 100-110 г белков, 60 % из которых животные;
- 100-110 г жиров, 20-25 % из которых растительные;
- 400-450 г углеводов;
- 12-15 г соли;
- 1,5 л жидкости.
Лечебная диета № 11 имеет энергоценность, равную 2900-3100 калориям.
Примерное меню диеты при лечении туберкулеза
1-й завтрак: салат из свежей капусты с яблоками со сметаной, омлет из двух яиц, каша овсяная молочная, чай, кофе или какао с молоком.
2-й завтрак: бутерброд с сыром и сливочным маслом, томатный или иной сок.
Обед: сельдь с растительным маслом и зеленым луком, борщ на мясном бульоне со сметаной, курица жареная с отварным рисом, компот.
Полдник: отвар шиповника, печенье или выпечка.
Ужин: зразы мясные, фаршированные луком и яйцом, картофельное пюре, запеканка из гречневой крупы с творогом, чай с медом.
Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ? С чем связаны возможны
 |
| Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания |
Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ?
С чем связаны возможные ошибки в диагностике?
Какова основная роль b-агонистов в терапии бронхиальной астмы?
Как назначаются кортикостероиды?
Несмотря на возросшую компетентность врачей и доступность эффективных методов лечения, смертность от бронхиальной астмы остается высокой. Предотвратить многие смертельные исходы и даже избежать большинства случаев госпитализации можно было бы при проведении правильного лечения.
Необходимо помнить, что ведение больных астмой — процесс сложный и длительный.
Недооценка степени несостоятельности дыхания. Тяжесть состояния пациента и степень несостоятельности его дыхательной системы можно не распознать, если пренебречь тщательным выяснением всех проявлений болезни и построением диаграммы измерений максимальной скорости потока (МСП) выдыхаемого воздуха.
Зачастую у больных астмой снижены виды на будущее, хотя некоторые и склонны недооценивать серьезность симптомов своего заболевания. Чтобы выявить такую недооценку, нужно подробно расспросить пациента, бывает ли у него кашель или хриплое дыхание ночью или при физической нагрузке.
Если пациентам не удается достичь наилучшей возможной функции легких, то для коррекции этого состояния необходимо для начала вычислить нормальную МСП выдыхаемого воздуха для данного пациента, пользуясь диаграммой, прилагаемой к пикфлуометру.
Если измеренная МСП более чем на 20% меньше вычисленной, стоит провести исследование обратимости этого состояния, что делается путем сопоставления МСП или жизненной емкости легких (ЖЕЛ) до и после лечения.
Необходимая терапия может состоять всего лишь в однократном приеме бронходилятатора, но если это не увеличивает МСП на 20%, то есть до вычисленного уровня, могут понадобиться более серьезные меры, например трехнедельный курс системных кортикостероидов (30 мг преднизолона в день для взрослых). Таким образом выясняется наилучший достижимый уровень МСП, на который ориентируются в последующем лечении.
Иногда пациенты сообщают об уменьшении одышки, но при этом значения МСП не изменяются. В таких случаях необходимо провести измерение ЖЕЛ с помощью спирометра, которое может подтвердить улучшение, не определяемое по МСП (рис. 2). Спирометрами в настоящее время укомплектованы все врачебные приемные.
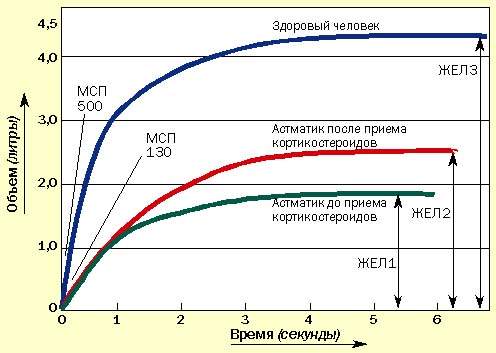 |
| Рисунок 2. Изменение ЖЕЛ под влиянием курса кортикостероидов. МСП может не измениться, но увеличение ЖЕЛ свидетельствует об улучшении состояния |
Бронхиальная астма, замаскированная под хроническое обструктивное заболевание легких (ХОЗЛ). Страдающие одышкой пациенты, которым поставлен диагноз ХОЗЛ или эмфизема, могут иметь скрытый бронхоспастический элемент, обусловленный бронхиальной астмой.
Таким пациентам необходимо провести исследование обратимости процесса, как описано выше. Любое улучшение функции легких можно поддержать, проводя адекватное лечение бронхиальной астмы. При отсутствии улучшения легочной функции назначение кортикостероидов ничем не оправдано, а только приводит к нежелательным побочным эффектам, таким как остеопороз.
Что должен помнить врач, наблюдающий больных с бронхиальной астмой
- Сказал ли я, что нужно применять спейсер при ингалировании кортикостероидов?
- Проверил ли я навыки ингаляции?
- Осмотрел ли я всех пациентов, недавно перенесших тяжелые приступы или госпитализацию?
- Все ли пациенты с повторными назначениями регулярно приходят на прием?
- Все ли я сделал, чтобы исключить астму у пациентов с ХОЗЛ?
- Проводятся ли регулярные проверки для достижения единообразного подхода к ведению астматиков?
Постоянный прием b-агонистов короткого действия. Показано, что лечение астмы постоянным приемом b-агонистов увеличивает гиперреактивность легких и утяжеляет бронхиальную астму [1]. Если пациент использует b-агонисты скорее регулярно, чем случайно, их применение должно сопровождаться назначением ингаляционных кортикостероидов или, если кортикостероиды уже применяются, увеличением их дозы до достаточной, чтобы контролировать астму. Таким образом, b-агонисты оставляют на случаи одышки и хрипов.
Последние методические указания по лечению бронхиальной астмы в Британии рекомендуют начинать с высокой дозы ингаляционных или системных кортикостероидов для достижения быстрого контроля, затем постепенно снижать дозу до минимальной, обеспечивающей нормальное самочувствие пациента и оптимальные значения МСП или ЖЕЛ на фоне минимального применения бронходилятатора (рис. 3). Быстрое облегчение состояния, достигаемое при применении кортикостероидов, улучшает настроение пациента и увеличивает его доверие к лечению.
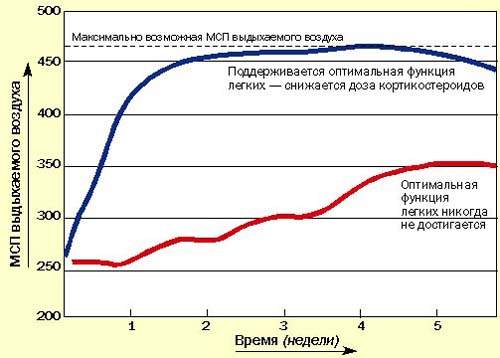 |
| Рисунок 3. Рекомендуется начинать с высоких доз кортикостероидов, а затем постепенно снижать дозу до минимальной (оптимальные значения МСП или ЖЕЛ) |
Последние данные свидетельствуют о том, что назначать кортикостероиды нужно как можно раньше всем астматикам, и не только для контролирования симптомов, но и для предотвращения прогрессирующих структурных повреждений легких, обусловленных хроническим воспалением [2,3]. Это означает, что кортикостероиды следует предпочесть b-агонистам, как только диагноз подтверждается МСП-диаграммой. b-агонисты остаются препаратами резерва на крайний случай.
Возможность альтернативного лечения. Хотя ингалируемые кортикостероиды должны быть краеугольным камнем в лечении астмы, в случаях, трудно поддающихся лечению, можно использовать и некоторые другие препараты. Доказано, что противовоспалительным эффектом обладают теофиллины в достаточно небольших дозах, но надо учитывать в каждом индивидуальном случае их возможное взаимодействие с другими препаратами.
Пожилым пациентам целесообразно назначать ипратропиум. Иногда оказываются эффективными недокромил и кромогликат.
Бронходилятаторы длительного действия, такие как сальметерол, могут облегчать состояние, особенно ночью, блокируя бронхоконстрикторные механизмы. Однако необходимо, чтобы все вышеперечисленные препараты сопровождались применением адекватных доз кортикостероидов.
Техника ингаляции. Нужно добиться, чтобы у пациентов выработались правильные навыки обращения с ингалятором. Врач должен помочь подобрать тот тип ингалятора, который наиболее удобен пациенту, и проверить его работоспособность. Для этого в кабинете врача должен быть полный набор ингаляторов.
Спейсеры. Применяемые вместе с аэрозольными ингаляторами, спейсеры облегчают проникновение препарата в легкие и снижают как накопление его в глотке, так и системное всасывание за счет проглатывания.
Спейсеры помогают координировать выброс препарата со вдохом. Это особенно важно при ингалировании кортикостероидов. Так как кортикостероиды применяются только дважды в день, громоздкий спейсер можно хранить дома.
Спейсеры обеспечивают лучшее накопление препарата в легких, чем распылители. Необходимо правильно их применять: встряхнуть ингалятор, чтобы лекарство смешалось с носителем, и однократно впрыснуть смесь с последующим скорейшим вдохом [4].
Триггерные факторы. Нераспознанные триггерные факторы могут быть и дома, и на работе, и на отдыхе, то есть практически в любом месте. Выявить источник поможет анамнез. Например, при профессиональной бронхиальной астме состояние улучшается во время отпуска и в выходные дни. Отсутствие раздражителя уменьшает или устраняет проявления болезни и снижает необходимость в лекарствах.
Проблемой, которую часто не принимают во внимание, может быть пассивное курение. Такие препараты, как b-блокаторы и нестероидные противовоспалительные средства (НПВС), также могут вызывать астму.
Использование распылителей (небулайзеров) без фоновой кортикостероидной терапии. При лечении острого астматического приступа без назначения пероральных кортикостероидов все еще используют распылители, которые обеспечивают проникновение более высокой дозы b-агонистов. Это действительно снимает бронхоспазм, но поскольку высокая доза b-агонистов не воздействует на сопутствующий воспалительный процесс, необходимо сразу же дать больному кортикостероиды внутрь, чтобы предотвратить нарастание приступа; эффект бронходилятаторов снижается по мере увеличения отека слизистой.
Если тяжесть приступа такова, что требуется небулайзер, необходимо назначить системные кортикостероиды. Даже при умеренном приступе бронходилятаторы сами по себе приносят лишь временное облегчение и есть опасность повторения приступа — возможно, глубокой ночью!
Несвоевременное назначение оральных кортикостероидов. Если не проводить противовоспалительной терапии, у больных нарастает отек слизистой, что приводит к повторению приступов. Такие пациенты часто нуждаются в госпитализации и назначении высоких доз кортикостероидов в течение нескольких дней, прежде чем у них наступит стабилизация состояния.
Пациенты, подверженные быстроразвивающимся приступам, нуждаются в как можно более раннем назначении кортикостероидов и бронходилятаторов. Они должны уметь распознавать ухудшение состояния, всегда иметь под рукой кортикостероиды и знать, как их использовать. Не следует заставлять этих пациентов дожидаться прихода к ним врача (рис. 4).
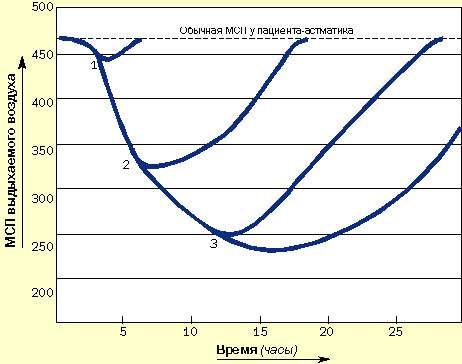 |
| Рисунок 4. Зависимость развития острых приступов от времени назначения кортикостероидов и как результат применения длительных курсов системной кортикостероидной терапии. (1) Кортикостероиды назначены сразу после возникновения приступа: выздоровление наступает быстро. (2) Кортикостероиды назначены через 6 часов: выздоровление замедлено. (3) Кортикостероиды назначены позже чем через 12 часов: приступ тяжелый и длительный, выздоровление наступает медленно |
Пациенты с постепенным развитием приступов могут подождать и посмотреть, помогает ли увеличенная доза ингаляционных кортикостероидов в сочетании с бронходилятаторами.
Неадекватный курс системных кортикостероидов. Иногда назначенные кортикостероиды отменяют до полного купирования приступа, что ведет к сохранению гиперреактивности бронхов и очередному приступу.
Подобная цепь событий может привести пациента к ложному заключению, что у него бронхиальная астма, трудно поддающаяся лечению.
Прекращение наблюдения за пациентом после острого приступа или госпитализации. Трудности возникают при отмене системного кортикостероида и назначении ингаляционного. В этот переходный период необходимо тщательное наблюдение; по достижении стабилизации состояния дозу ингалируемого кортикостероида постепенно снижают до минимально необходимой, чтобы заболевание никак себя не проявляло и функция легких была оптимальной.
Целью последующего лечения становится поддержание наивысшей МСП, достигнутой в больнице после курса системных кортикостероидов.
Консультация, проведенная через некоторое время после выписки, дает хорошую возможность проверить план ведения пациента, выяснить, что не так, и внести соответствующие поправки.
Кашель и хрипы с гнойной мокротой иногда принимают за легочную инфекцию. Однако мокрота больных астмой содержит гораздо больше эозинофилов, чем полиморфных клеток и бактерий. В пожилом возрасте левожелудочковая недостаточность и сердечная астма должны наводить на мысль о предшествующей бронхиальной астме. Будьте осторожны с b-блокаторами!
Внезапная одышка может быть обусловлена пневмотораксом или легочной эмболией. Хрипы встречаются при туберкулезе легких, бронхиальной карциноме или инородном теле и могут быть четко локализованы. Следовательно, у любого пациента с астмой, развившейся во взрослом возрасте, необходимо провести рентгенологическое исследование органов грудной клетки.
После установления диагноза основная цель врача — освободить пациента от проявлений болезни и оптимизировать функцию легких, а также установить контроль за болезнью. Для этого специально обученный медперсонал должен обучать больных и проверять правильность выполнения ими всех назначений.
Конечно, в некоторых случаях это может оказаться затруднительным, однако план предписанных действий способно усвоить абсолютное большинство больных.
Все пациенты должны:
- уметь распознать начало приступа
- знать, как применять высокие дозы b-агонистов;
- самостоятельно начать прием преднизолона внутрь;
- знать, когда звонить врачу или отправляться в больницу;
- все страдающие от приступов, должны быть обеспечены кортикостероидами.
Литература
1. Sears M. R., Taylor D. R. et al. Regular inhaled b-agonist treatment in bronchial asthma. Lancet 1990;336:1491–1396.
2. Tari Haahtela et al. Comparinson of terbutaline with budesonide in newly detected asthma. N Engl J Med 1991;325:388–392.
3. Redingon A. K., Howarth P. H. Airway remodelling in asthma. Thorax 1997;52:310–312.
4. O'Callaghan C., Barry P. Spacer devices in the treatment of asthma. BMJ 1997;314:1061–1062.
Спирометрия при хронической бронхиальной астме
Бочкообразная грудная клетка при хронической бронхиальной астме возникает из-за задержки воздуха в периферических отделах легких, что приводит к постоянному поддержанию грудной клетки в состоянии вдоха. Задержанный воздух не выдыхается и бесполезно занимает большую часть легких (остаточный объем). Это снижает объем воздуха (жизненную емкость легких), входящего в легкое.
Воздух задерживается из-за хронического воспаления, вызывающего отек слизистой периферических бронхиол. При лечении кортикостероидами отек спадает и воздух высвобождается. Это доказывается увеличением ЖЕЛ, определенной спирометрически. МСП может не изменяться (см. рис. 2.)
Читайте также:

